丙型肝炎病毒NS3-4A丝氨酸蛋白酵素抑制药物之发展
丙型肝炎病毒蛋白酶抑制剂研发现状分析

丙型肝炎病毒蛋白酶抑制剂研发现状分析阿丽塔;刘晓婷;张玢;杜建;张燕舞【期刊名称】《中国药业》【年(卷),期】2012(021)007【摘要】In order to have a full sense of the research and development status of HCV protease inhibitors, we systemically surveyed theHCV protease inhibitors in clinical trails launched to the market. We found that there have been two HCV protease inhibitors launchedto the market, Telaprevir and Boceprevir. Telaprevir and Boceprevir would be used in combination with interferon and ribavirin and it'sincreased the cure rate. There are several protease inhibitors, and the big advantage we are hoping for from the second - wave proteaseinhibitors are improvements in the pharmacokinetic profile, dosing intervals, and perhaps some advances with respect to safety andtolerability.%为全面系统地了解国内外丙型肝炎病毒NS3/4A蛋白酶抑制剂的研发现状,笔者调研了国内外处于临床研究阶段和已上市的蛋白酶抑制剂.目前仅有2种丙型肝炎病毒NS3/4A蛋白酶抑制剂上市,即2011年美国食品和药物管理局批准的Vertex公司研发的药物Telaprevir和默克公司研发的药物Boceprevir.Telaprevir和Boceprevir需与目前的丙型病毒性肝炎标准疗法联合使用,临床治愈率高于标准疗法,Telaprevir的临床效果略微优于Boceprevir.部分处于临床开发状态的第2代蛋白酶抑制剂与Telaprevir和Boceprevir相比,在安全性、耐受性、服用便利性、疗效上更胜一筹.【总页数】2页(P1-2)【作者】阿丽塔;刘晓婷;张玢;杜建;张燕舞【作者单位】中国医学科学院医学信息研究所图书馆,北京,100005;中国医学科学院医学信息研究所图书馆,北京,100005;中国医学科学院医学信息研究所图书馆,北京,100005;中国医学科学院医学信息研究所图书馆,北京,100005;中国医学科学院医学信息研究所图书馆,北京,100005【正文语种】中文【中图分类】R978.7【相关文献】1.第二代丙型肝炎病毒NS3/4A丝氨酸蛋白酶抑制剂研究进展 [J], 王路;陆涛;王海勇;王振2.丙型肝炎病毒蛋白酶抑制剂高通量筛选模型的建立及应用 [J], 李健蕊;武燕彬;司书毅;陈鸿珊;蒋建东;彭宗根3.FDA批准口服丙型肝炎病毒蛋白酶抑制剂Victrelis [J],4.丙型肝炎病毒NS3丝氨酸蛋白酶抑制剂研究进展 [J], 曹璐璐;刘兆鹏5.新的HCV蛋白酶抑制剂可有效抵抗丙型肝炎病毒 [J],因版权原因,仅展示原文概要,查看原文内容请购买。
以流感病毒神经氨酸酶和丙型肝炎病毒NS34A蛋白酶为靶点的抗病毒先导化合物的发现

以流感病毒神经氨酸酶和丙型肝炎病毒NS3/4A蛋白酶为靶点的抗病毒先导化合物的发现流感是由流感病毒引起的急性上呼吸道传染病,每年都会造成几十万人的死亡,是人类生命健康的一大威胁。
近年来,由于流感病毒的不断变异,人感染高致病性禽流感病毒如H5N1、H7N9等病例的频繁出现造成了极大的社会恐慌,耐药病毒株的出现使目前的抗流感病毒形势更加严峻。
神经氨酸酶(NA)是位于流感病毒表面的重要糖蛋白,在病毒感染时可以水解宿主细胞表面的唾液酸与糖蛋白之间糖苷键促使病毒释放,同时可以防止子代病毒富集。
NA还可以水解呼吸道黏膜中的唾液酸,促进病毒在呼吸道中的传播,在病毒的复制和感染周期中发挥了重要作用。
NA虽然亚型众多,但其活性位点的十几个氨基酸却在所有甲型和乙型流感病毒中高度保守,是NA抑制剂设计的重要理论基础。
扎那米韦(zanamivir)和奥司他韦(c seltamivir)上市以来,NA抑制剂成为抗流感病毒的重要措施,先后又有帕拉米韦(peramivir)和拉尼米韦(Laninamivir)在几个国家上市。
NA也成为抗流感病毒药物设计的重要靶点,人们设计、合成了多种结构类型的NA抑制剂,还有很多天然产物分子被报道也具有一定的NA抑制活性。
近年来,由于NA抑制药物广泛应用于临床,已经有耐药病毒株出现,oseltamivir由于是口服制剂,应用最为广泛,但病毒耐药性也最为严重。
Zanamivir 和 peramivir也有耐药病毒株开始出现。
因此,开发新型、高效、安全的NA抑制剂仍是目前抗流感病毒领域的研究热点。
丙型肝炎是由丙型肝炎病毒(HCV)引起的,可发展为慢性肝炎、肝硬化及肝癌等严重的肝脏疾病。
全球已有约1.8亿人感染了HCV,每年会引起几十万人的死亡,是人类健康的又一大威胁。
目前尚无疫苗可以有效的预防HCV感染。
NS3/4A是HCV的重要功能蛋白,具有丝氨酸蛋白酶活性,可以水解HCV的多聚蛋白前体形成成熟的NS3~NS5B蛋白,在病毒的复制和感染周期中发挥了重要作用。
HCV药物研发进展综述 丙型肝炎与抗丙肝药物解析

HCV药物研发进展综述(一):丙型肝炎与抗丙肝药物药渡经纬 2016-01-28 导读:丙肝病毒感染全球流行,是肝硬化和肝癌的主要原因。
然而过去人类并没有特异的丙肝治疗药物,自2011年FDA批准2个NS3/4A抑制剂上市后,在2013和2014年全球爆发式的批准上市了疗效惊人的抗丙肝药物和抗丙肝药物组合。
2013年和2014年,全球包括5个单药、3个复方药在内共批准上市8个新分子实体用于治疗丙肝。
其中包括了疗效惊人并在市场销售上的表现堪称史诗级的新药索非布韦(Sofosbuvir)。
文内所涉药物统计自药渡网,截止时间2015年12月31日。
本文将分6期向大家介绍一下丙肝和抗丙肝药物的现状与研发进展,同时还对比解析了一下国际上现行的主要抗丙肝治疗组合,最后和大家聊聊中国丙肝的现状和治疗选择。
∙第一期:丙型肝炎与抗丙肝药物∙第二期:NS3/4A蛋白酶抑制剂研究进展∙第三期:NS5A抑制剂研究进展∙第四期:NS5B抑制剂研究进展∙第五期:国际上主要抗丙肝治疗组合解析∙第六期:中国丙肝现状和抗病治疗选择1. 病毒性肝炎肝炎是我们日常生活中经常听到的名称和疾病,而平时咱们所说的肝炎一般都是病毒性肝炎。
病毒性肝炎是病毒感染引起的,肝细胞损伤及之后免疫系统对肝细胞进行攻击导致的急慢性肝炎(图1)。
研究表明,病毒性肝炎对肝的损害主要源自与免疫系统对机体的攻击。
图1 病毒性肝炎是病毒感染引起的病毒性肝炎主要分甲到戊5种肝炎,他们的特点如表1。
2. 丙型肝炎丙型肝炎是由丙肝病毒感染引起的。
而丙肝病毒感染流呈全球流行状态,是导致肝硬化和肝癌的最主要病因(图2)。
图 2 丙肝病毒感染进展世界卫生组织(WHO)最近数据显示,丙肝病毒全球流行率约为3%,感染人数近2亿,其流行率在不同的国家和地区表现出很大的不同(图3)。
图3 HCV疫情分布(数据来自/)据卫计委公布的数据显示,最近10年来我国丙肝病毒感染报告病例数呈逐年上升趋势,从2006年的70681例,急速增长到2012年的201622例,虽在之后稍微稳定在20万出头,但总趋势仍不乐观(图4)。
丙型肝炎病毒蛋白酶抑制剂研发现状分析

毒 的复制 , 特别 是对于那些 能避开宿 主免疫 系统清 除的丙型肝
炎 病 毒 。 白 酶 抑 制 剂 能 给 病 毒 以 双 重 打 击 , 型 肝 炎 病 毒 蛋 丙 N34 S / A蛋 白酶抑 制 剂 的 研 究是 抗 丙 型 肝 炎病 毒 研 究 最 活跃 的方 向之 一 【。 此 , 者 系统 调 研 了 处 于 临床 研究 状态 和 已上 市 的丙 5为 笔 型 肝炎 病毒 N 3 4 S / A蛋 白酶抑 制剂 , 以期为 国内科研人 员 提供参 考 。 1 部 分 丙 型肝 炎 病 毒 N 3 4 蛋 白酶 抑 制 剂 S/A
2 1 年 4月 5日 第 2 02 l卷第 7期
Vo. , . , M , 01 1 21 No 7 Ap 5 2 2
中l 虱蔼
Chi ar na Ph mac utc l e in s
・
药学专论 ・
P am a e t a o o rp s h r c ui lM n g a h c
表 1 部 分 丙型 肝 炎 病毒 N 3 4 蛋 白酶 抑 制 剂 药物 S /A
肝炎患病人数 相对 甲型病毒性肝炎和 乙型病毒 性肝炎来说要少
得 多 , 其 危 险 程 度 并 不 比两 者 低 。 但 目前 全 球 每 年 约 有 30万 ~ 0
司美格鲁肽机制

司美格鲁肽机制司美格鲁肽(Simeprevir)是一种用于治疗慢性丙型肝炎的药物,属于直接作用的抗病毒药物(Direct-Acting Antiviral,简称DAA)。
它通过抑制丙型肝炎病毒(HCV)的复制和繁殖,发挥治疗作用。
本文将从多个角度介绍司美格鲁肽的机制。
一、丙型肝炎病毒的复制过程在了解司美格鲁肽的机制之前,我们首先来了解一下丙型肝炎病毒的复制过程。
丙型肝炎病毒是一个RNA病毒,其复制过程包括以下几个关键步骤:病毒进入宿主细胞、病毒RNA合成蛋白质、病毒RNA复制和病毒颗粒组装与释放。
二、司美格鲁肽的作用机制司美格鲁肽是一种非结构蛋白NS3/4A蛋白酶抑制剂,它主要通过抑制丙型肝炎病毒的NS3/4A蛋白酶活性,从而阻断了病毒复制的关键步骤。
NS3/4A蛋白酶是丙型肝炎病毒中一个重要的蛋白质复合物,它具有蛋白酶活性和RNA解旋酶活性。
蛋白酶活性能够切割多个丙型肝炎病毒的聚合酶前体蛋白,从而产生成熟的聚合酶。
RNA解旋酶活性则能够解旋病毒RNA,为病毒RNA复制提供所需的单链RNA。
司美格鲁肽通过与NS3/4A蛋白酶结合,竞争性地占据酶活性位点,阻断了蛋白酶活性的产生,从而抑制了丙型肝炎病毒的复制。
此外,司美格鲁肽还能够抑制RNA解旋酶的活性,进一步阻碍病毒RNA 的复制。
三、司美格鲁肽的治疗效果临床研究表明,司美格鲁肽联合其他药物治疗慢性丙型肝炎能够获得较高的治愈率。
与传统的干扰素和利巴韦林治疗相比,司美格鲁肽具有更好的安全性和耐受性,能够显著提高患者的生活质量。
四、司美格鲁肽的用法和注意事项司美格鲁肽一般口服给药,每日一次。
在使用司美格鲁肽治疗慢性丙型肝炎时,需要密切监测患者的肝功能和病毒负荷,以及与其他药物的相互作用。
然而,司美格鲁肽也存在一些不良反应和禁忌症。
常见的不良反应包括头痛、乏力、恶心、呕吐等,严重的不良反应可能导致肝功能异常、皮疹等。
此外,司美格鲁肽不适用于肝功能不全或丙型肝炎病毒基因型1a/1b以外的感染。
中国司美替尼临床实验

中国司美替尼临床实验司美替尼(Simeprevir)是一种口服直接抗病毒药物,属于丙型肝炎病毒NS3/4A蛋白酶抑制剂。
它通过抑制NS3/4A蛋白酶的活性,阻止丙型肝炎病毒在肝细胞内复制,从而减轻并治疗丙型肝炎的症状。
近年来,中国在司美替尼的临床实验方面取得了重要进展。
一、临床试验目的中国司美替尼临床实验的主要目的是评估该药物的疗效和安全性,为丙型肝炎患者提供更有效的治疗选择。
它的临床试验也旨在验证该药物在中国人群中的适应症和用药指导,为国内研究和临床应用提供可靠的数据支持。
二、临床试验设计与方法1. 受试者选择参与中国司美替尼临床试验的受试者主要是丙型肝炎病毒感染引起的慢性肝炎患者,其血清学和临床特征符合病毒性肝炎的诊断标准。
2. 试验分组临床试验采用随机、双盲、安慰剂对照的设计,将受试者分为药物组和安慰剂组。
药物组接受司美替尼的治疗,而安慰剂组则接受安慰剂治疗。
3. 临床观察指标临床试验主要观察指标包括丙型肝炎病毒RNA的清除率、肝功能指标的改善情况、疾病进展情况、不良反应发生率等。
通过临床数据的收集和分析,评估药物的疗效和安全性。
三、临床试验进展与结果中国司美替尼临床实验已经在多个医疗机构展开,并取得了一定的进展。
根据初步的结果显示,该药物在丙型肝炎的治疗中具有较好的疗效和安全性,可有效减轻病情并改善肝功能。
同时,不良反应发生率较低,临床可耐受性良好。
四、临床实验意义与展望中国司美替尼临床试验的进展和结果对于丙型肝炎的治疗具有重要的意义。
它为中国患者提供了新的治疗选择,并为国内的研究和应用提供了宝贵的数据支持。
未来,司美替尼的临床应用将进一步扩大,为更多人群提供有效的治疗方案。
总结:中国司美替尼临床实验通过评估该药物的疗效和安全性,为丙型肝炎患者提供有效的治疗选择。
临床试验采用随机、双盲、安慰剂对照的设计,观察指标主要包括丙型肝炎病毒RNA的清除率、肝功能指标的改善、疾病进展情况和不良反应发生率等。
小分子药物治疗丙型肝炎的疗效和安全性

小分子药物治疗丙型肝炎的疗效和安全性丙型肝炎是由丙型肝炎病毒(HCV)引起的一种肝炎疾病。
该病毒通过血液传播,感染者往往表现为慢性肝炎,并长期存在丙型肝炎病毒复制。
随着丙肝病毒感染的增加,丙型肝炎已成为全球主要的公共卫生问题之一。
长期存在的丙型肝炎病毒感染可引起肝脏纤维化、肝硬化和肝癌等严重并发症。
对于丙型肝炎的治疗,除了控制丙肝病毒的复制外,还需评估治疗方案的疗效和安全性。
近年来,随着药物研究的进展,一些新的小分子药物已被开发出来,用于治疗丙型肝炎。
这些小分子药物主要包括直接抗病毒药物(DAAs)和免疫调节剂(IMs)。
直接抗病毒药物是针对丙型肝炎病毒复制过程中的关键步骤进行设计的药物,其作用机制主要是通过抑制病毒复制酶来抑制病毒的复制。
目前常用的直接抗病毒药物包括NS3/4A蛋白酶抑制剂、NS5A蛋白抑制剂和NS5B聚合酶抑制剂等。
这些药物能够显著降低丙肝病毒的复制水平,从而达到治疗的目的。
免疫调节剂主要通过调节宿主免疫系统来抑制丙型肝炎的病毒复制。
这些药物主要包括干扰素和核苷类似物等。
干扰素通过调节宿主免疫反应来阻断病毒复制,但其疗效相对较低,且常伴有明显的副作用。
核苷类似物是一类模拟自然核苷酸的化合物,可以直接插入到病毒DNA或RNA链中,从而终止其复制过程。
目前,临床研究已证实,小分子药物治疗丙型肝炎的疗效和安全性均好于传统的免疫调节剂。
以直接抗病毒药物为主的小分子药物治疗方案已成为目前临床治疗丙型肝炎的首选方法。
一项关于小分子药物治疗丙型肝炎的大规模临床试验的结果显示,治疗12周的病例中,有超过90%的患者实现了完全的病毒学反应,即基因组中没有检测到丙肝病毒的存在。
与免疫调节剂相比,小分子药物治疗的成功率更高且疗程更短,减少了患者的治疗负担。
小分子药物治疗丙型肝炎的安全性也得到了充分的验证。
临床试验结果显示,小分子药物治疗患者的不良反应较少且较轻微,患者的生活质量也得到了明显的改善。
丙型肝炎病毒(HCV)NS34A蛋白酶作用底物DDB1的鉴定及其对HCV复制影响和细胞抗病毒反应的调节

丙型肝炎病毒(HCV)NS3/4A蛋白酶作用底物DDB1的鉴定及其对HCV复制影响和细胞抗病毒反应的调节全世界大约3%的人口感染了丙型肝炎病毒(Hepatitis C Virus, HCV),其中三分之二的HCV感染者会发展成为长期的慢性肝炎,造成肝组织纤维化、肝硬化等病变,最终导致肝细胞癌的发生。
HCV NS3/4A蛋白酶是由NS3和NS4A结合形成,并负责切割加工多聚蛋白中NS3-NS5B区段,对于HCV的感染和复制有着重要作用。
除此之外,NS3/4A蛋白酶还能切割宿主蛋白VISA、 TRIF,使其去功能化,抑制I型干扰素和促细胞炎症因子的表达,逃逸天然免疫的细胞抗病毒反应。
蛋白质组学已成为分子细胞生物学研究中不可或缺的一项工具。
它广泛应用于鉴定分析多组分的蛋白复合物和细胞器组分,以及寻找转录后修饰和进行各种复杂的功能型筛选。
在本项研究中,我们通过Flag标签一步纯化方法和液相色谱-质谱联用(LC-MS),以HCVNS3/4A蛋白酶为目的蛋白,筛选获得侯选蛋白DDB1。
DDB1是Cullin4E3泛素连接酶复合物中的接头蛋白,在调节各种生理活动中均起着重要作用。
这种E3复合物以Cullin4为骨架,DDB1为接头,通过DDB1连接各类带有WD40结构域的底物受体(Substrate Receptor),再利用不同底物受体招募各类底物完成其对各项生理活动的调节。
在病毒感染的过程中,病毒蛋白能通过结合Cullin4-DDB1复合物调控宿主的免疫反应。
实验结果表明:体外过量表达NS3/4A和DDB1能检测到二者的相互作用。
并且同样的结果在HCV亚基因组复制子和HCV细胞培养系统中也得到验证。
体外过量表达NS3/4A和HCV感染Huh7细胞,NS3/4A均能以DDB1第378位半胱氨酸为切割位点切割DDB1。
DDB1对HCV在Huh7中的复制起着重要作用,在DDB1RNAi Huh7细胞中,HCV 进入细胞水平没有明显变化,但HCV的复制水平明显降低,并且新产生的病毒滴度也远远低于野生型细胞。
丙型肝炎病毒的突变与抗病毒药物耐药性

丙型肝炎病毒的突变与抗病毒药物耐药性概述丙型肝炎是一种由丙型肝炎病毒(HCV)引起的慢性肝炎,世界范围内广泛存在。
丙型肝炎病毒的突变性是导致抗病毒治疗困难和耐药性产生的重要原因之一。
了解丙型肝炎病毒的突变特点以及与抗病毒药物耐药性的关系,对于制定有效的治疗策略具有重要意义。
丙型肝炎病毒的突变特点丙型肝炎病毒是一种RNA病毒,其基因组具有高度变异性。
这种突变性主要来源于病毒复制过程中的错误复制和基因重组。
丙型肝炎病毒的突变可导致其基因组的不同区域发生变异,其中最为重要的是病毒外膜蛋白(E1和E2)和病毒内膜蛋白(NS3、NS5A和NS5B)的变异。
突变与抗病毒药物耐药性的关系丙型肝炎病毒的突变对抗病毒药物的耐药性具有重要影响。
丙型肝炎抗病毒治疗的基础是抗病毒药物,包括干扰素和直接抗病毒药物(DAAs)。
然而,由于丙型肝炎病毒的高度变异性,其突变可以导致抗病毒药物的失效和耐药性的产生。
丙型肝炎病毒突变与DAAs的耐药性DAAs是目前临床上主要用于治疗丙型肝炎的抗病毒药物。
然而,丙型肝炎病毒的突变可以导致DAAs的耐药性产生。
研究发现,丙型肝炎病毒的NS3、NS5A 和NS5B基因区域的突变与DAAs的耐药性密切相关。
这些突变可以影响DAAs与病毒蛋白的结合,从而降低药物的疗效。
突变监测与临床应用针对丙型肝炎病毒的突变监测对于指导抗病毒治疗具有重要意义。
通过对患者样本中丙型肝炎病毒基因组的测序和突变分析,可以及时发现耐药性相关的突变,并根据突变情况调整治疗方案。
突变监测的临床应用可以提高抗病毒治疗的成功率,减少耐药性的产生。
突变与个体化治疗丙型肝炎病毒的突变性使得每个患者的病毒株可能存在差异。
因此,个体化治疗策略的制定对于提高治疗效果至关重要。
通过对患者病毒株的突变分析,可以根据突变情况选择最合适的抗病毒药物组合,从而提高治疗成功率。
结论丙型肝炎病毒的突变性是导致抗病毒治疗困难和耐药性产生的重要原因之一。
替拉瑞韦:一种HCVNS34A蛋白酶抑制剂
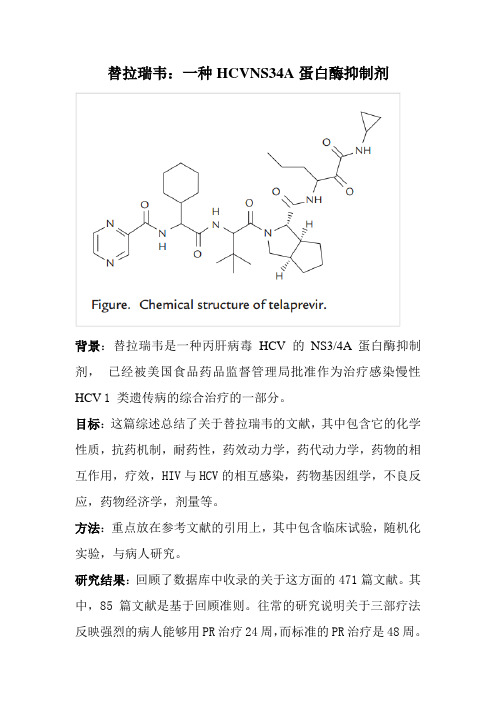
替拉瑞韦:一种HCVNS34A蛋白酶抑制剂背景:替拉瑞韦是一种丙肝病毒HCV的NS3/4A 蛋白酶抑制剂,已经被美国食品药品监督管理局批准作为治疗感染慢性HCV 1 类遗传病的综合治疗的一部分。
目标:这篇综述总结了关于替拉瑞韦的文献,其中包含它的化学性质,抗药机制,耐药性,药效动力学,药代动力学,药物的相互作用,疗效,HIV与HCV的相互感染,药物基因组学,不良反应,药物经济学,剂量等。
方法:重点放在参考文献的引用上,其中包含临床试验,随机化实验,与病人研究。
研究结果:回顾了数据库中收录的关于这方面的471篇文献。
其中,85篇文献是基于回顾准则。
往常的研究说明关于三部疗法反映强烈的病人能够用PR治疗24周,而标准的PR治疗是48周。
两个报道总结T加PR治疗方法非常不划算,由于替拉瑞韦价格昂贵。
一个报道称,假如感染了HCV的1类遗传病的患者比例达到50%,那么T加PR疗法将会非常划算。
结论:替拉瑞韦作为治疗慢性HCV 1类遗传病制剂的一部分,极大地增加了把SVR应用于PR的病人成功的可能性。
然而,由于高昂的费用,包含替拉瑞韦在内的三部疗法可能仅限于应用在对两步疗法反应性低的病人上面。
耐药性的机制:替拉瑞韦包含一个单股的,长达9600个核苷酸的核糖核酸RNA基因组,在绑定在要紧的细胞核糖体之后,HCV 的RNA基因组转变为一个大的多聚蛋白质,这个又反过来转变为受感染的细胞内质网状质的结构型的蛋白质(核心,E1,E2,P7)与非结构型的蛋白质(NS2, NS3, NS4A,NS4B与NS5B)。
结构性的蛋白质参与了完整的病毒的形成,它从细胞里面出来,再感染其他细胞。
非结构性的蛋白质关于HCV的RNA基因组与病毒的复制非常重要。
替拉瑞韦是一个可逆的HCV NS3/4A丝氨酸的 PI。
非结构性的蛋白质3既有蛋白酶又有解旋酶的活性,而且病毒性的NS4A辅因子蛋白质关于NS3是务必的。
替拉瑞韦通过两步附着在 NS3/4A蛋白酶上。
抗丙型肝炎病毒药物研究进展

抗丙型肝炎病毒药物研究进展王靖;何小羊【期刊名称】《国际药学研究杂志》【年(卷),期】2015(42)5【摘要】慢性丙型肝炎病毒(HCV)感染是全球性的公共卫生问题之一,可导致严重的肝病,包括肝硬化及肝癌. 传统的标准治疗方案利巴韦林+聚乙二醇化干扰素对病毒响应率低,副作用大,难以有效治疗HCV感染. 近年来,多种新类型HCV抑制剂得以开发,包括直接抗病毒药物(DAA)以及宿主靶向药物. 这些药物针对病毒生命周期中的必需蛋白,主要包括NS3/4A蛋白酶、NS5B聚合酶、NS5A蛋白或病毒复制相关宿主因子,具有较高的抗病毒活性及良好的安全性和耐受性. 核苷类NS5B聚合酶抑制剂sofosbuvir的成功上市,使HCV的治疗取得了突破性进展.本文综述了近年来抗HCV药物的发展情况,总结了各类抗HCV药物的结构、作用机制及相关抗病毒性质.%Chronic hepatitis C virus (HCV) infection is one of global public health problems, and predominantly results in severe hepatic diseases including hepatic cirrhosis and hepatocellular carcinoma. The traditional standard of care for chronic HCV is the combination of ribavirin and pegylated interferon, which is insufficient to cure the HCV infection due to the suboptimal sustained viral response and severe side effects. Recently new therapeutic approaches have been developed, including direct-acting antiviral agents (DAA) and host-targeting agents, which target essential proteins or host factors in HCV life cycle, such as NS3/4A protease, NS5B polymerase and NS5A protein. These agents exhibit high efficacy,improving safety and tolerability. Thus, the approval of the nucleotide polymerase inhibitor sofosbuvir provides a breakthrough therapy against chronic hepatitis C infection. This review describes the current different classes of HCV inhibitors during the last decades, and their chemical structures, mechanisms and related anti-viral property.【总页数】10页(P551-560)【作者】王靖;何小羊【作者单位】450001郑州,郑州大学药学院;100850北京,军事医学科学院放射与辐射医学研究所;100850北京,军事医学科学院放射与辐射医学研究所【正文语种】中文【中图分类】R916.1;R916.2【相关文献】1.抗丙型肝炎病毒新型药物研究进展 [J], 罗燕2.抗丙型肝炎病毒药物研究进展 [J], 吴晓明;王国成;刘斌3.抗丙型肝炎病毒药物评价模型研究进展 [J], 王小红4.抗丙型肝炎病毒药物的研究进展 [J], 曾菁;彭芳5.直接抗丙型肝炎病毒药物的药物相互作用 [J], 姜波;陈万生因版权原因,仅展示原文概要,查看原文内容请购买。
慢性丙型肝炎治疗药物蛋白酶抑制剂研究进展

慢性丙型肝炎治疗药物蛋白酶抑制剂研究进展
李秀池;肖召安
【期刊名称】《中国药业》
【年(卷),期】2014(000)013
【摘要】慢性丙型肝炎是由丙型肝炎病毒( HCV )引起的一种常见的慢性肝病。
感染病毒后,患者一般无明显症状,少数可出现全身乏力、食欲减退、恶心和右季肋部疼痛或不适,也可伴有低热或黄疸,实验室检查血清中抗-HCV及HCV-RNA 阳性。
如果HCV-RNA阳性无论肝功能是否正常,均应规范治疗。
慢性丙型肝炎的治疗主要是用干扰素联合利巴韦林,在治疗方案的基础上若能引入蛋白酶抑制剂则可获得更佳的疗效。
该文对蛋白酶抑制剂的研究进展进行了综述。
【总页数】2页(P113-114)
【作者】李秀池;肖召安
【作者单位】重庆市开县人民医院药剂科,重庆 405400;重庆市开县人民医院药剂科,重庆 405400
【正文语种】中文
【中图分类】R978.7
【相关文献】
1.慢性丙型肝炎特异性靶向治疗药物的研究进展 [J], 杨艳华;谢青
2.慢性丙型肝炎治疗新纪元——口服逆转录酶和蛋白酶抑制剂的临床应用 [J], 丁洋;夏婷婷;窦晓光
3.慢性丙型肝炎患者NS3/4A蛋白酶抑制剂预存耐药的临床研究 [J], 李展翼;严颖;刘莹;蔡庆贤;赵志新
4.慢性丙型肝炎病毒感染治疗药物研究进展 [J], 高传义;李勇;惠守红;徐莹
5.慢性丙型肝炎的治疗药物研究进展 [J], 王为;周国华
因版权原因,仅展示原文概要,查看原文内容请购买。
丙肝最新治疗方案

丙肝最新治疗方案丙肝最新治疗方案简介丙肝,全称为丙型肝炎(Hepatitis C),是由丙型肝炎病毒(HCV)引起的一种肝炎病毒感染。
该病毒通过血液传播,通常由注射毒品共用针头、输血或器官移植等途径传播。
丙肝感染者可能在数周到数十年内无症状,但长期感染可能导致严重的肝脏疾病,如肝硬化和肝癌。
随着医学技术的发展,丙肝的治疗方案也在不断地更新与改进。
本文将介绍一些最新的丙肝治疗方案。
直接抗病毒药物治疗目前,最常用且最有效的丙肝治疗方案是直接抗病毒药物(Direct-Acting Antiviral Agents, DAA)的联合治疗。
这些药物通过直接抑制病毒的复制过程,从而干扰病毒的生命周期,减少病毒在体内的数量。
药物分类直接抗病毒药物主要分为三类:NS3/4A蛋白酶抑制剂、NS5A蛋白酶抑制剂和NS5B聚合酶抑制剂。
常用的直接抗病毒药物有:- NS3/4A蛋白酶抑制剂:包括代表药物有Telaprevir和Boceprevir等;- NS5A蛋白酶抑制剂:如Ledipasvir、Daclatasvir等;- NS5B聚合酶抑制剂:例如Sofosbuvir、Dasabuvir等。
治疗方案选择在制定治疗方案时,医生会根据患者的病毒基因型、临床表现、肝功能等因素来选择合适的药物组合。
一般来说,根据不同的基因型和治疗史,丙肝患者可以选择以下几种治疗方案:1. 单药制剂方案:使用某一种直接抗病毒药物进行治疗;2. 双药制剂方案:联合使用两种直接抗病毒药物进行治疗;3. 三药制剂方案:联合使用三种直接抗病毒药物进行治疗。
治疗疗程与疗效直接抗病毒药物治疗丙肝的疗程一般为8至24周,具体疗程根据患者的基因型、治疗史和肝功能而定。
治疗结束后,医生会根据病毒消失的情况进行复查,以确定是否达到治愈的效果。
根据研究数据显示,直接抗病毒药物治疗的成功率可高达90%以上。
个体化治疗与合并疗法在某些特殊情况下,医生可能会采用个体化治疗方案或结合其他治疗方法来提高治疗效果。
抗丙肝治疗方案

抗丙肝治疗方案概述丙肝,即丙型肝炎,是由丙型肝炎病毒(HCV)引起的一种传染性疾病,主要通过血液传播。
该病毒可引起急性或慢性肝炎,长期感染可能导致肝硬化、肝癌等严重后果。
抗丙肝治疗方案的目标是消除病毒、预防肝炎的进展,并改善患者的肝功能。
抗丙肝治疗药物直接作用的抗病毒药物目前,丙肝的主要治疗药物是直接作用的抗病毒药物(DAA),它们通过抑制病毒的复制和繁殖来达到治疗的效果。
常用的DAA药物包括:1.NS3/4A蛋白酶抑制剂:包括西帕韦(Simeprevir)、布卡韦(Boceprevir)、提泊特(Telaprevir)等。
2.NS5A蛋白抑制剂:包括达卡他韦(Daclatasvir)、卡巴韦(Ledipasvir)等。
3.NS5B聚合酶抑制剂:包括索非布韦(Sofosbuvir)、维杀力(Velpatasvir)等。
抗丙肝治疗方案根据患者的具体情况,抗丙肝治疗方案可以有所不同。
常见的治疗方案包括:1.常规治疗方案:包括使用干扰素和利巴韦林的联合治疗。
这种方案的疗程通常为24到48周,治疗成功率相对较低,并且会出现较多的副作用。
2.DAA治疗方案:DAA药物的出现使得丙肝的治疗更加简单和有效。
根据丙肝病毒基因型和患者的肝功能等因素,可以选择不同的DAA药物组合来进行治疗。
治疗疗程通常为8到12周,治疗成功率高达90%以上。
此外,DAA治疗方案的副作用较少,对患者的生活质量影响较小。
抗丙肝治疗的注意事项治疗前的准备工作在开始抗丙肝治疗之前,患者需要进行一系列的检查,以了解丙肝的病情和肝功能状态。
这些检查包括肝功能测试、病毒基因型检测、肝炎病毒血清学检测等。
此外,患者还需要告知医生自己是否有其他慢性疾病、是否正在使用其他药物等信息,以便医生制定个性化的治疗方案。
治疗期间的注意事项在接受抗丙肝治疗期间,患者应注意以下事项:1.遵守医生的用药指导:按照医生的建议,准确地进行药物的使用,注意剂量和疗程。
2.定期复查肝功能:在治疗期间,定期进行肝功能检查,以了解丙肝病情的变化和治疗效果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CHEMISTRY THE CHINESE CHEM. SOC., TAIPEIJune. 2006 Vol. 64, No.2, pp.225~234NS3-4A亮1* 1 力2*1 立2 ValeantNS3-4A 利 NS3-4A 類 來 臨 類NS3-4A 類hepatitis C virus, HCV 類 類 狀 了 療 不 惡 (cirrhosis) (liver failure) (hepatocellular carcinoma)1 療HCV RNA 類 host cell (uncoating) RNA (single-stranded RNA genome) RNA (life cycle) 1) (translation) 列 2) (template) (replicate) RNA 3) RNA 粒 類 HCV 異2 療 來了 -α(Interferon-α) ribavirin 類 50% 3, 4 更 更NS3-4A226 年 六HCV RNA 利 (codons) (encode) 裂 ( ) (capsid) (envelop) (structural protein) (core protein) E1, E2糖 (glycoprotein) 離 (integral membrance protein) P7 六(nonstructural protein),NS2, NS3, NS4A, NS4B, NS5A NS5B裂(signal peptidase)來切 C/E1, E1/E2, E2/P7 P7/NS2 (virally encoded)NS2 (NS2 autoprotease)來切 NS2/NS3 連 NS3-4A (NS3-4A serine protease) 行 切 來 裂 3, 5 理論 便 領 NS3-4A RNA (polymerase) (inhibitor) 兩 6NS3-4A x-ray異 (heterodimeric) 了 20kDa NS3 N- (N-terminus domain) (cofactor) NS4A 7, 8 (chymotrypsin)狀 兩 NS3-4A離 來NS3-4ANS3-4A 理 NS3-4A (peptide substrate) 度 類 (inhibitor) (substrate binding site) 了 (cavity) (flap) 9不利 不 NS3-4A 裂 10, 11 (in vitro) NS3-4A 不 度 (leads) 數 (peptidomimetic) (drug candidate) 來(1) BILN 2061 1998年 Boehringer Ingelheim了 NS5A/5B 裂 N- 六 (DDIVPC-OH, 1) NS3-4A (IC 50 = 71µM)10 1 N-(2, IC 50 = 28µM) C- (C-terminus) cysteine 12 3(IC 50 = 150 µM) 4(IC 50 = 54 µM)HCV RNA年 六 227norvaline 1-aminocyclopropyl carboxylic acid 來 略 六C- N- P2 proline 不 P4 P5 了 13了 行 (structure-activity relationship)量 來不 proline 3 proline C-3benzyloxy 5 IC 50 = 7 µM) 3 20 naththen-1-ylmethoxy (6, IC 50 = 0.39 µM) 400 若 P4 P5(residue) NS3-4A nM 數量 7(IC 50 = 0.027 µM) 8(IC 50 = 0.013 µM)H 2P1P6P2P3P4P51 23 45 6 7 8228 年 六類 例 不易 利 度(bioavailability) (conformational flexibility) 14 Boehringer Ingelheim 行 類 類 類 不 類 (molecular modeling) X-ray 15 (protease -ligand complex) 行了六5 NS3 ( ) 8a六 (P1 → P4 ) S1-S3 binding pocket P5P6 不參 裸露 六 P3 異 P1 P1 α 理 論 P1 P3 連 來 力 16, 179 IC 50 = 0.047 µM) 10 IC 50 = 0.011µM) 9 10 4 10(EC 50 = 0.077 µM) 9(EC 50 > 5.0µM) 10 scaffold 了 drug candidate BILN 2061(11)18P1P6P2P3P4P55 NS3 (docking)332H臨 (clinical trials) NS3 BILN 2061 HCV (genotype 1b: Ki = 0.66 nM; genotype 1a: Ki = 0.30 nM) 19 pharmacokinetic 了不 臨 24-28 量(virus load) 降 臨 II 20 不 不 若 異(mutation) BILN 2061 (Asp168, Ala156, Arg155) ( ) BILN 2061 類 行 BILN 2061 21BILN 2061 NS3-4A年 六 229H2Me+Boc2H2RTBTU, DIPEA, DMF2MeHCl / dioxane2MeNOHCO2MeMeODIED, PPh32Me21) NaOH, THF-MeOH-H2O2) i-BuOCOCl, Et3N, thenCH2N2/Et2O3) HBr, THF4) i-PrNHCSNH2, i-PrOH2Me2BILN 2061BILN 2061230 年 六(2) VX-950VX-950(12) Vertex/Mitsubishi Eli Lilly NS3-4A 類 不 類 peptidyl aldehydes peptidyl carboxylic acids peptidyl α-ketoamides peptidyl α-ketoacids 都 22 α-ketoamides 力 類 ketoamide C- 23α -ketoamide六 VX-950 行 略24 例 13 P2 不 bicycloproline P1′ A-A ′ (IC 50 (µM) / A-A ′: 0.123; B-A ′: 0.30; A-B ′ : 2.60; B-B ′: 0.315)臨 preclinical VX-950 異 (genotype 1b: IC 50 = 354 nM, genotype 1a: IC 50 = 280 nM) VX-950 臨 II 25 24cP2P1'R' =NH A'NH PhB'P2 modified analogues:P3P 3P1P 3VX-950VX-950年 六 231(3) Schering-Plough Research InstituteNS3-4ASchering-Plough Research Institute 類SCH 503034(14) 臨 I 28 VX-950α-ketoamide了 (Ki = 14nM) SCH 503034 療降 27 SCH 503034( 六)28SCH 503034 Schering-Plough Research Institute 了 列 類 (15 → 18)29 (Ki = 15 nM)x-ray 類 利(Ser139)Ala156 29b, cH 2CH 3+BocHN O OH N2CH 3O BocHN CH tert-butyl isocyanate 3SCH 503034(14)HCl 六 SCH 503034232 年 六1513論來 類 力 來 異 領 不 力 了 HCV NS3-4A 都不 度 了 理 力 識 益 參參 料1.Cohen, J. et al. Science 1999, 285, 26-30.2.Neumann, A. U. et al. Science 1989, 282, 103-107.3.Di Bisceglie, A. M.; McHutchison, J.; Rice, C. M. Herpetology 2002, 35, 224-231.4.(a) Chander, G. Herpetology 2002, 36, 135. (b) Lesk, A. M.; Fordham, W. D. J. Mol. Biol . 1996, 28, 551-557.(c) Hoofmagle, J. H.; Di Bisceglie, A. M. N. Engl. J. Med . 1997, 336, 347-351.5.(a) Lindenbach, B. D.; Rice, C. M. Science 2005, 436, 933-938. (b) Choo, O. L. et al. Science 1989, 244, 359-364.6.(a) Francesco, R. D.; Migliaccio, G . Science 2005, 436, 953-960. (b) Bartenschlagar, R. Antiviral Chem. Chemother . 1997. 8, 281-288.7.Dubuisson, P. F.; Rey, F. A.; Moradpour, D.; Pawlotsky, J. M. Herpetology 2004, 39, 5-19.8.(a) Love, R. A. et al. Cell 1996, 87, 331-342. (b) Kim J.L. et al . Cell 1996, 87, 343-355. (c) Yan, Y . et. al . Protein Sci . 1998, 7, 837-847. (d) Yao, N.; Hesson, T.; Cable, M.; Hong, Z.; Kwong, A. D.; Le, H. V .; Weber, P. C. Nat. Struct. Biol . 1997, 4, 463-467.9.Yan, Y . et al. Cell 1996, 87, 837-847.10.Brunet, M. L.; Bailey, M.; Fazal, G.; Goulet, S.; Halmos, T.; Laplante, S.; Maurice, R.; Poirier, M.; Poupart, M. A.; Thibeault, D.; Wernic, D.; Lamarre, D. Bioorg. Med. Chem. Lett . 1998, 8, 1713-1718.11.Stinkuhler, C.; Biasiol, G .; Brunetti, M.; Urbani, A.; Koch, U.; Cortese, R.; Pessi, A.; De Francesco, R. Biochemistry 1998, 37, 8899-8905.12.Llinas _ Brunet, M et al. Bioorg. Med. Chem. Lett . 1998, 8, 2719-2723.13.Llinas _ Brunet, M et al. Bioorg. Med. Chem. Lett . 2000, 10, 2267-2270.14.Williams D. A.; Lemke, T. L. “Foye’s Principles of Medicinal Chemistry ” Fifth Edition, Lippincott Williams & Wilkins, pp 114-142.15.(a) LaPlante, S. R. et al . J. Biol. Chem . 1999, 274, 18618-18625. (b) Cicero, D. O. et al . J. Mol. Biol. 1999, 289, 385-393. (c) Barbato, G. et al. EMBO J . 2000, 19, 1195-1202. (d) Di. Marco, S. et al . J. Biol. Chem . 2000, 275, 7152-7158.年 六 23316.(a) Poupart, M. A. et al.J. Org. Chem. 2001, 66,4743-4750. (b) Tsantrizos Y. S. et al. PTC Patent.[Boehringer Ingelheim Ltd.] WO 00/59929 2000. (c) Goudreau, N. et al. J. Org. Chem. 2004, 69, 6185-6201. 17.Tsantrizos Y. S. et al. Angew. Chem. Int. Ed. 2003, 42,1356-1360.18.Llinas _ Brunet, M et al .J. Med. Chem. 2004, 47,1605-1608.marre D. et al. Nature, 2003, 426, 186-190.20.(a) Lin, C. et al. J. Biol. Chem. 2004, 279, 17508-17514.(b) Lin, C. et. al. J. Biol. Chem. 2005, 280,36784-36791.21.Faucher, A. M. et al. Org. Lett. 2004, 6, 2901-2904.22.(a) Tung, R. et al. PCT Patent (Vertex): WO/98/17679,10/18/1996. (b) PCT patent (Vertex): WO/99/50230, 3/31/1998. (c) Perni, R. B. Bioorg. Med. Chem. 2003, 13, 4059-4062. (d) PCT patent (BI): WO/99/07734, 11/8/1997 (e) Tung, R. et al. US Patent (Vertex) 6, 265, 380 B1, 7/24/2001. (f) PCT patent: WO/99/64442, 10/6/1998. 23.(a) Perni, R. B. et al. Antimicrobial, Agents andChemother.2006, 50, 899-909. (b) Ingallinella, P.Biochemistry2002, 41, 5483-5488.24.(a) Yvonne Y. et al. Bioorg. Med. Chem. Lett.200414,251-256. (b) Frantz V. et al. Bioorg. Med. Chem. Lett.200414, 257-261. (c) Chen, S. H. et al. Letters in Drug Design & Discovery2005, 2, 118-123. (d) Yvonne Y. et al. Bioorg. Med. Chem. Lett. 200414, 5007-5011.25.Vincenzo, S. Current Option in Investigational Drugs(Thomson Scientific) 2005, 6(8), 831-837.26.Malcolm, B. C. et al. Antimicrobial, Agents andChemother.2006, 50, 1013-1020.27.Tong X. et al. Antiviral Research2006, 70, 28-38.28.Njooroge, F. G. et al. US Patent (Schering-OloughCorporation): US/2005/0249702 A1, 11/10/2005.29.(a) Chen, K. X. et al. J. Med. Chem. 2006, 49, 995-1005.(b) Chen, K. X. et al. J. Med. Chem. 2006, 49, 567-574.(c) Chen, K. X. et al. Angew. Chem. Int. Ed. 2005, 44,7024-7028. (d) Chen, K. X. et al. J. Med. Chem. 2005, 48, 6229-6235.234 年 六 The Development of Inhibitors of the HepatitisC Virus NS3-4A Serine ProteaseJia-Liang Zhu*1, Yen-Jun Ko1, Yi-Li Ding*2 1Department of Chemistry, National Dong-Hwa University, Hualien, 974 Taiwan2Valeant PharmaceuticalAbstractIn the life cycle of hepatitis C virus (HCV), NS3-4A serine protease plays an essential role in maturation of viral proteins. Thus, it represents a particularly important target for developing the anti-HCV drugs. In the efforts of inhibiting NS3-4A protease, it was found that some peptide products derived from sequences of the HCV NS3 protease substrates are competitive inhibitors. On the basis of this observation, several peptidomimetic drug candidates have been developed. The discovery processes of them are briefly summarized in this article.Key words: hepatitis C virus (HCV), NS3-4A serine protease, peptidomimetic drugs, inhibitor。
