线路板制造中溶液浓度计算方法
PCB电路板制造中溶液浓度算法

PCB电路板制造中溶液浓度算法在PCB电路板制造过程中,溶液浓度是一个非常重要的因素,对于电路板的质量和性能有着直接的影响。
下面将介绍一种常用的溶液浓度算法,质量比浓度算法。
质量比浓度是指溶液中溶质的质量与溶液总质量的比值。
在PCB电路板制造中,常见的溶液包括腐蚀剂、电镀液等,溶液浓度的调节与控制对于腐蚀和电镀的效果有着重要的影响。
首先,我们需要明确溶液的质量和浓度的概念。
溶液的质量是指溶液中溶质的总质量,单位通常是克(g)。
而溶液的浓度则是指溶质在单位溶液中的质量,通常以质量比表示,单位是克/升(g/L)。
为了准确计算溶液的浓度,我们需要准备好实验室所需的器材:天平、容量瓶和溶液配制用的试剂。
下面是计算溶液浓度的步骤:第一步:准备一个称量瓶,并使用天平将溶质的质量精确称量。
记下溶质的质量,单位是克(g)。
第二步:准备一个容量瓶,并将一定量的溶剂(通常为水)加入容量瓶中。
第三步:将步骤一中称量好的溶质加入到容量瓶中的溶剂中,然后加入足够的溶剂,使溶液的总体积达到预定值。
第四步:摇匀容量瓶中的溶液,使溶质均匀分布在溶液中。
第五步:使用天平将称量瓶中的溶质重量减去空瓶的重量,可以得到溶质的净质量。
第六步:根据步骤五中得到的溶质净质量和容量瓶中溶液的总体积,计算溶液的浓度。
即浓度(g/L)=溶质净质量(g)/溶液总体积(L)。
需要注意的是,在实际操作中,还需要考虑一些其他因素。
比如,溶质在溶液中的溶解度,不同溶质的溶解度是不同的,需要根据实际情况进行调整。
此外,为了保证测量的准确性,还需要进行多次实验,取平均值作为最终结果。
总而言之,质量比浓度是一种常用的溶液浓度算法,在PCB电路板制造过程中起着重要的作用。
通过准确计算溶液的质量和体积,并进行合理控制,可以保证电路板制造质量的稳定和可靠性。
在实际应用中,还需要考虑到多种因素的综合影响,以为制造出优质的PCB电路板提供技术支持。
溶液的配制步骤浓度计算公式是什么

溶液的配制步骤浓度计算公式是什么配制溶液的七大步骤为:计算、称量、溶解、转移、洗涤、定容、摇匀。
溶液浓度计算公式是:浓度计算公式=溶液质量÷溶液质量×100%,而物质的量浓度=溶质的物质的量÷溶液的体积。
质量百分浓度:质量分数,m/m,这是一种最为常见的方法,主要是指的100克的溶液中,溶质的质量,按照克数来计算。
配制溶液的七大步骤计算:计算配制所需固体溶质的质量或液体浓溶液的体积。
根据要配制溶液的量,计算出所需的溶质质量、液体体积,只有准确的计算,配制出来的溶液浓度才能确定,才能保证检验、实验、化验结果的准确性。
称量:用托盘天平称量固体质量或用量筒(应用移液管,但中学阶段一般用量筒)量取液体体积。
对于配制标准溶液,所需的溶质质量需用到分析天平进行精准称量。
溶解:在烧杯中溶解或稀释溶质,恢复至室温,如不能完全溶解可适当加热,并用玻璃棒搅拌。
转移:将烧杯内冷却后的溶液沿玻璃棒小心转入一定体积的容量瓶中,玻璃棒下端应靠在容量瓶刻度线以下。
洗涤:用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入容器中,振荡,使溶液混合均匀。
定容:向容量瓶中加水至刻度线以下1cm~2cm处时,改用胶头滴管加水,使溶液凹面恰好与我们需要配制的溶液体积刻度线相切。
摇匀:盖好瓶塞,用食指顶住瓶塞,另一只手的手指托住瓶底,反复上下颠倒,使溶液混合均匀,然后给溶液装瓶贴签,标注溶液名称,浓度,配制日期,配制人员,保质日期等信息。
溶液浓度计算公式是什么浓度计算公式=溶液质量÷溶液质量×100%,而物质的量浓度=溶质的物质的量÷溶液的体积。
常见的浓度表示法有三种:质量百分浓度:质量分数,m/m,这是一种最为常见的方法,主要是指的100克的溶液中,溶质的质量,按照克数来计算。
溶质的百分浓度:(溶质质量(g))/溶液质量(g))×100%=溶质质量(g))/(溶质质量(g)+溶剂质量(g))×100%。
化学溶液与浓度计算

化学溶液与浓度计算化学溶液是由溶质和溶剂组成的混合物,其中溶质是溶解在溶剂中的物质。
溶液的浓度是衡量溶质在溶液中的相对数量的指标。
了解并能够计算溶液的浓度对于化学实验和工业生产中的配制溶液和控制反应条件非常重要。
本文将介绍几种常见的用于计算化学溶液浓度的方法和公式。
1. 质量百分比(w/w)浓度计算质量百分比是指溶质质量占整个溶液质量的比例。
计算公式如下:质量百分比(w/w)= (溶质的质量 / 溶液的质量) × 100%例子:假设我们有一个溶液中含有80克的溶质,总质量为200克,那么该溶液的质量百分比浓度为:质量百分比(w/w)= (80克 / 200克) × 100% = 40%2. 体积百分比(v/v)浓度计算体积百分比是指溶质体积占整个溶液体积的比例。
计算公式如下:体积百分比(v/v)= (溶质的体积 / 溶液的体积) × 100%例子:如果我们有100毫升的溶液,其中溶质的体积是20毫升,那么该溶液的体积百分比浓度为:体积百分比(v/v)= (20毫升 / 100毫升) × 100% = 20%3. 摩尔浓度(mol/L)计算摩尔浓度是指单位体积(通常是升)的溶液中溶质的摩尔数。
计算公式如下:摩尔浓度(mol/L)= 溶质的摩尔数 / 溶液的体积(升)例子:假设我们有0.5摩尔的溶质溶解在1升的溶液中,那么该溶液的摩尔浓度为:摩尔浓度(mol/L)= 0.5摩尔 / 1升 = 0.5 mol/L4. 摩尔分数计算摩尔分数是指溶质的摩尔数占整个溶液摩尔数总和的比例。
计算公式如下:摩尔分数 = 溶质的摩尔数 / (溶质的摩尔数 + 溶剂的摩尔数)例子:假设我们有2摩尔的溶质和3摩尔的溶剂,那么该溶液中溶质的摩尔分数为:摩尔分数 = 2摩尔 / (2摩尔 + 3摩尔) = 0.4化学溶液与浓度计算对于研究溶解反应、催化剂的使用、溶解度的调节等领域都具有重要意义。
溶液的浓度及其计算方法

溶液的浓度及其计算方法溶液是由溶剂和溶质组成的均匀混合物。
溶剂是溶解其他物质的介质,而溶质是溶解在溶剂中的物质。
溶液的浓度是描述溶液中溶质含量的一个指标,它反映了溶液中溶质的多少。
常用的溶液浓度单位有质量分数、摩尔浓度等。
一、质量分数质量分数是溶液中溶质的质量与溶液总质量之比,用百分数表示。
计算公式为:质量分数 = (溶质质量 / 溶液总质量) × 100%二、摩尔浓度摩尔浓度是溶液中溶质的物质的量与溶液体积之比,用摩尔/升(mol/L)表示。
计算公式为:摩尔浓度 = (溶质物质的量 / 溶液体积)三、物质的量浓度物质的量浓度是溶液中溶质的物质的量与溶液体积之比,用摩尔/升(mol/L)表示。
计算公式为:物质的量浓度 = (溶质物质的量 / 溶液体积)四、质量摩尔浓度质量摩尔浓度是溶液中溶质的质量与溶液体积之比,用克/升(g/L)表示。
计算公式为:质量摩尔浓度 = (溶质质量 / 溶液体积)五、稀释溶液稀释溶液是指将浓溶液加入适量的溶剂中,使其浓度降低的过程。
稀释溶液时,溶质的物质的量不变,只有溶剂的体积增加。
根据稀释定律,稀释前后溶质的物质的量相等,可以得到以下关系:原溶液的物质的量浓度 × 原溶液体积 = 稀释后溶液的物质的量浓度 × 稀释后溶液体积六、溶液的配制配制溶液时,首先要计算所需的溶质质量和溶剂体积,然后将溶质溶解在溶剂中。
在配制一定浓度的溶液时,可以通过上述的计算公式来确定所需的溶质质量和溶剂体积。
七、溶液的性质溶液具有均一性和稳定性的特点。
均一性意味着溶液中溶质和溶剂混合均匀,稳定性意味着溶液的浓度在一定条件下不会发生变化。
综上所述,溶液的浓度及其计算方法是化学中的基本知识点。
掌握质量分数、摩尔浓度等浓度单位及其计算方法,能够帮助我们更好地理解和应用化学知识。
习题及方法:1.习题:某溶液中溶质的质量分数为10%,如果向该溶液中加入10克水,求稀释后溶液的质量分数。
配制溶液的浓度计算公式(一)

配制溶液的浓度计算公式(一)配制溶液的浓度计算公式在化学实验中,我们经常需要配制溶液,而溶液的浓度是一个非常重要的参数。
下面将列举几种常见的配制溶液浓度计算公式,并进行举例解释说明。
1. 体积浓度(C)体积浓度是指单位体积溶液中所含溶质的质量或物质的量。
体积浓度的计算公式为:C = m / V其中,C为体积浓度,m为溶质质量,V为溶液体积。
例子:如果我们有5克氯化钠溶解在100毫升水中,求该溶液的体积浓度。
解答:根据体积浓度的计算公式,我们可以得到:C = 5g / 100mL = g/mL因此,该溶液的体积浓度为 g/mL。
2. 摩尔浓度(C)摩尔浓度是指单位体积溶液中所含溶质的物质的量。
摩尔浓度的计算公式为:C = n / V其中,C为摩尔浓度,n为溶质的物质的量(单位为摩尔),V为溶液体积(单位为升)。
例子:如果我们有摩尔盐酸溶解在1升水中,求该溶液的摩尔浓度。
解答:根据摩尔浓度的计算公式,我们可以得到:C = mol / 1L = mol/L因此,该溶液的摩尔浓度为 mol/L。
3. 百分比浓度百分比浓度是指溶质的质量和溶液的质量之间的比值,以百分数表示。
百分比浓度的计算公式为:百分比浓度(%)= (m溶质 / m溶液) × 100%其中,m溶质为溶质的质量,m溶液为溶液的质量。
例子:如果我们有25克盐溶解在100克溶液中,求该溶液的百分比浓度。
解答:根据百分比浓度的计算公式,我们可以得到:百分比浓度= (25g / 100g) × 100% = 25%因此,该溶液的百分比浓度为25%。
4. 摩尔分数(X)摩尔分数是指溶质的摩尔数和溶液中总物质的摩尔数之比。
摩尔分数的计算公式为:X = n溶质 / n溶液其中,X为摩尔分数,n溶质为溶质的摩尔数,n溶液为溶液中总物质的摩尔数。
例子:如果我们有2摩尔氯化钠和1摩尔水混合,求氯化钠的摩尔分数。
解答:根据摩尔分数的计算公式,我们可以得到:X = 2 mol / (2 mol + 1 mol) =因此,氯化钠的摩尔分数为。
溶液中的各种浓度计算方法

溶液中的各种浓度计算方法在化学实验中,我们常常需要计算溶液的浓度。
溶液浓度是指溶质相对于溶剂的比例或含量的测量,通常用浓度来表示。
在本文中,我们将介绍几种常见的溶液浓度计算方法。
一、质量浓度(C)质量浓度是指溶质在溶液中的质量与溶液总质量之比。
通常用C表示,其计算公式为:C = (质量溶质 / 体积溶液) × 100%其中,质量溶质表示溶质的质量,体积溶液表示溶液的体积。
例如,某溶液中含有25g的盐溶解在500mL的水中,我们可以通过以下计算得到溶液的质量浓度:C = (25g / 500mL) × 100% = 5%二、体积浓度(Cv)体积浓度是指溶质在溶液中的体积与溶液总体积之比。
它常用于气体溶解度的计算。
计算公式如下:Cv = (体积溶质 / 体积溶液) × 100%其中,体积溶质表示溶质的体积,体积溶液表示溶液的体积。
例如,某气体在100mL的水中溶解了15mL,我们可以通过以下计算得到气体溶解度的体积浓度:Cv = (15mL / 100mL) × 100% = 15%三、摩尔浓度(Cm)摩尔浓度是指溶质的摩尔数与溶液总体积之比。
其计算公式如下:Cm = 摩尔数 / 体积溶液其中,摩尔数表示溶质的摩尔数,体积溶液表示溶液的体积。
例如,某溶液中含有0.2 mol的氯化钠,并且溶液体积为200 mL,我们可以计算出溶液的摩尔浓度:Cm = 0.2 mol / 0.2 L = 1 mol/L四、摩尔分数(X)摩尔分数是指溶质的摩尔数与溶质的摩尔数之和之比。
通常用X表示,其计算公式如下:X = 溶质摩尔数 / (溶质摩尔数 + 溶剂摩尔数)其中,溶质摩尔数表示溶质的摩尔数,溶剂摩尔数表示溶剂的摩尔数。
例如,某溶液中含有0.5 mol的NaCl和0.8 mol的水,我们可以通过以下计算得到NaCl的摩尔分数:X = 0.5 mol / (0.5 mol + 0.8 mol) = 0.38五、百分比体积(%V/V)百分比体积是指溶质的体积与溶液总体积之比,通常以百分数表示。
化学中的溶液的浓度计算

化学中的溶液的浓度计算一、引言溶液是化学中常见的一种物质状态,对于研究溶液的浓度计算是化学学习的基础和重要内容之一。
本教案将围绕化学中的溶液浓度计算展开论述,介绍不同类型的浓度计算方法和应用。
二、溶液的浓度及其表示方法1. 溶液的浓度是指溶质在溶剂中的质量或摩尔量与溶液总质量或溶液总体积之比。
2. 常用的表示溶液浓度的方法有质量百分比、摩尔浓度、体积百分比和体积浓度等。
三、质量百分比溶液浓度计算1. 质量百分比的计算公式为:质量百分比=溶质的质量/溶液的质量×100%。
2. 通过给定溶液中溶质和溶剂的质量,可以计算质量百分比溶液浓度。
四、摩尔浓度计算1. 摩尔浓度是指单位体积溶液中的摩尔量,计量单位为mol/L。
2. 摩尔浓度的计算公式为:摩尔浓度=溶质的摩尔量/溶液的体积。
五、体积百分比溶液浓度计算1. 体积百分比是指溶质在溶液中的体积与溶液总体积之比,计量单位为%。
2. 体积百分比溶液浓度的计算公式为:体积百分比=溶质的体积/溶液的体积×100%。
六、体积浓度计算1. 体积浓度是指单位体积溶液中溶质的体积,计量单位为mL/L。
2. 体积浓度的计算公式为:体积浓度=溶质的体积/溶液的体积。
七、浓度计算的应用举例1. 利用浓度计算可以进行溶液的稀释和浓缩操作,实现目标浓度的溶液。
2. 通过浓度计算可以确定反应物的摩尔比例及产物的摩尔量,为化学反应的设计提供依据。
八、小结通过本教案的学习,了解了溶液的浓度及其表示方法,掌握了质量百分比、摩尔浓度、体积百分比和体积浓度等浓度计算方法,以及浓度计算的应用。
溶液的浓度计算是化学学习中的重要内容,对于深入理解和应用化学知识具有重要意义。
九、参考资料1. 张教授,化学中的溶液浓度计算,化学学习杂志,2018年。
2. 徐老师,化学实验中的浓度计算方法与技巧,化学实验与研究,2019年。
3. 杨同学,溶液浓度计算的应用案例分析,化学应用研究,2020年。
线路板常识

1)、粉红圈的造成原因:由于在沉铜时,压板未能把内层铜和半固化片压紧,这样沉铜时的药水就会从缝隙中渗进去,把里面的内层的黑膜腐蚀掉,这样就会变成一条裂缝,且是粉红圈。
另外造成的厚因:1、树脂与黑氧化结合力不足;2 、prepreg 胶含量不足;3 、压合时,升温太慢4、氧化铜有问题;5、钻孔太猛。
2)、粉状沉铜(即铜粗):1、板子留缸过久;2 、浓度过高;3 、温度过高;4 、活化剂污染铜缸。
3)、铜面颜色呈红或黑色:1、铜缸Temp 低;2、过久停留在活化缸中;3、铜缸浓度低;4、铜缸负荷过重。
4)、孔内无铜主要厚因:1、镀锡锌不良(从切片上可看出,图形电镀是没有包住全板电镀且有的带倾斜状)2 、沉铜出问题(从切片上可看出图形包住全板)3 、干膜塞孔引起(从切片上可看出无铜处是有的地方是有一点铜的图形不包全板)4、 PTH气泡造成(从切片上可看出无铜的地方是对称的,是图形电镀包住全板。
5、图形汽泡(图形不包住全板)6、背光不良(它的无铜与干菲林塞孔的切片差不多,不过它的图形包住全板)5)、绿油塞孔的好处:防止在喷锡时在孔口上有锡球产生,且凝固,有了绿油自然就有一种保护作用。
且只能从CS面进行塞孔,不能双面塞孔因为双面塞孔,中间会有汽泡,一是温度升高会爆炸。
6)、反缸过剧原因:1、温度过高2、浓度过高3 、隋板金属4 、活化剂污染7)、深孔怎样镀铜:垂直挂镀:此时孔呈卧姿,对电流有关,使药水在孔中往复来回,电流密度最大只能15ASF,若孔太深,则更换整流器这种方法高电流与低电流镀铜的厚度凑巧不多,(便宜又经济)。
水平连线自走高速镀铜:优点:槽液自下向上强力涌流,比垂直挂镀镀小孔好完全自动化,无需上下挂架,对薄板镀铜效果更好缺点:成本贵,连线太多,小毛病不断发生,在多产量情况下阳极消耗太快每隔三天就要停机半天;双面有盲孔时,很难克服朝下者孔底铜厚不足。
8)、铜壁太薄会吹孔:原因是在漂锡时孔破太多使基材吸饱水后,在高温中大量的水蒸气向孔中喷出推开液锡造成吹锡。
化学溶液的浓度计算

化学溶液的浓度计算在化学实验中,溶液的浓度是一个重要的参数。
通过对溶液中溶质和溶剂的量的比例进行测量和计算,可以得到溶液的浓度。
本文将介绍几种常用的计算溶液浓度的方法。
一、质量浓度(Mass Concentration)质量浓度是指溶质在溶剂中的质量与溶液总质量之比。
通常用g/mL或g/L表示。
计算公式为:质量浓度(g/mL)= 溶质质量(g)/ 溶液体积(mL)质量浓度(g/L)= 溶质质量(g)/ 溶液体积(L)例如,有100 g NaCl 溶解在1000 mL水中,计算其质量浓度:质量浓度(g/mL)= 100 g / 1000 mL = 0.1 g/mL质量浓度(g/L)= 100 g / 1 L = 100 g/L二、摩尔浓度(Molar Concentration)摩尔浓度是指溶质在溶液中的物质的量与溶液总体积之比。
通常用mol/L表示。
计算公式为:摩尔浓度(mol/L)= 溶质物质的量(mol)/ 溶液的体积(L)例如,有0.5 mol的NaCl溶解在2 L的溶剂中,计算其摩尔浓度:摩尔浓度(mol/L)= 0.5 mol / 2 L = 0.25 mol/L三、体积浓度(Volume Concentration)体积浓度是指溶质在溶液中的体积与溶液总体积之比。
计算公式为:体积浓度(mL/mL)= 溶质体积(mL)/ 溶液体积(mL)体积浓度(L/L)= 溶质体积(L)/ 溶液体积(L)例如,有50 mL的酒精混合在200 mL水中,计算其体积浓度:体积浓度(mL/mL)= 50 mL / 200 mL = 0.25 mL/mL体积浓度(L/L)= 0.05 L / 0.2 L = 0.25 L/L四、等级法浓度(Normality)等级法浓度是指溶液中含有1摩尔的化学当量的物质。
计算公式为:等级法浓度(N)= 溶质化学当量(mol)/ 溶液的体积(L)例如,有0.2 mol的HCl溶解在1 L的溶液中,计算其等级法浓度:等级法浓度(N)= 0.2 mol / 1 L = 0.2 N综上所述,我们介绍了几种常用的化学溶液浓度计算方法,包括质量浓度、摩尔浓度、体积浓度和等级法浓度。
PCB制造之溶液浓度计算方法

PCB制造之溶液浓度计算方法在印制电路板制造技术,各种溶液占了很大的比重,对印制电路板的最终产品质量起到关键的作用。
无论是选购或者自配都必须进行科学计算。
正确的计算才能确保各种溶液的成分在工艺范围内,对确保产品质量起到重要的作用。
根据印制电路板生产的特点,提供六种计算方法供同行选用。
1.体积比例浓度计算:•定义:是指溶质(或浓溶液)体积与溶剂体积之比值。
•举例:1:5硫酸溶液就是一体积浓硫酸与五体积水配制而成。
2.克升浓度计算:•定义:一升溶液里所含溶质的克数。
•举例:100克硫酸铜溶于水溶液1 0升,问一升浓度是多少?100/10=10 克/ 升3.重量百分比浓度计算(1) 定义:用溶质的重量占全部溶液重理的百分比表示。
(2) 举例:试求3克碳酸钠溶解在100克水中所得溶质重量百分比浓度? 4.克分子浓度计算•定义:一升中含1 克分子溶质的克分子数表示。
符号:M、n 表示溶质的克分子数、V 表示溶液的体积。
如:1升中含1克分子溶质的溶液,它的克分子浓度为1M含1/10克分子浓度为0.1M,依次类推。
•举例:将100克氢氧化钠用水溶解,配成500毫升溶液,问这种溶液的克分子浓度是多少?解:首先求出氢氧化钠的克分子数:5. 当量浓度计算•定义:一升溶液中所含溶质的克当量数。
符号:N(克当量/升)•当量的意义:化合价:反映元素当量的内在联系互相化合所得失电子数或共同的电子对数。
这完全属于自然规律。
它们之间如化合价、原子量和元素的当量构成相表关系。
元素=原子量/ 化合价•举例:钠的当量= 23/仁23;铁的当量=55.9/3=18.6•酸、碱、盐的当量计算法:A酸的当量=酸的分子量/酸分子中被金属置换的氢原子数B碱的当量=碱的分子量/碱分子中所含氢氧根数C盐的当量=盐的分子量/盐分子中金属原子数金属价数6.比重计算•定义:物体单位体积所有的重量(单位:克/ 厘米3)•测定方法:比重计。
•举例:A.求出100毫升比重为1. 42含量为69%的浓硝酸溶液中含硝酸的克数?解:由比重得知1 毫升浓硝酸重1. 42 克;在1. 42 克中69% 是硝酸的重量,因此1 毫升浓硝酸中硝酸的重量=1.42 X (60/100)=0.98(克)•B.设需配制25克/升硫酸溶液50升,问应量取比量1. 84含量为98%硫酸多少体积?解:设需配制的50升溶液中硫酸的重量为W则W 25克/升50 =1250克由比重和百分浓度所知,1 毫升浓硫酸中硫酸的重量为:1.84 X(98/100)= 18(克);则应量取浓硫酸的体积1250/18 = 69. 4(毫升)•波美度与比重换算方法:A.波美度二144.3-(144.3/ 比重);B = 144.3/(144.3- 波美度)。
PCB电路板制造中溶液浓度算法

PCB电路板制造中溶液浓度算法在PCB电路板制造过程中,溶液浓度的控制是非常关键的一个环节。
正确的溶液浓度可以保证电路板的质量和稳定性,而不正确的溶液浓度则可能导致电路板质量不稳定,甚至出现故障。
因此,制造过程中要根据实际情况来调整和控制溶液的浓度,以确保电路板的质量。
一般来说,溶液的浓度是通过溶质的质量与溶剂的质量之比来表示的。
在PCB电路板制造中,常用的溶液包括酸性浸镀铜溶液、酸性蚀刻剂溶液、清洗剂溶液等。
这些溶液的浓度直接影响着电路板的制作效果和质量。
对于酸性浸镀铜溶液来说,其主要成分是铜盐和酸。
铜盐的浓度应该在一定范围内,以保证电路板表面的镀铜均匀性和质量。
通常情况下,铜盐的浓度应该控制在5-25g/L之间。
酸的浓度也是非常重要的,一般情况下,酸的浓度应该在10-100g/L之间。
如果浓度过低,可能导致电路板表面粗糙度增加,甚至影响到电路板的导电性能;如果浓度过高,可能导致电路板表面铜层表面变得坚硬,不易粘贴其他元件。
对于酸性蚀刻剂溶液来说,其主要成分是酸和氯化物。
酸的浓度通常在5-50g/L之间,氯化物的浓度通常在20-100g/L之间。
酸蚀刻可以在一定程度上去掉电路板上的铜层,因此需要根据具体情况来控制蚀刻液的浓度,以保证蚀刻效果和速度。
除了酸性溶液之外,清洗剂溶液的浓度也是需要注意的。
清洗剂主要是用来去除电路板表面的残留物,以保证电路板表面的干净度和光洁度。
清洗剂的浓度通常在2-10g/L之间,根据实际情况来调整浓度以保证清洗效果。
在制造过程中,通常会根据实际情况来进行溶液的浓度调整。
可以通过配方来控制溶液的成分比例,也可以通过检测来确定溶液的浓度是否在合适的范围内。
常用的检测方法包括电导率测量、PH值测量、密度测量等。
通过这些方法可以准确地确定溶液的浓度,从而保证电路板的质量和稳定性。
总而言之,溶液浓度在PCB电路板制造中是非常重要的一个参数。
正确的溶液浓度可以保证电路板的质量和稳定性,而不正确的溶液浓度则可能导致电路板质量不稳定,甚至出现故障。
溶液的浓度计算与标准溶液制备

溶液的浓度计算与标准溶液制备溶液的浓度是指所溶质的质量或摩尔数与溶剂质量或摩尔数之间的比值。
溶液的浓度计算是化学实验中常用的计算方法,也是一项基本实验技能。
标准溶液则是一种与其它溶液浓度相对固定并经过精确测量的溶液,用于溶液浓度的标定及实验结果的验证。
本文将介绍溶液浓度的计算方法以及标准溶液制备的步骤。
一、溶液的浓度计算溶液的浓度可以用质量浓度、体积浓度和摩尔浓度等表示,下面将分别介绍这些计算方法。
1. 质量浓度计算质量浓度是指单位体积溶液中溶质的质量,计算公式为:质量浓度(g/L)= 溶质的质量(g)/ 溶液的体积(L)例如,如果需要制备1000 mL 浓度为0.5 g/L的盐水溶液,可以按照如下步骤计算所需的盐的质量:质量 = 质量浓度 ×溶液的体积 = 0.5 g/L × 1000 mL = 0.5 g因此,需要称取0.5 g的盐溶解于1000 mL溶剂中即可制备所需的盐水溶液。
2. 体积浓度计算体积浓度是指单位体积溶液中溶质的体积,计算公式为:体积浓度(V/V) = 溶质的体积(mL)/ 溶液的体积(mL)例如,如果需要制备100 mL 体积浓度为20%的乙醇溶液,可以按照如下步骤计算所需的乙醇体积:乙醇的体积 = 体积浓度 ×溶液的体积 = 20% × 100 mL = 20 mL因此,需要取20 mL的乙醇溶解于80 mL溶剂中即可制备所需的乙醇溶液。
3. 摩尔浓度计算摩尔浓度是指单位体积溶液中溶质的物质的摩尔数,计算公式为:摩尔浓度(mol/L)= 溶质的摩尔数(mol)/ 溶液的体积(L)例如,如果需要制备500 mL 摩尔浓度为0.1 mol/L的硫酸溶液,可以按照如下步骤计算所需的硫酸的摩尔数:摩尔数 = 摩尔浓度 ×溶液的体积 = 0.1 mol/L × 0.5 L = 0.05 mol因此,需要取0.05 mol的硫酸溶解于500 mL溶剂中即可制备所需的硫酸溶液。
化学溶液的浓度计算及稀释方法

化学溶液的浓度计算及稀释方法化学溶液的浓度是指单位体积溶液内所含溶质的量。
准确计算和稀释溶液的浓度对于实验室和工业应用都非常重要。
本文将介绍化学溶液浓度的计算方法以及常见的稀释方法。
一、浓度计算方法1. 质量浓度计算质量浓度是指单位溶液质量中溶质的质量,通常用克/升(g/L)表示。
质量浓度的计算公式为:质量浓度 = 溶质质量(g)/ 溶剂体积(L)2. 体积浓度计算体积浓度是指单位溶剂体积中所含溶质的体积,常用的单位为摩尔/升(M),也可以用千克/升(kg/L)或毫摩尔/升(mmol/L)。
体积浓度的计算公式为:体积浓度 = 溶质物质的量(mol)/ 溶剂体积(L)3. 百分浓度计算百分浓度是指溶质质量与溶液总质量之间的比例,通常以百分比表示。
百分浓度的计算公式为:百分浓度 = (溶质质量(g)/ 溶液总质量(g))× 100%4. 摩尔浓度计算摩尔浓度是指单位溶剂体积中所含溶质的物质的量,常用的单位为摩尔/升(M)。
摩尔浓度的计算公式为:摩尔浓度 = 溶质物质的量(mol)/ 溶剂体积(L)二、浓度的稀释方法浓度的稀释是指通过加入溶剂使溶质的浓度降低的过程。
1. 体积稀释法体积稀释法是指通过加入适量的溶剂来减少原有溶液的浓度。
计算稀释后的浓度可以使用以下公式:C1V1 = C2V2其中,C1为初始浓度,V1为初始体积,C2为稀释后浓度,V2为稀释后体积。
2. 纯净溶液配制法纯净溶液配制法是指将一定量的溶质溶解在足够量的溶剂中,制得所需浓度的溶液。
这种方法适用于需要较大量溶液的情况。
3. 级联稀释法级联稀释法是指将初始浓度的溶液连续稀释,直到获得所需浓度的溶液。
这种方法适用于需要较小体积高浓度溶液的情况。
4. 密度稀释法密度稀释法是指通过加入适量的溶剂来改变溶质的浓度,其中溶液的密度是通过测量得到的。
这种方法适用于浓度较大的溶液。
总结:化学溶液的浓度计算及稀释方法对实验室和工业应用都非常重要。
溶液浓度计算量化溶液中的物质含量

溶液浓度计算量化溶液中的物质含量溶液浓度是指溶液中溶质的质量或摩尔数与溶剂的质量或体积之比。
溶液浓度的计算对于化学实验、药学制剂等领域都非常重要,因为它可以帮助我们准确测量溶液中所含的物质含量。
本文将介绍几种常见的溶液浓度计算方法,以帮助读者更好地理解和计算溶液的物质含量。
一、质量浓度计算公式质量浓度是指单位体积溶液中溶质的质量,常以克/升(g/L)表示。
质量浓度的计算公式为:质量浓度(g/L)= 溶质质量(g)/ 溶剂体积(L)例如,在100毫升的溶剂中,溶解了5克的氯化钠。
那么,质量浓度可以通过以下计算得出:质量浓度(g/L)= 5g / 0.1L = 50g/L二、摩尔浓度计算公式摩尔浓度是指单位体积溶液中溶质的物质的摩尔数,常以摩尔/升(mol/L)表示。
摩尔浓度的计算公式为:摩尔浓度(mol/L)= 溶质物质的摩尔数 / 溶剂体积(L)例如,在500毫升的溶剂中,溶解了0.1摩尔的盐酸。
那么,摩尔浓度可以通过以下计算得出:摩尔浓度(mol/L)= 0.1mol / 0.5L = 0.2mol/L三、体积百分比浓度计算公式体积百分比浓度是指溶质的体积与溶液总体积的百分比,常以体积百分比(%)表示。
体积百分比浓度的计算公式为:体积百分比浓度(%)= 溶质体积(ml)/ 溶液总体积(ml) × 100%例如,在200毫升的溶液中,所含乙醇的体积为40毫升。
那么,体积百分比浓度可以通过以下计算得出:体积百分比浓度(%)= 40ml / 200ml × 100% = 20%四、密度计算浓度公式密度是指单位体积溶液的质量,常以克/毫升(g/mL)表示。
有时候,为了计算溶液中物质的含量,我们需要先计算溶液的密度。
密度计算浓度的公式为:密度(g/mL)= 溶质质量(g)/ 溶液体积(mL)例如,一个溶液的质量为50克,体积为40毫升。
那么,该溶液的密度可以通过以下计算得出:密度(g/mL)= 50g / 40mL = 1.25g/mL通过上述的几种溶液浓度计算方法,我们可以准确地计算出溶液中的物质含量。
PCB线路板厂各种化验方法及计算公式(绝密)
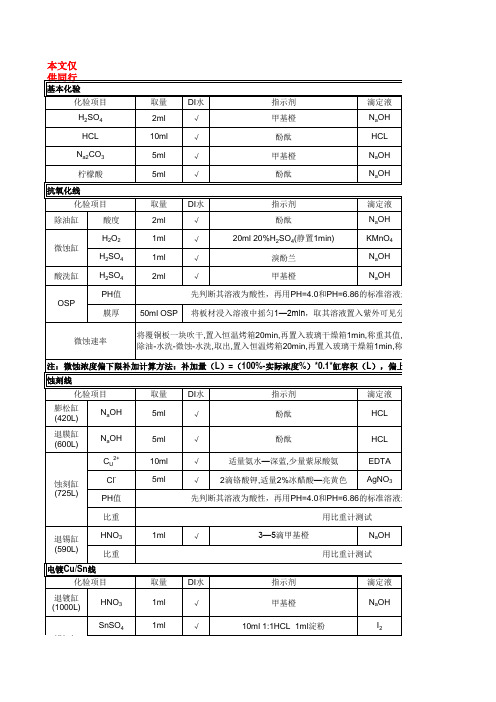
基本化验 化验项目 H2SO4 HCL Na2CO3 柠檬酸 抗氧化线 化验项目 除油缸 微蚀缸 H2SO4 酸洗缸 OSP 膜厚 微蚀速率 50ml OSP 将板材浸入溶液中摇匀1—2min,取其溶液置入紫外可见分光光度计中 H2SO4 PH值 1ml 2ml √ √ 酸度 H2 O 2 取量 2ml 1ml DI水 √ √ 指示剂 酚酞 20ml 20%H2SO4(静置1min) 溴酚兰 甲基橙 滴定液 NaOH KMnO4 NaOH NaOH 取量 2ml 10ml 5ml 5ml DI水 √ √ √ √ 指示剂 甲基橙 酚酞 甲基橙 酚酞 滴定液 NaOH HCL NaOH NaOH
入紫外可见分光光度计中 ,经抗氧化线中 称重其值.
偏上限补加DI水稀释。(微蚀缸容积为 偏上限补加 水稀释。(微蚀缸容积为390L) 水稀释。(微蚀缸容积为 ) 最终状态 无色 无色 紫色 砖红色颗粒 分析值 0.8*N滴*△V 0.8*N滴*△V 158.85*N滴*△V 177.5*N滴*△V 控制范围 3%—5% 3%—5% 135g/l—165g/l 165g/l—190g/l 8.2—8.9 0.19—0.21 黄色 63.01*N滴*△V 300g/l—420g/l 0.19—0.21 最终状态 黄色 蓝色 分析值 63.01*N滴*△V 10.74*N滴*△V 控制范围 200g/l—400g/l 35g/l—45g/l
1ml 2ml 2ml 2ml 2ml 40ml
电镀Desmear/Pth线 线 电镀
化验项目
KmnO4缸 膨松缸 中和缸
溶液浓度与摩尔浓度的计算方法

溶液浓度与摩尔浓度的计算方法在化学中,溶液浓度是描述溶液中溶质含量的重要指标。
而摩尔浓度则是一种特殊的溶液浓度表示方法,它以溶质的摩尔数来衡量溶液的浓度。
下面我们将详细介绍溶液浓度和摩尔浓度的计算方法。
一、溶液浓度的计算方法溶液浓度是指溶质在溶剂中的含量,通常用质量浓度、体积浓度、摩尔浓度等方式进行表达。
1. 质量浓度质量浓度是指单位体积溶液中溶质的质量。
它的计算方法是,将溶质的质量除以溶液的体积,得到的结果即为质量浓度。
质量浓度(g/L)= 溶质质量 (g) / 溶液体积 (L)例如,一瓶500 mL的盐水中溶解了20 g的食盐,那么盐水的质量浓度为:质量浓度 = 20 g / 0.5 L = 40 g/L2. 体积浓度体积浓度是指单位体积溶液中溶质的体积。
例如,酒精溶液的体积浓度常以百分数体积来表示。
体积浓度(%V/V)= 溶质体积 (mL) / 溶液体积 (mL) × 100%举个例子,如果100 mL溶液中有20 mL的酒精,那么酒精溶液的体积浓度为:体积浓度 = 20 mL / 100 mL × 100% = 20%二、摩尔浓度的计算方法摩尔浓度是指溶质的摩尔数与溶液的体积之比,它是描述溶液浓度的常用方式。
摩尔浓度 (mol/L) = 溶质物质的摩尔数 (mol) / 溶液的体积 (L)例如,如果有0.2 mol的氯化钠溶解在500 mL的溶剂中,那么溶液的摩尔浓度为:摩尔浓度 = 0.2 mol / 0.5 L = 0.4 mol/L摩尔浓度的计算方法可以通过知道物质的摩尔数和溶液的体积来实现,也可以通过其他浓度单位转化得到。
三、摩尔浓度与溶液浓度之间的关系摩尔浓度与溶液浓度可以相互转化,通过摩尔质量可以将溶质的质量浓度转化为摩尔浓度,反之亦可。
摩尔质量 (g/mol) = 物质的质量 (g) / 物质的摩尔数 (mol)例如,如果要将质量浓度为40 g/L的CaCl2溶液转化为摩尔浓度,首先需要知道CaCl2的摩尔质量为110.98 g/mol。
溶液中的浓度计算

溶液中的浓度计算在日常生活中,浓度是一个非常常见的概念,特别是在涉及到溶液的时候。
浓度得出的结论可以告诉我们相对溶质和溶剂的数量,而且对许多问题的解决和实验室测试都非常有用。
本文将讨论如何正确计算溶液中的浓度以及讨论如何解决一些常见问题,因此,如果你是一名学生或者对此有兴趣,那么这篇文章一定值得一读。
浓度的定义浓度是指在一个溶液中溶质占有的比例。
通常使用资本字母"c"表示,以毫摩尔/升为单位。
也就是说,当浓度等于一摩尔时,我们可以说溶液含有一摩尔的溶质(分子或离子)在每升溶液中。
在某些情况下,我们会使用通量密度作为浓度单位,其中通量密度是溶液中的溶质泊松数与溶液的密度的乘积。
计算浓度溶液中的浓度可以通过几种方式来计算,其中最常见的是体积法和质量法。
体积法:使用体积法计算溶液的浓度是最普遍的方式之一。
这种方法涉及到测量溶液和加入其中的溶质的体积。
在这种情况下,我们可以通过简单地以溶质的摩尔量除以溶液的体积,来得出溶液的浓度。
举个例子,在一个容器中加入了5克NaCl,并加入了100毫升(ml)的水,溶解后,我们可以通过以下公式计算出溶液的浓度(假设NaCl的摩尔质量为58.44g/mol):NaCl的摩尔量=5/58.44=0.0856 摩尔溶液的浓度=0.0856摩尔/ 0.1升=0.856摩尔/升质量法:质量法计算浓度的方法是根据溶质的质量来推算。
这种方法涉及到两个因素:溶解物的质量和溶液的体积。
在这种情况下,我们可以通过以下公式计算溶解物的体积:溶质的质量/摩尔质量。
例如,如果我们想要制备浓度为2M的HCl,以1 L的溶液中,我们需要知道需要溶解多少克的HCl(假设HCl的摩尔质量为36.45 g/mol):HCl的摩尔质量=36.45克/摩尔2摩尔的HCl在1 L(1000 ml)溶液中需要溶解72.9克的HCl:2摩尔/L的HCl= 2mol/L x 36.45 g/mol = 72.9克/L或72.9 g/1000 ml注意单位的换算:1标准大气压下,1L=1000ml和1g=1000mg。
溶液的制备与浓度计算

溶液的制备与浓度计算一、溶液的制备方法1.固体溶解于液体:将一定量的固体物质称量,并加入一定量的溶剂中,通过搅拌或加热等方式使溶质完全溶解于溶剂中。
其中,溶质是指固体,溶剂是指液体。
2.液体溶解于液体:将一定量的液体溶质称量,并加入一定量的溶剂中,通过搅拌或加热等方式使溶质完全溶解于溶剂中。
其中,溶质和溶剂均为液体。
二、溶液的浓度计算方法溶液的浓度是指溶质在溶剂中所占的比例或浓度大小,常用的浓度计量单位有摩尔浓度、质量浓度、体积分数、体积比和百分比等。
下面将介绍几种常见的浓度计算方法。
1. 摩尔浓度(Molarity)计算方法摩尔浓度是指单位体积溶液中溶质的物质的摩尔数。
摩尔浓度的计算公式为C = n/V,其中C表示摩尔浓度,n表示溶质的物质的摩尔数,V 表示体积(单位是升)。
例如,一定体积的溶液中含有0.5摩尔NaCl,则摩尔浓度为0.5 mol/L。
2. 质量浓度(Mass concentration)计算方法质量浓度是指单位体积溶液中溶质的质量的大小。
质量浓度的计算公式为C=m/V,其中C表示质量浓度,m表示溶质的质量,V表示体积(单位是升)。
例如,一定体积的溶液中含有50克NaCl,则质量浓度为50g/L。
3. 体积分数(Volume fraction)计算方法体积分数是用溶质的体积与溶液总体积之比来表示溶液中溶质的含量。
体积分数的计算公式为Vf=Vs/V,其中Vf表示溶液中溶质的体积,Vs表示溶质的体积,V表示溶液的总体积。
例如,一定体积的溶液中含有30毫升NaCl,则体积分数为30mL/1000mL=0.034. 体积比(Volume ratio)计算方法体积比是溶质的体积与溶剂的体积之比。
体积比的计算公式为Vr=Vs/Vm,其中Vr表示溶质的体积比,Vs表示溶质的体积,Vm表示溶剂的体积。
例如,一定体积的溶液中含有10升NaCl和5升水,则体积比为10L/5L=25. 百分比(Percentage concentration)计算方法百分比是指溶质在溶液中的含量百分比。
PCB电路板制造中溶液浓度算法

PCB电路板制造中溶液浓度算法在印制电路板制造技术中,各种溶液占了很大的比重,这些溶液对印制电路板的最终产品质量起到非常关键的作用。
不管是自配还是选购,科学的计算都是必不可少的。
在这里我们供六种计算方法供同行选用。
1、重量百分比浓度计算(1)定义:用溶质的重量占溶液重理的百分比表示。
(2)举例:试求3克碳酸钠溶解在100克水中所得溶质重量百分比浓度?2、克分子浓度计算?定义:一升中含1克分子溶质的克分子数表示。
符号:M、n表示溶质的克分子数、V表示溶液的体积。
如:1升中含1克分子溶质的溶液,它的克分子浓度为1M;含1/10克分子浓度为0.1M,依次类推。
举例:将100克氢氧化钠用水溶解,配成500毫升溶液,问这种溶液的克分子浓度是多少?解:首先求出氢氧化钠的克分子数:3、体积比例浓度计算:定义:是指溶质(或浓溶液)体积与溶剂体积之比值。
举例:1:5硫酸溶液一体积浓硫酸与五体积水配制而成。
4、克升浓度计算:定义:一升溶液里所含溶质的克数。
举例:100克硫酸铜溶于水溶液10升,问一升浓度是多少?100/10=10克/升5、比重计算定义:物体单位体积的重量(单位:克/厘米3)。
测定方法:比重计。
在电镀过程中,涉及到参数的计算如电镀的厚度、电镀时间、电流密度、电流效率的计算。
当然电镀面积计算也是非常重要的,能确保印制电路板表面与孔内镀层的均匀性和一致性,比较精确的计算的被镀面积。
目前所采用的面积积分仪(对底片的板面积进行计算)和计算机计算软件的开发,使印制电路板表面与孔内面积更加精确。
但有时还采用手工计算方法,下例公式就用得上。
1、镀层厚度的计算公式:(厚度代号:d、单位:微米)d=(C×Dk×t×ηk)/60r2、电镀时间计算公式:(时间代号:t、单位:分钟)t=(60×r×d)/(C×Dk ×ηk)3、阴极电流密度计算公式:(代号:、单位:安/分米2)ηk=(60×r×d)/(C ×t×Dk)4、阴极电流以效率计算公式:Dk=(60×r×d)/(C×t×Dk)6、当量浓度计算定义:一升溶液中所含溶质的克当量数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
线路板制造中溶液浓度计算方法
在印制电路板制造技术,各种溶液占了很大的比重,对印制电路板的最终产品质量起到关键的作用。
无论是选购或者自配都必须进行科学计算。
正确的计算才能确保各种溶液的成分在工艺范围内,对确保产品质量起到重要的作用。
根据印制电路板生产的特点,提供六种计算方法供同行选用。
1.体积比例浓度计算:
· 定义:是指溶质(或浓溶液)体积与溶剂体积之比值。
· 举例:1:5硫酸溶液就是一体积浓硫酸与五体积水配制而成。
2.克升浓度计算:
· 定义:一升溶液里所含溶质的克数。
· 举例:100克硫酸铜溶于水溶液10升,问一升浓度是多少?
100/10=10克/升
3.重量百分比浓度计算
(1)定义:用溶质的重量占全部溶液重理的百分比表示。
(2)举例:试求3克碳酸钠溶解在100克水中所得溶质重量百分比浓度?
4.克分子浓度计算
· 定义:一升中含1克分子溶质的克分子数表示。
符号:M、n表示溶质的克分子数、V表示溶液的体积。
如:1升中含1克分子溶质的溶液,它的克分子浓度为1M;含1/10克分子浓度为0.1M,依次类推。
· 举例:将100克氢氧化钠用水溶解,配成500毫升溶液,问这种溶液的克分子浓度是多少?
解:首先求出氢氧化钠的克分子数:
5. 当量浓度计算
· 定义:一升溶液中所含溶质的克当量数。
符号:N(克当量/升)。
· 当量的意义:化合价:反映元素当量的内在联系互相化合所得失电子数或共同的电子对数。
这完全属于自然规律。
它们之间如化合价、原子量和元素的当量构成相表关系。
元素=原子量/化合价
· 举例:
钠的当量=23/1=23;铁的当量=55.9/3=18.6
· 酸、碱、盐的当量计算法:
A 酸的当量=酸的分子量/酸分子中被金属置换的氢原子数
B 碱的当量=碱的分子量/碱分子中所含氢氧根数
C 盐的当量=盐的分子量/盐分子中金属原子数金属价数
6.比重计算
· 定义:物体单位体积所有的重量(单位:克/厘米3)。
· 测定方法:比重计。
· 举例:
A.求出100毫升比重为1.42含量为69%的浓硝酸溶液中含硝酸的克数?
解:由比重得知1毫升浓硝酸重1.42克;在1.42克中69%是硝酸的重量,因此1毫升浓硝酸中
硝酸的重量=1.42×(60/100)=0.98(克)
· B.设需配制25克/升硫酸溶液50升,问应量取比量1.84含量为98%硫酸多少体积?
解:设需配制的50升溶液中硫酸的重量为W,则W=25克/升 50=1250克
由比重和百分浓度所知,1毫升浓硫酸中硫酸的重量为:1.84×(98/100)=18(克);则应量取浓硫酸的体积1250/18=69.4(毫升)
· 波美度与比重换算方法:
A.波美度= 144.3-(144.3/比重); B=144.3/(144.3-波美度)。
