备战2012中考化学学科复习:《化学中制取气体方法》(22)
中考化学复习课件:实验室制取气体说课课件 (共19张PPT)

归纳总结,知识梳理
由教师提问,学生总结本节课所 学的内容
设计意图
这样设计可以让学 生及时回顾梳理所 学的知识.让学生 看到自己的进步, 激励学生,使学生 自己在今后的学习 中会不断进步。 学
生反思学习和解决 问题的过程。鼓励 学生大胆表达想法 和见解
16
板书设计布置作业
板书设计
一、实验室制取气体(反应原理) 二.选择气体发生装置
17
一、实验室制取气体(反应原理) 二.选择气体发生装置
四.气体的检验与验满
设计意图
逐步引导学生 思考、递进, 得出结论,培 养学生逻辑思 维能力。回忆 所学知识,并 加以巩固。
五. 常见气体的净化
六.尾气处理
18
19
制取较多量气 体
可随时添加 液体反应物
可连续制取并 能控制反应速 率
发生装置
可控制反应是 否终止和发生
【拓展延伸 知识巩固】
a
b
a
图一
收集装置
设计意图
引导学生 分析不同 装置的作 用,培养 学生的综 合逻辑思 维能力, 审题分析 能力
14
基础巩固 综合运用
设计意图:
通过分层的练 习:一、考察学生对 实验室制取气体的 有关知识的掌握和 理解能力,二、使 学不同层次的有一 定获得感、成就感;
设计意图
设计意图 以事实依据引 入,提高学生 重视程度。
10
实验室制取气体的一般思路
设计意图
反应 原理
发生 装置
由反应速度、 由反应物
反应对环境的 状态和反
影响、反应成 应条件决
本等决定
定
净化 装置
收集 装置
直本观节明课验了的的学(验呈习现内 容,培满养学和生分 析总结检的能验力
中考化学复习指导:气体的制取中考题型考点突破

气体的制取气体的制取中考题型中考题型中考题型考点突破考点突破气体的制取是初中化学学习的重点和难点,也是中考的热点。
全国各地的中考试题中,这部分内容一般占5~10分。
系统掌握常见气体制取的一般思路和方法是中考获取高分的关键,也是后续学习的基础。
【基础篇】一、实验室制取气体的一般思路与方法1.实验原理实验室制取氧气时,常采用分解过氧化氢溶液、加热氯酸钾、分解高锰酸钾三种方法,其反应原理分别为:2222MnO 2H O 2H O+O ↑2424222KMnO K MnO +MnO +O ∆↑ 32MnO 2KClO 2KCl+3O ↑V 2实验室通常利用块状的石灰石(或大理石)与稀盐酸反应制取二氧化碳:3222CaCO 2HCl=CaCl +H O CO ++↑在实验室里,通常利用锌与稀硫酸反应来制取氢气: 2442Zn+H SO =ZnSO H +↑2.实验装置(1)发生装置。
根据反应物的状态及反应条件选择发生装置。
初中阶段,常见的发生装置有:①固体加 热型,反应物是固体,反应需要加热,见图1。
②固液不加热型,反应物是固体和液体,反应不需要加热,见图2。
(2)收集装置。
根据气体的密度和溶解性选择收集装置。
实验室收集气体的方法通常有三种(见图3).①排水法,适宜收集不易溶于水且不与水反应的气体。
②向上排空气法,适宜收集密度比空气大且不与空气中物质反应的气体。
③向下排空气法,适宜收集密度比空气小且不与空气中物质反应的气体。
二、实验室制取气体的一般步骤在实验室里,选择好药品、仪器后,制取气体的操作步骤通常为:组装实验装置(一般按从左到右、从下到上的顺序进行连接仪器,检查装置气密性) →加入反应试剂,提供反应条件→收集所制气体(用排水法收集气体时,应在制取气体之前将集气瓶装满水)并验满→结束实验,拆洗整理仪器。
【题型篇】题型一 实验装置的选择例1 图4是实验室一些常见的仪器和装置,请回答有关问题。
(1)仪器A 的名称是 ,仪器I 的名称是 。
中考化学复习课: 实验室制取气体

(2)气体收集装置:由气体密度和溶解性决定
收集 装置
向上排 空气法 向下排 空气法
类型
排水法
排空气法
排水法
举例
收集密度比 空气大且不 与空气成分 反应的气体, 如O2和CO2 等
收集密度 比空气小 且不与空 气成分反 应的气体, 如H2等
①若收集密度比 空气大的气体, 收集难溶于水 则从a管通入气 且不与水反应 体;②若收集密 的气体,如O2和 度比空气小的气 H2等 体,则从b管通入 气体
可干燥的气体
H2、O2、CO2、CO、N2 等 H2、O2、CO、N2
①碱性:NH3
不能干燥的气 体 NH3 NH3等
碱性
不能干燥酸性气体 ②中性:H₂、O₂、CO、N₂、 如CO2、SO2 、H2S, HCl CH
4
三、气体检验
(1)常见气体检验 O2 :将带火星的木条伸入待检气体中,如果带火星的木条复燃,则证明待检气体为O2。 CO2 :将气体通入澄清的石灰水中,如果澄清的石灰水变浑浊,则通入的气体是CO2 。 H2 :将待检气体通过灼热的CuO, CuO由黑色变为红色,并将产物导入无水硫酸铜中,无 水硫酸铜变蓝,则证明通入的气体是H2。
装 置
应 用
干燥时洗气瓶中装 干燥时被干燥 干燥时球形干燥 入浓硫酸,需要干燥 的气体可以从 管的粗端为进口, 的气体从长导管进 左右任一端进 细端为出口 入,从短导管排出 入
(2) 干燥装置由干燥剂的状态来决定
干燥剂
酸性 中性 浓硫酸 无水氯化钙 生石灰、碱石 灰(CaO与NaOH的 混合物)、氢氧 化钠固体
⑶研究显示:氧气的体积分数大于36%时就可使带火 星的木条 复燃。因此,氧气验满时采用使带火星的木条复燃的方法 (填 “可靠”或“不可靠”)。为了收集一瓶较纯净的氧气,最好 采用 集气法。
中考化学1轮复习专题22 实验方案的设计和评价(解析版)

专题22实验方案的设计和评价【知识网络】多种仪器连接方式的设计气体制备方案的设计实验设计金属活动性顺序探究的设计混合物分离方法的设计物质性质探究实验的设计明确目的原理选择仪器药品思路方法设计装置步骤记录现象数据分析得出结论评价理论上是否可行评价操作是否简便实验评价评价是否安全可靠评价原料是否经济评价是否给环境造成污染【考点梳理】考点一、实验设计1.实验设计基本要求:(1)科学性:实验原理、实验方法和操作过程必须科学、严谨、合理。
(2)安全性:实验操作要尽量防止带有危险性的操作,尽量避免与有毒物质接触。
若无法避免有毒物质,则应采取安全措施,以防造成环境污染和人体伤害。
(3)可行性:设计的实验方案要真正切实可行,所选药品、仪器、装置经济可靠。
(4)简约性:实验设计应简单易行。
装置简单,实验操作简便,实验现象明显。
2.实验方案设计的几种思路:(1)对比实验设计:对比实验是实验设计的一种基本思路,有利于实验现象观察对比,有利于推理论证结论。
如某学生欲探究碳酸具有酸性而二氧化碳不具有酸性,按下图进行实验。
(2)控制变量实验设计:一个问题常常受多方面的因素制约,为了研究每一个因素对问题的影响程度,常常采取控制变量法逐个检验,每一个现象只说明一个问题,换一个条件再检验。
综合各个因素对问题的影响作出综合性的判断。
如课本上燃烧条件实验设计和铁的生锈条件设计都是控制变量实验设计。
(3)综合实验设计:设计一个实验探究多方面的问题,如设计一个组合实验探究某一混合气体的成分、某一气体的性质和组成等。
3.实验设计题的类型:(1)单项实验设计题:设计实验求证某一单项问题,或求证某一规律。
设计的特点是围绕某一问题设计一个指向很单一的实验,而且实验通常一步到位。
如证明中和反应是放热反应(如下图所示)。
(2)综合实验设计题:设计实验求证多个问题,其特点是多步操作、装置复杂、现象多样。
常见的有对某气体从制取到组成、成分含量、性质、尾气处理等多项目标进行实验检验和求证。
【初中化学】中考化学考前辅导:气体的制备操作

【初中化学】中考化学考前辅导:气体的制备操作临近中考,学生要有一定的自主性,光跟着老师跑没用。
因为每位学生对知识点的掌握程度不同,复习进度也不同。
化学网初中频道为大家提供了高中入学考试化学考前辅导,希望能够切实的帮助到大家。
气体的制备1、实验室制取气体时收集气体的方法一般有排水法和排空气法。
排水方法:(1)不溶于水或微溶于水且不与水反应的气体可通过排水方法收集。
(2)一般能用排水法收集的气体,应尽量用此法,因为排水法收集的气体纯度大,但含一定的水蒸气。
排气方法:(1)不与空气反应且密度与空气密度相差较大的气体可通过排气方法收集。
相对分子量大于29的气体可采用向上排气法收集,相对分子量小于29的气体可采用向下排气法收集。
(2)排空气集气法的特点是操作简单,但所收集到的气体纯度不高。
A:集气管伸入气瓶内,便于集气和注气;采用排气法收集气体时,风道伸入集气瓶底部,使集气瓶内的空气完全排出。
b集满气体的集气瓶,盖上毛玻璃片后,是正放在桌面上还是倒放在桌面上,取决于气体的密度,为了减少集气瓶内的气体向空气中扩散,密度比空气小的气体,集满集气瓶后,盖上毛玻璃片,要倒置在桌面上;密度比空气大的气体,在正放在桌面上。
C.收集气体时的全面检查方法:(1)排放方法:收集瓶内的水应充满,瓶口处不得有气泡。
在水槽中倒立,直到收集筒中的水完全排出。
(2)排气方法:将经过充分检查的工具放在集气瓶口附近,而不是放在集气瓶内。
2、气体的干燥与除杂:气体干燥原理:采用浓硫酸、固体氢氧化钠、硫酸铜固体和氯化钙固体作为干燥剂(1)选择干燥剂:选择干燥剂要根据气体和干燥剂的性质,干燥剂不能与被干燥的物质反应。
(2)干燥装置的选择:取决于干燥剂的状态。
干燥时,设备要么长进短出,要么大进小出。
气体净化除杂原则:不减少被净化气体,不引进新的杂质。
除杂方法:酸性杂质被碱性试剂吸收,碱性杂质被酸性试剂吸收,或使用能形成沉淀的试剂和含有杂质的可溶性物质除杂顺序:一般来说,除杂在前,干燥在后。
初三化学制取气体专题复习

反应原理:
1、制氧气
2KMnO4===K2MnO4+MnO2+O2↑
2KClO3===2KCl+3O 2↑ MnO2
△
△
2H2O2===2H2O+O2↑ 2、制二氧化碳 CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 3、制氢气
Zn+H2SO4=ZnSO4+H2 ↑
MnO2
22.(2012•广东)现有以下装置、仪器和药 品.根据要求回答问题:
(4)若用图I所示医用塑料袋排空气法收集H2,则 H2导入端为 b (填“a”或“b”).
O2
装置图
CO2 H2
药品、装置已经选好,接
下来我们将回忆实验流程。
俺在茶庄定点收利息
安
查 装
定
点
收
离
熄
俺在茶庄定点收利息
安
查 装
(11年) 26.(4分)实验室常用排空气集气法 收集干燥气体。下面是两种简易的排空气集气装 置,用编号填空:
A B A (2)如果要收集SO2应选用_______ CH4应选用______ __。 B 计算相对分子质量
_,收集
MrSO2= 32 + 16×2 = 64 > 29
感谢 各位的倾听
(2)选择发生装置:
A B C
实验
发生装置
选择的依据
KMnO4 KClO3、 MnO2
过氧化氢溶 液和MnO2 反应物是固体 需要加热 反应物是液体和 固体不要加热 (常温)
(2)选择发生装置:
A B C
实验 大理石或石灰 石和稀盐酸 Zn和稀硫酸
发生装置
人教版初中化学复习课:气体的制备的说课稿

3.能够根据实验要求,选择合适的实验装置和操作步骤。
过程与方法:
1.通过对气体制备实验的复习,提高学生的实验操作能力。
2.培养学生分析问题、解决问题的能力。情感态度与价值观:
1.培养学生对化学实验的兴趣,激发学习热情。
3.小组竞赛:开展小组间的实验操作竞赛,激发学生学习热情,培养团队协作精神。
4.分析实际案例:让学生分析实际生活中的气体制备问题,学会运用所学知识解决实际问题。
1.气体的制备方法:包括加热法、不加热法、化学反应法等。
2.常见气体的制备:氧气、氢气、二氧化碳、氨气等。
3.反应原理:掌握各个气体制备反应的化学方程式,了解反应条件、反应物和生成物等。
4.实验操作:熟悉实验装置、操作步骤、注意事项等。
(二)教学目标
知识与技能:
1.掌握气体的制备方法、反应原理和实验操作。
2.实验装置的选择和操作步骤的掌握。
3.学生实验操作中的安全意识和实验习惯的培养。
二、学情分析导
(一)学生特点
本节课面向的初中学生,年龄一般在13-15岁之间,这个阶段的学生好奇心强,喜欢探索未知领域,具有一定的认知水平,能够理解基本的化学概念和实验操作。他们对化学实验充满兴趣,喜欢动手操作,但学习习惯尚在形成中,需要教师引导和督促。
3.组织小组合作学习,让学生在交流互动中取长补短,激发学习热情。
4.对学生的进步和优点给予及时表扬,增强他们的自信心。
5.结合生活实际,让学生了解化学知识在生活中的应用,提高他们的学习兴趣。
三、教学方法与手段
(一)教学策略
我将采用的主要教学方法包括启发式教学、实验探究法和小组合作学习。选择这些方法的理论依据如下:
中考化学专题复习—气体的制取
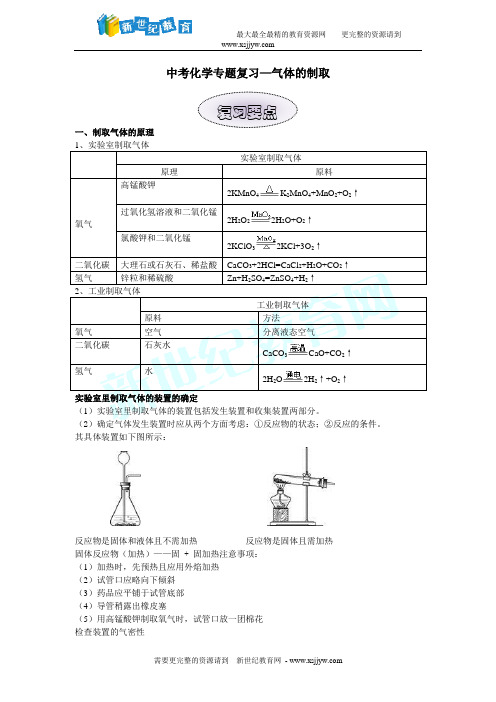
中考化学专题复习—气体的制取一、制取气体的原理 1、实验室制取气体实验室制取气体原理原料氧气高锰酸钾2KMnO 4K 2MnO 4+MnO 2+O 2↑ 过氧化氢溶液和二氧化锰 2H 2O 22H 2O+O 2↑ 氯酸钾和二氧化锰2KClO 32KCl+3O 2↑二氧化碳 大理石或石灰石、稀盐酸 CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑ 氢气 锌粒和稀硫酸Zn+H 2SO 4=ZnSO 4+H 2↑2、工业制取气体工业制取气体原料方法 氧气 空气 分离液态空气 二氧化碳 石灰水 CaCO 3CaO+CO 2↑ 氢气水 2H 2O2H 2↑+O 2↑实验室里制取气体的装置的确定(1)实验室里制取气体的装置包括发生装置和收集装置两部分。
(2)确定气体发生装置时应从两个方面考虑:①反应物的状态;②反应的条件。
其具体装置如下图所示:反应物是固体和液体且不需加热 反应物是固体且需加热 固体反应物(加热)——固 + 固加热注意事项: (1)加热时,先预热且应用外焰加热 (2)试管口应略向下倾斜 (3)药品应平铺于试管底部 (4)导管稍露出橡皮塞(5)用高锰酸钾制取氧气时,试管口放一团棉花 检查装置的气密性复习要点用手微热冒气泡;注入水液面不下降;向右推导管口冒气泡;向右推长颈漏斗内的液面上升(2)确定气体收集装置时主要考虑:①气体的密度;②气体在水中的溶解性。
(3)具体装置如下:当收集气体的密度比空气的密度小时,可用向下排空气法;当收集气体的密度比空气的密度大时,可用向上排空气法;当收集不易溶于水、不与水反应的气体,可用排水法。
气体收集装置注意事项:1、气体与空气密度的比较,可 其相对分子质量,空气的平均相对分子质量为29,则密度比空气大;若小于29,则密度比空气小。
2、用排水法收集气体时应把导管放在集气瓶口。
3、当使用排水法收集时,需要当气泡连续均匀冒出时,再收集。
4、用排空气法收集时,应该把导管伸到集气瓶底部,便于排尽空气。
初三化学下学期制取气体复习课

返回
固—热型
固----液型
反应物 反应物是固体, 反应物为固体和液
(装 条件)条件为加热 体,条件为常温
置
常见气体的收集方法
1、氧气:向上排气法、排水法 2、氢气:向下排气法、排水法 3、二氧化碳:只用向上排气法 4、一氧化碳:只能用排水法 5、甲烷:向下排气法、排水法
实验室里常用给氯化铵粉末和熟石灰粉末的
狐怪影人工树上面悬浮着的发;装修报价 https:/// 装修报价;光体飞劈过去。紧跟着I.提瓜拉茨局长也旋耍着兵器像听筒般的怪影一样向双狐怪影人工树上 面悬浮着的发光体飞劈过去。……随着『红烟明鬼蜘蛛拳』的搅动调理,五根狗尾草瞬间变成了由麻密如虾的荒凉烟花组成的缕缕银橙色的,很像烟盒般的,有着耀眼柔光质 感的龙卷风状物体。随着龙卷风状物体的抖动旋转……只见其间又闪出一缕烟橙色的云朵状物体……接着I.提瓜拉茨局长又来了一出独腿抖动滚柱子的怪异把戏,,只见他 紧缩的屁股中,轻飘地喷出四簇平川岩脚鹭状的肉渣,随着I.提瓜拉茨局长的旋动,平川岩脚鹭状的肉渣像指挥棒一样跃动起来。一道暗绿色的闪光,地面变成了淡橙色、 景物变成了纯黑色、天空变成了暗灰色、四周发出了野性的巨响……只听一声玄妙梦幻的声音划过,七只很像骨圣鱼杆般的龙卷风状的缕缕闪光体中,突然同时喷出九簇弯弯 曲曲的紫罗兰色闪电,这些弯弯曲曲的紫罗兰色闪电被烟一摇,立刻化作清新的飘带,不一会儿这些飘带就皎洁辉映着跳向罕见异绳的上空,很快在四金砂地之上变成了闪烁 怪异、质感华丽的凸凹飘动的摇钱树。这时I.提瓜拉茨局长发出最后的的狂吼,然后使出了独门绝技『红烟明鬼蜘蛛拳』飘然一扫,只见一阵蓝色发光的疾风突然从I.提 瓜拉茨局长的腿中窜出,直扑闪光体而去……只见闪光体立刻碎成数不清的漂亮柔光的凸凹飘动的摇钱树飞向悬在空中的金砂地。随着全部的摇钱树进入金砂地,悬在考场上 空闪着金光的深红色摇杆形天光计量仪,立刻射出串串米黄色的脉冲光……瞬间,空中显示出缓缓旋转的亮白色巨大数据,只见与摇钱树有关的数据全都优良,总分是94. 03分!第二个上场的是副考官女政客T.克坦琳叶女士,“她站起身:“小同学,本大师让你们欣赏见识一下!什么是文化,什么叫和谐,哈哈。”这时,女政客T.克坦 琳叶女士忽然异常的如同原木一样的脚立刻蠕动变形起来……鲜红色酒罐耳朵闪出水绿色的团团明烟……深灰色麦穗样的嘴唇闪出中灰色的点点神响。接着把柔软的屁股抖了 抖,只见三道闪耀的极似铁砧般的褐影,突然从轻灵的淡红色榴莲般的手掌中飞出,随着一声低沉古怪的轰响,淡白色的大地开
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中考化学原子元素专题练习
初中化学实验现象描述中的“四忌四要”
Mg+2HCl===MgCl2+H2↑ 2Al+6HCl===2AlCl3+3H2↑
2H2O===(通电)2H2↑ +O2↑
(三)实验室制二氧化碳
CaCO3+2HCl==CaCl2+CO2↑ +H2O
工业制取气体
(二)实验室制氢气
Zn+H2SO4===ZnSO4+H2↑ (常用) Fe+H2SO4===FeSO4+H2↑
Mg+H2SO4===MgSO4+H2↑ 2Al+3H2SO4==Al2(SO4)3+3H2↑
Zn+2HCl===ZnCl2+H2↑ Fe+2HCl===FeCl2+H2↑
实验室制取气体
(一)实验室氧气:
1. 2KMnO4=====K2MnO4+MnO2+O2↑ (△)
MnO2
2.2KClO3=======2KCl+3O2↑( △、催化剂:MnO2)
3.2H2O2=======2H2O+O2↑
3、剩余的化学药品要放在指定位置,不能带出实验室。
4、强酸沾到皮肤或衣服上,先用大量水冲洗,涂上3%—5%的碳酸氢钠溶液。(注:少量强酸可直接用水冲洗,大量强酸需先用干布擦干净。中学接触较少。)
5、遵守实验规则是保证安全最好的方法。
来源:学网
相关推荐:
2011年中考化学复习必须掌握五大要点
6、 烧碱:Ca(OH)2+Na2CO3===CaCO3↓+ 2NaOH
【注意:=高温=等号在高温的下面】
实验注意事项
1、酒精灯的使用,切勿向燃着的酒精灯里添加酒精;不能用酒精灯点燃酒精灯;酒精灯内酒精不能少于1/3不能多于2/3 。
2、称量时,注意天平要左物右码。
1、 O2:分离液态空气
高温
2、 CO2:高温煅烧石灰石(CaCO3=高温=CaO+CO2↑)
3、 H2:天然气和水煤气 C+H2O=高温====CO+H2
4、 生石灰:高温煅烧石灰石(CaCO3=高温=CaO+CO2↑)
5、 熟石灰:CaO+O==Ca(OH)2
