二类疫苗接种情况报表
常规免疫接种率监测及中国免疫规划信息管理系统使用要点介绍

预防接种卡、证的建立和管理
建立—“全面、及时、准确、细致”
基层接种人员定期了解本地区新生儿出生情况,加强与各部
门合作和联系;要在儿童出生后尽快建卡建证;准确记录儿 童的出生日期,换算成公历;填写完整、不能漏项
使用—“正确使用、妥善保管”
正确使用,如实记录、详细填写 定期整卡 妥善保管、建立制度(建卡、转卡、整卡制度等)
• 2014年12月31日前,乡级单位纳入该系统。
疫苗出入库信息报告时限
• 县、乡级应在上一级疾控机构下发疫苗后1 周内进行确认入库,并于出入库实际操作 完成后1周内进行系统出库。
• 县级出库类型:下发/售出、退回上级、报 废
• 乡级出库类型:下发/售出、退回上级、使 用、报废
年度计划管理
– 年度计划(采购计划):县级、乡级分 别在每年6月和5月底前向上一级疾控机 构报告下一年度计划。
常规免疫报表
档案 内容
存档 方式
上报 时限
国家免疫规划疫 苗常规接种情况报 表
二类疫苗接种情 况统计表
接种率总结
分项目、按 年度存档
报表每月5日 前(系统) 纸质:填写常 规报表时要到村 级
当前存在的主要问题
常规免疫监测系统难以掌握基层真实接种情况, 报告接种率高(99.99%)估算接种率成疑问? (人口估算150%,疫苗估算60%)( “分母-分 子问题”完整性差、“笔头接种”现象,无法信 服) 1岁以内疫苗接种率高,其他年龄接种率低 城区交叉接种、流动儿童管理困难 。。。。。。。
1
50
2
40
3
45
4
55
5
50
6
48
50
45
一类二类疫苗报表范本
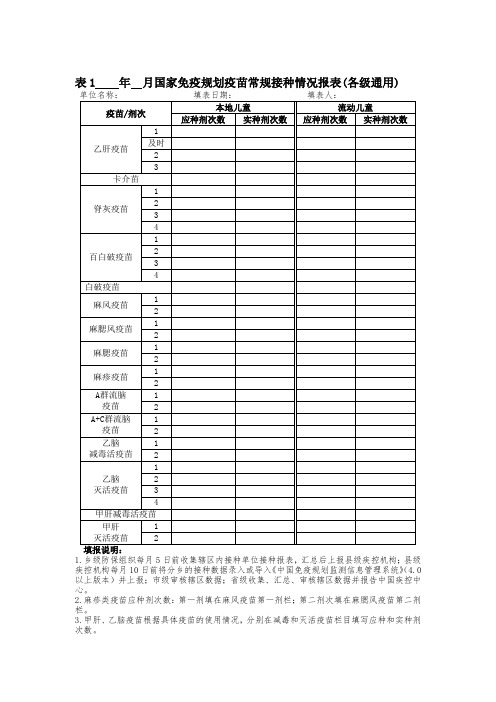
表1 年月国家免疫规划疫苗常规接种情况报表(各级通用) 单位名称:填表日期:填表人:疫苗/剂次本地儿童流动儿童应种剂次数实种剂次数应种剂次数实种剂次数乙肝疫苗1 及时2 3卡介苗脊灰疫苗1 2 3 4百白破疫苗1 2 3 4白破疫苗麻风疫苗1 2麻腮风疫苗1 2麻腮疫苗1 2麻疹疫苗1 2A群流脑疫苗1 2A+C群流脑疫苗1 2乙脑减毒活疫苗1 2乙脑灭活疫苗1 2 3 4甲肝减毒活疫苗甲肝灭活疫苗1 2填报说明:1.乡级防保组织每月5日前收集辖区内接种单位接种报表,汇总后上报县级疾控机构;县级疾控机构每月10日前将分乡的接种数据录入或导入《中国免疫规划监测信息管理系统》(4.0以上版本)并上报;市级审核辖区数据;省级收集、汇总、审核辖区数据并报告中国疾控中心。
2.麻疹类疫苗应种剂次数:第一剂填在麻风疫苗第一剂栏;第二剂次填在麻腮风疫苗第二剂栏。
3.甲肝、乙脑疫苗根据具体疫苗的使用情况,分别在减毒和灭活疫苗栏目填写应种和实种剂次数。
表2 年月第二类疫苗接种情况报表(各级通用)单位名称:填表日期:年月日填表人:序号疫苗名称接种剂次数序号疫苗名称接种剂次数01 乙肝疫苗21 肺炎7价疫苗02 脊灰灭活疫苗22 出血热疫苗03 白破疫苗23 钩体疫苗04 麻风疫苗24 炭疽疫苗05 麻腮疫苗25 狂犬病疫苗06 麻腮风疫苗26 抗狂犬病血清07 风疹疫苗27 抗狂犬病免疫球蛋白08 腮腺炎疫苗28 伤寒疫苗09 乙脑减毒活疫苗29 痢疾疫苗10 乙脑灭活疫苗30 布氏菌疫苗11 流脑A+C群结合疫苗31 鼠疫疫苗12 流脑A+C+Y+W135疫苗32 霍乱疫苗13 甲肝减毒活疫苗33 森林脑炎疫苗14 甲肝灭活疫苗34 登革热疫苗15 甲乙肝联合疫苗35 气管炎疫苗16 b型流感嗜血杆菌疫苗3617 水痘疫苗3718 轮状病毒疫苗3819 流感疫苗3920 肺炎23价疫苗40填报说明:1.本表分月统计第二类疫苗接种情况;替代国家免疫规划疫苗的第二类疫苗接种情况,同时纳入本表报告。
国家免疫接种率和免疫水平监测管理办法

苗,
性,≥1:320 计算保 者占 75%
护水平
间接血凝试验 白喉类毒 锡克氏试验
素
抗毒素≥0.01IU/ml ≥80% 96 小时判定,局部反 阴转率≥80% 应直径≤10mm 为阴 性
破 伤 风 类 间接血球凝集试验 毒素
抗毒素≥0.01IU/ml ≥85%
微量血球凝集抑制试验 血凝抑制抗体≥1:2 ≥85%
1.2 第二类疫苗接种情况报告 接种单位每半年将本责任区内接种第二类疫苗的品种、受种人数
向所属的县级卫生行政部门和疾病预防控制机构报告。报告内容见
《附件五》表 3-1-5、表 3-1-6。 1.3 接种率调查
县级以上疾病预防控制机构应当定期或根据实际工作情况不定期
对本行政区域内儿童完成国家免疫规划疫苗的接种率进行抽样调查。 1.3.1 调查内容 1.3.1.1 适龄儿童建卡率、建证率,乙肝疫苗、卡介苗、脊灰疫苗、 百白破疫苗、麻疹疫苗的合格接种率和“五苗”全程覆盖率,乙肝疫苗 首剂及时接种率,卡介苗疤痕率等; 1.3.1.2 不合格接种原因; 1.3.1.3 未接种原因。 1.3.2 调查方法 1.3.2.1 评价县级以上单位接种率:组群抽样法,具体方法参见有关 材料。 1.3.2.2 评价乡级接种率:批质量保证抽样法,具体方法参见有关材 料。 1.4 接种率评价 1.4.1 国家免疫规划疫苗常规报告接种率的评价 1.4.1.1 评价内容及方法 (1)常规报告接种率的及时性、完整性和正确性评价 ①及时率:在规定时限内报告单位数占应报告单位数的比例。 ②完整率:在规定时限内实际报告以及无漏项单位数占应报告单位数 的比例。 ③正确率:报表中无逻辑性、技术性错误的单位数占应报告单位数的 比例。 (2)常规报告接种率的可靠性评价
第二类疫苗接种公示牌

1、对免疫球蛋白过敏或有其他严重过敏史者。
1.本品不得用静脉注射。
2.本品肌内注射不需做过敏试验。
3.如有异物或摇不散的沉淀,安瓿出现裂纹或过期失效等情况,不得使用。
流感病毒裂解疫苗
本株病毒引起的流行性感冒
8月龄以上
上臂外侧三角肌内注射
8月龄-3岁 0.25ml3岁以上0.5ml
注射用母牛分枝杆菌说明书
增强免疫力、抵抗力
5岁以上与成人剂量相同,5岁以下酌减剂量。
上臂三角肌肌内深注射
2岁以下0.5ml、2-5岁0.8ml。
1、对本品过敏者。
2、严重心脏病患者。
3、妊娠期妇女
4、极度衰弱及重症贫血者
个别患者可能出现局部出现皮疹、结硬或者发热
冻干人用狂犬病疫苗
狂犬病
所有人群
上臂三角肌内注射
2、对本品过敏者
3、患急性疾病、严重慢性疾病。慢性疾病的急性发作期和发热期
4、妊娠期妇女
5、患有癫痫和其他神经系统疾病者
1患有家族性惊厥史者、患有慢性疾病者、患有癫痫病者、过敏体质者。
2注射候出现任何神经系统反应这,禁止再次使用
3严禁冻结
AC群脑膜炎球菌(结合)b型流感嗜血杆菌(结合)联合疫苗
脑脊髓膜炎、肺炎、败血症、会厌症
2、患严重疾病(急性或慢性感染)、发热者禁用。
3、育龄妇女接种本疫苗后至少3个月应避孕。
4、注射过人免疫球蛋白者,至少应间隔一个月后方可接种本疫苗。
少数人可有短暂发热、轻微皮疹或疱疹。一般不需特殊处理,必要时可对症治疗。
口服轮状病毒活疫苗
婴幼儿A群轮状病毒引起的腹泻。
主要为2月龄~3岁婴幼儿,每年1剂次。
二类疫苗接种公示作用介绍及禁忌症不良反应
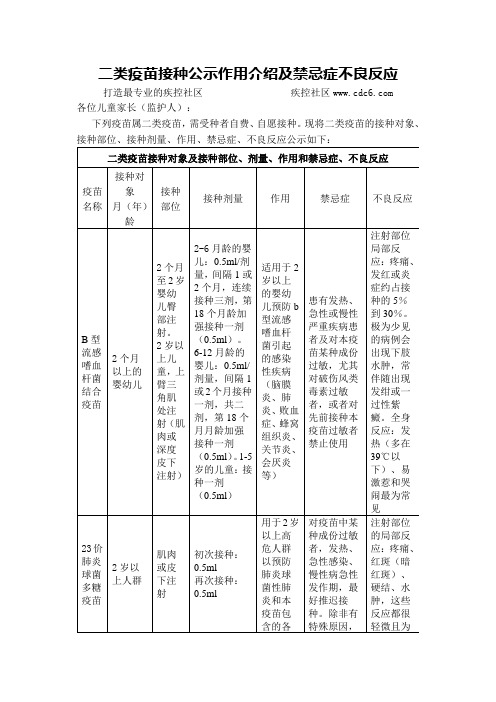
乙型肝炎人免疫球蛋白
适用于乙型肝炎表面抗原阳性的母亲所生的婴儿、意外感染的人群、与乙型肝炎患者和乙型肝炎病毒携带者密切接触者
肌内注射
一次注射量儿童为100IU,成人为200IU,必要时可间隔3-4周再注射一次
冻干水痘减毒活疫苗
12月龄以上的健康水痘易感者
上臂外侧三角肌下缘附着处(皮下注射)
0.5ml
预防水痘
对本品任一组分(包括新霉素)有过敏反应史的个体、妊娠期妇女、患严重疾病(急性或慢性感染)、发热或任何一种晚期免疫病的个体、全身使用类固醇治疗的个体、淋巴细胞总计数少于1200/mm3或表现有细胞免疫功能缺陷的个体、有先天性免疫病史或密切接触的家庭成员中有先天性免疫病史的个体
每次注射0.5 ml
预防A群、C群脑膜炎球菌引起的感染性疾病,如脑脊髓膜炎、肺炎等
对疫苗的成份,尤其是对破伤风类毒素过敏者。癫痫、脑部疾患及有过敏者、肾脏病、心脏病、活动性结核患者及HIV感染者、急性传染病及发热者
偶有短暂的发热、皮疹等不良反应,注射局部有可能出现疼痛、红肿或硬结,可自行缓解。极少数的儿童还可能出现嗜睡或烦躁
23价肺炎球菌多糖疫苗
2岁以上人群
肌肉或皮下注射
初次接种:0.5ml
再次接种:0.5ml
用于2岁以上高危人群以预防肺炎球菌性肺炎和本疫苗包含的各种血清型引起的系统性肺炎球菌感染
对疫苗中某种成份过敏者,发热、急性感染、慢性病急性发作期,最好推迟接种。除非有特殊原因,否则本疫苗不推荐给三年内已接种者
注射部位的局部反应:疼痛、红斑(暗红斑)、硬结、水肿,这些反应都很轻微且为一过性的。系统反应:淋巴结病、发热、风疹、关节痛、过敏反应、头痛、肌痛、不适、衰弱及疲劳等
南宁市某社区适龄儿童第二类疫苗接种情况分析

本研究采用问卷调查的方法,由经过培训的调查员进行入户调查。问卷内容包括 儿童基本信息、疫苗接种情况、家长对疫苗接种的认知和态度等。同时,还收集 了儿童预防接种证等相关资料,以核实疫苗接种情况。
03
适龄儿童第二类疫苗接种 情况
接种率及影响因素分析
接种率
该社区适龄儿童的第二类疫苗接种率达到95%,显示出较高的接种率。
05
适龄儿童第二类疫苗接种 策略建议
加大宣传力度,提高家长接种意识
1 2 3
定期开展宣传活动
通过宣传讲座、社区宣传栏、网络平台等多种 形式,定期向家长普及疫苗接种的重要性和相 关知识,提高家长接种意识。
加强与家长的沟通
建立有效的沟通机制,定期与家长进行交流, 了解他们的疑虑和困惑,及时解答问题,消除 接种顾虑。
限制
本研究仅针对南宁市某社区的适龄儿童进行调查,不能代表 整个南宁市的情况。此外,由于时间限制,仅收集了近一年 的疫苗接种数据,可能存在数据不全面或偏差。
不足
本研究仅对第二类疫苗的接种情况进行了调查和分析,未涉 及第一类疫苗的接种情况。此外,影响因素的分析仅考虑了 儿童和家庭因素,未涉及医疗机构、政策等因素的影响。
女性儿童
女性儿童的接种率略高于男性儿童,可能 与家长对女性儿童健康的关注程度有关。
VS
男性儿童
男性儿童的接种率略低于女性儿童,需要 加强对男性儿童接种的宣传和推广。
04
适龄儿童第二类疫苗接种 效果评估
接种后免疫效果评估
01
02
03
抗体水平检测
在疫苗接种后,对适龄儿 童进行抗体水平检测,以 评估疫苗的免疫效果。
不良反应处理措施
研究有效的处理措施,以应对接种后可能出现的不良反应。
接种率监测和评价

组群抽样法—抽样步骤 (5)
确定第1个被抽样单位。R接近并小于累计 人口数的备选抽样单位(村),即确定为 第1个被抽样单位;本例10 724小于表1中的 编号2组的累计人口数(22 000),因此编 号为2的村即为第1个被调查单位。
报告单位不完整 应种对象掌握不全 对报告接种率分析利用不够 抽样调查接种率实施过程中随意性强 没有按照规定开展免疫效果监测
接种率监测分类
被动监测----报告接种率 主动监测----调查接种率
接种率报告
接种率报告
年 用)
年
月国家免疫规划疫苗常规接种情况报表(各级通 月第二类疫苗接种情况报表(各级通用)
快速评价方法
快速评价方法的优点是调查时无人为干扰,能 快速地、真实地了解当地儿童是否接受预防接 种,特别是近期的接种情况;缺点是由于是家 长回忆,不能全面、准确地了解具体接种疫苗 的种类、时间。
主要用于对当地某一种疫苗近期开展接种情况 的评价、强化免疫评价、流动儿童的接种情况 评价以及上级对下级单位的突击检查等。
计算全年(或半年)的累计接种率,则累计实种人 数是指1-12月(或1-6月)实种人数的总和;累计应 种人数则指1-11月(或1-5月)实种人数总和加上12 月(或6月)应种人数。
累计接种率计算举例
【例】某乡卫生院1-6月的接种人数如下表,试计算该地上半年
的累计接种率。
月份 当月达到免疫月(年) 本次应种
调查结果的评价及分析
接种率完成情况; 调查接种率是否达到国家规定要求; 未接种原因,不合格接种原因; 影响接种率的主要原因; 与以前的接种率调查结果进行比较,评价进展情
国家一类、二类疫苗接种信息公示栏
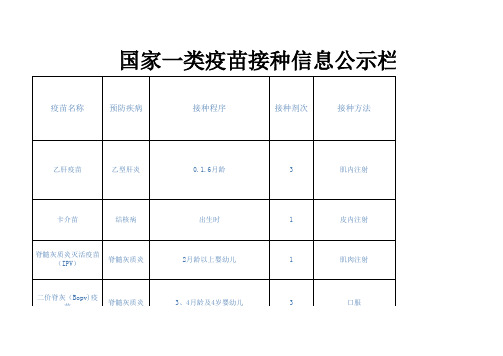
国家一类疫苗接种信息公示栏(政府提供、免二价脊灰(Bopv)疫接种对象皮下注射1接种程序疫苗价格进口(20ug)18月龄预防疾病甲型肝炎甲肝疫苗疫苗名称(酵母)国家二类疫苗接种信息公示栏(知情、自愿、自费乙型肝炎易感染者2月龄至3岁婴幼儿2月龄以上婴幼儿6月龄及以上儿童人群每人一次口服3.0ml。
每年应服一次12月龄以下接种三针次,1.5岁加强一针。
6、9月龄初免种第一针0、1、6月进口(10ug)进口(20ug)国产(20ug)国产(60ug)乙型肝炎婴幼儿A群轮状病毒引起的腹泻流感嗜血杆菌引起的感染性疾病A群和C群流行性脑脊髓膜炎口服轮状疫苗b型流感嗜血杆菌结合疫苗(Hib)A+C群结合流脑疫苗重组乙型肝炎疫苗(酵母)成人儿童2岁以上高危人群6月龄以上流感易感者2周岁以上儿童及成人3月龄以上婴幼儿12月龄以上健康水痘易感人群3周岁以上接种一针3、4、5月龄各接种一针,1.5岁加强一针12月龄后接种第一针2周岁后免疫6月-2岁儿童接种两针次,3周岁以上接种成人剂量249肺炎球菌性肺炎流行性感冒A群、C群、Y群、W135群流脑百日咳白喉破伤风及流感嗜血杆菌引起的感染性疾病水痘A+C+Y+W135群多糖流脑疫苗无细胞百白破b型流感嗜血杆菌联合疫苗(四联)水痘疫苗23价肺炎球菌多糖疫苗流感疫苗肠道病毒71型灭活疫苗预防EV71感染所致的手足口病免疫程序2剂次,间隔1个月6月龄至3岁EV71易感者18月龄以上的甲肝易感者18月龄初免,24-30月龄加强。
甲型肝炎甲肝灭活疫苗示栏(政府提供、免费接种)功能低下等不良反应及注意事项或注射局部微痛,一般不超过2天。
自行缓解。
偶有皮疹,必要时对症治禁忌症酵母成分过敏者接种方法严重疾病者;免疫缺陷者;栏(知情、自愿、自费接种)可出现疼痛、硬结、发红或炎症,偶可见不典型皮疹、发热等。
偶有短暂低热,一般可自行缓解。
如有严重反应及时诊治。
偶有轻微局部反应,罕见轻度和中度发热,一过性皮疹,一般不超过3天,必要时可对症治疗。
GAVI免疫规划信息管理系统

6.疫苗耗损情况 7.疫苗领发情况 8.注射器的领发、使用、销毁记录 9.冷链设备分布 10.冷链设备温度记录和维修、使用记录 11.接种证、卡(簿) 12.预防接种资料/接种率报告 13.疫情资料 14.经费预算、决算及使用情况 15.其他
√
√ √ √ √ √ √ √ √ √ √
乡级应收集的免疫规划资料的内容-2
乡级
√ √/▲
第一类疫苗及配套注射器使用情况月报表 疫苗出入库登记表
注射器出入库登记表 疫苗运输记录表 冷链设备档案表 疫苗报损申请表 冷链设备温度记录表 新生儿乙肝疫苗首针及时接种率报表 儿童预防接种年龄组人口统计表
流动儿童调查统计报表 疑似预防接种异常反应(AEFI)个案登记表
疑似预防接种异常反应(AEFI)个案报告卡 群体性疑似预防接种异常反应登记表 国家免疫规划疫苗常规接种情况报表 第二类疫苗接种情况报表 国家免疫规划疫苗针对疾病主动监测记录表 国家免疫规划疫苗针对疾病主动监测报表 接种单位档案表
山西省预防接种二类疫苗接种情况调查表 -
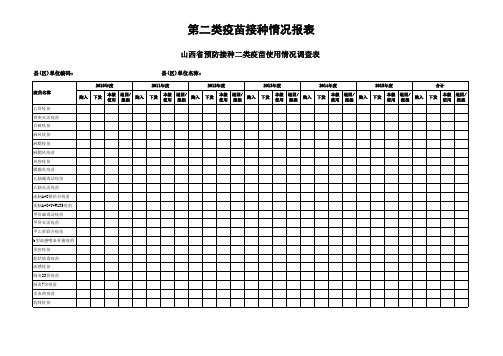
山西省预防接种二类疫苗使用情况调查表
县(区)单位编码:
2010年度 疫苗名称 购入 乙肝疫苗 脊灰灭活疫苗 白破疫苗 麻风疫苗 麻腮疫苗 麻腮风疫苗 风疹疫苗 腮腺炎疫苗 乙脑减毒活疫苗 乙脑灭活疫苗 流脑A+C群结合疫苗 流脑A+C+Y+W135疫苗 甲肝减毒活疫苗 甲肝灭活疫苗 甲乙肝联合疫苗 b型流感嗜血杆菌疫苗 水痘疫苗 轮状病毒疫苗 流感疫苗 肺炎23价疫苗 肺炎7价疫苗 出血热疫苗 钩体疫苗 下发 本级 退回/ 购入 使用 报损
县(区)单位名称:
2011年度 下发 本级 退回/ 购入 使用 报损 2012年度 下发 本级 退回/ 购入 使用 报损 2013年度 下发 本级 退回/ 购入 使用 报损 2014年度 下发 本级 退回/ 购入 使用 报损 2015年度 下发 本级 退回/ 购入 使用 报损 合计 下发 本级 退回/ 使用 报损
第二类疫苗接种情况报表
炭疽疫苗 狂犬病疫苗 抗狂犬病血清 抗狂犬病免疫球蛋白 伤寒疫苗 痢疾疫苗 布氏菌疫苗 鼠疫疫苗 霍乱疫苗 森林脑炎疫苗 登革热疫苗 气管炎疫苗 DTaP-Hib四联疫苗 DTaP-IPV/Hib疫苗 总 计
填表说明:1、购入=下发+本级使用+退回/报损;2、表格填报数据以县区疾控部门统一汇总后填入表格中。
ቤተ መጻሕፍቲ ባይዱ
常规免疫接种率监测及中国免疫规划信息管理系统使用要点介绍
格审核数据质量,
• 县级疾控机构每月10日前登陆GAVI系统审确保核报预告防数接据的种准门诊
上报的表格并上报市级。
确性和完整性
接种率评价——可靠性评价
• 图表法 • 差值(D)法 • 比值(R)评价法 • 脱漏率 • 其它评价方法
接种率计算
本次接种某疫苗某剂(次)实种人数
接种率=
× 100%
本次接种某疫苗某剂(次)应种人数
某疫苗某针(次)累计实种人数
累计接种率=
× 100%
某疫苗某针(次)累计应种人数
累计接种率计算举例
• 【例】某乡卫生院1-6月的接种人数如下表,试计算该地上半年
的累计接种率。
月份 当月达到免疫月(年)本次应种 本次实种 未种人数 接种率(%) 龄儿童数 (m) 人数(a) 人数(b) (c) (d)
报表形式
接种大卡
各接种点常规免疫完成情况记录表,适用于接种点 登记汇总
常规免疫接种情况月报表
分表1-1、表1-2、表2-1、表2-2, 常规免疫接种情况统 计汇总报表,由乡级及乡级以上单位逐级统计上报
山东省儿童预防接种登记簿-大卡
按年度存放 每年1本或每村(管区)1本 在接种点保存,保管期限应在儿童满7周岁后再保存不少于15年 包含了预防接种证上的所有疫苗
目录
常
中息
年
规
国管
报
免
免理
表
疫
疫系
资
接
规统
料
种
划监
管
率
信测
理
监
测
1
2
3
一、常规免疫接种率监测
第二类(自费)疫苗接种告知表
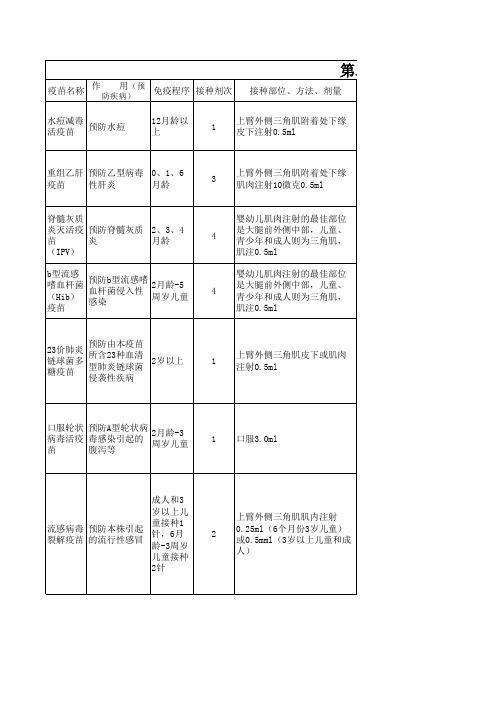
预防由本疫苗 所含23种血清 型肺炎链球菌 侵袭性疾病
2岁以上
1
上臂外侧三角肌皮下或肌肉 注射0.5ml
口服轮状 病毒活疫 苗
预防A型轮状病 毒感染引起的 腹泻等
2月龄-3 周岁儿童
1 口服3.0ml
成人和3
岁以上儿
流感病毒 预防本株引起 裂解疫苗 的流行性感冒
童接种1 针,6月 龄-3周岁
儿童接种
1、对该疫苗所含任何成分过敏 者,如新霉素等,或以前接种本 疫苗过敏者。 2、发热或急性疾病期患者,就 推迟接种本疫苗。
1、常见不良反应:疼痛、红肿、硬 结等; 2、极罕见不良反应:局部肿胀和淋 巴结肿大。
急性严重发热性疾病患者应推迟 1.轻度不良事件:常见的在接种疫苗后
接种。已知对疫苗中任何成分过 24小时内在注射部位感觉疼痛和触痛。
一过性累及肾脏、神经紊乱、如脑脊髓膜
(1)由于狂犬病是致死性疾
病,暴露后程序接种疫苗无任何
禁忌证。(2)暴露前程序接种 注射后有轻微局部及全身反应,可自
时遇发热、急性疾病、严重慢性 行缓解,偶有皮疹。若有速发型过敏
疾病、神经系统疾病、过敏性疾 反应、神经性水肿、荨麻疹等较严重
病或对抗生素、生物制品有过敏 副反应者,可作对症治疗。
已知对本疫苗的某种成份过敏。 发热、急性疾病、慢性疾病急性 发作期应推迟接种。
一般来说是轻微和一过性的,主要表 现为接种部位的局部反应(疼痛、红 斑、水肿)。全身反应(发热、头痛 、头晕、关节痛、肌痛、恶心、腹 痛)少见。个别病例会出现典型的过 敏反应(搔痒、皮疹、荨麻疹)。
注意事项
收费标准 (元)
热、急性疾病者、慢性疾病的急 一般无需治疗,一至二天后可自行缓解。
接种率整改报告

接种率整改报告篇一:2014年10月接种率报告分析2014年11月接种率报告分析为了解我乡本月扩大国家免疫规划疫苗接种实施情况,及时发现和解决接种工作中存在的问题,总结经验,督促落实,推动我乡扩大国家免疫规划工作持续发展。
现对我乡2014年11月月接种服务分析总结如下:1第一类疫苗接种情况:乙肝应种139人,实种104人,接种率74%,及时率71.6%,脱漏率-21.8 %。
脊灰应种280人,实种238人,接种率85%,及时率82.3%,脱漏率-16.3 %百白破应种222人,实种179人,接种率80.6%,及时率79.3%,脱漏率-37.5%麻风应种79人,实种51人,接种率64.5%,及时率63.5%,麻腮风应种57人,实种44人,接种率77.2%,及时率75.7%,A群应种132人,实种102人,接种率77.3%,及时率74.2%,乙脑应种171人,实种121人,接种率70.1%,及时率68.4%,甲肝应种54人,实种46人,接种率85.2%,及时率82.8%,白破应种122人,实种99人,接种率81.1%,及时率78.4%,A+C 应种205人,实种169人,接种率82.4%,及时率81.3%李彬彬,性别男,2014年07月16日生,出生地厦门,现住址大槐树,接种记录为糖丸2014〃11〃17 百白破2014〃11〃17 许若晴,性别女,2014年06月03日生,出生地洛阳,现住址岗刘,接种记录为糖丸2014〃11〃28百白破2014〃11〃28杨星辰,性别男,2014年04月1日生,出生地南曹,现住址大桥,接种记录为百白破2014〃11〃032、我乡预防接种门诊疫苗使用数与本月的疫苗领取数如下:3、二类疫苗接种,接种水痘疫苗5人,Hib疫苗67人。
二、分析报表显示A群流脑、麻疹类疫苗接种率较低,A+C疫苗、脊灰疫苗接种率较高,二类疫苗接种率较低,。
三、下阶段工作措施1、针对接种率低的疫苗,每星期查漏和预约接种,采取多种样式的通知方式,加强预防接种知识的宣传力度,提高人群的知晓率,提高应种疫苗的接种率;2、加强对接种人员的培训力度,提高与监护人的沟通与互动能力;3预防接种结束后,尽快、准确录入儿童接种信息并及时上传。
二类疫苗接种公示(必须公示)
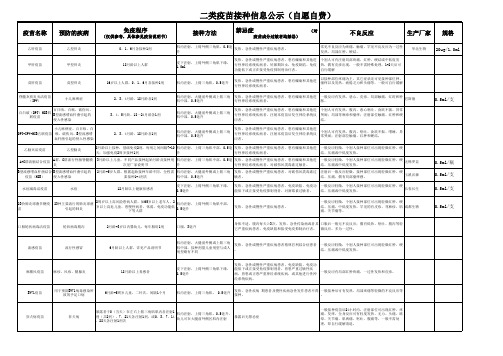
二类疫苗接种信息公示(自愿自费)
注:1.优先接种一类疫苗,根据《中华人民共和国传染病防治法》和《疫苗流通和预防接种管理条例》,公民如无禁忌,应当免费接种一类疫苗; 2.二类疫苗自愿自费接种,且不得与一类疫苗在同一天内接种,间隔不少于14天;3.部分二类苗不列入程序,可以在一类疫苗接种禁忌或家长自愿选择时进行二类苗替代:A+C群流脑结合疫苗替代A群流脑疫苗;脊髓灰质炎灭活疫苗替代脊灰减毒活疫苗、DPT-IPV-HIB五联疫苗替代脊灰疫苗无细胞百白破; 4.对某疫苗成分过敏者均禁忌接种该疫苗。
二类苗不列入程序,可。
二类疫苗公示模板

甲型肝炎灭活疫苗
预防甲型病毒性肝炎
1-15岁儿童接种1剂,16岁以上用成人剂量,初次免疫接种1剂,间隔6个月加强1剂
上臂三角肌皮下注射0.5ml
已知对疫苗任一成分,包括辅料及抗生素过敏者,患严重疾患、慢性病的急性发作期或发热者、免疫缺陷、免疫功能低下或正在接受免疫抑制治疗者、未控制癫痫和其它进行性神经系统疾病者禁用。
二类疫苗接种信息公示栏(知情、自愿、自费接种)
疫苗名称
作用
免 疫 程 序
接种途径及剂量
禁 忌 症
不良反应及注意事项
疫苗价格
预防接种服务价格
B型流感嗜血杆菌疫苗
预防B型流感嗜血杆菌引起的疾病,如:脑膜炎、肺炎、败血症、关节炎、会厌炎等
2-6月龄内接种3剂,6-12月龄接种2剂,间隔1个月,第二年或18月龄时加强1剂;1-5岁未接种过的儿童应接种1剂
肌肉或深度皮下注射,6-36个月儿童0.25ml,3岁以上儿童和成人0.5ml
对鸡蛋或疫苗中其他成分过敏者、格林巴利综合症患者和治愈者、中重度急性发热性疾病和慢性病急性发作期禁用。
个别人有局部疼痛,偶见红、肿、瘙痒。全身反应偶见发热、疲劳乏力、头痛、头晕、恶心。鉴于流感病毒易变异的原因,需要每年接种一次。
疫苗复溶后用于肌肉注射或深度皮下注射0.5ml
对疫苗中任何成分过敏者及既往接种b型流感嗜血杆菌疫苗后有过敏症状者禁用,患急性严重发热性疾病推迟接种。
个别接种后48小时内局部偶有发红、肿胀和疼痛,发热、食欲不振、烦躁不安、呕吐及异常哭闹,一般无需特殊处理,必要时对症治疗。
元/支
27元/剂次
口服轮状病毒活疫苗
元/支
23价肺炎球菌多糖疫苗
预防23种肺炎球菌血清型引起的系统性肺炎球菌感染
疫苗接种体检、告知、接种登记表(新)
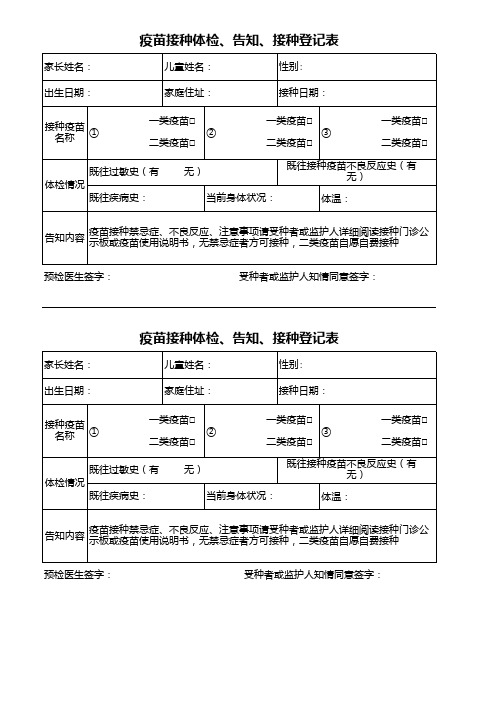
疫苗接种体检、告知、接种登记表
儿童姓名:
性别:
家庭住址:
接种日期:
接种疫苗 名称
①
一类疫苗□ ②
二类疫苗□
一类疫苗□ ③
二类疫苗□
一类疫苗□ 二类疫苗□
既往过敏史(有 体检情况
既往疾病史:
无)
既往接种疫苗不良反应史(有 无)
当前身体状况:
体温:
告知内容
疫苗接种禁忌症、不良反应、注意事项请受种者或监护人详细阅读接种门诊公 示板或疫苗使用说明书,无禁忌症者方可接种,二类疫苗自愿自费接种
体温:
告知内容
疫苗接种禁忌症、不良反应、注意事项请受种者或监护人详细阅读接种门诊公 示板或疫苗使用说明书,无禁忌症者方可接种,二类疫苗自愿自费接种
预检医生签字:
受种者或监护人知情同意签字:
预检医生签字:
受种者或监护人知情同意签字:
家长姓名: 出生日期:
疫苗接种体检、告知、接种登记表
儿童姓名:
性别:
家庭住址:
接种日期:
接种疫苗 名称
①
一类疫苗□ ②
二类疫苗□
一类疫苗□ ③
二类疫苗□
一类疫苗□ 二类疫苗□
既往过敏史(有 体检情况
既往疾病史:
无)
既往接种疫苗不良反应史(有 无)
当前身体状况:
(完整版)防疫各种表格
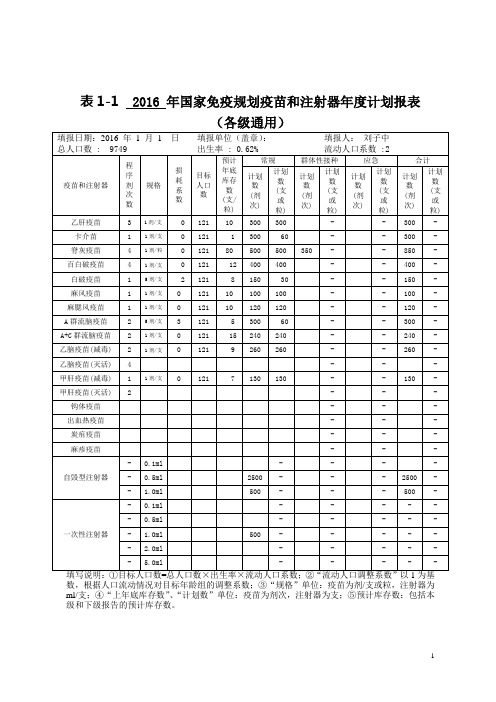
表1-1 2016 年国家免疫规划疫苗和注射器年度计划报表(各级通用)数,根据人口流动情况对目标年龄组的调整系数;③“规格”单位:疫苗为剂/支或粒,注射器为ml/支;④“上年底库存数”、“计划数”单位:疫苗为剂次,注射器为支;⑤预计库存数:包括本级和下级报告的预计库存数。
表1-2第二类疫苗采购计划表采购单位:大唤起乡卫生院填表时间:2016 年1 月 1 日表1-3疫苗出入库登记表疫苗名称:生产企业:批号:疫苗属性:1第一类2第二类剂型:1液体2冻干3丸剂 4 其他规格:剂/支或粒有效日期:年月日批准文号:批签发合格证明编号:进口通关单编号:填写说明:①疫苗按品种、生产企业和批号管理;②“出入库类型”:领取/购进、下级退回、下发/售出、报废、退回上级;③“来源/去向单位”:入库为来源单位,出库为去向单位;④批号按疫苗标明的实际批号填写;⑤表格的具体形式可根据需要调整,但应包括以上内容。
表1-4注射器出入库登记表注射器类型:1自毁型2一次性生产企业:规格:ml/支批号:有效日期:年月日注射器属性:1第一类2第二类批准文号:填写说明:①注射器按类型、生产企业、规格和批号管理;②“出入库类型”:领取/购进、下级退回、下发/售出、报废、退回上级;③“来源/去向单位”:入库为来源单位,出库为去向单位;④表格的具体形式可根据需要调整,但应包括以上内容。
表1-5疫苗盘点统计表报表单位(盖章)2015年12月31日报表人:表2-1冷链设备档案表设备名称:⑴冷藏车⑵疫苗运输车⑶普通冷库⑷低温冷库⑸普通冰箱⑹冰衬冰箱⑺低温冰箱⑻冷藏箱⑼备用冷库制冷机组⑽发电机设备编码:003设备来源:⑴中央财政⑵省财政⑶市财政⑷县财政⑸国际项目⑹自购⑺其他来源生产企业:中科美菱低温科技有限责任公司设备型号:YCD-EL200型出厂编号:111011136 总容积:200 升到货日期:2012年4 月20 日启用日期:年月日收货人签名:保管人签名:当前状态:⑴正常⑵待修⑶报废⑷备用当前使用单位:大唤起乡卫生院维修记录:报废记录:填写说明:①每个冷链设备填写一张冷链设备档案表,设备的当前运转状态应根据变化情况随时修改;②容积单位全部换算为升;③冷藏包和冰排在“冷链设备运转状况报表”中每年汇总报告一次。
3.1.2 本月所有儿童国家免疫规划疫苗基础预防接种情况统计汇总表...

名 称 接种部位 接种途径 剂 量 剂次 接种时间 1 2 3 4 注:接种疫苗名称应填写通用名;接种部位指1上臂三角肌/2臀部/3大腿前内侧/4其它部位;接种途径指1 肌内/2皮下/3皮内/4口服/5其它(请说明);接种时间精确到分。
本月(次)应报单位数 本月(次)实报单位数 报告率 %
报告
单位 国标
编码
(县) 去年
人口
总数 去年
出生
人数 本月(次)基础免疫应种人数 本月(次)基础免疫受种人数 卡介苗 脊灰疫苗 百白破疫苗 麻疹疫苗 乙肝疫苗 卡
介
7. 监护人姓名:
8. 联系地址:
9. 联系电话:
② 应种和受种人数均包括12月龄内和12月龄以上的儿童;
③ 国标编码、去年人口总数、去年出生人口数仅在每年第1次报表填写。
填报人 审核人 填报单位(印章) 填报日期 年 月 日
介
苗 脊灰疫苗 百白破疫苗 麻疹疫苗 乙肝疫苗 1 2 3 1 2 3 1 2 3 1 2 3 1 2 3 1 首剂及时接种 2 3 合计 备注:① 本表供乡级及乡级以上单位填报;
2. 发生年份 □□□□
3. 编码: □□□□
4. 姓名:
苗 脊灰疫苗 百白破疫苗 麻疹疫苗 乙肝疫苗 1 2 3 1 2 3 1 2 3 1 2 3 1 2 3 1 首剂及时接种 2 3 合计 备注:① 本表供乡级及乡级以上单位填报;
实际报出日期: 年 月 日 单位负责人(签章): 制表人(签章):
3.1.6 第二类其他疫苗购进和接种情况统计(表3-1-6)
第二类其他疫苗接种情况统计表
疫苗名称 规格 购苗数量 受种人数 库存数量
免疫规划填空题

三、填空题1、省、自治区、直辖市人民政府在执行国家免疫规划时,根据本行政区域的(传染病流行情况)、(人群免疫状况)等因素,可以增加免费向公民提供的疫苗种类,并报国务院卫生主管部门备案。
2、疫苗生产企业、疫苗批发企业在销售疫苗时,应当提供由药品检验机构依法签发的(生物制品每批检验合格)或者(审核批准证明复印件),并加盖企业印章;疫苗批发企业经营进口疫苗的,还应当提供(进口药品通关单复印件),并加盖企业印章。
3、疾病预防控制机构、接种单位在接收或者购进疫苗时,应当向疫苗生产企业、疫苗批发企业索取前款规定的证明文件,并保存至超过疫苗有效期(2)年备查。
4、各级疾病预防控制机构依照各自职责,根据国家免疫规划或者接种方案,开展与预防接种相关的(宣传)、(培训)、(技术指导)、(监测)、(评价)、(流行病学调查)、(应急处置)等工作5、疾病预防控制机构、接种单位在收货时应核实疫苗运输的(设备)、(时间)(温度记录)等资料,并对疫苗(品种)、(剂型)、(批准文号)、(数量)、(规格)、(批号)、(有效期)(供货单位)、(生产厂商)等内容进行验收,做好记录。
符合要求的疫苗,方可接收。
6、医疗卫生人员在实施接种前,应当告知受种者或者其监护人所接种疫苗的(品种)、(作用)、(禁忌)、(不良反应以及注意事项),询问受种者的(健康状况)以及(接种禁忌)等情况,并如实记录告知和询问情况。
7、接种第二类疫苗的建议信息应当包含(所针对传染病的防治知识)、(相关的接种方案)等内容,但不得涉及具体的(疫苗生产企业)和(疫苗批发企业)。
8、预防接种异常反应,是指合格的疫苗在实施规范接种过程中或者实施规范接种后造成受种者(机体组织器官)、(功能损害),相关各方均无过错的药品不良反应。
9、因接种单位违反预防接种工作规范、免疫程序、疫苗使用指导原则、接种方案等原因给受种者造成损害,需要进行医疗事故技术鉴定的,按照(《医疗事故技术鉴定办法》)办理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(各级通用)
省市县乡(镇、街道)村(居委会)
疫苗
接种剂次数
疫苗
接种剂次数
乙肝疫苗
出血热疫苗
白破疫苗
钩体疫苗
麻风疫苗
炭疽疫苗
麻腮疫苗
狂犬病疫苗
麻腮风疫苗
抗狂犬病免疫球蛋白
风疹疫苗
抗狂犬病血清
腮腺炎疫苗
伤寒疫苗
乙脑减毒活疫苗
痢疾疫苗
乙脑灭活疫苗
布氏菌疫苗
A+C群流脑疫苗
鼠疫疫苗
A+C+Y+W135流脑疫苗
霍乱疫苗
甲肝减毒活疫苗
森林脑炎疫苗
甲肝灭活疫苗
登革热疫苗
甲乙肝联合疫苗
气管炎疫苗
B型流感嗜血杆菌疫苗
脊灰灭活疫苗
水痘疫苗
百白破疫苗
轮状病毒疫苗
流感疫苗
23价肺炎球菌疫苗
7价肺炎结合疫苗
填写说明:本表用于全人群第二类疫苗接种情况报告(含应急接种疫苗和第一类疫苗的替代疫苗);乡级防保组
织每月5日前汇总上报县级疾病预防控制机构,县级疾控机构每月10日前将分乡的接种数据录入或导入《中国免疫
规划监测信息管理系统》(4。0以上版本)并上报;市级审核辖区数据;省级收集、汇总、审核辖区数据并报告中国
疾控中心。
