初中化学教材九年级上册常见化学方程式汇编
化学九年级上册方程式

化学九年级上册方程式
1. 红磷燃烧:红磷这小家伙在氧气里一烧,就变成了五氧化二磷。
方程式是:4P + 5O₂点燃 2P₂O₅。
2. 硫燃烧:硫粉燃烧起来,和氧气结合生成二氧化硫,就像一场火热的约会!方程式:S + O₂点燃 SO₂。
3. 铁在氧气中燃烧:铁可真是个热情的家伙,在氧气里一烧,就变成了四氧化三铁。
方程式:3Fe + 2O₂点燃 Fe₃O₄。
4. 过氧化氢分解制取氧气:过氧化氢在二氧化锰这个“小助手”的帮助下,分解成水和氧气,就像变魔术一样!方程式:2H₂O₂ MnO₂ 2H₂O + O₂↑。
5. 氯酸钾受热分解制取氧气:氯酸钾在加热和二氧化锰的催化下,分解成氯化钾和氧气,努力地为我们产生氧气呢!方程式:2KClO₃加热 2KCl + 3O₂↑。
6. 高锰酸钾受热分解制取氧气:高锰酸钾加热之后,就分解成了锰酸钾、二氧化锰和氧气,这可是个大变身!方程式:2KMnO₄加热 K₂MnO₄ + MnO₂ + O₂↑。
7. 水通电分解:水通上电,就分解成了氢气和氧气,这电的力量可真神奇!方程式:2H₂O 通电 2H₂↑ + O₂↑。
8. 氢气燃烧:氢气和氧气一相遇,燃烧起来就生成了水,真是一场美丽的“结合”。
方程式:2H₂ + O₂点燃 2H₂O。
化学九年级上册全部化学方程式

化学九年级上册全部化学方程式1. 镁在空气中燃烧:2Mg + O2 =点燃= 2MgO2. 铁在氧气中燃烧:3Fe + 2O2=点燃= Fe3O43. 铜在空气中受热:2Cu + O2 =加热= 2CuO4. 铝在空气中燃烧:4Al + 3O2 =点燃= 2Al2O35. 氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 =点燃= 2P2O57. 硫粉在空气中燃烧:S + O2 =点燃= SO28. 碳在氧气中充分燃烧:C + O2 =点燃= CO29. 碳在氧气中不充分燃烧:2C + O2 =点燃= 2CO10. 一氧化碳在氧气中燃烧:2CO + O2 =点燃= 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 =点燃=CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O13.玻义耳研究空气的成分实验2HgO =加热= Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 =加热= K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2 (MnO2催化剂)=2H2O+ O2 ↑(实验室制氧气原理2)16.水在直流电的作用下分解(研究水的组成实验):2H2O =通电= 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水:H2O + CO2==H2CO319.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO =加热= Cu + H2O22. 镁还原氧化铜:Mg + CuO =加热= Cu + MgO23. 碳在氧气中充分燃烧:C + O2 =点燃= CO224.木炭还原氧化铜:C+ 2CuO =高温=2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 =高温= 4Fe + 3CO2↑26.煤炉的底层:C + O2 =点燃= CO227.煤炉的中层:CO2 + C =高温= 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 =点燃= 2CO229.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分H2CO3 == H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3=高温= CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O34.一氧化碳还原氧化铜:CO+ CuO =加热= Cu + CO235.一氧化碳的可燃性:2CO + O2 =点燃= 2CO236.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑37.甲烷在空气中燃烧:CH4 + 2O2 =点燃= CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O 39.氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O40.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO41.铁在氧气中燃烧:3Fe + 2O2 =点燃= Fe3O442. 铜在空气中受热:2Cu + O2 =加热=2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O344. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg 55.3CO+ 2Fe2O3 高温4Fe + 3CO2↑56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH 77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓+ NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。
九上所有化学方程式35个

九上所有化学方程式35个1. NaCl + H2O → NaOH + HCl(氯化钠溶于水反应)2. C3H8 + 5O2 → 3CO2 + 4H2O(烷烃燃烧反应)3. CaCO3 → CaO + CO2(石灰石溶解反应)4. 2H2S + 3O2 → 2SO2 + 2H2O(硫化氢氧化反应)5. CH4 + 2O2 → CO2 + 2H2O(甲烷燃烧反应)6. C6H12O6 + 6O2 → 6CO2 + 6H2O(糖分解反应)7. Ca + 2HCl → CaCl2 + H2(钙与盐酸反应)8. Cu + 2AgNO3 → 2Ag + Cu(NO3)2(铜与银试剂反应)9. H2SO4 + 2KOH → K2SO4 + 2H2O(酸和碱反应)10. Mg + 2HCl → MgCl2 + H2(镁与盐酸反应)11. 2Na + 2H2O → 2NaOH + H2(钠与水反应)12. Pb + 2HCl → PbCl2 + H2(铅与盐酸反应)13. CH3COOH + NaOH → CH3COONa + H2O(醋酸与碱反应)14. Fe + 2HCl → F eCl2 + H2(铁与盐酸反应)15. N2 + 3H2 → 2NH3(氨的合成反应)16. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O +5Cl2(还原性氧化物与酸反应)17. 2NaOH + H2SO4 → Na2SO4 + 2H2O(碱和酸反应)18. 2Fe + 3O2 → 2Fe2O3(铁氧化反应)19. 2H2 + O2 → 2H2O(氢气燃烧反应)20. 2K + 2H2O → 2KOH + H2(钾与水反应)21. 2Fe2O3 + 3C → 4Fe + 3CO2(铁氧化物焚烧反应)22. 2H2S + 3O2 → 2SO2 + 2H2O(硫化氢氧化反应)23. C2H6 + 7O2 → 2CO2 + 3H2O(乙烷燃烧反应)24. 2Mg + O2 → 2MgO(镁氧化反应)25. 2KClO3 → 2KCl + 3O2(氯酸钾分解反应)26. 2NaCl + H2SO4 → Na2SO4 + 2HCl(盐酸与氯化钠反应)27. Na + H2O → NaOH + 1/2H2(钠与水反应)28. 2NH3 + H2SO4 → (NH4)2SO4(硫酸与氨反应)29. 2Na + 2H2O → 2NaOH + H2(钠与水反应)30. 2C2H5OH + 3O2 → 4CO2 + 6H2O(乙醇燃烧反应)31. 2C + O2 → 2CO(一氧化碳合成反应)32. BaCl2 + 2NaOH → Ba(OH)2 + 2NaCl(氯化钡与碱反应)33. 2Al + 6HCl → 2AlCl3 + 3H2(铝与盐酸反应)34. 2Na2O2 + 2H2O → 4NaOH + O2(过氧化钠溶于水反应)35. CaCO3 → CaO + CO2(石灰石溶解反应)。
九年级上册化学所有化学方程式

九年级上册化学所有化学方程式九年级上册化学所有化学方程式如下:一、跟氢有关的化学方程式:1. 2H2+O2点燃2H2O现象:淡蓝色的火焰2. Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成3. Mg+H2SO4==MgSO4+H2↑现象:同上4. Fe+H2SO4==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体5. 2Al+3H2SO4==Al2(SO4)3+3H2↑现象:有气体生成6. Zn+2HCl==ZnCl2+H2↑现象:同上7. Mg+2HCl==MgCl2+H2↑现象:同上8. Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体9. 2Al+6HCl==2AlCl3+3H2↑现象:有气体生成10. H2+CuO====Cu+H2O现象:由黑色的固体变成红色的,同时有水珠生成高温11. 2Fe2O3+3H2=====2Fe+3H2O现象:有水珠生成,固体颜色由红色变成银白色高温二、与氧气相关反应:1. 单质与氧气的反应:(化合反应)(1)镁在空气中燃烧:2Mg + O2点燃2MgO(2)铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4(3)铜在空气中受热:2Cu + O2加热2CuO(4)铝在空气中燃烧:4Al + 3O2点燃2Al2O3(5)氢气中空气中燃烧:2H2+ O2点燃2H2O(6)红磷在空气中燃烧(研究空气组成的实验):4P + 5O2点燃2P2O5(7)硫粉在空气中燃烧:S + O2点燃SO2(8)碳在氧气中充分燃烧:C + O2点燃CO2(9)碳在氧气中不充分燃烧:2C + O2点燃2CO(10)一氧化碳在氧气中燃烧:2CO + O2点燃2CO2(11)甲烷在空气中燃烧:CH4+ 2O2点燃CO2+ 2H2O(12)酒精在空气中燃烧:C2H5OH+ 3O2点燃2CO2+ 3H2O(13)氧化汞分解实验:2HgO△Hg+ O2↑。
人教版九年级(上册)化学常用化学方程式

人教版九年级(上册)化学常用化学方程式1,高锰酸钾制取氧气:
2,过氧化氢制取氧气:
3,氯酸钾制取氧气:
4,磷在氧气中燃烧:
5,硫在氧气中燃烧:
6,铁在氧气中燃烧:
7,木炭在氧气中燃烧:
8,电解水:
9,铁与硫酸铜的反应:
10,镁与氧气的反应:
11,氧化铜与氢气的反应:
12,氢氧化钠与硫酸铜的反应:
13,碳酸钙与盐酸制取二氧化碳:
14,氧化钙与水的反应:
15,二氧化碳与氢氧化钙的反应:16,乙烯在氧气中燃烧:
17,用氢气和三氧化二铁置换铁:18,用一氧化碳和三氧化二铁置换铁:19,氧化汞加热分解:
20,锌与盐酸的反应:
21,碳酸分解:
22,用碳和氧化铜置换铜:
23,乙醇在氧气中燃烧:
24,锌与硫酸的反应:。
九年级上册化学方程式大全汇总

一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 加热2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O57. 硫粉在空气中燃烧:S + O2 点燃SO28. 碳在氧气中充分燃烧:C + O2 点燃CO29. 碳在氧气中不充分燃烧:2C + O2 点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2物质与氧气的反应制取氧气水通电分解工业制取二氧化碳:高温煅烧石灰石:CaCO3 高温CaO +CO2↑氢气还原氧化铜:H2 + CuO 加热Cu + H2O木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO2一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO2。
初中化学教材九年级上册常见化学方程式整理汇编
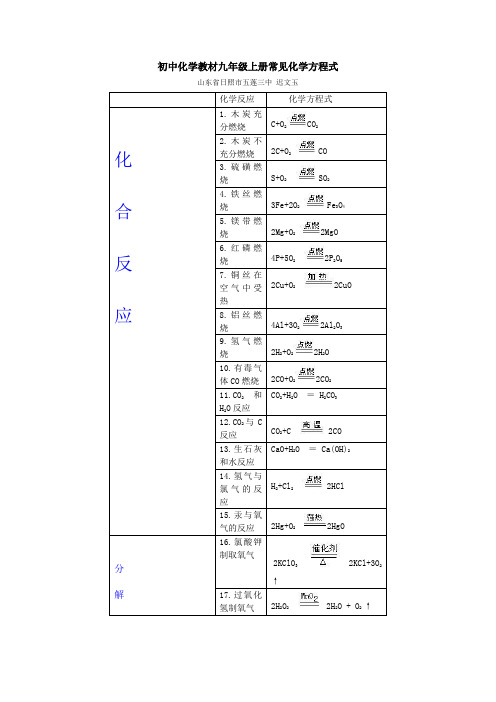
CO2+Ca(OH)2═CaCO3↓+H2O
33.大理石与稀盐酸反应
CaCO3+2HCl=CaCl2+H2O+CO2↑
34.苏打与稀盐酸反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
35.硫酸铜与氢氧化钠反应
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
2Cu+O2 2CuO
8.铝丝燃烧
4Al+3O2 2Al2O3
9.氢气燃烧
2H2+O2 2H2O
10.有毒气体CO燃烧
2CO+O2 2CO2
11.CO2和H2O反应
CO2+H2O=H2CO3
12.CO2与C反应
CO2+C 2CO
13.生石灰和水反应
CaO+H2O=Ca(OH)2
14.氢气与氯气的反应
21.碳酸钙煅烧
CaCO3 CaO+CO2↑
22.氧化汞分解
2HgO 2Hg+O2↑
23.碳酸氢钠受热分解
2NaHCO3 Na2CO3&
反
应
24.碳还原氧化铜
C+2CuO 2Cu+CO2↑
25.镁带与盐酸反应
Mg+2HCl == MgCl2+H2↑
26.氢气还原氧化铜
H2+CuO Cu+H2O
其
他
36.乙醇燃烧
C2H5OH+3O2 2CO2+3H2O
37.一氧化碳还原氧化铜
CO+CuO Cu+CO2
九年级上册化学化学方程式归纳集锦

九年级上册化学化学方程式归纳集锦一、各物质在氧气中燃烧方程式及现象1、4P + 5O2 点燃2P2 O5(验证空气含量,书P27)现象:2、C + O2 点燃CO2现象:3、S + O2 点燃SO2 (比较其在空气中燃烧的现象)现象:4、3Fe + 2O2 点燃Fe3O4 (注:铁在空气中不燃烧)现象:5、2Mg + O2 点燃2MgO现象:二、实验室制氧气原理:(氧气的物理性质、收集方法、检验、验满)MnO26、2H 2O 22H 2O+O 2↑2KCl + 3O2 ↑7、2KClO3MnO2△8、2KMnO4 △K2 MnO4 + MnO2 + O2 ↑(装置、操作步骤及注意事项书P34-35)三、水的电解(氢气的物理性质、收集方法、验纯及用途,书P46-47)9、2H2 O 通电2H2 ↑+ O2↑结论:1、2、与正极相连的气体为_______,与负极相连的气体为_______,正负极生成气体的体积比为__________,可用八个字概括_______________________四、碳在空气中燃烧(碳几种单质的物理性质及用途,碳的化学性质)10、2C + O2 点燃2CO(氧气不足)C + O2 点燃CO2 (氧气充足)五、碳的还原性11、C+ 2CuO 高温2Cu + CO2 ↑现象:12、3C+ 2Fe2O3高温4Fe + 3CO2↑13、C+ CO2高温2CO六、二氧化碳(物理性质、制取原料、收集方法、验证、验满、注意事项)14、CaCO 3+ 2HCl === CaCl2 + H2 O + CO2↑(实验室制法)15、CaCO3高温CaO + CO2 ↑16、CO2 + H2O === H2 CO3(碳酸可以使紫色石蕊溶液变_________)17、H2 CO3 === H2 O + CO2↑(碳酸的不稳定性)18、Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O(检验CO2)现象:七、一氧化碳(物理性质、化学性质)19、CO + O2 点燃2CO2(火焰呈______色)20、CO + Fe2 O3高温2Fe + 3CO2 21、CO+ CuO△Cu + CO2 22、CH4 + 2O2 点燃CO2 + 2H2 O 23、2H2 + O2 点燃2H2 O24、C2 H5OH + 3O2 点燃2CO2 + 3H2 O25、Zn+H2SO4===ZnSO4+H2↑(实验室制氢气)。
初三化学方程式汇总上册

初三化学方程式汇总上册
一、金属与氧气反应
1. 镁在空气中燃烧:2Mg + O2点燃2MgO
2. 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4
3. 铜在空气中受热:2Cu + O2加热2CuO
4. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3
二、非金属与氧气反应
1. 氢气在氧气中燃烧:2H2 + O2点燃2H2O
2. 硫在氧气中燃烧:S + O2点燃SO2
3. 红磷在氧气中燃烧:4P + 5O2点燃2P2O5
4. 碳在氧气中充分燃烧:C + O2点燃CO2
三、酸与金属反应
1. 镁与稀盐酸反应:Mg + 2HCl = MgCl2 + H2↑
2. 铝与稀硫酸反应:2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
3. 铜与稀盐酸不反应。
四、碱与金属反应
1. 镁与氢氧化钠溶液反应:2NaOH + Mg + H2O = Mg(OH)2↓+ 2NaCl
2. 铝与氢氧化钠溶液反应:6NaOH + 2Al + 6H2O = 2Al(OH)3↓+ 6NaCl
3. 铜与氢氧化钠溶液不反应。
五、盐与金属反应
1. 铁与硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu
2. 镁与氯化铜溶液反应:Mg + CuCl2 = MgCl2 + Cu
3. 铜与硝酸汞溶液反应:Cu + Hg(NO3)2 = Cu(NO3)2 + Hg。
九上全部化学方程式总结

九上全部化学方程式总结化学方程式是描述化学反应过程的符号表示方法。
在九年级的化学学习中,学生主要学习了酸碱中和反应、氧化还原反应、还原反应以及金属活动性等方面的知识。
下面将对九年级全部化学方程式进行总结。
一、酸碱中和反应:1.酸和碱反应生成盐和水的反应:HCl + NaOH → NaCl + H₂OH₂SO₄ + 2NaOH → Na₂SO₄ + 2H₂O2HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + 2H₂O2.酸和金属碱反应生成盐和水的反应:HCl + NaOH → NaCl + H₂OHNO₃ + KOH → KNO₃ + H₂OH₂SO₄ + 2KOH → K₂SO₄ + 2H₂O二、氧化还原反应:1.金属和非金属元素的氧化反应:2Mg + O₂ → 2MgO2Na + Cl₂ → 2NaClCa + S → CaS2.金属和酸的反应:Zn + 2HCl → ZnCl₂ + H₂Mg + 2HNO₃ → Mg(NO₃)₂ + H₂O + NO₂3.金属和盐酸的反应:Mg + 2HCl → MgCl₂ + H₂Zn + HCl → ZnCl₂ + H₂4.单质和氧气的反应:C + O₂ → CO₂S + O₂ → SO₂2Fe + 3O₂ → 2Fe₂O₃5.金属和非金属氧化物的反应:Na₂O + H₂O → 2NaOHMgO + H₂O → Mg(OH)₂CaO + H₂O → Ca(OH)₂三、还原反应:1.金属氧化物还原反应:2Na + 2H₂O → 2NaOH + H₂2Al + 3H₂O → Al₂O₃ + 3H₂2Zn + O₂ → 2ZnO2.金属酸还原反应:Zn + H₂SO₄ → ZnSO₄ + H₂3Fe + 4H₂SO₄ → 3Fe₂(SO₄)₃ + 4H₂O + SO₂3.单质还原反应:C + 2H₂O → CO₂ + 2H₂S + 2H₂O → H₂S + H₂SO₄四、金属活动性:1.金属置换反应:Zn + CuSO₄ → ZnSO₄ + CuMg + FeSO₄ → MgSO₄ + FeFe + Zn(NO₃)₂ → Fe(NO₃)₂ + Zn2.金属和酸的反应:Zn + 2HCl → ZnCl₂ + H₂Mg + 2HNO₃ → Mg(NO₃)₂ + H₂O + NO₂以上是九年级化学学习中的一些常见化学方程式。
初三化学上册化学方程式

初三化学上册化学方程式
1、氢氧化钠+氯气=氯化钠+氢气
2、锂+氧=锂氧化物
3、硫+水=硫酸
4、蒸汽加热乙醇=乙醛及水
5、磷酸铵+碳酸钾=磷酸二钾+二氧化碳
6、硫+碱=元素硫+盐
一、氢氧化钠+氯气=氯化钠+氢气
在室温下,氯气(Cl2)可以用得其他化学反应。
例如它可以与氢氧化钠(NaOH)发生以下化学反应,生成氯化钠(NaCl)加氢气(H2)的反应条件下反应方程式如下:
NaOH + Cl2 = NaCl + H2
二、锂+氧=锂氧化物
锂(Li)与氧(O2)化学反应可以生成锂氧化物(Li2O),它的反应方程式如下:
Li + O2 = Li2O
三、硫+水=硫酸
硫(S)与水(H2O)发生反应可以生成硫酸(H2SO4)。
它的反应条件是在高温、饱和气氛下,反应方程式如下:
S + H2O = H2SO4
四、蒸汽加热乙醇=乙醛及水
乙醇(C2H5OH)在蒸汽加热下可以生成乙醛(CH3CHO)和水(H2O),反应方程式为:
C2H5OH = CH3CHO + H2O
五、磷酸铵+碳酸钾=磷酸二钾+二氧化碳
磷酸铵(NH4H2PO4)与碳酸钾(K2CO3)结合可以生成磷酸二钾(K2H2PO4)与二氧化碳(CO2),反应方程式为:
NH4H2PO4 + K2CO3 = K2H2PO4 + CO2
六、硫+碱=元素硫+盐
硫(S)与碱(NaOH)发生反应可以生成元素硫(S0)和盐
(Na2SO4),反应方程式为:
S + NaOH = S0 + Na2SO4。
九年级上册化学化学方程式汇总

CO2+CaOH2=CaCO3↓+ H2O
19
镁在二氧化碳中燃烧
2Mg+CO2点燃2MgO +C
20
碳和二氧化碳反应
C+CO2高温2CO
21
实验室制二氧化碳
CaCO3+ 2HCl==CaCl2+ CO2↑+ H2O
22
工业制取二氧化碳
CaCO3高温CaO + CO2↑
23
一氧化碳在空气中燃烧
HCl + NaOH == NaCl + H2O 2HCl + CaOH2== CaCl2+ 2H2O
H2SO4+ 2NaOH == Na2SO4+ 2H2O H2SO4+ BaCl2== BaSO4↓+ 2HCl
2HCl + Na2CO3== 2NaCl + CO2↑+ H2O
2HCl + CaCO3== CO2↑+ CaCl2+ H2O实验室制备CO2
2HCl +Zn == ZnCl2+ H2↑ H2SO4+ Fe == FeSO4+ H2↑
2HCl + Fe == FeCl2+ H2↑
Fe2O3+3H2SO4== Fe2SO43+ 3H2O Fe2O3+6HCl == 2FeCl3+ 3H2O
CuO + 2HCl == CuCl2+ 2H2O CuO +H2SO4== CuSO4+ H2O
CaOH2+ CO2== CaCO3↓+ H2O澄清石灰水变浑浊的原因
九年级上册化学方程式汇总
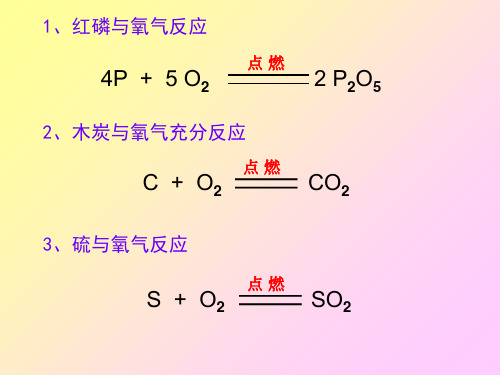
23、空气中加热铜粉
2Cu + O2
2 CuO
24、氧化汞分解
2HgO
2 Hg + O2
25、二氧化碳与水反应
CO2 + H2O
26、生石灰与水反应
CaO + H2O
27、碳酸分解
H2CO3
H2CO3 Ca(OH)2 CO2 + H2O
28、二氧化碳使澄清石灰水变浑浊
CO2 + Ca(OH)2
CaCO3 + H2O
点燃
2C + O2
2 CO
18、碳与二氧化碳反应
高温
C + CO2
2 CO
19、木炭还原氧化铜
高温
C + 2CuO
2Cu + CO2
20、焦炭还原氧化铁
高温
3C + 2Fe2O3
4Fe + 3CO2
21、一氧化碳还原氧化铜
CO + CuO
Cu + CO2
22、一氧化碳燃烧
点燃
2CO + O2
2 CO2
1、红磷与氧气反应
4P + 5 O2
点燃
2 P2O5
2、木炭与氧气充分反应
点燃
C + O2
CO2
3、硫与氧气反应
点燃
S + O2
SO2
4、铁丝与氧气反应
点燃
3Fe + 2 O2
5、铁在空气中缓慢氧化
Fe3O4
4Fe + 3 O2
6、高锰酸钾制取氧气
2FO2 + O2
12、氢气与氧气反应
点燃
初三上册化学方程式大全(10篇)

初三上册化学方程式大全(10篇)1.初三上册化学方程式大全篇一跟氢有关的化学方程式:2H2+O2点燃====2H2O现象:淡蓝色的火焰Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成H2+CuO====Cu+H2O现象:由黑色的固体变成红色的,同时有水珠生成高温2Fe2O3+3H2=====2Fe+3H2O现象:有水珠生成,固体颜色由红色变成银白色跟碳有关的化学方程式:C+O2点燃====CO2(氧气充足的情况下)现象:生成能让纯净的石灰水变浑浊的气体2C+O2点燃====2CO(氧气不充足的情况下)现象:不明显高温C+2CuO=====2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成高温3C+2Fe2O3=====4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的'气体生成CO2+C高温====2CO现象:黑色固体逐渐减少3C+2H2O=CH4+2CO现象:生成的混和气体叫水煤气,都是可以燃烧的气体2.初三上册化学方程式大全篇二跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温FeO+CO===Fe+CO2现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温Fe2O3+3CO====2Fe+3CO2现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温CuO+CO====Cu+CO2现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成3.初三上册化学方程式大全篇三跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致4.初三上册化学方程式大全篇四跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O现象:无明显现象2NaOH+SO2==Na2SO3+H2O现象:无明显现象5.初三上册化学方程式大全篇五跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl现象:有白色的不溶于强酸的沉淀生成跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O现象:生成白色沉淀跟几种金属及其盐有关的化学方程式:铜:CuSO45H2O△====CuSO4+5H2O↑现象:固体由蓝色变为白色高温CuO+CO====Cu+CO2现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H2+CuO====Cu+H2O现象:固体由黑色逐渐变成红色,同时有水珠生成Cu+2AgNO3==Cu(NO3)2+2Ag现象:铜表面慢慢生成了银白色金属CuCl2+2NaOH==Cu(OH)2↓+2NaCl现象:生成了蓝色絮状沉淀CuO+H2SO4==CuSO4+H2O现象:黑色固体溶解,生成蓝色溶液6.初三上册化学方程式大全篇六跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H22O现象:不明显HCl+AgNO3==AgCl↓+HNO3现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成7.初三上册化学方程式大全篇七跟二氧化碳有关的化学方程式:C+O2点燃====CO2现象:生成能使纯净的石灰水变浑浊的气体Ca(OH)2+CO2===CaCO3↓+H2O现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2现象:白色固体逐渐溶解Ca(HCO3)△====CaCO3↓+CO2↑+H2O现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu2(OH)2CO3△====2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显CaCO3高温====CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成8.初三上册化学方程式大全篇八1、2Mg+O2点燃2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2、2Hg+O2点燃2HgO银白液体、生成红色固体拉瓦锡实验3、2Cu+O2Δ2CuO红色金属变为黑色固体4、4Al+3O2点燃2Al2O3银白金属变为白色固体5、3Fe+2O2点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe+3O2高温2Fe2O36、C+O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊7、S+O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰8、2H2+O2点燃2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料9、4P+5O2点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10、CH4+2O2点燃2H2O+CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧11、2C2H2+5O2点燃2H2O+4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属12、2KClO3MnO22KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气O213、2KMnO4ΔK2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气14、2HgOΔ2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验15、2H2O通电2H2↑+O2↑水通电分解为氢气和氧气电解水16、Cu2(OH)2CO3Δ2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热17、NH4HCO3ΔNH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失18、Zn+H2SO4=ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气19、Fe+H2SO4=FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解20、Mg+H2SO4=MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解9.初三上册化学方程式大全篇九1、氧化性:2FeCl3+Fe===3FeCl22FeCl3+Cu===2FeCl2+CuCl2(用于雕刻铜线路版)2FeCl3+Zn===2FeCl2+ZnCl2FeCl3+Ag===FeCl2+AgCFe2(SO4)3+2Ag===FeSO4+Ag2SO4(较难反应)Fe(NO3)3+Ag不反应2FeCl3+H2S===2FeCl2+2HCl+S2FeCl3+2KI===2FeCl2+2KCl+I2FeCl2+Mg===Fe+MgCl22、还原性:2FeCl2+Cl2===2FeCl33Na2S+8HNO3(稀)===6NaNO3+2NO+3S+4H2O3Na2SO3+2HNO3(稀)===3Na2SO4+2NO+H2O2Na2SO3+O2===2Na2SO43、与碱性物质的作用:MgCl2+2NH3.H2O===Mg(OH)2+NH4ClAlCl3+3NH3.H2O===Al(OH)3+3NH4ClFeCl3+3NH3.H2O===Fe(OH)3+3NH4Cl10.初三上册化学方程式大全篇十1.需水浴加热的反应列表有:(1)银镜反应;(2)乙酸乙酯的水解;(3)苯的硝化;(4)糖的水解;(5)酚醛树脂的制取;(6)固体溶解度的测定;凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
九年级上册化学方程式大全

九年级上册化学方程式大全方程是指含有未知数的等式。
是表示两个数学式(如两个数、函数、量、运算)之间相等关系的一种等式,使等式成立的未知数的值称为“解”或“根”。
求方程的解的过程称为“解方程”。
九年级上册化学方程式大全:【盐酸方程式】NaOH(也可为KOH)+HCl==NaCl+H2O现象:不明显HCl+AgNO3==AgCl↓+HNO3现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O现象:红色固体逐渐溶解,形成*的溶液Fe(OH)3+3HCl==FeCl3+3H2O现象:红棕色絮状沉淀溶解,形成了*的溶液Cu(OH)2+2HCl==CuCl2+2H2O现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成【硫酸方程式】2NaOH(或KOH)+H2SO4==Na2SO4+2H2O现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O现象:红色固体溶解,生成*溶液CuO+H2SO4==CuSO4+H2O现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致【*方程式】Fe2O3+6HNO3==2Fe(NO3)3+3H2O现象:红色固体溶解,生成*溶液CuO+2HNO3==Cu(NO3)2+H2O现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致【置换反应】(1)盐(溶液)+金属单质-------另一种金属+另一种盐铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu(2)盐+酸--------另一种酸+另一种盐碳酸钠与稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑碳酸氢钠与稀盐酸反应:NaHCO3+HCl==NaCl+H2O+CO2↑(3)盐+碱--------另一种碱+另一种盐氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH (4)盐+盐-----两种新盐氯化钠溶液和*银溶液:NaCl+AgNO3==AgCl↓+NaNO3硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl1,氧化性:2FeCl3+Fe===3FeCl22FeCl3+Cu===2FeCl2+CuCl2(用于雕刻铜线路版)2FeCl3+Zn===2FeCl2+ZnCl2FeCl3+Ag===FeCl2+AgClFe2(SO4)3+2Ag===2FeSO4+Ag2SO4(较难反应)Fe(NO3)3+Ag不反应2FeCl3+H2S===2FeCl2+2HCl↑+S↓2FeCl3+2KI===2FeCl2+2KCl+I2FeCl2+Mg===Fe+MgCl2TlCl3+2Ag===2AgCl+TlCl(*、铅、铋的高价化合物都有强氧化性) 2,还原性:2FeCl2+Cl2===2FeCl3SnCl2+Cl2===SnCl4(SnCl2有强还原性)3Na2S+8HNO3(稀)===6NaNO3+2NO↑+3S↓+4H2O3Na2SO3+2HNO3(稀)===3Na2SO4+2NO↑+H2O2Na2SO3+O2===2Na2SO43,与碱性物质的作用:MgCl2+2NH3.H2O===Mg(OH)2↓+NH4ClAlCl3+3NH3.H2O===Al(OH)3↓+3NH4ClFeCl3+3NH3.H2O===Fe(OH)3↓+3NH4Cl4,与酸性物质的作用:Na3PO4+HCl===Na2HPO4+NaClNa2HPO4+HCl===NaH2PO4+NaClNaH2PO4+HCl===H3PO4+NaClNa2CO3+HCl===NaHCO3+NaClNaHCO3+HCl===NaCl+H2O+CO2↑3Na2CO3+2AlCl3+3H2O===2Al(OH)3↓+3CO2↑+6NaCl 3Na2CO3+2FeCl3+3H2O===2Fe(OH)3↓+3CO2↑+6NaCl 3NaHCO3+AlCl3===Al(OH)3↓+3CO2↑3NaHCO3+FeCl3===Fe(OH)3↓+3CO2↑3Na2S+Al2(SO4)3+6H2O===2Al(OH)3↓+3H2S↑3NaAlO2+AlCl3+6H2O===4Al(OH)3↓+3NaCl5,不稳定性:Na2S2O3+H2SO4===Na2SO4+S+SO2↑+H2ONH4HCO3===NH3+H2O+CO2↑2KNO3===2KNO2+O2↑Cu(NO3)2===CuO+3NO2+O2↑2KMnO4===K2MnO4+MnO2+O2↑(用于实验室准备氧气)2KClO3===2KCl+3O2↑2NaHCO3===Na2CO3+H2O+CO2↑Ca(HCO3)2===CaCO3+H2O+CO2↑CaCO3===CaO+CO2↑MgCO3===MgO+CO2↑H2SO3===H2O+SO2↑ThI4==高温==Th+2I2↑(部分金属的碘化物高温下不稳定,分解反应用于提纯金属) 2NH4ClO4==Δ==N2↑+2O2↑+Cl2↑+4H2O↑(高氯酸铵用作火箭助推物,分解产生的大量气体能推动火箭升空)2ClO2==加热或震荡==Cl2+2O2(二氧化氯不稳定,会爆炸性分解)2BaO2==△==2BaO+O2↑(过氧化钡能在700℃分解)。
初三上册化学方程式汇总完整版

初三上册化学方程式汇总Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-初三化学上册化学方程式汇总一.物质与氧气的反应:(1)单质与氧气的反应:现象1.镁在空气中燃烧:2Mg+O2点燃2MgO(发出耀眼白光、放热、生成白色粉末)2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O4(剧烈燃烧火星四射,放热、生成黑色固体)3.铜在空气中受热:2Cu+O2△2CuO(红色固体变为黑色)4.铝在空气中氧化:4Al+3O22Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧:4P+5O2点燃2P2O5(放热、生成大量白烟)7.硫粉在空气中燃烧:S+O2点燃SO2(硫在空气里燃烧发出微弱的淡蓝色火焰,在氧气中燃烧得更旺发出蓝紫色火焰,放热、生成有刺激性气味的气体)8.碳在氧气中充分燃烧:C+O2点燃CO2(发出白光、放热、生成一种能使石灰水变浑浊的无色气体)9.碳在氧气中不充分燃烧:2C+O点燃2CO (2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精/乙醇在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O二.实验室制取氧气、二氧化碳、氢气原理★★★★13.加热高锰酸钾:2KMnO4△K2MnO4+MnO2+O2↑★14.加热氯酸钾(二氧化锰做催化剂):2KClO3MnO22KCl+3O2↑★15.双氧水制取氧气:2H2O2MnO22H2O+O2↑★16.△实验室制取二氧化碳:CaCO3+2HClCaCl2+CO2↑+H2O17.实验室制取氢气:Zn+H2SO4(稀)ZnSO4+H2↑三.利用氢气、碳、一氧化碳还原性的反应:18.一氧化碳还原四氧化三铁:Fe3O4+4CO高温3Fe+4CO219.氢气还原氧化铜:CuO+H2高温H2O+Cu★20.木炭还原氧化铜:2CuO+C高温CO2↑+2Cu(有红色固体生成,有能使澄清石灰水变浑的气体生成)21.焦炭还原氧化铁:2Fe2O3+3C高温4Fe+3CO2↑22.焦炭还原四氧化三铁:Fe3O4+2C高温3Fe+2CO2↑★23.一氧化碳还原氧化铜:CuO+CO高温Cu+CO2(黑色粉末变红色,有能使澄清石灰水变浑的气体生成)★24.一氧化碳还原氧化铁:Fe2O3+3CO高温2Fe+3CO2(炼铁原理)(红色粉末变黑色,有能使澄清石灰水变浑的气体生成)25..二氧化碳与碳高温下反应:C+CO高温2CO 四.其它反应:26.碳酸不稳定而分解:H2CO3CO2↑+H2O(红色石蕊试液变紫)★27.水在直流电的作用下分解:2H2O通电2H2↑+O2↑(生成无色气体,正氧负氢,氢二氧一)28.二氧化碳溶解于水:CO2+H2O==H2CO3(紫色石蕊试液变红)29.高温煅烧石灰石:CaCO3高温CaO+CO2↑(工业制二氧化碳)★30.检验二氧化碳的方法;石灰水露置在空气中产生一层白膜;刚粉刷的墙壁出汗;石灰水变浑浊;石灰水瓶壁有一层白膜CO2+Ca(OH)2CaCO3↓+H2O31.铁与硫酸铜反应:Fe+CuSO4FeSO4+Cu(生成红色固体,蓝色溶液变为浅绿色)32.碳酸钠与盐酸反应(泡沫灭火器原理):Na2CO3+2HCl2NaCl+CO2↑+H2O33.氢氧化钠与硫酸铜反应:CuSO4+2NaOHCu(OH)2↓+Na2SO4(有蓝色沉淀生成)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学教材九年级上册常见化学方程式汇编
化学反应化学方程式特征及现象
化合
反
应1.木炭充分燃
烧C+O2CO2
“百炼成钢”原理
2.木炭不充分
燃烧2C+O2 2CO
生成有毒气体
3.硫磺燃烧
S+O2 SO2
有蓝(紫)色火焰.生成刺
激性气体
4.铁丝燃烧
3Fe+2O2 Fe3O4
火星四射.生成黑色
固体
5.镁带燃烧
2Mg+O2 2MgO
有耀眼白光,生成白
色固体
6.红磷燃烧
4P+5O22P2O5
有大量白烟生成
7.铜丝在空气
中受热2Cu+O22CuO
亮红色固体变成黑
色固体
8.铝丝燃烧
4Al+3O22Al2O3
火星四射,生成白色
固体
9.氢气燃烧
2H2+O22H2O
有淡蓝色火焰
10.有毒气体CO
燃烧2CO+O22CO2
有蓝色火焰
11.CO2和H2O反
应
CO2+H2O = H2CO3生成物能使石蕊变
红
12.CO2与C反应
CO2+C 2CO
所有物质中都含碳
元素
13.生石灰和水
反应
CaO+H2O = Ca(OH)2实验室制氢氧化钙,
反应放热
14.氢气与氯气
的反应H2+Cl2 2HCl
15.汞与氧气的
反应2Hg+O22HgO
银白色液体变成粉
红色固体
分解反应16.氯酸钾制取
氧气
2KClO3 2KCl+3O2↑
加热固体混合物制
取氧气
17.过氧化氢制
氧气2H2O2 2H2O + O2↑
常温下固液混合物
制取氧气
18.高锰酸钾制
氧气2KMnO4K2MnO4+MnO2+O2↑
加热纯净物制取氧
气
19.水电解
2H2O 2H2↑+O2↑
分解产生两种气体
单质
20.碳酸分解H2CO3= H2O+CO2↑
21.碳酸钙煅烧
CaCO3CaO+CO2↑
工业制取二氧化碳
22.氧化汞分解
2HgO 2Hg+O2↑产生银白色液体金属
23.碳酸氢钠受
热分解2NaHCO3Na2CO3+CO2↑ +H2O
干粉灭火器的原理
置换反应24.碳还原氧化
铜C+2CuO 2Cu+CO2↑
黑色固体混合物加热生
成红色固体
25.碳还原氧化
铁3C+2Fe2O3 4Fe+3CO2↑
固体混合物反应生
黑色固体
26.碳还原四氧
化三铁2C+Fe3O4 3Fe+2CO2↑
黑色固体混合物加热生
黑色固体
27.镁带与盐酸
反应
Mg+2HCl == MgCl2 +H2↑该反应放热
28.氢气还原氧
化铜H2+CuO Cu+H2O
单质气体还原氧化铜,生
红色固体
29.锌与稀硫酸
反应
Zn+H2SO4 == ZnSO4 +H2↑实验室制取氢气
30.铁丝与硫酸
铜反应
Fe+CuSO4 == FeSO4+Cu白色固体表面附有红色
(湿法炼铜)
复分解反应31.氢氧化钠溶液
吸收CO2CO2+2NaOH═Na2CO3+H2O氢氧化钠变质,吸收
二氧化碳
32.氢氧化钙溶液吸收CO2CO2+Ca(OH)2═CaCO3↓+H2O石灰水变浑浊,检验
二氧化碳
33.大理石与稀盐酸反应CaCO3+2HCl=CaCl2+H2O+CO2↑实验室
制CO2
碳酸盐或
碳酸氢盐
遇酸生成
CO2
34.苏打与稀盐酸反应Na2CO3+2HCl=2NaCl+H2O+CO2↑泡沫灭火
器的原理
35.硫酸铜与氢氧
化钠反应
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4有蓝色沉淀
其他36.乙醇燃烧
C2H5OH+3O22CO2+3H2O
绿色燃料燃烧
37.一氧化碳还原
氧化铜CO+CuO Cu+CO2
化合物的气体还原
氧化铜
38.一氧化碳还原
氧化铁3CO+Fe2O32Fe+3CO2
工业用赤铁矿炼铁
39.一氧化碳还原四
氧化三铁4CO+Fe3O43Fe+4CO2
工业用磁铁矿炼铁
40.甲烷燃烧
CH4+2O2CO2+2H2O
有蓝色火焰。
