氢在Gasar工艺常用纯金属中的溶解度
钢中氢气体知识问答(3)
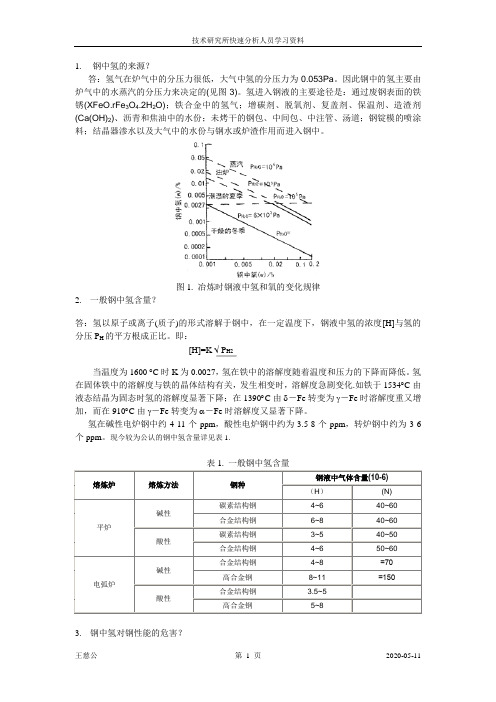
1.钢中氢的来源?答:氢气在炉气中的分压力很低,大气中氢的分压力为0.053Pa。
因此钢中的氢主要由炉气中的水蒸汽的分压力来决定的(见图3)。
氢进入钢液的主要途径是:通过废钢表面的铁锈(XFeO.rFe3O4.2H2O);铁合金中的氢气;增碳剂、脱氧剂、复盖剂、保温剂、造渣剂(Ca(OH)2)、沥青和焦油中的水份;未烤干的钢包、中间包、中注管、汤道;钢锭模的喷涂料;结晶器渗水以及大气中的水份与钢水或炉渣作用而进入钢中。
图1. 冶炼时钢液中氢和氧的变化规律2.一般钢中氢含量?答:氢以原子或离子(质子)的形式溶解于钢中,在一定温度下,钢液中氢的浓度[H]与氢的分压P H的平方根成正比。
即:[H]=K √ P H2当温度为1600 ︒C时K为0.0027,氢在铁中的溶解度随着温度和压力的下降而降低。
氢在固体铁中的溶解度与铁的晶体结构有关,发生相变时,溶解度急剧变化.如铁于1534︒C由液态结晶为固态时氢的溶解度显著下降;在1390︒C由δ-Fe转变为γ-Fe时溶解度重又增加,而在910︒C由γ-Fe转变为α-Fe时溶解度又显著下降。
氢在碱性电炉钢中约4-11个ppm,酸性电炉钢中约为3.5-8个ppm,转炉钢中约为3-6个ppm。
现今较为公认的钢中氢含量详见表1.表1. 一般钢中氢含量3.钢中氢对钢性能的危害?答:氢溶入钢中会降低钢的塑性和韧性。
研究表明,氢含量高不仅会导致钢的伸长率和面缩率急剧降低,还易产生氢致裂纹缺陷。
钢在冷却放置过程中,氢呈过饱和固溶体状态,由于其具有极强的扩散能力,很可能聚集在某些部位,使钢产品的局部压力增高,产生白点,形成内裂,进一步诱发高碳钢的疲劳损伤,严重影响其使用性能。
另一方面,冷却放置时,氢也能扩散到大气中,从而降低钢中的氢含量,减弱其危害。
4. 如何降低钢中氢?答:溶解在钢中的氢和氮以原子状态存在,其溶解反应为:{}[]H H =2%21在一定温度下达到平衡时: []212%H H P H K =[]2%H H P K H ⋅=上式说明氢在钢中的溶解度与作用在钢液面上的氢的分压的平方根成正比,即称西华特定律。
氢气在镍钯溶解度-概述说明以及解释

氢气在镍钯溶解度-概述说明以及解释1.引言1.1 概述概述部分的内容应该涵盖对于氢气在镍钯溶解度的简要介绍以及研究背景。
可以按照以下方式进行撰写:概述氢气在镍和钯金属中的溶解度是氢材料学领域中一个重要的研究领域。
镍和钯是两个常用的催化剂和吸氢材料,对于氢能源存储、氢化反应和氢传递等领域具有广泛的应用。
了解氢气在镍和钯中的溶解度对于揭示氢在金属中的吸附、扩散和吸附行为,以及材料的氢化性能具有重要意义。
随着氢能源技术的发展和应用领域的拓展,对于氢气在金属中的溶解度进行深入研究成为研究的热点之一。
目前的研究表明,氢气在镍和钯中的溶解度受到多种因素的影响,如温度、压力、合金成分等。
其中,镍钯合金作为一种重要的氢吸附材料,其表面形貌、晶体结构和杂质掺杂等因素也会对氢气的吸附和扩散行为产生显著影响。
本文将重点探讨氢气在镍和钯金属中的溶解度,通过综合分析已有的研究成果,总结氢气在镍和钯中的溶解度规律,并展望未来研究的方向和发展趋势。
通过对氢在镍、钯金属中的溶解度的深入研究,有望为氢能源技术的进一步发展和应用提供有力的理论和实验支持。
同时,本文还将探讨氢气在镍钯合金中的溶解度与材料性能之间的关联,为材料设计和合金优化提供一定的参考和借鉴。
文章结构部分应该介绍文章的整体结构和内容安排,以便读者能够更好地理解文章的组织和主要内容。
在这个部分,可以简要描述每个章节的主题和目标,以及它们在整体文章中的位置和作用。
可以按照以下方式写作文章结构部分:1.2 文章结构本文按照如下结构展开,以便系统地探讨氢气在镍和钯中的溶解度。
第一部分是引言。
在引言中,我们将概述本文的研究背景和意义,并阐述本文的目的和重要性。
第二部分是正文。
正文分为两个章节,分别讨论氢气在镍和钯中的溶解度。
2.1 氢气在镍中的溶解度。
这一章节将详细介绍氢气在镍中的物理和化学特性,以及氢气在镍中的溶解行为和影响因素。
我们将探讨镍与氢气的相互作用机制,并讨论涉及到氢气溶解度的实验方法和测定结果。
钢中氢气体知识问答(3)

钢中氢气体知识问答(3)1.钢中氢的来源?答:氢气在炉气中的分压力很低,大气中氢的分压力为0.053Pa。
因此钢中的氢主要由炉气中的水蒸汽的分压力来决定的(见图3)。
氢进入钢液的主要途径是:通过废钢表面的铁锈(XFeO.rFe3O4.2H2O);铁合金中的氢气;增碳剂、脱氧剂、复盖剂、保温剂、造渣剂(Ca(OH)2)、沥青和焦油中的水份;未烤干的钢包、中间包、中注管、汤道;钢锭模的喷涂料;结晶器渗水以及大气中的水份与钢水或炉渣作用而进入钢中。
图1. 冶炼时钢液中氢和氧的变化规律2.一般钢中氢含量?答:氢以原子或离子(质子)的形式溶解于钢中,在一定温度下,钢液中氢的浓度[H]与氢的分压P H的平方根成正比。
即:[H]=K √ P H2当温度为1600 ?C时K为0.0027,氢在铁中的溶解度随着温度和压力的下降而降低。
氢在固体铁中的溶解度与铁的晶体结构有关,发生相变时,溶解度急剧变化.如铁于1534?C由液态结晶为固态时氢的溶解度显著下降;在1390?C由δ-Fe转变为γ-Fe时溶解度重又增加,而在910?C由γ-Fe转变为α-Fe时溶解度又显著下降。
氢在碱性电炉钢中约4-11个ppm,酸性电炉钢中约为3.5-8个ppm,转炉钢中约为3-6个ppm。
现今较为公认的钢中氢含量详见表1.表1. 一般钢中氢含量3.钢中氢对钢性能的危害?答:氢溶入钢中会降低钢的塑性和韧性。
研究表明,氢含量高不仅会导致钢的伸长率和面缩率急剧降低,还易产生氢致裂纹缺陷。
钢在冷却放置过程中,氢呈过饱和固溶体状态,由于其具有极强的扩散能力,很可能聚集在某些部位,使钢产品的局部压力增高,产生白点,形成内裂,进一步诱发高碳钢的疲劳损伤,严重影响其使用性能。
另一方面,冷却放置时,氢也能扩散到大气中,从而降低钢中的氢含量,减弱其危害。
4. 如何降低钢中氢?答:溶解在钢中的氢和氮以原子状态存在,其溶解反应为:{}[]H H =2%21在一定温度下达到平衡时: []212%H H P H K =[]2%H H P K H ?=上式说明氢在钢中的溶解度与作用在钢液面上的氢的分压的平方根成正比,即称西华特定律。
氢在钢中的溶解度

氢在钢中的溶解度钢是一种由铁和碳组成的合金,具有高强度和耐腐蚀性能。
然而,钢材在生产、加工和使用过程中,常常会与氢接触,导致氢在钢中的溶解。
氢在钢中的溶解度是指单位体积的钢中可以溶解的氢的质量。
了解氢在钢中的溶解度对于预防氢脆性破坏以及钢材的使用寿命具有重要意义。
氢在钢中的溶解度受多种因素的影响,其中包括温度、压力、氢气浓度、钢的化学成分和结构等。
首先,温度是影响氢在钢中溶解度的重要因素之一。
一般来说,随着温度的升高,钢中氢的溶解度会增加,因为高温可以提供更多的能量,促使氢原子从气相迁移到固相中。
但是,在一定范围内,溶解度也受到反应速率的影响,过高的温度可能会导致氢的释放,从而降低溶解度。
压力也会对氢在钢中的溶解度产生影响。
根据亨利定律,气体在液体中的溶解度与压力成正比。
因此,增加氢气的压力可以促使其在钢中的溶解度增加。
这也是为什么在高压氢气环境中,钢材更容易吸收氢气。
氢气浓度是另一个影响氢在钢中溶解度的因素。
当氢气浓度较高时,其分压也相应增大,从而增加了氢在钢中的溶解度。
因此,在与高浓度氢气接触的环境中,钢材更容易吸收氢气。
钢的化学成分和结构也会对氢在钢中的溶解度产生影响。
一些合金元素,如镍和铬,可以降低氢在钢中的溶解度。
这是因为这些元素与氢形成化合物,减少了氢在钢中的自由状态。
对于钢材的生产和使用,了解氢在钢中的溶解度至关重要。
过高的氢含量可能导致氢脆性破坏,使钢材失去原有的强度和韧性。
因此,在生产过程中,需要采取措施减少氢的吸收,如控制温度、压力和氢气浓度。
此外,也可以通过添加合金元素来降低氢在钢中的溶解度。
在使用过程中,应定期检查钢材中的氢含量,并及时采取措施处理含氢问题,以延长钢材的使用寿命。
氢在钢中的溶解度受温度、压力、氢气浓度、钢的化学成分和结构等多种因素的影响。
了解氢在钢中的溶解度对于预防氢脆性破坏以及延长钢材的使用寿命具有重要意义。
在钢材的生产和使用过程中,应注意控制氢的吸收,并采取相应的措施处理含氢问题。
基于Aspen Plus的氢气在烃类中溶解度的计算

基于Aspen Plus的氢气在烃类中溶解度的计算韩兴华;董婷;白昊;王艳红【摘要】运用 Aspen Plus闪蒸分离模块建立模拟流程,采用5个物性方程和经验公式计算氢气在十六烷-四氢萘混合溶剂中的溶解度.四氢萘的质量分数为0.226、0.339和0.539,氢气的质量流率为1.5 kg/h,混合溶剂的质量流率为500 kg/h,在温度为453.15,543.15和623.15 K,压力为1~11 MPa条件下,对氢气在十六烷和四氢萘混合溶剂中进行闪蒸平衡分离计算.对比模拟值和测量值,探讨物性方程的使用范围.在温度为543.15 K和673.15 K,压力为3~10 MPa条件下,选取 SRK和PENG-ROB物性方程和经验公式,分别对氢气在十氢萘、四氢萘、十二烷和十六烷中进行溶解度计算.结果表明,在一定的温度和压力下,选择合适的物性方程,运用Aspen Plus闪蒸分离模块可准确计算氢气在烃类中的溶解度.%A simulation model of flash separation unit is established using Aspen Plus.The solubility of hydrogen in hexadecane-1,2,3,4-tetrahydronaphthalene was determined with five property methods a-vailable in Aspen Plus and an empirical equation.The weight percent of 1,2,3,4-tetrahydronaphthalene is 0.226,0.339,0.539,at temperatures of 453.15 K,543.15 K to 623.15 K and pressures from 1 MPa to 1 1 MPa,the flash equilibrium calculation can be achieved when the mass flow of hydrogen is 1 .5 kg/h and the mass flow of mixture is 500 kg/h.The application of the property methods was discussed based on the average absolute deviation between the measured values and experimental results.At tem-perature of 543.15 K and 673.15 K and pressures of 3.0~10 MPa,the flash separator model is built to calculate solubility of hydrogen in hydrocarbons,naphthane,1,2,3,4-tetrahydronaphthalene,dodecane and hexadecane based on SRK,PENG-ROB and empirical equation.The results suggest that the flash separation unit of Aspen Plus can calculate hydrogen solubility in hydrocarbons accurately under a cer-tain temperature and pressure conditions when property methods are chosen correctly.【期刊名称】《中北大学学报(自然科学版)》【年(卷),期】2016(037)005【总页数】6页(P516-521)【关键词】Aspen Plus;物性方程;经验公式;氢气;溶解度【作者】韩兴华;董婷;白昊;王艳红【作者单位】中北大学化工与环境学院,山西太原 030051;中北大学化工与环境学院,山西太原 030051;一重集团大连设计研究院有限公司,辽宁大连 116000;中北大学化工与环境学院,山西太原 030051【正文语种】中文【中图分类】TP391.9汽柴油中微量的含硫组分燃烧后生成的SOx,不仅会导致酸雨,还会使发动机尾气处理系统失效,从而导致机动车尾气中NOx、 CO、颗粒物等有毒物排放. 随着我国将在全国范围内实施车用柴油国IV排放标准(S<50 ppm),超深度加氢脱硫技术备受关注. 工业上多采用氧化铝负载的CoMo和NiMo硫化物为催化剂,过渡金属磷化物、氮化物是目前研究较多的一类高活性加氢精制催化剂[1-2]. 研究工作通常选用模拟油进行实验,即将典型的含硫或含氮化合物溶解在纯溶剂或混合溶剂中,例如十氢萘、十二烷和十六烷等惰性溶剂[3],加氢催化剂的活性与溶剂有关[4-5]. 此外,在众多储氢技术中,将氢气以氢化物形式储存在液体烃类化合物中被认为是一项潜在可行的方案[6]. 而在筛选及评价潜在的有机液体储氢化合物时,氢气的溶解度也是一重要参数. 因此,测定和模拟计算氢气在这些烃类溶剂中的溶解度具有重要的意义.刘晨光等[7]在温度22~250 ℃和压力2~12 MPa 条件下,测定了氢气在甲苯、正庚烷、汽柴油等馏分的溶解度. 罗化峰等[8]分别测定了氢气在混合组分十六烷-四氢萘、四氢萘-喹啉和十六烷-喹啉中的溶解度,并且利用数学模型和P/N/A两种方法计算氢气的溶解度,结果表明数学模型在计算氢气在有机混合溶剂中的溶解度方面具有很好的应用价值. Korsten和Hoffman等[9]根据修正的亨利定律(经验公式),计算氢气和硫化氢在溶剂中的溶解度. 王世丽等[10]运用ChemCAD闪蒸分离模块建立模拟流程,模拟计算氢气在间二甲苯、甲苯、环己烷等溶剂中的溶解度.本研究利用Aspen Plus软件建立模拟流程,进行氢气在烃类中溶解度模拟实验.在模拟过程中,选用SRK、 PENG-ROB、 PSRK、 PR-BM和RK-ASPEN 5个物性方程和经验公式计算氢气在十六烷-四氢萘混合溶剂中的溶解度,对比模拟值、计算值和实验值,探索物性方程的使用范围. 因缺少氢气在十氢萘、四氢萘、十二烷和十六烷中溶解度的实验值,所以选择合适的物性方程和经验公式计算氢气在烃类中的溶解度,为溶剂效应的研究提供理论基础.利用Aspen Plus V8.6建立模拟流程,采用分离过程单元操作,以传质分离单元闪蒸分离器为主要操作单元进行单级气液平衡分离过程计算. 模拟流程建立步骤:点击flash2#、进料流股、产物流股等图标,建立闪蒸流程图;在Properties模块中,选择工程单位、组分、物性方程;在Simulation模块中,定义流股,输入设备参数,运行模拟流程. 流程如图 1 所示.Korsten和Hoffman提出的氢气在溶剂中溶解度计算的经验公式见式(1)、式(4)~式(7)[9]. 式(1)中,H为亨利系数,MPa/(mol·m-3);λ为氢气溶解度系数,(NL H2)/[(kg oil)·(MPa)]; vN为标况下的摩尔体积,22.4 L/mol;ρL为液体的密度,kg/m3. 式(2)和式(3)中[11],E为亨利系数,kPa; Co为溶液的总浓度,kmol/m3;ρS为溶剂密度,kg/m3;MS为溶剂摩尔质量,kg/kmol. 式(4)中,T为温度,℃;ρ20 为溶剂在20 ℃的密度,g/cm3. 式(5)中,ρ0为溶剂在15.6 ℃,压力为 101.3 kPa 的密度,lb/ft3. 式(6)中,ΔρP为压力引起的密度变化,lb/ft3; P为压力,pisa. 式(7)中,ΔPT为温度引起的密度变化,lb/ft3; T为温度,°Ra.[T-520]-[8.1×10-6-0.062 2×10-0.764(ρ0+ΔρP)]·[T-520]2.2.1 模拟值和计算值在流程模拟过程中,不同的软件选用相同的物性方程,模拟计算结果有可能也不一致. 本文采用Aspen Plus V8.6,选取SRK、 PENG-ROB、 PSRK、 PR-BM和RK-ASPEN,并采用经验式(1)~式(7) 计算氢气在间二甲苯溶剂中的溶解度. Aspen Plus V8.6软件中的操作条件如下:以氢气、间二甲苯为主要组分,进料温度为393 K,压力为8 MPa,间二甲苯进料流率为500 kg/h,氢气进料流率为0.5 kg/h;闪蒸分离器操作条件为:温度353 K,压力0.989~4.718 MPa. 将计算出的结果与王世丽运用ChemCAD软件计算结果对比,见表 1. 从表1可看出,压力在0.989~1.968 MPa,Aspen Plus中SRK物性方程比Chem CAD中SRK 方程更接近实际值;压力在2.968~4.718 MPa,Aspen Plus中PENG-ROB物性方程比Chem CAD中PENG-ROB方程更接近测量值[10,12]. PSRK 和RK-ASPEN热力学方程也可用于计算低压下氢气在间二甲苯中的溶解度,但PR-BM方程不适于计算氢气在间二甲苯中的溶解度. 采用经验公式的计算值低于测量值,并且只有在高压4.718 MPa时,与测量值吻合.SRK状态方程适合于低压下正规溶液(烃类所形成的溶液可看作正规溶液) 的模拟计算,而在中高压下,该方法的模拟结果与PENG-ROB相比,偏离较大. 因此,Aspen Plus中SRK和PENG-ROB更适合研究氢气在烃类中溶解度的模拟计算,即选择合适的物性方程,运用Aspen Plus闪蒸分离模块可准确计算氢气在烃类中溶解度. 采用经验公式计算氢气在烃类溶液中的溶解度,不需要考虑氢气和间二甲苯的流率比例. 但进料流股中组分分流率比例选择不合适,软件不能进行闪蒸平衡计算[10],因此经验公式可弥补软件的不足.2.2 氢气在十六烷-四氢萘混合溶剂中的溶解度选取Aspen Plus V8.6中的SRK、 PENG-ROB、 PSRK、 PR-BM和RK-ASPEN 5个物性方程和经验公式,计算氢气在十六烷-四氢萘混合溶剂中的溶解度,模拟和计算结果见表 2. Aspen Plus V8.6操作条件如下:以氢气、十六烷-四氢萘混合溶剂为主要组分,进料温度为623.15 K,压力为11 MPa,混合溶剂的进料流率为500 kg/h,氢气进料流率为1.5 kg/h;闪蒸分离器操作条件为表2中的温度和压力. 从表 2 可看出,SRK和RK-ASPEN方程的模拟值接近,PSRK和PENG-ROB方程的模拟值接近. 在相同温度和压力下,模拟值比计算值更接近测量值. 因此,运用Aspen Plus计算氢气在烃类中的溶解度在一定的条件下是可行的.四氢萘的质量分数为0.226%和0.369%时,在453.15 K,2~10 MPa时,PR-BM方程适于计算氢气的溶解度;在543.15 K,2~10 MPa时,SRK和RK-ASPEN方程适于计算氢气的溶解度,大于10 MPa时,PENG-ROB方程适于计算氢气的溶解度;在623.15 K,3~10 MPa时,PSRK和PENG-ROB方程适于计算氢气的溶解度. 当四氢萘的质量分数为0.539%时,在453.15 K,2~6 MPa 时,PR-BM方程适于计算氢气的溶解度,8~10 MPa时,SRK和RK-ASPEN方程适于计算氢气的溶解度;在543.15 K,4~8 MPa,SRK和RK-ASPEN方程适于计算氢气的溶解度,大于10 MPa时,PENG-ROB方程适于计算氢气的溶解度;在623.15 K,3~5 MPa,SRK和RK-ASPEN方程适于计算氢气的溶解度,7~9 MPa时,PSRK和PENG-ROB方程适于计算氢气的溶解度. 温度在543.15~623.15 K,压力小于 2 MPa,没有合适的物性方程计算氢气的溶解度.2.3 氢气在烃类中的溶解度的计算以十氢萘为环烷烃、十二烷和十六烷为直链烷烃,运用Aspen Plus V8.6和经验公式进行氢气在环烷烃和直链烷烃中溶解度计算. 基于上述结论,以四氢萘和十氢萘为溶剂,在543.15 K,3~8 MPa,选用SRK方程,8~10 MPa,选用PENG-ROB;在623.15 K,3~5 MPa,选用SRK方程,5~10 MPa,选用PENG-ROB方程. 以十二烷和十六烷为溶剂,在543.15 K,2~9 MPa,选用SRK方程,大于 10 MPa,选用PENG-ROB方程;在623.15 K,3~10 MPa,选用PENG-ROB方程. 模拟值和计算值见表3,在相同的温度和压力下,氢气在环烷烃的溶解度模拟值小于在直链烷烃的模拟值. 这一结论也符合刘晨光实验测定的结论,即在相同的温度和压力下,氢气在芳烃中的溶解度小于在直链烷烃中的溶解度[7]. 采用经验公式得出的计算值和运用Aspen Plus运行出的模拟值,两者的数量级相同.若氢气的溶解度不是控制加氢精制反应的主要因素,可采用经验公式计算氢气的溶解度;若氢气的溶解度是主要因素,可运用Aspen Plus软件模拟计算氢气的溶解度.SRK、 PENG-ROB、 PSRK、 PR-BM和RK-ASPEN 5个物性方程都有其使用范围. SRK和RK-ASPEN方程的模拟值接近,PSRK和PENG-ROB方程的模拟值接近. 采用经验公式计算的氢气溶解度小于测量值,但数量级相同. 运用Aspen Plus 闪蒸分离模块建立模拟流程,选择合适的物性方程,进行氢气在十六烷-四氢萘混合溶剂中溶解度的模拟计算,模拟值与测量值接近一致. 氢气在不同溶剂中溶解度的差异,可用于讨论加氢脱硫、加氢脱氮及加氢脱氧等反应过程的溶剂效应,也有助于有机液体储氢载体的选择.【相关文献】[1]Zhao H, Oyama S T, Freund H J, et al. Nature of active sites in Ni2P hydrotreating catalysts as probed by iron substitution[J]. Applied Catalysis B: Environmental, 2015,164(1):204-216.[2]李贵贤,曹彦伟,李梦晨,等. 煤焦油加氢脱氮反应网络及催化剂研究进展[J]. 化工进展,2015,34(5):1283-1290. Li Guixian, Cao Yanwei, Li Mengchen, et al. Research progress in deep hydrodenitrogenation reaction network and its catalysts for coal-tar[J]. Chemical Industry and Engineering Progress, 2015, 34(5):1283-1290. (in Chinese)[3]Chávez L M, Alonso F, Ancheyta J. Vapor-liquid equilibrium of hydrogen-hydrocarbon systems and its effects on hydroprocessing reactors[J]. Fuel, 2014, 138(138):156-175. [4]孙志超. 金属磷化物催化剂制备、改性及其加氢脱硫(氮)反应性能[D]. 大连:大连理工大学,2014.[5]董婷. Ni2P/SiO2催化剂上愈创木酚的加氢脱氧研究[D]. 大连:大连理工大学,2014.[6]Aslam R, Müller K, Müller M, et al. Measurement of hydrogen solubility in potential liquid organic hydrogen carriers[J]. Journal of Chemical & Engineering Data, 2016, 61:643-649.[7]刘晨光,阙国和. 氢气在石油馏分中溶解度的测定[J]. 炼油设计,1999,29(5):33-36. Liu Chenguang, Que Guohe. Determination of hydrogen solubilities in petroleum fractions[J]. Petroleum Refinery Engineering, 1999, 29(5):33-36. (in Chinese)[8]罗化峰,郭剑虹,凌开成,等. 氢气在烃类混合溶剂中高压溶解度的测定[J]. 煤炭转化,2011,34(2):55-58. Luo Huafeng, Guo Jianhong, Ling Kaicheng, et al. Determination on the solubility of hydrogen in hydrocarbon mixtures at high pressures[J]. Coal Conversion, 2011, 34(2):55-58. (in Chinese)[9]Korsten H, Hoffmann U. Three-phase reactor model for hydrotreating in pilot trickle-bed reactors[J]. AIChE Journal, 1996, 42(5):1350-1360.[10]王世丽,刘永刚,张瑞芹. 运用ChemCAD计算氢气在烃类中的溶解度[J]. 现代化工,2013,33(5):114-118. Wang Shili, Liu Yonggang, Zhang Ruiqin. Calculation of hydrogen solubility in hydrocarbons by ChemCAD[J]. Modern Chemical Industry, 2013, 33(5):114-118. (in Chinese)[11]谭天恩,窦梅. 化工原理(下)[M]. 北京:化学工业出版社,2013.[12]赵亮富,赵玉龙,吕朝晖,等. 氢气和一氧化碳在混二甲苯中的溶解度[J]. 化学反应工程与工艺,2000,16(4):396-400. Zhao Liangfu, Zhao Yulong, Lv Chaohui, et al. Solubility of H2 and CO in mixed xylene[J]. Chemical Reaction Engineering and Technology, 2000, 16(4):396-400. (in Chinese)。
钢焊接接头中氢的溶入与扩散行为研究进展

2 . L u o y a n g S h i p Ma t e r i a l R e s e a r c h I n s t i t u t e , L u o y a n g 4 7 1 0 2 3 , C h i n a )
A b s t r a c t : I n t h i s p a p e r , t h e r e s e a r c h p r o g r e s s e s o f h y d r o g e n a b s o r p t i o n a n d h y d r o g e n d i f f u s i o n i n s t e e l w e l d e d j o i n t s a r e s u mm a —
过程 中氢 溶 入行 为 的相 关 研 究 , 图 1所 示 为 S h e a实验 测 得光 谱 中氢 的相 对 强 度 与 电弧 气 氛
等人研究揭示 氢Biblioteka 导致焊 接 冷裂纹 产生 的主要原
因 以来 , 学 者们 对 钢 焊 接 中 的氢 开展 了大 量 的研 究 工作 , 逐 步明确 了焊接 中氢 的来 源 、 焊 接接 头 中
o f s t e e l s a r e me a s u r e d. The i nf lu e n c i n g f a c t o r s o f hy d r o g e n d i f f us i o n a nd e f f us i o n t o g e t he r wi t h c ha r a c t e r s o f hy d r o g e n d i s t r i b u t i on a r e pr e l i mi n a r y l y s t u d i e d.
氢氧化镍的溶解度-解释说明

氢氧化镍的溶解度-概述说明以及解释1.引言1.1 概述氢氧化镍是一种重要的化学物质,具有广泛的应用价值。
其溶解度是指在特定条件下溶于溶剂中的量,对于氢氧化镍的生产和应用具有重要意义。
本文旨在探讨氢氧化镍的溶解度及其影响因素,以及其在工业生产和科学研究中的应用。
通过对氢氧化镍溶解度的研究,可以更好地理解其性质,为相关领域的技术和产品提供重要的理论基础和实践指导。
1.2 文章结构文章结构部分:本文分为引言、正文和结论三个部分。
在引言部分,将对氢氧化镍的溶解度进行概述,介绍文章的结构和目的。
在正文部分,将详细讨论氢氧化镍的性质、溶解度的影响因素和氢氧化镍的应用。
最后在结论部分,对文章进行总结,展望氢氧化镍溶解度的未来研究方向,并得出结论。
1.3 目的本文的目的是探讨氢氧化镍在溶液中的溶解度,并分析影响氢氧化镍溶解度的因素。
通过对氢氧化镍溶解度的研究,探讨其在工业生产和化学实验中的应用,并对未来可能的技术发展进行展望。
最终旨在为相关领域的科研工作者、工程技术人员和学生提供参考,为氢氧化镍的应用和产业发展做出贡献。
2.正文2.1 氢氧化镍的性质氢氧化镍,化学式为Ni(OH)2,是一种无机化合物,常见的形式是绿色固体。
其具体性质包括:1. 物理性质:氢氧化镍是一种绿色粉末状固体,在常温下不溶于水。
它具有一定的吸湿性,可以在空气中逐渐吸收水分变成氢氧化镍的水合物。
2. 化学性质:氢氧化镍在高温下会发生分解,放出氧气。
它可以被强酸或强碱溶解,生成相应的镍盐。
3. 结构性质:氢氧化镍的晶体结构是层状结构,每一层由Ni(OH)6八面体和NiO6八面体交替排列而成。
在晶体中,氢氧化镍的层状结构能够相互堆叠形成结晶体。
总的来说,氢氧化镍具有一定的稳定性和化学活性,其特有的物理和化学性质使其在许多领域具有重要的应用价值。
2.2 溶解度的影响因素氢氧化镍的溶解度受多种因素影响,包括温度、溶剂、压力和pH值等。
首先,温度是影响氢氧化镍溶解度的重要因素之一。
镁熔液中氢气泡析出动力学模型

镁熔液中氢气泡析出动力学模型许四祥;侍海东;张炳刚;徐起兵【摘要】针对镁熔液中氢气泡的析出过程,分析氢气泡析出的动力学特性.考虑多种因素对氢气泡析出影响,对镁熔液中氢气泡上浮运动进行受力分析,利用牛顿第二定律得出氢气泡上浮运动过程中的瞬时加速度方程,并结合气体状态方程、传质边界层方程及流函数等相关性质,推导出镁熔液中氢气泡在析出过程中气泡速度、气泡半径、气泡上浮高度与时间变化关系的动力学模型.采用龙格库塔算法将模型方程在MATLAB中进行编程计算,得到气泡传质速率与时间及气泡半径与时间的关系曲线.研究结果表明:氢气泡形核后析出,随着上浮高度的增加,气泡速度与半径都随之变大,加速度先增大后减小;临近界面处,气泡趋于某一速度值析出并破裂.此模型为镁熔液中氢气泡的形成机理提供了一定的理论基础,对镁合金液态质量控制具有重要意义.【期刊名称】《中南大学学报(自然科学版)》【年(卷),期】2015(046)012【总页数】5页(P4448-4452)【关键词】镁;氢;动力学模型;MATLAB【作者】许四祥;侍海东;张炳刚;徐起兵【作者单位】安徽工业大学机械工程学院,安徽马鞍山,243002;安徽工业大学机械工程学院,安徽马鞍山,243002;安徽工业大学机械工程学院,安徽马鞍山,243002;安徽工业大学机械工程学院,安徽马鞍山,243002【正文语种】中文【中图分类】TG243+.1镁熔液中氢含量已成为影响镁制品综合性能的关键因素之一[1],尤其在铸造镁合金液态质量检测过程中,氢含量直接决定零件成型后质量[2−3],由于镁合金熔炼时吸氢,导致在铸件中出现显微气孔,严重影响其力学性能。
近年来国内外对镁熔液中氢的研究越来越多,张伟华等[4−5]研究了镁等金属熔体中氢气泡的形核机理并通过Gasar工艺法得到了氢在镁等常用纯金属中的溶解度计算公式;许四祥等[6]也对镁及其合金熔液中氢含量进行了研究,得出了纯镁熔液及镁合金熔液中氢含量的数学模型。
氢在铁中的溶解度
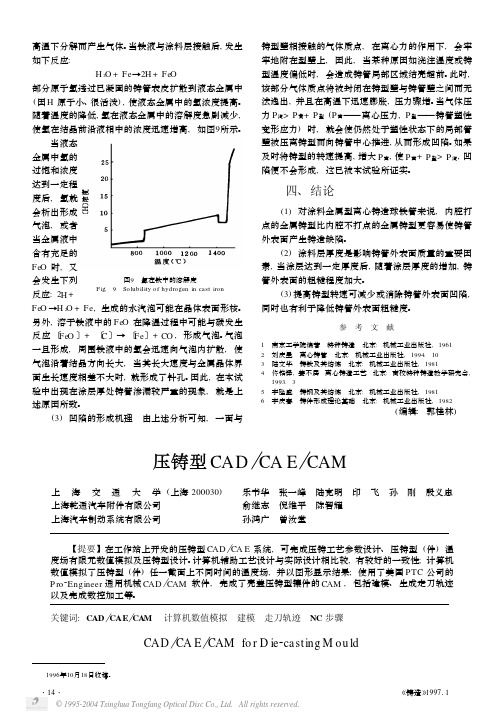
图9 氢在铁中的溶解度F ig .9 So lubility of hydrogen in cast iron高温下分解而产生气体。
当铁液与涂料层接触后,发生如下反应:H 2O +Fe →2H +FeO部分原子氢透过已凝固的铸管表皮扩散到液态金属中(因H 原子小、很活泼),使液态金属中的氢浓度提高。
随着温度的降低,氢在液态金属中的溶解度急剧减少,使氢在结晶前沿液相中的浓度迅速增高,如图9所示。
当液态金属中氢的过饱和浓度达到一定程度后,氢就会析出形成气泡,或者当金属液中含有充足的FeO 时,又会发生下列反应:2H +FeO →H 2O +Fe ,生成的水汽泡可能在晶体表面形核。
另外,溶于铁液中的FeO 在降温过程中可能与碳发生反应〔FeO 〕+〔C 〕→〔Fe 〕+CO ,形成气泡。
气泡一旦形成,周围铁液中的氢会迅速向气泡内扩散,使气泡沿着结晶方向长大,当其长大速度与金属晶体界面生长速度相差不大时,就形成了针孔。
因此,在本试验中出现在涂层厚处铸管渗漏较严重的现象,就是上述原因所致。
(3)凹陷的形成机理 由上述分析可知,一面与铸型壁相接触的气体质点,在离心力的作用下,会牢牢地附在型壁上,因此,当某种原因如浇注温度或铸型温度偏低时,会造成铸管局部区域结壳超前。
此时,该部分气体质点将被封闭在铸型壁与铸管壁之间而无法逸出,并且在高温下迅速膨胀,压力骤增。
当气体压力P 汽>P 高+P 型(P 离——离心压力,P 型——铸管塑性变形应力)时,就会使仍然处于塑性状态下的局部管壁被压离铸型而向铸管中心推进,从而形成凹陷。
如果及时将铸型的转速提高,增大P 离,使P 离+P 型>P 汽,凹陷便不会形成,这已被本试验所证实。
四、结论(1)对涂料金属型离心铸造球铁管来说,内腔打点的金属铸型比内腔不打点的金属铸型更容易使铸管外表面产生铸造缺陷。
(2)涂料层厚度是影响铸管外表面质量的重要因素,当涂层达到一定厚度后,随着涂层厚度的增加,铸管外表面的粗糙程度加大。
高中化学第一章化学反应与能量检测选修4

第一章化学反应与能量检测(时间:90分钟满分:100分)一、选择题(本题包括18个小题,每小题3分,共54分)1中国锅炉燃煤采用沸腾炉逐渐增多,采用沸腾炉的好处在于()匸①增大煤炭燃烧时的燃烧热并形成清洁能源②减少炉中杂质气体(如SQ等)的形成③提高煤炭的热效率并减少CQ的排放④使得燃料燃烧充分,从而提高燃料的利用率B. ①③④ A.①②D.③④ C.②③答案:D2下列反应中,放出热量的是()匸①NaQH溶液中加入盐酸②由乙醇制③铝热反应④由氯酸钾制QD.①④ C.①③ B.②③ A.①②答案:C3下列有关光合作用的说法错误的是()匸A. 将无机物转化为有机物B. 反应物的总能量高于生成物的总能量C. 将太阳能转变为化学能D•是自然界碳元素循环的重要途径答案:B4下列说法中正确的是()1A. 在化学反应中,发生物质变化的同时不一定发生能量变化B. △ H>0表示放热反应,△ H<0表示吸热反应C. △ H的大小与热化学方程式中的各物质的化学计量数无关D. 反应产物的总焓大于反应物的总焓时,△ H>0答案:D5根据以下三个热化学方程式:2H2S(g)+3Q2(g) 2SQ(g)+2H 20(1) △ H=-Q匕1kJ • mol - ;2H 2S(g)+0 2(g)----- 2S(s)+2H 20(1) △ H=- Q1 _ -1-答案:AkJ • mol ;2H2S(g)+O2(g) ------- 2S(s)+2H 2O(g) △ H=-Q kJ • mol。
判断Q、Q、Q三者关系正确的是()B. Q>Q3>Q2 A. Q>Q>QD. Q>Q>Q C. Q>Q>Q6在一定条件下,C0和CH4燃烧的热化学方程式分别为:匸2C0(g)+Q(g)——2CQ(g) △ H=- 566 kJ • mol-1CH4(g)+2O2(g)——CQ(g)+2H 20(1)△ H=- 890 kJ • mol-1由1 mol CO和3 mol CH 4组成的混合气体在上述条件下完全燃烧时,释放的热量为()D.3 867 kJ C.3 236 kJ B.2 953 kJ A.2 912 kJ解析:1 mol CO完全燃烧放出的热量是L kJ,3 mol CH完全燃烧放出的热量是890 kJ X 3,566释放的总热量应当是(t +890X 3) kJ=2 953 kJ 。
金属体系中氢进入及破坏过程的电化学方法研究_柯克

[ 4 ]
, 若有边缘 反应 以非 扩散 穿透方 式进 行的 情
, 一般情况是界面和扩散混合
况 , 氢最大浓度不在阴极表面 , 而在表面以下一定距 离处 , 该处的渗透质子或氢原子达到静止状态 , 与离 子嵌入材料的情形相似[ 4] . 但边缘反应的实验验证 工作均末进行过 . 要证实边缘反应这个构想 , 中子散 射
[ 1] [ 1, 2 ] 情况) 或有效扩散率( 有陷阱时) . 类似于用气
R T) , E b 是陷阱结合能) . 陷阱结合能是描述陷阱的 有效性的一个重要参数 , 特别从氢脆的角度来看时 , 但要获得 Eb 必须精确测量暂态过程 . 高结合能陷阱 ( 如沉积物/ 基体界面) 常导致 氢脆 , 但 在较弱陷阱 ( 如位错) 也存在时不会导致氢脆[ 3] . 在渗氢试验测量中主要要求是真正保持了扩散 条件 . 这对获得氢的晶格扩散率测量很重要 . 可以通 过检查 tL 是否与 L 成正比加以证明 . 若 tL 与 L 不成正比 , 则渗透过程不是处于扩散单一控制 , 而是 ( 界面 +扩散) 混合控制或者界面控制 . 另一个好的 检验扩散条件的方法可在稳态条件下进行 , 下面将 作叙述 .
[ 4]
2 Devanathan Stachurski 电池
2氢气性质与制造(修改完)

第二章氢气性质与用途氢是元素周期表中第一种元素,也是最轻的元素,原子量为1.0079,它是组成水、石油、煤炭及有生命体等的一个主要元素,由两个氢原子结合在一起成为氢分子,即氢的单质。
氢是自然界中较为丰富的物质,也是应用最广泛的物质之一。
氢是太阳大气的主要组成部分,以原子百分数计,它占81.75%,它是太阳发生热核反应的主要原料,是人们赖以生存的最大能量来源。
氢在地球的地壳外层的三界(大气、水和岩石)里,以原子百分数计占17%,以质量百分数计只约占1%。
虽然存在量少,但分布很广。
氢主要以化合状态存在于各种化合物,如水、有机物和生物体中,仅在天然气和煤矿气中有少量单质氢存在。
氢气是重要的工业原料,在化学工业、半导体工业及冶金工业等中均占有重要的地位,特别是在化学工业中以氢为原料可生产许多重要的化工产品,如合成氨、甲醇、精炼各种石油产品及合成多种有机化学产品。
氢也可作为燃料,是城市煤气及工业燃料的重要组成部分。
大部分氢气是生产后就地消耗使用,如石油工业的制氢装置就是为精制各种石油产品和合成各种有机化学品提供原料。
2.1氢气的性质2.1.1氢气的物理性质元素氢有三种同位素:氕(符号H)、氘(符号D)和氚(符号T)。
它们的原子的原子核内虽都只含有1个质子,但同时分别含有0、1和2个中子,三者因此在质量上差别很大,超过了其它任何元素的同位素之间的质量差别,导致它们的单质(如H2、D2)在物理性质(如相变热、蒸汽压等)方面差别比较显著。
由于自然界中普通氢内含有99.9844%氕和0.0156%氘(以原子数计),所以普通氢基本上显示同位素氕的性质。
氚是一种不稳定的放射性同位素。
氢气是一种无色无味的气体,在所有气体中,其密度最小,只有0.08987g/l。
氢气有最快的扩散速度。
采用致冷剂将氢气进行冷冻或高压氢气通过绝热膨胀,将温度降至其临界温度以下,压力高于临界压力,均可将氢气液化,液态氢在减压下蒸发可形成固态氢。
钢中氢的来源及控制对策

钢中氢的来源及控制对策
2.试验条件 2.试验条件
2.1 试验工艺及主要设备参数 80tLD-CB(冶炼周期31min)→80tLF(冶炼周期35—55min)→240×1400mm断面弧形 板坯铸机(中包容量15t,浇注周期35min)。 2.2 试验方案 为了检测钢液中真实的氢含量,采用浸入式直读测氢仪(Multi—LabHydris System) 对“转炉炼钢+LF炉+连铸”各工位钢液在线测氢及对原辅料进行详细的水分分析,详 细的测试方案见表1。
5.1 措施 [H]在钢液中的溶解遵循sivert定律(式1),在温度为1600℃,氢分压 为 1atm 条 件 下 可 算 出 [H] 的 溶 解 度 为 0.00268% ( 即 27ppm ) 。 由 此 在 1600℃条件下,式(1)可改写为式(2),[H]在钢液中的溶解随氢分压 的增加而增加[1]。 1670 − −1.68 (1) (2) [ H %] = 0.00268 PH T [ H %] = 10 PH
表1 钢液测氢试验方案 1
名称 转炉速补料 转炉用辅料及合金 出钢结束 LF用辅料及合金 LF精炼过程 连铸中间罐、结晶器覆盖剂 中间罐 N2、O2、Ar气体 检测内容 水分含量、用量、补炉后烘烤时间 水分含量及用量、加入时机 钢液测氢 水分含量及用量 钢液测氢 水分含量及用量 钢液测氢 水分含量
钢中氢的来源及控制对策
5.1.2 加强耐材烘烤 要求转炉补炉后烘烤时间不小于2h,加强钢包及中间罐的烘烤效果,防 止耐材干燥不彻底导致钢水增[H]。 5.1.3 提高转炉吹炼操作水平 通过优化枪位控制及加料时机,促进转炉渣的早化、化透。提高转炉的 脱磷率,减少冶炼过程化渣剂的消耗量。并严格控制后吹过程中辅料的 加入量,严禁在此期间配加镁球。
铝合金铸件中夹杂和氢含量关系

铝合金铸件中夹杂和氢含量关系随着汽车工业的发展铝合金铸件的使用越来越多,对铸件的要求也越来越高。
除要求保证化学成分、力学性能和尺寸精度外,铝合金铸件还不允许有缩孔、缩松、气孔、渣孔等铸造缺陷。
铝液净化处理是保证高质量铝合金产品的措施之一,也是提高铝合金综合质量的主要手段。
铝液的精炼效果对气孔、缩孔、夹杂的形成有重要的影响,且直接影响铝合金铸件的物理性能、力学性能。
没有高质量的铝液,即使后续处理再先进,缺陷一旦产生它就始终存在产品之中,高质量的铸件就难以获得。
因此必须重视铝液中的气体和夹杂物,并采取措施来清除铝液中的气体和夹杂物。
1、铝液中的气体和夹杂物铝液中的气体主要是氢气(约占80%~90%),其次是氮气、氧气、一氧化碳等。
氢几乎不溶于固态铝,而在液态溶解度很大。
氢在固相线上下的溶解度为每100g 铝液的氢含量是0.65mL和0.034mL(氢在0.1MPa的条件下),即氢在固液两相的溶解度相差19.1倍,而每100g熔融铝中正常的氢含量为0.1~0.4mL。
由于溶解度的不同氢就倾向于从熔体中逸出,当氢气压力大于表面张力和液体静压力时就形成气泡,进而在铸件中产生针孔。
因此,在铝合金熔体净化方面,主要存在的问题是铝合金的含氢量较高,而现有手段不能满足高质量铝合金铸件的生产要求。
通常每100g铝的含氢量在0.1~0.2mL时基本能满足生产要求,对特殊要求的铸件(像航空铸件)每100g铝的含氢量要在0.06mL以下。
夹杂是指在液相线以上的任何固体及液体以外的物质。
铝液中常见的非金属杂质有氧化物、氮化物、碳化物、硼化物等,大都以颗粒状存在,典型的颗粒尺寸在1~30μm范围内。
除来自炉料外,主要是熔化过程中化学反应的产物。
铝表面的氧化膜厚度在2~10μm,接近熔点时增至200μm,液面上的氧化膜不仅更厚,而且结构发生了变化;面向铝液一侧是致密的对铝液有保护作用,而铝液外侧是疏松的,内有直径5~10μm的小孔并被氢、空气、水汽充满,如果将液膜搅入铝液就会增杂、增气。
氢在钢中的溶解度

氢在钢中的溶解度【原创实用版】目录1.氢在钢中的溶解度概述2.氢在钢中的溶解度影响因素3.氢在钢中的溶解度对钢性能的影响4.控制氢在钢中的溶解度的方法正文1.氢在钢中的溶解度概述氢在钢中的溶解度是指在特定温度和压力条件下,钢中可以溶解的氢的最大量。
氢在钢中的溶解度是一个重要的参数,因为它直接影响到钢的性能和质量。
2.氢在钢中的溶解度影响因素氢在钢中的溶解度受多种因素影响,主要包括以下几个方面:(1) 温度:氢在钢中的溶解度随温度的升高而增加。
在高温下,钢中的氢溶解度较大,而在低温下,氢的溶解度较小。
(2) 压力:氢在钢中的溶解度随着压力的增加而减小。
在高压下,钢中的氢溶解度较小,而在低压下,氢的溶解度较大。
(3) 钢的化学成分:钢中的化学成分对氢的溶解度也有影响。
例如,钢中的碳、氮、硫等元素会降低氢的溶解度,而合金元素如铬、镍、钼等则会提高氢的溶解度。
3.氢在钢中的溶解度对钢性能的影响氢在钢中的溶解度对钢的性能和质量具有重要影响。
当钢中的氢溶解度较高时,会导致以下问题:(1) 氢致脆性:氢在钢中溶解度高时,会导致钢的韧性降低,脆性增加,容易发生断裂。
(2) 氢致孔隙:氢在钢中溶解度高时,会在钢的晶粒内部形成气孔,导致钢的性能下降。
(3) 氢致变形:氢在钢中溶解度高时,会导致钢的晶粒发生变形,从而影响钢的性能和尺寸稳定性。
4.控制氢在钢中的溶解度的方法为了保证钢的性能和质量,需要控制氢在钢中的溶解度。
主要方法包括:(1) 冶炼过程中控制氢的生成:通过优化冶炼工艺,降低氢的生成量,从而降低氢在钢中的溶解度。
(2) 控制钢的化学成分:通过调整钢的化学成分,使其不利于氢的溶解,从而降低氢在钢中的溶解度。
(3) 控制钢的加工工艺:通过优化钢的加工工艺,如控制轧制温度、轧制速度等,降低氢在钢中的溶解度。
综上所述,氢在钢中的溶解度对钢的性能和质量具有重要影响。
氢在钢中的溶解度

氢在钢中的溶解度概述氢在钢中的溶解度是指氢气在钢材中的溶解程度。
在某些情况下,钢材中的氢气可以对钢材的性能和可靠性产生负面影响。
了解氢在钢中的溶解度对于理解氢脆性、氢腐蚀以及氢诱发的应力开裂等问题非常重要。
氢在钢中的溶解氢气可以通过吸附、溶解和扩散等方式存在于钢材中。
其中,氢在钢中的溶解是最主要的方式。
钢材中的氢气可以溶解在钢的晶格中,形成固溶体。
氢在钢中的溶解度取决于多种因素,包括温度、压力、合金成分以及钢的微观结构等。
影响因素温度温度是影响氢在钢中溶解度的重要因素。
一般来说,随着温度的升高,氢在钢中的溶解度会增加。
这是因为高温会增加氢气的动能,使其更容易克服钢材表面的吸附力,进而溶解到钢的晶格中。
压力压力也会对氢在钢中的溶解度产生影响。
高压可以增加氢气与钢材之间的接触面积,有利于氢气的吸附和溶解。
因此,较高的压力通常会导致较高的氢溶解度。
合金成分钢材的合金成分对氢在钢中的溶解度起着重要作用。
一些合金元素,如镍、铬和钼等,可以促进氢在钢中的溶解,从而提高氢溶解度。
这是因为这些合金元素与氢之间会发生化学反应,形成稳定的化合物,有利于氢的溶解。
微观结构钢材的微观结构也对氢在钢中的溶解度产生影响。
一般来说,细小的晶粒和高密度的晶界对氢的扩散具有较高的阻碍作用,从而降低氢在钢中的溶解度。
此外,钢材中的缺陷和孔隙也会影响氢的溶解度。
氢在钢中的行为氢在钢中的存在可以导致多种问题,如氢脆性、氢腐蚀以及氢诱发的应力开裂等。
氢脆性氢脆性是指钢材在存在氢气的条件下变得易于断裂的性质。
氢脆性是由于氢在钢中的存在导致钢材的塑性降低所致。
氢会聚集在钢材中的缺陷和应力集中区域,导致局部应力集中,从而引发断裂。
氢腐蚀氢腐蚀是指钢材在存在氢气的条件下发生腐蚀的现象。
氢可以与钢材中的金属元素发生化学反应,形成氢化物,导致钢材的腐蚀。
氢腐蚀对钢材的性能和可靠性产生负面影响,降低了钢材的寿命。
氢诱发的应力开裂氢诱发的应力开裂是指钢材在受到应力的作用下,由于氢的存在而引发的裂纹扩展。
焊缝金属扩散氢测定

便在焊缝中产生氢气孔。
精品PPT
LNPU
碳钢或低合金钢焊缝,若含氢量高,则常常在其拉伸 或弯曲断面上出现银白色圆形局部脆断点,即所谓 的白点 (2)氢使焊缝在室温附近塑性严重下降,称为氢脆
精品PPT
LNPU
焊接材料的选择对扩散氢含量的影响 图1 为不同类型的焊条在相同焊接条件下焊 后熔敷金属的扩散氢含量
精品PPT
LNPU
精品PPT
LNPU 降低焊缝扩散氢含量, 对焊接材料采取措施:
①在药皮的组元中尽可能少加或不加含结晶 水、化合水多的物质; ②在粘结剂—水玻璃 的使用中采取最佳的钾钠搭配,使其防吸湿 效果最好,并加入一定量的海藻胶和氧化镁 以改善压涂性能和增加焊条药皮表面的微 密度,从而降低了药皮的吸湿量; ③在药皮 组元中采用了较强的脱氢物质; ④对焊条进 行适当而充分的高温烘焙。
精品PPT
LNPU
近30 年来,随着铁路运输技术的根本 变化,时速超过200 km、单轴负荷超过30t 的高速及重载列车相继出现,对铁路用钢 (铁轨用钢、车轮用钢等) 提出了更高的要 求,需要钢种具有更高的耐磨损、抗疲劳断 裂等性能
精品PPT
ห้องสมุดไป่ตู้
LNPU 以铁轨用钢为例,重轨是一种高强度的细 珠光体钢,对钢中氢有比较高的敏感性。钢 中氢含量过高可导致轨头部中间位置白点 的产生,白点在轨道中会成为受载荷时的应 力集中区域,沿着白点发展疲劳裂纹从而导 致轨道在低应力条件下断裂,造成事故
测定扩散氢的技术条件 甘油法扩散氢测定的评定标准 测定扩散氢的技术条件GB3965-1995 试
金属中氢的分析技术进展(1)

综述与评论文章编号:1000-7571(2007)03-0037-08金属中氢的分析技术进展王 蓬,王海舟(钢铁研究总院,北京 100081)摘 要:介绍了金属中氢的存在状态及其对材料的影响。
总结了近年来金属中氢的检测方法及目前实验室常用的测氢设备以及分析方法。
除常规取样、实验室检测方法外,由于工艺的要求,在线检测手段发展越来越快。
钢液、铝液中氢的在线测量技术越来越多地应用到实际生产中,并已经研制出可在线同时检测钢液中氧、氮、氢3种气体元素的检测设备。
熔敷金属中氢的检测已经逐渐由热导法替代了传统的水银法和甘油法。
关键词:氢;溶解度;熔融;热抽取;扩散;金属;进展中图分类号:O659 文献标识码:A收稿日期:2006-06-01作者简介:王 蓬(1972-),女,博士,高级工程师,从事气体分析研究,E 2mail :peng 2wang2008@ 。
氢是地表分布最广的元素之一,一般情况下,进入金属中的氢是极为有害的。
金属材料经常发生的氢损伤现象,就是与氢有关的断裂现象。
主要表现为材料的力学性能发生恶化:氢通过软化或硬化机制改变材料的屈服强度,塑性明显降低,诱发裂纹萌生,最后导致断裂、滞后破坏、塑性-脆性转变和低温脆性断裂等等。
近30年来,随着铁路运输技术的根本变化,时速超过200km 、单轴负荷超过30t 的高速及重载列车相继出现,对铁路用钢(铁轨用钢、车轮用钢等)提出了更高的要求,需要钢种具有更高的耐磨损、抗疲劳断裂等性能。
以铁轨用钢为例,重轨是一种高强度的细珠光体钢,对钢中氢有比较高的敏感性。
钢中氢含量过高可导致轨头部中间位置白点的产生,白点在轨道中会成为受载荷时的应力集中区域,沿着白点发展疲劳裂纹从而导致轨道在低应力条件下断裂,造成事故。
因此,分析氢在金属中含量的高低[1]、深入研究和监控冶炼过程中钢水氢含量变化具有重要意义[2-6]。
1 氢在金属中的溶解度及存在状态溶解的氢以独立的形式存在于固体或液体金属中。
多晶硅生产用氢气中金属杂质的测定 电感耦合等离子体质谱法-讨论稿

ICS 77.040H17 T/CNIA 团体标准T/CNIA XXXX-XXXX多晶硅生产用氢气金属杂质的测定电感耦合等离子体质谱法(讨论稿)XXXX-XX-XX发布XXXX-XX-XX实施中国有色金属工业协会发布中国有色金属学会T/CNIA XXXX-XXXX前言本标准按GB/T 1.1-2009给出的规则起草。
本标准由全国有色金属标准化技术委员会(SAC/TC 243)归口。
本标准起草单位:内蒙古通威高纯晶硅有限公司本标准主要起草人:警告——使用本标准的人员应有正规实验室工作的实践经验。
本标准并未指出所有可能的安全问题。
使用者有责任采取适当的安全和健康措施,并保证符合国家有关法规规定的条件。
多晶硅生产用氢气金属杂质的测定电感耦合等离子体质谱法1 范围本标准规定了用电感耦合等离子体质谱仪(ICP-MS)测定多晶硅生产用氢气中钠、镁、铝、钙、铬、锰、铁、镍、铜、锌元素含量的分析方法。
本标准适用于氢气中钠、镁、铝、钙、铬、锰、铁、镍、铜、锌元素含量的测定。
各元素测定范围0.01ng/g~100ng/g。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 3723 工业用化学产品采样安全通则GB/T 4842 氩GB /T 11446.1 电子级水GB /T 25915.1 洁净室及相关受控环境第1部分:空气洁净度等级3 原理气体中金属元素通过洗气瓶中的吸收液进行吸收和富集,吸收液由载气(高纯氩)引入雾化系统进行雾化,以气溶胶形式进入等离子体,在高温和惰性气体中被去溶剂化、汽化解离和电离,转化成带正电的正离子,经离子采集系统进入质谱仪,质谱仪根据质荷比进行分离,根据元素质谱峰强度测定样品中相应元素的含量。
4 试剂和材料4.1 试验用水:符合GB /T 11446.1中EW-Ⅰ级的要求。
