大学化学复习题 答案
《大学化学》复习学习材料、试题与参考答案

《大学化学》习题答案复习学习材料、试题与参考答案一、单选题1.江、河水中含的泥沙悬浮物在出海口附近都会沉淀下来,原因有多种,其中与胶体化学有关的是(B)A.盐析作用B.电解质聚沉作用C.溶胶互沉作用D.破乳作用2.下列各组量子数合理的是(C)A.B.C.D.3.下列各物质的分子间只存在色散力的是(A)A.B.C.D.4.下列物质中不属于毒品的是(B)A.吗啡B.黄曲霉素C.海洛因D.冰毒5.下列物质中,属于致癌物质的是:(B)A.谷酰胺B.苯并芘C.谷氨酸D.谷胱甘肽6.稀溶液依数性中心的核心性质是(D)A.溶液的沸点升高B.溶液的凝固点下降C.溶液是有渗透压D.溶液的蒸气压下降7.盖斯定律适用条件是(B)A.定温或定压B.定压或定容C.定温或定容D.不确定8.下列各种与爱滋病人接触途径中不会感染爱滋病的是(C)A.共用注射器B.性接触C.握手D.母婴传播9.导电性能最好的金属是(A)10.在定温定压条件下,某反应的,这表明该反应(B)A.正向自发进行B.逆向自发进行C.视具体情况而定D.不能确定11.下列哪种现象不属于稀溶液的依数性:(D)A.凝固点降低B.沸点升高C.渗透压D.蒸气压升高12.真实气体行为接近理想气体性质的外部条件是:(B)A.低温高压B.高温低压C.低温低压D.高温高压13下列分子中键角最大的是:(C)A.B.C.D.14.已知氢氧化合反应:,反应,要有利于取得的最大转化率,可采取的措施是(A)A.低温高压B.高温低压C.低温低压D.高温高压15.下列对于功和热叙述中正确的是(A)A.都是途径函数,无确定的变化途径就无确定的数值B.都是途径函数,对应于某一状态有一确定值C.都是状态函数,变化量与途径无关D.都是状态函数,始终态确定,其值也确定16.试指出下列物质中何者不含有氢键(B)A.B.HIC.D.17.在下列溶液中AgCl的溶解度最小的是(B)A.0.1mol/L的NaCl溶液B.0.1mol/L的溶液C.0.1mol/L的溶液D.0.5mol/L的溶液18.下列常用的能源中,属于新能源的是(C)A.石油B.天然气C.氢能D.水能19.下列各物质的化学键中,只存在键的是(C)A.B.C.D.无法确定20.将非挥发性溶质溶于溶剂中形成稀溶液时,将引起(A)A.沸点升高B.熔点升高C.蒸气压升高D.都不对21.以电对与组成原电池,已知,则反应物是(A)A.B.C.D.22.下面的叙述中违背平衡移动原理的是(C)A.升高温度平衡向吸热方向移动B.增加压力平衡向体积缩小的方向移动C.加入惰性气体平衡向总压力减少的方向移动D.降低压力平衡向增加分子数的方向移动23.电镀工艺是将欲镀零件作为电解池的(A)A.阴极B.阳极C.阴阳两极D.无法确定24.已知下列反应的平衡常数:(1)A=B;;(2)B+C=D;;则反应:A+C=D的平衡常数是下列中的(B)A.B.C.D.25.下列各物质中,含有氢键的是(A)A.HFB.NaClC.D.26.在定温定压条件下,某反应的ΔG>0,这表明该反应(A)A正向自发进行B逆向自发进行C视具体情况而定D不能确定27.试指出下列物质中何者不含有氢键(B)A.B(OH)3B.HIC.CH3OHD.H2NCH2CH2NH228.电镀工艺是将欲镀零件作为电解池的(A)A阴极B阳极C阴阳两极D无法确定29.在稀醋酸溶液中,加入等物质量的固态NaAc,在混合溶液中不变的量是A.PhB.电离度C.电离常数D.OH-离子的浓度31.下列各物质结构中,含有叁键的是 (C)A.乙烯B.H2OC.N2D.BF332.一支充满氢气的气球,飞到一定高度即会爆炸,这主要取决于一定高度上的(D)A.外压B.温度C.湿度D.外压和温度二、多选题33.下列各种与爱滋病人接触途径中会感染爱滋病的是 (ABD)A.共用注射器B.性接触C.握手D.母婴传播34.下列对于功和热叙述中错误的是 (BCD)A.都是途径函数,无确定的变化途径就无确定的数值B.都是途径函数,对应于某一状态有一确定值C.都是状态函数,变化量与途径无关D.都是状态函数,始终态确定,其值也确定35.下面的叙述中违背平衡移动原理的是 (ABD)A.升高温度平衡向吸热方向移动B.增加压力平衡向体积缩小的方向移动C.加入惰性气体平衡向总压力减少的方向移动D.降低压力平衡向增加分子数的方向移动三、判断题36.在晶态高聚物中,通常可同时存在晶态和非晶态两种结构。
大学无机化学复习题答案答案

一、填空题1. 完成下列表格化合物BP VP LP 杂化形式 理想电子对构型分子构型 CO 2 4/2=2 2 0 sp 直线 直线CCl 4 (4+4)/2=4 4 0 sp 3 正四面体 正四面体NH 3(5+3)/2=4 3 1 不等性sp 3 正四面体 三角锥(四面体) BCl 3 (3+3)/2=3 3 0 sp 2 正三角形 正三角形 H 2O (6+2)/2=4 2 2 不等性sp 3 正四面体 V (角)形 H 2S (6+2)/2=422 不等性sp3 正四面体 V (角)形 NO 3-(5+1)/2=3 3sp 2正三角形正三角形2. 完成下列表格3.Cr 铬 1s 22s 22p 63s 23p 63d 54s 1 四周期,第6族(VIB) Zn 锌1s 22s 22p 63s 23p 63d 104s 2 四周期,第12族(IIB) Cu 2+ 铜1s 22s 22p 63s 23p 63d 9 四周期,第11族(IB) 3. [Ag(NH 3)2]OH 的中文名称是_氢氧化二氨合银(I ),中心Ag +的配位数是__2__。
三氯化六氨合钴(III )的化学式是 [Co(NH 3)6]Cl 3 。
[Cr(NH 3)5H 2O]Cl 3的中文名称是_三氯化五氨·一水合铬(III ),中心原子的配位数是_6_,配位原子是 N ,O 。
5. 元反应2A(g)+B(g)→2C(g) ,写出该反应的速率方程_v=kc(A)2c(B)_(或v=kp(A)2p(B)_)____,对A 而言反应级数为__2__,总反应级数为___3__,如果缩小反应体系的体积增加体系压力,正反应速率 增加 ,会使平衡向__右__移动,则C 的产量__增加__。
4. 已知反应2Al(s) + 3Cl 2(g)2AlCl 3(s)在298K 时的r m H θ∆=-1411.26kJ∙mol -1,则f m H θ∆(AlCl 3(s))= _-705.63_ kJ∙mol -1.二、简答题1. [H +]+[HCO 3-]+2[H 2CO 3]=[OH -][H +]+[H 2PO 3-]+2[H 3PO 3]= [OH -]+[PO 33-]2. 2MnO 4-+SO 32-+2OH -=2 MnO 42-+ SO 42-+H 2O 4Zn+10HNO 3=NH 4NO 3 +4Zn(NO 3)2+3H 2O3Br 2+6KOH=5KBr+KBrO 3+3H 2O3K 2MnO 4 +2H 2O= 2KMnO 4+ MnO 2 +4KOH三、计算题(1) 解:设需用HAc x L,则NaAc 用0.5-x L体系H 2O-C 2H 5OH CH 3Cl- CH 3Cl C 2H 5OH –CCl 4 Cl 2- Cl 2 分子间作用力 氢键取向力 诱导力色散力取向力 诱导力 色散力诱导力 色散力色散力()lg ()a c Ac pH pK c HAc θ-=+0.5(0.5)0.55 4.75lg0.50.5x x ⨯-=+ 0.5lg 5 4.750.25x x -=-= 0.18x L =需用NaAc 0.5-0.18=0.32L(2)因为c/Ka > 380 所以151.01076.1][--+⋅⨯⨯=⋅=L mol cK H a θ[H +] = 1.3 ⨯ 10-3 mol·dm -3(3)31()(298)(298)178.32298(160.5110)130.49f m f m f m G T H K T S K KJ molθθθ--∆=∆-∆=-⨯⨯=⋅ (2分)323ln 130.49108.315298ln 1.3510r m G RT K K K θθθθ-∆=-⨯=-⨯⨯=⨯。
大学有机化学期末复习模拟考试试卷(答案)

CH 3CHCH 2COOHBr大学化学有机化学期末复习测试卷班别_________ 姓名___________ 成绩_____________要求: 1、本卷考试形式为闭卷,考试时间为两小时。
2、考生不得将装订成册的试卷拆散,不得将试卷或答题卡带出考场。
3、考生只允许在密封线以外答题,答在密封线以内的将不予评分。
4、考生答题时一律使用蓝色、黑色钢笔或圆珠笔(制图、制表等除外)。
5、考生禁止携带手机、耳麦等通讯器材。
否则,视为为作弊。
6、不可以使用普通计算器等计算工具。
一.命名法命名下列化合物或写出结构式(每小题1分,共10分)1. 2.3. 4.5.6. 邻苯二甲酸二甲酯7.苯乙酮8. 间甲基苯酚9. 2,4–二甲基–2–戊烯CHCH 2(CH 3)2CHCOCH(CH 3)2(CH 3)2CHCH 2CH C(CH 3)2(CH 3)2CHCH 2NH 210. 环氧乙烷二.选择题(20分,每小题2分) 1.下列正碳离子最稳定的是( )(a) (CH 3)2CCH 2CH 3, (b) (CH 3)3CCHCH 3, (c) C 6H 5CH 2CH 2+++2.下列不是间位定位基的是( )3.下列卤代烃与硝酸银的乙醇溶液作用,生成沉淀最快的是( ) A B C4.不与苯酚反应的是( )A 、NaB 、NaHCO 3C 、FeCl 3D 、Br 25. 发生S N 2反应的相对速度最快的是( ) (a) CH 3CH 2Br, (b) (CH 3)2CHCH 2Br, (c) (CH 3)3CCH 2Br6.下列哪种物质不能用来去除乙醚中的过氧化物( ) A .KI B 硫酸亚铁 C 亚硫酸钠 D 双氧水 7.以下几种化合物哪种的酸性最强( ) A 乙醇 B 水 C 碳酸 D 苯酚8. S N 1反应的特征是:(Ⅰ)生成正碳离子中间体;(Ⅱ)立体化学发生构型翻转;(Ⅲ)反应速率受反应物浓度和亲核试剂浓度的影响;(Ⅳ)反应产物为外消旋混合物( )A.I 、IIB.III 、IVC.I 、IVD.II 、IV 9.下列不能发生碘仿反应的是( )A B C D 10.下列哪个化合物不属于硝基化合物( )A B C DACOOHBSO 3HCCH 3DCHOCH 2Cl Cl CH 2CH 2Cl CH 3C CH 3O CH 3CHCH 3OHCH 3CH 2CH 2OHCH3CCH2CH3O CH 3NO 2NO 2CH 3CH 3CH 2NO 2CH 3ONO 2三.判断题(每题1分,共6分)1、由于烯烃具有不饱和键,其中π键容易断裂,表现出活泼的化学性质,因此其要比相应烷烃性质活泼。
大学有机化学期末复习三套试题及答案之二

有机化学试题及答案(二)一、命名下列化合物或者写出化合物的名称(共8 题,每题 1 分,共计 8 分)1.CH3CH3CH2CHCHCH 3CH 2CH32.CH 3CH=CCH 3CH 33.NO 2NHNH 24.CH 2CH 3CH 35.CH3CH2CHO6.2, 2-二甲基 -3, 3-二乙基戊烷7.3, 4-二甲基 -2- 戊烯8.α- 甲基 - β- 氨基丁酸二、判断题(共8 小题,每题 2 分,共 16 分)1、由于烯烃具有不饱和键,其中π键容易断裂,表现出活泼的化学性质,因此其要比相应烷烃性质活泼。
()2、只要含有α氢的醛或者酮均能够发生碘仿反应。
()3、脂环烃中三元环张力很大,比较容易断裂,容易发生化学反应,通常比其他大环活泼些。
()4、羧酸在 NaBH 4的作用下能够被还原为相应的醛甚至醇。
()5、醛酮化学性质比较活泼,都能被氧化剂氧化成相应的羧酸。
()6、环己烷通常稳定的构象是船式构象。
()7、凡是能与它的镜象重合的分子,就不是手性分子,就没有旋光性。
()8、芳香胺在酸性低温条件下,与亚硝酸反应,生成无色结晶壮的重氮盐,称为重氮化反应。
()三、选择题(共 4 小题,每题 2 分,共 8 分)1、下列物质在常温下能使溴水褪色的是()A 丙烷B 环戊烷C 甲苯D 乙烯2、羧酸衍生物中,下列哪种最容易水解()A 酰卤B 酸酐C 酰胺D 酯CH 3CH CCH 33、按照马氏规则,Cl 与 HBr 加成产物是()BrCH 3CHCHCH 3 CH3CHCHCH 3CH 3CH2CCH 3 CH 3CHCHCH 3A ClB Cl BrC Br ClD Br Br4、下列物质容易氧化的是()A 苯B 烷烃C 酮D 醛四、鉴别题(共 6 题,每题 4 分,任选 4 题,共计 16 分)(1)乙烷、乙烯、乙炔(2)甲苯、 1-甲基 -环己烯、甲基环己烷Cl CH 2Cl Cl Cl(3)(4)乙醛、丙醛、丙酮CH 2OH CH3OH(5)BrCH 2Br(6)CH3五、选用适当方法合成下列化合物(共7 题,每题 4 分,共 28 分)(1)丙炔异丙醇(2)甲苯邻、对硝基苯甲酸(3) 1-溴丙烷3-溴丙烯CH3CH3CH2CH2 C CH3 CH3C CCH2CH2CH3(4)O CH3(CH 3)2 CHOH (CH 3)2CCOOH(5) OH(6) CH3 CH2CH 2OH HC CCH 3(7) H2C CHCH3 H2C CHCH2COOH六、推导题(共 5 小题,每题 6 分,任选 4 题,共 24 分)1、A、B 两化合物的分子式都是C6H 12,A 经臭氧氧化并与锌和酸反应后得到乙醛和甲乙酮,B 经高锰酸钾氧化只得丙酸,写出 A 和 B 的结构式,并写出相关反应方程式。
【大学期末考试复习题】大一普通化学试卷及答案

)
A . H 2(g) +
1 2
O 2(g) = H 2O (g)
B.
H 2(g) + Cl 2(g) = 2HCl(g)
C. CaO(s) +CO 2 (g) = CaCO 3(s) 6 .下列物质酸性最强的是 (A)H 3PO4 (B) HClO
D . Fe2O3 (s) + 6HCl(aq) = FeCl 3(aq) +3H 2 O (l) ( )
3 2+
-
3
2+
(1mol/dm ) 的 电 动 势 为
3
3
E1 ;另一电池反应② Cu(s)+Cl 2 (g)=2Cl (1mol/dm )+Cu (1mol/dm ) 的电动势为 E2, 则 E1 和 E2 比值为 ------------------------------------------------ ( A. E1/E 2 =1 B. E
-----------
(
)
4 .用铁粉与稀硫酸作用制备硫酸亚铁时加入过量铁粉的目的是 A . 增加产量 B . 减少产量 C. 防止 Fe → Fe
?
--------2+
(
3+
)
3+
2+
D . 防止 Fe →焓变
? r H m 与生成物的 ? f H m 相等的是 --- (
? ? ?
( ? r Sm > 0
?
)
>0 ,
?
? r Sm < 0 ? r Sm > 0
?
?
? rH m > 0
D . ? r H m < 0 , ? r Sm < 0 K 1 ,那么反应 2A + B = 2D 在同一温度下 ( = 1/2 K 1
《大学化学》复习题库及答案

一、选择题1、自然界中,有的树木可高达100m ,能提供营养和水分到树冠的主要动力为( C )。
(A)因外界大气压引起树干内导管的空吸作用(B)树干中微导管的毛吸作用(C)树内体液含盐浓度高,其渗透压大(D)水分与营养自雨水直接落到树冠上2、在恒温抽空的玻璃罩中封入两杯液面相同的糖水(A)和纯水(B)。
经历若干时间后,两杯液面的高度将是( A )。
(A)A 杯高于B 杯 (B)A 杯等于B 杯(C)A 杯低于B 杯 (D)视温度而定3、活化能的降低,主要是达到( A )目的。
(A )提高反应速率 (B )平衡向正方向移动(C )平衡向反方向移动 (D )增大反应热效应4、298K ,下列反应的△r G m θ 等于AgCl(S)的△f G m θ 的为( B )。
(A) 2Ag(S)+Cl 2(g) ═ 2AgCl(S)(B) Ag(S)+ 21Cl 2(g) ═ AgCl(s)(C) Ag(s)+Cl(g) ═ AgCl(s)(D)Ag+(aq)+Cl -(aq) ═ AgCl(s)5、H 2PO 4-的共轭碱是( B )(A)H 3PO 4 (B)HPO 42- (C)PO 43- (D) OH -6、一定温度下,将等物质的量的气态CO 2和O 2装入同一容器中,则混合气体的压力等于( B )。
(A)CO 2单独存在时的压力 (B)O 2单独存在时的压力(C)CO 2和O 2单独存在时的压力之和(D)CO 2和O 2单独存在时的压力之积7、pH=2的溶液中的H +离子浓度是pH=6的溶液中H + 离子浓度的( D )。
(A)4倍 (B)40倍 (C)4000倍 (D)10000倍8、根据酸碱质子理论,下列化学物质中既可作为酸又可以作为碱的是 ( D )。
(A)NH 4+ (B)H 2CO 3 (C) H 3O + (D)H 2O9、已知反应A + B =2C 的标准平衡常数为K 1Ө ,那么反应2A + 2B = 4C 在同一温度下的标准平衡常数K 2Ө为( D )(A)K 2Ө=K 1Ө (B)K 2Ө= (K 1 Ө)1/2 (C) K 2 Ө = 1/2 K 1 Ө (D)K 2 Ө = (K 1 Ө)210、封闭体系与环境之间( D )。
大学化学考试复习题及答案

一、选择题(每小题2分,共30分)()1。
下列含氧酸中属于一元酸的是(A)H3AsO3(B)H3BO3(C)H3PO3(D)H2CO3( )2.. 干燥氨气可选择的干燥剂是(A) 浓H2SO4(B)CaCl2 (C)P2O5 (D)CaO()3. 加热分解可以得到金属单质的是(A)Hg(NO3)2 (B)Cu(NO3)2(C)KNO3 (D)Mg(NO3)2()4。
下列物质中,既能和H2S反应,又能和HNO3反应的是(A)FeCl3(B)SO2 (C)KI (D)SO3()5. 制备F2实际所采用的方法是(A) 电解HF;(B)电解CaF2(C)电解KHF2(D)电解NH4F()6. 下列各对物质在酸性溶液中能共存的是(A)FeCl3与KI;(B)FeCl2与Br2;(C)FeCl3与KBr; (D)KI与KIO3()7. 下列各对元素中,化学性质最相似的是(A)Be与Mg;(B)Mg与Al;(C)Li与Be;(D)Be与Al( )8.既易溶于稀NaOH又易溶于氨水的是(A) Cu(OH)2(B)Ag2O (C)Zn(OH)2 (D)Cd(OH)2()9.向Hg2(NO3)2溶液中加入NaOH溶液,生成的沉淀是(A) Hg2O (B)HgOH (C) HgO+Hg (D)Hg(OH)2+Hg()10.在下列各对物质中,能够发生反应的一对是(A)FeSO4和I2(B)BaSO4和浓HNO3 (C)Ag和HI (D) H2S和AlCl3()11.酸性介质中,不能将Mn2+氧化为MnO4—的是(A)(NH4)2S2O8(B)NaBiO3(C)K2Cr2O7(D)PbO2( )12.下列金属单质中,熔点最高的是(A) V (B)Cr (C) W (D)Mn()13. 某金属离子在八面体弱场中的磁矩为5.90B。
M.,在八面体强场中的磁矩不为零,则该离子可能是(A)Co3+(B) Co2+(C)Fe3+(D) Fe2+()14.将H2O2加入H2SO4酸化的高锰酸钾溶液中,H2O2起什么作用?(A)氧化剂作用(B) 还原剂作用(C) 还原H2SO4(D)分解成氢和氧( ) 15。
大学生化学元素周期表复习题及答案

大学生化学元素周期表复习题及答案一、复习题1. 元素周期表是什么?它的历史背景是什么?2. 描述元素周期表的结构和布局。
3. 什么是周期?什么是周期表中的主周期和副周期?4. 以下元素属于同一周期的是:氢(H)、锂(Li)、鈹(B)、碳(C)、氮(N)、氧(O)、氟(F)、氦(He)。
请写出它们所属的主周期和副周期。
5. 以下元素属于同一族的是:氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)、钍(Th)、钫(Fm)。
请写出它们所属的族。
6. 根据元素周期表来判断,铍(Be)和锌(Zn)谁的原子半径更大?为什么?7. 氮(N)的电子构型是1s²2s²2p³。
请判断氮(N)是金属、非金属还是半金属。
8. 中子数、原子序数和电子数分别代表什么?9. 请写出以下元素的化学符号和它们的原子序数:铁、铜、镁、锰、钠、磷、铝。
10. 拼写出以下元素名称的正确拼写:铝、镍、钨、铒、亚铜、碘、氘。
二、答案1. 元素周期表是元素根据原子序数、原子构型和化学性质等规律排列而成的表格。
它的历史背景可追溯到19世纪初,由德国化学家门德莱夫根据元素的性质和周期性规律提出了最早的元素周期表。
2. 元素周期表的结构由水平周期和竖直族组成。
水平周期代表元素的周期数,竖直族代表元素的性质和化学反应规律。
元素周期表通常由一系列方格组成,每个方格代表一个元素,按照原子序数从左上角到右下角依次排列。
3. 周期是指原子核周围电子排布的规律性重复出现。
主周期是指1至7周期,副周期是指1至4副周期。
主周期和副周期之间的区别在于主周期内元素的化学性质和电子结构更为相似,而副周期内元素的性质相对较为离散。
4. 主周期和副周期的划分依据原子序数,根据元素周期表可以得出:氢(H)、锂(Li)、鈹(B)、碳(C)、氮(N)、氧(O)、氟(F)、氦(He)属于第1周期。
5. 氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)、钍(Th)、钫(Fm)属于第16族。
华南理工大学有机化学期末复习试卷(含答案)
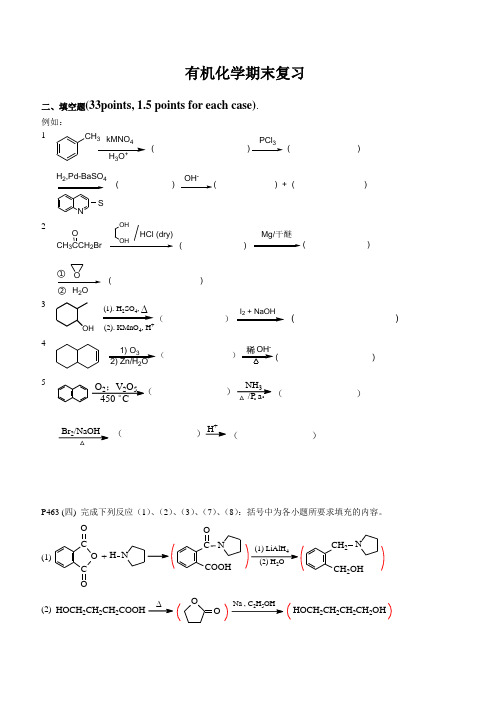
有机化学期末复习二、填空题(33points, 1.5 points for each case). 例如: 1CH 3kMNO43+( )PCl 3( )H 2,Pd-BaSO 4NS( )OH -2CH 3CCH 2BrMg/干醚HCl (dry)OH OHO H 2OO( )( )( )①②3OH(1). H SO ,∆(2). KMnO 4, H+))(41) O 32) Zn/H 2O- )5NH 3/P a Br 2/NaOHH +△△..O 2;V 2O 5 C 。
450( ( )( )( )P463 (四) 完成下列反应(1)、(2)、(3)、(7)、(8):括号中为各小题所要求填充的内容。
(1)C O CO ONH +COOHCON 4(2) H 2OCH 2OHCH 2N(2) HOCH 2CH 2CH 2COOH25∆OOHOCH 2CH 2CH 2CH 2OH(3)CH 2=C COOHCH 3323CH 2=CCOClCH 3CH 2=C COOCH 2CF 3CH 3(7)C NH CO O22COOHNH 2(8)COOHCHOCOClH , Pd-BaSO 3P509,15.15 写出下列季铵碱受热分解时,生成的主要烯烃结构。
P522,15.23 完成下列反应式。
P527,(八) 写出下列反应的最终产物:(1) CH 2ClNaCNLiAlH 4(CH 3CO)2O(CH 2CH 2NHCOCH3)(2)NO Fe, HCl22NO (CH 3)2N )(3)CH 3(CH 2)2CH=CH HBr ROORCN Na CO OH 2O, HO -( CH 3(CH 2)2CH 2CH 2NH 2 )(4)O322N(CH 3)2O)P616,20.2 写出下列反应式中(A )~ (H)的构造式。
三、选择题(反应快慢,鉴别试剂,物质的稳定性,能否发生某种反应等) 例如:P404,11.8 指出下列化合物中,哪个可以进行自身的羟醛缩合。
大学化学复习题及答案

B. 灯光变暗
C. 灯光明暗程度变化不明显
D. 灯光变亮
解
3. 现将足量分别放入下列物质中,①20ml 0.01mol?L-1 KCl溶液 ②30ml 0.02mol?L-1 CaCl2溶液 ③40ml 0.03mol?L-1 HCl溶液 ④10ml蒸馏水 ⑤50ml 0.05mol?L-1 AgNO3溶液的溶解度由大到小的排列顺序是(D)
C. 蛋壳浸泡在白醋中有气体放出
D. 试纸显示白醋的为
34.PH=4的醋酸和氯化铵溶液中,水的电离程度的关系前者与后者的比较(B)
A. 大于
B. 小于
C. 等于
D. 无法确定
35.享有“未来的金属”的美誉的是: C
A. 铁
B. 镍
C. 钛
D. 铜
36.已知H2(g)+Cl2(g)=2HCl(g) △H=―184.6kJ?mol-1, 则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的 △H为(D)
B. P2(V2-V1)
C. [P2V2γ/(1-γ)](1/V2γ-1)- (1/ V1γ-1)
D. (P2V2-P1V1)/(1-γ)
7. 工业上制备纯净的氯化锌时,将含杂质的氧化锌溶于过量的盐酸,为了除去杂质需要调节溶液的pH到4,应加入试剂是(C)
A. 氢氧化钠
B. 氨水
C. 氧化锌
A. 能量的循环供给
B. 能量的不断供给
C. 无能量供给
D. 能量的自我供给
32.下列不是化工能源的是: A
A. 氢气
B. 煤
C. 石油
D. 天然气
大学无机化学期末复习题及答案

无机化学复习题(答案)一.填空(1)共价键的键参数是指键长,键角和键能。
(2)弱电解质的解离度与解离常数的平方根成正比,与弱电解质浓度的平方根成反比的这种关系叫做稀释定律。
(3)化学平衡是指一个化学反应处于正反应速率与逆反应速率相等的表观静止状态。
(4)在弱电解质或难溶强电解质的溶液中加入与弱电解质或与难溶强电解质不具有相同离子的易溶强电解质使弱电解质或难溶强电解质的解离度增大或溶解度升高的现象叫盐效应。
(5)气体的分压是指混合气体中某一组分单独占有混合气体的体积时所具有的压力。
(6)一化学反应的反应浓度(或分压)商Q与K O比较,当 Q < K O时平衡正向移动,而当Q >K O 时平衡逆向移动。
(7)分子内相邻原子或离子间主要的、强烈的相互作用力称为化学键。
(9)状态函数的改变量只取决于系统的始态与终态 ,而与系统变化的途径无关。
(11)任何温度都能自发的化学反应必然具有△H < 0 和△S > 0的特点。
(14)体系与环境之间既无能量交换又无物质传递的体系被称为隔离体系。
(15)改变平衡系统的条件之一温度,浓度,压力平衡向减弱这个改变的方向移动;这个原理被称为吕查德原理。
(16)若干个能级相近的原子轨道相互混合形成电子云高度集中于某一方向且彼此间获得最大夹角,的新的原子轨道,这种新的原子轨道称为杂化轨道。
(17) 摩尔分数是指混合物中某一组分的摩尔数与混合物总摩尔数的百分比。
(20)酸碱质子理论又称为共轭酸碱理论。
该理论中酸的定义是:质子的给出体,碱的定义是:质子的接受体。
二.选择题(单选)1.下列分子的Δf H0m(B,物态,T) 值不等于零的是( C )。
A.石墨(s) B.H2(g) C.H2O(g) D.Cl2(g)4.关于缓冲溶液的性质,正确的说法是:( B )A. 在醋酸溶液中加入过量氢氧化钠,所得溶液有缓冲作用B. 在氢氧化钠溶液中加入过量醋酸,所得溶液有缓冲作用C.在盐酸溶液中加入过量氢氧化钠,所得溶液有缓冲作用D.在氢氧化钠溶液中加入过量盐酸,所得溶液有缓冲作用5.某温度下,反应2A + B= D 的k0 =5,则反应2D = 4A +2 B的标准平衡常数为:( C )A.25B. 0.2C. 0.04D. 1011.下列水溶液中(各相关物质浓度均为0.10 mol·L-1),pH值最小的是:( A )A. HOAc-HCl混合溶液;B. HOAc-NaOAc混合溶液;C. NH4Cl水溶液;D. pH = 1的水溶液12.反应H2(g)+Br2 (g)= 2HBr(g)在800K时Kθ=3.8×105,1000K时Kθ=1.8×103,则此反应是:( B )A.吸热反应;B. 放热反应;C. 无热效应的反应;D. 无法确定15.既能衡量元素金属性强弱,又能衡量其非金属性强弱的物理量是:( A )A. 电负性;B. 电离能;C. 电子亲核能;D. 偶极矩17. 已知下列反应的平衡常数:H 2 (g) + S (s) == H 2S (g) : θ1K ; O 2 (g) + S (s) == SO 2 (g): θ2K ;则反应:H 2 (g) + SO 2 (g) == O 2 (g) + H 2S (g) 的平衡常数为:( D )A. θ1K -θ2K ;B. θ1K ·θ2K ; C. θ2K /θ1K ; D. θ1K /θ2K 18.表示正确的一组量子数是 ( 4 ) (1)(4、1、2) (2) (2、0、-1)(3)(3、1、2) (4) (3、2、-2)22.下列哪种条件其过程必然是自发的 ( 4 )(1)△H >0 △S >0 (2)△H <0 △S <0 (3)△H >0 △S <0 (4)△H <0 △S >0三. 完成下表表:1四.回答下列问题2. 能否将0.1mol/L 的NaOH 溶液稀释至C OH - = 1.0×10-8mol/L?答:不能! 因为纯水的自偶解离已经使CH+ = 1.0×10-7mol/L。
大学化学专升本期末考试总复习资料

大学化学专升本期末考试总复习资料一、名词解释(每题2分,共10分)1.相平衡:2.配位数:3.稳定扩散:4.晶体:5.固溶体:答案:1.研究多相系统中,系统的状态随温度、压力、组分浓度等变化而变化的规律。
2.在晶体结构中,一个原子(或离子)周围,与后直接相邻结合的原子(或所有异号离子)的个数。
3.在垂直方向的任一平面上,单位时间内通过该平面单位面积的粒子数一定。
4.内部质点在三维空间按周期性重复排列的固体或具有格子构造的固体。
5.凡在固态条件下,一种组分(溶剂)内“溶解”了其他组分(溶质)而形成的单一均匀地晶态固体称为固体溶液,简称固溶体。
二、简答题(每题5分,共20分)1.简答如何检验和消除测量过程中的误差以提高分析结果的准确度。
答:误差主要来源有系统误差和随机误差。
为了减少随机误差,需要仔细地进行多次测定取平均结果。
系统误差是由固定的原因产生的,是由规律性的,因此首先要知道误差来源,再用适当的方法校正。
2.什么是副反应系数,什么是条件平衡常数?答:副反应系数:主反应中收影响组分在副反应中个存在形式的总浓度与其平衡浓度的比值。
条件平衡常数:利用副反应系数对收影响的主反应进行修正,得到此结果下的实际有效平衡常数。
3.简述物理吸附与化学吸附的区别。
答案:物理吸附的作用是范德华力,化学吸附是化学键力。
物理吸附可以是多层或者单层,化学只有单层。
物理吸附热小,化学大,物理吸附无或较差选择性,化学较强,物理吸附有可逆性,化学没有,物理吸附平衡容易达到,化学吸附不易达到。
4.试判断下列过程熵变的正负号(1)溶解少量食盐于水中;(2)水蒸气和炽热的碳反应生成CO和H;(3)冰熔化变为水;(4)石灰水吸收CO2;(5)石灰石高温分解。
答案:(1)+;(2)+;(3)+;(4)—;(5)+三、论述题(每题10分,共30分)1.影响化学反应速率的主要因素有哪些?质量作用定律的意义是什么?对一般的化学反应,速率方程式的反应级数能否直接根据化学反应方程式来写?为什么?答:影响化学反应速率的主要因素有:浓度、温度、压力和催化剂。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《大学化学》复习题答案
一、是非题:请在各题括号中,用“√”、“×”分别表示题文中叙述是否正确。
(√) 1. 电子云是描述核外某空间电子出现的几率密度的概念。
(√)2. 同种原子之间的化学键的键长越短,其键能越大,化学键也越稳定。
(√)3.系统经历一个循环,无论多少步骤,只要回到初始状态,其热力学能和焓的变化量均为零。
(√)4. AgCl在NaCl溶液中的溶解度比在纯水中的溶解度小。
(×)5. 原子轨道的形状由量子数m决定,轨道的空间伸展方向由l决定。
二、选择题
(1)某元素原子基态的电子构型为1s22s22p63s23p5,它在周期表中的位置是:a a.p区ⅦA族b.s区ⅡA族
c.ds区ⅡB族d.p区Ⅵ族
(2)下列物质中,哪个是非极性分子:b
a.H2O b.CO2c.HCl d.NH3
(3)极性共价化合物的实例是:b
a.KCl b.HCl c.CCl4d.BF3
(4)下列物质凝固时可以形成原子晶体的是:c
a. O
2 b. Pt, c. SiO
2
d. KCl
(5)在298K,100kPa下,反应
2H2(g)+O2(g)=2H2O(1)Δr H mΘ= -572 kJ·mol-1
则H2O(l)的Δf H mΘ为:d
a.572 kJ·mol-1b.-572 kJ·mol-1
c.286 kJ·mol-1d.-286 kJ·mol-1
(6)定温定压下,已知反应B=A的反应热为Δr H m1Θ,反应B=C的反应热为Δr H m2Θ,则反应A=C的反应热Δr H m3Θ为:d
a.Δr H m1Θ+Δr H m2Θb.Δr H m1Θ-Δr H m2Θ
c.Δr H m1Θ+2Δr H m2Θd.Δr H m2Θ-Δr H m1Θ
(7)已知HF (g )的标准生成热Δf H m Θ
= -565 kJ ·mol -1,则反应H 2(g)+F 2(g)=2HF(g)的Δr H m Θ为:d
a .565 kJ ·mol -1
b .-565 kJ ·mol -1
c .1130 kJ ·mol -1
d .-1130 kJ ·mol -1
(8)在氨水溶液中加入固体NH 4Cl 后,氨水的离解度:d
a .没变化
b .微有上升
c .剧烈上升
d .下降
(9)N 的氢化物(NH 3)的熔点都比它同族中其他氢化物的熔点高得多,这主要由于NH 3:c
a .分子量最小
b .取向力最强
c .存在氢键
d .诱导力强
(10)在一定条件下,一可逆反应其正反应的平衡常数与逆反应的平衡常数关系是:c
a .它们总是相等
b .它们的和等于1
c .它们的积等于1
d .它们没有关系
(11)下列反应及其平衡常数H 2 (g)+S(s)=H 2S (g ) K 1Θ;(g)SO (g)O S(s)22=+ K 2Θ,则反应S(g)H (g )O (g )SO (g )H 2222+=+的平衡常数K Θ是:d
a. K 1Θ+K 2Θ b .K 1Θ- K 2Θ c .K 1Θ×K 2Θ. d .K 1Θ÷K 2Θ
(12)在298K 时石墨的标准摩尔生成焓Δf H m Θ为:c
a .大于零
b .小于零
c .等于零
d .无法确定
(13)不合理的一套量子数(n ,l ,m ,m s )是:b
a .4,0,0,21+
b .4,0,-1,21-
c .4,3,+3,21-
d .4,2,0,2
1+
(14)向HAc 溶液中,加入少许固体物质,使HAc 离解度减小的是:b
a .NaCl
b .NaA
c c .FeCl 3
d .KCN
(15)3NH 溶于水后,分子间产生的作用力有:d
a .取向力和色散力
b .取向力和诱导力
c.诱导力和色散力d.取向力、色散力、诱导力及氢键(16)25℃时,Mg(OH)2的K spΘ为1.2×10-11,在0.01mol · L-1的NaOH溶液中的溶解度为:c
a.1.2×10-9 mol · L-1b.2.4×10-9 mol · L-1
c.1.2×10-7 mol · L-1d.1.7×10-5 mol · L-1
(17)已知EΘ(Fe3+/Fe2+)=0.770V,EΘ(Cu2+/Cu)=0.340V,则反应
2Fe3+(1mol·L-1)+Cu=2Fe2+(1mol·L-1) + Cu2+(1mol·L-1)可以:b a.呈平衡状态b.自发正向进行
c.自发逆向进行d.前三者都错
(18)已知Fe3++e = Fe2+,EΘ= 0.770V,测定一个Fe3+/Fe2+电极电势E= 0.750 V,则溶液中必定是:d
a.c(Fe3+)<1 b.c( Fe2+)<1
c.c( Fe2+)/ c(Fe3+)<1 d.c(Fe3+)/ c( Fe2+)<1
(19)角量子数l描述核外电子运动状态的:c
a.电子能量高低;b.电子自旋方向;
c.电子云形状;d.电子云的空间伸展方向;
(20)以下各组物质可做缓冲对的是:a
a.HCOOH—HCOONa b.HCl一NaCl
c.HAc—H2SO4d.NaOH—NH3·H2O
三、填空题
1.写出具有下列指定量子数的原子轨道符号:
A. n=4,l=1____4p________
B. n=5,l=2 ______5d______
2.写出下列原子在基态时的电子排布
(1). Mn: 1s22s22p63s23p63d54s2; (2). Fe___1s22s22p63s23p63d64s2;
3. 等性sp2、sp3杂化轨道的夹角分别为__120_____._109.5____.
4. 在定温定压下已知反应A=3B的反应热为Δr H m1Θ,反应3A=C的反应热为
Δr H m2Θ,则反应9B=C的反应热Δr H m3Θ为(Δr H m2Θ- 3Δr H m1Θ)。
5. CaO(s)+ CO2(g)= CaCO3(s)的平衡常数表达式为(KΘ=1/P CO2 )。
6. 25℃时Ag2CrO4的溶解度为( 6.1 ×10-4)。
(K spΘ(Ag2CrO4)=9.0×10-10)。
7. 已知:Zn2+ + 2e-EΘ(Zn2+/Zn )
= -0.762 8V, 那么
2
1Zn2+ + e-Zn EΘ(Zn2+/Zn )= ( -0.762 8V)由此可知,标准电极电势EΘ由( 物质的电势)决定,与电极反应中(计量系数)无关。
8. 某元素电子构型为[Ar]3d54s2,此元素位于( 4 )周期,( 7 )族。
9. 命名下列配合物:a. [Ni(en)2]Cl2( 二氯化二-乙二胺合镍(II)) b. Na3[AlF6] ( 六氟合氯酸钠)
五、简答题
1、用四个量子数描述基态C原子外层p轨道上2个电子的运动状态?
2. BF
3分子构型是平面三角形,而NF
3
分子构型是三角锥形,试用杂化轨道理论
解释.
3. CH4、H2O、NH3中心原子杂化态皆是sp3,其键角大小是否相同?为什么?其
空间构型各为何?
2、化学Ag++Fe2+=Fe3++Ag在原电池中发生,试写出原电池符号和电极反应。
六、计算题
1. 对于A(s)+B2+(aq)=A2+(aq)+B(s)反应,已知A2+的初始浓度为零,B2+的初始浓度为0.06 mol·L-1,平衡时B2+的浓度为0.02 mol·L-1,计算上述反应25℃时的KΘ。
解:0.04/0.02=2
2.浓度均为0.01mol·L-1的Cl—和CrO42-的混合溶液中,逐滴加入AgNO3溶液,何种离子先沉淀?当第二种离子沉淀时先沉淀离子的浓度是多少?(K spΘ(AgCl)=2×10-10,K spΘ(Ag2CrO4)=1×10-12)
解:AgCl先沉淀
[Cl-]=2×10-5。
