手册报核情况说明表2017
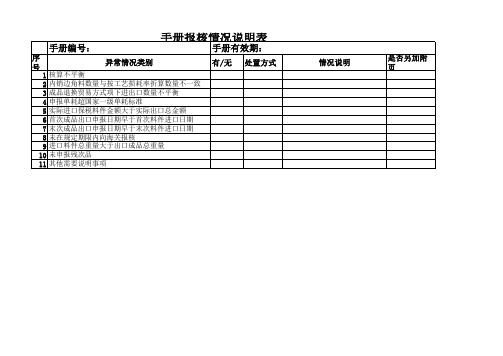
手册报核情况说明表
手册编号:
序号
1 2 3 4 6 7 8 9 10 11
手册有效期:
异常情况类别 有/无 处置方式 情况说明 是否另加附页
核算不平衡 内销边角料数量与按工艺损耗率折算数量不一致 成品退换贸易方式项下进出口数量不平衡 申报单耗超国家一级单耗标准 实际进口保税料件金额大于实际出口总金额 首次成品出口申报日期早于首次料件进口日期 末次成品出口申报日期早于末次料件进口日期 未在规定期限内向海关报核 进口料件总重量大于出口成品总重量 未申报残次品 其他需要说明事项
我司承诺以上说明及提交的随附资料真实,合法,完整,有效,并承担相应法律责任!
企业经办人签字: 单位公章: 日期:
血液安全技术核查指南[2017]_医疗机构部分
![血液安全技术核查指南[2017]_医疗机构部分](https://img.taocdn.com/s3/m/13d365d19fc3d5bbfd0a79563c1ec5da50e2d6bf.png)
血液安全技术核查指南(2017)——医疗机构部分
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
专业整理
备注:
1.核查时,应对所列条款进行逐项核查,每个条款的核查结果评定为A、B、C或D。
符合核查标准第一项评为A,符合第二项评为B,符合第三项评为C,符合第四项评为D(第1、7、9、14和19条款包含第四项)。
2.医疗机构核查总评结果分为优、良、合格或不合格。
“优”的标准:所有条款没有得D,同时得到10个及以上的A或15个及以上的B;“良”:所有条款没有得D,同时得到6-9个A或10-14个B;“合格”:所有条款没有得D,同时少于6个A或10个B;“不合格”:得一个及以上的D。
提出批评,并要求限期整改。
专业整理
3.核查情况描述主要记录亮点工作,需要特殊说明的情况,不合格或提出批评的情况。
4.凡有“*”标记的条款,均为涉及影响患者安全条款,对此类条款应重点核查。
5.此表格由被检查单位先自查,并对自查结果进行描述,列出支持评分的依据。
核查总评结果:
核查人员(签名):被检查单位临床用血负责人(签名):
核查日期:2017年月日专业整理。
(全)企业所得税年报报表及填表说明2017版

中华人民共和国企业所得税年度纳税申报表
《中华人民共和国企业所得税年度纳税申报表(A类,2017年版)》
封面填报说明
《中华人民共和国企业所得税年度纳税申报表(A类,2017年版)》(以下简称申报表)适用于实行查账征收企业所得税的居民企业纳税人(以下简称纳税人)填报。
有关项目填报说明如下:
1.“税款所属期间”:正常经营的纳税人,填报公历当年1月1日至12月31日;纳税人年度中间开业的,填报实际生产经营之日至当年12月31日;纳税人年度中间发生合并、分立、破产、停业等情况的,填报公历当年1月1日至实际停业或法院裁定并宣告破产之日;纳税人年度中间开业且年度中间又发生合并、分立、破产、停业等情况的,填报实际生产经营之日至实际停业或法院裁定并宣告破产之日。
2.“纳税人统一社会信用代码(纳税人识别号)”:填报工商等部门核发的统一社会信用代码。
未取得统一社会信用代码的,填报税务机关核发的纳税人识别号。
3.“纳税人名称”:填报营业执照、税务登记证等证件载明的纳税人名称。
4.“填报日期”:填报纳税人申报当日日期。
5.纳税人聘请中介机构代理申报的,加盖代理申报中介机构公章,并填报经办人及其执业证件号码等,没有聘请的,填报“无”。
企业所得税年度纳税申报表填报表单A000000 企业基础信息表
A100000 中华人民共和国企业所得税年度纳税申报表(A类)
A101010 一般企业收入明细表
A101020 金融企业收入明细表。
YYT 0287-2017版质量手册

***********有限公司质量手册版本号A/0依据:GB/T 19001—2016(ISO 9001:2015,IDT) YY/T 0287—2017 (ISO 13485:2016, IDT)编制:审核:批准:20 - - 发布20 - - 实施*************有限公司发布************有限公司编号:GW-QM-01 章节: 01编号: GW-QM-02 章节: 02编号: GW-QM-03 章节: 03标题:质量手册发布令质量手册发布令2017年,公司依据GB/T 19001-2016 idt ISO 9001:2015《质量管理体系要求》、YY/T 0287-2017 idt ISO 13485:2016 《医疗器械质量管理体系用于法规要求》标准,以及《医疗器械生产质量管理规范》,并结合公司的实施情况,编制了A/0版《质量手册》,于年月日发布。
该手册规定了公司质量管理体系要求。
本公司依此要求进行医疗分析仪器的设计和开发、生产、安装和服务以及相关服务的设计、开发和提供。
也可用于内部和外部(包括认证机构)评定公司满足顾客要求和符合产品法规要求的能力。
本《质量手册》由质量部组织编写,手册的有效性由管理者代表负责审核,经总经理批准后《质量手册》即成为公司范围内质量体系的基本要求和重要法规,公司全体员工均必须遵照执行。
手册的修改需得到总经理批准。
本《质量手册》未经总经理批准,不允许任何人向外借阅。
***********有限公司总经理:年月日标题:管理者代表任命书任命书为确保和保持质量体系的有效运行,协助最高管理者对质量管理体系运作的领导,实现对顾客和产品质量的承诺,现任命同志为南京***********有限公司管理者代表,此任命自签发之日起正式生效。
总经理:2017年3月20日标题:企业概况公司概况南京***********有限公司是经江苏省科技厅评审、国家科技部审定的高新技术企业,是集科研、生产、经营为一体的民营高新技术企业实体。
国军标GJB9001C:2017全套文件(手册+程序文件共135页)

国军标GJB9001C:2017全套文件(手册+程序文件共135页)质量管理体系文件CDM.QM.01-2018质量手册+程序文件【依据GB/T19001-2016(ISO9001:2015,IDT)和GJB9001C-2017编制】(第 E/0 版)编制审核批准发放日期 2018-04-01发放编号 CDM.12410.4/012018-04-01发布 2018-04-01实施.1质量手册目录01质量手册目录 (1)02质量手册批准书 (3)03任命书 (4)04公司概况 (5)1 质量手册说明 (7)2 组织机构 (9)3 质量管理体系活动职责分配 (11)4 质量管理体系 (14)4.1 总要求 (14)4.2 文件要求 (16)4.2.3文件控制程序●(CDM.QP.01) (19)4.2.4记录控制程序●(CDM.QP.02) (24)5 管理职责 (27)5.1 管理承诺 (27)5.2 以顾客为关注焦点 (27)5.3 质量方针 (28)5.4 质量策划 (29)5.5 职责、权限和沟通 (30)5.6 管理评审程序(CDM.QP.03) (37)6 资源管理 (40)6.1 资源提供 (40)6.2 人力资源控制程序(CDM.QP.04) (41)6.3 基础设施控制程序(CDM.QP.05) (45)6.4 工作环境控制程序(CDM.QP.06) (48)6.5 信息管理创新★(CDM.QP.07) (50)7 产品实现 (54)7.1 产品实现的策划的策划程序(CDM.QP.08) (55)7.2 与顾客有关过程(CDM.QP.09) (59)7.3 设计和开发控制程序(CDM.QP.10) (64)7.3.4 设计和开发评审程序(CDM.QP.11) (71)7.3.8 新产品试制程序★CDM.QP.12) (74)7.4 采购和外包过程控制程序(CDM.QP.13) (77)7.5 生产和服务提供控制程序(CDM.QP.14) (81)7.5.6 关键/特殊过程控制程序(CDM.QP.15) (88)7.6 监视和测量设备控制程序(CDM.QP.16) (91)7.7 技术状态管理控制程序(CDM.QP.17) (94)8 测量、分析和改进 (97)8.1 总则 (97)8.2 监视和测量8.2.1 顾客满意度测量程序(CDM.QP.18) (99)8.2.2 内部审核程序●(CDM.QP.19) (103)8.2.3 过程监视和测量程序(CDM.QP.20) (107)8.2.4 产品监视和测量程序(CDM.QP.21) (109)8.3 不合格品控制程序●(CDM.QP.22) (113)8.4 数据分析控制程序(CDM.QP.23) (116)8.5 改进8.5.1 改进控制程序(CDM.QP.24) (120)8.5 纠正程序控制程序●(CDM.QP.25) (123)8.5 预防措施控制程序●(CDM.QP.26) (125)CDM.QP.26 不良成本控制程序 (125)图1组织机构图(2) (130)图2质量管理体系模式图(5.4.1) (131)图3产品实现过程图(7.1) (132)图4合同评审流程图(7.2) (133)图5电机生产工艺流程图 (134)表1 程序文件目录 (135)表2 质量手册会签表 (136)表3 质量手册会签表 (137)表4 质量手册更改记录 (138)0.2《质量手册》批准书有限公司企质办,依据GB/T19001—2016《质量管理体系—要求》(ISO9001:2015,IDT)和GJB9001C—2017标准要求和国家颁布的法律法规,结合公司实际,编制完成了《质量手册(2018版/E版)》,通过审订正式批准颁布。
2021年QC080000-2017内部审核检查记录表(HSPM内部审核查检表)
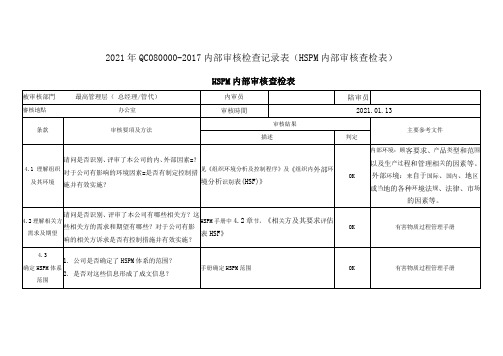
2021年QC080000-2017内部审核检查记录表(HSPM内部审核查检表)
HSPM内部审核查检表
備注﹕O合格△次要缺點×主要缺點 NA與本部門無關
HSPM内部审核查检表
備注﹕O合格△次要缺點×主要缺點 NA與本部門無關
HSPM内部审核查检表
備注﹕O合格△次要缺點×主要缺點 NA與本部門無關
HSPM内部审核查检表
備注﹕O合格△次要缺點×主要缺點 NA與本部門無關
HSPM内部审核查检表
备注﹕O合格△次要缺点×主要缺点 NA与本部门无关
HSPM内部审核查检表
備注﹕
O 合格 △次要缺點 ×主要缺點 NA 與本部門無關
HSPM 内部审核查检表
備注﹕O合格△次要缺點×主要缺點 NA與本部門無關。
财务报表情况说明书

财务报表情况说明书财务报表情况说明书一、企业概况本企业属于服务性企业,成立于2017年。
是以绿化施工为主的公司,主营业务收入占企业总收入的比重为100%。
公司现有资产总额已达16万元,其中包括流动资产13.14万元,占总资产的比例为82%;固定资产2.87万元,占资产总额的比例为18%。
负债总额达2万元,资产负债率为12.5%,其中流动负债2万元,占负债总额的100%,所有者权益14万元,占企业资产总额的87.5%。
二、企业经营情况分析1、本年主营业务收入24万元,比去年同比增长14万元,增长率140%。
2、本年管理费用15.83万元,比去年同比增长3.52万元,增长率28.6%,管理费用占主营业务收入的66%。
3、本年主营业务税金及附加1.36万元,比去年同比增长0.79万元,增长率138.6%,主营业务税金及附加占主营业务收入的5.67%。
4、本年营业利润6.8万元,比去年同比增长7.9万元;营业利润占主营业务收入的28.33%。
三、利润实现和分配情况1、本年实现利润总额6.8万元,净利润5.1万元。
2、全年上交所得税1.7万元。
3、本年职工工资总额8.4万元,职工人数7人,职工全年平均收入1.2万元。
四、资金增减和周转情况1、本年应收账款周转率为79%;流动资产周转率为218%;固定资产周转率为667%;总资产周转率为172%。
2、企业的发展能力指标情况:主营业务收入增长率为140%。
五、总结说明公司由于成立时间短,刚刚起步,虽然经营效益增长很快,但不确定因素很多,主要是应收账款增加较大,后期应积极回款;同时职工工资总额占比较高,应很好控制。
二○一三年四月二十八日财务报表情况说明书 [篇2]一、企业生产经营的基本情况靖边县佳贝钻井技术服务有限责任公司成立于2004年3月,在靖边县工商行政管理局办理了登记注册,注册资金500万元,出资人为:祁健洲465万元,占比93%;孔令梅35万元,占比7%,公司地址靖边县河东三岔路西侧,占地面积380平米,总建筑面积360平米,公司现有员工43人,企业类型属有限责任公司。
车险理赔操作手册(核赔篇)2017版

内部资料请勿外传车险理赔操作手册(理算核赔支付篇)2017版编者:黄菊秀理赔事业部二○一六年十二月目录公司十项服务承诺 (1)理赔人员十项禁令 (4)单证收集 (6)理算 (17)核赔 (32)归档 (41)公司十项服务承诺中国大地保险,将秉承“诚信为先,稳健经营,价值至上,服务社会”的经营理念,弘扬“简单、高效、务实、合规”的企业文化,贯彻“以客户为中心”的服务理念,以良好的信誉向社会和广大客户提供高品质的保险服务。
为进一步提升客户服务质量,保护保险消费者权益,中国大地保险向社会和广大客户郑重做出如下承诺:一、365天×24小时专线畅通无忧。
95590全国统一服务专线,全天候提供报案、咨询、投诉、承保理赔信息查询和客户回访等服务。
二、365天×24小时查勘。
接到报案后10分钟内与客户联系,在约定的时间内查勘。
需现场查勘的车险案件,市区30分钟、郊区60分钟内到达现场。
因特殊情况延误的,将提前联系客户说明情况。
三、365天×8小时定损。
定损时严格遵循客观、公正、合理原则,不强制指定修理厂或零配件供应商。
如客户需要,可以推荐二级及以上资质良好的修理厂。
四、10万元以下车险案件1个工作日内赔付。
对保险责任明确、索赔材料齐全的10万元以下的车险赔案,与客户达成赔偿协议后,1个工作日内付款。
五、车险小额案件快赔。
对保险责任明确的5000元(含)以下车险小额非人伤赔案,可以现场定损或采取微信自助查勘,远程定损;现场收集索赔材料,限时赔付;上门递交索赔材料的,如保险责任明确、索赔材料齐全,30分钟内付款。
六、车险免上门交单。
对于符合条件的1万元(含)以下车险非人伤赔案,在查勘定损时现场收集索赔材料;客户现场不能提供的,可以通过网络、微信、邮寄等方式提交;也可以根据客户需求,安排上门收单服务;索赔材料不齐全的一次性通知客户补充提供。
七、人伤温情关怀。
提供小额人伤现场调解、住院伤员定期探视、伤残鉴定陪同、医疗救援指导、人伤理赔及诉讼调解专业建议和咨询等服务;对案件事实清楚、损失金额基本确定的,可根据客户需求提前赔付。
关于发布进料加工贸易手册核销业务操作指南
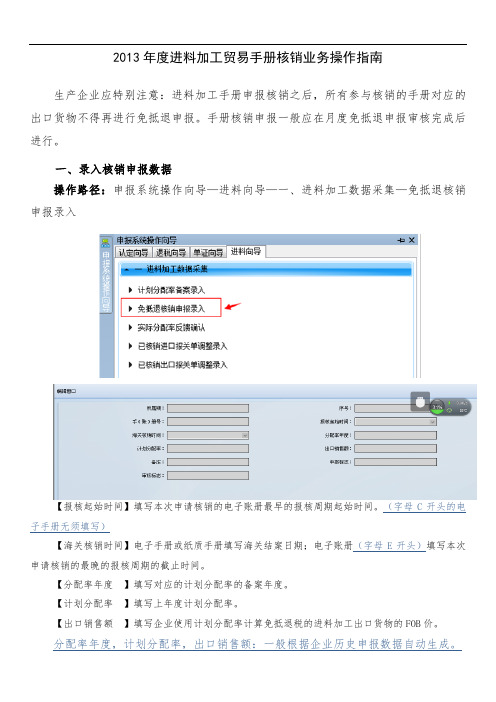
2013年度进料加工贸易手册核销业务操作指南生产企业应特别注意:进料加工手册申报核销之后,所有参与核销的手册对应的出口货物不得再进行免抵退申报。
手册核销申报一般应在月度免抵退申报审核完成后进行。
一、录入核销申报数据操作路径:申报系统操作向导—进料向导—一、进料加工数据采集—免抵退核销申报录入【报核起始时间】填写本次申请核销的电子账册最早的报核周期起始时间。
(字母C开头的电子手册无须填写)【海关核销时间】电子手册或纸质手册填写海关结案日期;电子账册(字母E开头)填写本次申请核销的最晚的报核周期的截止时间。
【分配率年度】填写对应的计划分配率的备案年度。
【计划分配率】填写上年度计划分配率。
【出口销售额】填写企业使用计划分配率计算免抵退税的进料加工出口货物的FOB价。
分配率年度,计划分配率,出口销售额:一般根据企业历史申报数据自动生成。
注意事项:1、逐份手册进行核销数据录入。
其中,进料加工手册项需录入上年度海关核销的全部进料加工登记手册、账册编号(纸质或电子手册号通常以C开头,电子账册号通常以E开头)。
2、进料加工手册实行年度核销政策,一年只核销一次,时间是每年的一月到四月,上一年度在海关所有核销的手(账)册号必须全部录入。
3、报完正常退税,再申报手册核销,否则系统会报错。
核销申报应在月度免抵退申报完成后进行,核销申报所属期应与最近一次已完成的免抵退税申报所属期一致。
如企业已经完成201402的免抵退申报,但是尚未完成201403的申报,此时做进料加工核销,申报年月应该是201402。
二、生成核销申报电子数据操作路径:申报系统操作向导—进料向导—生成进料加工申报—二、生成进料加工数据注意事项:1、生成进料加工数据:所属期填核销申报所属期。
2、生成进料加工数据的时候提示:该所属期已经申报。
如果申报数据有问题需要调整申报,可以通过“向导—进料加工反馈接收—撤销进料加工数据”撤销申报后重复上述步骤。
三、打印《申报表》操作路径:申报系统操作向导—进料向导—三、打印进料加工报表,选择“进料加工业务免抵退税核销申报表”进行打印注意事项:生成申报正式文件并通过申报系统上报电子数据后,生产企业持系统打印的加盖公章的《生产企业进料加工业务免抵退税核销申报表》,向第十九税务所申请核销。
QC080000-2017有害物质管理稽核评价表
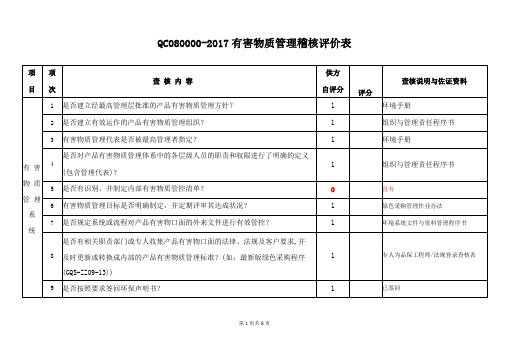
在接客户新产品订单前,是否有对客户关于产品有害物质方面(如物料与技术等) 的要求进行评审并纳入组织的产品规格?
1
样品试作管制程序
2
零件设计标准书或材料规格书中是否明确说明符合客户有害物质管控的规格要
求,包括外包部份?(如最新版的最新版绿色采购程序(GQS-ZZ09-13))
1
绿色采购管理作业办法
3
仓储人员等)制定了有关有害物质管理的教育培训程序规定?
1
环境教育训练管理计划?
1
环境教育训练管理程序书
13
有害物质管理的教育训练计划是否按期实施?
1
环境教育训练管理程序书
14
有害物质管理的教育训练是否建立考核机制并执行?
1
环境教育训练管理程序书
15
是否建立有害物质管理系统内部稽核的程序规定?
1
专人为品保工程师/法规登录查核表
9
是否按照要求签回环保声明书?
1
已签回
第1页共8页
10
是否明确定义产品有害物质相关技术文件(如物质成份宣告表、测试报告、环保
声明书等)依客户规定要求保存并执行?(规定至少保存3年)
0
没有,是一年
11
是否对于从事影响产品HSF质量相关工作的人员(如工程人员、品保/品管人员、
(包含管理代表)?
1
组织与管理责任程序书
5
是否有识别、并制定内部有害物质管控清单?
0
没有
6
有害物质管理目标是否明确制定,并定期评审其达成状况?
1
绿色采购管理作业办法
7
是否规定系统或流程对产品有害物口面的外来文件进行有效管控?
1
环境系统文件与资料管理程序书
原创精品ISO IEC17025-2017实验室管理体系全套文件(质量手册及程序文件)

ISO/IEC17025-2017 实验室管理体系全套文件质量手册及程序文件ISO/IEC17025-2017实验室管理体系质量手册实施日期:2018年01月01日 XXX公司实验室B质量手册修改记录C目录A 批准页B 修改页C 目录D 质量手册发布令E 公正性声明F 质量方针和质量目标G 质量手册管理0引言0.1 公司概况0.2 组织架构1 范围1.1总则1.2应用2 规范性引用文件3 术语和定义4通用要求4.1 公正性4.2 保密性5 结构要求6资源要求6.1 总则6.2 人员6.3 设施和环境条件6.4 设备6.5 计量溯源性6.6 外部提供的产品和服务7过程要求7.1 要求、标书和合同评审7.2 方法的选择、验证和确认7.3 抽样7.4 检测或校准物品的处置7.5 技术记录7.6 测量不确定度的评定7.7结果有效性的保证7.8结果的报告7.9投诉7.10不符合工作7.11数据控制和信息管理8管理要求8.1 方式8.2 管理体系文件8.3 管理体系文件的控制8.4 记录控制8.5 风险和机会的管理措施8.6 改进8.7 纠正措施8.8 内部审核8.9 管理评审附录A计量溯源性附录B管理体系方式附件1任命书附件2授权书附件3授权签字人识别附件4检定、校准和检测项目一览表附件5管理体系程序文件清单附件6公司和实验室平面图D质量手册发布令公司全体职工:为了保证本公司检验检测工作的质量,确保检验检测结果的公正性、准确性和科学性,公司为满足实验室要求,依据ISO /IEC17025:2017《检测和校准实验室能力的通用要求》,并结合实验室实际情况重新编制了《实验室管理体系质量手册》现予以批准。
本手册于二○一八年一月一日起正式实施。
《实验室管理体系质量手册》是描述实验室管理体系的纲领性文件,是实验室管理体系运行的行为准则和评审的依据,也是实验室质量保证能力的证实,手册所涉及的单位和员工都必须严格执行,确保实验室质量方针的实现。
GJB-2017-C-版《质量手册》参考模板(WORD)

版本号:C0编号:XXXXX-XXXX状态:(受控印章)质量手册(模板)编辑:审核:批准:XXXXXXXXXXXX公司二〇XX年XX月更改控制页目录引言 1 ..................................具体按《质量手册》实际内容定。
前言本手册于XXXX年XX月按照GB/T19001-94的要求制定并首次发布,XXXX年XX月按照GB/T19001-2008和GJB9001B-2009的要求重新修订为B版,XXXX年XX月按照GB/T19001-2016和GJB9001C-2017的要求重新修订为C版。
本手册为公司质量管理体系的基础要求,为了便于识别各行业标准的特殊要求,针对GB/T19001-2008标准内容采用小四号宋体字表示;GJB9001C-2017标准内容采用小四号楷体字表述。
程序文件和三层次文件均按此执行。
本手册的附录A、B是资料性附录。
本手册由质量管理部提出并归口。
本手册由质量管理部负责起草。
本手册主要起草人:XXX、XXX、XXX、XXX、XXX。
引言0.1 总经理授权书授权书兹委任 XXX (先生/女士)担任XXXXXXXXX公司总经理,代表法人对公司进行管理,全权负责公司工作。
法人(签名):日期:年月日0.2 管理者代表任命书任命书兹任命 XXX 为管理者代表,负责确保XXXXXXXX公司质量管理体系的建立、实施和保持;领导质量管理体系的管理和内部审核工作,负责向总经理报告质量管理体系运行情况,需要改进的包括资源需求的情况;确保在全体员工中提高满足顾客要求的意识。
授权质量管理部为质量管理体系建立、实施和保持的主管部门,协助管理者代表完成质量管理体系运行的日常事务管理工作;负责质量管理体系的外部联络工作。
总经理(签名):日期:年月日0.3 质量手册颁布令质量手册颁布令产品质量是永恒的主题,是公司的生命。
关注顾客期望是公司的焦点,追求持续改进是公司永恒的目标。
ISO17025:2017内审检查表-质量负责人

7.10.3
当评价表明不符合工作可能再次发生时,或对实验室的运行与其管理体系的符合性产生怀疑时,实验室是否采取纠正措施?
暂无不符合
符合
要素
条款
检查内容
审核方法和凭证
客观记录
审核结果
8.1.1
实验室是否建立、编制、实施和保持管理体系,该管理体系是否能够支持和证明实验室持续满足本准则要求,并且保证实验室结果的质量?
有程序文件清单,有记录清单,有质量手册。
符合
8.2.5
参与实验室活动的所有人员是否可获得适用其职责的管理体系文件和相关信息?
质量手册和程序文件已经下发到相关人员,并且已经组织过学习。
符合
8.3.1
实验室是否控制与满足本准则要求有关的内部和外部文件?
查文件控制程序
是
符合
8.3.2
实验室是否确保:
查文件清单、外来文件清单
实验室是否有形成文件的过程来接收和评价投诉,并对投诉作出决定?
查客户服务和处理投诉的程序
程序文件名称:客户服务和处理投诉的程序,文件编号:HKPKC-207-19
符合
要素
条款
检查内容
审核方法和凭证
客观记录
审核结果
7.9.2
利益相关方有要求时,是否可获得对投诉处理过程的说明?
在接到投诉后,实验中心是否确认投诉与其负责的实验室活动的相关性,如相关,是否做出处理?
是
符合
除满足第4条款至第7条款的要求,实验室是否按方式A或方式B实施管理体系?
查质量手册确认是方式A还是方式B
质量手册明确定义是方式A
符合
8.1.2
实验室管理体系是否至少包括下列内容:
有文件清单,建立了文件控制程序,左边的相关条款都包含在我们的相关体系范围内。
中华人民共和国海关加工贸易货物监管办法(2017修改)-海关总署令第235号

中华人民共和国海关加工贸易货物监管办法(2017修改)正文:----------------------------------------------------------------------------------------------------------------------------------------------------中华人民共和国海关加工贸易货物监管办法(2014年3月12日海关总署令第219号公布根据2017年12月20日海关总署令第235号公布的《海关总署关于修改部分规章的决定》》修改)第一章总则第一条为了促进加工贸易健康发展,规范海关对加工贸易货物管理,根据《中华人民共和国海关法》(以下简称《海关法》)以及其他有关法律、行政法规,制定本办法。
第二条本办法适用于办理加工贸易货物手册设立、进出口报关、加工、监管、核销手续。
加工贸易经营企业、加工企业、承揽者应当按照本办法规定接受海关监管。
第三条本办法所称“加工贸易”是指经营企业进口全部或者部分原辅材料、零部件、元器件、包装物料(以下统称料件),经过加工或者装配后,将制成品复出口的经营活动,包括来料加工和进料加工。
第四条除国家另有规定外,加工贸易进口料件属于国家对进口有限制性规定的,经营企业免于向海关提交进口许可证件。
加工贸易出口制成品属于国家对出口有限制性规定的,经营企业应当向海关提交出口许可证件。
第五条加工贸易项下进口料件实行保税监管的,加工成品出口后,海关根据核定的实际加工复出口的数量予以核销。
加工贸易项下进口料件按照规定在进口时先行征收税款的,加工成品出口后,海关根据核定的实际加工复出口的数量退还已征收的税款。
加工贸易项下的出口产品属于应当征收出口关税的,海关按照有关规定征收出口关税。
第六条海关按照国家规定对加工贸易货物实行担保制度。
未经海关批准,加工贸易货物不得抵押。
第七条海关对加工贸易实行分类监管,具体管理办法由海关总署另行制定。
质量管理体系各部门内部审核检查表(包含完整检查内容)

√
2.组织过程管理的要求是否形成了文件并批准实施?
《质量环境管理手册》有经过审核批准;
√
5.1领导作用和承诺
最高管理者对满足顾客要求有何想法?现以何方式传达满足顾客要求的重要性.
质量方针:全员参与、客户满意、持续改进、精益求精。
√
是否确定了最高管理者的职责,并发布实施?
质量管理体系各部门内部审核检查表
(包含完整检查内容)
1.管理层
2.生产部
3.品质部
4.采购部
5.工程部
6.仓库PMC
7.资材部
8.行政部
9.业务部
内部审核检查表
审核部门
管理层
审核日期
2018-1-17
版本
01
审核员
陪审员
判 定
标准条款
审核内容
审核记录
严重
轻微
观察
OK
上一次内审与最近外审的问题点
无
4.1
是
√
组织是否通过使用质量方针、质量目标、审核结果、数据分析、纠正和预防措施以及管理评审,致力于提高QMS的有效性?
是
√
组织持续改进QMS绩效是否明显?有充分的、可靠的事实或数据对比予以证明?
质量目标达成分析检讨;
√
10.2不合格和纠正措施
1.组织是否建立并保持了“数据分析和改进控制程序”?该程序是否按照标准要求作出以下的规定:
《质量环境管理手册》管理者代表经过任命,并规定了其职责;
√
5.2方针
最高管理者是否建立了公司的质量管理体系方针并形成文件?
质量方针:全员参与、客户满意、持续改进、精益求精。
√
ISO17025-2017管理体系四阶记录-常用表单(实例)

IS017025-2017体系四阶记录-所有表格清单(实例)序号记录名称文件编号1 质量目标实现检查表……………………………………………QRD0201-20212 质量目标完成情况统计表………………………………………QRD0202-20213 文件发放审批表…………………………………………………QRD0301-20214 文件修改记录表…………………………………………………QRD0302-20215 文件发放回收登记表……………………………………………QRD0303-20216 文件修改通知……………………………………………………QRD0304-20217 文件销毁记录……………………………………………………QRD0305-20218 测量及数据处理软件评审表……………………………………QRD0306-20219 计算机软件、数据修改申请表…………………………………QBD0307-202110 泄密情况处置表…………………………………………………QRD0308-202111 质量监督记录表…………………………………………………QRD0309-202112 质量监控计划表…………………………………………………QRD0310-2021 12 质量监控评审报告………………………………………………QRD0311-202114 技术规范查新记录………………………………………………QRD0312-202115 文件定期审查表…………………………………………………QRD0313-202116 外来文件确认表…………………………………………………QRD0314-202117 受控文件一览表…………………………………………………QRD0315-202118 文件修改申请表…………………………………………………QRD0316-202119 要求、标书和合同评审表………………………………………QRD0401-202120 计量器具检定/校准合同………………………………………QRD0402-202121 校准/检测分包方评审表………………………………………QRD0501-202122 校准/检测分包协议……………………………………………QRD0502-202123 校准/检测分包情况登记表……………………………………QRD0503-202124 采购申请表………………………………………………………QRD0601-202125 采购计划表………………………………………………………QRD0602-202126 供应商评价表……………………………………………………QRD0603-202127 合格供应商登记表………………………………………………QRD0604-202128 材料验收领用单…………………………………………………QRD0605-2021第1页共4页序号记录名称文件编号29 消耗材料领用单…………………………………………………QRD0606-202130 客户信息反馈表…………………………………………………QRD0701-202131 客户满意度调查表………………………………………………QRD0702-202132 投诉登记表………………………………………………………QRD0801-202133 投诉处理报告……………………………………………………QRD0802-202134 纠正和预防措施要求表…………………………………………QRDl001-202135 改进、纠正和预防措施实施表…………………………………QRDl002-202136 预防措施制定、执行、监控计划表……………………………QRDl003-202137 质量记录登记表…………………………………………………QRDl301-202138 文件借阅登记表…………………………………………………QRDl302-202139 会议记录…………………………………………………………QRDl302-202140 内部审核计划表…………………………………………………QRDl401-202141 内审实施计划表…………………………………………………QRDl403-202142 内审员委派表……………………………………………………QRD1402-202143 内部审核检查表…………………………………………………QRDl403-202144 内部审核报告……………………………………………………QnDl404-202145 不符合报告………………………………………………………QRDl405-202146 管理评审计划表…………………………………………………QRDl501-202147 管理评审通知单…………………………………………………QRDl502-202148 管理评审报告……………………………………………………QRDl503-202149 员工技术履历表…………………………………………………QRDl70l-202150 人员培训计划表…………………………………………………QRDl702-202151 人员培训记录表…………………………………………………QRDl703-202152 人员考核计划表…………………………………………………QRD1704-202153 人员考核记录表…………………………………………………QRDl705-202154 实验室环境监控记录(恒温室)………………………………QRDl801-202155 实验室环境监控记录(检测室)………………………………QRDl802-202156 检定/校准/检测方法确认表…………………………………QRDl901-2021第2页共4页序号记录名称文件编号57 计量器具现场校准/检定委托单………………………………QRDl902-202158 定量包装商品样品验收、退样登记表…………………………QRDl903-202159 产(商)品抽样单………………………………………………QRDl904-202160 偏离许可申请审批表……………………………………………QRD1905-202161 购置仪器设备申请表……………………………………………QRD2001-202162 仪器设备验收报告………………………………………………QRD2002-202163 仪器设备使用记录………………………………………………QRD2003-202164 仪器设备报废/停用申请表……………………………………QRD2004-202165 仪器设备维修申请表……………………………………………QRD2021-202166 新项目(扩项)申请表…………………………………………QRD2006-202167 新项目(扩项)评审表…………………………………………QRD2007-202168 新项目(扩项)验收表…………………………………………QRD2021-202169 更新标准、规程能力评审表……………………………………QRD2009-202170 能力分析表………………………………………………………QBD2010-202171 标准物质一览表…………………………………………………QRD2011-202172 仪器设备使用授权表……………………………………………QRD2012-202173 样品存贮条件记录表……………………………………………QRD2013-202174 仪器设备一览表…………………………………………………QRD2014-202175 仪器设备领(借)用登记表……………………………………QRD2015-202176 仪器设备维护保养记录…………………………………………QRD2016-202177 仪器设备档案卡…………………………………………………QRD2017-202178 周期检定/校准计划实施记录…………………………………QRD2101-202179 仪器设备期间核查计划表………………………………………QRD2102-202180 运行检查记录……………………………………………………QRD2102-202181 计量产品检验抽样单……………………………………………QRD2201-202182 计量器具校准/检定委托单……………………………………QRD2301-202183 样品标识…………………………………………………………QRD2302-202184 检定/校准/检测结果异常情况记录表………………………QRD2401-2021第3页共4页序号记录名称文件编号85 实验室比对、能力验证计划实施记录…………………………QRD2402-202186 能力验证(比对)计划及方案…………………………………QRD2502-202187 能力验证(比对)报告…………………………………………QRD2502-202188 证书/报告发放登记表………………………………………… QRD250l-202189 证书/报告修改记录…………………………………………… QRD2502-2021第4页共4页质量目标实现检查表质量目标完成情况统计表QRD0202-2021编制:审核:批准:日期:文件发放审批表QRD0301-2021文件修改记录表文件发放回收登记表文件修改通知文件销毁记录测量及数据处理软件评审表计算机软件、文件、数据修改申请表泄密情况处置表质量监督记录表质量监控计划表质量监控评审报告技术规范查新记录注:最新打√、非最新打×审核:查新:日期:文件定期审查表外来文件确认表受控文件一览表文件修改申请表要求、标书和合同评审表QRD0402-2021计量器具检定/校准合同甲方(委托方):联系人:联系电话:乙方(受委托方):联系人:联系电话:根据《中华人民共和国计量法》、《中华人民共和国计量法实施细则》等法律、法规的要求,甲方为确保单位内部质量管理体系的正常运行,保证计量器具的受检率,将需要检定/校准的计量器具委托乙方进行检定/校准。
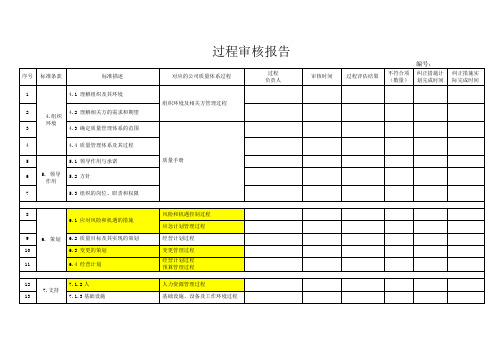
ISOTS22163:2017过程审核报告
44
8.5.4 防护
产品防护控制过程
45
仓储管理过程
46
8.5.5 交付后活动
售后服务管理过程
47
8.5.6 更改控制
变更管理过程
48
8.5.7 生产计划
生产计划控制过程
49
8.6 产品和服务的放行
产品检验控制过程
50
8.7 不合格输出的控制
不合格输出控制过程
51
8.8 RAMS&LCC
人力资源管理过程
13
7.1.3基础设施
基础设施、设备及工作环境过程
14
7.1.4 过程运行环境
15
7.1.5监视和测量资源
监视和测量设备控制过程
16
7.1.6组织的知识
知识管理过程
17
7.2 能力
人力资源管理过程
18
7.3 意识
19
7.4 沟通
沟通管理过程
20
7.5 成文信息
文件管理过程
21
记录管理过程
22
8.运行
8.1 运行的策划和控制
项目管理过程
23
8.1.1 过程转移和外包的策划
外包过程
24
8.1.2 投标管理
投标管理过程
25
8.1.3 项目管理
项目管理过程
26
8.1.4 配置管理
配置管理过程
27
8.1.5 变更管理
变更管理过程
28
8.2 产品和服务的要求
产品和服务要求评审过程
29
8.2.1 顾客沟通
5
5. 领导作用
5.1 .3 组织的岗位、职责和权限
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
我司承诺以上说明及提交的随附资料真实、合法、完整、有效,并承担相应法律责任! 单位公章:
日 期:20 年 月 日
填表说明:1.表格中“有/无”栏请根据手册情况相应填写“Y”或“N”; 2.表格中“处置方式”栏请根据实际处置情况填写“补税”、“整改”或“说明原因”; 3.表格中“情况说明”栏请针对报核手册出现异常情况的具体原因进行解释说明; 4.如情况说明过长无法填入“情况说明”栏,请在“是否另加附页”栏填“Y”后另加附页并加盖公章,否则此栏不填。
附件1
手册报核情况说明与按工艺损耗率折算数量不一致 3 成品退换贸易方式项下进出口数量不平衡 4 申报单耗超国家一级单耗标准 5 实际进口保税料件金额大于实际出口总金额 6 首次成品出口申报日期早于首次料件进口日期 7 末次成品出口申报日期早于末次料件进口日期 8 未在规定期限内向海关报核 9 进口料件总重量大于出口成品总重量 10 未申报残次品 11 其他需要说明的事项 企业经办人签字: 手册有效期: 有/无 处置 方式 情况说明 是否另 加附页
