第十二章湿空气
工程热力学第12章混合气体和湿空气

4
平均摩尔质量, 折合摩尔质量
pV mRg,eqT MeqRg,eq R
平均气体常数, 折合气体常数
(Mv)0 22.4103m3 / mol
neq Σni
neqMeq niMi
理想气体混合物可作为具有Rg,eq、Meq的“某种”理想气体。
第12章开篇
第十二章 混合气体和湿空气
Gas mixtures and moist air
? ★ 神舟×号飞船发射前1天下午来自发射场的电话
气体中含有杂质水蒸气,按设计总压0.1MPa时含量在××以 下,现场验收总压 x MPa,测试数据为┄,气体合格否
★ 冷却塔操作人员的疑惑
? 某次数据记载:
冷水温度低于湿 空气入口温度
pa
p pv
p
d汽膜 d主流
25
26
12-4 湿空气的焓-湿图(psychrometric chart)
一、湿空气的焓
h
H ma
maha mvhv ma
ha
dhv
kJ/kg干空气 kJ/kgDA
h 1.005t d
25011.86t
kJ/kgDA
C
kg/kgDA
C
hv 25011.8903t hv 25011.842t hv 25011.964t
t/ C
1 10
20 30
ps / kPa 0.6556 1.2279 2.3385 4.2451
如 pv = 0 .656 6 kPa,1℃时 pv = ps,无吸湿能力
10℃时pv < ps,有吸湿能力。
21
第12章-理想气体混合物及湿空气-理想气体混合物部分.

p, T
n= n1+ n2+ ┅ +ni + ┅ + nn V=V1+ V2+ ┅ + Vi+ ┅ + Vn
V Vi
理想气体混合物的总体
积等于各组成气体分体积之 和,称为亚美格(Amagat)分 体积定律
Vi V
ni n
xi
或 Vi xiV
三、wi、xi、i的转算关系
xi i
质量kg
m mi
摩尔数kmol
n ni
容积m3
V Vi
相对成分 相对成分=
分量 总量
质量分数:
wi
mi m
,
wi 1
摩尔分数:
xi
ni n
,
xi 1
体积分数:
i
Vi V
,
i 1
Vi为分体积
2、混合气体折合摩尔质量
Meq xiMi
3、混合气体的折合气体常数
第十二章 理想气体混合物
§12-1 理想气体混合物
假定: 1.混合气体内部无化学反应,成分不变; 2.各组元气体都有理想气体的性质, 3.混合后仍具有理想气体的性质; 4.各组元气体彼此独立,互不影响。
一、混合气体的折合摩尔质量及折合气体常数
1、混合气体成分的几种表示方法:
绝对成分
项目
混合气体 第i种组成气体
xi
M eq Mi
wi
xi
Rg ,i Rg ,eq
wi
四、混合气体的比热容、热力学能、焓和熵
1、比热容
c wici Cm xiCm,i C iCi
沪科版九年级物理第十二章第三节汽化与液化课件

第十二章 温度与物态变化
三、汽化和液化
在这两种情况下,水在物态变化上有什 么相同点?有什么不同点? 都是水变成水蒸气,是汽化现象。
两种方式:沸腾和蒸发。
1.沸腾:
加盖烧杯 温度计
在一定温度下 在液体内部和表面同 时发生的
石棉网 铁架台
剧烈的 汽化现象。
观察水沸腾的装置
酒精灯
水的沸腾
提出问题
沸点与气压有关系,而且实验时 各种仪器的精密度不一样。
今天用的温度计是酒精 还是煤油温度计? 煤油温度计。
因为在标准大气压下,酒精的沸点 是78℃,而煤油的沸点是150℃,所以 应该用煤油温度计测量水的温度。
2.蒸发
日光下的湿衣服,温度没有达到水 的沸点也会变干。
在任何温度下
只在液体的表面发生 的 缓慢的 汽化现象。
哪些因素能够影响蒸发的快慢?
挂在屋里干得快, 还是放在太阳下 干得快呢?
太阳下
影响蒸发快慢的因素:
液体的温度
温度高, 蒸发得快。
温度低, 蒸发的慢。
折叠着放在太阳下 晒还是撑开了晒?
撑开
影响蒸发快慢的因素:
液பைடு நூலகம்的温度
温度高, 蒸发得快。 温度低, 蒸发的慢。 表面积大, 蒸发得快。
液体的表面积
酒精蒸发吸收手背以及周围的热量。
2.把酒精反复涂在温度计的玻璃泡上, 用扇子扇,温度计读数有什么变化? 如果温度计上不涂酒精,用扇子扇,温度 计读数会变化吗? ①温度计读数先下降后上升。 ②温度计读数不变。
实验表明:
液体在蒸发过程中吸热,致使液
体和它依附的物体温度下降。
刚从水中出来,感觉特别冷 天热时,狗常把舌头伸出来
3.下列关于液体沸腾时的特点说法不正确的是 ( C ) A. 液体沸腾时温度保持不变 B. 液体沸腾时需要吸热 C. 沸腾是只发生在液体内部的一种汽化现象 D. 水沸腾时的温度不一定是100℃
工程热力学与传热学12)_湿空气

以及理想气体摩尔成分xv与分压力pv的 关系,相对湿度可以表示为:
pv vs v mv xv ps vv s ms xs
三、饱和蒸汽压、露点、绝热饱和温度
未饱和湿空气达到饱和有三种典型的途径:
1、温度不变的情况下,水 分向空气中蒸发,蒸汽 的分压力增加,可以达 到饱和空气状态,如图 中定温过程A-C。达到 饱和时,蒸汽分压力就 是对应此空气温度的饱 和蒸汽压力ps。
水蒸气饱和压力
• 的变化范围为 0~1(0%~100%,对
于饱和空气,其相对湿度为1或100%)
• 相对湿度 愈小,表明什么? • 相对湿度 愈小,表示空气中水蒸气离 饱和状态越远,即越干燥,此时空气吸 收水分的能力越强;反之空气愈潮湿, 吸湿能力越弱。★
根据水蒸气的理想气体状态方程: RvT RvT pv ps vv vs 和湿空气中水蒸气组元的状态方程: mv pv V RvT
绝热
四、湿空气的含湿量d
定义:1kg干空气所携带的水蒸气质量,称 “含湿量”
水蒸气的摩尔质量 =18.016×103kg/mol
由分压力定律可知:理想 气体混合物中各组元的摩 尔数之比,等于其分压力 之比
kg kg ( 干空气)
mv M v nv d ma M a na
干空气的摩尔质量 =28.97×103kg/mol
当我们给盛有空气的密闭容器加热的时候,则其压强当然也会 增大.而对大气来说情况就不同了.当某一区域的大气温度因某种 因素而升高时,必将引起空气体积的膨胀,空气分子势必要向周围 地区扩散.温度高,气体分子固然会运动得快些,这将成为促进压 强增大的因素.但另一方面,随着温度的升高,气体分子便向周围 扩散,则该区域内的气体分子数就要减少,从而形成一个促使压强 减小的因素.而实际的情况乃是上述两种对立因素共同作用的结 果.至于这两种因素中哪个起主要作用,我们不妨来看一看大陆及 海洋上气压随气温变化的实际情况.我们说,夏季大陆上气温比海 洋上高,由于大陆上的空气向海洋上扩散,而使大陆上的气压比海 洋上低;冬季大陆气温比海洋上低,由于海洋上空气要向大陆上扩 散,又使大陆上气压比海洋上高.而由此可见,在温度变化和分子 扩散两个因素中,扩散起着主要的、决定性的作用.应当指出,这 里所说的扩散,是指空气的横向流动.因为由空气的纵向流动并不 能改变竖直气柱的重量(有的文献②把因温度而产生的气压变化说 成是空气沉浮的结果,这是不妥的),因而也就不能改变大气的压 强(对重力加速度g因高度变化而产生的影响完全可以忽略).
北京科技大学研究生考试初试-871工程热力学大纲

考试科目名称:871工程热力学《工程热力学》考试大纲工程热力学课程是热能与动力工程、建筑环境与设备专业的一门重要技术基础课,它的教学目的与任务是:让学生学习关于能量守恒与转换的理论基础,使学生牢固地掌握工程热力学的基本理论、基本知识和相应的热工分析、计算能力,并进一步得到基本技能的训练。
为学习专业课提供充分的理论准备,也为学生以后解决生产实际问题和参加科学研究打下必要的理论基础。
其考试大纲内容如下:一、第一章基本概念要求熟练掌握:系统,平衡状态和状态参数,温度温标,压力,状态方程,准静态过程和可逆过程,循环,功和热量;透彻理解以下的基本概念:热力系统,热力学状态、平衡状态、准静态过程、可逆过程和不可逆过程、功与热量。
二、第二章热力学第一定律要求熟练掌握热力学第一定律基本表达式——基本能量方程,总能,热力学能,焓,膨胀功,技术功,热力学第一定律的第一解析式和稳定流动能量方程式及其应用,循环功之间及循环净功与循环净热量之间关系,循环热效率概念与计算公式;透彻理解以下概念:热力学第一定律的实质—能量守衡与转换定律在热现象中的应用,能量方程的内在联系与共性,热变功的实质。
会进行功和热量的计算,以及功和热量在p-v图和T-s图上的表示。
三、第三章气体和蒸汽的性质要求熟练掌握理想气体和实际气体的概念、理想气体状态方程、理想气体的比热容和热力学能、焓、熵的定义、计算;水蒸气的性质:水蒸气的饱和状态、饱和温度、饱和压力、饱和湿蒸汽、干度、三相点,水蒸气状态的确定。
四、第四章气体和蒸汽的基本热力过程要求熟练掌握理想气体的基本热力过程:定温、定压、定容、定熵和多变过程的过程方程、参数变化和过程中功及热量的计算及其p-v图和T-s图。
水的定压加热汽化过程及其在p-v图和T-s上的表示;会计算水蒸气定压过程的热量,水蒸气绝热过程的功。
五、第五章热力学第二定律熟练掌握热过程的方向性、热力学第二定律的表述;卡诺循环和卡诺定理、克劳修斯积分不等式、熵流和熵产、熵方程、孤立系统的熵增原理;作功能力、作功能力损失与熵产和火用平衡方程。
工程热力学 第十二章 理想气体混合物及湿空气 图文

平均气体常数, 折合气体常数
理想气体混合物
u
cv
t2 t1
(t2
t1 )
h
cp
t2 t1
(t2
t1 )
cp cv Rg,eq
因此,把理想气体混合物看出是气体常数和摩 尔质量分别为Rg,eq和Meq的某种假想气体。
pV m混 Rg,eqT
南京航空航天大学
混合气体的分压力定律
分压力——组分气体处在与混合气体相同容积、 相同温度单独对壁面的作用力。
1 ln 2
pN2 ,2 pB1
南京航空航天大学
2R ln 1 2R ln 2 2
湿空气与干空气
地球上的大气由氮、氧、氩、二氧化碳、水蒸 气及极微量的其他气体组成。水蒸气以外的所有组 成气体称为干空气,看作是不变的整体。湿空气是 指含有水蒸气的空气。
南京航空航天大学
成分 O2 N2 Ar CO2
pV nRT p1V n1RT piV ni RT pmV nm RT
南京航空航天大学
Vpi RT ni nRT
p pi 道尔顿分压力定律
混合气体的分体积定律
分体积——组分气体处在与混合气体同温、 同压单独占有的体积。
pV nRT
pV1 n1RT pVi ni RT
pVm nmRT
T
ps
干空气 +
过热水蒸气
pv
pv < ps(T)
南京航空航天大学
加入水蒸气,pv
s
未饱和湿空气和饱和湿空气
2、饱和湿空气
干空气 +
饱和水蒸气
T
ps
pv = ps(T)
南京航空航天大学
湿空气
分析湿空气时假定: 1)把气相混合物看作是理想气体混合物; 2)当蒸汽凝结成液相或固相时,液相或固相
初中物理九年级第十二章《温度与物态变化》知识重点梳理知识点拨

第十二章温度与物态变化●学习要求1.知道摄氏温度。
记住在1个标准大气压下冰水混合物和沸水的温度。
了解液体温度计的构造和原理。
会用常见温度计测量温度。
会使用体温计。
了解人的正常体温。
了解一些生活环境中的温度值。
2.知道固体、液体和气体三种物态。
知道物态变化。
能列举自然界和生活中不同状态的物质。
3.知道熔化和凝固现象和条件。
记住1个标准大气压下冰的熔点和水的凝固点。
了解晶体和非晶体,了解它们的熔化和凝固图像。
了解熔化和凝固过程中的吸热和放热。
解释熔化和凝固的有关现象。
4.知道汽化和液化现象。
知道蒸发和沸腾是汽化的两种方式。
知道影响蒸发快慢的因素。
探究水沸腾的条件及温度变化的特点。
记住1个标准大气压下水的沸点。
了解沸点与气压的关系。
了解汽化和液化过程中的吸热和放热。
解释汽化和液化的有关现象。
5.了解升华和凝华现象。
了解升华和凝华过程中的吸热和放热。
解释升华和凝华的有关现象。
6.了解合理利用和保护水资源的重要性,有节水意识,树立可持续发展的意识。
●知识点拨第一节温度与温度计一、物态变化物质有三种状态,分别为固态、液态和气态。
物质由一种状态向另一种状态的变化称为物态变化。
二、温度(1)温度表示物体的冷热程度,常用单位:摄氏度,国际单位:开尔文,热力学温度(T)和摄氏温度(t)的换算关系是T=273.15+t。
(2)人的正常体温是37℃;水在0℃时可能会结冰。
◎常见的一些温度值——冰的熔点00C,对人体舒适的环境温度250C,人体正常体温370C,在1个标准大气压下水沸腾的温度定为1000C,在1个标准大气压下将纯净的冰水混合物的温度定为00C。
三、温度计(1)作用:测量物体的温度。
(2)常用温度计是根据液体的热胀冷缩原理制成的。
(3)常见的液体温度计有温度计、寒暑表和体温计。
(4)液体温度计的使用:做到四“会”。
①会“选”:使用前首先观察它的量程、分度值和零刻度。
②会“放”:测量时温度计的玻璃泡应被包围在被测物体内;测量液体温度时,温度计的玻璃泡要浸没在被测液体中,但不能接触容器的壁和容器的底部。
化工原理--第十二章 干燥

二、物料衡算
L, t0 , H0
新鲜空气
预热器 L, t1 , H1 废气 L, t2 , H2
干 燥 器
产品 G2, w2, (X2)
湿物料 G1, w1, (X1),
符号说明: L:绝干空气流量,kg干气/s; G1、G2:进、出干燥器的湿物料量,kg湿料/s; Gc:湿物料中绝干物料量,kg干料/s。
式中:r0——0℃时水蒸汽汽化潜热,其值为2492kJ/kg。
例12-1教材p/225
(五)干、湿球温度 (1)干球温度:在空气流中放置一支普通温度 计,所测得空气的温度为t,相对于湿球温度而 言,此温度称为空气的干球温度。 (2)湿球温度:如图所示,用水润湿纱布包裹 温度计的感湿球,即成为一湿球温度计。将它 置于一定温度和湿度的流动的空气中,达到稳 态时所测得的温度称为空气的湿球温度,以tw表 示。
第四节 干燥速率和干燥时间
对于物料的去湿过程经历了两步:首先
是水分从物料内部迁移至表面,然后再由表 面汽化而进入空气主体。故干燥速率不仅取 决于空气的性质及干燥操作条件,而且还与 物料中所含水分的性质有关。
一、物料中的水分 根据物料所含水分能否用干燥的方法除去可分为平 衡水分与自由水分。 平衡水分:等于或小于平衡含水量,无法用相应空 气所干燥的那部分水分。 自由水分:湿物料中大于平衡含水量,有可能被该 湿空气干燥除去的那部衡算
一、湿物料中含水率的表示方法 1.湿基含水量w
湿物料中水分的质量 kg水/kg湿料 w 湿物料总质量
2.干基含水量X
湿物料中水分的质量 kg水/kg绝干物料 X 湿物料中绝干物料的质 量
3.二者关系
X w 1 X
或
w X 1 w
说明:干燥过程中,湿物料的质量是变化 的,而绝干物料的质量是不变的。因此,用 干基含水量计算较为方便。
工程热力学名词解释

1.第一章 基本概念及定义 2.热能动力装置:从燃料燃烧中得到热能,以及利用热能所得到动力的整套设备(包括辅助设备)统称热能动力装置。
3.工质:热能和机械能相互转化的媒介物质叫做工质,能量的转换都是通过工质状态的变化实现的。
4.高温热源:工质从中吸取热能的物系叫热源,或称高温热源。
5.低温热源:接受工质排出热能的物系叫冷源,或称低温热源。
6.热力系统:被人为分割出来作为热力学分析对象的有限物质系统叫做热力系统。
7.闭口系统:如果热力系统与外界只有能量交换而无物质交换,则称该系统为闭口系统。
(系统质量不变) 8.开口系统:如果热力系统与外界不仅有能量交换而且有物质交换,则称该系统为开口系统。
(系统体积不变) 9.绝热系统:如果热力系统和外界间无热量交换时称为绝热系统。
(无论开口、闭口系统,只要没有热量越过边界) 10.孤立系统:如果热力系统和外界既无能量交换又无物质交换时,则称该系统为孤立系统。
11.表压力:工质的绝对压力>大气压力时,压力计测得的差数。
12.真空度:工质的绝对压力<大气压力时,压力计测得的差数,此时的压力计也叫真空计。
13.平衡状态:无外界影响系统保持状态参数不随时间而改变的状态。
充要条件是同时到达热平衡和力平衡。
14.稳定状态:系统参数不随时间改变。
(稳定未必平衡) 15.准平衡过程(准静态过程):过程进行的相对缓慢,工质在平衡被破环后自动恢复平衡所需的时间很短,工质有足够的时间来恢复平衡,随时都不致显著偏离平衡状态,那么这样的过程就称为准平衡过程。
它是无限接近于平衡状态的过程。
16.可逆过程:完成某一过程后,工质沿相同的路径逆行回复到原来的状态,并使相互作用所涉及的外界亦回复到原来的状态,而不留下任何改变。
可逆过程=准平衡过程+没有耗散效应(因摩擦机械能转变成热的现象)。
17.准平衡与可逆区别:准平衡过程只着眼工质内部平衡;可逆过程是分析工质与外界作用产生的总效果,不仅要求工质内部平衡,还要求工质与外界作用可以无条件逆复。
化工原理下 第十二章 干燥

湿空气的饱和湿度是温度的函数。
12.2.1 湿空气的性质
2.相对湿度 在一定总压下,湿空气中水汽分压p与同温度下纯水的饱 和蒸汽压ps之比,称为相对湿度,用 φ表示,即
相对湿度代表空气中水汽含量的相对大小。当p=0时,φ=0, 表示湿空气中不含水分,为绝干空气。当p=ps时,φ=1, 表示湿空气被水汽饱和,为饱和湿空气,这种湿空气不能用 作干燥介质。可见,φ越小,空气的吸湿能力越大。
12.2.1 湿空气的性质
一、湿空气中水蒸汽含量的表示方法 在干燥过程中,湿空气中水蒸汽含量的表示方法有两种: 1.湿度 又称湿含量,是湿空气中水汽的质量与绝干空气质量之比 (质量比),用H表示,单位kg水汽/kg干空气。
12.2.1 湿空气的性质
即
当湿空气中的水汽分压p等于该空气温度下纯水的饱和 蒸汽压ps时,湿空气再不能吸收水分,此时湿空气达到饱和 状态,其湿度称为饱和湿度,用Hs表示:
12.2.2 湿空气的湿度图
对于不饱和湿空气,组分数C为2,相数φ为1,根据相 率,可知其自由度:F = C-φ+2 = 2-1+2 = 3 在总压一定的条件下,只要再任意规定两个任意参数, 湿空气的状态即被唯一确定。这两个任意参数一般定为:湿 空气的温度和湿度。 湿度图包括五种线: 1、等干球温度线 3、等相对湿度线
12.1 概述
干燥法去湿的分类: 1、按供热方式分: (1)传导干燥 热能通过传热壁面以传导的方式传给物料,产生的湿分 蒸汽被气相(又称干燥介质)带走。如:纸制品铺在热滚筒上 进行干燥。 (2)辐射干燥 由辐射器产生的辐射能以电磁波的形式到达物料表面, 被物料吸收而重新变为热能,从而使湿份气化。如:红外线 干燥自行车表面油漆。 (3)介电加热干燥 将需要干燥的物料置于高频电场中,电能在物料中转变 成热能,使液体很快升温而气化。这种加热过程发生在物料 内部,故干燥速率较快。如:微波炉
热力学复习大纲

复习大纲绪论重点:了解工程热力学的主要内容及研究方法第一章基本概念及定义重点:工质热力系统、边界、热力系统的类型工质的热力学状态、参数 6个基本状态参数状态方程、坐标图平衡状态、准平衡(静态)过程过程功和热量、热力循环第二章热力学第一定律重点:实质热力学能、总能、推动功流动功、焓第一定律的基本能量方程热量的符号、功量的符号开、闭口系统能量方程第三章气体和蒸气的性质重点:理想气体状态方程比热容、热力学能、焓和熵水蒸汽1点2线3区 5态第四章气体和蒸气的基本热力过程重点:可逆多变过程、定温、定压、定容、定熵过程综合分析第五章热力学第二定律重点:表述卡诺循环克劳休斯积分熵方程孤立系统熵增原理火用第六章实际气体的性质及热力学一般关系式一般了解:范德瓦尔方程对应态原理通用压缩因子图麦克斯韦关系热系数热力学能、焓和熵、比热容的一般关系式第七章气体与蒸气的流动重点:稳定流动的基本方程:连续性方程、能量方程、过程方程、声速方程滞止参数的意义及其计算促使流速改变的条件:力学条件几何条件喷管形状的确定及计算临界压力比背压变化对喷管流动、出口参数的影响第八章压气机的热力过程重点:余隙容积产生、影响多级压缩、中间冷却第九章气体动力循环重点:混合加热理想循环热效率定压、定容加热理想循环热效率比较及分析燃气轮机装置循环热效率提高燃气轮机循环热效率的措施第十章蒸汽动力装置循环重点:朗肯循环由来热效率分析再热循环热效率回热循环热效率第十一章制冷循环重点:压缩空气制冷循环组成、设备、制冷系数压缩蒸汽制冷循环组成、设备、制冷系数两种循环的异同热泵循环第十二章理想气体混合物及湿空气重点:混合气体分压力、分体积定律成分:质量分数、摩尔分数、体积分数,三者的关系湿空气、干空气饱和、不饱和、露点相对湿度、含湿量干、湿球温度h-d图及其应用复习题(题中涉及的有关水蒸汽的数据,考试时均会给出,不用自己查表。
复习题中所需要的数据,需要自己找相关图表查数)习题:课本上的例题、课后思考题、留的作业题第一章基本概念及定义1、热力平衡状态2、准静态过程3、热力系统4、功量与热量第二章热力学第一定律1、热力学第一定律2、技术功3、课后思考题2-4、2-5.(P56)4、一蒸汽锅炉每小时生产P1 = 20 bar , t1= 350℃的蒸汽10吨,设锅炉给水温度t2= 40℃,锅炉效率ηK = 0.78,煤的发热值QL= 29700 KJ/Kg,求锅炉的耗煤量。
12第12章理想气体混合物及湿空气详解

Rg,eq
R M eq
pV mi RgiT mR g,eqT
Rg,eq wi Rgi
由摩尔成分的定义可得:
ni mi M i M eq xi wi n m M eq M i
考虑到:
R Mi Rg,i M eq Rg,eq
Rg,i Rg,eq
可见,摩尔分数不仅取决于质量分数,还和各组分气体的气体常 数(或摩尔质量)有关。
Rg ,eq Rg,i wi Rg,H2 wH2 Rg,CO2 wCO2 4.124 kJ/(kg K) 0.1 0.189 kJ/(kg K) 0.9 0.5825 kJ/(kg K)
干空气的分压力 pa , 水蒸气的分压力 pv p = pa + pv
三、相对湿度
湿度—空气的潮湿程度,与空气中所含水蒸气量有关。
1、绝对湿度(absolute humidity)
每立方米湿空气中水蒸气的质量,即湿空气中水蒸气的密度ρv , 单位kg/m3 1 pv 1 pv vv RgvT v 1) v 理想气体 vv vv RgvT 2)
xCO2 xH2
可见,质量分数高的组分,摩尔分数未必高。
12-2 混合物的比热容、热力学能、焓和熵
一、比热容 混合气体吸收的总热量 Q
Q
i
1kg混合物吸收的热量应等于各组分吸收热量之和,即
q wi qi
根据比热容的定义式得
c
q
dT
(wi
qi
dT
) wi ci
dpi dpi dT xi R Rxi T pi pi
0 pi2 S n混 S混m 2 Rxi ln pi1
工程热力学与传热学12)_湿空气解读

示。
绝热
四、湿空气的含湿量d
定义:1kg干空气所携带的水蒸气质量,称
“含湿量”
由分压力定律可知:理想
水蒸气的摩尔质量 =18.016×103kg/mol
气体混合物中各组元的摩 尔数之比,等于其分压力
之比
d
mv ma
M vnv M ana
kg kg (干空气)
干空气的摩尔质量 =28.97×103kg/mol
六、 冷却塔
利用蒸发冷却, 将热水降温,获 得工业用循环水。
图书例
温度、湿度与大气压强
物理学告诉我们:“大气压的变化跟天气有密切的关 系.一般地说,晴天的大气压比阴天高,冬天的大气压比夏 天高.”对这段叙述可归结为温度、湿度与大气压强的关系 问题.
我们通常所称的大气,就是包围在地球周围的整个空气 层.它除了含有氮气、氧气及二氧化碳等多种气体外,还含 有水汽和尘埃.我们把含水汽很少(即湿度小)的空气称 “干空气”,而把含水汽较多(即湿度大)的空气称“湿空 气”.不要以为“干”的东西一定比“湿”的东西轻.其实, 干空气的分子量是28.966,而水汽的分子量是18.016,故干 空气分子要比水汽分子重.在相同状况下,干空气的密度也 比水汽的密度大.水汽的密度仅为干空气密度的62%左右.
随t 增大斜率增大。
h cp,at d (hc cp,vt ) h d t hc cp,vt
湿空气
4、等相对湿度线(等 )
• 定 线是一组向上凸的曲线群。
• 露点td 是湿空气冷却到=100%时的温
度。因此含湿量 d 相同,状态不同的湿 空气具有相同的露点。
湿空气
5、水蒸气分压力线
由于地球上的大气总量是基本上恒定的.当一个地区 的气温增加时,往往伴随着另一个地区温度的降低,这 就为高温处的空气向低温处扩散带来了可能.而扩散的 结果常常是高温处的气压比低温处低.当我们生活的北 半球是接受太阳热量最多的盛夏时,南半球却是接受太 阳热量最少的严冬.这时,由于北半球的空气要向南半 球扩散而使北半球的气压较南半球要低.而由于大气总 量基本不变,则此时北半球的气压就低于标准大气压, 南半球的气压当然也就会高于标准大气压.同样,空气 的反方向扩散又会使北半球冬季的气压高于标准大气 压.因而,在北半球,冬季的大气压就会比夏季要 高.当然,大气压的变化是很复杂的,但对科普的说法 作上述解释还是可以的
12工程热力学第十二章 湿空气
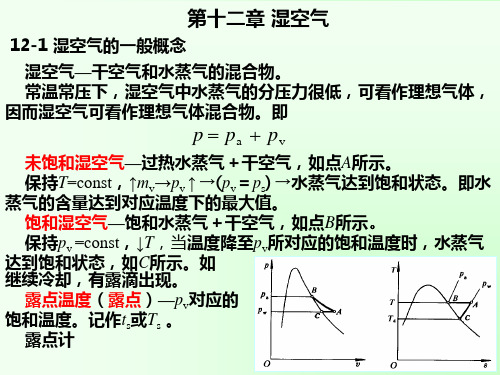
h3 h4 = q + 0.001( d 3 d 4 ) h v
式中: 为冷却介质带走的热量; 为凝结水的比焓. 式中:q为冷却介质带走的热量;hv为凝结水的比焓.
三,绝热加湿过程 在绝热的条件下, 湿空气吸收水分, 在绝热的条件下 , 湿空气吸收水分 , 其 含湿量增加的过程, 含湿量增加的过程 , 称为湿空气的绝热加湿 过程. 过程. 绝热加湿过程中, 绝热加湿过程中 , 单位质量干空气的湿 空气吸收的水分为 d2 - d1 , 湿空气的焓增为 水分带入的能量, 水分带入的能量,即 h2 h1 = 0.001( d 2 d 1 ) h v 式中: 为水的焓. 式中:hv为水的焓.因为水分带入湿空气中的能量0.001(d2-d1) hv 相比很小,可忽略不计, 与湿空气的焓h1,h2相比很小,可忽略不计,即
mv pv ρv = = V Rg, v T ρv = 相对湿度 ρs 说明了吸收水蒸气的能力. ↓→吸收水蒸气的能力 吸收水蒸气的能力↑ 说明了吸收水蒸气的能力. ↓→吸收水蒸气的能力↑,当 =
饱和湿空气) 吸收水蒸气的能力为零. 100% (饱和湿空气)→吸收水蒸气的能力为零. 由理想气体状态方程, 由理想气体状态方程,相对湿度可表示为 pv = ps 相对湿度的测量:毛发湿度计 相对湿度的测量: 干湿球温度计
1212-4
湿空气的热力过程
湿空气热力过程的分析,主要讨论湿空气的状态变化, 湿空气热力过程的分析,主要讨论湿空气的状态变化,及其与 外界的能量交换情况. 外界的能量交换情况. 一,加热过程 加热过程一般在定压条件下完成. 加热过程一般在定压条件下完成. 特征: 特征:湿空气T↑,d=const. 过程线沿定含湿量线向温度升高的方向进行, 过程线沿定含湿量线向温度升高的方向进行, 过程中, 过程中,h↑, ↑. 加热过程中,吸热量等于焓值的增加,即 加热过程中,吸热量等于焓值的增加,
气压传动基础知识

二、理想气体的状态变化过程 1. 等容变化过程(查理定律) p1 p2 常数 T1 T2
2. 等压变化过程(盖-吕萨克定律)
v1 v2 常数 T1 T2
第二节
气体状态方程
二、理想气体的状态变化过程 3. 等温变化过程
p1v1 p2v2 常数
4. 绝热变化过程
p v p v 常数
第二节
气体状态方程
二、理想气体的状态变化过程 4. 多变过程
第二节
气体状态方程
第三节 逻辑运算简介
一、逻辑“或”和逻辑“与”
OR Operation
INPUTS INPUT A LOW 0 LOW HIGH HIGH 0 1 1 INPUT B LOW 0 HIGH LOW HIGH 1 0 1
《气动技术技术》/《气压传动》
主要内容
① 气压传动的基础知识、组成及特点。
② 气动元件,含气源装置、气马达、气缸、气压控制方向 阀、气压控制压力阀、气压控制流量阀和附件,要掌握这 些元件的工作原理、图形符号、结构形式等。 ③ 气动回路实例分析(安装、使用、维护)。
第一章 气压传动基础知识
第一节 空气的物理性质
一、空气的性质 空气的组成 空气的密度和黏度 二、湿空气 绝对湿度 相对湿度 三、气体体积的易变特性
第一章 气压传动基础知识
一、空气的性质
1、空气的组成
第一章 气压传动基础知识
一、空气的性质 相对分子量:
化学式子当中,是拿一个分子质量和一个碳原子的 1/12的比值。 与原子的质量计量一样,分子的质量计量 也先后存在3个量名称:相对分子质量、分子质量和分子 量。众所周知,分子的质量为组成分子的各原子的质量之 和。
工程热力学-第十二章 理想气体混合物及湿空气
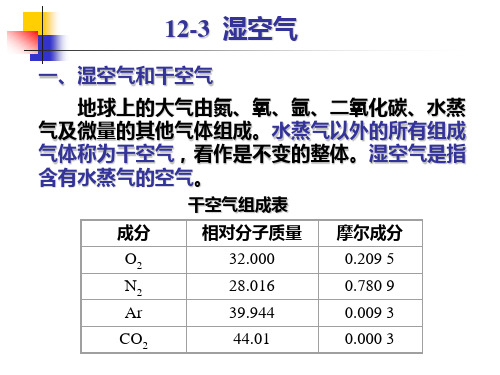
含湿量d
d = 0.622
j
p-
ps j ps
焓-湿图以1kg干空气量的湿空气为基准
注意:h-d 图随 pb 改变而改变
温度范围:-20~50℃,总压力:0.1MPa
h-d 图由下列五种线群组成: 1、等湿线(等d 线)
等d线是一组平行于纵坐标的直线群。
h
d
2、等焓线(等h线)
h = 1.005t + d (2501+ 1.86t )
t
100%
pv
d
6、露点td
pv下饱和湿空 h
气 1
h
td
t
100%
pv
d
温度范围:-20~50℃,总压力:0.1MPa
12-7 湿空气过程及其应用
湿空气热力过程求解主要研究过程中湿空气焓 值及含湿量与温度、相对湿度之间的变化关系;
研究方法:利用稳定流动能量方程和质量守恒 方程,并利用湿空气焓湿图。
露点可用湿度计 或露点仪进行测量 。
湿润的夏天水管上常出现水珠?
干燥的冬天pv小,td< 0.0 oC 结霜 结雾? 整个空气温度降低,水出来的过程
T
pv=0.04bar 大气温度t=30oC d td=28.98oC 冷水管t=20oC
s
12-4 湿空气的状态参数
一、相对湿度
绝对湿度:每立方米湿空气中水蒸气的质量 kg/m3
一般d很小,因此等h线与等t线接近重合。 因此等h线是一组与横坐标轴成135°的直线群。
h 135度 h
d
3、等温线(等t 线)
h = 1.005t + d (2501 + 1.86t )
¶h ¶d
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
h2 kJ/kg
干空气
1.005t2 C d 2 kg/kg干空气 2501 1.86 t2 C
h2 1.005 kJ/(kg K) 10 C 0.007 63 kg/kg干空气 2 501 kJ/kg 1.86 kJ/(kg K) 10 C 29.27 kJ/kg干空气
h v 2501 c pt 2501 1.85t KJ/Kg(水)
h 1.005t d (2501 1.85t ) KJ/Kg(a)
四、 湿空气的比体积:
RgT v (1 d ) P
1 d Rg Rga Rgv 1 d 1 d
50m3的房间内空气 t1=30℃,1 =60%,被等压冷却到t2= 10℃。 已知 pb= 0.1013MPa 。求:1)初态时td,d1及H;2)凝结水量 Δmv;3)放热量Q 。 解:1) 查表
0.016 0 kg/kg干空气 2 501 kJ/kg 1.86 kJ/(kg K) 30 C
H1 ma h1 56.78 kg 71.06 kJ/kg干空气 4 034.8 kJ
2)
t2 td1
pv2 ps2
ps2 1 227.1Pa pv2
i 1
m u m1u1 m2u2 m3u3 ... mnun mi ui
i 1 n mi u ui g i ui i 1 m i 1 n
n
2、混合气体的焓:等于各组成气体焓 之和
H H1 H 2 H 3 ... H n H i
如
t / C
当
1
10
20
30
ps / kPa 0.6556 1.2279 2.3385 4.2451
20 C pv ps 空气未饱和
pv 0.655 6 kPa
1 C
pv ps
空气饱和
空气达成饱和的途径
t 不变,pv 上升,pv = ps(t)
Pv 不变,t 下降,t = ts (pv)
2. 分容积定律(law of partial volume)
分容积——组分气体处在与混合气体同温同压单独 占有的体积。
pV nRT
pV1 n1 RT
pVi ni RT
pVm nm RT
V Vi
pVi RT ni nRT pV nRT 分容积定律
二、理想气体混合物的成分
i 1
n
dP dT dsi c pi Rgi i T pi
dP dT ds wi c pi wi Rgi i T pi
12–3 湿空气
一、干空气和湿空气
地球上的大气由氮、氧、氩、二氧化碳、水蒸气及极微量 的其他气体组成。水蒸气以外的所有组成气体称为干空气, 看作是不变的整体。因此,大气是干空气与水蒸气组成的混 合气体。 一、空气的组成: 湿空气=干空气+水蒸气 二、湿空气的性质(通常由过热水蒸气和干空气组成) 理想气体 1、状态方程:
1.质量分数 wi :
2.体积分数i :
n mi w1 w2 wn wi wi m i 1
Vi i V ni xi : n
1 2 n i
i 1
n
3.摩尔分数
xi
x1 x2 xn xi
i 1
n
4.容积分数和摩尔分数相等
湿空气的状态参数
一 、相对湿度:空气中实际水蒸汽含量与同一温度下饱和空气 所能含水蒸汽量的比值
mv V v ms ms s V P v RvT P v 1 0 0 % P P s s RvT
mv
Pv -水蒸汽分压力,Pa
Ps
-饱和蒸汽压,Pa
s
pv ps
pv ps
3)
Q ma h2 h1 56.78 kg 29.27 71.06 kJ/kg干空气 2 372.58 kJ
mi ni M i Mi Mi wi xi m n M eq M M eq
M i R gi M eq R geq R
xi
R
Mi M eq R gi
R geq
wi xi
Rgeq Rgi
gi
Rgeq
wi
xi 1
Rgeq Rgi wi
12-2理想气体混合物的比热容、热力学能、焓和熵 一、理想气体混合物的比热容
mv1 ma d 57.68 kg干空气 0.016 0 kg/kg干空气 0.91 kg
h1kJ/kg
干空气
1.005t1 C d1kg/kg干空气 (2501 1.86 t1 C )
h1 1.005 kJ/(kg K) 30 C 71.06 kJ/kg干空气
i 1
n
m h m1h1 m2 h2 m3h3 ... mn hn mi hi
n mi h hi g i hi i 1 m i 1 n i 1
n
三、混合气体的熵: 等于各组成气体熵之和
S Si
i 1
n
1千克混合气体
s wi si
二、未饱和湿空气(unsaturated air)和 饱和湿空气(saturated air)
饱和空气:当空气中的水蒸汽含量超过某一限度时(在一定 的温度下,湿空气所含的水蒸汽量有一个最大限度),便有 部分水蒸汽凝结而从空气中析出。这种水蒸气含量达到最大 值时的空气称作饱和空气。 饱和空气 = 干空气 + 干饱和水蒸汽
未饱和空气 = 干空气 + 过热水蒸汽
空气中的水蒸气
过热 t ts pv 空气未饱和
饱和 t ts pv 空气饱和 空气饱和与否取决于t,pv
饱和时:水蒸汽的分压力称为饱和水蒸汽分压力Ps (饱和蒸汽压) 它就是同温度时水的饱和压力。如25摄氏度时对应的是0.0317bar。 饱和蒸汽分压力Ps和饱和温度Ts是一一对应的,知道其一, 可以查得另一个。
三、露点(dew point)
在一定的大气压力下,未饱和的湿空气在含湿量不变的条件 下,冷却到饱和状态时的温度称为露点温度。
湿空气中水蒸气压力pv所对应 的饱和温度,td=ts(pv) 。
当湿空气被冷却时(或与某冷表面接触时), 只要湿空气温度大于或等于其露点温度, 则不会出现结露现象。
12-4
1. 分压力定律(Dalton law of partial pressure) 分压力——组分气体处在与混合气体相同容积、相同 温度单独对壁面的作用力。
pV nRT
p1V n1 RT
piV ni RT
pmV nm RTFra bibliotekp pi
分压力定律
Vpi RT ni nRT pV nRT
第十二章 理想气体混合物及湿空气
12-1理想气体混合物
12-2理想气体混合物的比热容、热力学能、焓和熵 12-3湿空气 12-4湿空气的状态参数 12-5湿球温度和绝热饱和温度 12-6湿空气的焓—湿图 12-7湿空气过程及其应用
12理想气体的混合物及湿空气
12–1理想气体的混合物 一、分压力定律和分容积定律
Paa RaT
气体常数
Pvv RvT
Rv 461J /(Kg.k )
Ra 287J /(Kg.k )
T-湿空气的热力学温度(K)
Ta Tv T
a
P a
RaT
PaV ma RaT
干空气的分压
v P V mv RvT v
水蒸汽的分压
P v
RvT
V-湿空气的总体积(m3)
吸湿 能力 下降
0 1
=0 干空气 0 < < 1 未饱和空气 =1 饱和空气
二、含湿量d (humidity; humidity ratio) 只有干空气的质量,
以1 kg干空气为计算基准
不会随着湿空气的温 度和湿度而改变。
在含有1 kg干空气的湿空气中所含有的水蒸汽质量称为湿 空气的含湿量(湿空气中的水蒸汽质量与干空气质量之比)。 pvV mv v Rg,vT d pv 0.622 ma paV a pa Rg,aT
Va Vv V
2 、干空气与水蒸汽的分压(空气的压力)
空气的压力就是大气压力:
ma RaT mv RvT Pb Pa Pv V V
水蒸气分压力的大小是反映空气中水蒸汽数 量的一个参数
湿空气中的水分含量虽然较少,但它与 干空气却有很大不同,湿空气中水蒸汽的含量 及相态都可能发生变化,大气中发生的雨、雪、 雾、露、雹等自然现象都是由于湿空气中水蒸 汽的相态变化所致。所以在通风、空调等干燥 工程中,不能忽视空气中的水蒸汽。
=0时:绝对干空气 =100%时:饱和空气,没吸湿能力
(2)空气能够容纳水蒸汽的多少与Ps有关,即和温度有关。
一定量的空气温度越高,Ps越大,能够容纳水蒸汽量越多(水 蒸汽分压力越大)。
当Pb不一定时,d和Pv相互不独立。d是温度T和 相对湿度的函数。
三、湿空气的焓 在空气调节中,空气的压力变化很小,可近似 于定压过程,因此可直接用空气的焓变化来度量空 气吸或放热量。 湿空气的焓是指1kg干空气的焓和dkg水蒸汽的 焓的总和
三、混合气体的平均摩尔质量和平均气体常数
平均摩尔质量:混合物的总质量与混合物总摩尔数的比
n
M eq
m n
n M
i 1 i
i
n
xi M i i M i
i 1 i 1
