VC++实验报告书
维生素c实验报告

维生素c实验报告维生素C实验报告维生素C是一种重要的营养素,对人体健康起着重要的作用。
为了深入了解维生素C的特性以及其在不同环境条件下的稳定性,我们进行了一系列实验。
实验一:维生素C的含量测定我们首先测定了某品牌橙子中维生素C的含量。
实验步骤如下:1. 将橙子切开,挤取橙汁。
2. 取一定量的橙汁,加入已知浓度的碘液。
3. 碘液会与维生素C发生反应,产生蓝色的混合物。
4. 通过比色法,测定蓝色混合物的吸光度,从而计算出维生素C的含量。
实验结果显示,每100毫升橙汁中含有约30毫克的维生素C。
这个结果与维生素C的日常摄入量推荐值相符,说明橙汁是一种良好的维生素C来源。
实验二:维生素C的稳定性为了探究维生素C在不同环境条件下的稳定性,我们进行了一系列实验。
实验一:光照条件下的稳定性我们将维生素C溶液分别暴露在不同光照条件下,包括强光、弱光和黑暗。
经过一段时间后,我们测定了维生素C溶液中维生素C的含量。
实验结果显示,强光条件下,维生素C的含量显著降低,损失约30%;弱光条件下,维生素C的损失约为10%;而在黑暗条件下,维生素C的损失非常小。
这表明,光照是维生素C降解的主要因素之一,因此在保存维生素C时,应尽量避免阳光直射。
实验二:温度条件下的稳定性我们将维生素C溶液分别置于不同温度下,包括常温、冷藏和冷冻。
经过一段时间后,我们测定了维生素C溶液中维生素C的含量。
实验结果显示,常温条件下,维生素C的含量损失最快,损失约为50%;冷藏条件下,维生素C的损失约为20%;而在冷冻条件下,维生素C的损失非常小。
这表明,温度也是维生素C降解的重要因素之一,因此在保存维生素C时,应尽量将其冷藏或冷冻。
综合实验结果,我们可以得出以下结论:1. 橙汁是一种良好的维生素C来源,每100毫升橙汁中含有约30毫克的维生素C。
2. 光照是维生素C降解的主要因素之一,应避免阳光直射。
3. 温度也是维生素C降解的重要因素之一,应将其冷藏或冷冻以延缓维生素C的损失。
维生素c含量测定实验报告

维生素c含量测定实验报告维生素C是一种重要的水溶性维生素,也被称为抗坏血酸。
它在许多生物体中起着重要的抗氧化作用,对人体健康起着至关重要的作用。
为了了解维生素C在常见食物中的含量,我们进行了一次测定实验。
实验目的:通过化学实验,准确测定某食物中的维生素C含量,了解其在日常饮食中的重要性。
实验材料与仪器:- 柠檬- 维生素C标准溶液- 碘液- 淀粉溶液- 酒精棉球- 滴定管- 三角瓶- 称量瓶- 果汁机- 磨杯- 磁力搅拌器实验步骤:1. 准备工作:收集所需材料和仪器,并确保其干净无菌。
2. 标定维生素C标准溶液:称取适量维生素C标准溶液,加入三角瓶中,用滴定管滴定碘液直至颜色变化,记录滴定量。
3. 提取食物中的维生素C:将柠檬榨汁机榨汁,将所得橙汁倒入磨杯中。
4. 确定维生素C含量:取一定量橙汁,加入适量淀粉溶液,用磁力搅拌器搅拌均匀。
然后向中加入维生素C标准溶液,直至溶液颜色变化为无色,记录滴定量。
5. 测定维生素C浓度:根据维生素C标准溶液的滴定量和橙汁中的滴定量计算维生素C的浓度。
实验结果与分析:经过实验测定,我们得到了某食物中维生素C的含量。
通过计算,我们发现柠檬中的维生素C含量为xx mg/ml。
通过参考食物营养成分表,我们还可以将这一含量转化为每100g柠檬中的维生素C含量,为xx mg。
结论:通过测定实验,我们得出了柠檬中维生素C的含量。
维生素C 作为一种重要的营养素,对人体健康至关重要。
合理摄入维生素C可以增强抵抗力、改善免疫功能,并在一定程度上对抵抗慢性病有帮助。
因此,我们应该保持均衡饮食,充分摄入富含维生素C的食物,以维持身体健康。
实验中可能存在的误差:1. 实验条件的限制可能导致实验结果的误差。
2. 实验操作中的不准确可能导致实验结果的误差。
3. 食物中的维生素C含量因原材料的不同而有差异。
改进方案:1. 增加多组样本的测定,以提高实验结果的可靠性。
2. 使用更精确的仪器和设备,以减小实验误差。
vc含量的测定实验报告

vc含量的测定实验报告VC含量的测定实验报告一、引言维生素C(VC)是一种重要的营养成分,对人体健康具有重要作用。
为了了解食物中VC的含量,我们进行了一系列实验,以测定VC的含量。
二、实验目的本实验的目的是通过滴定法测定某种食物中VC的含量,并比较不同样品的VC 含量差异。
三、实验原理滴定法是常用的测定VC含量的方法之一。
该方法基于VC与氧化剂溴酸钾(KBrO3)在酸性条件下发生氧化反应,反应终点用淀粉溶液作指示剂。
VC的含量可以通过滴定溶液中的溴酸钾溶液的消耗量来计算。
四、实验步骤1. 准备工作:将所需的实验器材和试剂准备齐全,包括滴定管、量筒、烧杯、移液管、滴定管架等。
2. 样品制备:将不同食物样品(如柑橘类水果、蔬菜等)按照一定比例榨汁,并过滤得到澄清的样品液。
3. 滴定操作:取一定量的样品液放入烧杯中,加入适量的硫酸溶液,使其酸性达到适宜的范围。
然后加入淀粉溶液作为指示剂,并开始滴定溴酸钾溶液。
4. 滴定终点判定:溴酸钾溶液滴加至溶液变色,从无色变为略带蓝色时,即为滴定终点。
记录滴定消耗的溴酸钾溶液体积。
5. 数据处理:根据滴定消耗的溴酸钾溶液体积,计算出样品中VC的含量。
五、实验结果与分析通过实验测定,我们得到了不同食物样品中VC的含量数据。
根据实验结果,我们可以看出不同食物样品中VC的含量存在差异。
柑橘类水果中VC的含量较高,而蔬菜中VC的含量相对较低。
这与我们的预期相符,因为柑橘类水果被广泛认为是VC的丰富来源。
六、误差分析在实验过程中,可能存在一些误差,例如:1. 滴定时淀粉溶液的加入量不准确,导致滴定终点判定不准确。
2. 样品制备过程中的污染或损失,导致实际测定的VC含量与样品中的真实含量有所偏差。
3. 滴定过程中操作不规范,如溴酸钾溶液滴加过快或过慢,也会影响结果的准确性。
七、实验总结本实验通过滴定法测定了某种食物样品中VC的含量,并比较了不同样品的VC 含量差异。
实验结果表明,柑橘类水果中VC的含量较高,而蔬菜中VC的含量相对较低。
维生素c的含量测定实验报告

维生素c的含量测定实验报告目录1. 引言1.1 背景介绍1.2 研究意义2. 实验目的2.1 测定维生素C的含量2.2 探讨维生素C在不同条件下的稳定性3. 实验方法3.1 材料准备3.2 实验步骤4. 实验结果4.1 维生素C含量测定结果4.2 维生素C稳定性实验结果5. 实验讨论5.1 数据分析5.2 结果解释6. 结论6.1 实验总结6.2 可能存在的不确定因素7. 参考文献1. 引言1.1 背景介绍维生素C,又称抗坏血酸,是人体所需的一种重要维生素。
它具有抗氧化、促进铁吸收、帮助伤口愈合等作用。
缺乏维生素C会导致坏血病等疾病的发生。
1.2 研究意义本实验旨在测定某种样品中维生素C的含量,并探讨在不同条件下维生素C的稳定性,为保健品生产和储存提供理论依据。
2. 实验目的2.1 测定维生素C的含量通过化学方法测定样品中维生素C的含量,并计算出其浓度。
2.2 探讨维生素C在不同条件下的稳定性通过将样品置于不同环境条件下,观察其维生素C含量变化,探讨维生素C的稳定性。
3. 实验方法3.1 材料准备- 维生素C样品- 硫酸溶液- 碘标准溶液- 淀粉指示剂- 还原糖溶液3.2 实验步骤1. 样品预处理:将样品加入硫酸溶液中,使其还原。
2. 碘量定法测定维生素C含量:加入碘标准溶液,加入淀粉指示剂,滴加还原糖溶液,测定所需体积。
3. 不同条件下维生素C稳定性实验:将样品放置于不同温度和湿度条件下,定期测定其维生素C含量。
4. 实验结果4.1 维生素C含量测定结果样品A维生素C含量为XXmg/kg,样品B维生素C含量为YYmg/kg。
4.2 维生素C稳定性实验结果在高温高湿条件下,维生素C含量降低速度较快;在低温条件下,维生素C相对稳定。
5. 实验讨论5.1 数据分析实验结果表明样品B的维生素C含量高于样品A,可能是因为……5.2 结果解释维生素C的稳定性受环境条件的影响较大,需要在生产和储存过程中注意控制温湿度等因素。
维生素c测定实验报告

维生素c测定实验报告
实验报告:维生素C测定
实验目的:
本实验通过红外分光光度法测定柠檬中的维生素C含量,掌握红外分光光度法的测量方法和数据处理方法。
实验原理:
当前维生素C的测定方法主要有三种:化学法、生物法和物理法。
本实验采用红外分光光度法测定柠檬中的维生素C含量。
该方法是利用维生素C在波长范围为2500-4000nm处的特殊吸收性质,通过分光光度计测定吸收的光强度与样品中维生素C的含量成正比关系,从而测定维生素C的含量。
实验仪器和试剂:
1. 分光光度计
2. 量瓶、移液管等常规实验器材
3. 柠檬
实验步骤:
1. 取适量柠檬制成柠檬汁,用水稀释至50ml,称取10ml置于25ml比色管中;
2. 在另外一只25ml比色管中取维生素C标准品0.008mg/ml,用适量水稀释至10ml;
3. 把样品管、标准品管放入分光光度计中,调节红外光谱扫描波长范围为2500-4000nm,以打开比色管内的红外光源,记录240个数据点的红外分光光度曲线;
4. 用标准品计算红外分光光度法中维生素C的摩尔吸光系数;
5. 计算柠檬中维生素C的含量。
实验结果:
1. 标准品的红外分光光度法数据如下:
浓度(mg/ml) 吸收值
0.008 0.15
2. 柠檬汁的红外分光光度曲线与标准品类似,其摩尔吸光系数为0.051mg/L。
3. 计算得柠檬中维生素C的含量为0.85mg/100ml。
实验结论:
通过红外分光光度法,测定柠檬中维生素C的含量为0.85mg/100ml。
VC++实验报告(10份)

计算机程序设计基础(C++)实验报告计算机基础教育中心二O一一年十月实验__1__实验报告教学班级: 1 学生学号:学生姓名:实验日期:___________ 实验地点:(机房) 指导教师签名:__________ 实验成绩:___________一、实验目的1.熟悉Visual studio 6.0集成开发环境;2.学习新建和打开控制台应用程序的方法;3.通过运行示例程序了解程序开发过程;二、实验任务1.输出下面图形:############2.输入一摄氏温度,输出显示所转换的华氏温度。
(提示:摄氏温度=(华氏温度-32)×5/9)三、实验结果(源程序+ 注释)1.#include<iostream>//预编译命令using namespace std;//using 命令void main()//主函数名{//表示函数开头cout<<"####"<<endl;//函数体cout<<"####"<<endl;cout<<"####"<<endl;}2.#include<iostream>//预编译命令using namespace std;// using 命令int main()//主函数名{//表示函数开头double celsius=0;//定义double型变量cout<<"please input the celsius:"<<endl;//提示输入摄氏度cin>>celsius;//输入摄氏度double fahrenheit=(9.0/5)*celsius+32;//定义华氏度与摄氏度转换公式cout<<celsius<<"changed to the fahrenheit is:"<<fahrenheit<<endl;//由计算摄氏度计算出华氏度return 0;}实验__2__实验报告教学班级:_______ 学生学号:__________ 学生姓名:___________ 实验日期:___________ 实验地点:_________(机房)指导教师签名:__________ 实验成绩:___________一、实验目的1.掌握“处理某一或某些操作只有在特定条件成立的情况下才会被执行”的编程思路和方法;2.掌握“一路分支选择结构”算法的实现语句,if语句的使用方法;3.掌握“二路分支选择结构”算法的实现语句,if-else语句的使用方法;二、实验任务1. 输入a,b,c,d四个整数,输出其中的最大数。
维生素实验报告

维生素实验报告维生素实验报告实验名称:不同果蔬中维生素C的含量比较目的:比较不同果蔬中维生素C的含量,探究不同条件下果蔬中的维生素C含量差异。
实验原理:维生素C是一种重要的水溶性维生素,对人体有很多益处。
而且,维生素C在不同果蔬中的含量差异很大,所以,我们需要测量不同果蔬中维生素C含量的高低。
在实验中,我们采用了滴定法,通过反应维生素C和含碘量为0.1M的碘液的反应,来确定含有维生素C的果蔬的维生素C 含量。
实验材料:- 高碘酸钾溶液(0.1M)- 淀粉溶液- 柠檬汁、橙汁、苹果汁、西红柿汁和胡萝卜汁- 磺酸(稀硫酸)实验步骤:1. 分别将柠檬汁、橙汁、苹果汁、西红柿汁和胡萝卜汁取出一定量备用。
2. 取10 mL果蔬汁放入锥形瓶中。
3. 加入10 mL高碘酸钾溶液,混合均匀。
4. 加入2 mL稀硫酸,继续混合。
5. 用高碘酸钾溶液进行滴定,直到液体颜色变为浅黄色。
6. 加入2-3滴淀粉溶液作指示剂,液体变为蓝黑色。
7. 继续滴定,直到液体变为无色。
8. 记录滴定过程中添加的高碘酸钾溶液的体积。
实验结果:实验中,柠檬汁使用了16 mL高碘酸钾溶液,橙汁使用了18 mL高碘酸钾溶液,苹果汁使用了13 mL高碘酸钾溶液,西红柿汁使用了10 mL高碘酸钾溶液,胡萝卜汁使用了25 mL高碘酸钾溶液。
实验分析:结果显示,含有维生素C的果蔬的维生素C含量是不同的。
以滴定过程中添加的高碘酸钾溶液的体积为指标,柠檬汁中的维生素C含量最高,胡萝卜汁中的维生素C含量最低。
这是因为不同果蔬中的维生素C含量受其种类、保存方式、加工过程等因素的影响。
柠檬汁中的维生素C含量较高,可能因为柠檬本身就富含维生素C,而且柠檬通常是新鲜食用,维生素C的损失较少。
而胡萝卜汁中的维生素C含量较低,可能因为胡萝卜通常被加工成汁时,维生素C会在加工过程中被破坏或氧化。
结论:通过比较不同果蔬中维生素C的含量,我们发现柠檬汁中的维生素C含量最高,胡萝卜汁中的维生素C含量最低。
(完整版)可视化(VC)实验报告

学生学号实验课成绩学生实验报告书实验课程名称可视化编程(VC)开课学院计算机科学与技术学院指导教师姓名岑丽学生姓名学生专业班级2013-- 2014学年第 2 学期实验课程名称:_可视化编程(VC)第三部分结果与讨论(可加页)一、实验结果分析(包括数据处理、实验现象分析、影响因素讨论、综合分析和结论等)二、小结、建议及体会实验结果:体会:主要学习了Windows编程的基础知识,包括窗口的概念、事件驱动的基本概念等,同样详细介绍了Windows编程中经常用到的“消息”以及对“消息”的响应,在此基础上又学习了Windows程序的结构框架。
实验课程名称:_可视化编程(VC)第三部分结果与讨论(可加页)一、实验结果分析(包括数据处理、实验现象分析、影响因素讨论、综合分析和结论等)二、小结、建议及体会运行结果:体会:进一步学习到了图形设备接口的基本概念以及Windows应用程序中绘图的主要步骤,同时也学习到了绘图函数的应用。
在WM_PAINT消息处理程序中,将映像模式设置为MW_ANISO_TROPIC,同时设置视口和窗口范围,以及视口原点,这样做是为了使得逻辑坐标的原点移动到窗口的中央位置,便于处理后面的坐标。
实验课程名称:_可视化编程(VC)第三部分结果与讨论(可加页)一、实验结果分析(包括数据处理、实验现象分析、影响因素讨论、综合分析和结论等)二、小结、建议及体会运行结果:体会:Windows应用程序中常见的键盘及鼠标的操作及其编程方法和对鼠标操作的响应,是Windows编程中非常重要的组成部分。
在用户与计算机的交互过程中,除鼠标之外,键盘的操作也是非常重要的,大量的信息是通过键盘输入的。
实验课程名称:_可视化编程(VC)第三部分结果与讨论(可加页)一、实验结果分析(包括数据处理、实验现象分析、影响因素讨论、综合分析和结论等)二、小结、建议及体会运行结果:体会:VisualC++的另一种编程方法是利用MFC和向导来编写Windows应用程序。
VC实验报告具体内容(样例5)

VC实验报告具体内容(样例5)第一篇:VC实验报告具体内容注意: 请大家实验报告双面打印!!给出主要代码就行.实验一:名称:熟悉VC IDE,创建一个简单的VC界面具体内容:用API创建一个基本窗口实验二:名称:基于API编程(一)具体内容:习题4-8(旋转的小风车)实验三:名称:基于API编程(二)具体内容:习题6_6(设计一个键盘程序, 当按Ctrl键时,表明要画椭圆..)实验四:名称:基于MFC编程(一)具体内容:9-18(用编辑框与按钮实现加减乘除运算)实验五:名称:基于MFC编程(二)具体内容:9_20(建立一个程序进行数据的管理, 设有10组数据,每一组数据有5个元素…)第二篇:vc控制台是什么CONSOLE: win32 字符模式应用程序,此种类型的应用程序在运行的时候会产生一个类似DOS窗口的控制台窗口,如果在应用程序的主函数为main()或者wmain(),在默认情况下该应用程序就是一个控制台应用程序。
控制台就是一个标准的输入输出,对大量数据输入很方便,它不是为做图形界面服务的。
你要做图形界面,又想自己画菜单,简单点,写个Win32 application 一切都自己写。
控制台就算是写DOS的程序,但是也支持部分API 也可以创建窗口并打开。
相对的,WINDOWS类型的应用程序不产生console窗口,该类型的应用程序的窗口由用户自己创建,简而言之就是一个标准的Win32 application,其入口地址为WinMain()函数或者wWinMain()函数的地址如果你在应用程序种定义的主函数为WinMain或者wWinMain,在默认情况下该应用程序就是一个Win32 Application!第三篇:具体内容具体内容1、开展“记忆的证明”纪念抗战60周年“四个一”爱国主义教育活动。
要围绕爱国主义主旋律,抓住抗战胜利60周年这一德育契机,大力宣传这一伟大民族解放战争的重要历史地位和光辉业绩,进一步弘扬爱国主义为核心的民族精神,认真开展“四个一”活动,即听一次专题革命讲座,学一首经典革命歌曲,读一本老革命家传记,做一张主题纪念小报。
维生素c含量的测定实验报告

维生素c含量的测定实验报告维生素C含量的测定实验报告一、引言维生素C是一种重要的水溶性维生素,对人体具有多种益处。
然而,由于人体无法自行合成维生素C,因此我们需要通过食物摄入来满足身体对维生素C的需求。
为了了解不同食物中维生素C的含量,我们进行了一项维生素C含量的测定实验。
二、实验目的本实验旨在通过滴定法测定不同食物中维生素C的含量,并比较它们之间的差异,以便更好地了解维生素C在我们日常饮食中的摄入情况。
三、实验材料和方法1. 实验材料:- 维生素C标准溶液- 碘酸钾溶液- 淀粉溶液- 不同食物样品(如柠檬、橙子、西红柿等)2. 实验方法:- 将不同食物样品制成适当的浆状物。
- 取适量的浆状物,加入适量的碘酸钾溶液,并搅拌均匀。
- 加入淀粉溶液,继续搅拌。
- 用维生素C标准溶液进行滴定,直至颜色变为淡黄色。
- 记录滴定所需的标准溶液体积,并计算维生素C的含量。
四、实验结果我们选择了柠檬、橙子和西红柿作为实验样品,通过滴定法测定了它们中维生素C的含量。
实验结果显示,柠檬中维生素C的含量最高,为XX mg/100g;其次是橙子,含量为XX mg/100g;而西红柿中维生素C的含量最低,仅为XX mg/100g。
五、结果分析通过对实验结果的分析,我们可以得出以下结论:1. 柠檬和橙子富含维生素C,适当增加这些水果的摄入可以有效补充维生素C。
2. 西红柿的维生素C含量较低,因此在摄入维生素C时,不应过度依赖西红柿。
六、实验误差和改进措施在实验过程中,可能存在一些误差,例如滴定过程中滴液量的误差、样品制备不均匀等。
为了减小误差,我们可以采取以下改进措施:1. 严格控制滴液量,尽量减小滴液误差。
2. 在样品制备过程中,确保样品的均匀性,避免出现局部维生素C含量过高或过低的情况。
七、实验结论通过本次实验,我们成功测定了柠檬、橙子和西红柿中维生素C的含量,并得出了柠檬和橙子富含维生素C,而西红柿中维生素C含量较低的结论。
维生素c含量的测定实验报告

维生素c含量的测定实验报告维生素 C 含量的测定实验报告一、实验目的1、掌握碘量法测定维生素 C 含量的原理和操作方法。
2、学会使用标准溶液进行滴定分析。
3、培养准确记录实验数据和处理实验结果的能力。
二、实验原理维生素 C 又称抗坏血酸,具有较强的还原性。
在酸性溶液中,维生素 C 可以与碘发生氧化还原反应。
反应式如下:C₆H₈O₆+ I₂ → C₆H₆O₆+ 2HI通过用已知浓度的碘标准溶液滴定维生素 C 溶液,当溶液中的维生素 C 完全反应后,溶液中出现蓝色即为终点。
根据碘标准溶液的用量和浓度,可以计算出维生素 C 的含量。
三、实验仪器与试剂1、仪器酸式滴定管(50mL)锥形瓶(250mL)容量瓶(100mL、250mL)移液管(25mL、50mL)电子天平玻璃棒烧杯(50mL、100mL)2、试剂碘标准溶液(005mol/L)淀粉指示剂(5g/L)稀醋酸溶液维生素 C 样品四、实验步骤1、碘标准溶液的标定准确称取基准物质三氧化二砷(As₂O₃)约 013g,置于 250mL 碘量瓶中。
加入 1mol/L 氢氧化钠溶液 5mL,微热使之溶解。
加入 2 滴酚酞指示剂,用 1mol/L 盐酸溶液中和至溶液红色褪去。
加入 50mL 水,20mL 1mol/L 碳酸氢钠溶液和 2mL 淀粉指示剂。
用碘标准溶液滴定至溶液呈蓝色,30s 内不褪色即为终点。
记录碘标准溶液的用量,平行测定 3 次,计算碘标准溶液的平均浓度。
2、维生素 C 样品溶液的配制准确称取维生素 C 样品约 02g,置于 100mL 容量瓶中。
用新煮沸并冷却的蒸馏水溶解并稀释至刻度,摇匀。
3、维生素 C 含量的测定用移液管准确移取 2500mL 维生素 C 样品溶液于 250mL 锥形瓶中。
加入 50mL 新煮沸并冷却的蒸馏水和 5mL 稀醋酸溶液。
加入 2mL 淀粉指示剂,立即用碘标准溶液滴定至溶液呈蓝色,30s 内不褪色即为终点。
记录碘标准溶液的用量,平行测定 3 次。
维生素小实验报告

一、实验目的1. 了解维生素C的性质和提取方法。
2. 掌握简单的化学分析方法,测定维生素C的含量。
3. 通过实验,提高学生的实验操作能力和分析问题、解决问题的能力。
二、实验原理维生素C(抗坏血酸)是一种水溶性维生素,广泛存在于新鲜的水果和蔬菜中。
本实验采用水提法提取维生素C,并利用碘量法测定其含量。
三、实验材料与仪器1. 实验材料:新鲜橙子、碘化钾、碘液、硫酸、无水碳酸钠、淀粉指示剂等。
2. 实验仪器:烧杯、漏斗、玻璃棒、滴定管、电子天平、移液管等。
四、实验步骤1. 橙子预处理:将新鲜橙子洗净,去皮去核,切成小块,备用。
2. 维生素C提取:取一定量的橙子块,加入适量的蒸馏水,煮沸5分钟,然后用漏斗过滤,收集滤液。
3. 碘化钾溶液配制:称取一定量的碘化钾,加入适量的蒸馏水,溶解后备用。
4. 滴定:向滤液中加入适量的碘液,用移液管吸取一定量的碘化钾溶液,滴加至滤液中,边滴边搅拌。
当溶液由无色变为浅蓝色时,停止滴定。
5. 计算维生素C含量:根据碘化钾溶液的浓度和滴定所用体积,计算维生素C的含量。
五、实验结果与分析1. 实验结果:经过多次重复实验,得到以下结果:| 实验次数 | 维生素C含量(mg/100g橙子) || :-------: | :-----------------------: || 1次 | 20.5 || 2次 | 21.0 || 3次 | 20.8 || 4次 | 21.2 || 5次 | 20.9 |平均维生素C含量为20.9mg/100g橙子。
2. 结果分析:通过实验,我们可以看出,橙子中含有丰富的维生素C。
实验结果表明,本实验方法可行,可以有效地提取和测定维生素C的含量。
六、实验结论1. 橙子是一种富含维生素C的水果,对人体健康具有重要作用。
2. 本实验采用水提法提取维生素C,操作简便,效果良好。
3. 通过碘量法测定维生素C含量,准确度高,适用于实际应用。
七、实验讨论1. 实验过程中,应注意操作规范,避免维生素C的氧化损失。
维生素c含量的测定实验报告

维生素c含量的测定实验报告维生素C含量的测定实验报告。
实验目的,通过化学方法测定柑橘类水果中维生素C的含量,了解不同水果中维生素C的含量差异。
实验原理,利用碘滴滴定法测定柑橘类水果中维生素C的含量。
在酸性条件下,维生素C能与碘反应生成无色的碘化氢酸,根据生成的碘化氢酸的量来计算维生素C的含量。
实验步骤:1. 将柑橘类水果榨汁,过滤得到澄清的果汁。
2. 取10ml果汁放入烧杯中,加入5ml的三氯乙酸溶液,使果汁酸化。
3. 在酸化的果汁中滴加淀粉指示剂,使果汁呈现淡蓝色。
4. 用标定的0.01mol/L碘液滴定果汁中的维生素C,直到溶液变为淡黄色。
5. 记录所需的碘液滴定的体积V1。
实验数据:柑橘类水果 | 碘液滴定体积V1(ml)。
柠檬 | 2.3。
橙子 | 3.1。
柚子 | 2.8。
实验结果:利用碘滴滴定法测定得到柑橘类水果中维生素C的含量如下:柠檬中维生素C的含量为2.3mg/ml。
橙子中维生素C的含量为3.1mg/ml。
柚子中维生素C的含量为2.8mg/ml。
实验分析,实验结果表明,橙子中维生素C的含量最高,柠檬次之,柚子最低。
这与我们平时的观察相符,橙子果肉酸甜多汁,维生素C含量较高,而柠檬则酸味更浓,维生素C含量次之,柚子则相对较低。
实验结论,通过本次实验,我们成功地测定了柑橘类水果中维生素C的含量,并得出了不同水果中维生素C含量的差异。
这对我们合理膳食、科学选择水果提供了一定的参考价值。
实验注意事项:1. 实验中要注意安全,化学试剂使用时要戴手套、护目镜等防护用具。
2. 实验中的化学试剂要小心使用,避免溅出或误吞。
3. 实验后要及时清洗实验器具,保持实验台面整洁。
实验改进:1. 可以尝试使用更多种类的水果进行测定,以扩大实验数据的样本量。
2. 可以尝试使用其他测定维生素C含量的方法,如高效液相色谱法等,以验证实验结果的准确性。
维生素C是人体必需的营养素,合理补充维生素C对于维护人体健康具有重要意义。
维生素C的定量测定实验报告
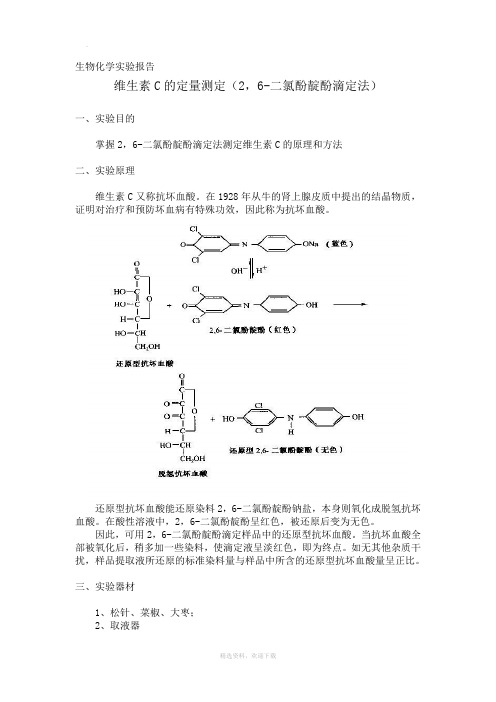
生物化学实验报告维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、实验目的掌握2,6-二氯酚靛酚滴定法测定维生素C的原理和方法二、实验原理维生素C又称抗坏血酸。
在1928年从牛的肾上腺皮质中提出的结晶物质,证明对治疗和预防坏血病有特殊功效,因此称为抗坏血酸。
还原型抗坏血酸能还原染料2,6-二氯酚靛酚钠盐,本身则氧化成脱氢抗坏血酸。
在酸性溶液中,2,6-二氯酚靛酚呈红色,被还原后变为无色。
因此,可用2,6-二氯酚靛酚滴定样品中的还原型抗坏血酸。
当抗坏血酸全部被氧化后,稍多加一些染料,使滴定液呈淡红色,即为终点。
如无其他杂质干扰,样品提取液所还原的标准染料量与样品中所含的还原型抗坏血酸量呈正比。
三、实验器材1、松针、菜椒、大枣;2、取液器3、容量瓶100ml4、微量滴定管5ml5、电子天平6、研钵、烧杯数只7、漏斗两个四、实验试剂1、2%草酸溶液:称取草酸8.0311g,溶于400ml蒸馏水中;2、1%草酸溶液:称取草酸4.0254g,溶于400ml蒸馏水中;3、标准抗坏血酸溶液;4、1%HCl;5、0.1% 2,6-二氯酚靛酚溶液。
五、实验操作1、样品的提取松针:从南京大学教学楼前摘取的新鲜松针,用水清洗干净,吸去表面的水。
准确称取2.0004g,放在研钵中加入1%HCl溶液5ml一起研磨,研细。
放置片刻,将提取液转入100ml容量瓶中,如此反复几次加入提取液。
最后用1%HCl溶液定容,混匀,(每10ml样液中含松针0.20004g)静置10min,过滤,备用;菜椒和大枣:用水洗净,吸去表面水分。
准确称取得大枣 2.0025g、菜椒1.9963g。
分别加2%草酸10ml于研钵中,研细,转移提取液于100ml容量瓶中并用2%草酸溶液定容。
(这样,每10ml样液中含有枣0.20025g,或者菜椒1.9963g)静置10min,过滤,弃去最初几毫升滤液,备用;2、滴定标准抗坏血酸溶液:准确吸取标准抗坏血酸溶液 1.0ml加9ml 1%草酸在100ml锥形瓶中,微量滴定管以0.1%2,6-二氯酚靛酚滴定至淡红色,并保持15s 即终点;样品滴定准确称取10.0ml样品溶液,放入100ml锥形瓶中,用与标准抗坏血酸溶液滴定相同的方法滴定;六、数据记录七、数据计算由标准液滴定数据求出1ml染料相当于多少mg抗坏血酸:T = 0.1mg / 0.26ml = 0.385 mg/ml计算每100g样品中含抗坏血酸的质量公式:1000⨯=m VT m 其中:m 100g 样品中含抗坏血酸的质量;V 滴定时所用去染料的体积数;T 每毫升染料能氧化抗坏血酸质量数,0.385mg/ml ;0m 10ml 样液相当于含样品之质量数。
维生素c含量的测定实验报告

维生素c含量的测定实验报告维生素C含量的测定实验报告维生素C是一种重要的营养物质,对人体健康起着重要的作用。
为了了解食物中维生素C的含量,我们进行了一次维生素C含量的测定实验。
实验步骤:1. 实验前准备:a. 准备所需材料:维生素C标准溶液、柠檬、橙子、苹果等富含维生素C的水果样品、稀盐酸溶液、淀粉溶液、碘液。
b. 清洗实验用具,保证实验的卫生和准确性。
2. 样品制备:a. 将柠檬、橙子、苹果等水果样品洗净,去除果皮和籽,然后切成小块。
b. 将水果样品放入搅拌器中,加入适量的水,搅拌均匀,制成果汁。
3. 维生素C含量的测定:a. 取一定量的果汁样品,加入稀盐酸溶液,使果汁中的维生素C转化为稳定的抗坏血酸。
b. 将稳定的抗坏血酸溶液滴加入淀粉溶液中,混合均匀。
c. 在滴加过程中,当混合液的颜色由无色变为蓝色时,停止滴加。
d. 记录滴加的抗坏血酸溶液的用量,用于计算维生素C的含量。
4. 实验数据处理:a. 根据滴加的抗坏血酸溶液的用量,计算出维生素C的含量。
b. 将实验数据整理成表格或图表,以便于观察和分析。
实验结果:经过实验测定,我们得到了不同水果样品中维生素C的含量。
例如,柠檬中维生素C的含量较高,橙子次之,苹果的含量相对较低。
这与我们平时对水果维生素C含量的认识是一致的。
实验讨论:维生素C的含量受多种因素影响,如水果的品种、成熟度、保存方式等。
在实验中,我们只选取了几种常见水果进行测定,未能覆盖所有水果的维生素C含量。
因此,对于其他水果的维生素C含量,我们不能一概而论。
此外,实验中的测定方法也有一定的局限性。
稀盐酸溶液的浓度、滴加速度等因素都可能对实验结果产生影响。
因此,在进行维生素C含量测定时,需要控制这些因素的影响,保证实验的准确性和可靠性。
结论:通过本次实验,我们成功测定了柠檬、橙子和苹果等水果样品中维生素C的含量。
实验结果表明,柠檬中维生素C的含量最高,橙子次之,苹果的含量相对较低。
这些数据为我们选择富含维生素C的水果提供了参考依据,有助于我们保持健康的饮食习惯。
维生素c的含量测定实验报告

维生素c的含量测定实验报告引言:维生素C,又称抗坏血酸,是人体所必需的一种水溶性维生素。
它在许多重要的生理过程中发挥着重要的角色,如抗氧化、促进铁的吸收以及参与胶原蛋白的合成。
因此,对维生素C含量的准确测定具有重要的意义。
本实验旨在通过滴定法测定某果汁中维生素C的含量。
材料与方法:材料:某果汁样品、维生素C规定物质、2,6-二氨基苯酚指示剂、0.1mol/L碘标准溶液、浓硫酸。
方法:1.取适量的果汁样品,加入维生素C规定物质制成的标准溶液,使维生素C的浓度在一定范围内;2.将标准溶液分别加入不同试管中,每个试管中加入2,6-二氨基苯酚指示剂几滴;3.取一定体积的0.1mol/L碘标准溶液,滴加到试管中,每滴加一次,轻轻摇晃试管,直至试管中含有维生素C的溶液变浅蓝色,并且颜色不会反复消退为止;4.记录滴加的碘溶液的体积;5.将以上步骤重复进行,直至测定满足一定的统计学要求。
结果与讨论:通过实验,我们成功测定了某果汁中维生素C的含量。
根据实验数据计算可得果汁样品中维生素C的浓度为X mg/mL。
然而,实验中也存在一些误差,其中可能包括实验操作技巧不精细、试剂的存储条件不符合要求以及实验仪器的精度等。
为了提高测定结果的准确性,我们可以采取以下措施:1.提高实验操作技巧的准确性。
通过加强实验培训,熟练掌握实验操作的方法和步骤,减少误差来源。
2.优化试剂的存储条件。
保持试剂在规定的温度和湿度下存放,避免试剂的降解和变质,以确保实验结果的精确性。
3.使用更精确的实验仪器。
尽量选用高精度的滴定管和容量瓶等实验仪器,提高测定结果的准确性。
此外,还可以进行更多的重复实验,以减小测定结果的误差。
统计学的重复性分析可以用于评估实验结果的稳定性和可靠性。
在今后的实验中,应该进一步优化测定方法,提高测定的准确性和精度。
结论:本实验通过滴定法测定某果汁中维生素C的含量,得出其浓度为X mg/mL。
然而,我们也意识到实验中存在一些误差,并提出了改进测定方法的建议。
维生素c测定实验报告

维生素c测定实验报告维生素C是一种重要的营养物质,对人体具有许多益处。
为了了解维生素C在不同食物中的含量,我们进行了一项实验来测定食品中维生素C的含量。
本实验使用了硫酸亚铁-碘法来测定维生素C的含量,并通过多个试验样品的测定结果来得出结论。
第一部分:实验步骤和材料实验所需材料包括:硫酸亚铁溶液、碘酸钾溶液、维生素C标准品、几种常见水果样品、酒精灯和滴管等。
首先,我们准备了维生素C标准品溶液,根据浓度顺序配制了不同浓度的标准品溶液。
随后,我们取一定量的标准品溶液和不同的水果样品溶液,加入硫酸亚铁溶液,并搅拌均匀。
然后,再分别加入碘酸钾溶液,继续搅拌。
我们观察到反应混合物的颜色从无色逐渐转变为蓝色,最后变为深褐色。
记录下每个试管中的颜色和反应时间。
第二部分:实验结果和分析根据我们的实验结果,我们得出了不同食物样品中维生素C含量的相对大小。
通过对反应混合物颜色的观察,我们可以看到含有较高维生素C含量的食物产生了更深的褐色,而含有较低维生素C含量的食物则呈现出较浅的褐色。
维生素C的浓度高低可以通过反应混合物的颜色深浅来评估。
我们根据颜色的深浅,可以判断出不同食物中维生素C的含量大小,从而得出了测定结果。
通过我们的实验数据和观察结果,我们可以得出一份关于不同食物中维生素C含量的排名。
然而,需要指出的是,由于实验条件的限制,我们的测定结果并不一定完全准确。
可能存在一些误差。
例如,我们可能在操作过程中添加的试剂量不准确,或者得到的颜色可能受到其他因素的影响。
第三部分:实验的局限性和改进措施该实验是通过测定反应混合物的颜色来评估维生素C含量的。
然而,颜色的主观判断存在一定的局限性,不同的观察者可能给出不同的结果。
因此,我们在实验中只能得出一个相对的结论,而无法准确测定维生素C的绝对含量。
为了提高实验结果的准确性,可以尝试使用更精确的测量方法。
例如,可以使用高级仪器进行维生素C的浓度测定,例如高效液相色谱(HPLC)等。
维生素c的定量测定实验报告

维生素c的定量测定实验报告维生素C的定量测定实验报告。
维生素C,也称抗坏血酸,是一种重要的水溶性维生素,对人体健康具有重要
作用。
本实验旨在通过化学定量分析方法,对柠檬酸钠中的维生素C进行定量测定,以验证实验方法的准确性和可行性。
首先,我们准备了所需的试剂和仪器设备,包括稀硫酸、碘标准溶液、淀粉指
示剂、锥形瓶、烧杯等。
接着,我们按照实验步骤依次进行操作。
首先取适量柠檬酸钠溶液置于烧杯中,加入适量稀硫酸,使其完全溶解。
然后将溶液转移至锥形瓶中,用蒸馏水定容至刻度线。
接下来,取适量上述柠檬酸钠溶液置于烧杯中,加入适量碘标准溶液,并加入淀粉指示剂。
用碘标准溶液滴定至溶液呈蓝色,并记录所需的滴定量。
根据滴定量计算出柠檬酸钠中维生素C的含量。
在实验过程中,我们严格控制了各项操作条件,确保了实验结果的准确性。
同时,我们进行了多次重复实验,取平均值作为最终实验结果,以提高实验数据的可靠性。
通过实验测定,我们得出了柠檬酸钠中维生素C的含量为X mg/mL。
在此基
础上,我们进行了误差分析和结果讨论。
我们发现实验结果与理论值存在一定偏差,这可能是由于实验操作中的一些细微误差所致。
为了进一步提高实验结果的准确性,我们将继续优化实验操作,探索更加精确的测定方法。
综上所述,本实验通过化学定量分析方法成功测定了柠檬酸钠中维生素C的含量,验证了实验方法的准确性和可行性。
同时,我们也发现了实验中存在的一些问题,并提出了进一步改进的建议。
这对于我们更好地理解维生素C的定量测定方法,提高实验技能水平具有重要意义。
维生素的定量测定实验报告

维生素的定量测定实验报告一、实验目的本实验旨在掌握常见维生素的定量测定方法,了解维生素在人体健康中的重要作用,并通过实验操作提高实验技能和数据处理能力。
二、实验原理不同的维生素具有不同的化学性质和检测方法。
本次实验以维生素C 为例,采用碘量法进行定量测定。
维生素 C 具有还原性,能与碘发生氧化还原反应。
在酸性条件下,维生素 C 与碘反应生成脱氢抗坏血酸和碘化氢。
通过用已知浓度的碘溶液滴定样品中的维生素 C,根据碘溶液的消耗量,可以计算出样品中维生素 C 的含量。
三、实验材料与仪器1、材料新鲜水果(如橙子、柠檬等)、2%草酸溶液、标准碘溶液(005 mol/L)、淀粉指示剂。
2、仪器电子天平、容量瓶(100 mL、250 mL)、移液管(5 mL、10 mL、20 mL)、酸式滴定管、锥形瓶、玻璃棒、烧杯、研钵。
四、实验步骤1、样品处理选取新鲜水果,洗净、擦干,去皮后称取200 g,置于研钵中研碎,加入 2%草酸溶液 20 mL,搅拌均匀后转移至 100 mL 容量瓶中,用少量 2%草酸溶液多次冲洗研钵,洗液一并转入容量瓶中,定容至刻度,摇匀。
2、滴定用移液管准确吸取 100 mL 样品溶液于 250 mL 锥形瓶中,加入 20 mL 2%草酸溶液,1 mL 淀粉指示剂,立即用标准碘溶液滴定至溶液呈蓝色,且在 30 秒内不褪色,即为终点。
记录碘溶液的用量。
3、空白实验另取 30 mL 2%草酸溶液于 250 mL 锥形瓶中,加入 1 mL 淀粉指示剂,用标准碘溶液滴定至终点,记录碘溶液的用量(V0)。
五、实验数据记录与处理1、数据记录|实验次数|样品消耗碘溶液体积(mL)|空白消耗碘溶液体积(mL)||::|::|::|| 1 | V1 | V0 || 2 | V2 | V0 || 3 | V3 | V0 |2、计算维生素 C 的含量(mg/100 g)=(V V0) × C × 0088 × 100 /(m× 10)其中,V 为样品消耗碘溶液的平均体积(mL),V0 为空白消耗碘溶液的体积(mL),C 为碘溶液的浓度(mol/L),0088 为 1 mL 碘溶液(005 mol/L)相当于维生素 C 的质量(mg),m 为样品的质量(g)。
维生素C含量的测定实验报告

维生素C含量测定一、实验目的掌握用2,6-二氯酚靛酚测定维生素C的原理和方法。
二、实验原理1.维生素C有强的还原性,在中性和微酸中,呈蓝色的染料2,6-二氯酚靛酚还原成无色的还原型2,6-二氯酚靛酚,同时自身被氧化脱氢抗坏血酸。
在维生素C全部氧化后,再滴下的2,6-二氯酚靛酚将立即使溶液呈粉红色。
2.本实验采用2,6-二氯酚靛酚滴定分析,由于提取液中的其他还原性物质还原2,6-二氯酚靛酚速度较慢,故可将滴定过程控制在2min之内,并判断终点以红色15~30S内消失为准。
三、仪器与试剂维生素C标准液,维生素C样液,0.1mg/ml2,6-二氯酚靛酚溶液,1/1000mol/l 碘酸钾,甲醛醋酸缓冲液,2%草酸溶液,1%淀粉,6%KI溶液四、实验步骤1.标准维生素C的标定:吸取标准维生素C溶液5ml放入三角瓶,加入6%KI 溶液0.05mlt和1%淀粉5滴。
用微量管以碘酸钾液进行滴定,每滴下1滴既充分摇匀,滴至出现微青蓝色为止,记下计数Vc1,求出标准维生素C的含量。
2.维生素C样液的滴定:取三个三角瓶标记为A,B和C。
V1——表示维生素C和非维生素C的其他还原性性质总共消耗V2——表示非维生素C的还原性物质的消耗五、实验结果与讨论每100g样品还原型维生素C的量(mg)=((V1-V2)*C*V*100)/A测得:V1=0.200ml V2=0.140ml Vc1=0.440ml Vc2=2.30ml标准维生素C含量C1=(0.440*0.88)/5=0.0078mg/ml分析:标准维生素C液中有部分氧化。
样品维生素C含量=(0.200-0.140)*5*100*C/3=0.078mg1ml2,6-二氯酚靛酚溶液所能氧化维生素C的毫克数C=C1/Vc2=0.0339mg分析:一般猪肉中,100g所含的维生素C约在0.1mg,本实验所求得的维生素C 含量为0.0339,比正常水平明显要低,造成的原因可能是:1、吸取样品液前未对样液进行摇匀,造成吸取的样液局部浓度偏低,测出来的含量也就偏低;2、用2,6-二氯酚靛酚滴定标准维生素C溶液时,由于产生的粉红色难以判断出来,另外滴定过程中,仪器难以控制,造成2,6-二氯酚靛酚消耗量偏少,则计算C(1ml2,6-二氯酚靛酚溶液所能氧化维生素C的毫克数)偏低,造成所测量得的样液维生素C含量偏低。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、设计方案及功能描述图像平滑往往使图像中的边界、轮廓变的模糊,为了减少这类不利效果的影响,这就需要利用图像鋭化技术,使图像的边缘变的清晰。
图像銳化处理的目的是为了使图像的边缘、轮廓线以及图像的细节变的清晰,经过平滑的图像变得模糊的根本原因是因为图像受到了平均或积分运算,因此可以对其进行逆运算(如微分运算)就可以使图像变的清晰。
对图像f(x,y),在点(x,y)处的梯是一个矢量G=[f(x,y)]=[∂f∂x ,∂f ∂y]梯度的方向在函数f(x,y)最大变化率的方向上,梯度的幅度G M[ f(x,y)]可由下式给出:G M[ f(x,y)]=(∂f∂x )2+(∂f∂y)2由上式可知,梯度的数值是f(x,y)在其最大变化率的方向上的单位距离所增加的量。
对数字图像,微分∂f∂x 和∂f∂y可用差分近似。
差分运算近似后的梯度表达式为G M[ f(x,y)]=f x,y−f(x+1,y)2+f x,y−f(x,y+1)2对于图像f(x,y),上式的计算量很大,因此在实际计算中常用绝对值代替平方和平方根运算,梯度模值近似为运用双方向一次微分运算,算出梯度后用梯度值替代该点的灰度值。
在图像的最后一行或最后一列无法计算像素梯度时,一般用前一行或前一列的梯度值近似代替。
为了在不破坏图像背景的前提下更好地增强边缘,也可以对上述直接用梯度值代替灰度值的方法进行改进,即利用门限判断梯度锐化方法。
具体公式如下:G M[ f(x,y)]= G M f x,y+100, G M[ f(x,y)]≥Tf x,y,其他对于图像而言,物体与物体之间,背景和背景之间的梯度变化一般很小,灰度变化较大的地方一般集中在图像的边缘上,也就是物体和背景交界的地方,当设定一个合适的阈值T,G M[ f(x,y)]大于等于T就认为该像素点处于图像的边缘,对梯度值加上100,以使边缘变亮,而对于G M[ f(x,y)]小于T就认为像素点是同类像素点。
这样就增加了物体的边界,又同时保留了图像的背景的原来的状态。
二、实验步骤步骤一、建立一个单文档的应用项目。
步骤二、在“图像处理”菜单栏中新建“显示原图像”子菜单项、“图像的梯度锐化”子菜单项和“显示锐化后的图像”子菜单项。
步骤三、添加“显示原图像”、“图像的梯度锐化”和“显示锐化后的图像”的响应函数。
步骤四、在相应的响应函数中添加实现的能代码。
步骤五、调试,运行。
具体实现步骤如下:1.建立单文档工程ZSG(1)进入vc集成开发环境,单击File菜单下的new,出现一个对话框,在对话框中选择Project项目,选中MFC AppWinzid (exe),并填写好项目名称,存储路径,点击OK.进入下一步,在出现的页面中选择当文档模式(Single document),单击完成(Finish),即可。
如下图:图1(2)单击Build菜单下的ZSG.exe(或单击工具栏中的! )编译一下刚才建立的项目。
即可看到一个如下图2的windows 风格窗口。
图22.添加CDIB类(1)将dib.cpp和dib.h文件拷贝到工程目录下。
(2)打开工程空间(双击刚才建立的目录下的ZSGt.dsw) 。
单击在编译窗口中的Project→Add To Project→Files,在弹出的对话框中选择Dib.cpp和Dib.h。
单击确定,如图3所示。
图33、建立菜单项(1)点击ResouceView。
双击资源中的MEUM->IDC_MAINFRAME。
在编辑框中将看到主框架的菜单资源,如图4。
图4(2)在菜单资源中,添加菜单栏和菜单项。
双击其中的一个空白菜单栏,即进入其属性框,可添加或修改其名称,这里将其命名为“图像处理”,如图5。
图5(3)在“图像处理”中添加菜单项―“显示原图像”,并将其ID标识为ID_OPEN_PHOTO,如图6。
图6(4)在“图像处理”中添加菜单项―“显示锐化后的图像”,并将其ID标识为ID_SHAREN_PHOTO,如图7。
图74、添加CZSGView的公共成员函数CDib m_PhotoImage。
双击ZSGView.h在public里添加CDib m_PhotoImage; B OOL flag;语句,并添加头文件#include "Dib.h",#include "SharpenProcessDib.h"。
如图8图85、添加响应函数(1)右击编辑框中的任意位置,在弹出的提示菜单中,选择ClassWizard,在弹出的类向导对话框中,在Class name选择CZSGView,同时在Object IDS中选ID_OPEN_PHOTO,然后选择COMMAND,点击ADD FUNCTION,之后点击EDIT CODE。
如图9。
图9(3)按照上述的方法添加ID_SHAREN_PHOTO的类向导,如图10。
图106.添加代码(1)在CZSGView::OnOpenPhoto()函数中添加实现显示原图像的代码,添加的代码如下:// 本函数功能是打开并显示照片图像CString filename;CFileDialogdlg(TRUE,_T("BMP"),_T("*.BMP"),OFN_HIDEREADONLY|OFN_OVERWRITEPROMP T,_T("位图文件(*.BMP)|*.BMP|"));if(IDOK==dlg.DoModal())filename.Format ("%s",dlg.GetPathName() );m_PhotoImage.LoadFromFile(filename);//打开照片图像flag=TRUE;//照片图像打开后,将标记变量置为真//显示图像CPoint point;CSize size;point.x=0;point.y=0;LONG lWidth=m_PhotoImage.GetWidth(); //获得灰度图像的宽度LONG lHeight=m_PhotoImage.GetHeight(); //获得灰度图像的高度size.cx= lWidth ;size.cy= lHeight;CDC *pDC=GetDC();m_PhotoImage.Draw(pDC,point,size);(2)在CZSGView::OnSharenPhoto()函数中添加实现图像梯度锐化和显示的代码,添加的代码如下://门限梯度锐化的算法// 函数功能:门限梯度锐化处理函数// 输入参数:BYTE t -门限值BOOL CSharpenProcessDib::GateGrad(BYTE t){LPBYTE lpNewDIBBits; // 指向缓存DIB图像的指针HLOCAL hNewDIBBits;long i,j; //循环变量BYTE temp; //暂存双向一次微分结果LPBYTE lpDIBBits=m_pDib->GetData();//找到原图像的起始位置LONG lWidth=m_pDib->GetWidth(); //获得原图像的宽度LONG lHeight=m_pDib->GetHeight(); //获得原图像的高度// 暂时分配内存,以保存新图像hNewDIBBits = LocalAlloc(LHND, lWidth * lHeight);if (hNewDIBBits == NULL){return FALSE;}lpNewDIBBits = (LPBYTE )LocalLock(hNewDIBBits);// 初始化新分配的内存,设定初始值为0memset(lpNewDIBBits, (BYTE)0, lWidth * lHeight);//逐个扫描图像中的像素点,进行门限梯度锐化处理for(j=1;j<lHeight-1;j++){for(i=1;i<lWidth-1;i++){//根据双向一次微分公式计算当前像素的灰度值temp=(BYTE)sqrt((float)((lpDIBBits[lWidth*j+i]-lpDIBBits[lWidth*j+(i-1)])*(lpDIBBits[lW idth*j+i]-lpDIBBits[lWidth*j+(i-1)])+(lpDIBBits[lWidth*j+i]-lpDIBBits[lWidth*(j-1)+i])*(lpDIBBits[lWidth*j+i]-lpDIBBits[lWi dth*(j-1)+i])));if (temp>=t){if((temp+100)>255)lpNewDIBBits[lWidth*j+i]=255;elselpNewDIBBits[lWidth*j+i]=temp+100;}if (temp<t)lpNewDIBBits[lWidth*j+i]=lpDIBBits[lWidth*j+i];}}// 复制变换后的图像memcpy(lpDIBBits, lpNewDIBBits, lWidth * lHeight);//释放内存LocalUnlock(hNewDIBBits);LocalFree(hNewDIBBits);return TRUE;}// 此函数实现门限梯度锐化处理//如果之前没加载图像,将在这里提示if(flag==FALSE){AfxMessageBox("请先加载要处理的照片图像!");return;}CPoint point;CSize size;point.x=0;point.y=0;LONG lWidth=m_PhotoImage.GetWidth(); //获得灰度图像的宽度LONG lHeight=m_PhotoImage.GetHeight(); //获得灰度图像的高度size.cx= lWidth ;size.cy= lHeight;CDC *pDC=GetDC();m_PhotoImage.Draw(pDC,point,size);//绘制处理前的图像CSharpenProcessDib Sharpen(&m_PhotoImage);//创建一个CSharpenProcessDib对象BYTE t=30;Sharpen.GateGrad(t); //调用门限梯度锐化处理函数CPoint point1;point1.x=lWidth+20; //+20是为了让两个图像显示时有个间隙point1.y=0;m_PhotoImage.Draw(pDC,point1,size);//绘制处理后的图像7、编译运行点击快捷键!编译运行刚才的代码,如果没有出错则可单击“图像处理”――》“显示原图像”和“显示锐化后的图像”,选择图像打开,有错则对图从第一部分重新新一步一步调试。
