燃料及其应用
九年级上册化学燃料及其运用洋葱

九年级上册化学燃料及其运用洋葱
化学燃料及其运用洋葱
化学燃料是指能够燃烧产生热能的物质,用于供给能量。
常见的化学燃料包括煤炭、石油、天然气和木柴等。
这些燃料主要由碳和氢构成,当其与氧气发生化学反应时,会产生水和二氧化碳,并释放出大量的热能。
洋葱是一种常见的蔬菜,不仅可以用于烹饪,还具有一些特殊的化学性质。
洋葱含有硫化合物,这些化合物能够刺激眼睛,使人流泪。
洋葱中的硫化合物在切割时与空气中的酸性物质反应,产生一种刺激性的物质,进入到眼睛中会引起泪腺分泌泪液的反应,以此来清洗眼球表面。
与化学燃料有关的洋葱使用是洋葱灯。
洋葱灯是一种利用洋葱作为容器、蜡烛作为燃料的照明工具。
制作洋葱灯时,将洋葱切割成一半,并在内部挖去一部分洋葱肉,然后放入蜡烛,并点燃蜡烛。
蜡烛燃烧时,会产生热能,将热能传递给洋葱,使其发出光亮。
这种照明方式在露营或户外活动中常被使用,因为洋葱灯便于制作,并且既能照亮周围环境,又能作为一种风景装饰。
总的来说,化学燃料及其运用洋葱主要涉及化学燃料的定义、洋葱的化学性质以及洋葱灯的制作和运用。
这个话题不仅能帮助我们理解燃料的概念,还能通过洋葱的特殊性质进行实际应用。
高一化学燃料知识点总结归纳

高一化学燃料知识点总结归纳在高一化学学习中,燃料是一个重要的领域,我们需要了解不同类型的燃料及其应用。
本文将对高一化学燃料知识点进行总结归纳,以帮助大家更好地理解和掌握相关知识。
I. 燃料的定义和分类燃料是指可以燃烧并释放能量的物质。
根据燃料来源和化学组成不同,燃料可以分为化石燃料和生物质燃料两大类。
1. 化石燃料化石燃料是来自生物化石或地球内部变化的物质,主要包括石油、天然气和煤炭。
石油是一种液态燃料,由于其高能量密度和易于储存和运输的特点,广泛用于交通工具和能源供应。
天然气主要是甲烷,也是一种重要的燃料,广泛应用于家庭和工业生产。
煤炭是一种固态燃料,它的燃烧可以产生大量的热能,用于电力和工业。
2. 生物质燃料生物质燃料是指来自植物和动物的有机物,如木材、秸秆、农作物残余物等。
生物质燃料的燃烧过程中产生的二氧化碳可以被植物再次吸收,形成一个循环,因此它被认为是一种可再生的能源。
II. 燃烧反应和热量计算燃料在燃烧过程中会产生热量,并与氧气发生氧化反应。
在学习燃烧反应时,我们需要了解燃料的化学式和反应方程式,并能够计算燃烧产生的热量。
1. 燃烧反应燃料的燃烧反应一般为燃料与氧气的反应,产生二氧化碳、水和能量。
例如,甲烷的燃烧反应为:CH4 + 2O2 → CO2 + 2H2O。
2. 热量计算燃烧反应释放的热量可以通过计算燃烧热来获得。
燃烧热是指完全燃烧1摩尔燃料所释放的热能。
我们可以使用燃烧热公式进行计算,如甲烷的燃烧热为-890 kJ/mol。
III. 燃料的利用与环保问题燃料的利用不仅与能源供应有关,也与环境保护密切相关。
在研究燃料利用和环境问题时,我们需要了解燃料的燃烧特性以及燃烧产生的污染物。
1. 燃料的利用燃料在不同的场合有着不同的利用方式。
例如,石油可以通过精馏分离出不同的燃料,如汽油、柴油和液化石油气,以满足不同机械设备的需求。
同时,燃料还可以用于发电,通过燃烧产生蒸汽驱动涡轮机发电。
初中化学第七单元 燃料及其利用

图7-11 粉尘爆炸实验 现象:实验中观察到塑料盖被弹起
分析:面粉燃烧产生大量的气体和热量,使金属筒内压强增大
《“四清”回归教材PPT》
第七单元 燃料及其利用
图7-12 加油站严禁烟火
图7-13 一些与燃烧和爆炸有关的图标
《“四清”回归教材PPT》
第七单元 燃料及其利用
练习与应用
1.消防员用高压水枪灭火,此措施依据的灭火原理是什么? 答:破坏燃烧的条件,利用水蒸发时吸热来降低温度,使温度降到可燃 物的着火点以下。
《“四清”回归教材PPT》
第七单元 燃料及其利用
5.请你用化学知识解释成语“釜底抽薪”“钻木取火”“火上浇油”。
答:三个成语都体现了燃烧的条件这一化学知识。 “釜底抽薪”:薪指柴,是可燃物,即通过清除可燃物的方法达到灭火的目的。 “钻木取火”:木头本身是可燃物,且较为粗糙,在摩擦时会产生热量,当温度 上升达到木屑的着火点时,又有氧气的存在,满足燃烧的三个条件,所以就会 发生燃烧。 “火上浇油”:油是常见的可燃物燃烧时会放出热量,因此向火中浇油会使燃烧 更旺。
实验7-3 在一支试管中加入一小匙干燥的生石灰(或几小块食品袋中的干燥剂,主要成 分为CaO),再加入约2mL水.观察现象,并用手轻轻触碰试管外壁。
现象
生石灰与水剧烈反应,产生大量 水蒸气,放热
手的感觉 手触摸试管外壁时,试管外壁发烫
化学方程式
CaO+H2O===Ca(OH)2
图7-14 生石灰与水反应放出热量
《“四清”回归教材PPT》
第七单元 燃料及其利用
3.用生煤火炉时,可点燃木柴(劈柴)来引燃煤,你能解释这是为什么吗? 答:不同物质的着火点不同。木柴的着火点比煤低,易被点燃。所以生 煤火时先点燃木柴,再利用木柴燃烧放出的热量引燃煤块就容易的多了。
燃料及其应用

大气污染
大气污染
燃料燃烧会产生各种有害气体和颗粒物,如硫氧化物、氮氧化物、一氧化碳和烟尘等。这些污染物不 仅对人体健康产生负面影响,还会导致酸雨、光化学烟雾等环境问题。
大气污染的治理
为了减少大气污染,需要采取一系列措施,如控制燃煤质量、采用清洁燃烧技术、推广新能源汽车等 。此外,还需要加强环境法规的制定和执行,提高公众环保意识。
太阳能发电
太阳能电池板将光能转换为电能。
03
燃料对环境的影响
碳排放
碳排放
燃料燃烧会产生大量的二氧化碳,这 是全球气候变暖的主要原因之一。碳 排放不仅影响全球气候,还对人类健 康产生负面影响,如引发呼吸道疾病 等。
碳排放的减少
为了减缓全球气候变暖,需要减少燃 料燃烧产生的碳排放。可以通过使用 更高效的能源、推广可再生能源、提 高能源利用技术和采用碳捕获和储存 技术等手段来实现。
02
研发更高效、低耗的发动机技术,提高燃油利用率。
混合动力技术
03
将电动机和内燃机结合,实现能源的互补和优化,提高燃料效
率。
感谢您的观看
THANKS
液体燃料
石油
石油是主要的液体燃料来源,可用于汽车、飞机、船舶等交通工具以及工业生 产。其优点是能量密度高、便于运输,但开采和使用过程中会对环境造成污染。
生物燃料
生物燃料是从生物质中提取的燃料,如乙醇和生物柴油。其优点是可再生、环 保,但生产过程中需要大量土地和资源。
气体燃料
天然气
天然气是一种清洁的燃气,可用于家庭取暖、烹饪和工业生 产。其优点是燃烧无烟、环保,但运输和储存难度较大。
化工生产
石油和天然气是许多化工产品的主 要原料,如塑料、合成纤维和化肥。
燃料的利用和环境保护

建设一批可再生能源示范项目,推动可再生 能源的广泛应用和产业快速发展。
减少温室气体排放的措施
强化节能减排
加强节能减排工作,推行清洁生产、 绿色制造等技术,降低能源消耗和排 放。
发展低碳产业
推动低碳产业的发展,鼓励企业采用 低碳技术和生产方式,减少碳排放。
推广低碳交通
推广低碳交通方式,发展公共交通和 新能源汽车,减少交通碳排放。
燃料的发现
随着文明的进步,人们开始发现 并利用各种新的燃料资源,如煤 炭、石油和天然气等。
燃料在历史时期的利用
古代燃料的利用
在古代,燃料主要用于烹饪、取暖和 照明。木材、草和动物脂肪是当时最 主要的燃料。
工业革命时期的燃料
随着工业革命的到来,煤炭和石油开 始被广泛用于发电和工业生产。
现代燃料的种类与用途
燃料的利用和环境 保护
contents
目录
• 燃料的历史与演变 • 燃料的利用方式 • 环境保护的重要性 • 燃料的清洁利用技术 • 环境保护的实践与措施 • 燃料利用和环境保护的未来展望
01
CATALOGUE
燃料的历史与演变
燃料的起源与发现
燃料的起源
燃料的历史可以追溯到史前时期 。最早的燃料使用者是古人类, 他们发现并开始利用木材、草和 其他可燃物质。
05
CATALOGUE
环境保护的实践与措施
提高能源利用效率的措施
优化能源结构
提高清洁能源比重,降低传统 化石能源比重,通过技术进步 和产业升级,提高能源利用效
率。
强化能源管理
加强能源计量、监测和统计, 建立完善的能源管理体系,提 高能源利用效率。
推广节能技术
推广先进的节能技术和设备, 提高能源利用效率。
第七单元 燃料及其应用
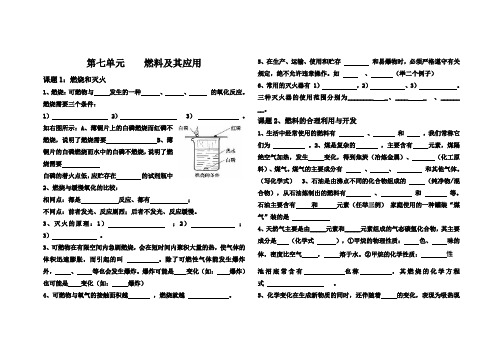
第七单元燃料及其应用课题1:燃烧和灭火1、燃烧:可燃物与发生的一种、、的氧化反应。
燃烧需要三个条件:1) 2) 3)。
如右图所示:A、薄铜片上的白磷燃烧而红磷不燃烧,说明了燃烧需要 B、薄铜片的白磷燃烧而水中的白磷不燃烧,说明了燃烧需要白磷的着火点低,应贮存在的试剂瓶中2、燃烧与缓慢氧化的比较:相同点:都是反应、都有;不同点:前者发光、反应剧烈;后者不发光、反应缓慢。
3、灭火的原理:1);2);3)。
3、可燃物在有限空间内急剧燃烧,会在短时间内聚积大量的热,使气体的体积迅速膨胀,而引起的叫。
除了可燃性气体能发生爆炸外,、等也会发生爆炸。
爆炸可能是变化(如:爆炸)也可能是变化(如:爆炸)4、可燃物与氧气的接触面积越,燃烧就越。
5、在生产、运输、使用和贮存和易爆物时,必须严格遵守有关规定,绝不允许违章操作。
如、(举二个例子)6、常用的灭火器有 1),2)、3)。
三种灭火器的使用范围分别为________ _、____ _ 、______ __。
课题2、燃料的合理利用与开发1、生活中经常使用的燃料有、和,我们常称它们为。
2、煤是复杂的,主要含有元素,煤隔绝空气加热,发生变化,得到焦炭(冶炼金属)、(化工原料)、煤气。
煤气的主要成分有、、和其他气体。
(写化学式) 3、石油是由沸点不同的化合物组成的(纯净物/混合物),从石油炼制出的燃料有、和等。
石油主要含有和元素(任举三例)家庭使用的一种罐装“煤气”装的是4、天然气主要是由_____元素和_____元素组成的气态碳氢化合物,其主要成分是(化学式),①甲烷的物理性质:色、味的体,密度比空气,溶于水。
②甲烷的化学性质:性池沼底常含有也称,其燃烧的化学方程式。
5、化学变化在生成新物质的同时,还伴随着的变化,表现为吸热现象和现象,如燃烧,伴随有现象。
6、要使燃料充分燃烧,要注意两点:一是;二是。
7、煤燃烧时会排出(化学式)、(化学式)等污染物,这些气体溶于雨水,会形成。
低热值气体燃料燃烧技术及其工业应用

低热值气体燃料燃烧技术及其工业应用
低热值气体燃料燃烧技术是利用低热值气体作为燃料进行燃烧过程的技术。
低热值气体燃料主要指氢气、合成气、炉煤气、沼气、焦炉煤气等。
低热值气体燃烧技术的工业应用非常广泛。
以下是一些常见的工业应用:
1. 发电:利用低热值气体燃料发电是一种常见的应用。
这种发电方式可以有效地利用低热值气体,提高能源利用效率。
例如,合成气发电站使用合成气作为燃料,通过燃烧发电。
2. 加热和蒸汽产生:低热值气体燃料可以用于加热工业生产过程中的原料或介质,以及产生蒸汽用于供热或发电。
例如,炉煤气可以用于炉膛加热,并产生蒸汽用于供暖或发电。
3. 炼化与化工过程中的燃料:在炼油、化工等行业中,低热值气体燃料可以作为燃料供给燃烧炉或其他热源设备,为炼化和化学过程提供所需的能量。
4. 燃气轮机和燃气内燃机动力装置:低热值气体燃料可以用于驱动燃气轮机或燃气内燃机动力装置。
这种应用能够转化低热值气体的化学能为机械能,提供动力。
5. 城市燃气供应:低热值气体燃料还可以作为城市的燃气供应,用于家庭和工业用户的烹饪、供暖等需求。
低热值气体燃料燃烧技术的工业应用对能源的有效利用具有重要意义,可以提高能源利用效率,降低能源消耗和环境污染,促进可持续发展。
九年级上册化学燃料及其运用洋葱

九年级上册化学燃料及其运用洋葱
化学燃料是指能够产生燃烧现象并释放能量的物质。
常见的化学燃料有煤炭、石油、天然气等,但在一些特殊情况下,一些生物物质也可以作为燃料使用,洋葱就是其中之一。
洋葱是一种常见的蔬菜,它含有大量的水分、蛋白质、脂肪和碳水化合物等有机物。
这些有机物在燃烧时会与氧气反应,产生热量和二氧化碳、水等副产物。
由于洋葱中的有机物与碳氢化合物的含量较高,它可以被用作一种简单的燃料。
使用洋葱作为燃料时,首先需要将其切成薄片或碎块,以增加其表面积。
然后将洋葱放入一个容器中,加入适量的氧气,点燃洋葱。
在燃烧过程中,洋葱的有机物与氧气反应,释放出热量、二氧化碳和水等产物。
这些产物可以用来进行实验室的化学反应,或者提供热量用于加热等应用。
然而,由于洋葱所含有的有机物相对较少,其作为燃料的效能和能量密度较低。
因此,在实际应用中,洋葱燃料的使用较为有限,更多的是作为一种教学和实验的材料。
总的来说,洋葱作为一种化学燃料的使用在实际中不常见,主要用于教学和实验,用来展示有机物的燃烧现象以及提供能量等方面的应用。
在日常生活中,我们更常使用煤炭、石油等常见的化石燃料来满足能源需求。
燃料电池的原理及其应用案例

燃料电池的原理及其应用案例随着全球环保意识的加强,能源领域也在不断探索创新方案。
燃料电池作为一种新兴的清洁能源,受到了广泛关注。
那么什么是燃料电池?它的原理是什么?有哪些应用案例呢?今天我们就来一起了解一下。
一、燃料电池的原理燃料电池的核心原理是利用氢气与氧气之间的化学反应,将化学能转化为电能。
具体的反应过程如下:在正极(即阳极):氢分子(H2)经过催化剂的作用分解成为离子态的氢气(H+)和电子(e-)。
2H2 -> 4H+ + 4e-在负极(即阴极):氧气与水分子(H2O)反应,生成氢氧离子(OH-)。
电子通过外部电路将阴极流回阳极,与氢离子结合,生成水分子,并释放出电子。
O2 + 4H+ + 4e- -> 2H2O整个反应过程是电化学过程,化学反应产生电子,电子通过外部载流体系向负极流动,从而在利用一次电化学反应中实现了电能的转化。
二、燃料电池的应用案例燃料电池应用领域广泛,目前主要应用于交通工具、家用电力和移动电源等领域。
1、交通工具燃料电池汽车是目前应用最广泛的燃料电池产品,其优点在于零排放、低噪音、高效率等。
目前全球已有多家汽车厂商推出燃料电池汽车,如丰田、本田、日产等。
2、家用电力燃料电池强化了家庭的能源独立和可再生性,成为家庭能源基础设施的新选择。
目前一些国内国际厂商也开始将目光投向家用能源领域。
如阿里巴巴旗下的菜鸟物流,正在推广利用燃料电池的货车,以提高物流效率、减少降低污染。
3、移动电源应用最广泛的移动电源领域是智能手机、平板电脑、移动硬盘、数码相机等,这些产品对于电力源的轻量化、小型化、大容量化的需求与燃料电池特性相近。
近年来,越来越多的厂商将燃料电池作为向纵深发展的新方向,作为移动电源市场的一种新选择。
三、总结燃料电池是一种环保、高效的新型能源方案,其应用不仅提高了环保意识,同时也带来了经济效益和发展机遇。
目前,燃料电池技术还存在一些挑战,如成本高、稳定性差、可扩展性弱等,但随着技术的不断发展和突破,相信燃料电池将会逐渐成为未来能源领域的重要力量。
初中化学燃料及其利用教案

初中化学燃料及其利用教案教案:燃料及其利用一、教学目标:1.了解什么是燃料,掌握燃料的定义和特点。
2.了解燃料的分类及其特点。
3.了解煤、石油和天然气的形成和利用。
二、教学内容:1.燃料的定义和特点。
2.燃料的分类和特点。
3.煤、石油和天然气的形成和利用。
三、教学过程:导入:教师用图片或视频展示不同的燃料,引导学生讨论他们的共同点和不同点。
1.燃料的定义和特点:教师介绍燃料的定义:燃料是一种燃烧产生热能的物质,它能够为人类生产和生活提供能量。
教师解释燃烧产生热能的过程,并引发学生思考:为什么燃料能够产生热能?学生思考后,教师进一步解释:燃料中的化学能在燃烧时转化为热能和光能。
2.燃料的分类和特点:教师介绍常见的燃料分类:固体燃料、液体燃料和气体燃料。
教师依次介绍固体燃料、液体燃料和气体燃料的特点和应用范围。
-固体燃料:如煤、木材等,密度大、容易储存和运输,燃烧时间较长,广泛应用于供暖和发电。
-液体燃料:如石油、天然气等,密度适中,易于储存和运输,燃烧时间适中,广泛应用于交通运输和发电等领域。
-气体燃料:如天然气、丙烷等,密度小,易于储存和运输,燃烧时间较短,广泛应用于家用燃气和燃气发电等领域。
3.煤、石油和天然气的形成和利用:教师简要介绍煤、石油和天然气的形成过程:-煤:由古代植物经过长时间压实而形成,是地下埋藏的矿物燃料。
-石油:由古代生物的遗体经过长时间压实而形成,是液体燃料。
-天然气:由古代生物的遗体通过压力和温度作用下形成,是气体燃料。
教师介绍煤、石油和天然气的利用方式和应用范围:-煤:使用煤可以发电、供暖、冶炼和化工等。
-石油:使用石油可以制造汽车燃料、润滑油、化妆品等。
-天然气:使用天然气可以供应家庭烹饪用气、发电和工业生产等。
四、课堂小结:教师引导学生回顾今天的课程内容,并对燃料的定义、分类及其利用进行总结。
五、课后作业:让学生选择一个燃料进行深入研究,包括燃料的特点、形成过程和利用方式等,并撰写一篇100字以上的作文。
燃料及其燃烧特性

03
燃烧特性
燃烧过程
熄火阶段
当燃料与氧化剂耗尽或燃烧条件不再满足 时,燃烧终止。
燃烧过程
燃烧是燃料与氧化剂之间的化学反应,释 放出能量。这个过程可以分为预混合、点 火、燃烧和熄火四个阶段。
预混合阶段
燃料与氧化剂预先混合,形成可燃混合物 。
燃烧阶段
燃料与氧化剂在火焰中继续反应,释放出 能量。
燃料及其燃烧特性
目录
• 燃料简介 • 燃料特性 • 燃烧特性 • 燃料与燃烧技术 • 燃料与能源未来发展
01
燃料简介
燃料的定义与分类
分类
燃料可以根据来源分为化石燃 料、生物燃料和核燃料等。
生物燃料
如木材、农作物废弃物等,由 生物质在一定条件下转化而成。
定义
燃料是能够提供能量的物质, 通常在燃烧过程中释放能量。
燃料的重要性
01
02
03
提供能量
燃料是提供能量的主要来 源,支撑着人类社会的生 产和生活活动。
促进经济发展
燃料的应用促进了交通运 输、工业生产和能源产业 的发展,对经济发展具有 重要意义。
影响环境
燃料的燃烧会产生污染物, 对环境造成影响,因此需 要合理利用和开发清洁能 源。
02
燃料特性
物理特性
化石燃料
如煤、石油和天然气,由古代 生物遗体在长期的地质过程中 形成。
核燃料
如铀、钚等放射性元素,可用 于核裂变反应释放能量。
燃料的应用领域
能源供应
燃料是能源的主要来源,用于发电、供暖、交通 运输等领域。
工业生产
燃料广泛应用于各种工业生产过程,如钢铁、化 工、陶瓷等。
交通运输
燃料是交通工具的主要能源,如汽车、飞机和船 舶等。
初中化学知识点归纳:第七单元 燃料及其应用

第七单元《燃料及其应用》第一节 燃烧和灭火一、 燃烧⏹ 定义:通常的燃烧是指可燃物跟氧气发生的一种发光、放热的剧烈的氧化反应。
⏹ 探究燃烧的条件(本实验要在通风橱或抽风设备下进行):【实验操作】a. 如右图(1),在500mL 的烧杯中注入400mL热水,并放入用硬纸圈圈住的一小块白磷。
在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷,观察现象。
b. 如右图(2),用导管对准上述烧杯中的白磷,通入少量氧气(或空气),观察现象。
【实验现象】a. 铜片上的白磷燃烧,铜片上的红磷和水中的白磷没有燃烧。
b. 白磷在水下燃烧。
【实验分析】如右图(1)。
①与②对比,说明:物质是否发生燃烧与可燃物燃烧所需要的温度有关。
①与③对比,说明:物质是否发生燃烧与是否与氧气(空气)接触有关。
③与图(2)对比,再次说明:燃烧必须有氧气(空气)。
【实验结论】燃烧的条件:可燃物、与氧气(或空气)接触、温度达到着火点 ⏹ 通风橱是一种不完善的尾气处理装置,若改进上述实验,可将红磷和白磷装入密闭的容器内(还要套一个气球),这样便于进行尾气处理。
⏹ 燃烧的条件:① 可燃物;② 与氧气(或空气)接触;③ 温度达到着火点。
【注意事项】① 着火点不是固定不变的。
对固体燃料来说,着火点的高低跟表面积的大小、颗粒可惜的粗细、导热系数的大小等都有关系。
② 并非所有的燃烧都需要氧气,如氢气在氯气中燃烧生成氯化氢。
③ 只有三个条件全部满足,燃烧才能发生。
⏹ 自燃:由缓慢氧化引起的自发燃烧。
二、 灭火⏹ 灭火的原理:(1)①清除可燃物或使可燃物与其他物品隔离;②隔绝氧气(空气);③降低可燃物的温度,使其降低到着火点以下。
【注意事项】①着火点是可燃物着火燃烧时所需的最低温度,是物质的一种性质,不随外界条件的变化而变化。
②在燃烧的三个条件中,只需破坏一个条件就可以使燃烧停止。
⏹灭火器◆泡沫灭火器的反应原理:Na2CO3+2HCl=2NaCl+H2O+CO2↑◆干粉灭火器的反应原理:2NaHCO 3Na2CO3+H2O+CO2↑◆二氧化碳灭火器内盛装的是液态二氧化碳,使用时不会留下任何痕迹。
九年级上册燃料及应用知识点

九年级上册燃料及应用知识点燃料是我们日常生活中非常重要的能源来源,我们离不开燃料的供应。
九年级上册物理课程中,我们学习了关于燃料及其应用的相关知识点。
本文将就这些知识点进行详细探讨。
一、燃料的定义和分类燃料是指在适当的条件下能够燃烧,释放出能量的物质。
根据其来源和性质的不同,燃料可以分为化石燃料、生物质燃料和可再生能源三类。
1. 化石燃料化石燃料主要是指石油、煤炭和天然气等,它们是遥远地质时代植物和动物的遗存物质,富含碳元素,是人类主要的能源来源之一。
化石燃料是非常重要的能源,但同时也带来了环境污染和气候变化等问题。
2. 生物质燃料生物质燃料是指植物或动物的可再生有机物质,如木材、秸秆、沼气等。
它们可以通过燃烧释放出能量,同时又可以再生,减少对环境的影响。
生物质燃料是一种可持续的能源形式,能够有效解决能源短缺和环境问题。
3. 可再生能源可再生能源指的是能够源源不断地获得和利用的能源,如太阳能、风能、水能等。
与化石燃料相比,可再生能源更加环保和可持续,是未来能源发展的重要方向。
二、燃烧的条件与类型燃烧是指物质在适当的条件下与氧气反应,释放出能量的过程。
燃烧的条件主要有燃料、氧气和着火温度三个要素。
1. 燃料燃料是燃烧的物质基础,它需要具备易燃性和热量高的特点。
易燃性指的是燃料在一定条件下能够燃烧并释放出能量,而热量高则表示单位质量的燃料能够释放出较大的能量。
2. 氧气氧气是燃烧必需的物质,它与燃料反应,使得燃料能够充分氧化并释放出能量。
在空气中,氧气的含量为约21%,是燃烧过程中必不可少的。
3. 着火温度着火温度是指燃料在一定条件下开始燃烧的最低温度。
当燃料达到着火温度时,燃料与氧气发生反应,燃烧才能够持续进行。
根据燃烧过程中是否产生明火,燃烧可以分为明火燃烧和隐火燃烧两种类型。
明火燃烧是指燃烧时产生明显的火焰和烟雾,如蜡烛燃烧;隐火燃烧是指燃烧时没有明显的火焰和烟雾,如煤气燃烧。
三、燃烧的能量转化燃烧释放的能量主要以热能为主,同时还会产生其他形式的能量转化。
燃料及其应用

1.燃烧:(3)注意点:A:燃烧是剧烈的氧化反应,有发光,放热等现象,在缓慢氧化反应的过程中也有放热的想象,只是不易被察觉,如铁生锈,食物的腐败等。
B:燃烧必须三个条件同时满足才会进行。
1.灭火的原理:(1)消除可燃物(2)隔绝氧气(或空气)(3)降温到着火点以下。
注:燃烧的三个条件必须同时满足时才会进行燃烧,但是灭火只要三者中有一个满足就可以达到灭火的目的了。
2.灭火的常用方法:(1)将可燃物撤离燃烧区,与火源隔离(2)将可燃物与氧气(或者空气)隔离。
(3)用大量的冷却剂(如水等)去冷却可燃物,使温度降低到燃烧点一下。
(4)用灭火器灭火3.常见灭火器:泡沫灭火器:扑灭木材、棉布等燃烧引起的失火。
干粉灭火器:扑灭一般的失火外,还可以扑灭电器、油、气等燃烧引起的失火。
液态二氧化碳灭火器:扑灭图书、档案、贵重设备、精密仪器等处的失火注意:用水灭火的原理;燃烧木柴时,通常把木柴架空才能燃烧得更旺;例1、镁等活泼金属可以在二氧化碳中剧烈燃烧,金属钠遇水可能会发生爆炸,它们都不与煤油反应,有的还可以保存在煤油中。
试推测比镁、钠都活泼的金属钾着火,可以用作灭火剂的是A.水B.干冰C.黄沙D.煤油例2、“可燃冰”是天然气与水在一定条件下形成的晶体物质,化学式可用CH4·8H2O表示,主要存在于冻土层和海底大陆架中,每1 m3“可燃冰”能释放出20m3的甲烷气体.下列说法中不正确的是A.“可燃冰”将成为人类新的后继能源B.“可燃冰”是可再生能源C.“可燃冰”具有清洁卫生的优点D.我国青藏高原冻土层可能存在“可燃冰”4.易燃物和易爆物的安全知识:(1)爆炸的定义:可燃物在有限的空间内急剧的燃烧,就会在短时间内聚集大量的热,使得气体的体积迅速的膨胀而引起爆炸。
(2)爆炸物:可燃性气体,面粉,煤粉等粉尘(3)注意事项:A:爆炸可能是物理变化也可能是化学变化B: 可燃性气体在点燃或加热前都要检验纯度,以防止发生爆炸的危险C:油库、面粉加工厂门口贴有“严禁烟火”的标志:空气中常混有可燃性气体或粉尘,接触到明火,就有发生爆炸的危险D:可燃物与氧气的接触面积越大,燃烧越剧烈(4)爆炸,燃烧,缓慢氧化的异同:A:定义:B:发生条件:燃烧:可燃物;与空气或氧气接触;温度达到着火点爆炸:剧烈燃烧;有限空间缓慢氧化:与空气或者氧气接触C:防范措施:燃烧:可燃物与其他物品隔离;与空气隔离;降低温度至着火点以下。
九年级(7 燃料及其应用)

第七单元 燃料及其利用一、 燃烧的条件可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫做燃烧,燃烧需要三个条件: (1)可燃物; (2)氧气(或空气);(3)达到燃烧所需的最低温度(也叫着火点)。
二、灭火的原理和方法(蜡烛的燃烧现象为什么不同?)清除可燃物或使可燃物与其他物品隔离,隔绝氧气(或空气),以及使温度降到着火点以下,都能达到灭火的目的。
灭火器 灭火原理适用范围泡沫灭火器灭火时,能喷射出大量二氧化碳及泡沫,它们能粘附在可燃物上,使可燃物与空气隔绝,达到灭火的目可用来扑灭木材,棉布等燃烧引起的失火。
的干粉灭火器利用压缩的二氧化碳吹出干粉(主要含有碳酸氢钠)来灭火具有流动性好、喷射率高、不腐蚀容器和不易变质等优良性能,除可用来扑灭一般火灾外,还可用来扑灭油、气等燃烧引起的失火二氧化碳灭火器在加压时将液态二氧化碳压缩在小钢瓶中,灭火时再将其喷出,有降温和隔绝空气的作用灭火时不会因留下任何痕迹而使物体损坏,因此可用于扑灭图书、档案、贵重设备、精密仪器等处的失火。
使用时,手一定要先握在钢瓶的木柄上,否则,会把手冻伤。
生活小常识:1.炒菜时油锅中的油不慎着火,可用锅盖盖灭2.堆放杂物的纸箱着火时,可用水扑灭3.扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉。
三、易燃物和易爆物的安全知识可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。
小结:1.可燃物与氧气发生的一种发光发热的剧烈的氧化反应叫做燃烧,燃烧需要三个条件:(1)可燃物;(2)氧气(或空气);(3)达到的燃烧所需的最低温度(也叫着火点)2.灭火的原理:(1)清除可燃物或使可燃物与其他物品隔离;(2)隔绝氧气(或空气);(3)使温度降到着火点以下。
3.在生产、运输、使用和贮存易燃物和易爆物时,必须严格遵守有关规定,绝不允许违章操作。
燃料和热量天然气天然气主要是由碳和氢组成的气态碳氢化合物,其中最主要的是甲烷(CH4)。
乙醇燃料及其在发动机中的应用

乙醇燃料及其在发动机中的应用
乙醇燃料在发动机中的应用主要通过液态掺烧(与汽油以一定比例混合)形式应用于点燃式发动机上。
乙醇作为一种燃料,具有一些优点。
首先,乙醇汽油的辛烷值高,可以达到110左右,可以替代无铅抗爆添加剂甲基叔丁基醚(MTBE)。
高压缩比可以提高发动机的热效率和动力性,加上其蒸发潜热大,可提高发动机的进气量,从而提高发动机的动力性。
其次,乙醇是含氧燃料,蒸发潜热高,车用乙醇汽油含氧量达35%,使燃料燃烧更加充分,有效降低和减少了有害尾气的排放。
此外,乙醇是优良溶剂,可以有效地消除油箱、油路系统中燃油杂质的凝结。
而且,因为车用乙醇汽油的燃烧特性,能有效的消除火花塞、燃烧室、气门、排气管消声器部位积炭的形成,避免了因积炭形成而引起的故障,延长部件使用寿命。
然而,使用乙醇燃料也需要注意一些问题。
例如,在使用高比例乙醇如E85或E100时,通常需要适合燃用乙醇的特制发动机,其供油系统、进气系统材料需经防腐处理。
此外,乙醇对汽车供油系统的橡胶部件有一定的溶胀作用,对油泵的密封及其他部件的合成橡胶材料大都有轻微的腐蚀、溶胀、软化或龟裂作用。
燃烧的化学原理应用有哪些

燃烧的化学原理应用有哪些简介燃烧是指物质在与氧气反应时产生可见光和释放热能的化学过程。
在自然界和人类生活中,燃烧广泛应用于许多方面。
本文主要介绍燃烧的化学原理及其在生活、工业和科学研究中的应用。
燃烧的化学原理燃烧反应通常需要燃料、氧气和适宜的温度。
燃料是提供能量的物质,它可以是固体、液体或气体。
氧气则是燃烧反应的氧化剂,通过与燃料分子中的碳、氢等元素发生氧化反应释放能量。
燃烧反应是一个自持续的链式反应过程,其中包含着引发反应和传递能量的步骤。
燃烧在生活中的应用1.加热和烹饪:人们在生活中常常使用燃烧来进行加热和烹饪。
炉灶、电磁炉、微波炉等设备利用燃料的燃烧反应产生热能,以加热食物或烹饪食材。
2.提供光和热:燃烧可以用于提供光和热能,如蜡烛、灯泡、煤气灯等都是通过燃烧反应产生可见光和热能来实现照明和取暖。
燃烧在工业中的应用1.能源生产:燃烧广泛应用于能源生产,包括化石燃料的燃烧、核能的利用等。
化石燃料的燃烧产生的热能被用于发电、工业生产等领域。
2.化学合成:燃烧常常用于化学合成反应中,如煤矿气、天然气等是许多化学品的重要原料。
燃烧在科学研究中的应用1.燃烧分析:燃烧分析是一种常用的化学分析方法,通过将样品进行完全燃烧,测定样品中的元素组成和含量。
该方法在环境监测、食品检验、医药研究等领域都有广泛的应用。
2.火焰试验:火焰试验是一种常用的实验方法,通过对物质燃烧时的火焰颜色、形状等特征进行观察和分析,进行物质的鉴定和分析。
结论燃烧作为一种重要的化学反应,在生活、工业和科学研究的各个领域都有重要的应用。
通过燃烧的化学原理,我们可以获得能源、进行化学合成,以及进行化学分析等。
燃烧的应用不仅方便了我们的生活,也推动了社会的发展和科学的进步。
绿色燃料的制备及其在能源领域中的应用

绿色燃料的制备及其在能源领域中的应用随着全球环境问题的不断加剧和人们对可持续发展的日益追求,绿色能源逐渐成为了当今的热门话题。
作为核心的绿色能源之一,绿色燃料备受关注。
本文将阐述绿色燃料的制备以及其在能源领域中的应用。
绿色燃料的制备绿色燃料是指在生产、运输和使用过程中对环境和人体健康影响较小的燃料。
从制备方法上来分,可以分为化石燃料替代燃料、生物燃料和太阳能燃料。
首先,化石燃料替代燃料是目前应用较广泛的绿色燃料之一。
通过改变化石燃料中的化学成分,可以制备出一系列的替代品,如甲醇、合成气、乙醇等。
这类燃料可以替代传统的化石燃料,从而降低二氧化碳等有害物质的排放。
其次,生物燃料也是一类较常见的绿色燃料。
生物燃料主要以生物质作为原料,包括生物柴油、生物乙醇、生物气体等。
这类燃料不仅能够替代化石燃料,还具有可再生的特点,因此也被广泛应用。
最后,太阳能燃料是一类能够直接利用太阳能的燃料,包括太阳能电池、太阳能电解制氢燃料电池等。
这类燃料从源头上就避免了有害物质的产生,因此具有很高的环保价值。
绿色燃料在能源领域中的应用绿色燃料在能源领域中的应用有很多,下面将对这些应用进行介绍。
第一,汽车领域。
现今,汽车正在成为环保型车辆,而绿色燃料就是其中的重要选择。
电动汽车、油电混合汽车和氢燃料汽车等都是绿色燃料在汽车领域中的应用。
这些车辆无论是从马力还是从排放上比传统车辆都有很大的提升,因此未来将有更多的车辆选择绿色燃料。
第二,能源发电领域。
发电行业是二氧化碳排放最高的行业之一,而绿色燃料能够有效减少这一排放量。
例如,太阳能燃料可以直接将太阳能转化为电能,而生物质燃料可以利用废弃物等作为原料燃烧发电,从而降低二氧化碳排放量。
第三,家庭和工业用能领域。
绿色燃料在家庭和工业用能领域中也逐渐发挥作用。
一些能源设备采用绿色燃料,如太阳能电池灯具、生物质炉灶和生物质蒸汽锅炉等,这些绿色燃料在节能减排中发挥了很大的作用。
结语绿色燃料的制备及其在能源领域中的应用是现今环保和可持续发展的热点之一。
核反应堆的燃料性能与应用研究

核反应堆的燃料性能与应用研究在当今能源需求不断增长的时代,核能作为一种高效、清洁的能源形式,正发挥着越来越重要的作用。
而核反应堆的燃料性能及其应用研究则是核能领域的核心课题之一。
首先,让我们来了解一下核反应堆燃料的主要成分。
目前,广泛使用的核燃料是铀和钚。
铀在自然界中存在着多种同位素,其中铀 235是能够发生链式裂变反应的关键同位素。
然而,天然铀中铀 235 的含量仅约 07%,为了满足核反应堆的需求,需要通过一系列的工艺将其浓缩。
钚 239 则通常是在核反应堆中通过铀 238 吸收中子转化而来。
核反应堆燃料的性能主要体现在几个关键方面。
燃料的裂变性能决定了反应堆的功率输出和能量转化效率。
高裂变性能的燃料能够产生更多的能量,同时也能提高反应堆的运行经济性。
燃料的稳定性和耐久性对于反应堆的安全运行至关重要。
在高温、高压以及强辐射的环境下,燃料需要保持结构的完整性,避免出现燃料棒破裂等严重事故。
此外,燃料的放射性毒性和半衰期也需要考虑。
放射性毒性较低、半衰期较短的燃料在处理和处置上相对较为容易。
不同类型的核反应堆对燃料的要求也有所不同。
例如,压水堆通常使用低浓缩铀作为燃料,而快中子反应堆则能够利用钚等易裂变材料,实现核燃料的增殖。
在研究核反应堆燃料性能时,需要综合考虑反应堆的类型、运行条件以及安全要求等因素。
在应用方面,核反应堆燃料的发展为人类带来了诸多好处。
核能发电是目前核能应用的主要领域之一。
相比于传统的化石能源发电,核能发电具有高效、稳定、低碳排放等优点。
一座大型核电厂能够为成千上万的家庭和企业提供可靠的电力供应,大大减轻了对传统能源的依赖,减少了温室气体的排放,对缓解全球气候变化问题具有重要意义。
除了发电,核能还在医疗、工业、科研等领域有着广泛的应用。
在医疗领域,放射性同位素用于诊断和治疗疾病,如癌症的放疗。
在工业方面,利用核技术进行材料辐照改性、无损检测等。
在科研领域,核反应堆为基础科学研究提供了强大的实验手段,促进了物理学、化学、生物学等学科的发展。
燃料在社会发展中的应用教案

燃料在社会发展中的应用教案一、教学目标本课程旨在让学生了解燃料在社会发展中的应用,掌握燃料分类及其特点,并探究燃料在国家能源结构中的地位,让学生感受到燃料对人们生活的巨大影响。
二、教学内容本节课程内容主要包括以下几个方面:1、燃料的概念和分类2、燃料的性质及应用3、燃料的选用原则4、燃料在国家能源结构中的地位三、教学方法本节课程采用讲授、实验和探究相结合的方式进行教学,注重实践操作和理论知识的有机结合。
1、讲授:通过教师的讲授,让学生了解燃料的概念、分类、性质及应用,引导学生对燃料的认识和理解。
2、实验:通过实验操作,让学生亲自制作燃料,体验燃料的特性和应用,培养学生的动手能力和实践操作能力。
3、探究:通过探究燃料在国家能源结构中的地位,让学生了解到燃料对人们生活的巨大影响,激发学生的探究兴趣和思考能力。
四、课堂设计1、引入新课:通过图片及视频展示燃料在我们日常生活中的应用及对环境的影响,引导学生发表意见和感受,吸引学生的注意力,激发学生对燃料的兴趣和探究欲望。
2、知识讲解:对燃料的概念、分类、性质及应用进行讲解,注重理论知识和实际应用相结合,让学生通过实验操作深刻理解燃料的性质和特点。
3、实验操作:学生根据讲授内容和实验指导,进行燃料制作、点燃等操作,让学生亲身体验燃料的应用和特性,感知燃料的巨大能量及其应用价值。
4、探究分析:学生在实验操作之后进行讨论、分析,通过探究燃料在国家能源结构中的地位,让学生了解到燃料对国家经济发展的重要贡献。
5、课堂总结:通过回顾所学习的知识点及本次实验操作,让学生总结本节课的重点内容,并鼓励学生在日常生活中合理使用能源。
五、教学建议本课程可以在学生掌握基础化学知识之后进行,毕竟学生对于化学的一些基本概念有了解之后,对于燃料的认知和理解更为深刻。
在实验环节中,需要教师进行安全及操作指导,防止意外事故的发生。
同时,教师也需要及时引导学生进行讨论与分析,既保证实验进程顺利,又能通过讨论激发学生的思考能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
万邦一对一个性化辅导方案教师:学生:上课时间:8.30 第8 次课课题燃料及其应用考点分析1、熟记燃烧的三个条件2、为灭火提供正确的方法,并且根据燃烧条件解释灭火所用到的原理3、了解三大化石燃料的燃烧以及伴随的能量变化4、能够提供新能源,并掌握氢气做燃料的好处重点难点识记性知识的熟记问题解决能力的提升授课内容:第一部分燃烧和灭火一、燃烧1、概念:可燃物与空气中氧气发生的一种发光、放热的剧烈的氧化反应。
2、条件:(1)可燃物(2)氧气(或空气)(3)温度达到着火点(三者缺一不可,否则不能燃烧)如右图所示:A、薄铜片上的白磷燃烧而红磷不燃烧,说明了燃烧需要温度达到着火点;B、薄铜片的白磷燃烧而水中的白磷不燃烧,说明了燃烧需要氧气白磷的着火点低,应贮存在装有水的试剂瓶中3、燃烧与缓慢氧化的比较相同点:都是氧化反应、都放热;不同点:前者发光、反应剧烈,后者不发光、反应缓慢二、灭火的原理和方法1、燃烧的条件决定着灭火的原理,只要破坏燃烧的任何一个条件,就可以达到灭火的目的2、灭火的原理:(1)消除可燃物(2)隔绝氧气(或空气)(3)降温到着火点以下。
3、泡沫灭火器:扑灭木材、棉布等燃烧引起的失火。
干粉灭火器:扑灭一般的失火外,还可以扑灭电器、油、气等燃烧引起的失火。
液态二氧化碳灭火器:扑灭图书、档案、贵重设备、精密仪器等处的失火4、泡沫灭火器的反应原理,利用碳酸钠与浓盐酸迅速反应产生大量的二氧化碳来灭火化学反应方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑一、爆炸概念发生条件防范措施燃烧可燃物与氧气发生的一种发光、发热的剧烈的氧化反应可燃物;与空气或氧气接触;温度达到着火点可燃物与其他物品隔离;与空气隔离;降低温度至着火点以下爆炸可燃物在有限的空间内发生急剧燃烧,短时间内积聚大量的热,使气体体积迅速膨胀而引起爆炸剧烈燃烧;有限空间严禁烟火缓慢氧化反应进行得很慢,甚至不易察与空气或氧接触觉的氧化反应①可能是化学变化(火药爆炸)也可能是物理变化(车胎爆炸)②化学变化的爆炸:可燃物在有限空间内急速燃烧,放出的热使气体的体积迅速膨胀③可燃性气体(氢气、一氧化碳、甲烷)或粉尘(面粉、煤粉)与空气或氧气混合,遇到明火可能会发生爆炸;可燃性气体在点燃或加热前都要检验纯度,以防止发生爆炸的危险④油库、面粉加工厂门口贴有“严禁烟火”的标志:空气中常混有可燃性气体或粉尘,接触到明火,就有发生爆炸的危险⑤可燃物与氧气的接触面积越大,燃烧越剧烈常见灭火的方法①油锅着火,用锅盖盖灭②电器着火,先应切断电源③煤气泄漏,先应关闭阀门,再轻轻打开门窗,切忌产生火花④酒精在桌面上燃烧,用湿抹布扑盖⑤扑灭森林火灾,将大火蔓延前的一片树木砍掉其它:A、生煤炉火时,需先引燃纸和木材,因为纸和木材的着火点比煤低,容易点燃B、室内起火,如果打开门窗,会增加空气的流通,增加氧气的浓度,反应剧烈,燃烧更旺C、用扇子扇煤炉火,虽然降低了温度,但没有降至着火点以下,反而增加了空气的流通,所以越扇越旺。
用扇子扇蜡烛火焰,虽然增加了空气的流通,但却降低了温度至着火点以下,所以一扇就灭。
第二部分燃料和热量一、化石燃料①包括煤、石油、天然气(都是混合物)②是古代生物遗骸经一系列复杂变化而形成的③属于不可再生能源④合理开采,综合利用,节约使用1、煤①称为“工业的粮食”②组成:主要含碳元素,还含少量的氢、氮、氧、硫等元素③将煤隔绝空气加热,发生化学变化,得到焦炭(冶炼金属)、煤焦油(化工原料)、煤气(主要含氢气、一氧化碳、甲烷),用作燃料;煤气泄漏,会使人中毒,有可能发生爆炸)④煤燃烧会产生SO2、NO2等,会形成酸雨2、石油①称为“工业的血液”②从油井开采出来的石油叫原油,它不是产品③组成:主要含碳、氢元素④炼制原理:利用石油各成分的沸点不同,通过蒸馏使之分离(此分离过程是物理变化)⑤石油各产品:汽油、煤油、柴油(作燃料);沥青(筑路);石蜡(作蜡烛)等⑥石油不可以直接作燃料,会浪费资源3、天然气(1)、有石油的地方一般有天然气,主要成分是甲烷CH4,最简单的有机物,相对分子质量最小有机物A、甲烷的物理性质:无色、无味的气体,密度比空气小,极难溶于水。
B、甲烷的化学性质:可燃性CH4+2O2 CO2+ 2H2O (发出蓝色火焰)注意:1点燃甲烷前要检验纯度(2)、检验某可燃物是否含碳、氢元素的方法:点燃,在可燃物上方罩一个冷而干燥的烧杯,烧杯内壁出现水雾,说明生成了水,证明含有氢元素;把烧杯迅速倒过来,立即注入澄清石灰水,变浑浊,说明生成了二氧化碳,证明含有碳元素。
(如果某可燃物燃烧生成了二氧化碳和水,只能证明一定含碳、氢元素,可能含氧元素)(3)、鉴别氢气、一氧化碳、甲烷:检验燃烧的产物(导出点燃,在火焰上方分别罩一个冷而干燥的烧杯,看烧杯内壁是否出现水雾现象;把烧杯迅速倒过来,立即注入澄清石灰水,看是否变浑浊(4)、沼气的主要成分是甲烷,把秸秆、杂草、人畜粪便等废弃物放在密闭的沼气池中发酵,就可产生甲烷。
在农村,沼气可解决生活用燃料问题和改善环境卫生(5)、可燃冰:埋藏于海底,可以燃烧,主要成分是甲烷水合物,储量是化石燃料总和的两倍将成为替代化石燃料的新能源,开采时如果甲烷气体大量泄漏于大气中,造成的温室效应将比二氧化碳更严重(6)、西气东输:输的是天然气(7)、在化石燃料中,天然气是比较清洁的燃料二、化学变化中的能量变化,能量的变化通常表现为热量的变化a)放出热量:燃料燃烧放热(如化石燃料的燃烧);不通过燃料燃烧也可放热Mg+2HCl=MgCl2+H2↑; CaO+ H2O=Ca(OH) 2b)吸收热量: CO 2+C 2CO;Ba(OH)2 + 2NH4Cl = BaCl2+ 2NH3·H2O利用化学反应产生的能量做饭、取暖、发电、冶炼金属、发射火箭、开山炸石、拆除危旧建筑三、使燃料充分燃烧注意两点:燃烧时要有足够多的空气,燃料与空气有足够大的接触面。
燃料不充分燃烧的后果:产生的热量减少,浪费资源,产生大量的CO等物质污染空气四、燃气泄漏报警器安装的位置应根据燃气的密度决定,如果燃气的密度比空气的大,则安装在墙壁下方,反之,则安装在上方第三部分使用燃料对环境的影响一、燃料燃烧对空气的影响1、煤的燃烧。
煤燃烧时会产生二氧化硫、二氧化氮等污染物。
溶于水,当溶解在雨水中时,就形成了酸雨。
2、酸雨的危害:破坏森林、腐蚀建筑物、使水体酸化影响水生生物的生长等防止酸雨的措施:使用脱硫煤、使用清洁能源等3、汽车用燃料的燃烧。
汽油和柴油作为多数汽车的燃料,它们燃烧时产生的尾气中主要含有一氧化碳、未燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘等大气污染物。
减少汽车尾气对空气污染的措施:改进发动机的燃烧方式,使燃料充分燃烧;使用催化净化装置;使用无铅汽油;使用车用乙醇汽油;汽车用压缩天然气(主要成分是甲烷)作燃料;禁止没有达到环保标准的汽车上路二、使用和开发新的燃料及能源1、乙醇①属于绿色能源中的一种,属于可再生能源②由高粱、玉米、薯类等经发酵、蒸馏而得,俗称酒精③可燃性:C2H5OH+3O22CO2+3H2O④被用作酒精灯、火锅、内燃机的燃料⑤乙醇汽油是混合物,其优点:节省石油资源,减少汽车尾气的污染,促进农业生产2、氢气①最清洁、最理想的燃料:A、原材料资源丰富,B、放热量多,C、产物无污染。
②有可燃性 2H2 + O2 2 H2O③有还原性H2+CuO Cu+ H2O 用于冶炼金属④电解水可得到氢气2 H2O2H2↑+ O2↑,但耗用电能⑤不能广泛使用的原因:制取氢气成本太高且贮存困难3、氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑收集方法:向下排空法(密度比空气下)、排水法(难溶于水)不可用浓盐酸的原因浓盐酸有强挥发性;不可用浓硫酸或硝酸的原因浓硫酸和硝酸有强氧化性4、正在推广或使用的新能源:太阳能、风能、地热能、核能、潮汐能附:初中要求掌握的两种实验室制取气体的装置:一、固 + 固△气体发生装置图:制取氧气:反应原理:2KMnO4 K2MnO4 + MnO2 + O2↑2KClO3MnO2△2KCl+3O2↑二、固 + 液气体发生装置图:①制取氧气:反应原理:2H2O22H2O + O2↑②制取二氧化碳:反应原理: CaCO3+2HCl==CaCl2+H2O+CO2↑③制取氢气:反应原理:Zn+H2SO4=== ZnSO4+H2↑九年级上册化学化学方程式归纳集锦2Mg + O2 点燃2MgO 3Fe + 2O2点燃Fe3O44P + 5O2 点燃2P2 O5 C + O2点燃CO2S + O2 点燃SO2 2H 2O 2 2H 2O+O 2↑2KMnO4 △K2 MnO4 + MnO2 + O2 ↑ 2KClO3MnO2△2KCl + 3O2 ↑2H2 + O2 点燃2H2 O 2H2 O通电2H2 ↑+ O2↑C + O2 点燃CO2 2C + O2点燃2CO3C+ 2Fe2O3高温4Fe + 3CO2↑ C+ 2CuO高温2Cu + CO2 ↑CaCO 3+ 2HCl === CaCl2 + H2 O + CO2↑ CaCO3高温CaO + CO2 ↑CO2 + H2O === H2 CO3 H2 CO3 === H2 O + CO2↑Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O 2CO + O2 点燃2CO23CO+ Fe2 O3高温2Fe + 3CO2 CO+ CuO△Cu + CO2H2 + CuO △Cu + H2 O CH4 + 2O2点燃CO2 + 2H2 OC2 H5OH + 3O2 点燃2CO2 + 3H2 O Zn+H2SO4=== ZnSO4+H2↑MnO2MnO2△课堂训练:一、单项选择题(本大题包括16小题,每小题3分,共48分。
每小题有四个选项,其中只有一个选项符合题意)1.古语道:“人要实,火要虚”。
此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。
从燃烧的条件看,“火要虚”的实质是A.增大可燃物的热值 B.增大可燃物与空气的接触面积C.提高可燃物的着火点 D.提高空气中氧气的含量2.“低能耗”、“低废水”、“低废弃物”是低碳理念的重要内涵。
下列做法不符合低碳理念的是 A.推广利用太阳能 B.家庭电器长期处于待机状态C.循环使用生活用水 D.回收有机垃圾用于生产沼气3. 2010年4月20 ,位于墨西哥湾的一个石油钻井平台发生爆炸并引发大火,然后慢慢沉入海底。
之后发生漏油,每天多达5000桶以上,已持续了一个多月。
则下列说法正确的是A.石油燃烧属于物理变化 B.石油是纯净物C.此事件已对环境造成严重污染 D.为杜绝环境污染,人类应停止一切石油开采4. 2010年6月7日《海南日报》载:科学家发现“土卫六”表面遍布“湖海河流”,这些“湖海流”中的液体并非水,而是液态甲烷和液态乙烷(C2H6)。
