氯化氢与盐酸
氯化氢与盐酸

装 置 图
气体 类型
O2
固+固
H2 CO2
液+固(块状)
Cl2
液+固
加热
不加热
加热
有关仪器的名称:
铁架台(带铁圈、铁夹)、 酒精灯、圆底烧瓶、 石棉网、分液漏斗、 双孔塞、玻璃导管。
向上排空气法
排水法
向下排空气法
方法: 向上排空气法
改进后的装置
请思考图示装置都有哪些用途?
万能瓶
1.A进气,B口出空气,收集比空气重的气体 2.B进气,A口出空气,收集比空气轻的气体。 3. 充满水,B进气,A口出水,可作排水量气装置, 水排入量筒并能测量气体体积。 4. 在瓶内加入适量液态净化剂,从A口进气,B口出 气,可作为气体净化装置。
微热
或:2NaCl(固体)+H2SO4(浓)→ Na2SO4 +2HCl↑
反应有何特点?
温度不同,反应产物不同。
NaCl(固) + H2SO4(浓)
微热
NaHSO4 + HCl
难挥发酸、高沸点酸
易挥发酸、低沸点酸
思考:根据氯气的制法原理请设计制备 一瓶纯净的氯化氢气体的实验装置。
四种常见的气体发生装置
互动探究
给你提供以下仪器,画出制取氯化氢的实验装置 示意图
实验室制取HCl的装置图
三、盐酸
1、 物理性质: 纯净的盐酸是无色的液体,极易 挥发,常用的浓盐酸含氯化氢37%。
化学性质: 一元强酸,具有酸的通性 用途: 是除锈,制药的原料
2、
3、
讨论:
1、工业盐酸为什么显黄色?
2、工业制氯化氢中,氯气为什么 在内管,氢气为什么在外管?
盐酸化学式

盐酸化学式
化学式是指用元素符号和数字的组合表示物质组成的式子,盐
酸也叫氯化氢,它的化学式是HCl,从化学式可以看出,盐酸其实
就是由一个氢原子和一个氯原子通过共价键结合形成的双原子分子。
根据化学式本身的意义,可以从微观和宏观两方面说明盐酸化
学式代表的含义。
微观方面:1、HCl表示一个氯化氢分子;2、表示每个氯化氢
分子由一个氢原子和一个氯原子构成。
宏观方面:1、HCl可以表示盐酸这个物质;2、表示盐酸是由
氢元素和氯元素两种元素组成。
氯化氢及盐酸理化性质及危害特性表
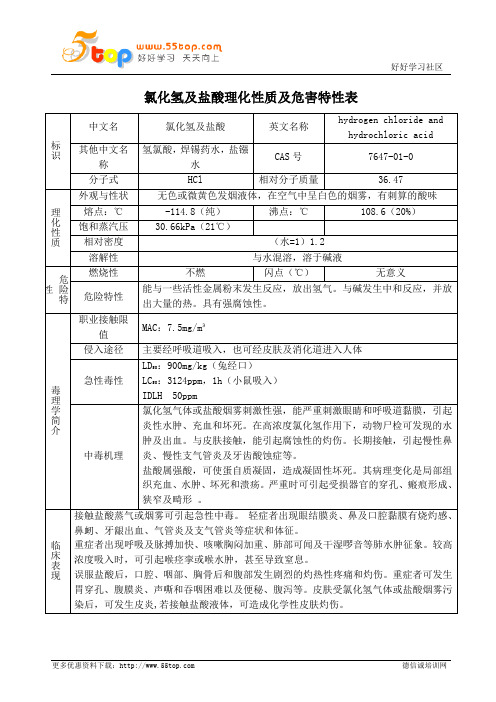
氯化氢及盐酸理化性质及危害特性表标识中文名氯化氢及盐酸 英文名称 hydrogen chloride and hydrochloric acid其他中文名称 氢氯酸,焊锡药水,盐镪水CAS 号 7647-01-0 分子式 HCl 相对分子质量 36.47 理化性质外观与性状无色或微黄色发烟液体,在空气中呈白色的烟雾,有刺算的酸味熔点:℃ -114.8(纯) 沸点:℃108.6(20%)饱和蒸汽压 30.66kPa (21℃)相对密度 (水=1)1.2 溶解性 与水混溶,溶于碱液危险特性燃烧性 不燃闪点(℃)无意义危险特性 能与一些活性金属粉末发生反应,放出氢气。
与碱发生中和反应,并放出大量的热。
具有强腐蚀性。
毒理学简介职业接触限值 MAC :7.5mg/m³侵入途径主要经呼吸道吸入,也可经皮肤及消化道进入人体 急性毒性LD 50:900mg/kg (兔经口)LC 50:3124ppm ,1h (小鼠吸入) IDLH 50ppm中毒机理氯化氢气体或盐酸烟雾刺激性强,能严重刺激眼睛和呼吸道黏膜,引起炎性水肿、充血和坏死。
在高浓度氯化氢作用下,动物尸检可发现的水肿及出血。
与皮肤接触,能引起腐蚀性的灼伤。
长期接触,引起慢性鼻炎、慢性支气管炎及牙齿酸蚀症等。
盐酸属强酸,可使蛋自质凝固,造成凝固性坏死。
其病理变化是局部组织充血、水肿、坏死和溃疡。
严重时可引起受损器官的穿孔、瘢痕形成、狭窄及畸形 。
临床表现接触盐酸蒸气或烟雾可引起急性中毒。
轻症者出现眼结膜炎、鼻及口腔黏膜有烧灼感、鼻衂、牙龈出血、气管炎及支气管炎等症状和体征。
重症者出现呼吸及脉搏加快、咳嗽胸闷加重、肺部可闻及干湿啰音等肺水肿征象。
较高浓度吸入时,可引起喉痉挛或喉水肿,甚至导致窒息。
误服盐酸后,口腔、咽部、胸骨后和腹部发生剧烈的灼热性疼痛和灼伤。
重症者可发生胃穿孔、腹膜炎、声嘶和吞咽困难以及便秘、腹泻等。
皮肤受氯化氢气体或盐酸烟雾污染后,可发生皮炎,若接触盐酸液体,可造成化学性皮肤灼伤。
氯碱氯化氢和盐酸生产基础知识讲解

机氯化物。 HC?lC2H2? C2H3C(l生产氯乙烯的)反应原理
C2H2+HCl→C2H3Cl(生产氯乙烯的反应原理) C2H2+Cl2→CHCCl (氯乙炔爆炸物) + HCl
氯化氢的水溶液称为盐酸,是最常用的无机强酸之一。氯
化氢与潮湿空气中的水分生成白色的烟雾。在干燥的状态下
石墨冷却器的技术特性
可用温度为:–20℃~165℃,可用的压力纵 向为0.4MPa,径向压力为o.4~0.6MPa,圆块 孔式石墨冷却器与石墨列管式冷却器相比,具 有更能经受压力冲击(列管式许用压力仅 0.2MPa)、更耐高温。
盐水工序基础知识
HCL合成炉 剖面图
HCL出口
至 HCL 总管
防爆膜 炉门
防爆膜 视镜
HCL 气体在炉中走向 石墨块
二、吸收器
将经过冷却至常温的氯化氢气体用水或稀盐酸 吸收,成为一定浓度的合格的工业盐酸.膜式吸收 塔是因为氯化氢气体溶于水所释放的熔解热可以经 过石墨管壁传给冷却水带走,因而吸收温度较低, 吸收率较高一般可以达到85%~90%甚至达到 95%以上,所以出酸浓度相应较高.膜式吸收塔 结构可分为三个部分上封头是个圆柱形石墨筒体, 在上官板的每个管端设置有吸收液的分配器,在分 配器内由尾气吸收塔来的吸收液经过环行的分布环 及分配管在分配,当进入处于同一水平面的分液管 v 形切口时吸收液呈螺旋线状的自上而下的液膜(又 称降膜)。
盐水工序基础知识
进气口
进液口
出水口
HCI吸收器 剖面图
下酸口
进水口 出气口
降膜式吸收塔的特点 一般用的膜式吸收塔优于绝热式填料吸收塔,主要是因为
氯化氢和盐酸

喷泉实验 目的: 目的:研究氯化氢的溶解性 现象:烧杯中的石蕊试液喷入烧瓶, 现象:烧杯中的石蕊试液喷入烧瓶, 变成红色,形成喷泉。 变成红色,形成喷泉。 1:500) 结论: 结论:氯化氢极易溶于水 (1:500)
所得盐酸溶液的物质的量浓度是多少?(标况下) 所得盐酸溶液的物质的量浓度是多少?(标况下) ?(标况下
2、盐酸的化学性质 盐酸溶液中存在哪些微粒? 盐酸溶液中存在哪些微粒?
HCl H2O
H+ + Cl- H+ + OH-
盐酸溶液中的微粒: 盐酸溶液中的微粒: H+、Cl-、H2O、(OH-)
酸的通性( (1) 酸的通性( H+ ): 使指示剂变红; A、使指示剂变红; B 、酸+ 碱→盐+ 水 : NaCl+ HCl+NaOH NaCl+H2O 碱性氧化物→ C、酸+碱性氧化物→盐+水: HCl+ 2HCl+CuO CuCl2+H2O 活泼金属→ 氢气: D、酸+活泼金属→盐+氢气: HCl+ 2HCl+Zn ZnCl2+H2↑ 新酸+新盐: E、酸+盐→新酸+新盐: HCl+ 2HCl+CaCO3 CaCl2+H2O+CO2↑
V / 22.4 C= V
045mol/L = 0.045mol/L
C=
V’ / 22.4 = 0.045mol/L 045mol/L V’
形成喷泉实验的条件? 形成喷泉实验的条件? 产生压力差 气体被溶液完全吸收
发生溶解——极易溶于水的气体 极易溶于水的气体 发生溶解 ( HCl 、NH3) 发生反应: 发生反应: CO2 —— NaOH 溶液
二、氯化氢的化学性质 1、干燥的氯化氢气体的化学性质稳定 2、和氨气反应 HCl +NH3 现象: 现象:产生白烟 NH4Cl
盐酸的物理化学性质

盐酸的物理化学性质盐酸是氢氯酸的俗称,是氯化氢(HCl)气体的水溶液,为无色透明的一元强酸。
接下来店铺为你整理了盐酸的物理化学性质,一起来看看吧。
盐酸的物理性质外观:无色液体,有腐蚀性。
为氯化氢的水溶液(工业用盐酸会因有杂质三价铁盐而略显黄色)。
有刺激性气味。
由于浓盐酸具有挥发性,挥发出的氯化氢气体与空气中的水蒸气作用形成盐酸小液滴,所以会看到酸雾。
pKa值:-7密度: 1.18g/cm3熔点: -27.32 ℃ (38%溶液)沸点:110 °C (20.2%溶液);48 °C(38%溶液)相对蒸气密度(空气=1):1.26饱和蒸气压(kPa):30.66(21℃)黏度:1.9 mPa·s, 25 °C(31.5%溶液)溶解性:与水混溶,浓盐酸溶于水有热量放出。
溶于碱液并与碱液发生中和反应。
能与乙醇任意混溶,氯化氢能溶于苯。
盐酸的化学性质强酸性1、和碱反应生成氯化物和水HCl + NaOH = NaCl + H2O2、能与碳酸盐反应,生成二氧化碳K2CO3 + 2HCl = 2KCl+ CO2↑ + H2O3、能与活泼金属单质反应,生成氢气Fe+ 2HCl =FeCl2+ H2↑4、能与金属氧化物反应,生成盐和水MgO+2HCl=MgCl2+H2O5、能用来制取弱酸CaCO3+2HCl=CaCl2+H2O+CO2↑(不用Na2CO3因为反应速率过快,实验室常用盐酸于制取二氧化碳的方法)CH3COONa+HCl=CH3COOH+NaCl6、能和盐反应,生成新酸和新盐2HCl+Na2SO3=SO2↑+H2O+2NaClNa2S2O3+2HCl=2NaCl+H2O+SO2↑+S↓另外,盐酸能与硝酸银溶液反应,生成不溶于稀硝酸的氯化银,氯化银极微溶于水,产生白色的凝乳状沉淀。
HCl+AgNO3===HNO3+AgCl↓还原性2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O4HCl(浓)+MnO2=加热=MnCl2+2H2O+Cl2↑14HCl(浓)+K2Cr2O7==3Cl2(气体)+2CrCl3+2KCl+7H2ONaClO+2HCl=NaCl+Cl2+H2O电离方程式HCl===H+ +Cl-盐酸的制备方法主要是用水吸收氯化氢而得。
氯化氢和盐酸的共同点

氯化氢和盐酸的共同点
氯化氢(HCl)和盐酸是同一种物质的不同形态:
1.共同成分:两者都含有相同的化学成分,即氯原子和氢原子。
2.化学键性质:在纯净的氯化氢分子中,氯与氢之间通过共价键结合。
而当氯化氢溶解于水中形成盐酸时,虽然分子间原有的共价键结构被破坏,但形成的水合氢离子(H3O+)和氯离子(Cl-)中依然包含氢与氯的化学键合作用。
3.酸性表现:无论是气态的氯化氢还是其水溶液——盐酸,都表现出酸性。
在水中,氯化氢完全离解产生氢离子和氯离子,导致溶液显酸性。
4.化学反应活性:它们都能参与许多化学反应,特别是作为酸参与酸碱中和反应、金属氧化物或金属氢氧化物的反应等。
5.挥发性:浓盐酸具有挥发性,能挥发出氯化氢气体,这一点上二者也有关联。
总结起来,氯化氢和盐酸的核心共同点在于它们都源于氯化氢分子,并且在合适的条件下都表现出强烈的酸性特征。
浓盐酸吸收氯化氢的原理

浓盐酸吸收氯化氢的原理浓盐酸吸收氯化氢是指使用浓盐酸(也就是浓硫酸)作为吸收剂来吸收氯化氢气体的一个过程。
这一吸收过程会发生化学反应,属于物理吸收和化学吸收的结合。
下面我从几个方面详细解释这个过程中的原理:一、反应原理浓盐酸吸收氯化氢时,会发生这样一个化学反应:HCl(g) + H2SO4(l) →H3SO4(l) + HCl(aq)即氯化氢气体被浓硫酸吸收,生成氯化氢和硫酸的溶液。
这里浓硫酸作为吸收剂,与氯化氢发生化学反应生成盐,属于化学吸收的一种。
二、吸收dynamics盐酸吸收氯化氢过程的动力学遵循气-液接触吸收的基本规律。
它包含气体分子从气体相向液相的传质过程:1. 气体分子在气液界面发生规律的molecular 碰撞;2. 分子通过液面进入液相,这一步决定了整个吸收速率;3. 气体分子在液体内部扩散和流动。
影响吸收动力学的主要因素还有气液接触方式、界面积大小、温度和压力等。
三、卤化氢溶解度卤化氢溶解度是影响盐酸吸收氯化氢效果的一个重要因素。
卤化氢如氯化氢、溴化氢在水中的溶解度较低,但在浓盐酸中溶解度会大大提高。
这是因为卤化氢和卤化氢钠生成复合离子,溶解度按照次序HCl > HBr > HI。
盐酸浓度越高,卤化氢溶解度越大。
四、热力学分析从热力学的Gibbs自由能变化来看,标准状态下吸收反应的ΔG小于0,说明反应可自发进行。
实际工业条件下,可以通过提高压力来增加反应的驱动力。
另外反应放热,具有良好的热动力学特征。
反应放热可以为后续的氯化氢回收提供热力条件。
五、工业应用案例工业上常用浓盐酸洗涤法来除去各种烃类气体中的痕量氯化氢、溴化氢等杂质。
例如在石油加工的裂化装置、催化重整装置中,都会用浓盐酸吸收法除去反应产生的氯化氢。
此外在一些有机合成过程中也会用到浓盐酸吸收氯化氢。
通过选择合适的操作条件,可以达到很高的去除率。
六、工艺优化方向为进一步提高浓盐酸吸收氯化氢的效果,可以从这些方面进行工艺优化:1. 增加气液接触面积,通常采用填料吸收塔来实现;2. 提高盐酸浓度,因为浓酸可以更好吸收氯化氢;3. 调节操作温度和压力,需要根据具体条件测试最佳参数;4. 回收吸收液中的氯化氢,降低酸液浓度的减少;5. 选择抗腐蚀材料,构建适合的反应设备。
制取盐酸的原理

制取盐酸的原理制取盐酸的原理是通过盐酸的制备反应,即盐酸酸化反应。
通常使用氯化氢气体和水反应制取盐酸。
氯化氢(HCl)是一种无色、刺激性气体。
它是一种强酸,具有极强的腐蚀性,容易溶解在水中形成盐酸(HCl(aq))。
制取盐酸的过程就是将氯化氢气体溶解在水中,生成盐酸溶液。
制取盐酸的反应式可以表示为:HCl(g) + H2O(l) →HCl(aq)具体的制备过程如下:1. 首先需要制备氯化氢气体。
氯化氢气体通常通过酸的金属盐与酸反应得到。
例如,可以通过硫酸(H2SO4)和氯化钠(NaCl)反应制备氯化氢气体。
反应式为:2H2SO4(aq) + 2NaCl(s) →2NaHSO4(aq) + 2HCl(g)2. 将制备好的氯化氢气体通入水中。
将含有氯化氢气体的气体通入到装有水的容器中,可以通过使用分液漏斗或气体导管实现。
通入气体的速率需要控制,以确保反应均匀进行。
3. 盐酸生成。
氯化氢气体与水反应后,生成盐酸溶液。
酸性溶液中的氯氢酸分子会与水中的水分子之间发生化学反应,结合生成盐酸的离子。
反应式为:HCl(g)+ H2O(l) →HCl(aq)4. 过程与控制。
在制备的过程中,需要注意以下几点:- 反应容器和设备应该具有一定的耐腐蚀性,以防止盐酸对其造成损害。
- 通入氯化氢气体的速率需要控制,以确保反应均匀进行,并避免过量的气体逸出。
- 制备过程通常在有足够通风的实验室环境下进行,以保证氯化氢气体的安全处理。
制取盐酸的原理可以通过酸碱理论进一步解释。
在水中,氯化氢气体会溶解产生氯氢酸分子(HCl)和氯化物离子(Cl-)。
氯氢酸是一种强酸,它能够与水分子中的氢键进行竞争性结合,从而形成离子状态的盐酸。
总结一下,制取盐酸的原理是通过盐酸的制备反应,即将氯化氢气体与水反应制备盐酸溶液。
氯化氢气体是一种强酸,其溶解在水中形成盐酸溶液。
制备盐酸的过程需要注意反应容器和设备的耐腐蚀性,控制气体的通入速率以及在有良好通风的实验室环境下进行。
hcl与naclo反应的方程式

hcl与naclo反应的方程式
盐酸与氯化钠反应
盐酸(HCl)与氯化钠(NaCl)之间的反应是一种酸碱中和反应。
这种反应会导致盐的形成,在这种情况下,产物是氯化氢(HCl)和
水(H2O)。
反应方程式
HCl + NaCl → NaCl + H2O
反应类型
中和反应是一种化学反应,其中酸和碱相互作用形成盐和水。
在酸碱中和反应中,酸提供氢离子(H+),而碱提供氢氧根离子(OH-)。
当这些离子结合时,它们会形成水(H2O)。
反应产物
此反应的产物是氯化氢(HCl)和水(H2O)。
氯化氢是一种强
酸,而水是一种中性化合物。
反应条件
盐酸与氯化钠的反应通常在室温下进行。
但是,反应速率可以
通过加热或添加催化剂来增加。
平衡常数
平衡常数是衡量反应在达到平衡时相对产物浓度的量度。
对于
盐酸与氯化钠的反应,平衡常数非常大,表明反应强烈偏向产物侧。
反应用途
盐酸与氯化钠的反应在工业和实验室中都有应用。
例如,该反
应用于生产氯化氢,这是许多化学过程的重要原料。
该反应还用于
生产食盐(NaCl),这是人类饮食中常见的成分。
安全注意事项
盐酸是一种腐蚀性物质,因此在处理时必须小心。
建议戴上手
套和护目镜,并在通风良好的区域进行反应。
如果盐酸与皮肤或眼睛接触,请立即用大量水冲洗。
盐酸中氯化氢分压计算公式

盐酸中氯化氢分压计算公式
在化学实验中,我们经常需要计算气体在混合气体中的分压。
盐酸中氯化氢分压计算公式是一个重要的公式,它可以帮助我们准确计算盐酸中氯化氢气体的分压。
盐酸中氯化氢分压计算公式可以表示为:
P(HCl) = X(HCl) P(total)。
其中,P(HCl)表示氯化氢气体的分压,X(HCl)表示氯化氢的摩尔分数,P(total)表示混合气体的总压强。
这个公式告诉我们,氯化氢气体的分压取决于氯化氢的摩尔分数以及混合气体的总压强。
通过这个公式,我们可以根据实验数据计算出氯化氢气体在盐酸中的分压,从而更好地理解和掌握气体在混合气体中的行为特性。
盐酸中氯化氢分压计算公式的应用不仅局限于化学实验室,它在工业生产和环境监测中也具有重要意义。
通过准确计算氯化氢气体的分压,我们可以更好地控制和管理气体的行为,保障生产安全
和环境健康。
总之,盐酸中氯化氢分压计算公式是化学领域中的重要工具,它帮助我们理解气体行为规律,指导实验操作,保障生产安全,促进科学研究的发展。
我们应该深入学习和掌握这个公式,发挥它在实践中的作用,为化学实验和工业生产提供更准确的数据支持。
氯化氢和盐酸

盐酸物理性质:
纯净的浓盐酸是无色,有刺激性气味和酸味的液体, 具有挥发性,有腐蚀性,浓盐酸在空气中会生成白雾。 工业品浓盐酸常因含有杂质而带黄色。
化学性质:
跟指示剂的反应
石蕊试液遇盐酸变 盐酸跟锌、铁等金属反应, 跟金属的反应 成红色,酚酞试液 都能生成氢气和相应的盐。 遇盐酸不变色。 跟金属氧化物的反应 Zn+2HCl=ZnCl2+H2↑ Fe2O3+6HCl= 2FeCl3+3H2O 跟碱的反应 Cu(OH)2+2HCl= CuCl2+2H2O Fe+2HCl= FeCl2+H2↑ 盐酸跟金属氧化物反应生成 跟硝酸银的反应 可溶性盐,可以用来除锈。 利用盐酸跟碱反应可以减少胃中 可用于制备氢气 盐酸的含量。 HCl+AgNO3= AgCl↓+HNO3
复分解反应的特征
AB + CDC= AD CCCB B B CB C B B CB + +
复分解反应发生的条件
H 2O Cu(OH)2 + 2HCl = CuCl2 + 2H2O
HCl + AgNO3 = AgCl ↓ + HNO3
CaCO3+2HCl=CaCl2+H2O+CO2↑
复分解反应发生的条件
HCl
碱溶液或水
倒吸
吸收不完全
防倒吸
• 2、化学性质
• 氯化氢与盐酸都可用HCl表示,但它们成分不同,性质不同。将两 者列表比较如下:
• 注意: • ①氯化氢与盐酸关系极为密切,可相互 转化 • ②物质的化学性质取决于构成该物质 的各种微粒的性质。如盐酸,由于HCl在 水中电离: • HCl=H++Cl- • 因此盐酸的化学性质就是H+、Cl-离子 性质的总和。
氯化氢和盐酸不一样吗?盐酸和氯化氢有什么区别?

氯化氢和盐酸不⼀样吗?盐酸和氯化氢有什么区别?氯化氢和盐酸不⼀样吗? 盐酸和氯化氢有什么区别,是同⼀种物质吗?我们经常会遇到这样的问题,下⾯和⼩编具体来看⼀下吧。
我们都知道⼀说氯化氢⽓体,可能⼤家都不知道,但是⼀说盐酸,想必⼤家都⾮常熟悉了,那么氯化氢⽓体究竟是什么样的⽓体呢。
我们从⽹上查阅资料知道氯化氢(HCl),⼀个氯化氢分⼦是由⼀个氯原⼦和⼀个氢原⼦构成的,是⽆⾊有刺激性⽓味的⽓体。
其⽔溶液俗称盐酸,学名氢氯酸。
相对分⼦质量为36.46。
氯化氢极易溶于⽔,在0时,1体积的⽔⼤约能溶解500体积的氯化氢。
所以说氯化氢是化合物,它有多种存在状态,可以是⽓体,可以是液体。
纯的氯化氢是分⼦化合物,通常条件下为⽓体,分⼦式为HCl。
盐酸是氯化氢的⽔溶液,分⼦式HCl。
盐酸是混合物,是氯化氢常溶解在⽔中形成,也就是氯化氢和⽔的混合物,不是化合物。
盐酸是氯化氢溶在⽔⾥后,离解成⽔合氢离⼦和氯离⼦的混合物,严格来说应该写为H3O+和Cl-,但作为反式来写,写为HCl即可。
“盐酸是混和物,是HCL(氯化氢)的⽔溶液氯化氢分⼦式是HCL,因此盐酸和氯化氢不是⼀种物质,可以这样说,盐酸是混合物,是氯化氢的⽔溶液,⽽氯化氢是纯净物,常温是⽓态的”。
⽽氯化氢主要⽤于制染料、⾹料、药物、各种氯化物及腐蚀抑制剂等⽅⾯。
盐酸是⼀种⽆机强酸,在⼯业加⼯中有着⼴泛的应⽤,例如⾦属的精炼。
盐酸往往能够决定产品的质量。
在⽇常⽣活中,利⽤盐酸可以与难溶性碱反应的性质,制取洁厕灵、除锈剂等⽇⽤品。
因此,氯化氢和盐酸不是同⼀种物质,千万可不要搞混了。
两者之前有着很⼤的区别,⼀定要根据实际情况来进⾏选择⽤哪种产品合适。
⼭东⾔赫化⼯有限公司作为地区⼀家⾼纯氯化氢⽓体、化学级氯化氢⽓体以及99%硫化氢⽓体产品代理供应机构,其代理的相关⼯业⽓体产品不仅种类多样,纯度不⼀,⽽且储量丰富,价格公道,完全能够满⾜⽣产以及实验室研究等各种需求,因⽽深受⼴⼤需求⼚家的好评,公司也才能成为地区最值得信赖的⽓体供应机构。
2014化学高二必修知识:氯化氢与盐酸

2014化学高二必修知识:氯化氢与盐酸
(1)、浓盐酸被二氧化锰氧化(实验室制氯气)
(2)、盐酸、氯化钠等分别与硝酸银溶液的反应(盐酸及氯化物溶液的检验;溴化物、碘化物的检验)
(3)、盐酸与碱反应
(4)、盐酸与碱性氧化物反应
(5)、盐酸与锌等活泼金属反应
(6)、盐酸与弱酸盐如碳酸钠、硫化亚铁反应
(7)、盐酸与苯酚钠溶液反应
(8)、稀盐酸与漂白粉反应
(9)、氯化氢与乙烯加成反应
(10)、氯化氢与乙炔加成反应(制聚氯乙烯)
(11)、漂白粉与空气中的二氧化碳反应(说明碳酸酸性强于HClO)
(12)、HF、HCl、HBr、HI酸性的比较(HF为弱酸,HCl、HBr、HI为强酸,且酸性依次增强)
(13)、用于人工降雨的物质有哪些?(干冰、AgI)
要多练习,知道自己的不足,对大家的学习有所帮助,以下是为大家总结的2014化学高二必修知识,希望大家喜欢。
hcl的化学名称

hcl的化学名称氯化氢,化学式为HCl,一个氯化氢分子是由一个氯原子和一个氢原子构成的,是无色有刺激性气味的气体。
其水溶液俗称盐酸,学名氢氯酸。
氯化氢极易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。
1hcl是什么化学名称1、氯化氢,化学式为HCl,一个氯化氢分子是由一个氯原子和一个氢原子构成的,是无色有刺激性气味的气体。
其水溶液俗称盐酸,学名氢氯酸。
氯化氢极易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。
2、氯化氢主要用于制染料、香料、药物、各种氯化物及腐蚀抑制剂。
2hcl的化学性质1、能与酸碱指示剂反应。
遇紫色石蕊试液,石蕊变红色,遇无色酚酞酝酿不变色。
2、能与活泼金属反应(金属活动性在氢前的金属)。
如镁,铝,锌、铁反应。
3、能与碱反应。
如氢氧化钠,氢氧化钙反应。
4、能与金属氧化物反应。
如氧化钙、氧化铁等。
5、与某些盐反应。
如碳酸盐(如碳酸钠,碳酸钙)、硝酸银反应。
3氯化氢的物理性质氯化氢是无色,熔点-114.2度,沸点-85度。
有窒息性的气味,对上呼吸道有强刺激,对眼、皮肤、黏膜有腐蚀。
密度大于空气,其水溶液为盐酸,浓盐酸具有挥发性。
摩尔质量36.4606g/mol外观无色吸湿性气体密度1.477g/L(25℃)(气)相对密度(水=1)1.19相对蒸气密度(空气=1)1.27熔点158.8K(-114.2℃)沸点187.9K(-85℃)溶解性(水)72g/100mL(20℃)(标准压强)饱和蒸气压(kPa)4225.6(20℃)。
4氯化氢是什么氯化氢是无色而有刺激性气味的气体。
浓盐酸为无色液体,将其装在瓶中,过一会儿瓶口会产生白雾(由于盐酸有强挥发性,白雾是氯化氢挥发后与空气中的水蒸气结合产生的盐酸小液滴),有刺鼻酸味。
工业用盐酸会因有杂质三价铁盐而略显黄色。
它易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。
氯化氢的水溶液呈酸性,叫做氢氯酸,属于强酸,习惯上叫盐酸。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
的液体由于重力而落回烧杯中 。
倒吸现象
防倒吸原理
实验室制取HCl的装置图
氯化氢与盐酸的对比
HCl
组成 构成微粒 有无酸性 能否使干燥蓝色 石蕊试纸变色
溶于水
挥发
氯化氢
纯净物 HCl分子 无酸性
不能
盐酸
盐酸
混合物 有H+、Cl-离子 有酸性
能
向上 体收集装置
验满:
A、使湿润的蓝色石蕊试纸立即变红 氯化氢溶于水显酸性
B、遇蘸有浓氨水的玻璃棒立即产生大量白烟
NH3+HCl→NH4Cl
利用氯化氢极易溶于水的性质,可用水吸收HCl
倒吸
水
水
漏斗防倒吸原理:当液体被倒吸进漏斗,由于漏斗的
容积很大,于是漏斗和烧杯的液面产生了液面差 ,漏斗中
HCl极易溶于水,烧瓶内的气压迅速降低,与外界大气 压产生了足够的压强差,外界大气压将烧杯内的液体压 入烧瓶中。
形成喷泉的组合
(1)常温常压下 HCl、NO2、NH3与水组合 能形成喷泉。
(2)酸性气体与NaOH溶液组合能形成喷泉, 例如CO2与NaOH,SO2与NaOH等。
氯化氢的制备
1、工业制氯化氢:
H2+Cl2
点燃
→
2HCl
2、实验室制法:
药品:固体NaCl 和 浓硫酸
1)、实验原理
微热
NaCl(固体)+H2SO4(浓)→ NaHSO4 +HCl↑
500-6000
NaCl(固体)+NaHSO4 →
Na2SO4 +HCl↑
NaCl(固) + H2SO4(浓) 微热 NaHSO4 + HCl
难挥发酸、高沸点酸
易挥发酸、低沸点酸
思考:根据氯气的制法原理请设计制备 一瓶纯净的氯化氢气体的实验装置。
一套较完整的制取气体的装置,包括:
气体发生装置
气体净化装置 气体收集装置 尾气处理装置
有关仪器的名称:
铁架台(带铁圈、铁夹)、 酒精灯、圆底烧瓶、 石棉网、分液漏斗、 双孔塞、玻璃导管。
浓硫酸 气体净化包括除杂、干燥等步骤
氯化氢与盐酸
HCl 的性质
一、物理性质:
1、色味态: 无色有刺激性气味的气体
2、密度:比空气重。
3、溶解性:HCl极易溶于水,通常条件下, 1体积 的水可以溶解大约500体积的氯化氢(1∶500)。 其水溶液为 盐酸。
喷泉实验
HCl
现象:
烧杯里的水喷入烧瓶中,形成红色喷泉。
原理:
HCl溶于水形成盐酸,使紫色石蕊试液变红。
