选修三测试
生物选修三测试题

生物选修三测试题1.从基因文库中获取目的基因的依据是基因的核苷酸序列和功能。
2.在基因表达载体的构建中,不正确的说法是所有基因表达载体的构建是完全相同的。
3.通过转基因技术,可以使人的糖蛋白基因得以表达的受体细胞是大肠杆菌。
4.该生物制品公司生产干扰素的方法是基因工程。
5.科学家将β-干扰素基因进行定点突变导入大肠杆菌表达,使干扰素第17位的半胱氨酸改变成丝氨酸,这是蛋白质工程技术。
6.动物细胞体外培养需要满足无毒、无菌、合成培养基需加血清、血浆、温度与动物体温相近、需要O2,不需要CO2和CO2能调节培养液pH这些条件。
7.蛋白质工程的基本流程是蛋白质分子结构设计、DNA合成、预期蛋白质功能、据氨基酸序列推出脱氧核苷酸序列。
8.要合成自然界中不存在的蛋白质,首先应设计氨基酸序列。
9.目前成功的蛋白质工程包括对胰岛素进行改造,生产速效型药品和生产体外耐保存的干扰素等。
10.动物细胞工程技术的基础是动物细胞培养。
11.关于细胞全能性的理解不确切的是高度分化的植物体细胞仍具有全能性,这是错误的理解。
B。
细胞内含有个体发育所需的全部基因,这使得细胞具有全能性的内在条件。
C。
试管苗是植物细胞在一定条件下表现全能性的结果,通过植物组织培养得到。
D。
动物体细胞也具有全能性,这得以证明是通过动物细胞培养获得细胞株或细胞系。
12.D。
13.A。
限制性核酸内切酶专一识别特定的核苷酸序列,并在特定的位点进行切割。
14.C。
与限制性核酸内切酶作用部位完全相同的酶是DNA连接酶。
15.B。
细菌质粒分子往往带有一个抗生素抗性基因,这个抗性基因的主要作用是有利于对目的基因是否导入进行检测。
16.B。
基因工程的正确操作步骤是②将目的基因导入受体细胞④获取目的基因①构建基因表达载体③检测目的基因的表达是否符合特定性状要求。
17.D。
将目的基因导入微生物细胞之前,要用Ca2+处理细胞,处理过的细胞叫做接受态细胞。
18.C。
质粒是一种独立于细菌染色体外的链状DNA分子,作为载体的质粒DNA分子上应有对重组DNA进行鉴定和选择的标记基因。
高中英语课时作业(译林版选修第三册)单元测试卷(三)

单元测试卷(三)第一部分听力(共两节,满分30分)第一节(共5小题;每小题分,满分分)听下面5段对话。
每段对话后有一个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。
听完每段对话后,你都有10秒钟的时间来回答有关小题和阅读下一小题。
每段对话仅读一遍。
1.Where does this conversation most probably take place?a bank. B.In a restaurant. C.In a hospital.2.What can we learn from this conversation?A.Mr. Davidson is busy right now.B.The man dialed the wrong number.C.The woman is quite familiar with the man.3.What are the speakers talking about?A.Colors. B.Mushrooms. C.Wallpaper.4.What do the speakers decide to do?A.Go out for dinner.B.Work overtime together.C.Bring some food back for dinner.5.Why doesn't the woman help the man?A.She is busy now. B.She is poor at physics.C.She has a headache.第二节(共15小题;每小题分,满分分)听下面5 段对话或独白。
每段对话或独白后有几个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。
听每段对话或独白前,你将有时间阅读各个小题,每小题5秒钟;听完后,各个小题将给出5秒钟的作答时间。
(必考题)高中化学选修三第三章《烃的衍生物》测试(含答案解析)

一、选择题1.(0分)[ID :140793]乙苯在催化剂作用下在550~600℃时脱氢生成苯乙烯:23223550600CFe O K O Cr O︒−−−−−−−→下列说法不正确的是A .乙苯和苯乙烯均能使溴水褪色,且褪色原理相同B .恒压下在进料中掺入大量高温水蒸气有利于提高苯乙烯的产量C .乙苯可由苯和乙烯反应得到,且该反应原子利用率能达到100%D .等质量的苯乙烯与苯燃烧时耗氧量相同2.(0分)[ID :140796]下列反应原理及对应的方程式均正确的是A .苯酚钠溶液中通入少量CO 2产生白色沉淀:2C 6H 5O -+CO 2+H 2O→2C 6H 5OH↓+2-3CO B .硫酸铜溶液中有少量Fe 3+,可加CuO 形成Fe(OH)3除去:2Fe 3++3CuO+3H 2O=2Fe(OH)3↓+3Cu 2+C .用溴水检验CH 2=CHCHO 中含有碳碳双键:CH 2=CHCHO+Br 2→CH 2BrCHBrCHOD .Ba(OH)2溶液中加入过量NH 4HSO 4溶液:Ba 2++2OH -++4NH +H ++2-4SO =BaSO 4↓+NH 3∙H 2O+H 2O3.(0分)[ID :140795]下列关于有机化合物的认识不正确的是A .甲醛在一定条件下既可以通过加聚反应又可以通过缩聚反应生成高分子化合物B .在酸性条件下,CH 3CO 18OC 2H 5的水解产物是CH 3COOH 和C 2H 518OH C .乙醇、乙醛、乙酸一定条件下均能与新制氢氧化铜悬浊液发生反应D .2-溴丁烷在氢氧化钠的乙醇溶液中反应可以生成2种不同的烯烃4.(0分)[ID :140778]下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是 A .金属钠B .溴水C .碳酸钠溶液D .紫色石蕊试液5.(0分)[ID :140775]有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。
人教版高中化学选修3第三章《 晶体结构与性质》测试题(含答案)

第三章《晶体结构与性质》测试题一、单选题1.下列有关晶体的说法中正确的是A.某晶体固态不导电,水溶液能导电说明该晶体是离子晶体B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力C.区分晶体和非晶体最科学的方法是对固体进行X﹣射线衍射实验D.任何晶体中,若含有阳离子也一定含有阴离子2.下列每组物质发生所述变化克服的作用属于同种类型的是()A.氯化铝和干冰升华B.钠和硫熔化C.食盐和氯化氢溶解于水D.二氧化硅和二氧化硫熔化3.对于氯化钠晶体,下列描述正确的是A.它是六方紧密堆积的一个例子B.58.5 g氯化钠晶体中约含6.02×1023个NaCl分子C.与氯化铯晶体结构相同D.每个Na+与6个Cl-作为近邻4.碳化硅(SiC)常用于电炉的耐火材料。
关于SiC说法正确的是A.易挥发B.能导电C.熔化时破坏共价键D.属于分子晶体5.下面有关晶体的叙述中,不正确的是A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子B.氯化钠晶体中,每个Na+周围距离相等且紧邻的Na+共有6个C.在冰中,每1molH2O分子形成2mol氢键D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子6.下列各组物质中,化学键类型相同,晶体类型也相同的是()A.C(金刚石)和CO2B.CH4和H2O C.NaBr和HBr D.Cl2和KCl 7.磷化硼是一种超硬耐磨涂层材料。
如图为其晶体结构中最小的重复单元。
下列有关说法正确的是B PA.磷化硼的化学式为2B.磷化硼晶体的熔点高,且熔融状态下能导电C.磷化硼晶体属于共价晶体D.磷化硼晶体在熔化时需克服范德华力8.下列各组顺序的排列错误的是A.半径:F—>Na+>Mg2+>Al3+B.沸点:H2O<H2S<H2SeC.酸性:HClO4>H2SO4>H3PO4D.熔点:SiO2>NaCl>CO29.北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。
高中化学选修三第三章《烃的衍生物》测试题(含答案解析)(28)

一、选择题1.(0分)[ID:140791]下列四种变化中,有一种变化与其他三种变化类型不同..的是光照CH3Cl + HClA.CH4 + Cl2−−−−−→B.CH3CH2OH + HBrΔ−−→CH3CH2Br + H2O−−−−→CH3CH=CH2↑+ NaBr + H2OC.CH3CH2CH2Br + NaOH乙醇ΔD.CH3COOCH2CH3+NaOHΔ−−→CH3COONa+C2H5OH2.(0分)[ID:140773]紫花前胡醇可从中药材当归和白芷中提取得到,能提高人体免疫力。
有关该化合物,下列叙述错误的是A.不能使酸性高锰酸钾溶液变色B.分子中有3种含氧官能团C.分子式为C14H14O4D.能够发生消去反应生成双键3.(0分)[ID:140769]下列有关的说法不正确的是A.不能发生消去反应、能与FeCl3发生显色反应B.能与新制的氢氧化铜反应C.与1mol NaHCO3反应生成2mol CO2D.1mol该物质与NaOH反应,最多消耗4mol NaOH4.(0分)[ID:140757]莨菪亭是一种植物生长激素,其结构简式如图所示。
下列有关莨菪亭的说法正确的是A.1 mol 该物质最多消耗 5 mol H2B.分子中所有碳原子可能处于同一平面C.该物质能发生加成、取代和消去反应D.1 mol 该物质最多能与 2 mol NaOH 反应5.(0分)[ID:140754]下列说法正确的是A.往苯酚钠溶液中通入CO2可制得苯酚,并得到碳酸钠B.将光亮铜丝在酒精灯火焰上加热后变黑,立即伸入无水乙醇中,铜丝能恢复成原来的颜色C.将卤代烃滴入AgNO3溶液中,根据生成沉淀颜色可以判断卤素原子种类D .将铁屑、溴水、苯混合可制得溴苯6.(0分)[ID :140752]芳香族化合物M 的结构简式为,下列关于有机物M 的说法正确的是A .有机物M 的分子式为C 10H 12O 3B .1 mol Na 2CO 3最多能消耗1 mol 有机物MC .1 mol M 和足量金属钠反应生成22.4 L 气体D .有机物M 能发生取代、氧化、酯化、加成和加聚反应7.(0分)[ID :140742]下列说法正确的是A .低级醇(甲醇、乙醇、丙醇、乙二醇)都能与水以任意比互溶B .正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高C .乙酸乙酯中的乙酸可以用NaOH 溶液洗涤后分液D .乙醇依次通过消去、取代、加成反应可生成乙二醇 8.(0分)[ID :140740]氟比洛芬()用于骨关节炎、肩周炎、网球肘等的镇痛、消炎,下列关于该化合物的说法正确的是A .分子中不含手性碳原子B .分子中所有碳原子可能在同一平面C .属于芳香烃D .1mol 该物质最多可与3molNaOH 反应9.(0分)[ID :140730]设N A 为阿伏加德罗常数的值,下列叙述正确的是( ) A .标准状况下,2.24 L CHCl 3的原子总数为0.1N AB .4.2 gC 3H 6中含有的碳碳双键数一定为0.1N AC .1 mol -OH 中电子数为10N AD .0.1 mol SiO 2晶体中含有Si-O 键的数目为0.4N A10.(0分)[ID :140716]下列离子方程式正确的是( )A .甘氨酸跟盐酸反应:HOOC-CH 2-NH 2+H +−−→HOOC-CH 2-NH +3B .高级脂肪酸跟氢氧化钠溶液反应:H ++OH -=H 2OC .苯酚钠溶液中通入少量CO 2:2C 6H 5O -+H 2O+CO 2→2C 6H 5OH+23CO -D .葡萄糖银镜反应:CH 2OH(CHOH)4CHO+2[Ag(NH 3)2]OH −−−→水浴加热CH 2OH(CHOH)4COO -+NH +4+3NH 3+2Ag↓+H 2O 11.(0分)[ID :140714]用下图所示装置进行实验,其中合理的是( )A.用图①装置配制银氨溶液B.装置②可除去甲烷中的乙烯C.装置③用于石油的分馏D.利用图④所示装置证明H2CO3酸性强于苯酚12.(0分)[ID:140709]利用化合物X和Y可以制备氧杂蒽酮类化合物中间体Z。
人教版高中化学选修三第一章 原子结构与性质 测试(含答案及详细解析)

绝密★启用前人教版高中化学选修三第一章原子结构与性质测试本试卷分第Ⅰ卷和第Ⅱ卷两部分,共100分第Ⅰ卷一、单选题(共20小题,每小题3.0分,共60分)1.已知某元素原子的价电子排布式为(n-1)d an s b,则下列说法正确的是()A.该元素是金属元素B.该元素位于周期表中d区C.该元素的族序数为a+bD.该元素位于周期表中第四周期2.下列说法中正确的是()A.电子云通常是用小黑点来表示电子的多少B.在同一能级上运动的电子,其运动状态肯定相同C.能层序数越大,s电子云的半径越大D.电子仅在激发态跃迁到基态时才会产生原子光谱3.下列化合物中阳离子半径与阴离子半径比值最小的是()A. MgI2B. KBrC. BaI2D. NaF4.下列关于能层与能级的说法中正确的是()A.原子核外每一个能层最多可容纳的电子数为n2B.任一能层的能级总是从s能级开始,而且能级数等于该能层数C.不同能层中s电子的原子轨道半径相同D.不同能层中p电子的原子轨道能量相同5.22Na是制造核弹的主要原料之一,下列关于基态22Na的说法正确的是()A.电子排布式为B.原子结构示意图为C.电子排布式为1s22s22p63s23p63d24s2D.22Na在化合物中通常显+1价6.下列电子层中,包含有f能级的是()A. K电子层B. L电子层C. M电子层D. N电子层7.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是()A. X与Y形成的化合物,X显负价,Y显正价B.最高价含氧酸的酸性:X对应的酸的酸性强于Y对应的酸的酸性C.气态氢化物的稳定性:H m Y小于H n XD.第一电离能Y一定小于X8.气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需要的最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
高中化学选修三第三章《烃的衍生物》测试题(含答案解析)(33)

一、选择题1.(0分)[ID :140793]乙苯在催化剂作用下在550~600℃时脱氢生成苯乙烯:23223550600C Fe O K O Cr O ︒−−−−−−−→下列说法不正确的是A .乙苯和苯乙烯均能使溴水褪色,且褪色原理相同B .恒压下在进料中掺入大量高温水蒸气有利于提高苯乙烯的产量C .乙苯可由苯和乙烯反应得到,且该反应原子利用率能达到100%D .等质量的苯乙烯与苯燃烧时耗氧量相同2.(0分)[ID :140792]已知:,如果要合成所用的原始原料可以是①2-甲基1-,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔③2,3-二甲基1-,3-戊二烯和乙炔 ④2,3-二甲基1-,3-丁二烯和丙炔 A .①④ B .②③ C .①③ D .②④3.(0分)[ID :140782]下到关于有机物的说法正确的是A .标准状况下, 22.4 LCCl 4含有的共价键数 目为4 molB .合成高聚物 的单体一共有三种C .相对分子质量为72的某烷烃,可能的一氯代物有7种D .维生素C 的结构简式是 ,存在2个手性碳原子4.(0分)[ID :140781]柠檬酸的结构简式为,下列说法正确的是A .柠檬酸中能发生酯化反应的官能团有2种B .1 mol 柠檬酸可与4 mol NaOH 发生中和反应C .1 mol 柠檬酸与足量金属Na 反应生成4mol H 2D .与柠檬酸互为同系物 5.(0分)[ID :140763]某有机物结构如图所示,下列有关说法正确的是A.该有机物含有3种不同的官能团B.该有机物含有2个手性碳原子C.1 mol该有机物与溴水反应,最多消耗3 mol Br2D.1 mol该有机物与氢氧化钠溶液反应,最多消耗4 mol NaOH6.(0分)[ID:140762]化合物Z是合成某种抗结核候选药物的重要中间体,可由下列反应制得。
下列有关化合物X、Y和Z的说法正确的是A.X、Y、Z在浓硫酸催化下加热均能发生消去反应B.Y分子中的碳原子一定处于同一平面C.X分子只能发生取代反应D.X、Z分别在过量NaOH溶液中加热,均能生成丙三醇7.(0分)[ID:140755]用下列实验装置进行实验,能达到实验目的的是A.制取乙烯B.检验溴乙烷与NaOH 醇溶液共热产生乙烯C.验证酸性:盐酸>碳酸>苯酚D.制备和收集乙酸乙酯8.(0分)[ID:140743]某有机物是从蜂花属植物中提取得到的酸性物质,其结构如图。
【赢在课堂】高中生物选修三综合测试(有答案,详细解析)

综合测试(时间:60分钟,满分:100分)一、选择题(每小题2.5分,共50分)1.利用基因工程技术可使大肠杆菌生产人的胰岛素。
下列相关叙述,正确的是( )。
A.人和大肠杆菌在合成胰岛素时,转录和翻译的场所是相同的B.DNA连接酶能把两个黏性末端经碱基互补配对进行“缝合”C.通过检测,大肠杆菌中没有胰岛素产生则可判断重组质粒未导入受体菌D.在培养大肠杆菌的工程菌过程中,获得目的基因的工具酶有限制性核酸内切酶和DNA 聚合酶解析:主要考查基因工程的基本工具以及基本操作步骤。
人是真核生物,转录的场所主要在细胞核,大肠杆菌是原核生物,转录的场所在细胞质,所以A错误;DNA连接酶的作用是在基因工程第二步将目的基因与载体连接成重组DNA分子或形成基因表达载体,它能把两个黏性末端经碱基互补配对进行“缝合”,所以B正确;大肠杆菌中没有胰岛素产生,可能是重组质粒虽然导入受体菌,但目的基因未表达,所以C错误;获得目的基因的工具酶只有限制性核酸内切酶,所以D也错误。
答案:B2.限制酶是一种核酸切割酶,可辨识并切割DNA分子上特定的核苷酸碱基序列。
下图为四种限制酶Bam HⅠ、Eco RⅠ、Hin dⅢ以及BglⅡ的辨识序列。
箭头表示每一种限制酶的特定切割部位,其中哪两种限制酶所切割出来的DNA片段末端可以互补黏合?其正确的末端互补序列是什么?( )A.Bam HⅠ和EcoRⅠ;末端互补序列为—AATT—B.Bam HⅠ和Hin dⅢ;末端互补序列为—GATC—C.Eco RⅠ和Hin dⅢ;末端互补序列为—AATT—D.Bam HⅠ和BglⅡ;末端互补序列为—GATC—答案:D3.下图是将人的生长激素基因导入细菌B细胞内制“工程菌”的示意图。
已知细菌B 细胞内不含质粒A,也不含质粒A上的基因。
判断下列说法正确的是( )。
A.将重组质粒导入细菌B常用的方法是显微注射法B.将完成导入过程后的细菌涂布在含有氨苄青霉素的培养基上,能生长的只是导入了重组质粒的细菌C.将完成导入过程后的细菌涂布在含有四环素的培养基上,能生长的就是导入了质粒A 的细菌D.目的基因成功表达的标志是受体细胞能产生出人的生长激素解析:将目的基因导入细菌细胞中常用的方法是Ca2+处理法;基因必须保持结构的完整性才能得以表达,而氨苄青霉素抗性基因结构完整,能够表达而使细菌具有对氨苄青霉素的抗性,在含有氨苄青霉素的培养基上能存活的是导入了质粒A或导入了重组质粒且能成功表达的细菌;由于将人的生长激素基因导入质粒的四环素抗性基因上,破坏了四环素抗性基因的完整性,导入了重组质粒的细菌也没有对四环素的抗性,在含有四环素的培养基上不能存活。
高中物理选修3-4全册综合测试(全册)

选修3-4综合测试(考试时间:90分钟,满分100分)一、选择题(本题包括14小题。
在每小题给出的四个选项中。
有的小题只有一个选项正确。
有的小题有多个选项正确。
全部选对的得4分,选不全的得2分,选错或不答的得0分,共56分)1、以下说法中正确的是()A.简谐运动中回复力总指向平衡位置;B.太阳光是偏振光;C.电磁波是横波,它的传播不须要介质;D.家电的遥控器是利用红外线的遥感。
2、依据麦克斯韦电磁场理论,下列说法中正确的是()A.改变的电场肯定产生改变的磁场B.匀称改变的电场肯定产生匀称改变的磁场C.稳定的电场肯定产生稳定的磁场D.周期性改变的电场肯定产生同频率的周期性改变的磁场3、一列声波从空气传入水中,已知水中声速较大,则( )A.声波频率不变,波长变小B.声波频率不变,波长变大C.声波频率变小,波长变大D.声波频率变大,波长不变4、如图所示,在一根张紧的水平绳上,悬挂有 a、b、c、d、e五个单摆,让a摆略偏离平衡位置后无初速释放,在垂直纸面的平面内振动;接着其余各摆也起先振动。
下列关于其余各摆说法中正确的有()A.各摆均做自由振动B. c摆的振幅最大C.摆长与a相差越大的,振幅越小D.各摆的振动周期与a摆相同5、如图所示,从点光源S发出的一细束白光以肯定的角度入射到三棱镜的表面,经过三棱镜的折射后发生色散现象,在光屏的ab间形成一条彩色光带.下面的说法中正确的是( )A.a侧是红色光,b侧是紫色光B.在真空中a侧光的波长小于b侧光的波长C .三棱镜对a 侧光的折射率大于对b 侧光的折射率D .在三棱镜中a 侧光的传播速率大于b 侧光的传播速率6、如图所示,表示横波在某一时刻的图像,其波速是8m/s ,则下列说法中正确的是 ( ) A .该波的周期为0.5s B .该波的振幅是5mC .从这一时刻起先经过1.75s ,质点a 经过的路程是70cmD . 从这一刻起先经过1.75s ,质点a 向右移动的距离为14m 7、一束可见光射到置于空气中的平行玻璃砖上,穿过玻璃砖后从下表面射出,变为a 、b 两束平行单色光,如图所示。
人教版高中物理选修三第三章《热力学定律》测试(包含答案解析)(1)

一、选择题1.(0分)[ID:130339]下列说法正确的是()A.布朗运动是悬浮在液体中固体颗粒的分子无规则运动的反映B.内能不同的物体,它们分子热运动的平均动能可能相同C.知道某物质的摩尔质量和密度可求出阿伏加德罗常数D.没有摩擦的理想热机可以把吸收的能量全部转化为机械能2.(0分)[ID:130332]一定质量的理想气体(不考虑气体分子势能),在温度升高的过程中()A.气体分子的平均动能可能不变B.外界一定对气体做功C.气体一定从外界吸收热量D.气体的内能一定增加3.(0分)[ID:130327]如图所示,一定质量的理想气体从状态a开始,经历ab、bc、cd、de 四个过程到达状态e,其中ba的延长线经过原点,bc连线与横轴平行,de连线与纵轴平行。
下列说法正确的是()A.ab过程中气体分子热运动平均动能增加B.bc过程中气体分子单位时间内击容器壁次数不变C.cd过程中气体从外界吸热小于气体内能增量D.de过程中气体对外放出热量,内能不变4.(0分)[ID:130322]A、B两装置,均由一支一端封闭、一端开口且带有玻璃泡的管状容器和水银槽组成,除玻璃泡在管上的位置不同外,其他条件都相同.将两管抽成真空后,开口向下竖直插人水银槽中(插入过程没有空气进入管内),水银柱上升至图示位置停止.假设这一过程水银与外界没有热交换,则下列说法正确的是A.A中水银的内能增量大于B中水银的内能增量B.B中水银的内能增量大于A中水银的内能增量C.A和B中水银体积保持不变,故内能增量相同D.A和B中水银温度始终相同,故内能增量相同5.(0分)[ID:130318]用密闭活塞封闭在气缸内一定质量的某种理想气体,如果气体与外界没有热交换,下列说法正确的是A.若气体分子的平均动能增大,则气体的压强一定增大B .若气体分子的平均动能增大,则气体的压强可能减小C .若气体分子的平均距离增大,则气体的压强一定增大D .若气体分子的平均距离增大,则气体的压强可能不变6.(0分)[ID :130311]下列说法不正确...的是 A .中国第一位进入太空的宇航员是杨利伟B .中国的卫星导航系统叫北斗导航系统C .能量是守恒的,我们不需要节约能源D .能量的耗散从能量转换的角度反映出自然界中宏观过程的方向性.能源的利用受这种方向性的制约,所以能源的利用是有条件的,也是有代价的.7.(0分)[ID :130302]如图所示,一定质量的理想气体密封在绝热(即与外界不发生热交换)容器中,容器内装有一可以活动的绝热活塞.今对活塞施以一竖直向下的压力F ,使活塞缓慢向下移动一段距离后,气体的体积减小.若忽略活塞与容器壁间的摩擦力,则被密封的气体( )图13-2-4A .温度升高,压强增大,内能减少B .温度降低,压强增大,内能减少C .温度升高,压强增大,内能增加D .温度降低,压强减小,内能增加8.(0分)[ID :130294]下列现象可以用热力学第一定律解释的是( )A .两物体接触后,热量自发地从高温物体传递到低温物体B .蒸汽机不能把蒸汽的内能全部转化为机械能C .叶片搅拌绝热容器中的水,引起水温升高D .利用能源的过程中会发生“能量耗散”现象9.(0分)[ID :130280]下列说法正确的是( )A .PM2.5是指空气中直径等于或小于2.5μm 的悬浮颗粒物,其飘浮在空中做无规则运动属于分子热运动B .当分子间的距离0r r 时,斥力等于引力,表现出合力为零,故分子势能为零C .涉及热现象的宏观自然过程都具有方向性,是不可逆的D .液晶的物理性质稳定,外界条件的变动不会引起液晶分子排列变化10.(0分)[ID :130269]下列说法中,能够发生且不违背热力学第二定律的是( ) A .一杯热茶自然放置,茶会自动变得更热B .电冰箱正常工作时把箱内低温物体的热量传递到箱外高温物体C .只要对蒸汽机不断革新,它就可以把蒸汽的内能全部转化成机械能D.利用降低海水温度放出大量的热量来发电,从而解决能源短缺的问题11.(0分)[ID:130263]下列关于热现象的说法,正确的是()A.外界对物体做功,物体内能一定增加B.理想气体温度升高,气体内能一定增大C.当两个分子间的距离小于平衡距离时,分子间只有斥力作用D.物体吸收热量,同时对内做功,内能可能不变12.(0分)[ID:130254]根据热学知识可以判断,下列说法正确的是()A.载重汽车卸去货物的过程中,外界对汽车轮胎内的气体做正功B.气体的摩尔质量为M,分子质量为m,若1摩尔该气体的体积为V,则该气体分子的体积为mV MC.一定量100℃的水变成100℃的水蒸气,其分子之间的势能增加D.空调的压缩机制冷时,将热量从温度较低的室内送到温度较高的室外,所以这一过程不遵守热力学第二定律二、填空题13.(0分)[ID:130453]如图,一定质量的理想气体从状态a开始,经历过程①、②、③、④到达状态e。
(常考题)人教版高中化学选修三第三章《烃的衍生物》测试(包含答案解析)(1)

一、选择题1.(0分)[ID :140793]乙苯在催化剂作用下在550~600℃时脱氢生成苯乙烯:23223550600CFe O K O Cr O︒−−−−−−−→下列说法不正确的是A .乙苯和苯乙烯均能使溴水褪色,且褪色原理相同B .恒压下在进料中掺入大量高温水蒸气有利于提高苯乙烯的产量C .乙苯可由苯和乙烯反应得到,且该反应原子利用率能达到100%D .等质量的苯乙烯与苯燃烧时耗氧量相同2.(0分)[ID :140778]下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是 A .金属钠B .溴水C .碳酸钠溶液D .紫色石蕊试液3.(0分)[ID :140774]下列化学方程式正确的是 A .1-溴丙烷与氢氧化钾的乙醇溶液共热:CH 3CH 2CH 2Br+KOH 乙醇Δ−−−−→CH 3CH 2CH 2OH+KBr B .乙酸乙酯的制备:CH 3CO 18OH+CH 3CH 2OH浓硫酸ΔCH 3CO 18OCH 2CH 3+H 2OC .用银氨溶液检验乙醛中的醛基CH 3CHO+232Ag(NH )++2OH -水浴加热−−−−→CH 3COO -+4NH ++3NH 3+2Ag↓+H 2OD .实验室用液溴和苯在催化剂作用下制溴苯:2+Br 23FeBr −−−→2+H 2↑4.(0分)[ID :140771]苯甲酸()和山梨酸(CH 3CH=CHCOOH)都是常用的食品防剂。
下列物质只能与上述一种物质发生反应的是 A .Br 2B .H 2C .酸性KMnO 4D .C 2H 5OH5.(0分)[ID :140766]除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( ) 选项 混合物 试剂 分离方法 A 乙烷(乙烯) H 2 —— B 乙醇(水) 生石灰 过滤 C 溴苯(溴) NaOH 溶液 分液 D乙酸乙酯(乙酸)——分液A .AB .BC .CD .D6.(0分)[ID :140759]在给定条件下,下列选项所示的物质间转化均能实现的是A .ClCH 2-CH 2Cl ()NaOH aqΔ−−−−→HOCH 2-CH 2OH ()2Cu OHΔ−−−−→HOOC -COOH B .(C 6H 10O 5)n (淀粉)24浓H SO Δ−−−−−→C 6H 12O 6(葡萄糖)−−−−→酒化酶ΔC 2H 5OH C .CH 3CH 2OH 25P O Δ−−−→CH 2=CH 2催化剂−−−−−→[22CH CH ]n D .CH 3CH 2OH HBr 溶液Δ−−−→CH 3CH 2Br 24浓H SOΔ−−−−−→CH 2=CH 2 7.(0分)[ID :140749]根据下列实验操作和现象所得出的结论正确的是 选项 实验操作和现象结论A向锌粒和稀硫酸反应的试管中,滴加几滴CuSO 4溶液,气体生成速率加快CuSO 4是锌和稀硫酸反应的催化剂B 向5 mL 0.1 mol·L -1 KI 溶液中滴加2 mL 0.1 mol·L -1 FeCl 3,充分反应中向其中滴加KSCN 溶液,溶液变红 反应2Fe 3++2I -=2Fe 2++I 2具有限度 C 向苯酚浊液中加入Na 2CO 3溶液,振荡,浊液变澄清 酸性:苯酚>碳酸 D 向溴乙烷中加入NaOH 乙醇溶液,加热,产生气体通入酸性KMnO 4溶液,酸性KMnO 4溶液褪色反应生成了乙烯 A .AB .BC .CD .D8.(0分)[ID :140733]下列说法不正确...的是 A .反应A()HCl−−→B(C 5H 9Cl)中可能生成B .反应A()HCl −−→B(C 5H 9Cl)A −−−−→化合物的反应类型都是加成反应C .中的-CHO 与可分别用银氨溶液与酸性KMnO 4溶液检验D .甲醛与氨气制备乌洛托品()的最佳配比:n (NH 3):n (HCHO)=2:39.(0分)[ID :140724]同温同压下,一定量的某有机物和过量的金属钠反应产生aL 氢气,另取等量的该有机物与足量的NaHCO 3溶液反应,可以收集到二氧化碳气体bL 。
人教版高中化学选修3第三章《 晶体结构与性质》测试题(含答案)

第三章《 晶体结构与性质》测试题一、单选题1.下列说法正确的是A .第三周期主族元素从左到右,最高价氧化物中离子键的百分数逐渐增大B .大多数晶体都是过渡晶体C .过渡晶体是指某些物质的晶体通过改变条件,转化为另一种晶体D .2Na O 是纯粹的离子晶体,2SiO 是纯粹的共价晶体2.下列说法正确..的是 A .氯化铵固体受热分解和干冰升华均只需克服分子间作用力B .I 2、Br 2、Cl 2、F 2的熔、沸点逐渐降低C .HCl 气体溶于水和NaOH 熔化破坏的化学键类型相同D .NaF 、H 2SO 4中所含化学键的类型相同3.氮化硅(Si 3N 4)是一种新型的耐高温耐磨材料,氮化硅属于A .离子晶体B .分子晶体C .金属晶体D .原子晶体 4.有下列离子晶体的空间结构示意图:以M 代表阳离子,以N 代表阴离子,•为阳离子,。
为阴离子,化学式为MN 2的晶体结构为( )A .B .C .D . 5.下列生活中的问题,不能用电子气理论知识解释的是A .铁易生锈B .用金属铝制成导线C .用金箔做外包装D .用铁制品做炊具 6.北京大学和中国科学院的化学工作者已成功研制出碱金属与C 60形成的球碳盐K 3C 60,实验测知该物质属于离子晶体,具有良好的超导性。
以下有关分析正确的选项是 A .熔融状态下该晶体能导电B .K 3C 60中碳元素显-3价 C .K 3C 60中只有离子键D .C 60与12C 互为同素异形体7.下列叙述正确的是A .氯化铯晶体中,每1个Cs +与其他8个Cs +等距离紧邻B .金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子C .熔点由高到低的顺序是:金刚石>碳化硅>晶体硅D .PCl 3和了BCl 3分子中所有原子的最外层都达到8电子稳定结构8.碳化硅()SiC 的一种晶体具有类似金刚石的结构,其中C 原子和Si 原子的位置是交替的.在下列三种晶体:①金刚石②晶体硅③碳化硅中,它们的熔点由高到低的顺序是A.①②③B.①③②C.③①②D.②①③9.下列有关说法不正确的是A.水合铜离子的模型如图所示,1个水合铜离子中有4个配位键B.CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+ C.H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动D.金属Ag的原子堆积模型如图所示,该金属晶体为最密堆积,每个Ag原子的配位数均为1210.金属原子在二维空间里的两种放置方式如图所示,下列说法中正确的是A.图a为非密置层B.图b为密置层C.图a在三维空间里堆积可得到最密堆积D.图b在三维空间里堆积可得到最密堆积11.下下下下下下下下下下下下下下下下下下下下下下下D Ba(OH)2下下下下下MgA.A B.B C.C D.D12.金属晶体中金属原子有三种常见的堆积方式,六方最密堆积、面心立方堆积和体心立方堆积,如图a、b、c分别代表这三种晶胞的结构,其晶胞内金属原子个数比为A.3:2:1B.11:8:4C.9:8:4D.21:4:9 13.金属钠晶体(如图)为体心立方晶胞,晶胞的边长为a,假定金属钠原子为等径的刚性球,且晶胞中处于体对角线上的三个球相切,则钠原子的半径r为()A.a2B.3a C.3a D.2a14.有关晶体的叙述中正确的是A.在SiO2晶体中,最小的单元环是由6个硅原子组成的六元环B.在124g白磷(P4)晶体中,含P—P共价键个数为4N AC.金刚石的熔沸点高于晶体硅,是因为C—C键键能小于Si—Si键D.12g金刚石中含C原子与C—C键之比为1:215.已知硅酸盐中,通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。
《常考题》初中高中物理选修三第三章《热力学定律》阶段测试(含答案解析)
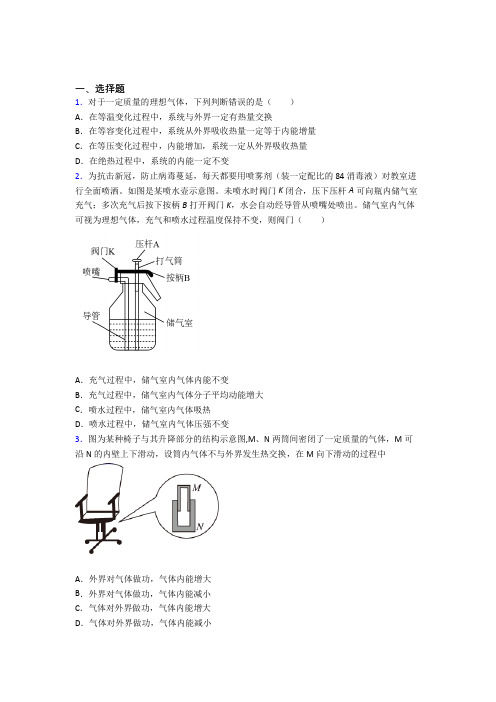
一、选择题1.对于一定质量的理想气体,下列判断错误的是()A.在等温变化过程中,系统与外界一定有热量交换B.在等容变化过程中,系统从外界吸收热量一定等于内能增量C.在等压变化过程中,内能增加,系统一定从外界吸收热量D.在绝热过程中,系统的内能一定不变2.为抗击新冠,防止病毒蔓延,每天都要用喷雾剂(装一定配比的84消毒液)对教室进行全面喷洒。
如图是某喷水壶示意图。
未喷水时阀门K闭合,压下压杆A可向瓶内储气室充气;多次充气后按下按柄B打开阀门K,水会自动经导管从喷嘴处喷出。
储气室内气体可视为理想气体,充气和喷水过程温度保持不变,则阀门()A.充气过程中,储气室内气体内能不变B.充气过程中,储气室内气体分子平均动能增大C.喷水过程中,储气室内气体吸热D.喷水过程中,储气室内气体压强不变3.图为某种椅子与其升降部分的结构示意图,M、N两筒间密闭了一定质量的气体,M可沿N的内壁上下滑动,设筒内气体不与外界发生热交换,在M向下滑动的过程中A.外界对气体做功,气体内能增大B.外界对气体做功,气体内能减小C.气体对外界做功,气体内能增大D.气体对外界做功,气体内能减小4.如图所示,一定质量的理想气体密封在绝热(即与外界不发生热交换)容器中,容器内装有一可以活动的绝热活塞.今对活塞施以一竖直向下的压力F ,使活塞缓慢向下移动一段距离后,气体的体积减小.若忽略活塞与容器壁间的摩擦力,则被密封的气体( )图13-2-4A .温度升高,压强增大,内能减少B .温度降低,压强增大,内能减少C .温度升高,压强增大,内能增加D .温度降低,压强减小,内能增加5.如图所示,一定质量的理想气体从状态A 依次经过状态B 、C 和D 后再回到状态A 。
其中,A →B 和C →D 为等温过程,B →C 为等压过程,D →A 为等容过程。
关于该循环过程中,下列说法正确的是( )A .A →B 过程中,气体吸收热量B .B →C 过程中,气体分子的平均动能减小C .C →D 过程中,单位时间内碰撞单位面积器壁的分子数减少D .D →A 过程中,气体分子的速率分布曲线不发生变化6.带有活塞的汽缸内封闭一定量的理想气体。
人教版化学选修三物质结构与性质测试考题(含答案)

绝密★启用前人教版化学选修三物质结构与性质测试考题本试卷分第Ⅰ 卷和第Ⅱ卷两部分,共100 分。
分卷I一、单选题(共10小题,每小题4.0分,共40 分)1.在硼酸[B(OH) 3]分子中,B 原子与3 个羟基相连,其晶体具有与石墨相似的层状结构。
则分子中B 原子杂化轨道的类型及同层分子间的主要作用力分别是( )A .sp,范德华力B.sp2,范德华力C.sp2,氢键D .sp3,氢键2.下列各组物质中,化学键类型都相同的是( )A.CaCl2 和NaOHB.Na2O 和Na2O2C.CO2和CS2D .HCl 和NaOH3.下列有关金属元素特征的叙述正确的是( )A.金属元素的原子只有还原性,离子只有氧化性B.金属元素在一般化合物中只显正价C.金属元素在不同的化合物中的化合价均不同D.金属元素的单质在常温下均为金属晶体4.前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有( )A.3 种B .4 种C.5 种D.6 种5.根据科学人员探测,在海洋深处的沉积物中含有可燃冰,主要成分是甲烷水合物。
有关其组成的两种分子的下列说法正确的是( )A .它们都是极性键构成的极性分子B.它们之间以氢键结合在一起C.它们的成键电子的原子轨道都是sp3—s D .它们的立体结构都相同6.金属的下列性质中和金属晶体结构无关的是( )A .良好的导电性B.反应中易失去电子C.良好的延展性D .良好的导热性7.下列对各组物质性质的比较中,不正确的是( )A.熔点:Li >Na>KB.导电性:Ag>Cu>Al >FeC.密度:Na﹤Mg ﹤AlD.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积8.下列各组微粒不是按半径逐渐增大的顺序排列的是( )A.Na、K、RbB.F、Cl、Br2+、Al 3+、Zn2+C.MgD.Cl -、Br-、I-9.下列分子中,属于易溶于水的一组是( )A.CH4、CCl4、CO2B.NH 3、HCl 、HBrC.Cl 2、H2、N2D.H2S、NO、SO210.下列叙述中,正确的是( )A .在一个基态多电子的原子中,可以有两个运动状态完全相同的电子B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子C.如果某一基态原子3p轨道上仅有2 个电子,它们自旋方向必然相反D .在一个基态多电子的原子中,M 层上的电子能量肯定比L 层上的电子能量高二、双选题(共4小题,每小题5.0 分,共20分)11.(多选)下列配合物的配位数不是 6 的是( )A.[Cu(NH 3)4]Cl 2B.Na2[SiF6]C.Na3[AlF 6]D.K 2[Co(SCN) 4]一个则无K+),下列说法正确的是()12.(多选)普鲁士蓝晶体结构如下图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是()A.化学式可以表示为KFe2(CN)6B.一个立方体中含有12个π键C.普鲁士蓝中含有配位键D.Fe3+周围有12 个Fe2+离子13.(多选)高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0 价,部分为﹣2 价.如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是()A.超氧化钾的化学式为KO 2,每个晶胞含有4个K+和4 个O2-B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+C.晶体中与每个K +距离最近的K+有8 个D.晶体中,0 价氧原子与﹣2 价氧原子的数目比为3:114.(多选)下列有关范德华力的叙述正确的是()A .范德华力的实质也是一种电性作用,所以范德华力是一种特殊化学键B.范德华力与化学键的区别是作用力的强弱问题C.稀有气体形成的晶体中原子之间不存在范德华力D .范德华力较弱,故破坏它需要的能量很少分卷II三、综合题(共4小题,每小题10.0分,共40 分)15.A ,B ,C,D 是四种短周期元素,E是过渡元素。
人教版高中化学选修3第三章《 晶体结构与性质》测试题(含答案)

第三章《晶体结构与性质》测试题一、单选题1.在单质的晶体中,一定不存在的粒子是A.原子B.阴离子C.阳离子D.分子2.关于非晶体的叙述错误的是()A.玻璃属于非晶体B.内部微粒的排列是长程无序和短程有序的C.非晶体材料的所有性能都优于晶体材料D.金属形成的合金也有非晶体3.有关晶体的叙述中,错误的是A.区分晶体和非晶体最可靠的科学方法是对固体进行X-射线衍射实验B.晶体与非晶体的本质区别在于是否具有规则的几何外形C.分子晶体熔化时,不破坏共价键;原子晶体熔化时,破坏共价键D.在金属铜的晶体中,由于存在自由电子,因此铜能导电4.下列有关物质性质的比较,结论正确的是A.碱性:LiOH<RbOH B.溶解度:Na2CO3<NaHCO3C.热稳定性:PH3<SiH4D.沸点:C2H5OH<C2H5SH5.下列各物质中,按熔点由高到低的顺序排列正确的是()A.CH4>SiH4>GeH4>SnH4B.KCl>NaCl>MgCl2>MgOC.Rb>K>Na>Li D.金刚石>Si>钠6.金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强,与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。
据此判断下列金属熔点逐渐升高的A.Li Na K B.Na Mg Al C.Li Be Mg D.Li Na MgH”的变化过程中,被破坏的作用力依次是7.在“冰→水→水蒸气→2A.分子间作用力、分子间作用力、分子间作用力B.分子间作用力、分子间作用力、共价键C.分子间作用力、共价键、共价键D.共价键、共价键、共价键8.F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次增强),都极易与水反应。
已知2232+12H O=2XeO +4Xe +24HF 6XeF +3O ↑↑,下列推测正确的是( )A .XeF 2分子中各原子均达到8电子的稳定结构B .某种氟化氙晶体的基本结构单元如图所示,可推知其化学式为XeF 6C .XeF 4与水反应时,每生成2 mol Xe 转移8 mol 电子D .XeF 2加入水中,在水的作用下,将生成Xe 和F 29.下列说法中正确的是( )A .P 4和CH 4都是正四面体分子且键角都为109o 28ˊB .H 2O 是一种非常稳定的化合物,这是由于氢键所致C .NO 3-和CO 32-和和和和和和和和和和和和和和和和D .金属晶体与熔融态的离子晶体导电都是物理变化10.冰晶石(化学式为Na 3AlF 6)的晶体结构单元如图所示(●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心)。
化学选修三物质结构与性质综合测试题及答案

化学选修三物质结构与性质综合测试题及答案一、选择题每小题3分,共54分;每小题只有一个....选项符合题意1.有关乙炔H-C=C-H分子中的化学键描述不正确的是A.两个碳原子采用sp杂化方式 B.两个碳原子采用sp2杂化方式C.每个碳原子都有两个未杂化的2p轨道形成π键D.两个碳原子形成两个π键2.下列物质中,难溶于CCl4的是A.碘单质 B.水C.苯酚 D.己烷3.下列分子或离子中,含有孤对电子的是A.H2O B.CH4C.SiH4D.NH4+4.氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为A .氨气分子是极性分子而甲烷是非极性分子;B.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化;C.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道;D.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强;5.对充有氖气的霓虹灯管通电,灯管发出红色光;产生这一现象的主要原因A.电子由激发态向基态跃迁时以光的形式释放能量B.在电流的作用下,氖原子与构成灯管的物质发生反应C.电子由基态向激发态跃迁时吸收除红光以外的光线D.氖原子获得电子后转变成发出红光的物质6.若某原子在处于能量最低状态时,外围电子排布为4d15s2,则下列说法正确的是A.该元素原子处于能量最低状态时,原子中共有3个未成对电子B.该元素原子核外共有6个电子层 C.该元素原子的M能层共有8个电子D.该元素原子最外层共有2个电子7.σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成;则下列分子中的σ键是由一个原子的s 轨道和另一个原子的p 轨道以“头碰头”方式重叠构建而成的是 A .H 28. 下列原子或离子原子核外电子排布不属于基态排布的是A. S 2-: 1s 22s 22p 63s 23p 6B. N: 1s 22s 22p 3C. Si: 1s 22s 22p 63s 23p 2D. Na: 1s 22s 22p 53s 29.元素电负性随原子序数的递增而增强的是,Si,Ge , P, As , P, Cl D. F, S, Cl 10.某元素质量数51,中子数28,其基态原子未成对电子数为 B.1 C. 211, 只有阳离子而没有阴离子的晶体是;A .金属晶体B .分子晶体C .离子晶体D .原子晶体12,下列关于物质熔点的排列顺序,不正确的是;A .HI >HBr >HCl >HFB .CI 4>CBr 4>CCl 4>CF 4C .KCl >KBr >KID .金刚石>碳化硅>晶体硅Na 2O Na AlF 3 AlCl 3 Al 2O 3 BCl 3 CO 2 SiO 2 920℃ ℃ 1291℃ 190℃ 2073℃ -107℃ -57℃ 1723℃A .只要含有金属阳离子的晶体就一定是离子晶体B .在上述共价化合物分子中各原子都形成8电子结构C .同族元素的氧化物可形成不同类型的晶体D .金属晶体的熔点不一定比离子晶体的高14、现有四种晶体,其离子排列方式如图所示,其中化学式不属AB 型的是A B CD15.x 、y 为两种元素的原子,x 的阴离子与y 的阳离子具有相同的电子层结构,由此可知的原子半径大于y 的原子半径; 的电负性小于y 的电负性阴离子的半径大于y阳离子的半径的第一电离能小于y 的第一电离能16.下列有关物质性质的比较顺序中,不正确的是A.热稳定性:HF>HCl>HBr>HI B.微粒半径:K+>Na+>Mg2+>Al3+C.酸性:HClO4<H2SO4<H3PO4<H2SiO3D.熔点:Li>Na>K>Rb17.下列现象与氢键有关的是:①NH3的熔、沸点比VA族其他元素氢化物的高②乙醇可以和水以任意比互溶③冰的密度比液态水的密度小4邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低5水分子高温下也很稳定A.①②B.①②③④⑤C.①②③④D.①②③18.钡在氧气中燃烧时的得到一种钡的氧化物晶体,其结构如下图所示,有关说法不正确的是A、该晶体属于离子晶体B、晶体的化学式为Ba2O 2C、该晶体晶胞结构与NaCl相似D、与每个Ba2+距离相等且最近的Ba2+共有12个二,填空题共46分19.14分1金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示;面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为________;2等径圆球在二维空间里进行排列,可形成密置层和非密置层,在图1所示的半径相等的圆球的排列中,A属于________层,配位数是________;B属于________层,配位数是________;3将非密置层一层一层地在三维空间里堆积,得到如图2所示的一种金属晶体的晶胞,它被称为简单立方堆积,在这种晶体中,金属原子的配位数是________,平均每个晶胞所占有的原子数目是________;20.8分按要求回答下列问题1石墨晶体中C-C键的键角为 ;其中平均每个六边形所含的C原子数为个;2金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有个C原子;Ba2+3白磷分子中的键角为 ,分子的空间结构为 ,每个P原子与个P原子结合成共价键;4 晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体;其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答;这个基本结构单元由_____个硼原子组成,共含有________个B-B键;21. 12分下表是元素周期表的一部分;表中所列的字母分别代表一种化学元素;ab c d e fg h i j k l mn p试回答下列问题:1请写出元素h的基态原子电子排布式;2i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示;若已知i的原子半径为d,N A代表阿伏加德罗常数,i的相对原子质量为M,请回答:①晶胞中i原子的配位数为 ,一个晶胞中i原子的数目为;②该晶体的密度为用字母表示;3c,d,e三种元素第一电离能由大到小的顺序为——————用元素符号表示4p的离子与4个a2e分子形成的阳离子中含的化学键有____________.22.12分用N A表示阿伏加德罗常数的值;下列叙述正确的画v,错误的画x.A.常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3N A B.标准状况下, L乙烷中共价键数目为6N AC.由CO2和O2组成的混合物中共有N A个分子,其中的氧原子数为2N AD.1 L浓度为1 mol·L-1的Na2CO3溶液中含有2N A个钠离子E.23 g钠在氧气中完全燃烧失去电子数为F. 2 mol·L-1的MgCl2溶液中含Mg2+数为2N AG.标准状况下,11.2 L的SO3所含分子数为甲乙H.室温下,8g甲烷含有共价键数为2N AI.2 mol重水含有N A个D2O分子J.2 mol钠与过量稀盐酸反应生成N A个H2分子K.1 g氢气含有N A个H2分子L.22.4 L水含有N A个H2O分化学试卷答案一.选择题1—5 BBADA 6----10 DBDCA 11---15 AABBC 16—18 CCB 二.19.12:12非密置层. 4. 密置层 636 .120.1120 ,2 26360, 正四面体, 3412, 302111S 2S 2P 3S212, 4,——————3N>O>C4配位键,共价键,D,H,J正确画V,其他错误画X。
人教版化学选修3第三章《 晶体结构与性质》测试题(含答案)

第三章《 晶体结构与性质》测试题一、单选题1.下列化合物中,属于原子晶体的是A .干冰B .氯化钠C .氟化硅D .二氧化硅 2.如图是a 、b 两种不同物质熔化时的温度变化曲线,下列说法正确的是( )A .a 没有固定的熔点B .a 是非晶体C .b 是晶体D .b 是非晶体 3.以下过程与化学键断裂无关的是A .氯化钠熔化B .干冰升华C .金刚石熔化D .金属汞汽化 4.下列叙述错误的是( )A .区别晶体与非晶体最科学的方法是对固体进行X −射线衍射实验B .外观呈现规则多面体的物质,内部微观粒子在三维空间一定呈周期性有序排列C .晶体具有各向异性,所以用红热的铁针刺中涂有石蜡的水晶柱面,熔化的石蜡呈椭圆形D .乙醇和水都是极性分子,符合相似相溶原理,且它们易形成分子间氢键,故乙醇易溶于水5.对于下列性质的比较正确的是A .离子半径:r(Cl -)>r(S 2-)>r(Na +)B .元素的电负性:Si<P<NC .稳定性:H 2O>H 2S>HClD .晶格能:MgO>NaBr>NaCl 6.晶体具有各向异性,如蓝晶石(Al 2O 3·SiO 2)在不同方向上的硬度不同;又如石墨在与层垂直的方向上的电导率是与层平行的方向上的电导率的4110。
晶体的各向异性主要表现在( )①硬度 ②导热性 ③导电性 ④光学性质A .①③B .②④C .①②③D .①②③④ 7.下列说法中错误的是①H 2O 汽化成水蒸气破坏分子间作用力、H 2O 分解为H 2和O 2,需要破坏共价键 ②C 4H 10的两种同分异构体因为分子间作用力大小不同,因而沸点不同③因为晶体硅的摩尔质量比金刚石的摩尔质量大,所以晶体硅的熔点比金刚石的高④SiO2与CO2的分子结构类似,所以化学性质类似⑤分子晶体中,共价键键能越大,该分子晶体的熔、沸点越高A.①②⑤B.①②③C.②④⑤D.③④⑤8.根据下表中的数据,结合学过的化学知识,判断下列说法正确的是A.以上四种物质中,只有SiCl4是共价化合物B.若上述数据变化规律具有普遍性,则可预测:LiCl 的沸点大于BCl3的沸点C.因为AlCl3的沸点低,所以工业上可用电解熔融AlCl3制备AlD.据上述数据,可判断NaCl、MgCl2为分子晶体9.下列对一些实验事实的理论解释正确的是()A.A B.B C.C D.D10.W、X、Y、Z均为短周期主族元素,原子序数依次增加,X、Y同周期,W、Z同主族,且X、Y最外层电子数之和是W、Z最外层电子数之和的6倍。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
选修三《现代生物科技专题》测试题
姓名:班级:分数:
1.随着科学技术的发展,人们可以根据需求来改造生物的性状。
如图是利用奶牛乳汁生产人类血清白蛋白的图解,据图回答问题。
(1)在基因工程中,我们称②为_______________,能实现②进入③的常用方法是____________。
(2)图中①一般经__________________处理可以得到③,从③到④的过程中一般利用去核后未
受精的卵细胞作为受体,而不用普通的体细胞。
(3)把⑤送入⑥的最佳时期是____________。
(4)⑦是⑥的后代,那么⑦的遗传性状和____________________最相似;如果②的数量太少,
常用____________来扩增;要实现⑦批量生产血清白蛋白,则要求③的性染色体是___________。
(5)⑦和某些转基因羊可通过分泌乳汁来生产人类所需药物,这类转基因动物被称为。
2.人组织纤溶酶原激活物(htPA)是一种重要的药用蛋白,可在转htPA基因母羊的羊乳中获得。
流程如下:
(1)htPA基因与载体用_______________ ___切割后,通过DNA连接酶连接,以构建重组
表达载体,为了便于检测与鉴定,重组表达载体的构成中必须有。
检测目
的基因是否已插入受体细胞DNA,可采用________________ __技术。
(2)为获取更多的卵(母)细胞,要对供体母羊注射促性腺激素,使其______________。
采集
的精子需要经过_______________,才具备受精能力。
(3)将重组表达载体导入后,为了获得母羊,移植前需对已成功转入目的基因的胚胎进行
______________ _。
利用胚胎分割和胚胎移植技术可获得多个转基因个体,这体现了早期
胚胎细胞的_______________。
(4)若在转htPA基因母羊的羊乳中检测到__________ __,说明目的基因成功表达。
3.降钙素是一种多肽类激素,临床上用于治疗骨质疏松症等疾病。
人的降钙素活性很低,半衰
期较短。
某科学机构为了研发一种活性高、
半衰期长的新型降钙素,从预期新型降钙素
的功能出发,推测相应的脱氧核苷酸序列,
并人工合成了两条各72个碱基的DNA单链,
两条链通过18个碱基对形成部分双链DNA
片段,再利用Klenow酶补平,获得双链DNA,
过程如下图。
在此过程中发现,合成较长的核苷酸单链易产生缺失碱基的现象。
分析回答下列问题:
(1)Klenow酶是一种_________酶,获取新型降钙素目的基因的方法是__________ __。
(2)获得的双链DNA经EcoR I(识别序列和切割位点.-G↓LAATTC-)和BamH I(识别序列和切割位点.-G↓GATCC-)双酶切后插入到大肠杆菌质粒中,筛选含重组质粒的大肠杆菌并进行DNA 测序验证。
①大肠杆菌是理想的受体细胞,这是因为它___________。
若选择动物乳房反应器生产新型降钙
素,则应将重组DNA导入__________细胞,成功后利用胚胎工程,先进行早期胚胎培养,最后
通过______________,即可获得转基因动物。
②设计EcoR I和BamH I双酶切的目的是__________________________。
要进行重组质粒的鉴
定和选择,需要大肠杆菌质粒中含有_________________。
(3)制备该新型降钙素,运用的是现代生物工程技术中的_________________工程。
4.美国科学家发现一头能天然抵抗结核病的奶牛“86牛”,其体内存在针对结核菌的抗毒素基因。
据此,科学家利用这头奶牛的体细胞进行一系列的研究并成功克隆出抗结核病的“抗病牛”。
过程如下:
(1)过程④表示____________,进行此过程需对B牛用激素进行__________处理。
(2)③过程中,重组胚胎培养到___________期时,可从其内细胞团分离出ES细胞,此细胞在功
能上具有发育的___________。
(3)ES细胞培养过程中在培养液中加入一定量的____________,以防止培养过程中的污染;同
时在使用合成培养基时,为保证细胞正常生长,在培养基中还要添加________ __等天然成分。
(4)ES细胞在__________上,或在添加抑制因子的培养液中能够维持不分化状态,因此进行过
程⑤时,需在培养液中加入_________ __,以获得产抗毒素细胞。
5、根据下面植物体细胞杂交技术流程图,回答相关问题。
(1)若运用传统有性杂交(即用番茄、马铃薯杂交)能否得到杂种植株?为什么?
________________________________________________________________________。
(2)在利用杂种细胞培育杂种植株的过程中,运用的技术手段是______ __,依据的原理是______________,其中过程②称为_____________ ___,与过程③密切相关的具有单层膜结构的细胞器为___________,过程④相当于_____________,⑤过程涉及的分裂方式为____________。
(3)已知番茄、马铃薯分别为四倍体、二倍体,则“番茄—马铃薯”属于________倍体植株。
(4)随“神六”太空旅行的种苗中,最受关注的是柴油树试管苗。
柴油树种子含有的柴油是植物细胞的代谢产物,可用植物组织培养来实现柴油的工业化生产。
若利用此技术,将柴油树细胞培养进行到______ __过程即可(填字母编号)。
(5)若培育抗虫棉,将抗虫基因通过适当的途径导入棉花受精卵,然后进行组织培养,该过程相当于________(填字母编号)。
(6)人工种子又称合成种子或种子类似物,它是20世纪生物技术在农业上的应用之一。
由发育
到________过程(填字母编号)的结构包裹上______ __可制备人工种子。
6.下图是单克隆抗体制备流程阶段示意图,据图回答下列问题:
(1)__________ __技术是进行单克隆抗体制备的基础。
(2)根据培养基的用途分类,图中HAT培养基属于______ _培养基。
(3)单克隆抗体与常规的血清抗体相比,最大的优越性是______________________ __。
(4)动物细胞融合除了采用植物细胞原生质体融合常用的诱导剂外,还可以采用______ __。
(5)选出的杂交瘤细胞既具备骨髓瘤细胞_________ _的特点,又具备淋巴细胞_______ _ _的特点。
(6)淋巴细胞是由动物体_____ _中的_____ _细胞分化、发育而来的。
(7)杂交瘤细胞从培养基中吸收葡萄糖、氨基酸的主要方式是______________。
7.下面两幅图分别是单克隆抗体制备过程和克隆羊培育过程示意图,请据图回答下列问题:
(1)图甲和图乙所示的过程中,都必须用到的动物细胞工程技术手段是_________ _。
(2)图甲中①注射病原入小鼠体内后,要经过__________细胞处理后,才能被免疫细胞识别。
②过程常在__________诱导下完成(3)单克隆抗体能定向攻击癌细胞,主要是利用其_________。
(4)图乙过程常选择___________期的卵母细胞做受体细胞,原因是_________ _。
若不考虑环境因素影响,克隆羊的性状全部像白面绵羊吗?_________。
原因是____________。
(5)图乙过程的技术具有多种用途,但是不能___________。
A.有选择地繁殖某一性别的家畜 B.繁殖家畜中的优良个体
C.用于保存物种 D.改变动物的核基因
(6)在目前现有技术条件下,还不能将从动物体内分离出来的成熟的体细胞直接培养成一个新个体,而是必须将体细胞的细胞核移植到去核的卵细胞中才能发育成新个体,你认为原因最可能是__________。
A.卵细胞大,便于操作 B.卵细胞含有的营养物质多
C.卵细胞细胞质可使体细胞核全能性得到表达 D.重组细胞才具有全能性
选修三测试答案
1、(1)目的基因显微注射法(2)胰蛋白酶(3)桑椹胚囊胚
(4)荷斯坦奶牛 PCR技术 XX (5)乳腺生物反应器
2、(1)同种限制性核酸内切酶(或同种限制酶)标记基因 DNA分子杂交(2)超数排卵;获能(处理)(3)性别鉴定全能性(4)htPA(或人组织纤溶酶原激活物)
3、(1)DNA聚合人工合成(2)①繁殖快、单细胞、遗传物质相对较少受精卵胚胎移植
②保证目的基因和载体定向连接标记基因(3)蛋白质
4、(1)胚胎移植同期发情 (2)囊胚全能性 (3)抗生素血清(或血浆) (4)饲养层细胞分化诱导因子
5、(1)不能,不同种的植物存在生殖隔离 (2)植物组织培养细胞的全能性原生质体融合高尔基体脱分化有丝分裂 (3)六(4)e (5)④⑤(6)f 人工种皮
6、(1)动物细胞培养(微生物培养) (2)选择(3)特异性强、灵敏度高(4)灭活的病毒(5)在体外大量增殖分泌特异性抗体 (6) 骨髓造血干(7)主动运输
7、(1)动物细胞培养 (2)吞噬细胞;灭活的病毒 (3)特异性
(4)MⅡ中;MⅡ期卵母细胞体积大,易操作,含有促使细胞核全能性表达的物质和营养;
不是;卵细胞细胞质的遗传物质也能控制某些性状 (5)D (6)C。
