重叠综合征
重叠综合征

特异性自身抗体包括抗合成酶(Jo-1、PL-7、PL12、OJ、EJ、KS)抗体,硬皮病相关白身抗体(硬 皮病特异性自身抗体:ACA、抗Scl-70、RNA聚 合酶1或Ⅲ、n抗体;硬皮病重叠相关自身抗体: 抗ulRNP、u2RNP、u3RNP、u5RNP、PM-Scl、 Ku和SRP、核孔蛋白抗体)。区别典型的PM和 DM与重叠综合征在判断疾病预后和治疗上有重要 意义。
典型的PM常呈慢性病程。50%患者埘糖皮质激 素治疗无效。单纯的DM几乎(92%)都是慢性病程, 但87%的患者对糖皮质激素治疗有效。肌炎重叠 综合征(通常伴有硬皮病特征)几乎都对糖皮质激 素有应答(约90%)。重叠综合征可根据自身抗体 分亚型:抗合成酶抗体、SRP和抗核孔蛋白抗体 标志对治疗抵抗的肌炎,而抗ulRNP、PM—Scl 或1.概述
目前已确定有6种弥漫性结缔组织病(diffuse connective
tissue diseases,DCTDs),包括系统性红斑狼疮(SLE)、系 统性硬化病(SSc)、多发性肌炎(PM)、皮肌炎(DM)、类风 湿关节炎(RA)、干燥综合征(ss)。这些病都是描述性综合 征,尚缺乏诊断的金标准。典型的DCTD容易诊断,但在 疾病早期阶段,常存在一些非特异性共同表现,如雷诺现 象、关节痛、肌痛、食管功能失调和抗核抗体(ANA)阳性 等,通常称为未分化结缔组织病(undifferentiated connective tissue disease,UCTD),其中只有35%进展 为某种DCTD。
肌炎重叠综合征的诊断,应符合炎性肌病加至少 1种或多种下列疾病特征或特异性自身抗体。疾病 特征包括:多关节炎、雷诺现象、指端硬化、近 掌指关节硬化、手指典型SSc型钙质沉着、食管 下端或小肠运动减弱、肺一氧化碳弥散量(DLCO) 低于正常预计值的70%、胸部X片或CT显示间质 性肺病、盘状狼疮、抗dsDNA抗体加低补体血症、 美国风湿病学会(ACR)的SLE诊断标准11条中4条 或4条以上特征、抗磷脂综合征。
重叠综合征24例临床分析

标 准 。其 中男 性 5例 、 女性 1 9例 ; 年龄 3 ~ 4 岁 , 28 平
性 4例 . 干 燥 综合 征 A抗 体 阳性 1 抗 3例 , 干燥 综 抗
合 征 B抗 体 阳性 9例 ,抗 n N R P抗 体 阳性 4例 , 抗
例 、 发 4例 、 诺 现 象 6例 、 脱 雷 口干 1 2例 、 干 1 眼 2 例 ; 肉及 关 节表 现 : 无力 2例 、 肌 肌 肌痛 3例 、 响吞 影
咽功 能 的食管 肌受 累 1 、 节 疼痛 8例 、 例 关 关节 肿胀
作 者单 位 :10 3 浙 江 杭州 , 江 大 学 医学 院 附属 第 一 医 300 浙
J一 抗 体 阳性 2例 , sl7 o1 抗 c O抗体 阳性 1 , 风湿 一 例 类
因子 阳性 3例 ,A C 阳性 3例 , 酶( 酸激 酶 、 pN A 肌 肌 乳 酸 脱 氢酶 、 草 转 氨 酶1 显 升高 6例 ,3 T 、 T 、 谷 明 T 、 4 F 3 F 4均升 高 1 , o s 间接 试验 阳性 l 。 T 例 C mb 直 例 23 辅助 检查 _ 肌 电图检查 6例 ,均显 示肌 源性 损 害 : 电图 1 异 常 ; 脑 例 X线检 查 2例 , 示双 手 、 显 足关
1 方 法 回顾 分 析 2 . 2 4例 重 叠综 合征 患 者 的 临床
表现 、 验室检查 、 实 辅助检 查 、 治疗及 转归 。
2 结果
21 临 床表 现 .
皮肤 黏膜 损 害 : 斑 1 红 6例 、 毛细 血
管 扩 张 8例 、 肤 硬 化 2例 、 敏 6例 、 皮 光 口腔 溃 疡 5
重叠综合征(专业知识值得参考借鉴)

重叠综合征(专业知识值得参考借鉴)一概述重叠综合征指的是患有两种或两种以上结缔组织病的重叠,亦称为重叠结缔组织病。
结缔组织病的重叠发生通常以传统的几个结缔组织病最常见,如系统性红斑狼疮、硬皮病、皮肌炎和多发性肌炎、类风湿关节炎、结节性多动脉炎等。
也有以其中的一种或两种与其他结缔组织病或自身免疫性疾病发生重叠,如干燥综合征、韦格纳肉芽肿、原发性胆汁性肝硬化等。
二病因重叠综合征的病因尚不清楚,主要与免疫功能异常、环境因素和遗传背景等相关。
发病机制还不清楚,可能是一种结缔组织病向另一种结缔组织病转化的过程。
三临床表现重叠综合征虽可在所有结缔组织病及其边缘病间重叠组合,实际上所见到的病例以系统性红斑狼疮、多发性肌炎/皮肌炎和系统性硬皮病间的重叠为主。
1.系统性红斑狼疮与系统性硬皮病重叠病初常表现为系统性红斑狼疮,以后出现皮肤硬化、吞咽困难及肺纤维化等表现。
一般面部红斑发生率较单纯系统性红斑狼疮低,雷诺现象发生率高。
抗dsDNA效价较低,狼疮细胞阳性率低。
ANA 呈高效价、高阳性率,成分为抗ENA抗体,荧光核型呈斑点型。
2.系统性红斑狼疮与多发性肌炎重叠除系统性红斑狼疮表现外,还有近端肌无力、肌痛及压痛、萎缩及皮下硬结。
血清ANA阳性率高,狼疮细胞检出率低。
低补体血症、高γ球蛋白血症。
血清肌浆酶如CPK、LDH及醛缩酶等增高,24小时尿肌酸排出量增加。
3.系统性红斑狼疮与类风湿关节炎(RA)重叠除系统性红斑狼疮症状外,还有关节炎、关节畸形等RA的表现。
血清类风湿因子(RF)及RA特异性抗体(抗CCP、AKA、APF等)可阳性。
4.系统性红斑狼疮与结节性多动脉炎(PAN)重叠系统性红斑狼疮与PAN重叠时,除系统性红斑狼疮表现外,有沿血管分布之皮下结节及腹痛,肾损害较单一系统性红斑狼疮时更重,肺部及中枢神经系统受累多见。
常见嗜酸性细胞增高,γ球蛋白高,但狼疮细胞阳性率低。
5.系统性硬皮病与多发性肌炎/皮肌炎重叠病人有近端肌无力、肌痛、关节痛、食管运动减慢及肺纤维化等改变。
重叠综合征最详细的介绍,重叠综合征是什么?

/
重叠综合征最详细的介绍,重叠综合征是什么?
重叠综合征的简介
重叠综合征(Overlap syndrome)指的是患有两种或两种以上结缔组织病间病情的重叠,亦称为重叠结缔组织病。
这种重叠可同时发生,好病人在同一时间符合两种或两种以上结缔组织病的诊断;亦可在不同时期先后发生另一种结缔组织病;或先有某一种结缔组织病,以后移行转变为另一种CTD。
这种转变可呈连续性或间隔一定时间后进行。
OS通常发生于6个弥漫性CTD,即SLE、RA、DM/PM、PSS、结节性多动脉炎(PN)及风湿热(RF)的重叠,亦可由6个CTD与近缘病如白塞病、干燥综合征、脂膜炎相重叠,此外尚可与其他自身免疫病如慢性甲状胆状腺炎、自身免疫性溶血性贫血等重叠。
重叠综合征的基本知识
是否属于医保:否
别名:重叠胶原病,重叠结缔组织病
发病部位:全身
传染性:无传染性
多发人群:有结缔组织病者
相关症状:无力、关节畸形、皮下结节、皮肤硬化
并发疾病:心血管疾病伴发的精神障碍重叠综合征要去什么医院,怎么检查治疗
就诊科室:风湿科
治疗费用:不同医院收费标准不一致,市三甲医院约(10000-50000元)
治愈率:70%
治疗方法:对症治疗、免疫抑制治疗
相关检查:尿肌酸、抗核抗体(ANA)、血清免疫球蛋白(Ig)、抗人球蛋白试验、尿谷草转氨酶(GOT)
文章来自:39疾病百科 /zdzhz/jbzs/。
重叠综合征是怎么回事?

重叠综合征是怎么回事?
*导读:本文向您详细介绍重叠综合征的病理病因,重叠综合征主要是由什么原因引起的。
*一、重叠综合征病因
西医:重叠综合征的病因尚不清楚,但是主要与免疫功能异常、环境因素和遗传背景相关。
中医:先天禀赋异常,久病肺虚,脾肾阳虚,每因感受外邪而加重,久则痰瘀交阻.临床可分为痰浊壅盛、痰热内蕴、痰瘀交阻、肺脾两虚、肺肾气虚五种证型辨证论治。
*二、发病机制
发病机制还清楚,可能是一种胶原病向另一种胶原病转化的过程。
*温馨提示:以上就是对于重叠综合征病因,重叠综合征是由什么原因引起的相关内容叙述,更多有关重叠综合征方面的知识,请继续关注疾病库,或者在站内搜索“重叠综合征”找到更多扩展内容,希望以上内容可以帮助到您!。
重叠综合征 病情说明指导书

重叠综合征病情说明指导书一、重叠综合征概述重叠综合征(overlap syndrome,OS)又称为重叠结缔组织病,指的是两种或两种以上结缔组织病同时或先后出现的疾病状态。
其发病原因暂时不明,可能与免疫功能异常、环境、遗传等因素有关。
本综合总有两种情况,一种是患者在同一时间内患有两种或两种以上结缔组织病;另一种是患者先后出现两种或两种以上结缔组织病。
随着对此病深入地认识,此病范畴已由6种传统结缔组织病,包括系统性红斑狼疮(SLE)、类风湿关节炎(RA)、多发性肌炎/皮肌炎(PM/DM)、进行性系统性硬化症(PSS)结节性多动脉炎(PN)和风湿热(RF)、扩展至结缔组织病及其近缘病,如贝赫切特综合征、干燥综合征、脂膜炎、韦氏肉芽肿与其他自身免疫性疾病的重叠。
其临床上主要表现为泛发性皮肤硬化、张口和吞咽困难、肺纤维化、四肢近端肌无力与肌痛、关节疼痛、肿胀甚至畸形等。
临床上常通过药物治疗缓解临床症状,防止病情进展。
英文名称:overlap syndrome,OS。
其它名称:重叠结缔组织病。
相关中医疾病:重叠痹病。
ICD疾病编码:暂无编码。
疾病分类:风湿免疫疾病。
是否纳入医保:部分药物、耗材、诊治项目在医保报销范围,具体报销比例请咨询当地医院医保中心。
遗传性:可能与遗传有关。
发病部位:全身。
常见症状:泛发性皮肤硬化、张口和吞咽困难、肺纤维化、四肢近端肌无力与肌痛、关节疼痛、肿胀甚至畸形。
主要病因:病因未明。
检查项目:血液检查、尿常规检查、自身抗体检测、CT检查、X线检查、MRI 检查、肌骨超声、心脏彩超。
重要提醒:一旦确诊,应积极进行治疗,以免疾病进展,危及患者生命。
临床分类:暂无资料。
二、重叠综合征的发病特点三、重叠综合征的病因病因总述:重叠综合征的发病原因和发病机制尚未明确,但目前认为重叠综合征的发生与免疫功能异常、环境因素和遗传背景相关。
基本病因:暂无资料。
危险因素:暂无资料。
诱发因素:暂无资料。
重叠综合征诊治策略ppt课件

8.肾脏
25%患者有肾脏损害
高滴度抗U1RNP抗体 弥漫性肾小球肾炎和实质间质性病变很少发生 通常为膜性肾小球肾炎 有时也可引起肾病综合征 多数患者没有症状 有些患者出现肾血管性高血压危象 与硬皮病肾危象类似
9.消化系统
胃肠道受累是有SSc特征患者的主要表现 约见于60~80%患者
表现: 上消化道运动异常 食道上部和下部括约肌压力降低,食道远端2/3蠕动 减弱,进食后发噎和吞咽困难 可有腹腔出血、胆道出血、十二指肠出血、巨结肠 、胰腺炎、腹水、蛋白丢失性肠病、原发性胆汁性 肝硬化、自身免疫性肝炎、吸收不良综合征 腹痛:可能由肠蠕动减退、浆膜炎 肠系膜血管炎、结肠穿孔或胰腺炎等所致
高滴度斑点型ANA和抗U1RNP抗体
临床综合征
雷诺现象、双手肿胀、多关节痛或关节炎、 肢端硬化、肌炎、食道运动功能障碍、肺动 脉高压等
临床表现
组成的各CTD(SLE, SSc, PM/DM或RA)的临床症 状多种临床表现并非同时出现 重叠的特征可以相继出现 不同的患者表现各异
1.早期症状 多有易疲劳、肌痛、关节痛和雷诺现象 手或手指肿胀+高滴度斑点型ANA- 仔细随诊 UCTD+高滴度抗U1RNP抗体→MCTD MCTD急性起病少见,表现 --PM、急性关节炎、无菌性脑膜炎、指趾坏疽、 高热、急性腹痛和三叉神经病
35%进展为某种DCTD 一种DCTD→另一种DCTD
Spliceosomes Nucleosomes Proteasomes
自身免疫应答
DCTDs自身免疫的靶抗原-剪接体
snRNP
U1 snRNP
重叠综合征PPT课件
其确切的机制尚不清楚,推断重叠综合征患者降低肺部过
度通气有可能会改善睡眠质量。
Kwon JS, et al. COPD. 2009;6:441-445.
OSA与重叠综合征的氧化应激反应
COPD与OSA存在氧化应激反应,反应产生大量ROS. 过量
1.49
Results.
治疗组 慢波睡眠时间%延长 (27.9±2.7 vs 42.3±4.2; p<0.01) 睡眠效率改善 (90.8±1.3 vs 94.4±1.5; p<0.05). AHI减低 (61.2±8.5 vs 43.1±8.6; p<0.05), 暂停相关觉醒 (22.2±7.6 vs 11.6±4.7; p<0.05), 最长呼吸暂停时间(S) (54.9±7.1 vs 37.8±5.6; p<0.01), 每小时低氧事件 (51.8±7.7 vs 37±7.8; p<0.01) 、 Epworth 评分(16.6±0.8 vs 9.2±0.9; p<0.001) 显著减低. 这些变化对照组未能见到. N-乙酰半胱氨酸显著减低血脂质过氧化物,增加抗氧化指标(谷胱 甘肽).
Lo´pez-Acevedo,et al.报告OSA患者中有10–20%为 重叠综合征。
最近的一篇综述指出,COPD与OSA共存的患者在成 年人群中近1%。
Lee R, et al. Curr Opin Pulm Med 2011,17:79–83 McNicholas WT. Am J Respir Crit Care Med 2009; 180:692–700.
帕金森叠加综合征、继发性帕金森综合征和遗传变性性帕金森综合征等疾病鉴别要点

帕金森叠加综合征、继发性帕金森综合征和遗传变性性帕金森综合征等疾病鉴别要点帕金森病是一种常见的神经系统变性疾病,病理上黑质多巴胺能神经元变性,纹状体神经递质多巴胺含量明显降低,临床上表现为静止性震颤、肌强直、运动迟缓和姿势平衡障碍等运动症状以及一系列的非运动症状。
临床上,帕金森病尤须注意与其他原因所致的帕金森综合征相鉴别,包括原发性帕金森病、帕金森叠加综合征、继发性帕金森综合征和遗传变性性帕金森综合征等。
帕金森病叠加综合征多系统萎缩(MSA)MSA包括橄榄脑桥小脑萎缩(MSA-C)和纹状体黑质变性(MSA-P)两大类。
临床表现为锥体外系、锥体系、小脑和自主神经等多系统损害,各种症状在不同亚型中可以存在重叠。
(1)MSA-C:小脑综合征为最常见的起始症状,临床多表现为步态蹒跚、四肢不灵活、精细动作困难、肌张力低下、意向性震颤、共济失调、构音障碍等。
构音障碍多表现为断续性、吟诗样、爆音性言语。
MRI可明显显示脑桥、小脑半球和(或)蚓部萎缩等。
脑桥“十字面包征”对于诊断和鉴别很有帮助。
注意,如果患者有家族史,需要考虑遗传性脊髓小脑共济失调。
(2)MSA-P:起病隐袭,具有帕金森病的某些临床特点,但是发展速度较帕金森病快,对左旋多巴治疗敏感性差。
特点为肌强直和运动迟缓为早期表现,但震颤少见。
吞咽和语言障碍并不少见,可出现锥体束征。
MRI的T2像显示壳核后外侧部的信号降低。
MSA-C型患者头颅MRI T2相上提示脑十字面包征”(白色箭头),同时伴有小脑半球及小脑蚓部萎缩。
MSA中的每一个类型均可以出现自主神经功能症状,包括直立性低血压导致的晕厥、性功能障碍、括约肌功能障碍、全身发汗异常等症状。
卧立位血压测定:直立位收缩压较卧位下降30mmHg以上,脉压下降20mmHg,而无代偿性心率。
肛门括约肌肌电图可呈神经源性改变。
进行性核上性麻痹特点包括:(1)40岁以后发病;(2)主要表现为对称性眼球垂直运动障碍,最早为向下注视障碍,逐渐发生上视运动困难,后期水平运动亦受限;(3)2/3患者的首发症状为步态不稳和平衡障碍,容易向后跌倒,有别于帕金森病向前跌倒;(4)颈部肌张力高,头颈后仰,轴性肌张力增高;(5)吞咽困难,构音障碍等假性延髓性麻痹症状常见;(6)眼睑失用;(7)左旋多巴治疗敏感性差;(8)头颅MRI可见中脑及脑桥萎缩,尤其在中脑被盖部的萎缩,形成细长、尖锐的“鸟嘴状”的形态。
中医治疗重叠综合征(完整版)

中医治疗重叠综合征(完整版)(一)辨证分型治疗1.寒凝血瘀证:主症:指(趾)端苍白或紫绀,遇寒则甚,肢温下降,肌肤刺痛或硬肿,关节酸痛,游走不定,舌苔白,舌质有瘀斑瘀点,脉沉细。
治法:温阳散寒,活血通络。
方药:桂枝四物汤加减。
制川乌9g(先煎),桂枝、赤芍、当归、川芎、红花、桃仁、炙地龙各9g,桑枝30g,生甘草3g,大枣5枚。
加减:关节酸痛较甚者,酌加秦艽9g,威灵仙12g。
2.阳虚血瘀证:主症:面色苍白,口唇无华,肌肤凝滞硬化,畏寒肢冷,关节僵硬冷痛,胸闷不舒,腰酸乏力,纳呆便溏,女子经少或经闭,男子阳痿遗精。
舌淡或青紫或舌体胖,脉沉缓。
治法:补肾壮阳,温经活络。
方药:右归饮加减。
桂枝、制附片各10g,鹿角片、山茱萸、熟地黄、肉苁蓉各12g,威灵仙、秦艽各6g,丹参、益母草各30g,淫羊藿、路路通各15g。
加减:血瘀症状明显,刺痛剧烈者加三棱、莪术。
3.阴虚血瘀证:主症:手脚弥漫性肿胀,伴有毛细血管扩张,盘状局限性红斑,或在手指关节背面有皮肌炎样的萎缩性红斑,指端粗厚,指关节伸侧面粗糙,甚至指端发生溃疡或坏死,或面部伴有蝶形红斑样皮损等。
常伴发热、关节疼痛、肌肉酸痛,周身倦怠等全身症状。
苔剥舌红或有瘀点、瘀斑,脉细涩。
治法:养阴清热,益气活血。
方药:麦味地黄丸加减。
天冬、麦冬各9g,生地黄30g,玄参12g,山茱萸12g,白花蛇舌草、鹿衔草、六月雪、虎杖、生黄芪、山药、丹参、鸡血藤各30g,炙地龙、乌梢蛇各15g。
加减:发热者,加生石膏18g,知母、黄柏各9g;自汗盗汗者加生牡蛎30g(先煎),生黄芪20g。
4.热毒瘀阻证:主症:高热,烦燥,面肤潮红,肌肉关节红肿热痛,皮肤紫斑,口渴饮冷,尿黄赤,便干。
舌红苔黄腻,脉数。
治法:清热解毒,凉血通络。
方药:犀角地黄汤加减。
水牛角30g,生地30g,赤芍、牡丹皮各15g,青蒿、连翘、黄芩、大青叶、白花蛇舌草各10g,丹参15g,鸡血藤、忍冬藤各30g,生甘草10g。
哮喘慢阻肺重叠综合征

根据患者的具体情况制定个体化的治疗方案,以提高治疗效果和患 者生活质量。
新型治疗手段
探索新型治疗手段,如细胞治疗、基因治疗等,为哮喘慢阻肺重叠综 合征的治疗提供更多选择。
社会支持与政策研究
社会认知提升
加强公众对哮喘慢阻肺 重叠综合征的认知,提 高患者自我管理和预防 意识。
医疗保障政策
诊断率
由于ACOS临床表现复杂, 诊断率较低,许多患者可 能长期被误诊或漏诊。
临床表现
症状
ACOS患者可能出现咳嗽、 咳痰、呼吸困难等症状, 其中呼吸困难常呈持续性, 且在活动后加重。
体征
肺部听诊可能闻及哮鸣音 和湿啰音,严重时可出现 桶状胸、呼吸浅快等 COPD典型体征。
病程
ACOS病程较长,且容易 反复发作,严重影响患者 的生活质量和预后。
研究制定针对哮喘慢阻 肺重叠综合征的医疗保 障政策,减轻患者经济 负担。
康复与护理支持
建立完善的康复与护理 支持体系,为患者提供 全方位的关怀和支持。
THANKS FOR WATCHING
感谢您的观看
03
哮喘慢阻肺重叠综合征 的诊断与鉴别诊断
诊断标准
支气管哮喘病史
症状和肺功能异常
患者通常有长期反复发作的哮喘病史, 症状包括喘息、胸闷、咳嗽等。
患者同时具备哮喘和慢阻肺的症状和 肺功能异常,如活动后气短、喘息、 咳嗽、咳痰等。
慢阻肺气流受限
在哮喘控制良好的情况下,患者仍存 在不可逆的气流受限,符合慢阻肺的 诊断标准。
新药研发
新型抗炎药物
研发针对哮喘慢阻肺重叠综合征的特异性抗炎药物,以减轻气道 炎症和气道重塑。
新型免疫调节剂
探索新型免疫调节剂,以调节免疫失衡,降低气道高反应性。
重叠综合征研究进展

Advances in Clinical Medicine 临床医学进展, 2023, 13(5), 8621-8626 Published Online May 2023 in Hans. https:///journal/acm https:///10.12677/acm.2023.1351205重叠综合征研究进展孙文娟,杨发满,李晓平青海大学附属医院老年医学科,青海 西宁收稿日期:2023年4月28日;录用日期:2023年5月21日;发布日期:2023年5月29日摘要 研究发现睡眠呼吸暂停综合征、慢性阻塞性肺疾病与炎症因子、维生素存在相关性,然而,关于OS 患者维生素D 状态及炎症因子的证据很少。
近期研究发现睡眠呼吸暂停综合征导致的慢性间歇性缺氧、高碳酸血症、炎症因子释放、交感神经激活等机制与慢性阻塞性肺疾病的不可逆性气道阻塞有一定的共通性。
本文就机制进一步阐述维生素D 状态及炎症因子在其两种疾病中的共同特点。
关键词重叠综合征,慢性阻塞性肺疾病,阻塞性睡眠呼吸暂停综合征,炎症因子,维生素D ,研究进展,综述 Advances in Research of Overlap SyndromeWenjuan Sun, Faman Yang, Xiaoping LiDepartment of Geriatrics, Qinghai University Affiliated Hospital, Xining Qinghai Received: Apr. 28th , 2023; accepted: May 21st , 2023; published: May 29th , 2023AbstractStudies have found that sleep apnea syndrome and chronic obstructive pulmonary disease are as-sociated with inflammatory factors and vitamins. However, there is little evidence on vitamin D status and inflammatory factors in patients with OS. Recent studies have found that the mechan-isms of chronic intermittent hypoxia, hypercapnia, inflammatory cytokine release, and sympa-thetic nerve activation caused by sleep apnea syndrome have certain commonness with irreversi-ble airway obstruction in chronic obstructive pulmonary disease. This article further elucidates the mechanism of vitamin D status and the common characteristics of inflammatory cytokines in both diseases.孙文娟等KeywordsOverlap Syndrome, Chronic Obstructive Pulmonary Disease, Obstructive Sleep Apnea Syndrome, Inflammatory Cytokines, Vitamin D, Research Progress, SummaryThis work is licensed under the Creative Commons Attribution International License (CC BY 4.0)./licenses/by/4.0/1. OS定义OS别名为重叠综合征,是1958年的时候一位名为Fenfley的作者提出的概念,此主要含义是指阻塞性睡眠呼吸暂停综合征(obstructive sleep apnea hypopnea syndrome, OSAHS)与慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)同时存在,为了更容易让人们理解,所以简称为OS [1],这是一种独特的综合征。
COPD与OSA重叠综合征

9.13±12.59
4.51 (1.36,11.59)
28.86 18.63
3.51 (1.35,8.81) *
22.32* 13.97*
Am J Respir Crit Care Med 2003;167:7–14
经过BMI校正后,两组无显著性差异
近期研究:OSAHS和COPD共存 可能是巧合
• 较长时间(常数分钟)的低氧和较缓慢 的恢复可以与OSA的间歇低氧鉴别,后 者的低氧很少超过1分钟,并且往往很快 就恢复到正常水平。
COPD
OSA
COPD睡眠低氧与OSA睡眠低氧
COPD与OSAHS睡眠低氧的异同
重叠综合征的流行病学研究
• 早期研究:认为两者同时存在的可能性非常 高
– Guilleminault 等研究了26例COPD患者,发现 其中22例伴呼吸暂停(85%)(因嗜睡而在睡眠 门诊就诊患者) – Bradley 等和Chaouat 等观察了OSA患者(n = 50和265)的COPD发生率,结果发现分别为 14% 和11% (40岁以上人群)
OSAHS影响 1、Sanders等发现与单纯阻塞性肺疾病患 者相比,重叠综合征者有较高的Epworth 睡眠评分,总睡眠时间缩短,睡眠效率下 降,觉醒指数增加 2、而重叠综合征与单纯SAHS患者相比, 两者的差别并不明显 —— 提示重叠综合征睡眠质量的下降主要 受SAHS的影响,而并非气流受限的程度 影响。
• 睡眠质量下降 1、总睡眠时间缩短、睡眠效率下降、微觉 醒指数增加 2、ESS评分增加 3、打鼾、夜间憋醒
• 睡眠质量下降原因 COPD的影响: 1、许多COPD患者睡眠质量差,EEG检查 也发现睡眠质量下降的证据,尤其是重 度COPD者。 2、另一方面,轻度COPD可能不影响睡眠 质量。在上面SHHS研究中观察到1138 例不伴OSA的轻度COPD患者,睡眠较 少受到影响,睡眠结构与FEV1水平无明 显相关性。
双合征名词解释

双合征名词解释
双合征(double crush syndrome)又称双卡综合征,是指周围神
经在其行程中受到两处压迫,引起的一系列症状和体征。
常见的双合征包括腕管综合征和肘管综合征。
腕管综合征是指正
中神经在腕管内受到压迫,导致手部麻木、疼痛、无力等症状。
肘管
综合征是指尺神经在肘部尺神经沟内受到压迫,导致手部麻木、无力、肌肉萎缩等症状。
双合征的发生是由于神经在两处受到压迫,导致神经传导受阻,从而引起症状。
治疗双合征的关键是解除神经压迫,可以通过手术或保守治疗来实现。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• Even by chance alone, a patient with one of the disorders has a greater than 10% chance of also having the other disease. Thus, when seeing a patient with either OSA or COPD, it is reasonable to screen for the other, based on history and review of systems.
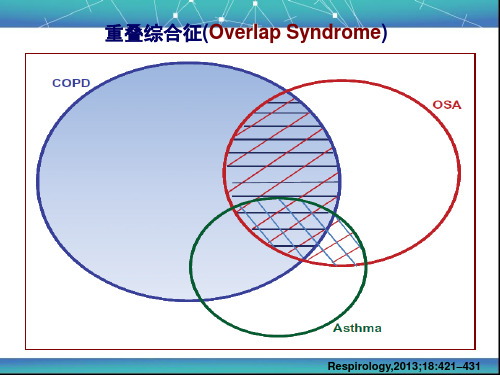
重叠综合征
Overlap Syndrome
王洪冰
参考文献 1.Update on obstructive sleep apnea and its relation to COPD . Int J Chron Obstruct Pulmon Dis. 2014; 9: 349–362 2.Sleep-Disordered Breathing and COPD: The Overlap Syndrome. Respir Care. 2010 October ; 55(10): 1333–1346.
(Sleep Heart Health Study and the MONICA-II study)
OS诊断
• 诊断OS有临床意义,首先,提供了有用的信息来治疗潜 在的疾病。其次,提醒医师在行压力滴定时应注意口鼻气 流而非饱和度。最后,还能提醒医师进行进一步的肺高压 的评价,如心超或右心导管。 • 许多患者是先有了OSA或COPD然后去看医生进行深入检 查。重度COPD经常有睡眠问题。然而,轻度者对睡眠影 响甚微。故而需要PSG筛查,但仍可能低估漏诊,因为一 些OSA患者几乎没有症状,但临床仍可能相关。
• OSA患者应询问吸烟史,这样能促进肺功能的监测。 • OSA伴有白天缺氧或高碳酸者应筛查COPD。 • ATS/ERS指南建议:所有轻度COPD及有肺高压迹象者, 应做睡眠检测。 • 有证据显示:OS合并肺高压者经常症状较轻。 比如, OS合并肺高压时其FEV1是1.8L,FEV1/FVC:0.64,醒时 PaO2:64mmHg。 而单纯COPD合并肺高压者 FEV1<1L,FEV1/FVC<0.50,醒时PaO2<55mmHg. •
睡眠与通气
• In normals, minute ventilation drops from wakefulness to non-REM sleep, and drops further during REM sleep (about 15%, compared to the awake value).——潮气量降低
• OS高碳酸也相比之下更严重,因此也具重要性。两种疾病都会导致 炎性反应,氧化应激如TNF、IL-6、IL-8等。Mc’等研究显示两种疾病 通过相同机制导致心血管疾病发生。之中机制是附加的还是协同性的 尚不得而知。死因多为心血管方面。一项研究显示OSA可致COPD急 性加重,并因此加速肺功能减退,使死亡率增加。
• Hawrylkiewicz等观察到16%的OSA患者有 肺高压,而OS患者中则86%的有肺高压。
• 即使重度OSA如果没有其他心肺疾病,也不会合 并显著的肺动脉高压,即使有也是轻度肺高压, 且临床意义不明确。 • 有些研究运用右心导管,证实了COPD伴白天缺 氧和高碳酸者存在休息和运动时肺动脉高压
OS死亡率
• OS死亡率直到近期才得到有效研究。一些卒于呼吸衰竭 的COPD患者,或更易卒于心血管病或肿瘤。因死亡多发 生于夜间。 • 如Mc'等报道1984年他们收入院的COPD患者比其他患者 更多卒于夜间,死者多为―blue-bloaters”。推测有些可能 是OS患者。同样一些OSA患者可意外卒于夜间,尤其凌 晨,通常死于心血管病。
OS死亡率
• 对于OSA患者,一些肺指标预示着OS患者的高死亡率,如合并COPD 、低FEV1、吸烟史。Lavie指导的最大一项单变量研究显示,COPD使 OSA患者死亡率提高了7倍。 • 相反地,COPD患者如果合并OSA也会使死亡率增加。Marin等比较 了COPD与OS患者用与不用CPAP治疗的情况,随访9年余,全因死亡 率在未治疗OS组为42.2%,在COPD组为24.2%。即使矫正了COPD 严重度,合并OSA仍然是死亡的危险因素。 • The exact mechanism(s) that account for this increased morbidity and mortality risk are not known exactly. Increased risk of death may be due to more prolonged hypoxia.
• Fin'等建议COPD伴夜间缺氧患者即使吸氧后仍有晨起头 痛者要行PSG检查。 • COPD患者仅做夜间氧饱和度检测无助于诊断,因为夜间 SaO2只反应COPD、某些COPD+OSA、或OSA,治疗则 不尽相同。对夜间缺氧的定义不同,则导致治疗的差别很 大。最后,很少的研究能证实,仅纠正夜间缺氧能改善 COPD的预后。
• 气管扩张剂:Martin等给36例重度COPD患者给予异丙托溴铵4次/日 。4周后,夜间缺氧有改善,睡眠质量向好,REM时间有所增加。 噻托溴铵也可改善夜间缺氧,睡眠质量没有变化。 LABA也有同样的 效果。 稳定期COPD口服激素可改善氧合和TST,据此推测吸入激 素也可取得同样效果,但尚无数据支持。因此,治疗COPD的药物也 能改善OS的夜间缺氧,从而减少对氧疗的依赖。但治疗COPD是否 因此而使OSA获益则不得而知。
• ATS/ERS指南建议:所有轻度COPD及有肺高压迹象者, 应做睡眠检测。
有证据显示:OS合并肺高压者经常症状较轻。 比如,OS合并肺高压时其 FEV1是1.8L,FEV1/FVC:0.64,醒时PaO2:64mmHg。 而单纯COPD合并肺高 压者FEV1<1L,FEV1/FVC<0.50,醒时PaO2<55mmHg.
OS与夜间缺氧
• OS有双重因素致夜间缺氧。 • OS夜间缺氧时间更长于单纯OSA;阻塞程度与长期低氧 相关。与单纯OSA相比,合并COPD使缺氧更长,也增加 死亡率。
肺动脉高压
• Acutely, nocturnal oxygen desaturation causes surges in both systemic and pulmonary blood pressure. It now seems likely that repetitive, transient oxygen desaturation can cause pulmonary hypertension.These consequences might help explain why nocturnal oxygen desaturation is a marker of increased mortality, and why COPD patients are reported to die more frequently at night than expected. • overlap-syndrome patients with pulmonary hypertension often have relatively mild abnormalities, as measured by spirometry or oxygenation, especially when compared to COPD-only patients with pulmonary hypertension
• Perhaps most clinically relevant, nocturnal oxygen desaturation is a marker of increased mortality in COPD.
•
Even without any upper-airway contribution, various studies have reported that 27–70% of patients with COPD with awake oxygen saturation of 90 – 95% can experience substantial desaturation at night, particularly during REM sleep 。
OS治疗
• 治疗手段:OS的治疗并非有别于OSA和COPD。 • 治疗目的:维持适当氧合和防止SDB。 • 减肥:减轻体重有益于OSA和肥胖者。然而对于COPD,体重减轻则会 增加死亡率,随疾病严重程度其恶液质也加重。因此,OS患者不建议 减轻体重;然而,轻度COPD或可获益于饮食控制和运动。
• 氧疗:对于白天和夜间缺氧的患者来说是基本的,已证实每日吸氧18 小时以上(包括睡中)可改善整体死亡率。比仅于夜间吸氧要有效果 。COPD仅伴夜间缺氧会增加死亡风险(与无夜间缺氧者比较,数据 仅来自一项回顾性分析)。另外,只纠正夜间缺氧(白天无缺氧)也 不能显著改善肺循环或死亡率,尽管可改善睡眠质量,而且医生也经 常这样给出建议。 • 单纯给OSAS患者氧疗和缺乏能改善的支持数据。尽管氧疗使夜间氧 合有所改善,但睡眠结构、醒觉、嗜睡等没有得到缓解,氧疗2周也 未能改善血压(而CPAP治疗2周后即可改善血压)。 • 仅有一个研究针对OS的氧疗,Alford等研究了20例OS患者给予4L/分 ,夜间缺氧有所改善,但OSA从25.7/h增加到了31.4/h,呼气末PCO2 从52.8增加到了62.3,PH也相应下降。因此,单纯氧疗不适用于OS 患者。
• Beker测量了正常人和COPD患者在清醒、NREN、REM中的分钟通 气量,发现COPD患者的从清醒时到NREM时降低了16%,到REM时 降低了32%,主要时由于潮气量的降低。 • O’Donoghue等发现高碳酸COPD患者在NREM是分钟通气量降低更 加严重。
