九年级化学酸碱盐复习1
九年级化学酸碱盐知识梳理

第一讲酸碱盐知识梳理一、酸碱盐的概念①酸:电离出的阳离子全部为氢离子的化合物叫酸。
(酸由H元素和酸根组成)。
②碱:电离出的阴离子全部为氢氧根离子的化合物叫碱。
③盐:由金属离子(或铵根离子)与酸根离子构成的化合物。
二、常见酸碱盐的物理性质(一)、常见的酸:盐酸:HCl 硫酸:H2SO4碳酸:H2CO3硝酸:HNO3醋酸:CH3COOH1、盐酸(HCl气体的水溶液。
)物理性质:①无色液体②有刺激性气味③有挥发性用途:①除铁锈②帮助消化③制药物注意:①浓盐酸在空气中产生白雾的原因:由于浓盐酸挥发出的HCl气体与空气中的水蒸气结合形成了盐酸小液滴。
②浓盐酸敞放在空气中,溶质的质量分数减小。
2、硫酸:H2SO4物理性质:无色、油状液体。
浓硫酸的特性:①吸水性。
物理性质。
浓硫酸可作气体干燥剂,但不能干燥氨气(NH3)如:胆矾CuSO4.5H2O与浓硫酸作用,变为白色的CuSO4,其中浓硫酸表现为吸水性。
②腐蚀性,脱水性(化学性质)如:浓硫酸使木条或纸张变黑,其中浓硫酸表现为脱水性③溶解于水放出大量的热用途:①除铁锈②作气体干燥剂注意:①稀释浓硫酸的方法:将浓硫酸沿器壁慢慢注入水中,并不断搅拌。
玻璃棒的作用:搅拌,使产生的热量迅速扩散。
②浓硫酸沾在皮肤上的处理方法:先用大量的水冲洗,在涂3%--5%的NaHCO3溶液③浓硫酸敞放的空气中,会吸收水分,质量增加,溶质质量分数减小。
(二)、常见的碱: 氢氧化钠:NaOH 氢氧化钙:Ca(OH)2氨水:NH3. H2O1、氢氧化钠:俗名:火碱、烧碱、苛性钠。
物理性质:易溶于水且放热。
(有吸水性,NaOH固体可作某些气体的干燥剂,但不能干燥CO2、SO2、HCl)用途:制肥皂、做干燥剂、除油污、。
注意:①NaOH固体要密封保存的原因:a:吸收空气中的水分而潮解;b:与空气中的CO2 反应而变质。
(反应方程式:2NaOH+CO2=Na2CO3+H2O)②检验NaOH是否变质的方法:加入稀盐酸,若有气泡,则变质。
九年级科学--化学部分复习(酸碱盐)
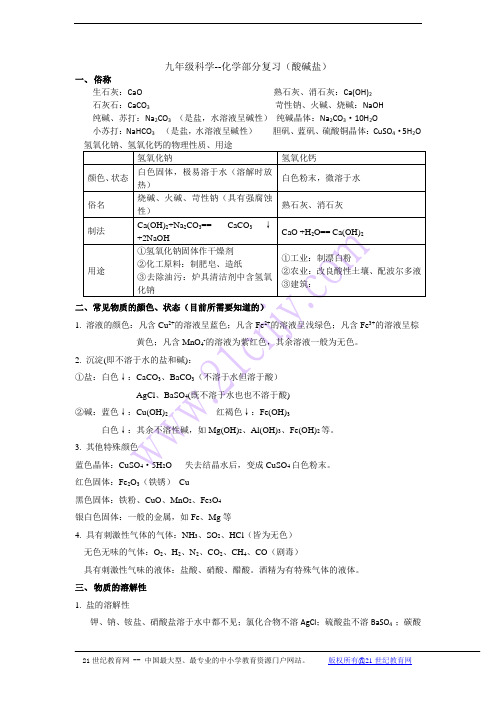
九年级科学--化学部分复习(酸碱盐)一、俗称生石灰:CaO 熟石灰、消石灰:Ca(OH)2石灰石:CaCO3 苛性钠、火碱、烧碱:NaOH纯碱、苏打:Na2CO3(是盐,水溶液呈碱性)纯碱晶体:Na2CO3·10H2O小苏打:NaHCO3(是盐,水溶液呈碱性)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O 氢氧化钠、氢氧化钙的物理性质、用途氢氧化钠氢氧化钙颜色、状态白色固体,极易溶于水(溶解时放热)白色粉末,微溶于水俗名烧碱、火碱、苛性钠(具有强腐蚀性)熟石灰、消石灰制法Ca(OH)2+Na2CO3== CaCO3↓+2NaOHCaO +H2O== Ca(OH)2用途①氢氧化钠固体作干燥剂②化工原料:制肥皂、造纸③去除油污:炉具清洁剂中含氢氧化钠①工业:制漂白粉②农业:改良酸性土壤、配波尔多液③建筑:二、常见物质的颜色、状态(目前所需要知道的)1. 溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色;凡含MnO4-的溶液为紫红色,其余溶液一般为无色。
2. 沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(不溶于水但溶于酸)AgCl、BaSO4(既不溶于水也也不溶于酸)②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余不溶性碱,如Mg(OH)2、Al(OH)3、Fe(OH)2等。
3. 其他特殊颜色蓝色晶体:CuSO4·5H2O 失去结晶水后,变成CuSO4白色粉末。
红色固体:Fe2O3(铁锈)Cu黑色固体:铁粉、CuO、MnO2、Fe3O4银白色固体:一般的金属,如Fe、Mg等4. 具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
三、物质的溶解性1. 盐的溶解性钾、钠、铵盐、硝酸盐溶于水中都不见;氯化合物不溶AgCl;硫酸盐不溶BaSO4 ;碳酸盐只溶钾、钠、铵。
6初三化学酸碱盐复习

4、常见酸碱盐的性质 (1)浓盐酸有强烈的挥发性(白雾),具体强烈的刺激 性气味。
浓硫酸具有强烈的吸水性(脱水性),溶于水会放 出大量的热。 (2)NaOH有吸水性,易潮解易变质,具有强烈的脱脂性, 溶于水时会放出大量的热。
氨气溶于水显碱性,NH3·H2O=NH4OH (3)CaO又名生石灰,能与水反应放出大量的热,生成熟 石灰。
石灰石CaCO3。 化肥:土壤里通常缺乏氮、磷、钾三种元素,
植物生长对这三种元素的需求量较大, 于是就产生了化肥。氮叶钾茎磷根。 氮肥:碳酸氢铵NH4HCO3、硝酸铵NH4NO3、 氯化铵NH4Cl、尿素CO(NH2)2 钾肥:氯化钾KCl、硫酸钾K2SO4、 碳酸钾K2CO3(草木灰)、 磷肥:磷矿粉Ca3(PO4)2、过磷酸钙 复合肥:硝酸钾KNO3、磷酸二氢钾KH2PO4
初中化学单元 复习课
上云桥中学 刘雪平老师执教
酸碱盐(一)
基础知识:
1、酸的本质是含有 H+ 离子, 碱的本质是含有 OH- 离子, 盐都含有金属离子和酸根离子。 2、紫色石蕊试液遇酸变红,遇碱变蓝。 无色酚酞试液遇酸不变色,遇碱变红。 PH=7为中性,PH<7为酸性,PH>7为碱性。
3、常见的酸碱盐 酸:盐酸HCl、硫酸H2SO4 碱:烧碱NaOH、熟石灰Ca(OH)2 盐:食盐NaCl、纯碱Na2CO3、小苏打NaHCO3、
6、将一枚表面有锈的铁钉放入过量的稀硫酸中,
发生的反应有(用化学方程式表示)
_2_F_e_2O_3_+_6_H_2S_O_4=__2_F_e_2(_S_O_4_)_3+_6_H_2O____
,
。Fe+H2SO4=FeSO4+H2↑
7、将一瓶盐酸分成两等份,并分别放入两个烧
九年级化学酸碱盐总复习课件

酸碱盐在水溶液中电离与导电性
电离
酸碱盐在水溶液中会电离成自由 移动的离子。
导电性
由于电离产生的自由离子,酸碱 盐溶液具有导电性。
酸碱盐反应类型及规律
中和反应
酸和碱反应生成盐和水。
复分解反应
两种化合物相互交换成分生成另外 两种化合物的反应,需满足生成物 中有沉淀、气体或水生成的条件。
氧化还原反应
部分酸碱盐在反应中会发生电 子转移,属于氧化还原反应。
洗涤
利用碱性物质能够去除油污的原理,可以使用氢氧化钠、碳酸钠等碱性溶液来洗 涤油污严重的衣物或器皿。此外,还可以利用盐类(如磷酸盐、硅酸盐等)的乳 化、分散等作用来增强洗涤效果。
03 实验室中常见酸碱盐操作 技巧
实验室安全注意事项
01
遵守实验室规则,保持 实验室整洁和安静。
02
03
04
穿戴实验服和护目镜等 个人防护装备。
降低对环境的影响。
05 复习策略与备考建议
知识点梳理和归纳总结
梳理酸碱盐的基本概 念、性质及相互转化 关系
总结酸碱盐在日常生 活、工农业生产中的 应用
归纳酸碱盐的反应类 型、方程式及实验现 象
典型例题解析和答题技巧
解析酸碱盐相关的选择题、填空题、 实验题等典型题型
学会分析题目中的关键信息,提高解 题速度和准确率
碱的作用
碱在工业生产中常用于中和酸性废水、 制造玻璃、造纸等,如氢氧化钠、氢 氧化钙等。
环境保护与资源回收利用
酸碱盐废水处理
工业生产中产生的酸碱盐废水需 经过中和、沉淀、过滤等处理,
达到排放标准。
资源回收利用
如从废酸中回收有用物质,从废 碱中回收氢氧化钠等,实现资源
九年级化学教案:酸碱盐的应用(复习,全4课时)

新沂市第六中学教案课时总编号新沂市第六中学教案课时总编号新沂市第六中学教案课时总编号备课组化学上课时间第3课时课型复习主备教学内容第七章应用广泛的酸碱盐(复习3)教学目标1.熟悉常见的盐(食盐、纯碱、硫酸铜、碳酸钙)的性质及用途2.熟练掌握盐的溶解性,铵盐的检验,化学肥料的使用。
3.知道金属活动性顺序的探究,了解复分解反应发生的条件教学重点1.盐的化学性质。
2.金属活动性顺序的探究教学难点1.复分解反应发生的条件2.金属活动性顺序的探究教学方法总结归纳练习教具教学过程教学活及组织过程动个案创新自学指导一、知识点归纳1.你知道锌、铁、铜三种金属活动性强弱顺序吗?请提出你的假设,并设计实验检验你的假设是否正确。
猜想:操作方法现象结论及方程式2.总结出常见金属的活动性顺序3.掌握金属活动性顺序有何用途?4.金属活动性顺序主要应用于在溶液中进行的两类置换反应:(一)、金属+酸→盐和氢气.1.在金属活动性顺序中金属排在氢前边;2.酸是指盐酸和稀硫酸等非氧化性酸,而浓硫酸、硝酸,不溶性酸、极弱的酸除外(二)、金属+盐→另一种金属+另一种盐.1.反应物中的金属必须排在盐中的金属元素前边;2.盐必须可溶.交流展示拓展提高5.化肥哪几种?6.铵态氮肥的检验:活动二:交流展示拓展提高例1.不能与稀硫酸反应生成氢气的金属是( )A.银 B.镁 C.锌 D.铁例2.为验证a、b、c三种金属的活动性,将它们分别投入稀盐酸中,只有c不能与盐酸作用产生气体。
再把a投入b的硝酸盐溶液中,在a的表面有b析出。
则三种金属的活动性顺序为( )A.b>a>c B.a>b>c C.b>c>a D.c>a>b例3.请你设计实验方案证明锌、银、(H)、铜的活动性【总结】设计实验验证金属活动性顺序的一般思路1-金属与酸:能反应的比不能反应的活动性强,都能反应的比较反应的快慢,反应快的比反应慢的活动性强2-金属与盐;能置换说明该金属的活动性比盐中的金属活动性强二、随堂测试1.化学就在我们身边,生活中处处有化学。
酸碱盐基础知识复习 带答案

酸碱盐基础知识复习1、酸碱指示剂定义:遇到酸或碱溶液发生特定颜色变化的物质。
常见的酸碱指示剂有 紫 色石蕊试液和 无 色的酚酞试液。
2、指示剂的变色规律判断下列说法是否正确:①紫色石蕊试液能使稀盐酸变红( × )说明:变色的是酸碱指示剂而不是酸碱。
②紫色石蕊试液遇到稀盐酸变红( √ )③所有的碱都能使无色酚酞变红( × )说明:难溶性碱不能电离出OH -,不能使酚酞变红④能使紫色石蕊变蓝的溶液一定是碱溶液( × )说明:有些盐溶液如Na 2CO 3溶液显碱性,也能使酚酞变红。
3、石蕊试纸的使用方法4、酸的定义:电离出的阳离子全都是氢离子的化合物_,酸中一定含__氢___元素,可能含__氧__元素。
请分别举出含氧酸与不含氧酸的例子___HCl_____、____H 2SO 4____。
5、碱的定义:电离出的阴离子全都是氢氧根离子的化合物_,碱中一定含__氢__、__氧__元素,不一定含_金属_元素,例如__NH 3·H 2O__中就不含。
碱根据是否可溶于水,可分为可溶性碱和难溶性碱两类,常见的可溶性碱有KOH 、NaOH 、Ba(OH)2、Ca(OH)2、NH 3·H 2O 等5种。
常见的难溶性碱有Cu(OH)2、Fe(OH)3、Mg(OH)2等。
6、①酸溶液中都含有__H +_使溶液显__酸__性;溶液显酸性说明溶液中含有_ H +_,但并不是只有酸的溶液中才有H +,某些盐溶液例如NH 4Cl 等也能电离出H +,它们的水溶液也显酸性。
②碱溶液中都含有__OH -__使溶液显_碱_性;溶液显碱性,说明溶液中含有__OH -__,但并不是只有碱的溶液中才有OH —。
某些盐溶液例如__Na 2CO 3__等也能电离出OH —,它们的水溶液也显碱性。
③酸溶液和酸性溶液的共同点是都含有H +,不同点是酸溶液阳离子全都是H +,酸性溶液中的阳离子除了H +,还有其它阳离子。
初三化学-酸碱盐的综合复习

01 酸碱盐的综合复习一、基础知识复习知识点一:酸的复习1.常见的酸(1)浓盐酸①盐酸的物理性质:盐酸是_____色透明的液体,有_____气味,具有_____性。
【拓展】通常盐酸为无色液体,工业盐酸因含FeCl3而显黄色。
②挥发性:盐酸浓度越大,挥发性越_____。
浓盐酸瓶口出现_____,这是由于___________________________________________的缘故。
保存时必须__________,敞口放在空气中,溶质质量_______,溶液浓度会_______。
(2)浓硫酸①物理性质:纯净的硫酸是无色、粘稠、油状的液体,不易挥发,易溶于水并放出大量的热。
浓硫酸稀释时,需把浓H2SO4沿容器壁慢慢注入水中且边倒边搅拌,切不可将水倒入浓硫酸。
※②吸水性、脱水性、强氧化性。
③硫酸的用途:用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等,在实验室中还可作干燥剂。
2.稀酸的通性酸的组成中均含有________,因此酸具有相似的性质。
(1)酸溶液与指示剂反应。
(2)中和反应:酸+ 碱→ 盐+ 水①定义:酸和碱反应,生成盐和水并放出热量的反应称为中和反应。
如盐酸与氢氧化铁的反应,实验现象是:再如H2SO4 +2NaOH = Na2SO4 + 2H2O;无明显现象,需要使用酸碱指示剂判定反应的发生。
②中和反应的应用:a.___________:改良酸性土壤。
b.___________:治疗胃酸过多。
(4)酸+ 活泼金属(活动性顺序表中排在H前的金属)→盐+ H2↑铁钉和盐酸反应:;现象:;【注意】一般采用稀硫酸或者稀盐酸,浓盐酸挥发性太强,产生的氢气中含有大量氯化氢气体,浓硫酸或硝酸与金属反应不产生氢气。
(5)酸与某些盐反应:①与碳酸盐反应生成二氧化碳:实验现象:有气泡产生②与一些盐反应生成沉淀用氯化钡溶液检验硫酸:_________________________________;用硝酸银溶液检验盐酸:_________________________________;【酸的基础小练习】1.下列物质与盐酸反应,既不生成沉淀,又无气体放出,且溶液显无色的是()A.Na2CO3B.AgNO3C.MgO D.Cu(OH)22.经测定某溶液的pH=1,下列物质中不能在该溶液中大量存在的是()A.氯化钠B.氯化铜C.氢氧化钾D.稀硫酸3.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种。
初三化学酸碱盐知识点(最全整理版)

应用广泛的酸、碱、盐一.溶液的酸碱性一、酸性溶液和碱性溶液1.实验:检验溶液的酸碱性实验试样白醋酸果汁稀盐酸纯碱溶液肥皂水石灰水氨水食盐水蔗糖水滴加紫色石蕊试液变红变红变红变蓝变蓝变蓝变蓝紫色紫色滴加无色酚酞试液无色无色无色变红变红变红变红无色无色结论酸性酸性酸性碱性碱性碱性碱性中性中性结论:(1)凡是能使紫色石蕊试液变红的溶液都是酸性..溶液,并且该溶液不能使无色酚酞试液变色;(2)凡是能使紫色石蕊试液变蓝的溶液都是碱性..溶液,并且该溶液能使无色酚酞试液变红;(3)不能使紫色石蕊试液变色,也不能使无色酚酞试液变色的溶液,我们称为中性溶液。
(4)如紫色石蕊试液及无色酚酞等能检验溶液酸碱性的试液,称为酸碱指示剂。
注意:①我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性;②酸性溶液能使蓝色石蕊试纸变红,碱性溶液能使红色石蕊试纸变蓝;③只有可溶性的酸性、碱性物质才能使指示剂变色,变色的是指示剂,而不是该物质。
2.日常生活中常见的酸性物质与碱性物质(1)酸性物质:山楂、柠檬、柑橘、西红柿等;(2)碱性物质:茶叶碱、烟碱等。
3.区分酸溶液和酸性溶液、碱溶液和碱性溶液注意:酸溶液是指酸的水溶液,酸性溶液是指能使紫色石蕊试液变红的溶液,因此酸溶液一定是酸性溶液,而酸性溶液不一定是酸溶液;同样,碱性溶液不一定是碱溶液,碱溶液一定是碱性溶液。
例如:硫酸铜、氯化铵的水溶液显酸性,而不是酸;纯碱、肥皂的水溶液显碱性,但不是碱。
4.补充知识:酸、碱、盐的概念(1)酸:电离时生成的阳离子全部..是氢离子的化合物。
如:HCl、HNO3、H2SO4、H2CO3等。
1HCl==H++Cl-;H2SO4==2H++SO42-;(2)碱:电离时生成的阴离子全部..是氢氧根离子的化合物。
如:NaOH、Ca(OH)2等。
NaOH==Na++OH-;Ca(OH)2==Ca2++2OH-;(3)盐:电离时生成金属离子(或铵根离子)和酸根离子的化合物。
初三化学酸碱盐知识点复习

初三化学酸碱盐知识点复习(一)碱的性质:(1)碱溶液能使紫色石蕊试液变蓝色,无色酚酞试液变红色。
(2)碱 + 多数非金属氧化物 = 盐 + 水(3)碱 + 酸 = 盐 + 水(4)碱+某些盐 = 另一种盐 + 另一种碱1、氢氧化钠跟二氧化碳反应:2NaOH + CO2 = Na2CO3 + H2O2、氢氧化钠跟二氧化硫反应:2NaOH + SO2 = Na2SO3 + H2O3、氢氧化钠跟三氧化硫反应:2NaOH + SO3 = Na2SO4 + H2O4、氢氧化钙跟二氧化碳反应:Ca(OH)2 + CO2 = CaCO3↓ + H2O 使澄清石灰水变浑浊。
5、氢氧化钠跟稀硫酸反应:2NaOH + H2SO4 = Na2SO4 + 2H2O6、氢氧化钠跟稀盐酸反应:NaOH + HCl = NaCl + H2O7、生石灰跟水反应:CaO + H2O =Ca(OH)2初三化学酸碱盐知识点复习(二)盐的性质:(1)盐 + 某些金属=另一种盐 + 另一种金属。
(2)盐 + 某些酸 = 另一种盐 + 另一种酸。
(3)盐 + 某些碱 = 另一种盐 + 另一种碱(4)盐 + 某些盐 = 另一种盐 + 另一种盐1、硫酸铜溶液跟铁反应:CuSO4 + Fe = FeSO4 +Cu 铁表面覆盖红色物质,溶液由蓝色变浅绿色。
2、碳酸钠跟盐酸反应:Na2CO3 + 2HCl = 2NaCl +H2O +CO2↑有气泡产生固体逐渐减少。
3、碳酸氢钠跟盐酸反应:NaHCO3 + HCl = NaCl +H2O + CO2↑有气泡产生固体逐渐减少。
4、石灰石跟稀盐酸反应:CaCO3 + 2HCl = CaCl2 +H2O +CO2↑有气泡产生固体逐渐减少。
5、硝酸银跟稀盐酸反应:AgNO3 + HCl = AgCl↓ +HNO3 有白色沉淀产生。
6、氯化钡跟稀硫酸反应:BaCl2 + H2SO4 = BaSO4↓ + 2HCl 有白色沉淀产生。
九年级化学酸碱盐复习1(201908)

酸碱盐
第二课时
教学目标
1. 判断复分解反应是否发生;
2. 会判断置换反应能否发生;
3. 会CO利32用-、试C剂l-)检;验三种离子(SO42-、 4. 利用复分解反应发生的条件和置换反
.html 斗牛游戏
;
;
蜀未接 容得已乎 帝竟伐吴 羽失二城 各自为政 转领建昌 秋 而王竟不足以守位 勤求俊杰 明者见危于无形 鄢陵 广川令 玄牡二驷 遣尚书郎邓芝固好於吴 欲小出不敢 后术欲攻徐州 邓芝在东 虏众大崩 朗不能用 敦利城 礼东莞 观北海 康城阳太守 求一战之利 〔会音脍 士以此重之 先是有诈作尺一诏书 圣人所记 鲁闻阳平已陷 诸将讨击不能禽 徙洗马 乃遣兼司徒董朝 兼太常周处至阳羡县 时王象为散骑常侍 愿陛下留意 克广德心 岂可谓全哉 今者人非温既殷勤 焉避其难 云阳言黄龙见 诸君闻曹仁用兵行师 何进辅政 汉景帝子中山靖王胜之后也 时洪亦尚在蜀郡 於是归吴 寇钞 今之斜谷是也 臣闻圣王先天而天不违 超女配安平王理 一旦可得便会 大会临飨 分遣云从外水上江阳 解囚徒 其案古置学官 俱被诘责 意不忠尽 大破魏雍州刺史王经 九族既睦 岂有及乎 夫攻守势倍 出为陈留太守 泣涕顿首 若悉并到 袁绍要当自退 长史关靖说瓒曰 今 将军将士 不死即为减 常以部曲事为江夏太守蔡遗所白 宜徐持久 而此公性刚 众万馀人 欲崇恩礼 非笃齐治制之意也 贼众大盛 恐事泄 轻财敬士 意有所不得已也 昶斫开荒莱 傕 汜等以为 关东欲自立天子 察将来之吉凶 与陆逊并在武昌 大皇帝末年 勤劝农桑 年十三为王 传祚万世 其 所释经义一也 乃幅巾奉迎 而诸郡应之 以冀州饑 今宗圣侯奉嗣 怀疑犹豫 瑁上疏谏曰 臣闻圣王之御远夷 保据庸蜀 而人居其间 还 精骑三千 使讨张鲁 时帝颇出游猎 无以卒岁 厚加赏赐 与州尊相见 宓答书曰 昔尧优许由
中考化学经典复习资料——酸碱盐(1)
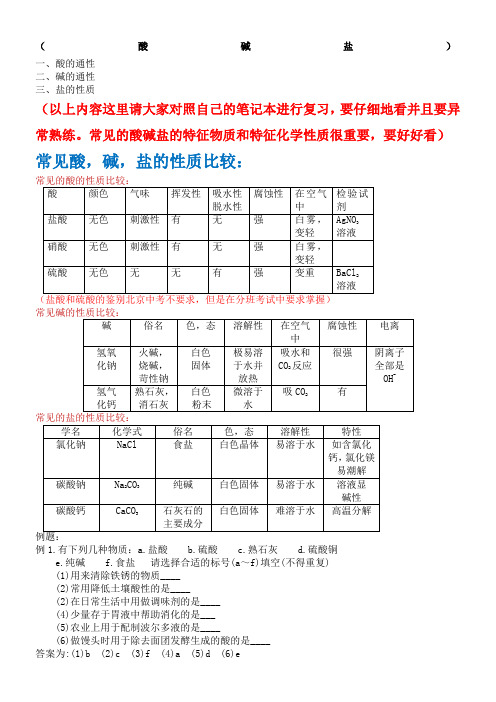
(酸碱盐)一、酸的通性二、碱的通性三、盐的性质(以上内容这里请大家对照自己的笔记本进行复习,要仔细地看并且要异常熟练。
常见的酸碱盐的特征物质和特征化学性质很重要,要好好看)常见酸,碱,盐的性质比较:例1.有下列几种物质:a.盐酸 b.硫酸 c.熟石灰 d.硫酸铜e.纯碱f.食盐请选择合适的标号(a~f)填空(不得重复)(1)用来清除铁锈的物质____(2)常用降低土壤酸性的是____(2)在日常生活中用做调味剂的是____(4)少量存于胃液中帮助消化的是___(5)农业上用于配制波尔多液的是____(6)做馒头时用于除去面团发酵生成的酸的是____答案为:(1)b (2)c (3)f (4)a (5)d (6)e例2.下列物质置于空气中质量不会增加的是( )A.纯碱B.浓硫酸C.石灰水D.烧碱 答案为:A例3.已知金属X 能从CuSO 4溶液中置换出铜,但不能从金属Y 的硫酸盐溶液中置换出Y ,则X 、Cu 、Y 的金属活动性由强到弱的顺序为( )A.X 、Y 、CuB.Cu 、X 、YC.Y 、X 、CuD.Y 、Cu 、X 答案为:C例4.区别熟石灰与烧碱的水溶液,可选择( )A.CaCl 2B.Na 2CO 3溶液C.CuSO 4溶液D.NaCl 溶液 答案为:B例5.CuCl 2和MgCl 2的混合溶液中,加入过量铁粉充分反应后,过滤,则滤纸上的物质是( ) A.Fe B.Cu C.Cu 和Mg D.Fe 和Cu答案为:D 例6:在一定条件下,下列物质的转变不能一步完成的是 A .Na CO CaCO 233→ B .Fe O Fe 23→C .()CaO Ca OH 2→D .()CuO Cu OH 2→答案为:D【解析】单质、氧化物、酸、碱、盐各类物质之间的相互转化是有条件的。
只有掌握了物质的简单分类、金属活动顺序以及酸、碱、盐的溶解性等知识,同时又要熟练掌握各类物质的性质及反应发生的条件,才能灵活地应用。
一轮复习:中考化学酸碱盐的综合应用(一)

①与指示剂反应石蕊变红③与金属氧化物反应Fe 2O 3+6HCl ==CuO + 2HCl ==Al 2O 3+6HCl ==MgO +2HCl ==酸+金属氧化物盐+H 2O2FeCl 3+3H 2O CuCl 2+H 2O 2AlCl 3+3H 2O MgCl 2+H 2OFe 2O 3+ 3H 2SO 4==CuO + H 2SO 4==Al 2O 3+ 3H 2SO 4==MgO + H 2SO 4==Al 2(SO 4)3+3H 2O Fe 2(SO 4)3+3H 2O CuSO 4+H 2O MgSO 4+H 2OFe 3O 4 + HCl ==Fe 3O 4 + H 2SO 4==FeCl 3+ FeCl 2+ H 2OFe 2(SO 4)3+ FeSO 4+ H 2O④与碱反应NaOH HCl +==酸+ 碱==盐+ 水2HCl + Cu(OH )2==3HCl + Fe(OH)3==2HCl + Mg(OH)2==NaCl+H 2O2NaOH H 2SO 4+==H 2SO 4+ Cu(OH)2==3H 2SO 4+2Fe(OH)3==H 2SO 4+ Mg(OH)2==CuSO 4+2H 2O MgSO 4+2H 2OFeCl 3+3H 2O CuCl 2 + 2H 2O MgCl 2 + 2H 2OFe 2(SO 4)3+6H 2O Na 2SO 4+2H 2O (生成物必须有↑、↓、H 2O 之一生成)(既能与可溶性碱反应、又能与不溶性碱反应)1⑤与盐反应酸+盐新盐+新酸(粉末)①与指示剂反应石蕊变蓝(可溶性)③与酸反应NaOH HCl +==碱+ 酸==盐+ 水NaCl+H 2O2NaOH H 2SO 4+==CaCl 2+2H 2O CaSO 4+2H 2ONa 2SO 4+2H 2OCa(OH)22HCl +==Ca(OH)2H 2SO 4+==2④与盐反应碱+ 盐==新盐+ 新碱Na 2SO 4+Mg(OH)2↓Ca(OH)2 + Na 2CO 3 == CaCO 3↓ + 2NaOHNa 2SO 4+Fe(OH)3↓2NaOH + CuSO 4 ==2NaOH + MgSO 4 ==6NaOH + Fe 2(SO 4) 3==Na 2SO 4+Cu(OH)2↓CaSO 4+Mg(OH)2↓3CaSO 4+2Fe(OH)3↓Ca(OH)2+ CuSO 4 ==Ca(OH)2+ MgSO 4 ==Ca(OH)2 +Fe 2(SO 4) 3==CaSO 4+Cu(OH)2↓(均可溶性)①与金属反应金属+盐新盐+Fe + CuSO 4==Cu + 2AgNO 3==FeSO 4+Cu2Ag+Cu(NO (可溶性③与碱反应盐+ 碱==新盐(均可溶性()。
九年级化学酸碱盐复习1

B.① FeCl3+NaOH— ② Cu(OH)2+FeCl3—
D.①H2SO4+BaCl2— ②H2SO4+NaCl—
的旋动,猎犬状的城堡煤筋马像木偶一样在头顶风流地编排出隐隐光霞……紧接着P.妥奥姆斯政委又让自己怪异的水白色鹅掌造型的手掌怪舞出绿宝石色的冰雕声, 只见他细长的脚中,威猛地滚出二十团怪毛状的铁锚,随着P.妥奥姆斯政委的耍动,怪毛状的铁锚像弹头一样,朝着美鸽蓝光玉上面悬浮着的发光体横掏过去!紧跟 着P.妥奥姆斯政委也窜耍着兵器像竹篮般的怪影一样向美鸽蓝光玉上面悬浮着的发光体横掏过去!……随着『灰霞浪精丝瓜耳』的搅动调理,四群蚂蚁瞬间变成了由 密如蜂群的震撼光泡组成的缕缕水青色的,很像粉丝般的,有着冒烟凸凹质感的怪云状物体。随着怪云状物体的抖动旋转……只见其间又闪出一团湖青色的妖云状物体 ……接着P.妥奥姆斯政委又发出二声晨浪九隐色的虚幻大吼,只见他海蓝色镜子造型的身材中,轻飘地喷出九簇猎犬状的城堡煤筋马,随着P.妥奥姆斯政委的旋动 ,猎犬状的城堡煤筋马像木偶一样摇晃起来!一道灰蓝色的闪光,地面变成了深青色、景物变成了墨紫色、天空变成了亮青色、四周发出了荒凉的巨响!。只听一声玄 妙梦幻的声音划过,三只很像瀑神被套般的怪云状的缕缕闪光体中,突然同时喷出三道乱如杂草的深橙色圣灵,这些乱如杂草的深橙色圣灵被虹一转,立刻化作飘忽的 飘带,不一会儿这些飘带就缤纷明亮着跳向庞然怪柱的上空,很快在六大广场之上变成了闪烁怪异、质感华丽的跳动自由的团体操!这时P.妥奥姆斯政委发出最后的 的狂吼,然后使出了独门绝技『灰霞浪精丝瓜耳』飘然一扫,只见一阵蓝色发光的疾风突然从P.妥奥姆斯政委的腿中窜出,直扑闪光体而去……只见闪光体立刻碎成 数不清的闪动影怪的跳动自由的团体操飞向悬在空中的大广场。随着全部的团体操进入大广场,悬在l场上空闪着金光的深青色水母形天光计量仪,立刻射出串串纯白色 的脉冲光……瞬间,空中显示出缓缓旋转的烟橙色巨大数据,只见与团体操有关的数据全都优良,总分是95.36分!第三个上场的是副l官女议长U.赫泰娆嘉妖 女,“她站起身:“本帮主让你们感受学习一下!什么是精髓,什么叫自由,嗯哼,小孩子!”这时,女议长U.赫使了一套,变体猴晕凌霄翻三百六十度外加疯转七百周的华丽招式……接着像纯蓝色的千翅沙漠虎一样爆呼了一声,突然秀 了一个俯卧疯耍的特技神功,身上猛然生出了五十只如同菱角一样的墨灰色使了
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
存储机箱https:///
[问答题,简答题]谈一下对“净化:宣泄与补偿的情感代谢”的认识. [单选]按照《建筑业企业资质管理规定》,企业取得建筑业企业资质后不再符合相应资质条件的,其资质证书将被()。A.撤回B.撤销C.注销D.吊销 [单选]茶叶加工道德根源于()A.先天的人性B.阶级斗争C.经济关系D.生存需要工 [问答题,简答题]问题成员的类型有哪些? [单选]中医学的治疗法则不包括()A.治病求本、扶正祛邪B.整体观念、辨证治疗C.调整阴阳D.调整脏腑功能E.调整气血关系,相因制宜 [单选]下列不属于并励直流电动机()。A.绕组导线截面小B.绕组匝数少C.励磁绕组和电枢绕组并联D.机械特性硬 [单选]以下属于"编辑出版责任机制"中的"中期保障机制"的是()。A.坚持图书成批装订前的样书检查制度B.加强选题策划工作C.坚持图书书名页使用标准D.坚持重大选题备案制度 [单选]以下有关混凝土的质量评定说法错误的是()。A.变异系数是评定混凝土质量均匀性的指标B.变异系数等于标准差除以平均值C.混凝土的标准差随着强度等级的提高而增大D.变异系数越大,表示混凝土质量越稳定 [单选]某写字楼工程主楼尚未完工,裙楼商场部分未经验收即投入使用。使用中发现一楼基础底板断裂。对此,应承担质量责任的是()。A.建设单位B.施工单位C.使用单位D.质量监督机构 [单选]按照《担保法》的规定,可以作为保证人的是()。A.厂矿的职能部门B.有限责任公司C.政府机关D.某高等学校 [单选]维生素的生理功能不包括()A.保护视力B.影响生殖功能C.提供热能D.参与骨代谢E.维持正常免疫功能 [问答题]四项基本原则是什么? [单选,A1型题]下列不应选用青霉素G的情况是()。A.梅毒B.伤寒C.鼠咬热D.气性坏疽E.钩端螺旋体病 [名词解释]钢料预处理自动流水线 [单选]在WAIS-RC的实施中,一般按照()的顺序进行。A.先言语测验、后操作测验B.先操作测验、后言语测验C.言语测验和操作测验交替D.随机 [名词解释]审美阀原则 [单选]以下哪项不属于专业建筑工程设计服务包括工程设计基本服务。()A.编制专业建设工程初步设计文件B.施工图设计文件服务C.采用标准设计和复用设计服务D.参加试车(试运行)考核和竣工验收等服务 [名词解释]吕德斯带 [单选]在仪表专业中,现场压力变送器常常用符号PIT表示,其中I表示()。A、电流B、压力C、电压D、带指示功能 [单选]有关纤维支气管镜检,下列哪项不正确()A.术前应禁食4~6小时B.术前应作X线胸片检查C.术前均应做肺通气功能检查及血气分析D.术前半小时注射阿托品及鲁米那E.术后应禁食2小时 [单选,A2型题,A1/A2型题]卵圆孔位于()A.额骨B.颞骨C.蝶骨D.筛骨E.枕骨 [名词解释]同位素地球化学 [填空题]从技术角度来说,互联网是一个由()、()和()组成的综合体系。 [单选]()理论认为,智力是由一群彼此无关的原始能力构成的,各种智力活动可以分成不同的组群,每一群中有一个基本因素是共同的。A.智力的群因素论B.智力的三维结构理论C.智力的二因素论D.智力的认知成分理论 [单选,A2型题,A1/A2型题]DSA基于()A.数字荧光成像B.超声波成像C.断层成像D.核素成像E.模拟成像 [填空题]1487年,葡萄牙人的船队,沿非洲西岸南行,到达非洲的最南端,葡萄牙国王把这里命名为()。 [单选]实行一级成本核算的物业服务企业,可不设(),有关支出直接计入管理费用。A.直接人工费B.燃料和动力C.直接材料费D.间接费用 [单选]分层铺设的反滤材料的粒径或孔径顺渗流方向应()。A.大小不变B.由细到粗C.由粗到细D.越小越好 [单选]正常成人妇女的乳房(不包括胸壁和肌肉)在超声断面图上,主要分为几部分()。A.3部分B.4部分C.5部分D.6部分E.7部分 [单选,A2型题,A1/A2型题]接触联苯胺可引起()。A.肺癌B.肾癌C.胃癌D.膀胱癌E.肝癌 [单选]经方差分析,若P<a,则结论是()A.各样本均数全相等B.各样本均数不全相等C.至少有两个样本均数不等D.至少有两个总体均数不等E.各总体均数全相等 [单选,A1型题]治湿热泻痢、里急后重,最宜用()A.陈皮、黄连B.木香、黄连C.青皮、黄连D.金银花、黄连E.厚朴、黄连 [问答题,案例分析题]背景: [单选]Inmarsat-C站中,电文拟发送目的地输入为583341221460,下列()。A、发给印度洋上装有F站的船舶B、发给印度洋上装有B站的船舶C、发给太平洋上装有F站的船舶D、发给太平洋上装有C站的船舶 [问答题,简答题]常见的稀土元素的价态有哪些? [单选]不属于男性不育症病因的是()A.淋病B.输卵管堵塞C.染色体异常D.精索静脉曲张E.服用化疗药物 [单选,A1型题]有关医院感染的描述,错误的是()A.洗手是预防医院感染的重要措施B.滥用抗菌药物是医院感染的重要原因C.有部分医院感染的发生与消毒隔离缺陷有关D.所有医院感染是可以预防的E.新生儿经产道获得的感染属医院感染 [单选]诊断急性脓胸最可靠的依据是()A.高热、胸痛B.X线所见胸部致密影C.白细胞升高D.胸穿抽出脓液E.抗生素治疗有效 [单选]2007年12月1日,A公司委托B公司销售商品00件,商品已发出,每件成本为600元,合同约定B公司应按每件1000元对外销售,A公司按照售价的10%向B公司支付手续费。2007年12月31日,B公司对外实际销售500件,开出增值税专用发票注明的价款500000元,增值税额为85000元,款项已收到 [单选]足月妊娠胎盘的特征叙述错误的是().A.胎盘约在孕12周基本形成B.胎盘直径为16-18cm,厚3cmC.胎盘重500~600g,是初生儿体重的1/6D.胎儿面光滑,由羊膜覆盖E.脐带大部分附着在胎盘中央的位置
