广西南宁市2016_2017学年高一化学下学期期中试题理
2017-2018学年广西南宁市第八中学高一下学期期中(4月)地理试题(文)
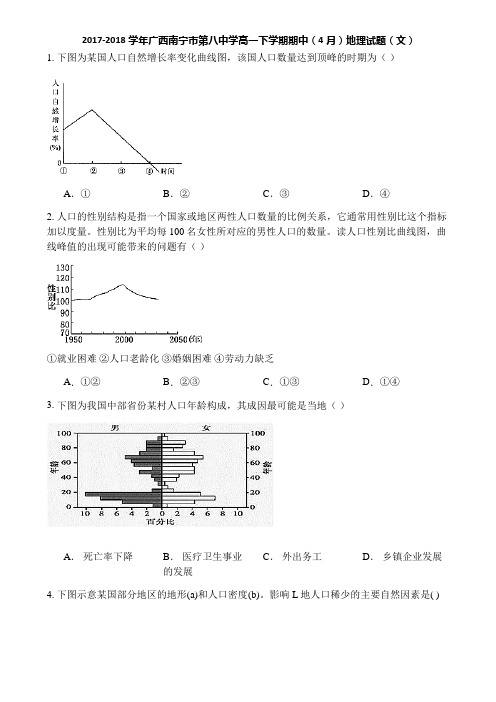
2017-2018学年广西南宁市第八中学高一下学期期中(4月)地理试题(文)1. 下图为某国人口自然增长率变化曲线图,该国人口数量达到顶峰的时期为()A.①B.②C.③D.④2. 人口的性别结构是指一个国家或地区两性人口数量的比例关系,它通常用性别比这个指标加以度量。
性别比为平均每100名女性所对应的男性人口的数量。
读人口性别比曲线图,曲线峰值的出现可能带来的问题有()①就业困难②人口老龄化③婚姻困难④劳动力缺乏A.①②B.②③C.①③D.①④3. 下图为我国中部省份某村人口年龄构成,其成因最可能是当地()A.死亡率下降B.医疗卫生事业C.外出务工D.乡镇企业发展的发展4. 下图示意某国部分地区的地形(a)和人口密度(b)。
影响L地人口稀少的主要自然因素是( )A.地形B.纬度位置C.洋流D.距海远近5. 人类密集地区称人类大陆。
在下面人类大陆图上,世界人口的分布()A.高纬度比低纬度多B.欧洲比亚洲多C.西半球比东半球多D.平原比山区多6. 下图为某四个地区人口“三率”统计图,关于四个地区人口问题或相应解决措施,描述正确的是A.甲地人口增长过快B.乙地应鼓励生育C.丙地经济发展水平低D.丁地人口平均寿命长7. 2010年底至2011年初,埃及、利比亚等国家的大量人口纷纷撤离该国家回国;其中我国开展海陆空全方位撤侨工作,于3月6日3.2万余人全部安全回国。
其原因是( )。
A.该国发生大范围的“流感”灾害B.石油资源大量开采,出现枯竭现象C.此时期发生了大范围的沙尘暴灾害D.政局动荡,使生活环境遭到破坏8. 每年8月底到11月初,河南周口都有大量的务工人员前往新疆打工,采摘棉花。
新疆每年对季节工的需求在50万人左右。
据此完成问题。
影响材料中人口流动的主导因素是( )A.经济因素B.自然环境因素C.文化教育因素D.政治因素9. 人口迁移率指人口迁移数占总人口数的比例,正值为迁入。
读图回答下列问题。
图中甲、乙、丙、丁各代表一个国家,依次是()A.苏丹、沙特阿拉伯、波兰、德国B.巴西、印度、德国、美国C.印度、中国、日本、德国D.尼日利亚、印度、德国、英国10. 水资源和耕地资源是影响一个地区人口容量的重要因素.根据下表数据,若不考虑其他条件,人口容量最小的省份可能是()A.吉林B.辽宁C.山西D.陕西11. 环境人口容量是指一个地区或一个国家能持续供养的人口数量.1850年,清朝的人口为4.3亿.当时的学者汪士铎惊呼:“人多之害,山顶已植黍稷,江中已有洲田,川中已辟老林,苗洞已开深菁,犹不足养…”而今天的中国,不但养活了13亿人,人们的生活水平比那个时代还提高了许多。
广西南宁市2023-2024学年高一下学期期末调研考试英语试题(含答案,含听力原文,无音频)

南宁市2023-2024学年高一下学期期末调研考试英语试卷试卷共8页,67小题,满分150分。
考试用时120分钟。
注意事项:1.考查范围:必修第一册至必修第三册。
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
4.考生必须保持答题卡的整洁。
考试结束后,请将答题卡交回。
第一部分听力(共两节,满分30分)做题时,先将答案标在试卷上,录音内容结束后,你将有两分钟的时间将试卷上的答案转涂到答题卡上。
第一节(共5小题;每小题1.5分,满分7.5分)听下面5段对话。
每段对话后有一个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。
听完每段对话后,你都有10秒钟的时间来回答有关小题和阅读下一小题。
每段对话仅读一遍。
例:How much is the shirt?A. £ 19.15.B. £ 9.18.C. £ 9.15.答案是C。
1. What is the weather like now?A. Cold.B. Hot.C. Warm.2. What is Steven doing?A. Gathering firewood.B. Having dinner.C. Preparing meat.3. Who does the man want to call?A. Tom.B. His secretary.C. The woman.4. How will the speakers go to the cinema?A. On foot.B. By car.C. By bus.5. What is the conversation mainly about?A. An expression.B. The Internet.C. A competition.第二节(共15小题;每小题1.5分,满分22.5分)听下面5段对话或独白,每段对话或独白后有几个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。
2022-2023学年广西南宁市高一下学期开学联考化学试卷含详解

高一年级化学试卷可能用到的相对原子质量:H 1C 12O 16Na 23S 32Cl 35.5Fe 56Cu 64Ba 137一、选择题:本题共15小题,每小题3分,共45分。
每小题只有一个选项符合题目要求。
1.下列过程不属于...化学变化的是A.图1家用天然气燃烧B.图2碳酸氢钠片可用于治疗胃酸过多C.图3海边停靠的邮轮侧面钢板出现锈迹D.图4利用焰色试验原理产生五彩缤纷的节日烟花2.下列分散系能产生丁达尔效应的是A.()3Fe OH 胶体B.液氯C.漂白粉D.盐酸3.下列单质与水的反应中,水作还原剂的是A.22Cl H O HCl HClO +=+ B.222Na 2H O 2NaOH H +=+↑C.2222F 2H O 4HF O +=+ D.23423Fe 4H OFe O 4H ++高温4.下列离子方程式中,书写正确的是A.将铁片放入足量的稀硫酸溶液中:322Fe 6H 2Fe3H +++=+↑B.将氯气通入石灰乳中:22Cl 2OH Cl ClO H O---+=++C.将4NaHSO 溶液滴入()2Ba OH 溶液中至溶液呈中性:2H OH H O+-+=D.将23Ag CO 固体投入稀硝酸中:2322Ag CO 2H 2Ag CO H O+++=+↑+5.用下列装置进行相应实验,装置正确且能达到相应实验目的的是A.用甲装置可配制一定物质的量浓度的硫酸溶液B.用乙装置进行铁与水蒸气的反应,点燃肥皂泡,可检验产物C.用丙装置可证明非金属性强弱:Cl C Si>>D.用丁装置先通入2CO ,后通入3NH ,可模拟“侯氏制碱法”制取3NaHCO 6.设A N 为阿伏加德罗常数的值,下列叙述正确的是A.0.1mol/L NaCl 溶液中含有的Na +数目为A 0.1N B.1821mol D O 中含有的中子数为A10N C.5.6g 铁在0.1mol 氯气中充分燃烧,转移电子数为A 0.3N D.标准状况下,44.8L 氦气中含有的原子总数为A 2N 7.下列各组转化关系,不能..由一步反应实现的是A.233Al O Al(OH)→ B.23Fe(OH)Fe(OH)→C.2Cl NaClO→ D.2223Na O Na CO →8.下列各组中的离子,能在溶液中大量共存的是A .酸性溶液:2Ca +、Cl -、23SO -、3NO -B.透明溶液:2Fe +、2Zn +、24SO -、2Cu +C.强碱性溶液:K +、2Ba +、3HCO -、Br -D.与铝反应可产生氢气的溶液:2Mg +、I -、3Fe +、24SO -9.X 、Y 、Z 、W 为原子序数依次增大的短周期主族元素。
2022-2023学年广西壮族自治区南宁市部分学校高二下学期期中地理试题(解析版)

广西壮族自治区南宁市部分学校2022-2023学年高二下学期期中地理试题学校:___________姓名:___________班级:___________考号:___________一、选择题组菊花是一种短日照花卉,其开花期对日照时长非常敏感,某品种菊花当日照时长低于10小时30分才进入开花期。
下表为成都市不同日期的日出、日落时间(北京时间),1.在自然状态下,该品种菊花在成都市进入开花期的时间可能是()A.2月B.5月C.8月D.11月2.若不考虑天气影响,以日照时间低于10小时30分期间为菊花花期,则花期结束后的一周内,成都()A.日出东北B.白昼渐长C.室内正午阳光面积增大D.正午日影渐长【答案】1.D 2.B【解析】1.利用表中日落时间减去日出时间计算出四个日期的昼长分别是11时33分、13时59分、12时46分、10时18分。
根据“某品种菊花只有当日照时长开始小于10小时30分钟时才进入开花期”,前三个日期的昼长都远长于10小时30分钟,而12月1日的昼长为10时18分,早已满足了菊花开花的日照需求。
由此可知,该品种菊花在成都市进入开花期的时间可能是12月1日之前的11月,D正确,ABC错误。
故选D。
2.如果以日照时间低于10小时30分期间为菊花花期,而12月1日的昼长为10时18分,与之关于冬至对称的日期为1月13日附近,也就是说花期结束时间在1月13日后,则花期结束一周内,期间直射点在南半球,向北移,则成都日出于东南,白昼渐长,A 错误、B正确;直射点在南半球,向北移,成都的正午太阳高度角增大,室内正午阳光面积减小,正午日影渐短,CD错误。
故选B。
【点睛】太阳直射赤道上,全球日出正东,日落正西;太阳直射北半球,除极圈外全球日出东北,日落西北;太阳直射南半球,除极圈全球日出东南,日落西南。
卡帕多西亚位于土耳其安纳托利亚高原中部高海拔沙漠的腹地,数亿年前这里的火山喷发,喷吐而出的火山碎屑物和熔岩堆积起来形成了凝灰岩(一种压实固结的火山碎屑岩)和熔岩层,经过长时间的变化,岩石千姿百态,其中头戴玄武岩“帽子”的圆锥形尖塔,被当地人称为“精灵烟囱”。
3.1 最简单的有机化合物--甲烷-2016-2017学年高一化学暑假作业含解析

知识梳理1。
甲烷的性质:①氧化反应(燃烧)CH4+2O2――→CO2+2H2O(淡蓝色火焰,无黑烟)②取代反应(注意光是反应发生的主要原因,产物有5种)CH4+Cl2―→CH3Cl+HCl CH3Cl +Cl2―→CH2Cl2+HClCH2Cl2+Cl2―→CHCl3+HClCHCl3+Cl2―→CCl4+HCl在光照条件下甲烷还可以跟溴蒸气发生取代反应,甲烷不能使酸性KMnO4溶液、溴水或溴的四氯化碳溶液褪色。
2. 烷烃的命名:(1)普通命名法:把烷烃泛称为“某烷”,某是指烷烃中碳原子的数目.1-10用甲,乙,丙,丁,戊,已,庚,辛,壬,癸;11起汉文数字表示。
区别同分异构体,用“正",“异”,“新”。
如:正丁烷,异丁烷;正戊烷,异戊烷,新戊烷。
(2)系统命名法:①命名步骤:a找主链-最长的碳链(确定母体名称);b编号-靠近支链(小、多)的一端;c写名称-先简后繁,相同基请合并.②名称组成:取代基位置-取代基名称母体名称③阿拉伯数字表示取代基位置,汉字数字表示相同取代基的个数CH3-CH-CH2-CH3CH3-CH-CH -CH32-甲基丁烷2,3-二甲基丁烷3。
同系物、同分异构体、同素异形体、同位素比较。
4. 烃的定义:仅含碳和氢两种元素的有机物称为碳氢化合物,也称为烃。
5。
烃的分类:饱和烃→烷烃(如:甲烷)脂肪烃(链状)烃不饱和烃→烯烃(如:乙烯)芳香烃(含有苯环)(如:苯)6。
比较同类烃的沸点:①一看:碳原子数多沸点高。
②碳原子数相同,二看:支链多沸点低。
常温下,碳原子数1-4的烃都为气体.跟踪练习1.烃是( )A。
含有C、H元素的有机物B。
含有C元素的化合物C. 仅由C、H两种元素组成的有机物D. 完全燃烧只生成CO2和H2O的化合物【答案】C2.以下关于甲烷的说法中,错误的是()A. 甲烷是最简单的有机化合物B. 甲烷分子具有正四面体结构C。
甲烷分子中的4个C-H键完全相同 D. 甲烷分子中具有非极性键【答案】D【解析】A、甲烷是最简单的有机化合物,故A正确;B、甲烷的空间构型是正四面体,故B正确;C、甲烷分子中4个碳氢键完全相同,故C正确;D、甲烷分子中只有碳原子和氢原子形成的极性共价键,故D错误;故选D。
2023-2024学年广西南宁市第三十三中学高一下学期5月月考化学试题

2023-2024学年广西南宁市第三十三中学高一下学期5月月考化学试题1.化学与环境、科技、生活、社会发展息息相关。
下列说法错误的是A.棉花、羊毛、天然橡胶都属于天然有机高分子材料B.聚乙烯(PE)可制成薄膜,用于食品、药物的包装材料C.纽扣银锌电池体形小,含有害物质少,用后不用分类回收D.“北斗三号”导航卫星使用的透光电极材料——石墨烯,属于新型无机非金属材料2.下列反应中属于取代反应的是A.nCH 2 =CHCH 3B.C.D.23.下列关于四种装置的叙述不正确的是A.电池I:铜表面产生气泡B.电池II:是充电电池,属于二次电池C.电池III:燃料电池有清洁、安全、高效的特点D.电池IV:锌筒作负极,被还原4.科学家研制的一种使沙漠变绿洲的新技术,是在沙漠中喷洒一定量的聚丙烯酸某酯()与水的混合物,使其与沙粒结合,起到既能阻止地下盐水上升,又能蓄积雨水的作用。
下列关于聚丙烯酸酯的叙述中,不正确的是A.合成聚丙烯酸酯的小分子有机物的结构简式为CH 2 =CHCOORB.聚丙烯酸酯没有固定的熔、沸点C.聚丙烯酸酯能使溴的CCl 4溶液和酸性KMnO 4溶液褪色D.由丙烯酸甲酯合成聚丙烯酸甲酯反应的原子利用率为100%5.下列关于有机物的叙述正确的是A.C 4 H 10有三种同分异构体B.甲烷和氯气物质的量比为1:1混合,发生取代反应只生成一氯甲烷C.乙烯能使酸性KMnO 4溶液和溴水褪色,二者反应原理相同D.苯乙烯( )分子内所有原子均可能在同一平面6.下列说法正确的是A.的一氯代物有3种B.PVC(聚氯乙烯)包装袋可用于食品包装C.沸点:己烷>异戊烷>新戊烷>丙烷D.烷烃常温下都为气态,都不溶于水7.以氨气为原料的燃料电池结构如图所示,下列说法正确的是A.负极的电极反应式为:B.外电路的电流方向为从a极流向b极C.当生成1 mol N 2时,电路中通过的电子的物质的量为3 molD.a极为电池的正极8.由乙烯推测丙烯()的结构或性质,以下关于丙烯的说法错误的是A.丙烯能使酸性高锰酸钾溶液褪色B.丙烯能在空气中燃烧,火焰明亮并伴有黑烟C.丙烯分子中所有的碳原子共平面D.丙烯与溴发生加成反应的产物是9.下列措施中,不能加快化学反应速率的是A.将食物储存在冰箱里B.往 H 2 O 2溶液中加入几滴 FeCl 3溶液C.用粉末状碳酸钙代替块状碳酸钙与稀盐酸反应D.用稀 H 2 SO 4与锌粒反应时加入几滴 CuSO 4溶液10.设N A为阿伏伽德罗常数的值,下列说法正确的是A.标准状况下,11.2LCHCl 3中含氯原子数目为1.5 N AB.16g甲烷分子中含有的极性共价键数目为4 N AC.足量铜与250mL16mol/L的浓硫酸加热充分反应,转移4 N A个电子D.一定条件下1molN 2和3molH 2反应后,体系中的分子数等于2 N A11.恒容密闭容器中,反应X(s)+2Y(g) 3Z(g)在一定条件下进行,下列不能说明反应达到平衡状态的是A.气体的密度不再变化B.Y与Z的物质的量之比为2:3C.气体的压强不再变化D.Y的消耗速率与Z的消耗速率之比为2:312.用下列实验装置进行相应实验,有关说法正确的是B.装置②可用于组装原电池A.装置①可用于测定锌与稀硫酸反应速率D.装置④可用于验证二氧化硫的漂白性C.装置③可用于观察甲烷取代反应的现象13.某实验小组用0.1KMnO4溶液和0.1H2C2O4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
2022-2023学年广西壮族自治区南宁市武鸣县师范中学高一化学下学期摸底试题含解析

2022-2023学年广西壮族自治区南宁市武鸣县师范中学高一化学下学期摸底试题含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 能使品红溶液褪色的气体是A. NH3B. HClC. CH4D. Cl2参考答案:D具有漂白性的物质能将品红漂白而褪色,比如SO2、Cl2,而NH3、HCl、CH4均没有漂白性,不能使品红褪色,故选D。
2. 下列说法中错误的是()A.化学反应中的能量变化通常表现为热量的变化B.需要加热才能发生的反应一定是吸热反应C.化学键的断裂和形成是化学反应中能量变化的主要原因D.反应物总能量和生成物总能量的相对大小决定了反应是放热还是吸热参考答案:B略3. 下列有关气体体积的叙述中,正确的是A.一定温度和压强下,各种气体物质体积的大小,由构成气体的分子大小决定B.一定温度和压强下,各种气体物质体积的大小,由构成气体的分子数决定C.不同的气体,若体积不同,则它们所含的分子数也不同D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L参考答案:B略4. 物质的鉴别有很多种方法,下列能达到鉴别目的的是①用水鉴别苯、乙醇、溴苯;②用饱和的Na2CO3溶液鉴别乙酸、乙酸乙酯和CCl4;③用酸性高锰酸钾鉴别正戊烷、己烯和乙醇;④用点燃的方法鉴别甲烷、乙烯和乙炔(C2H2)A.①② B.①②④ C.①③④ D.①②③④参考答案:B略5. 能源问题是当今世界发展的一个主要问题。
下列能源符合“绿色化学”的概念的是A.氢气B.煤C.沼气D.石油参考答案:A6. 下列实验仪器不宜直接用来加热的是()A.试管B.坩埚C.蒸发皿D.烧杯参考答案:D略7. 燃烧法是有机化学发展初期测定简单有机物组成的常用方法。
验证某有机物是否为含氧元素,应完成的实验内容是A.只有验证它完全燃烧后产物只有H2O和CO2B.只有测定其燃烧产物中H2O和CO2物质的量的比值C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比D.测定该试样完全燃烧后生成CO2和H2O以及消耗O2三者的物质的量之比参考答案:D略8. 某有机物的结构简式如右图,该物质应有的化学性质是①可燃烧;②可跟溴加成;③可使酸性KMnO4溶液褪色;④可跟NaHCO3溶液反应⑤可跟Cu(OH)2悬浊液反应;⑥可跟金属钠反应A.①②③⑥ B.②③④⑥ C.②③④⑤⑥ D.①②③④⑤⑥参考答案:D略9. 下列各组中物质间的反应,不能用同一离子方程式来表示的是A. 盐酸与碳酸钠溶液;稀硫酸与碳酸钾溶液B. 硫酸铜溶液与氢氧化钠溶液;硫酸铜与氢氧化钡溶液C. 铁与盐酸;铁与稀硫酸D. 氢氧化钾溶液与稀硫酸;氢氧化钾溶液与稀硝酸参考答案:B【详解】A.盐酸与碳酸钠溶液、稀硫酸与碳酸钾溶液反应的离子方程式均为:2H++CO32-=H2O+CO2↑,故不选A;B.硫酸铜溶液与氢氧化钠溶液反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓;硫酸铜与氢氧化钡溶液反应的离子方程式为:Cu2++SO42-+Ba2+2OH-=BaSO4↓+ Cu(OH)2↓;故选B;C.铁与盐酸、铁与稀硫酸反应的离子方程式均为:Fe+2H+=Fe2++H2↑,故不选C;D.氢氧化钾溶液与稀硫酸、氢氧化钾溶液与稀硝酸反应的离子方程式均为:OH-+H+=H2O,故不选D;本题答案为B。
广西南宁市2023-2024学年高二下学期期末考试 化学含答案

2023—2024学年南宁市高二年级下学期期末考调研测试高二化学试卷(答案在最后)试卷共6页,18小题,满分100分.考试用时75分钟.注意事项:1.考查范围:高考全部范围.2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上.3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷上无效.4.考生必须保持答题卡的整洁.考试结束后,请将答题卡交回.可能用到的相对原子质量:H 1O 16Na 23———一、选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项是最符合题目要求的.1.“挖掘文物价值,讲好广西故事”.下列广西文物中其主要成分不同于其他三种的是()选项ABCD文物名称西汉大铜马西汉弦纹玻璃杯西汉人面纹羊角钮铜钟商代兽面纹提梁铜卣A .AB .BC .CD .D2.硝酸铵爆炸时发生反应:43222480~5002NH NO 2N O 4H O ↑+↑+↑℃℃.下列叙述错误的是()A .基态N 原子价层由子排布图为B .水的电子式为H:O:HC .43NH NO 中阴离子空间结构为D .2N 的结构式为N N≡3.物质性质决定物质用途.下列对物质用途的解释合理的是()选项用途解释A 节日燃放焰火烟花中的金属元素发生电子跃迁B 乙酸乙酯溶解油漆乙酸乙酯和油漆都能燃烧生成2CO 和2H OC 工业用液氨作制冷剂断裂3NH 中极性键吸收热量D 红酒中2SO 作保鲜剂2SO 是极性分子A .AB .BC .CD .D4.利用废铜屑和稀硝酸制备硝酸铜晶体()322Cu NO 3H O ⎡⎤⋅⎣⎦,下列操作中所用到的仪器错误的是()硝酸与铜屑反应滤去残渣制热饱和溶液分离硝酸铜晶体A .具支试管B .烧杯C .蒸发皿D .分液漏斗A .AB .BC .CD .D5.短周期主族元素R 、X 、Y 、Z 的原子序数依次增大,气体中R 单质的密度最小,基态X 原子价层电子排布式为nnns np ,Y 的简单氢化物可与其最高价氧化物对应的水化物反应,基态Z 原子最外层电子数等于K 层电子数.下列叙述正确的是()A .原子半径:Z>Y>X>RB .最高价氧化物对应水化物的酸性:X>YC .电负性:Y>X>RD .由R 、X 、Y 组成的化合物一定只含共价键6.L DOPA -是具有口服活性的神经递质多巴胺的代谢前体,其结构简式如图所示.下列有关该化合物的叙述正确的是()A .所有原子可能共平面B .能与3FeCl 溶液发生显色反应C .1mol 该化合物最多能与24molH 加成D .1个该化合物分子含2个手性碳原子7.臭氧层是人类的保护伞.实验室检验3O 的原理是3222O 2KI H O 2KOH I O ++++.设A N 为阿伏加德罗常数的值.下列叙述错误的是()A .标准状况下,211.2LI 含原子数为A NB .316gO 和2O 的混合物含质子数为A 8NC .31molO 完全反应时转移电子数为A2N D .21molH O 含σ键数为A2N 8.古时可用4FeSO 制备硫酸,同时产生的硫酸可进一步制备硝酸,部分物质的转化如图所示:下列叙述正确的是()A .M 一定是红色粉末固体B .上述过程仅涉及1个氧化还原反应C .制备硝酸过程中浓硫酸表现出强氧化性D .采用“微热”避免硝酸分解9.下列实验方案能达到相应实验目的的是()选项实验目的实验方案A用NaOH 固体配制1100mL1.00mol L -⋅的NaOH 溶液称取4.0gNaOH 固体放入100mL 容量瓶中,加入蒸馏水溶解B证明氧化性:22Br I>向KI 溶液中加入少量溴水,振荡,再加入4CCl 充分振荡后,观察下层溶液颜色C测定新制氯水的pH 用干燥洁净的玻璃棒蘸取新制氯水,点在pH 试纸上,与标准比色卡对照D 除去2Cl 中的HCl 将混合气体通过NaOH 溶液A .AB .BC .CD .D10.香港理工大学应用物理系的黄海涛教授基于对钙钛矿结构的重新解读,提出钙钛矿晶格可作为构筑孤立活性位点的平台用于氧还原()ORR 选择性合成双氧水()22H O .下列叙述错误的是()A .质子()H +由a 极区向b 极区迁移B .a 极为阳极,发生氧化反应C .b 极反应式为222O 2e 2H H O -+++D .相同时间内,a 极生成的()2n O 等于b 极消耗的()2n O 11.下列离子方程式或化学方程式符合叙述的是()A .以铁为电极,电解饱和食盐水的总反应:2222H O 2Cl Cl 2OH H --+↑++↑通电B .乙酰胺在稀硫酸中共热:32233CH CONH H OCH COOH NH ∆++↑C .向废液中通入2H S 以除去222Cu :Cu H SCuS 2H ++++↓+D .乳酸合成聚乳酸可降解塑料:3||CH nH C OH HO[−−−→催化剂—3|CH O ||HC C O ]——n 2H nH O COOH+12.2SrF 可用作防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为anm ,下列说法正确的是()A .基态F -的核外电子排布式为2251s 2s 2pB .图中白色的球代表2Sr +C .每个2Sr+周围紧邻且等距离的2Sr+个数为12D .F -与2Sr+间的最近距离为anm 213.杭州亚运会2CO 合成甲醇做火炬燃料实现了零碳排放,反应2232CO (g)3H (g)CH OH(g)H O(g)++ 是合成甲醇的方式之一.向恒容密闭容器中充入22CO H 、和催化剂PST,500℃时反应历程如下(TS 表示过渡态,加*表示吸附在催化剂表面).下列说法错误的是()A .该合成甲醇的反应在低温下可自发进行B .反应历程中存在极性键、非极性键的断裂和极性键的形成C .生成3TS 的步骤为该反应的决速步骤D .通过选择更高效的催化剂可改变该反应的焓变14.常温下,向120mL0.1mol L -⋅氨水中滴加1VmL0.1mol L -⋅醋酸(HAc)溶液,溶液中()()()432c NH c Ac pX pX lg X,X ,c NH H O c(HAc)+-⎡⎤⎢⎥=-=⋅⎢⎥⎣⎦与pH关系如图所示.下列叙述错误的是()A .1L 直线代表()()2c Ac lgc HAc --与pH 的关系B .Q 点对应溶液中:()()()()4c NH c Acc H c OH +-+-===C .V 10mL =时溶液中:()()()()4c NH c Acc OH c H +--+>>>D .() 4.75b 32K NH H O 10-⋅=二、非选择题:本题共4小题,共58分.15.(14分)钴酸锂()2LiCoO 是锂离子电池的电极材料.以水钴矿(主要成分为23Co O ,含少量232Fe O MgO CaO SiO 、、、等杂质)为原料制备2LiCoO 的工艺流程如图所示.已知部分信息:①[]24Co(SCN)-在水中不稳定,易溶于有机溶剂;②常温下,()()119sp 2sp 2K MgF 4.010,K CaF 4.010--≈⨯≈⨯.回答下列问题:(1)钴位于元素周期表_____________区;23Li CO 中阴离子空间结构为________________.(2)滤渣的主要成分是_____________(填化学式);“酸浸”中不能用盐酸替代硫酸,可能的原因是______________________.(3)“除钙镁”中同时存在2CaF 和2MgF 时,滤液中()()22c Ca c Mg++=_____________.(4)在水中,稳定性:3Fe(SCN)_____________[]36FeF -(填“>”或“<”);“有机相”可循环用于_____________工序.(5)“煅烧”发生反应的化学方程式为____________________________.16.(15分)甲醇是重要的化工原料.工业上利用合成气(主要成分为2CO CO 、和2H )在催化剂的作用下合成甲醇.发生的主要反应如下:Ⅰ.2221CO (g)H (g)CO(g)H O(g)H ++∆ Ⅱ.232CO(g)2H (g)CH OH(g)H +∆ Ⅲ.22323CO (g)3H (g)CH OH(g)H O(g)H ++∆ (1)上述反应Ⅲ的3ΔH =_____________(用含1ΔH 和2ΔH 的式子表示).(2)在一恒容密闭容器加入一定量的2CO (g)和2H (g),只发生反应Ⅰ,测得其化学平衡常数的对数ln K 和温度的倒数()121T >T T的关系如图所示:①1ΔH _____________0(填“>”“<”或“=”),其理由是_____________.②能判断该反应达到化学平衡状态的依据是_____________(填字母).A .单位时间内消耗2CO 的物质的量和消耗CO 的物质的量相等B .容器内气体密度保持不变C .容器内2CO 的体积分数保持不变③反应在1t 时刻达到平衡后,在2t 时刻改变条件A 使化学反应速率发生变化的图像如图甲所示,改变条件B 使物质浓度发生变化的情况如图乙所示.图甲中2t 时刻改变的条件A 可能是_____________(写1条即可,下同),图乙中2t 时刻改变的条件B 可能是_____________.甲乙(3)T ℃时,保持压强恒定为25MPa,CO 和2H 的起始投料分别为1mol 和3mol ,只发生反应Ⅰ和反应Ⅲ,测得平衡时2CO 的转化率为20%,3CH OH 的选择性为70%[已知3CH OH 的选择性()()32n CH OH =100%n CO ⨯消耗],求:①平衡时()3n CH OH =_____________mol .②反应Ⅰ的p K =_____________(保留一位有效数字即可,p K 是用分压表示的平衡常数,分压=总压×物质的量分数)17.(15分)氨基磺酸()23H NSO H,Mr 97=是一种无味无毒的一元固体强酸,微溶于乙醇,260℃时分解,溶于水时存在反应:22344H O H NSO HNH HSO +.可用于制备金属清洗剂等,实验室用羟胺()2NH OH和2SO 反应制备氨基磺酸.已知:2NH OH 性质不稳定,加热时爆炸.室温下同时吸收水蒸气和2CO 时迅速分解.实验室常用亚硫酸钠粉末与75%硫酸制备2SO .根据下列装置回答相关问题:A B C D(1)仪器X 的名称是_____________.(2)气流从左至右,装置连接顺序是A→_____________→_____________→_____________→_____________(装置可以重复使用).(3)实验过程中,先旋开装置_____________(填“A ”或“C ”)的分液漏斗活塞,后旋开另一个活塞,其目的是_______________________________.(4)装置D 可以用下列装置_____________(填字母)替代.a .盛装饱和食盐水的洗气瓶b .盛装品红溶液的洗气瓶c .盛装碱石灰的U 型管d .盛装五氧化二磷的U 型管(5)下列叙述正确的是_____________(填字母).a .装置C 可采用热水浴加快反应速率b .本实验应在通风橱中进行c .实验完毕后,采用分液操作分离装置C 中混合物(6)产品纯度测定.取wg 氨基磺酸溶于蒸馏水配制成100mL 溶液,准确量取25.00mL 配制溶液于雏形瓶,滴加几滴甲基橙溶液,用1cmol L -⋅标准NaOH 溶液滴定至终点,消耗滴定液体积为VmL .产品纯度为_____________________%(用含w 、c 、V 代数式表示),若选用酚酞溶液作指示剂,测得结果可能会_____________(填“偏高”“偏低”或“无影响”).18.(14分)化合物Q 是合成一种解热、镇咳药物的中间体.一种合成Q 的路线如下:回答下列问题:(1)A 的化学名称为_____________,Q 中含氧官能团的名称为_____________.→的反应类型为_____________________,G中碳原子的杂化类型为_____________.(2)G H→的化学方程式为_______________________________.(3)H+F Q(4)在E的芳香族同分异构体中,同时满足下列条件的有_____________种,其中核磁共振氢谱上有4组峰的结构简式为_____________(不考虑立体异构,写一种即可).2molNaHCO反应.①苯环上有3个取代基;②1mol该有机物最多能与3(5)以苯、乙醛和乙炔为原料合成,设计合成路线如下:其中,X的结构简式为____________________________.2023—2024学年南宁市高二年级下学期期末考调研测试高二化学参考答案1.【答案】B【解析】铜马、铜钟、铜卣的主要成分均是铜合金,而玻璃杯的主要成分是硅酸盐,B 项符合题意.2.【答案】C【解析】基态N 原子2p 能级上有3个未成对电子,A 项正确;水是共价化合物,B 项正确;硝酸铵的阴离子是硝酸根离子,空间结构为平面三角形,不是三角锥形,C 项错误;2N 中存在氮氮三键,D 项正确.3.【答案】A【解析】电子从能量较高的能级跃迁至能量较低的能级上会以光的形式释放能量,A 项符合题意;乙酸乙酯和油漆的主要成分都是有机物,且都是弱极性分子,根据相似相溶原理,乙酸乙酯能溶解油漆,与可燃性无关,B 项不符合题意;液氨作制冷剂是因为液氨挥发时吸收大量热量,没有破坏化学键,C 项不符合题意;2SO 作保鲜剂是因为2SO 消耗了红酒中的微量2O ,2SO 表现出还原性,与2SO 是极性分子无关,D 项不符合题意.4.【答案】D【解析】将硝酸铜晶体与饱和硝酸铜溶液分离,采用过滤操作,不需要分液漏斗,D 项错误.5.【答案】C【解析】气体中,氢气密度最小,R 为氢;基态X 原子的价层电子排布式为222s 2p ,X 为碳;基态Z 原子最外层电子数和K 层电子数相等,Z 为镁;Y 的简单氢化物可与其最高价氧化物对应的水化物反应,且Y 的原子序数小于镁、大于碳,Y 为氮.原子半径:C>N ,A 项错误;3HNO 是强酸,23H CO 是弱酸,B 项错误;N 、C 、H 的电负性依次减小,C 项正确;4NH CN 中既含离子键,又含共价键,D 项错误.6.【答案】B【解析】该有机物中连有羧基的碳原子和亚甲基上的碳原子均采取3sp 杂化,所有原子不可能共平面,A 项错误;该有机物含(酚)羟基,能与3FeCl 溶液发生显色反应,B 项正确;1mol 该有机物分子含1mol 苯环,羧基不能与2H 加成,1mol 该有机物最多能与23molH 加成,C 项错误;1个该分子只含1个手性碳原子,D 项错误.7.【答案】A【解析】碘单质在标准状态下为固态,211.2LI 中所含原子数远大于A N ,A 项错误;3O 和2O 的混合气体可以看成由O 原子组成,即316gO 和2O 的混合物含1molO 原子,即含8mol 质子,B 项正确;31molO 完全反应时,只有1mol 氧原子由0价变为2 价,转移2mol 电子,C 项正确;1个水分子含2个σ键,D 项正确.8.【答案】D【解析】根据氧化还原反应原理,硫元素化合价降低,必有元素化合价升高,依题意,铁元素化合价升高,即铁元素化合价由2+价可能升至3+价,则M 可能是34Fe O (黑色)或23Fe O (红色),A 项错误;上述转化过程涉及两个氧化还原反应:硫酸亚铁分解的反应、二氧化硫被氧化生成硫酸的反应,B 项错误;制备硝酸的反应是复分解反应,没有发生氧化还原反应,该反应利用高沸点的硫酸制低沸点的硝酸,C 项错误;硝酸受热易分解,微热条件下制备硝酸,避免硝酸分解,D 项正确.9.【答案】B【解析】不能直接在容量瓶中溶解固体,称量NaOH 固体后应在烧杯中溶解、冷却、转移到容量瓶中定容,A 项不符合题意;向KI 溶液中加入少量溴水,振荡,发生氧化还原反应:22Br 2KI2KBr I ++,再加入4CCl 充分振荡后,若观察到下层溶液呈紫红色,说明氧化性:22Br I >,B 项符合题意;新制氯水具有漂白性,会使pH 试纸褪色,不能用pH 试纸测定新制氯水的pH ,C 项不符合题意;2Cl 和HCl 都能和NaOH 溶液反应,不能用NaOH 溶液除去2Cl 中的HCl ,应使用饱和食盐水,D 项不符合题意.10.【答案】D【解析】根据电源的正、负极可知,极为阳极,发生氧化反应,b 极为阴极,发生还原反应,质子()H +由阳极区向阴极区迁移,A 、B 项正确;b 极上2O 发生还原反应生成22H O ,C 项正确;a 极反应式为222H O 4e 4H O -+-+↑,根据电子守恒,b 极上消耗22molO 时,a 极上只生成21molO ,D 项错误.11.【答案】C【解析】铁为活泼电极,铁在阳极上优先发生氧化反应,A 项错误;在硫酸中3NH 不能大量存在,产物为硫酸铵、硫酸氢铵,B 项错误;根据原子守恒,水分子的化学计量数为(n 1)-,D 项错误.12.【答案】C【解析】基态F -的核外电子排布式为2261s 2s 2p ,A 项错误;由晶胞结构可知,位于顶点和面心的黑球的个数为1186482⨯+⨯=,位于体内的白球的个数为8,由氟化锶的化学式可知,黑球为2Sr +,白球为F -,B 项错误;由晶胞结构可知,位于顶点的2Sr +与位于面心的2Sr +的距离最近,则每个2Sr +周围紧邻且等距离的2Sr +个数为12,C 项正确;由晶胞结构可知,氟离子与锶离子间的最近距离为体对角线的14,即3anm 4,D 项错误.13.【答案】D【解析】由图像可知,该反应的ΔH<0,ΔS<0,由ΔG=ΔH TΔS 0-<可知该反应在低温下可自发进行,A 项正确;由反应历程图可知,该反应存在极性键、非极性键的断裂和极性键的形成,B 项正确;由图可知,生成3TS 的步骤活化能最大,故该步骤为反应的决速步骤,C 项正确;催化剂不能改变焓变,D 项错误.14.【答案】B【解析】根据电离常数表达式可知,()()()()4a w b 32132c Ac c NH lglg K (HAc)pH,lglg K pH pK NH H O ,L c(HAc)c NH H O -+-=---=++⋅⋅直线表示pH 增大,pX 减小,A 项正确;根据图中数据可计算:() 4.75a b 32K (HAc)K NH H O 10,Q -=⋅=点溶液显中性,即()()()()4c NH c Ac c H c OH +-+-=>=,B 项错误,D 项正确;加入10mL 醋酸溶液得到含起始浓度相等的4NH Ac 和32NH H O ⋅混合液,根据电离常数可知,4NH +与Ac -的水解程度相同,故以一水合氨电离为主,溶液显碱性,C 项正确.15.【答案】(1)d (1分)平面三角形(1分)(2)24SiO CaSO 、(2分)23Co O 有强氧化性,易氧化HCl 生成2Cl (2分)(3)100(2分)(4)<(2分)萃取(2分)(5)3232224CoCO 2Li CO O 4LiCoO 6CO +++高温(2分)【解析】(2)原料中含3+价钴,碳酸钴中为2+价钴.“酸浸”中加入双氧水,还原钴.说明23Co O 具有强氧化性,如果加入盐酸,可能产生氯气.(3)两种沉淀同时生成时,溶液中存在沉淀溶解平衡,()()()()2sp 22sp 2c Ca K CaF 100K MgF c Mg++==.(4)加入[]36KSCN,FeF -不会转化成3Fe(SCN),说明在水中稳定性:[]363FeF Fe(SCN)->.有机相主要成分是萃取剂,可循环用于“萃取”工序.(5)钴的化合价升高,在煅烧中,空气中2O 参与反应,并放出2CO .16.【答案】(1)12H +H ∆∆(2分)(2)①>(1分)随着温度升高,化学平衡常数增大,说明升高温度平衡正向移动,则该反应为吸热反应(2分)②AC (2分)③使用催化剂(或增大压强,2分)从体系中分离出2H (或降低温度,2分)(3)①0.14(2分)②3610-⨯(或0.006,2分)【解析】(1)根据盖斯定律可知,=+ⅢⅠⅡ,则312H H H ∆=∆+∆.(2)①随着温度升高,化学平衡常数增大,说明升高温度平衡正向移动,则该反应为吸热反应,1H 0∆>;②单位时间内消耗2CO 的物质的量和消耗CO 的物质的量相等,说明该反应的正反应速率等于逆反应速率,则反应达到平衡状态,A 项符合题意;反应前后,气体的质量不变,恒容密闭容器内气体的体积不变,则气体的密度始终保持不变,故容器内气体密度保持不变,不能说明该反应达到平衡状态,B 项不符合题意;容器内2CO 的体积分数保持不变,则()()22v CO =v CO 正逆,说明该反应达到平衡状态,C 项符合题意;③图甲中,2t 时刻,v v 正逆、同幅度增大,平衡未发生移动,则2t 时刻改变的条件可能是使用催化剂,且该反应是气体分子数不变的反应,增大压强也会同幅度增大v v 正逆、,且平衡不移动,故图甲中2t 时刻发生改变的条件是使用催化剂或增大压强;图乙中,2t 时刻,()2c CO 增大,()c CO 减小,平衡逆向移动,2t 时刻发生改变的条件可能是从体系中分离出2H ,且该反应是吸热反应,降低温度也能使平衡逆向移动,故图乙中2t 时刻发生改变的条件是从体系中分离出2H 或降低温度.(3)①2CO 和2H 的起始投料分别为1mol 和3mol ,平衡时2CO 的转化率为20%,3CH OH 的选择性为70%,则()3n CH OH 1mol 20%70%0.14mol =⨯⨯=;②由题意可得:Ⅰ.222CO (g)H (g)CO(g)H O(g)xmolxmolxmolxmol++ 转化Ⅲ.2232CO (g)3H (g)CH OH(g)H O(g)ymol3ymolymolymol++ 转化由①计算可知,()3n CH OH 0.14mol =,则y 0.14=,又2CO 的转化率为20%,则x+y 120%=⨯,则x 0.06=,则可计算出平衡时:()()()()2232n CO 0.8mol,n H 2.52mol,n(CO)0.06mol,n CH OH 0.14mol,n H O 0.2mol =====,则n 3.7ol ()2m =总,则反应Ⅰ的()()()23p 220.060.255p(CO)p H O 3.72 3.72K 6100.8 2.52p CO p H 553.72 3.72-⨯⨯⨯⋅==≈⨯⋅⨯⨯⨯.17.【答案】(1)三颈(口)烧瓶(1分)(2)D C D B →→→(2分)(3)A (2分)将装置中的空气排尽(2分)(4)d (2分)(5)b (2分)(6)38.8cVw(2分)偏高(2分)【解析】(2)依题意,必须先制备干燥的二氧化硫,否则产品会混有杂质硫酸氢铵.用氢氧化钠溶液吸收尾气,要防止氢氧化钠溶液中水挥发进入装置C .故装置排序为AD C D B →→→→.(3)装置C 中反应之前要排尽装置内2CO 、水蒸气,即先旋开装置A 中分液漏斗活塞,利用2SO 将装置中空气排尽.(4)装置D 中浓硫酸用于干燥2SO ,吸收水,可选择装有五氧化二磷的U 型管替代装置D .(5)依题意,羟胺加热时会发生爆炸,项错误;本实验有2SO 产生,应在通风橱中进行,b 项正确;氨基磺酸微溶于乙醇,采用过滤操作分离,C 项错误.(6)23H NSO H 是一元强酸,甲基橙作指示剂,滴定反应为23232H NSO H NaOHH NSO Na H O ++或()444424222NH HSO 2NaOHNH SO Na SO 2H O +++,产品纯度:()323100cV 109738.8cV 25.00w H NSO H 10w 0%%w-⨯⨯⨯=⨯=.若用酚酞作指示剂,消耗氢氧化钠溶液增多,测得结果偏高.18.【答案】(1)间苯二酚(1,3-苯二酚,1分)酯基、醚键(2分)(2)加成反应(1分)23sp sp 、(2分)(3)(2分)(4)6(2分)或(2分)(5)3|CH C H C CHOH≡—(2分)【解析】(2)由流程可知,G 和乙炔发生加成反应生成H,G 中碳原子的杂化类型为23sp sp 、.(3)根据H 、F 、Q 的结构可推知副产物为2H O .(4)由题意可知,满足条件的E 的芳香族同分异构体苯环上有2个羧基、1个甲基,共有2316++=种,其中核磁共振氢谱上有4组峰的结构简式为.(5)由合成路线可知,乙醛和乙炔发生G→>H的反应,则X的结构简式为3|CH C H C CHOH≡—,X与HCl发生加成反应生成Y,Y的结构简式为32||CH C H C CHOH Cl≡—,Y 与在3AlCl 的作用下反应生成.。
广西壮族自治区南宁市第二十五中学高一化学下学期期末试题含解析

广西壮族自治区南宁市第二十五中学高一化学下学期期末试题含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 对下列物质进行的分类正确的是A、纯碱、烧碱均属于碱B、CuSO4·5H2O属于纯净物C、凡能电离出H+的化合物均属于酸D、盐类物质一定含有金属阳离子参考答案:B略2. 科学家最近发现2种粒子:第1种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第2种是由四个氧原子构成的分子。
下列有关这两种粒子的说法不正确的是A、“四中子”不显电性B、“四中子”的质量数为4C、第2种粒子是氧气的另一种同位素D、等质量的O4和O3的原子数相等参考答案:C略3. 保护环境,就是关爱自己。
下列说法中你认为不正确的是A.空气质量日报的主要目的是树立人们环保意识,同时也让人们知道了二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物B.酸雨是指pH小于7的雨水C.为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须回收处理D.居室污染是来自建筑、装饰和家具材料散发出的甲醛等有害气体参考答案:B4. 甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸4种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙十丁→沉淀;乙+丁→无色无味气体。
则甲、乙、丙、丁4种溶液依次是()A. BaCl2、Na2CO3、盐酸、AgNO3B. BaCl2、Na2CO3、AgNO3、盐酸C. Na2CO3、盐酸、AgNO3、BaCl2D. AgNO3、盐酸、BaCl2、Na2CO3参考答案:B略5. 某化学兴趣小组设计了如图所示的浓HNO3与Cu 反应的微型实验。
下列说法中错误的是A. 挤压塑料瓶使浓HNO3进入干燥管就可引发反应B. 将装置口向上整起就可停止反应C. 蘸碱液的棉花可起到吸收NO2的作用D. 该装置适用于木炭与浓硝酸或浓硫酸的反应实验参考答案:D该装置的优点:控制反应的发生和停止,尾气被碱液吸收,对环境无危害;A、B、C均正确;木炭与浓硝酸或浓硫酸发生反应需要加热才能够进行,而该装置是在常温下进行的反应装置;D错误;正确选项:D。
广西南宁市高一物理下学期期末试卷(含解析)-人教版高一全册物理试题

2016-2017学年某某南宁市高一〔下〕期末物理试卷一、选择题〔共8小题,每一小题6分,总分为48分〕1.关于曲线运动,如下说法中正确的答案是〔〕A.物体做曲线运动时,有可能处于平衡状态B.做曲线运动的物体,速度可能不变C.所有做曲线运动的物体,速度一定发生改变D.所有做曲线运动的物体,加速度方向与速度方向始终一致2.用细线悬吊着一个质量为m的小球,使小球在水平面内做匀速圆周运动,细线与竖直方向夹角为α,线长为L,如下列图,如下说法中正确的答案是〔〕A.小球受重力、拉力、向心力B.小球受重力、拉力,两者的合力提供向心力C.小球受重力、拉力,拉力提供向心力D.小球受重力、拉力,重力提供向心力3.如下列图,皮带传动装置上有 A、B、C三点,OA=O′C=r,O′B=2r,如此皮带轮转动时如下关系成立的〔〕A.v A=v B,v B=v C B.ωA=ωB,v B>v C C.v A=v B,ωB=ωC D.ωA>ωB,v B=v C4.在下面列举的各个实例中,哪些情况机械能是守恒的?〔〕A.汽车在水平面上匀速运动B.羽毛球比赛中在空中运动的羽毛球C.拉着物体沿光滑斜面匀速上升D.如下列图,在光滑水平面上运动的小球碰到一个弹簧,把弹簧压缩后,又被弹回来5.2007年11月5日,“嫦娥一号〞探月卫星沿地月转移轨道到达月球,在距月球外表200km的P点进展第一次“刹车制动〞后被月球捕获,进入椭圆轨道Ⅰ绕月飞行,如下列图.卫星在P点经过几次“刹车制动〞,最终在距月球外表200km的圆形轨道Ⅲ上绕月球做匀速圆周运动.用T1、T2、T3分别表示卫星在椭圆轨道Ⅰ、Ⅱ和圆形轨道Ⅲ的周期,用a1、a2、a3分别表示卫星沿三个轨道运动到P点的加速度,如此下面说法正确的答案是〔〕A.T1>T2>T3B.T1<T2<T3C.a1>a2>a3D.a1<a2<a36.关于第一宇宙速度,如下说法中正确的答案是〔〕A.它是人造地球卫星绕地球飞行的最小速度B.它是近地圆轨道上人造卫星的最大运行速度C.它能使卫星进入近地圆形轨道的最小发射速度D.它是卫星在椭圆轨道上运行时在近地点的速度7.一个25kg的小孩从高度为 3.0m的滑梯顶端由静止开始滑下,滑到底端时的速度为2.0m/s.取g=10m/s2,关于力对小孩做的功,以下结果正确的答案是〔〕A.合外力做功50J B.阻力做功500JC.重力做功500J D.支持力做功50J8.如下列图,桌面高度为h,质量为m的小球,从离桌面高H处自由落下,不计空气阻力,假设桌面处的重力势能为零,小球落到地面前的瞬间的机械能应为〔〕A.mgh B.mgH C.mg〔H+h〕D.mg〔H﹣h〕二、解答题〔共2小题,总分为21分〕9.〔1〕在做“研究平抛运动〞实验时,除了木板、小球、斜槽、铅笔、图钉之外,如下器材中还需要的是.A.游标卡尺B.秒表 C.坐标纸 D.天平 E.弹簧秤 F.重垂线〔2〕实验中,如下说法正确的答案是.A.应使小球每次从斜槽上一样的位置自由滑下B.斜槽轨道必须光滑C.斜槽轨道末端可以不水平D.要使描出的轨迹更好地反映真实运动,记录的点应适当多一些E.为了比拟准确地描出小球运动的轨迹,应该用一条曲线把所有的点连接起来〔3〕在“研究平抛运动〞的实验中,用一张印有小方格的纸记录轨迹,小方格的边长L=1.25cm,假设小球在平抛运动途中的几个位置如图a、b、c、d所示,如此小球平抛的初速度的计算式为v0=〔用L、g表示〕,其值是.10.用200N的拉力将地面上的一个质量为10kg的物体提升10m〔g=10m/s2,不计空气阻力〕.拉力对物体所做的功为J;物体被提高后具有的重力势能是J〔以地面为零势能参考面〕;物体被提高后具有的动能是J.三、计算题〔共3小题,总分为31分〕11.把一个质量为1kg的物体放在水平面上,用8N的水平拉力使物体从静止开始运动,物体与水平面的动摩擦因数为0.2,物体运动2s时撤掉拉力.〔g取10m/s2〕求:〔1〕2s末物块的动能.〔2〕2s后物块在水平面上还能向前滑行的最大距离.12.我国“嫦娥一号〞月球探测器在绕月球成功运行之后,为进一步探测月球的详细情况,又发射了一颗绕月球外表飞行的科学试验卫星.假设卫星绕月球作圆周运动,月球绕地球也作圆周运动,且轨道都在同一平面内.己知卫星绕月球运动周期T0,地球外表处的重力加速度g,地球半径R0,月心与地心间的距离为r om,引力常量G,试求:〔1〕月球的平均密度ρ〔2〕月球绕地球运转的周期T.13.如图,一不可伸长的轻绳上端悬挂于O点,下端系一质量m=1.0kg的小球.现将小球拉到A点〔保持绳绷直〕由静止释放,当它经过B点时绳恰好被拉断,小球平抛后落在水平地面上的C点.地面上的D点与OB在同一竖直线上,绳长L=1.0m,B点离地高度H=1.0m,A、B两点的高度差h=0.5m,重力加速度g取10m/s2,不计空气影响,求:〔1〕地面上DC两点间的距离s;〔2〕轻绳所受的最大拉力大小.2016-2017学年某某南宁市金伦中学高一〔下〕期末物理试卷参考答案与试题解析一、选择题〔共8小题,每一小题6分,总分为48分〕1.关于曲线运动,如下说法中正确的答案是〔〕A.物体做曲线运动时,有可能处于平衡状态B.做曲线运动的物体,速度可能不变C.所有做曲线运动的物体,速度一定发生改变D.所有做曲线运动的物体,加速度方向与速度方向始终一致【考点】42:物体做曲线运动的条件.【分析】物体做曲线运动的条件是合力与速度不在同一条直线上,合外力大小和方向不一定变化,由此可以分析得出结论.【解答】解:A、处于平衡状态的物体的合外力为零,不会做曲线运动,故A错误;B、C、做曲线运动的物体速度的方向不断变化,所以速度一定发生变化,故B错误,C正确;D、物体做曲线运动的条件是合力与速度不在同一条直线上,由牛顿第二定律可知,加速度的方向与合外力的方向是一样的,所以做曲线运动的物体,加速度方向与速度方向不可能一致.故D错误;应当选:C2.用细线悬吊着一个质量为m的小球,使小球在水平面内做匀速圆周运动,细线与竖直方向夹角为α,线长为L,如下列图,如下说法中正确的答案是〔〕A.小球受重力、拉力、向心力B.小球受重力、拉力,两者的合力提供向心力C.小球受重力、拉力,拉力提供向心力D.小球受重力、拉力,重力提供向心力【考点】4A:向心力;37:牛顿第二定律.【分析】小球在水平面内做匀速圆周运动,由合外力提供向心力,分析小球实际受到的力即可.【解答】解:小球在水平面内做匀速圆周运动,对小球受力分析,如图,小球受重力、绳子的拉力,由两者的合力提供向心力,故ACD错误,B正确;应当选:B3.如下列图,皮带传动装置上有 A、B、C三点,OA=O′C=r,O′B=2r,如此皮带轮转动时如下关系成立的〔〕A.v A=v B,v B=v C B.ωA=ωB,v B>v C C.v A=v B,ωB=ωC D.ωA>ωB,v B=v C【考点】48:线速度、角速度和周期、转速.【分析】共轴转动时角速度相等,靠传送带传动时,两轮边缘各点线速度大小相等,根据v=rω,求出各点的线速度、角速度之比.【解答】解:除圆心外,同轮轴上的点,角速度相等,故:ωB=ωC同皮带上的点,线速度大小相等,即:v A=v B由v=ωr,即有角速度相等时,半径越大,线速度越大,如此得:v B>v C线速度相等时,角速度与半径成反比,如此得:ωA>ωB综合得到:ωA>ωB=ωC,v A=v B>v C应当选:C.4.在下面列举的各个实例中,哪些情况机械能是守恒的?〔〕A.汽车在水平面上匀速运动B.羽毛球比赛中在空中运动的羽毛球C.拉着物体沿光滑斜面匀速上升D.如下列图,在光滑水平面上运动的小球碰到一个弹簧,把弹簧压缩后,又被弹回来【考点】6C:机械能守恒定律.【分析】明确机械能守恒的条件,知道只有重力或弹力〔保守力〕做功时,物体的动能和势能相互转化,物体机械能才守恒.【解答】解:A、汽车在水平面上匀速运动时,消耗了燃料的能力转化为机械能,而机械能局部又转化为内能,故机械能不守恒,故A错误;B、羽毛球比赛中在空中运动的羽毛球由于阻力不能忽略,故有阻力做功,机械能不守恒,故B错误;C、拉着物体沿光滑斜面匀速上升时,动能不变,势能变大,故机械能变大,故C错误;D、地面光滑,小球碰到弹簧被弹回的过程中只有弹簧弹力做功,机械能守恒,故D正确.应当选:D5.2007年11月5日,“嫦娥一号〞探月卫星沿地月转移轨道到达月球,在距月球外表200km 的P点进展第一次“刹车制动〞后被月球捕获,进入椭圆轨道Ⅰ绕月飞行,如下列图.卫星在P点经过几次“刹车制动〞,最终在距月球外表200km的圆形轨道Ⅲ上绕月球做匀速圆周运动.用T1、T2、T3分别表示卫星在椭圆轨道Ⅰ、Ⅱ和圆形轨道Ⅲ的周期,用a1、a2、a3分别表示卫星沿三个轨道运动到P点的加速度,如此下面说法正确的答案是〔〕A.T1>T2>T3B.T1<T2<T3C.a1>a2>a3D.a1<a2<a3【考点】4H:人造卫星的加速度、周期和轨道的关系;4F:万有引力定律与其应用.【分析】根据开普勒第三定律比拟卫星在不同轨道上的周期大小.根据卫星所受的万有引力大小,通过牛顿第二定律比拟加速度的大小【解答】解:A、根据开普勒第三定律=k,半长轴越小,周期越小,所以卫星在轨道Ⅰ运动的周期最长,在轨道Ⅲ运动的周期最短.即T1>T2>T3.故A正确,B错误C、卫星的加速度由万有引力产生,根据m=ma得:a=,所以卫星在三个轨道运动到P点的万有引力大小相等,根据牛顿第二定律,加速度相等.即a1=a2=a3.故CD错误.应当选:A.6.关于第一宇宙速度,如下说法中正确的答案是〔〕A.它是人造地球卫星绕地球飞行的最小速度B.它是近地圆轨道上人造卫星的最大运行速度C.它能使卫星进入近地圆形轨道的最小发射速度D.它是卫星在椭圆轨道上运行时在近地点的速度【考点】4I:第一宇宙速度、第二宇宙速度和第三宇宙速度.【分析】第一宇宙速度又称为环绕速度,是指在地球上发射的物体绕地球飞行作圆周运动所需的最小初发射速度.【解答】解:A、人造卫星在圆轨道上运行时,运行速度为:v=,轨道半径越大,速度越小,故第一宇宙速度是卫星在圆轨道上运行的最大速度,故A错误,B、由A选项分析可知,当轨道半径是地球的半径时,如此第一宇宙速度即为近地圆轨道上人造地球卫星的运行速度,故B正确;C、物体在地面附近绕地球做匀速圆周运动的速度叫做第一宇宙速度,在地面附近发射飞行器,如果速度等于7.9km/s,飞行器恰好做匀速圆周运动,如果速度小于7.9km/s,就出现万有引力大于飞行器做圆周运动所需的向心力,做近心运动而落地,所以发射速度不能小于7.9km/s;故C正确.D、如果速度大于7.9km/s,而小于11.2km/s,它绕地球飞行的轨迹就不是圆,而是椭圆,所以卫星在椭圆轨道上运行时在近地点的速度大于7.9km/s,故D错误.应当选:BC.7.一个25kg的小孩从高度为 3.0m的滑梯顶端由静止开始滑下,滑到底端时的速度为2.0m/s.取g=10m/s2,关于力对小孩做的功,以下结果正确的答案是〔〕A.合外力做功50J B.阻力做功500JC.重力做功500J D.支持力做功50J【考点】62:功的计算.【分析】根据动能定理研究滑梯顶端由静止开始滑下滑到底端求出合力的功.根据合力功与分力功的关系求出分力功.【解答】解:A、根据动能定理研究滑梯顶端由静止开始滑下滑到底端得:w合=△E k=mv2﹣0=50J,故A正确.B、小孩由滑梯顶端由静止开始滑下滑到底端得过程中,小孩受重力、支持力、阻力,因为支持力与位移方向垂直,所以支持力做功为0,由于功为标量,w合=w G+w阻重力做功w G=mgh=750J,w阻=w合﹣w G=﹣700J,故B错误.C、根据B选项分析知道重力做功750J,故C错误.D、因为支持力与位移方向垂直,所以支持力做功为0,故D错误.应当选:A.8.如下列图,桌面高度为h,质量为m的小球,从离桌面高H处自由落下,不计空气阻力,假设桌面处的重力势能为零,小球落到地面前的瞬间的机械能应为〔〕A.mgh B.mgH C.mg〔H+h〕D.mg〔H﹣h〕【考点】6C:机械能守恒定律.【分析】小球落到地面瞬间重力势能可直接得到﹣mgh,但动能不知道,机械能不好直接确定.但最高点时速度为零,动能为零,机械能很快求出,根据小球下落过程中机械能守恒,落地时与刚下落时机械能相等,就能求出小球落到地面前的瞬间的机械能.【解答】解:以桌面为参考平面,小球在最高点时机械能E=mgH小球下落过程中机械能守恒,如此小球落到地面前瞬间的机械能为mgH.故ACD错误,B正确.应当选:B.二、解答题〔共2小题,总分为21分〕9.〔1〕在做“研究平抛运动〞实验时,除了木板、小球、斜槽、铅笔、图钉之外,如下器材中还需要的是CF .A.游标卡尺B.秒表 C.坐标纸 D.天平 E.弹簧秤 F.重垂线〔2〕实验中,如下说法正确的答案是AD .A.应使小球每次从斜槽上一样的位置自由滑下B.斜槽轨道必须光滑C.斜槽轨道末端可以不水平D.要使描出的轨迹更好地反映真实运动,记录的点应适当多一些E.为了比拟准确地描出小球运动的轨迹,应该用一条曲线把所有的点连接起来〔3〕在“研究平抛运动〞的实验中,用一张印有小方格的纸记录轨迹,小方格的边长L=1.25cm,假设小球在平抛运动途中的几个位置如图a、b、c、d所示,如此小球平抛的初速度的计算式为v0=〔用L、g表示〕,其值是0.70m/s .【考点】MB:研究平抛物体的运动.【分析】〔1、2〕在实验中要画出平抛运动轨迹,必须确保小球做的是平抛运动.所以斜槽轨道末端一定要水平,同时斜槽轨道要在竖直面内.要画出轨迹,必须让小球在同一位置屡次释放,才能在坐标纸上找到一些点.然后将这些点平滑连接起来,就能描绘出平抛运动轨迹.结合实验的原理确定所需的器材.〔3〕根据竖直方向上连续相等时间内的位移之差是一恒量求出相等的时间间隔,结合水平位移和时间间隔求出初速度.【解答】解:〔1〕解:在做“研究平抛物体的运动〞实验时,除了木板、小球、斜槽、铅笔、图钉之外,如下器材中还需要重锤线,确保小球抛出是在竖直面内运动,还需要坐标纸,便于确定小球间的距离.故C、F正确.应当选:CF.〔2〕A、实验中每次让小球从斜槽的同一位置由静止释放,故A正确.B、斜槽轨道不一定需要光滑,只要让小球从斜槽的同一位置由静止释放即可,故B错误.C、为了保证小球做平抛运动,斜槽的末端必须水平,故C错误.D、要使描出的轨迹更好地反映真实运动,记录的点应适当多一些,故D正确.E.为了比拟准确地描出小球运动的轨迹,应该用一条曲线把点平滑地连接起来,故E错误.应当选:AD.〔3〕在竖直方向上,根据△y=L=gT2得,T=,如此小球平抛运动的初速度=,代入数据解得v0=0.70m/s.故答案为:〔1〕CF,〔2〕AD,〔3〕、0.70m/s10.用200N的拉力将地面上的一个质量为10kg的物体提升10m〔g=10m/s2,不计空气阻力〕.拉力对物体所做的功为2000 J;物体被提高后具有的重力势能是1000 J〔以地面为零势能参考面〕;物体被提高后具有的动能是1000 J.【考点】6C:机械能守恒定律;62:功的计算.【分析】根据W=Flcosα求出拉力做的功,根据重力做功求出重力势能的增加量.根据动能定理求出物体提高后具有的动能.【解答】解:根据W=Flcosα得物体从静止开始提起5m拉力做功W=2000J物体从静止提升10m时,重力做负功为﹣mgh=﹣1000J,所以物体被提高后具有的重力势能是1000J.物体合力做的功等于动能变化,W合=F合l=1000J=△E k如此物体提高后增加的重力势能是1000J.故答案为:2000;1000;1000三、计算题〔共3小题,总分为31分〕11.把一个质量为1kg的物体放在水平面上,用8N的水平拉力使物体从静止开始运动,物体与水平面的动摩擦因数为0.2,物体运动2s时撤掉拉力.〔g取10m/s2〕求:〔1〕2s末物块的动能.〔2〕2s后物块在水平面上还能向前滑行的最大距离.【考点】66:动能定理的应用.【分析】〔1〕根据匀变速直线运动的运动学公式求出加速度的大小,再根据牛顿第二定律求出2s末物块的动能.〔2〕根据牛顿第二定律求出撤去外力后的加速度,匀加速直线运动的末速度为匀减速直线运动的初速度,根据速度位移公式求出匀减速直线运动的位移,从而求出物体在水平面上最大位移.【解答】解:〔1〕根据牛顿第二定律:F﹣f=ma解得: =6m/s2如此在2秒内末物体的动能为=72J〔2〕根据动能定理,取从静止到停止,如此有解得:x=36m答:〔1〕2s末物块的动能72 J;〔2〕2s后物块在水平面上还能向前滑行的最大距离36 m.12.我国“嫦娥一号〞月球探测器在绕月球成功运行之后,为进一步探测月球的详细情况,又发射了一颗绕月球外表飞行的科学试验卫星.假设卫星绕月球作圆周运动,月球绕地球也作圆周运动,且轨道都在同一平面内.己知卫星绕月球运动周期T0,地球外表处的重力加速度g,地球半径R0,月心与地心间的距离为r om,引力常量G,试求:〔1〕月球的平均密度ρ〔2〕月球绕地球运转的周期T.【考点】4H:人造卫星的加速度、周期和轨道的关系;4F:万有引力定律与其应用.【分析】1、抓住绕月外表飞行的卫星受到的万有引力提供圆周运动向心力可计算月球的质量,再根据密度的定义式可计算月球的密度.2、抓住地球外表重力与万有引力相等和月球受到地球的万有引力提供圆周运动向心力可计算月球绕地球运动的周期.【解答】解:〔1〕设卫星质量为m,对于绕月球外表飞行的卫星,由万有引力提供向心力得又据得〔2〕月球的球心绕地球的球心运动的周期为T.地球的质量为M,对于在地球外表的物体m表有即月球绕地球做圆周运动的向心力来自地球引力即得答:〔1〕月球的平均密度ρ为.〔2〕月球绕地球运转的周期T为.13.如图,一不可伸长的轻绳上端悬挂于O点,下端系一质量m=1.0kg的小球.现将小球拉到A点〔保持绳绷直〕由静止释放,当它经过B点时绳恰好被拉断,小球平抛后落在水平地面上的C点.地面上的D点与OB在同一竖直线上,绳长L=1.0m,B点离地高度H=1.0m,A、B两点的高度差h=0.5m,重力加速度g取10m/s2,不计空气影响,求:〔1〕地面上DC两点间的距离s;〔2〕轻绳所受的最大拉力大小.【考点】6C:机械能守恒定律;37:牛顿第二定律;4A:向心力.【分析】〔1〕从A到B由动能定理可得B位置时的速度,之后做平抛运动,由平抛规律求解;〔2〕在B位置,由牛顿第二定律可求轻绳所受的最大拉力大小.【解答】解:〔1〕设小球在B点速度为v,对小球从A到B由动能定理得:mgh=mv2①绳子断后,小球做平抛运动,运动时间为t,如此有:H=②DC间距离:s=vt解得:s=m≈1.414m〔2〕在B位置,设绳子最大力量为F,由牛顿第二定律得:F﹣mg=④联立①④得:F=2mg=2×1×10N=20N根据牛顿第三定律,有F'=F,因而轻绳所受的最大拉力为20N.答〔1〕DC两点间的距离1.414m;〔2〕轻绳所受的最大拉力20N.。
上海市高一下学期期中化学试卷(理科)

上海市高一下学期期中化学试卷(理科)姓名:________ 班级:________ 成绩:________一、选择题 (共25题;共50分)1. (2分) (2016高一下·长安期中) 下列关于 Co原子的叙述不正确的是()A . 中子数为33B . 电子数为33C . 质量数为60D . 质子数为272. (2分)某元素原子价电子构型3d54S2 ,其应在()A . 第四周期ⅡA族B . 第四周期ⅡB族C . 第四周期ⅦA族D . 第四周期ⅦB族3. (2分)炒菜时,加一点酒和醋能使菜味飘香可口,原因是()A . 有盐类物质生成B . 有酯类物质生成C . 有醇类物质生成D . 有酸类物质生成4. (2分)下列各项表达式错误的是()A . 氧元素的一种核素:B . 过氧化钠的电子式:C . 二氧化碳分子的结构式:O﹣C﹣OD . F﹣的结构示意图:5. (2分)下列说法正确的是()A . 共价化合物中可能含有离子键B . Ca2+、K+、Cl﹣、S2﹣四种离子的半径依次减小C . 、、三种原子的核外电子数分别为124、125、126D . ⅥA族元素氧、硫、硒(Se)的位置从上至下,故H2O、H2S、H2Se稳定性依次减弱6. (2分) (2016高二下·东台月考) 据报道,我国拥有完全自主产权的氢氧燃料电池车在北京奥运会期间为运动员提供服务.某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是()A . 正极反应式为:O2+2H2O+4e﹣=4OH﹣B . 工作一段时间后,电解液中KOH的物质的量不变C . 该燃料电池的总反应方程式为:2H2+O2=2H2OD . 该电池反应2.24 L H2(标准状况)时,有0.1 mol电子转移7. (2分) (2018高二上·江西期中) 将4 mol A气体和2 mol B气体充入2 L的密闭容器中,一定条件下发生如下反应:。
广西省南宁市第二中学2023-2024学年高一下学期期中考试语文试题(含解析)

南宁市第二中学2023-2024学年高一下学期期中考试语文试题(时间150分钟,共150分)注意事项:1.答卷前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号填写在答题卡上,并认真核准条形码上的准考证号、姓名、考场号、座位号及科目,在规定的位置贴好条形码。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
一、现代文阅读(35分)(一)现代文阅读Ⅰ(本题共5小题,17分)阅读下面的文字,完成小题。
材料一:中国的藏书文化包含着浓郁的人文主义精神,它的核心则是“仁人爱物”。
所谓“仁人”便是把书与人的关系紧密地联系起来,使所藏尽量发挥其培育人材的社会功能。
从官藏来看,早在老子主管周藏室时,便曾热情地接待孔子来查阅百二十国史记,彼此还进行了学术研讨。
魏晋时期,国家藏书还曾应读者的借阅要求而赠书,如西晋皇甫谧向晋武帝借书,武帝应求赠书一车。
唐宋各代也将官藏作部分开放,如北宋的官藏即向一些官员开放,如因工作需要还可经过一定手续外借。
清代尤其注重官藏利用问题,在《四库全书》纂修以前,多位学者就有机会抄录官藏《永乐大典》所收各书,有一些重要而散佚的著作得到抢救,学者全祖望、徐松等都做过抄录工作,而《宋会要辑稿》之类的重要典籍因此得以流传。
《永乐大典》还被《四库全书》当为采录佚书的来源之一,使古代文化得到更广泛的流传。
《四库全书》修成后,不仅北京文渊阁可有条件地备人参阅,更在南北要地分建六阁,以便各地士人就近抄用,嘉惠士林,保存和普及文化,所尽仁人之心,功不可没。
公藏如书院之藏书本以供士子阅读为主旨,自不待言。
至私藏之体现仁人之心更为显著。
东汉末年学者蔡邕私藏近万卷,当他发现王粲是一位文采斐然的好学之士,虽然其女蔡琰也颇有学识,但他还是将藏书数千卷赠予王粲以培育人材。
宋晃公武之所以能写出一部私家目录名著——《郡斋读书志》,也是得力于四川转运使井度的慷慨赠书五十箧,使晃公武合个人私藏去重后得24500余卷,乃录诸书要旨而成书,体现了藏书文化的仁人效果。
广西南宁市2023-2024学年高一下学期4月期中考试 数学含答案

南宁2023-2024学年度下学期高一期中考试数学(答案在最后)(时间120分钟,共150分)一、单选题(共8小题,每小题5分,共40分,每小题仅有一个正确选项.)1.已知i 是虚数单位,则i1i =-()A.12i 2- B.1i 2-+ C.2i 2+ D.12i 2+2.已知直线a ,b 和平面α,a ⊂α,b α⊂,则“//a α”是“//a b ”的()A.充分不必要条件B.必要不充分条件C.充分必要条件D.既不充分也不必要条件3.如图所示,ABC 中,点D 是线段BC 的中点,E 是线段AD 的靠近A 的三等分点,则BE =()A .2136BA BC +B.1133+BA BC C.2133+BA BC D.1136BA BC +4.已知向量()2,0a =r,,2b λ⎛⎫= ⎪ ⎪⎝⎭,若向量b 在向量a上的投影向量1,02c ⎛⎫ ⎪⎝=⎭,则b = ()A.B.C.104D.15.已知一个圆柱和一个圆锥的底面半径和高分别相等,圆柱的轴截面是一个正方形,则这个圆柱的侧面积和圆锥的侧面积的比值是()A.4B.5C.2D.56.已知m ,n 为实数,1i -(i 为虚数单位)是关于x 的方程20x mx n -+=的一个根,则m n +=()A.0B.1C.2D.47.如图,已知正方形ABCD 的边长为4,若动点P 在以AB 为直径的半圆上(正方形ABCD 内部,含边界),则PC PD ⋅的取值范围为()A.(]0,16 B.[]0,16 C.()0,4 D.[]0,48.在ABC 中,已知tan tan a ba b A B+=+,则ABC 的形状一定是()A.等腰三角形B.直角三角形C.等边三角形D.等腰直角三角形二、多选题(共4小题,每小题5分,共20分,每小题有多个正确选项,全部选对得5分,部分选对得2分,有选错或不选得0分.)9.下列说法错误..的是().A.过三个点有且只有一个平面B.已知直线,l m ,平面,αβ,l β ,m β∥,l ⊂α,m α⊂,则αβ∥C.已知直线,l m ,平面α,m l ∥,l α∥,则m α∥D.如果两个不重合的平面有一个公共点,那么它们有且只有一条过该点的公共直线10.复数21iz i+=-,i 是虚数单位,则下列结论正确的是()A.|z |5= B.z 的共轭复数为3122i +C.z 的实部与虚部之和为2D.z 在复平面内的对应点位于第一象限11.把函数()sin f x x =的图像向左平移3π个单位长度,再把横坐标变为原来的12倍(纵坐标不变)得到函数()g x 的图像,下列关于函数()g x 的说法正确的是()A.最小正周期为πB.在区间,36ππ⎡⎤-⎢⎥⎣⎦上的最大值为32C.图像的一个对称中心为,03π⎛-⎫⎪⎝⎭D.图像的一条对称轴为直线12x π=12.如图,在长方体1111ABCD A B C D -中,2AB BC ==,14AA =,E 是棱1BB 上的一点,点F 在棱1DD 上,则下列结论正确的是()A .若1A ,C ,E ,F 四点共面,则BE DF=B.存在点E ,使得//BD 平面1A CEC.若1A ,C ,E ,F 四点共面,则四棱锥11C A ECF -的体积为定值D.若E 为1BB 的中点,则三棱锥11E A CC -的外接球的表面积是32π三、填空题(每小题5分,共20分).13.半径为2cm ,圆心角为23π的扇形面积为.14.已知向量()1,2AB =-,()2,3AC = ,(),3AD m =-u u u r ,若B ,C ,D 三点共线,则m =______.15.在ABC 中,若1a =,15cos 4A =,b x =,三角形有唯一解,则整数x =______.16.如图,在正四棱台1111ABCD A B C D -中,112A B =,22AB =,该棱台体积1433V =,则该棱台外接球的表面积为__________.四、解答题(共70分,解答应写出文字说明,证明过程或演算步骤)17.已知平面向量,a b 满足||2a = ,||4b = ,a 与b的夹角为2π3.(1)求a b -;(2)当实数k 为何值时,()()a kb ka b +⊥-.18.已知ABC 中,角,,A B C 所对的边分别为,,a b c ,且sin sin 4cos 0sin sin B AC A B+-=.(1)证明:2222a b c +=;(2)若22sin cos sin sin BB A C=,求角A 的大小.19.如图,在正方体中,S 是11B D 的中点,,,E F G 分别是BC 、DC 、SC 的中点.(1)求证:平面EFG ∥平面11DBB D ;(2)若正方体棱长为1,过A 、E 、1C 三点作正方体的截面,画出截面与正方体的交线(不必说明画法与理由,但要说明点在棱的位置),并求出截面的面积.20.如图,现有一直径2AB =百米的半圆形广场,AB 所在直线上存在两点C ,D ,满足2OC OD ==百米(O 为AB 的中点),市政规划要求,从广场的半圆弧AB 上选取一点E ,各修建一条地下管道EC 和ED 通往C 、D 两点.(1)设EOB θ∠=,试将管道总长(即线段EC ED +)表示为变量θ的函数;(2)求管道总长的最大值.21.已知锐角三角形ABC 的内角,,A B C 的对边分别为,,a b c 且cos sin A c A +=.(1)求角C 的大小;(2)若2c =,角A 与角B 的内角平分线相交于点D ,求ABD △面积的取值范围.22.定义非零向量(),OM a b = 的“相伴函数”为()()sin cos f x a x b x x =+∈R ,向量(),OM a b =称为函数()()sin cos f x a x b x x =+∈R 的“相伴向量”(其中O 为坐标原点).记平面内所有向量的“相伴函数”构成的集合为S .(1)设()()ππ3cos 63h x x x x ⎛⎫⎛⎫=++-∈ ⎪ ⎪⎝⎭⎝⎭R ,请问函数()h x 是否存在相伴向量OM ,若存在,求出与OM共线的单位向量;若不存在,请说明理由.(2)已知点(),M a b 满足:10,2ba ⎛⎤∈ ⎥⎝⎦,向量OM的“相伴函数”()f x 在0x x =处取得最大值,求0tan2x 的取值范围.南宁2023-2024学年度下学期高一期中考试数学(时间120分钟,共150分)一、单选题(共8小题,每小题5分,共40分,每小题仅有一个正确选项.)1.已知i 是虚数单位,则i1i =-()A.12i 2- B.1i 2-+ C.2i 2+ D.12i 2+【答案】B 【解析】【分析】利用复数的四则运算法则即可得出结论.【详解】()()()i 1i i 1i 1i 1i 1i 2+-+==--+.故选:B.2.已知直线a ,b 和平面α,a ⊂α,b α⊂,则“//a α”是“//a b ”的()A.充分不必要条件B.必要不充分条件C.充分必要条件D.既不充分也不必要条件【答案】B 【解析】【分析】根据题意,由空间中的线面关系,即可判断.【详解】根据线面平行的判定定理可得,若//a b ,则//a α,即必要性成立,若//a α,则//a b 不一定成立,故充分性不成立,所以“//a α”是“//a b ”的必要不充分条件.故选:B3.如图所示,ABC 中,点D 是线段BC 的中点,E 是线段AD 的靠近A 的三等分点,则BE =()A.2136BA BC +B.1133+BA BC C.2133+BA BC D.1136BA BC +【答案】A 【解析】【分析】根据平面向量基本定理结合已知条件求解即可【详解】因为点D 是线段BC 的中点,E 是线段AD 的靠近A 的三等分点,所以BE BD DE=+1223BC DA =+12()23BC BA BD =+-121()232BC BA BC =+-2136BA BC =+,故选:A4.已知向量()2,0a =r ,3,2b λ⎛⎫= ⎪ ⎪⎝⎭,若向量b 在向量a 上的投影向量1,02c ⎛⎫ ⎪⎝=⎭,则b = ()A.B.C.4D.1【答案】D 【解析】【分析】利用b 在a上的投影向量的定义求解.【详解】解:由已知可得,b 在a 上的投影向量为()2,0222a ba a a aa λλλ⋅⋅===⨯,又b 在a 上的投影向量1,02c ⎛⎫ ⎪⎝=⎭,所以12λ=.所以1b ==== ,D 正确.故选:D.5.已知一个圆柱和一个圆锥的底面半径和高分别相等,圆柱的轴截面是一个正方形,则这个圆柱的侧面积和圆锥的侧面积的比值是()A.4B.5C.2D.5【答案】B 【解析】【分析】设出底面半径,由题意可得高,即可计算圆柱的侧面积和圆锥的侧面积,即可得解.【详解】设这个圆柱和圆锥的底面半径为r ,由圆柱的轴截面是一个正方形,故其高2h r =,则圆柱的侧面积212π24πS r r r =⨯=,圆锥的侧面积22πS r ==,则2125S S ==.故选:B .6.已知m ,n 为实数,1i -(i 为虚数单位)是关于x 的方程20x mx n -+=的一个根,则m n +=()A.0B.1C.2D.4【答案】D 【解析】【分析】由1i -是关于x 的方程20x mx n -+=的一个根,则1i +是关于x 的方程20x mx n -+=的一个根,结合根与系数的关系求解即可.【详解】由1i -是关于x 的方程20x mx n -+=的一个根,则1i +是关于x 的方程20x mx n -+=的一个根,则1i 1i 2m =-++=,(1i)(1i)2n =-⨯+=,即2m =,2n =,则4m n +=,故选:D.7.如图,已知正方形ABCD 的边长为4,若动点P 在以AB 为直径的半圆上(正方形ABCD 内部,含边界),则PC PD ⋅的取值范围为()A.(]0,16 B.[]0,16 C.()0,4 D.[]0,4【答案】B 【解析】【分析】根据已知条件及极化恒等式,结合向量的线性运算即可求解.【详解】取CD 的中点E ,连接PE,如图所示,所以PE 的取值范围是2AD AE ⎡⎤⎢⎥⎣⎦,,即2,⎡⎣,又由()()PC PD PE ED PE EC ⋅=+⋅+ 22244CD PE PE =-=-,所以[]0,16PC PD ⋅∈.故选:B.8.在ABC 中,已知tan tan a ba b A B+=+,则ABC 的形状一定是()A.等腰三角形B.直角三角形C.等边三角形D.等腰直角三角形【答案】B 【解析】【分析】根据正弦定理,结合同角的三角函数关系式、二倍角的正弦公式、正弦型函数的性质进行求解即可.【详解】根据正弦定理,由sin sin sin sin sin sin sin sin sin sin tan tan tan tan cos cos a b A B A Ba b A B A B A B A B A BA B+=+⇒+=⇒+=+22sin sin cos cos (sin cos )(cos sin )A B A B A A B B ⇒+=+⇒-=-2222sin cos 2sin cos sin cos 2sin cos A A A A B B B B ⇒+-=+-1sin 21sin 2sin 2sin 2A B A B ⇒-=-⇒=,因为,(0,π)A B ∈,所以2,2(0,2π)A B ∈,所以有22A B =,或22πA B +=,或223πA B +=,当22A B =时,有A B =,此时有ππsin cos 44A A A AB =⇒=⇒==,即π2C =,所以此时该三角形是等腰直角三角形;当22πA B +=时,即π2A B +=,所以此时三角形是直角三角形;当223πA B +=时,即3π2A B +=,不符合三角形内角和定理,舍去,综上所述:ABC 的形状一定是直角三角形,故选:B二、多选题(共4小题,每小题5分,共20分,每小题有多个正确选项,全部选对得5分,部分选对得2分,有选错或不选得0分.)9.下列说法错误..的是().A.过三个点有且只有一个平面B.已知直线,l m ,平面,αβ,l β ,m β∥,l ⊂α,m α⊂,则αβ∥C.已知直线,l m ,平面α,m l ∥,l α∥,则m α∥D.如果两个不重合的平面有一个公共点,那么它们有且只有一条过该点的公共直线【答案】ABC 【解析】【分析】由立体几何公理判断AD ,由面面平行的判定及线面关系判断CD .【详解】对于A ,过不共线的三个点有且只有一个平面,故A 错误;对于B ,如果一个平面内有两条相交直线与另一个平面平行,那么这两个平面平行,故B 错误;对于C ,若m l ∥,l α∥,则m α∥或m α⊂,故C 错误;对于D ,由平面相交公理,可知D 正确;故选:ABC .10.复数21iz i+=-,i 是虚数单位,则下列结论正确的是()A.|z |=B.z 的共轭复数为3122i +C.z 的实部与虚部之和为2 D.z 在复平面内的对应点位于第一象限【答案】CD 【解析】【分析】根据复数的四则运算,整理复数z ,再逐一分析选项,即得.【详解】由题得,复数22(2)(1)13131(1)(1)122i i i i z i i i i i ++++====+--+-,可得||2z ==,则A 不正确;z 的共轭复数为1322i -,则B 不正确;z 的实部与虚部之和为13222+=,则C 正确;z 在复平面内的对应点为13(,22,位于第一象限,则D 正确.综上,正确结论是CD.故选:CD【点睛】本题考查复数的定义,共轭复数以及复数的模,考查知识点全面.11.把函数()sin f x x =的图像向左平移3π个单位长度,再把横坐标变为原来的12倍(纵坐标不变)得到函数()g x 的图像,下列关于函数()g x 的说法正确的是()A.最小正周期为πB.在区间,36ππ⎡⎤-⎢⎥⎣⎦上的最大值为32C.图像的一个对称中心为,03π⎛-⎫⎪⎝⎭D.图像的一条对称轴为直线12x π=【答案】AD 【解析】【分析】根据伸缩平移变换可得函数()g x 的解析式,进而判断各选项中图像性质.【详解】()sin f x x =的图像向左平移3π个单位长度得函数sin 3y x π⎛⎫=+⎪⎝⎭,再把横坐标变为原来的12倍(纵坐标不变)得到函数()sin 23g x x π⎛⎫=+ ⎪⎝⎭,其最小正周期为22T ππ==,A 选项正确;由,36x ππ⎡⎤∈-⎢⎣⎦,得22,333x πππ⎡⎤+∈-⎢⎥⎣⎦,则当232x ππ+=,即12x π=时,()g x 取最大值为1,B 选项错误;令23x k ππ+=,Z k ∈,得+62k x ππ=-,Z k ∈,所以函数()g x 的对称中心为+,062k ππ⎛⎫- ⎪⎝⎭,Z k ∈,所以,03π⎛-⎫⎪⎝⎭不成立,C 选项错误;令232x k πππ+=+,Z k ∈,解得122k x ππ=+,Z k ∈,所以函数()g x 的对称轴为122k x ππ=+,Z k ∈,当0k =时,12x π=,D 选项正确;故选:AD.12.如图,在长方体1111ABCD A B C D -中,2AB BC ==,14AA =,E 是棱1BB 上的一点,点F 在棱1DD 上,则下列结论正确的是()A.若1A ,C ,E ,F 四点共面,则BE DF =B.存在点E ,使得//BD 平面1A CEC.若1A ,C ,E ,F 四点共面,则四棱锥11C A ECF -的体积为定值D.若E 为1BB 的中点,则三棱锥11E A CC -的外接球的表面积是32π【答案】BCD 【解析】【分析】利用假设法即可判断A ,利用线面平行的判定即可判断B ,利用棱锥体积公式即可判断C ,求出外接球半径,找到球心位置即可判断D.【详解】对A ,由1,,,A C E F 四点共面,得1//CF A E ,则1DF B E =,若E 不是棱1BB 的中点,则BE DF ≠,故A 错误.对B ,当E 是棱1BB 的中点时,取1AC 的中点G ,连接1,GE B D ,则G 为1B D 的中点.因为E 为1BB 的中点,则//GE BD .因为GE Ì平面1,A CE BD ⊄平面1A CE ,所以//BD 平面1A CE ,则B 正确.根据长方体性质知11//BB CC ,且1CC ⊂平面11A CC ,1BB ⊄平面11A CC ,所以1//BB 平面11A CC ,同理可得1//DD 平面11A CC ,则点E ,F 到平面11A CC 的距离为定值,又因为11A CC △的面积为定值,所以三棱锥11E A CC -和三棱锥11F A CC -的体积都为定值,则四棱锥11C A ECF -的体积为定值,故C 正确.取棱1CC 的中点1O ,由题中数据可得1122,4CE C E CC ===,则22211CE C E CC +=,所以1CC E 为等腰直角三角形,所以1O 是1CC E 外接圆的圆心,1CC E 外接圆的半径2r =.设三棱锥E -11A CC 的外按球的球心为O ,半径为R ,设1OO d =,则()22222211118(2)R d r O B A B d d =+=+-=+-,即2248(2)d d +=+-,解得2d =,则28R =,此时O 点位于1DD 中点,从而三棱锥11E A CC -的外接球的表面积是24π32πR =,故D 正确.故选:BCD.三、填空题(每小题5分,共20分).13.半径为2cm ,圆心角为23π的扇形面积为.【答案】243cm π【解析】【分析】求出扇形的弧长,利用扇形面积公式求解即可.【详解】因为半径为2cm ,圆心角为23π的扇形,弧长为43π,所以扇形面积为:221442233cm cm ππ⨯⨯=故答案为243cm π.【点睛】本题考查扇形的面积公式的应用,考查计算能力,属于基础题.14.已知向量()1,2AB =-,()2,3AC = ,(),3AD m =-u u u r ,若B ,C ,D 三点共线,则m =______.【答案】16-【解析】【分析】根据题意求,BC BD,结合向量共线的坐标运算求解.【详解】由题意可得:()()3,1,1,5BC AB AC BD AD AB m =-==-=+-,若B ,C ,D 三点共线,可知//BC BD,则115m +=-,解得16m =-.故答案为:16-.15.在ABC 中,若1a =,cos 4A =,b x =,三角形有唯一解,则整数x =______.【答案】1或4【解析】【分析】关键知道三角形有唯一解的充要条件是a h =或a b ≥,然后根据这个条件即可解得整数b 的值.【详解】如图:已知h 是AB 边上的高,由三角形有唯一解的等价条件是a h =或a b ≥,由1cos sin 4A A =⇒=,因为b x =,所以sin 4x h b A ==,又因为1a =,根据唯一解的条件可知:14x=或1x ≥,解得4x =或1x ≤,又因为x 为整数,b x =,所以b 的值为1或4.故答案为:1或4.16.如图,在正四棱台1111ABCD A B C D -中,11A B =,AB =,该棱台体积3V =,则该棱台外接球的表面积为__________.【答案】16π【解析】【分析】作出辅助线,找到球心的位置,求出外接球半径,得到外接球表面积.【详解】连接11,B D BD ,取11,B D BD 的中点,E F ,连接1,,C E CF EF ,则外接球球心在直线EF 上,设球心为O ,如图所示,则1OC OC R ==,则EF ⊥平面ABCD ,因为正四棱台1111ABCD A B C D -中,112A B =,22AB =,故114,2BD B D ==,所以11,2C E CF ==,设四棱台的高为h ,故(2211432222833h ⎡++⨯=⎢⎣,解得3h =故3E F 设OF m =,则22224OC OF CF m =+=+,)222221113OC C E OE m=+=+,故)222413m m +=+,解得0m =,故半径042R =+=,故该棱台外接球的表面积为24π16πR =.故答案为:16π【点睛】方法点睛:解决与球有关的内切或外接的问题时,解题的关键是确定球心的位置.对于外切的问题要注意球心到各个面的距离相等且都为球半径;对于球的内接几何体的问题,注意球心到各个顶点的距离相等,解题时要构造出由球心到截面圆的垂线段、小圆的半径和球半径组成的直角三角形,利用勾股定理求得球的半径四、解答题(共70分,解答应写出文字说明,证明过程或演算步骤)17.已知平面向量,a b 满足||2a = ,||4b = ,a 与b的夹角为2π3.(1)求a b -;(2)当实数k 为何值时,()()a kb ka b +⊥-.【答案】(1)(2)3132k -=【解析】【分析】(1)由a b -=(2)由题得()()0a kb ka b +⋅-= 列出方程,求解即可.【小问1详解】因为=2,4,a b a = 与b 的夹角为2π3,所以2π1cos 24432a b a b ⎛⎫⋅=⋅=⨯⨯-=- ⎪⎝⎭,所以a b -==.【小问2详解】因为()()a kb ka b +⊥-,所以()()()2221a kb ka b ka k a b kb+⋅-=+-⋅- ()2441160k k k =---=,化为2310k k +-=,解得32k -±=.18.已知ABC 中,角,,A B C 所对的边分别为,,a b c ,且sin sin 4cos 0sin sin B AC A B+-=.(1)证明:2222a b c +=;(2)若22sin cos sin sin BB A C=,求角A 的大小.【答案】(1)证明见解析(2)90 【解析】【分析】(1)借助正弦定理与余弦定理化简即可得;(2)借助正弦定理与余弦定理化简后可得2225a c b +=,结合(1)中所得可得,,a b c 间的关系,再借助余弦定理即可得解.【小问1详解】由正弦定理及条件可得4cos 0b aC a b+-=,由余弦定理可得22222402b a a b c ab ab++--⋅=,化简得2222a b c +=;【小问2详解】由22sin cos sin sin B B A C =得222222a c b b ac ac+-=,化简得2225a c b +=,又2222a b c +=,故c =,所以a =,故222222cos 02b c a A bc +-==.所以角A 为90 .19.如图,在正方体中,S 是11B D 的中点,,,E F G 分别是BC 、DC 、SC 的中点.(1)求证:平面EFG ∥平面11DBB D ;(2)若正方体棱长为1,过A 、E 、1C 三点作正方体的截面,画出截面与正方体的交线(不必说明画法与理由,但要说明点在棱的位置),并求出截面的面积.【答案】(1)证明见解析(2)作图见解析,截面面积62【解析】【分析】(1)根据中位线得到线线平行,根据线面平行的判定定理得线面平行,再根据面面平行的判定定理可得面面平行.(2)取11A D 的中点H ,连11,,,C H AH AE C E ,可证四边形1AEC H 为平行四边形,从而可得11,,,C H AH AE C E 就是交线,求出AE 和AE 上的高,可得截面面积.【小问1详解】连SB ,如图:因为E 、F 分别是BC 、DC 的中点,所以EF BD ∥,因为EF ⊄平面11DBB D ,BD ⊂平面11DBB D ,所以//EF 平面11DBB D ;因为E 、G 分别是BC 、SC 的中点,所以//EG SB ,因为EG ⊄平面11DBB D ,SB ⊂平面11DBB D ,所以//EG 平面11DBB D ;因为EF EG E = ,且EF ⊂平面EFG ,EG ⊂平面EFG ,所以平面//EFG 平面11DBB D .【小问2详解】取11A D 的中点H ,连11,,,C H AH AE C E ,因为1AC 与HE 交于正方体的中心,且互相平分,所以四边形1AEC H 为平行四边形,则11,,,C H AH AE C E就是截面与正方体的交线,过C 作AE 的延长线的垂线CM ,垂足为M ,连1C M ,因为1C C ⊥平面AB CD ,EM ⊂面ABCD ,所以1C C EM ⊥,因为1CC CM C = 且都在面1C CM 内,所以EM ⊥平面1C CM ,又1C M ⊂面1C CM ,所以1EM C M ⊥,所以11sin sin 225AB CM CE CEM CE AEB AE =⋅∠=⋅∠=⨯==,所以1305C M ==,所以截面面积为152AE C M ⨯==.20.如图,现有一直径2AB =百米的半圆形广场,AB 所在直线上存在两点C ,D ,满足2OC OD ==百米(O 为AB 的中点),市政规划要求,从广场的半圆弧AB 上选取一点E ,各修建一条地下管道EC 和ED 通往C 、D两点.(1)设EOB θ∠=,试将管道总长(即线段EC ED +)表示为变量θ的函数;(2)求管道总长的最大值.【答案】(1)()f θ=[]0,πθ∈,(2)【解析】【分析】(1)在DOE 和COE 中,根据余弦定理即可求得;(2)结合(1),对函数平方处理,可得()210f θ⎡⎤=+⎣⎦.【小问1详解】在DOE 中,由余弦定理得:2222cos EOD 4122cos 54cos ED OD OE OD OE θθ=+-⋅⋅∠=+-⨯⨯=-,在COE 中,由余弦定理得:()2222cos EOC 4122cos π54cos EC OC OE OC OE θθ=+-⋅⋅⋅∠=+-⨯⨯-=+,所以()EC ED f θ+=,[]0,πθ∈,∴将管道总长(即线段EC +ED )表示为变量θ的函数为:()f θ=[]0,πθ∈,【小问2详解】由(1)可得:()2210f θ⎡⎤==+⎣⎦10=+,因为,[]0,πθ∈,所以20cos 1θ≤≤,()2101020f θ⎡⎤=++⎣⎦(百米)当且仅当2cos 0θ=,即π2θ=时取等号,因为()0f θ=,∴()f θ≤=.∴管道总长的最大值为21.已知锐角三角形ABC 的内角,,A B C 的对边分别为,,a b c 且cos sin A c A +=.(1)求角C 的大小;(2)若2c =,角A 与角B 的内角平分线相交于点D ,求ABD △面积的取值范围.【答案】(1)π3C =(2)3,33⎛- ⎝⎦【解析】【分析】(1)利用正弦定理,将等式中的边化为角,根据和角公式以及同角三角函数的商式公式,可得答案;(2)法1:根据锐角三角形内角的性质,可得角的取值范围,利用正弦定理,用角表示边,将三角形的面积整理为三角函数,可得答案;法2:利用内切圆的性质得到内切圆半径r 关于角A 的表达式,利用三角恒等变换,结合锐角三角形内角的性质得到解A 的范围,从而得解.【小问1详解】cos sin A c A +=,cos sin sin )C A C A B A C +==+,cos sin sin cos cos C A C A A C C A +=+,sin sin cos C A A C =,又0πA <<,得sin 0A >,所以sin C C =,即sin tan cos C C C ==由0πC <<,解得π3C =.【小问2详解】法1:由题意可知2π3ADB ∠=,设DAB α∠=,π3ABD α∴∠=-,π022α<< ,又πππ20,32B α⎛⎫=--∈ ⎪⎝⎭ ,ππ,124α⎛⎫∴∈ ⎪⎝⎭,在ABD △中,由正弦定理可得:sin sin AB AD ADB ABD =∠∠.即:22ππsin sin 33AD α=⎛⎫- ⎪⎝⎭,π3AD α⎛⎫∴=- ⎪⎝⎭,11πsin 2sin 223ABD S AB AD ααα⎛⎫∴=⋅⋅=⨯- ⎪⎝⎭21cos 22sin cos sin 2sin 2cos 2233ααααααα-=-=-=+-1πsin 2cos 2sin 23223363ααα⎛⎫⎛⎫+-=+- ⎪= ⎪ ⎪⎝⎭⎝⎭,π3sin 2,36333α⎛⎛⎫∴+-∈ ⎪ ⎝⎭⎝⎦,所以三角形面积的取值范围为3,33⎛ ⎝⎦.法2:设ABC 内切圆半径为r ,由题知,D 为ABC 内切圆的圆心,由面积公式,得11sin ()22ABC S AC BC C AC BC AB r ∴=⋅⋅=⨯++⨯,所以2AB BC r AC BC AB ⋅⋅=++①,在ABC 中,由正弦定理可得:sin sin sin AB AC BC C B A ==.即:2π2πsin sin sin 33AC BC A A =⎛⎫- ⎪⎝⎭=,所以2πsin()33AC A -=,sin 3BC A =,代入①式,结合积化和差,和差化积公式,得2π2π2π32sin sin()[cos cos(2)]3332cos()32332A A A AB BC r AC BC AB ⋅----⋅⋅==++22π1π1cos(2)cos ()π13234)]32A A A -+--==--,由ABC 为锐角三角形,得π022ππ032A B A ⎧<<⎪⎪⎨⎪<=-<⎪⎩,解得ππ62A <<,所以11π1π12cos cos 223232ABD S AB r A A ⎡⎤⎤⎛⎫⎛⎫=⋅=⨯⨯--=-- ⎪ ⎪⎢⎥⎝⎭⎝⎭⎣⎦⎦ 23π3cos 333A ⎛⎫=-- ⎪⎝⎭,π3cos ,33333A ⎛⎛⎫∴--∈ ⎪ ⎝⎭⎝⎦,所以三角形面积的取值范围为3,33⎛ ⎝⎦.22.定义非零向量(),OM a b = 的“相伴函数”为()()sin cos f x a x b x x =+∈R ,向量(),OM a b = 称为函数()()sin cos f x a x b x x =+∈R 的“相伴向量”(其中O 为坐标原点).记平面内所有向量的“相伴函数”构成的集合为S .(1)设()()ππ3cos 63h x x x x ⎛⎫⎛⎫=++-∈ ⎪ ⎪⎝⎭⎝⎭R ,请问函数()h x 是否存在相伴向量OM ,若存在,求出与OM共线的单位向量;若不存在,请说明理由.(2)已知点(),M a b 满足:10,2b a ⎛⎤∈ ⎥⎝⎦,向量OM 的“相伴函数”()f x 在0x x =处取得最大值,求0tan2x 的取值范围.【答案】(1)存在,13,22⎛-- ⎝⎭或13,22⎛⎫ ⎪ ⎪⎝⎭(2)[4,0)3-【解析】【分析】(1)利用和差角公式化简函数()h x ,结合所给定义得到“相伴向量”)OM =,再求出与其共线的单位向量;(2)依题意可得()sin cos f x a x b x =+,再由辅助角公式化简,从而得到01tan tan x ϕ=,再根据b a的范围求出tan ϕ的范围,最后根据二倍角公式及函数的性质计算可得.【小问1详解】存在,1,22⎛⎫-- ⎪ ⎪⎝⎭或1,22⎛⎫ ⎪ ⎪⎝⎭.因为()ππ3cos 63h x x x ⎛⎫⎛⎫=++- ⎪ ⎪⎝⎭⎝⎭ππππcos cos sin sin3cos cos sin sin6633x x x x⎫⎛⎫=-++⎪ ⎪⎭⎝⎭ππππcos sin3cos cos3sin sin6633x x x x=-++33cos sin sin cos3cos2222x x x x x x=-++=+,所以函数()h x存在“相伴向量”)OM=,所以与OM共线的单位向量为)1,22OMOM⎛⎫== ⎪⎪⎝⎭或)1,22OMOM⎛⎫-==--⎪⎪⎝⎭.【小问2详解】(),OM a b=的“相伴函数”()()sin cosf x a x b x xϕ=+=+(其中tanbaϕ=),因为()f x在x x=处取得最大值,所以当0π2π,Z2x k kϕ+=+∈,即π2π,Z2x k k-ϕ=+∈时()f x,所以0πsin sin2πcos2x k-ϕϕ⎛⎫=+=⎪⎝⎭,0πcos cos2πsin2x k-ϕϕ⎛⎫=+=⎪⎝⎭,所以0cos1tansin tanxϕϕϕ==,因为1tan0,2baϕ⎛⎤=∈ ⎥⎝⎦,[)12,tanϕ∈+∞,所以[)cos1tansin tan2,xϕϕϕ∈==+∞,所以022tan2tan211tan tantanxxx xx==--,令0tant x=,[)2,t∈+∞,则011tantanx tx t-=-,因为1,y y tt==-均为[)2,+∞上的单调递减函数,所以1y t t =-在[)2,+∞上单调递减,所以00113tan ,tan 2x t x t ⎛⎤-=-∈-∞- ⎥⎝⎦,所以0020002tan 24tan 2,011tan 3tan tan x x x x x ⎡⎫==∈-⎪⎢-⎣⎭-,所以0tan 2x 的取值范围为4,03⎡⎫-⎪⎢⎣⎭.。
广西南宁市第三中学2023-2024学年高一下学期期末考试物理试卷

广西南宁市第三中学2023-2024学年高一下学期期末考试物理试卷一、单选题1.下列物理量属于标量的是( )A .动能B .动量C .速度D .冲量2.如图所示,足够长的光滑斜面A 静止在光滑水平面上,现物块B 以某一初速度冲上斜面,在物块B 从斜面底端冲到斜面最高点的过程中,对A 、B 组成的系统,下列说法正确的是( )A .动量守恒,机械能守恒B .动量守恒,机械能不守恒C .动量不守恒,机械能守恒D .动量不守恒,机械能不守恒3.如图所示,某小船船头垂直河岸渡河,已知该段河宽300m ,河水流速13m /s v =,船在静水中的速度25m /s v =,下列说法确的是( )A .小船做曲线运动B .小船渡河所用时间为60sC .小船的速度大小为4m /sD .小船渡河的位移大小为300m 4.如图所示,长1.6m 、一端固定有一质量为2kg 小球的轻杆绕O 点在竖直平面内做圆周运动,a 点为运动轨迹的最低点、b 为最高点,已知小球经过b 点时的速率为23m /s,10m /s g =。
下列说法正确的是( )A .小球经过b 点时受杆的作用力为零B .小球经过b 点时受杆的作用力竖直向下C .小球经过aD .小球经过a 点时的速率为8m /s5.一质量为m 的物块,在水平拉力F 的作用下从静止开始沿水平面运动,其阻力f 为物块重力的λ倍,水平拉力的大小F kx f =+,其中k 为比例系数,x 为物块运动的距离。
在物块运动的距离为s 的过程中拉力做的功为( )A .mgs λB .212ksC .()212ks mgs λ+D .212ks mgs λ+ 6.日常生活中常用高压水枪清洗汽车,某高压水枪喷口直径为D ,喷出水流的流速为v ,水柱垂直射向汽车表面后速度变为零。
已知水的密度为ρ。
下列说法正确的是( ) A .高压水枪单位时间内喷出的水的体积为2D v πB .高压水枪单位时间内喷出的水的质量为214D v ρ C .水柱对汽车的平均冲力为2214πρv D D .若高压水枪喷口的出水速度变为原来的2倍,则水柱对汽车的平均冲力为原来的2倍7.如图甲所示,足够长的水平传送带始终以恒定速率1v 运行,一质量为1kg m =、水平初速度大小为2v 的小物块,从与传送带等高的光滑水平面上的A 处滑上传送带;若从小物块滑上传送带开始计时,小物块在传送带上运动的v t -图像(以地面为参考系)如图乙所示,210m /s g =。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
广西南宁市2016-2017学年高一化学下学期期中试题理(共100分,考试时间90分钟)可能用到的相对原子质量:H-1 N-14 O-16 Fe-56 Cu-64一、选择题(每小题只有一个正确答案。
每小题2分,共44分)1.下列说法中正确的是()A.通常元素的化合价与其原子的质量数有密切的关系B.已知铱的一种核素是19177Ir,则其核内的中子数是114C.146C和147N的质量数相同,但质子数不同,所以互称为同位素D.任何元素的原子都是由核外电子和核内中子、质子组成的2.元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语。
下列有关化学用语的表示方法中正确的是()A.硫原子的原子结构示意图:B.NH4Cl的电子式:C.原子核内有10个中子的氧原子:188OD.用电子式表示氯化氢分子的形成过程:3.某元素的原子的最外层电子数是次外层的a倍(a>1),则该原子核内质子数是()A.2a B.a+2 C.2a+10 D.2a+24.元素的性质呈周期性变化的根本原因是()A.元素的相对原子质量的递增B.元素的原子半径呈周期性变化C.元素的原子核外电子排布呈周期性变化D.元素的金属性和非金属性呈周期性变化5.下列化学反应中起固氮作用的是()A.雷电使氮气和氧气反应生成了一氧化氮气体B.一氧化氮与氧气反应生成二氧化氮C.氨气经催化氧化生成一氧化氮D.由氨气制碳酸氢氨和硫酸氨6.右图中每条折线表示周期表ⅣA~ⅦA中某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是()A.SiH4B.HClC.PH3 D.H2S7.化学与生产、生活、社会密切相关,下列有关说法中正确的是()A.二氧化硫有毒,严禁将其添加到任何食品和饮料中B.古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中提取青蒿素是利用氧化还原反应原理C.面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为2∶1D.用K2FeO4代替Cl2处理饮用水,有杀菌消毒作用,但与氯气不同的是不产生有机氯对人体造成危害8.下列由相关实验现象所推出的结论正确的是()A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42﹣C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水9.下列各组物质中,化学键全部为共价键的是()A.NH4Cl、CO2、HCl B.O2、KF、SO2C.HCl、CH3COOH、CH4 D.Na2O2、N2、H2O10.含硒(Se)的保健品已开始进入市场。
已知硒与氧同主族,与钾同周期,则下列关于硒的叙述中,正确的是()A.非金属性比硫强B.氢化物比HBr稳定C.原子序数为34 D.最高价氧化物的水化物显碱性11.同主族元素形成的同一类型化合物,往往其结构和性质相似。
化合物PH4I是一种无色固体,下列对它的描述正确的是()A.它是一种共价化合物B.在加热条件下能稳定存在C.它能与NaOH溶液反应D.该化合物中每个原子都能满足8电子稳定结构12.下列事实与氢键有关的是()A.水加热到很高的温度都难以分解B.冰的密度小于水的密度C.钠投入盐酸溶液中比在水中反应剧烈D.HF、HCl、HBr、HI的热稳定性依次减弱13.设N A为阿伏加德罗常数的值,下列说法正确的是()A.标准状况下,每生成2.24 L O2,转移的电子数一定为0.4N AB.27g铝中加入1mol/L的NaOH溶液,转移电子数是3N AC.标准状况下,22.4L SO3所含的分子数为N AD.钾在空气中燃烧可生成多种氧化物,1mol钾充分燃烧时转移电子数为1N A14.下列陈述正确并且有因果关系的是( )15.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。
仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )16.“NaCl+CO 2+NH 3+H 2O=NaHCO 3↓+NH 4Cl”是著名的“侯氏制碱法”的重要反应。
下面是4位同学对该反应涉及的有关知识发表的部分见解。
其中不正确...的是( ) A .该条件下NaHCO 3的溶解度较其它盐要小 B .NaHCO 3不是纯碱C .析出固体后的溶液为NaHCO 3的不饱和溶液D .从该反应可以获得氮肥17.下列变化一定有旧的化学键断裂,新的化学键形成的是( )A .将氯化钠固体加热到熔融状态产生Na +和Cl ﹣B .将碘单质加热升华C .将氯化氢气体通入水产生H +和Cl ﹣D .在放电条件下氧气转化为臭氧18.已知短周期元素的离子:a A 2+、b B +、c C 3-、d D -都具有相同的电子层结构,则下列叙述不正确的是( )A .原子半径B >A >C >D B .原子序数d +1=b -1C.离子半径C3->D->B+>A2+D.单质的还原性A>B>D>C19.根据下表信息,判断以下叙述正确的是()A.M与T形成的化合物具有两性 B.单质与稀盐酸反应的剧烈程度为L<Q C.氢化物的热稳定性为H2T<H2R D.氢化物的沸点为H2T<H2R20.制备NH4Fe(SO4)2·12H2O的实验中,需对过滤出产品的母液(酸性)进行处理。
常温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是()A.通入过量SO2:Fe2+、H+、NH4+、SO42-B.加入过量NaOH溶液:Na+、NH4+、OH-、SO42-C.加入过量KSCN溶液:K+、SO42-、H+、Fe3+D.加入过量Na2SO3和NaOH混合溶液:Na+、Fe2+、SO42-、OH-21.短周期元素X、Y的原子序数相差2,下列叙述正确的是()A.X与Y不可能位于同一周期B.X与Y不可能形成原子个数比为1:1的离子化合物C.X离子与Y离子电子层结构可以相同,也可以不同D.X与Y形成的共价化合物中,各原子最外层一定满足8电子的稳定结构22.X、Y、Z 三种短周期元素,原子半径的大小关系为:r(Y)>r(X)> r(Z),原子序数之和为16。
X、Y、Z 三种元素的常见单质在适当条件下可发生如图所示变化,其中B 和C 均为10 电子分子。
下列说法不正确的是()A.X 元素位于ⅥAB.A 不能溶解于B 中C.B 的沸点高于C 的沸点D.A 和C 不可能发生氧化还原反应二、填空题(共56分)23.(12分)按要求填空。
(1)下列物质中属于同位素的是__________;属于同素异形体的是__________。
A.O2、O3B.3717Cl和3517ClC.Fe2+、Fe3+D.H2O、D2O、T2O(2)据报道,某些花岗岩会产生放射性的稀有气体氡,从而对人体产生伤害,请将以下Rn的原子结构示意图补全。
(3)下列四种物质中①Ar,②CO2,③K2S,④NaOH,只有存在共价键的物质是___;(填编号)用电子式表示③的形成过程:__________。
(4)硅酸盐的组成比较复杂,常用氧化物的形式表示。
石棉Mg3Ca(SiO3)4表示为氧化物形式为:__________。
(5)若K37ClO3+6H35C1===KCl+3Cl2↑+3H2O,则此反应中生成氯气的相对分子质量约为_________(计算结果保留三位有效数字)。
(6)将NaHSO4溶于水,破坏了NaHSO4中的______(填化学键类型),NaHSO4在熔融状态下电离,破坏了______(填化学键类型),写出其在熔融状态下的电离方程式_____________。
24.(10分)如图表示几种无机物之间的转换关系。
其中A、B均为黑色粉末,B为非金属单质,C为无色无毒气体,D为金属单质,E是红棕色气体,G是具有漂白性的气体,H的水溶液呈蓝色。
请回答下列问题:(1)A的化学式是,C的电子式是,Y的名称是.(2)反应①的化学方程式为.(3)19.2g的D与足量的一定浓度X的溶液反应,将所得到的气体与L O2(标准状况下)混合,恰好能被水完全吸收。
25.(13分)为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:(1)装置B中盛放的试剂是(填选项),实验现象为,化学反应方程式是。
A.Na2S溶液B.Na2SO3溶液C.Na2SO4溶液(2)装置C中盛放烧碱稀溶液,目的是。
(3)从该实验的现象得出氯元素比硫元素非金属性强的依据为。
(填序号)①氯原子比硫原子更容易获得电子形成离子;②次氯酸的氧化性比稀硫酸强;③S2﹣比Cl﹣还原性强;④HCl比H2S稳定。
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现的实验现象是,写出反应的离子方程式。
26.(8分)X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。
X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:(1)五种元素原子半径由大到小的顺序是(写元素符号)__________________________。
(2)X与Y能形成多种化合物,其中相对分子质量最小的分子中只含有_________ 键(填“离子”、“极性”或“非极性”)。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。
写出D的电子式:________。
如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。
由A转化为B的离子方程式为__________________________________________________。
27.(13分)X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,一般情况下X的单质只有氧化性:(1)写出实验室制取W2反应的离子方程式:。
(2)某小组设计如图所示的实验装置(图中夹持和加热装置略去),分别研究YX2、W2的性质。
①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”、“不相同”);若装置D中装的是铁粉,当通入W2时D中观察到的现象为;若装置D 中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学方程式为。
②若装置B中装入5.0mL 1.0×10﹣3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10﹣5mol电子,则该反应的化学方程式为。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母)可以看到白色沉淀生成。
