高一化学元素周期表知识精讲.doc
元素周期表知识精讲

一、元素周期表的结构(一)编排三原则:1. 按原子序数递增顺序从左到右排列。
2. 将电子层数相同的元素排列成一个横行。
3. 把最外电子层的电子数相同的元素按电子层数递增的顺序由上而下排列成纵行。
(二)周期:具有相同电子层数的元素按照原子序数递增的顺序排列的一行,叫周期。
(1)周期序数= 电子层数。
周期序数用阿拉伯数字表示。
(2)元素周期表目前有7个周期。
第1、2、3周期称为短周期,分别含有2、8、8种元素;第4、5、6、7周期称为长周期,分别含有18、18、32、26种元素;第7周期又称为不完全周期。
(三)族(1)元素周期表有18个纵行,称为族,共16个族。
族序数用罗马数字表示。
(2)元素周期表中含有7个主族(ⅠA族~ⅦA族)、7个副族(ⅢB族~ⅦB族、ⅠB族~ⅡB族)、1个第Ⅷ族(三个纵行)和1个0族(稀有气体)。
(3)主族元素族序数= 最外层电子数。
(4)稀有气体元素化学性质不活泼,很难与其他物质发生化学反应,把它们的化合价定为0,因而叫做0族。
二、元素的性质与元素在周期表中位置的关系(一)元素的金属性和非金属性与元素在周期表中位置1、同周期从左到右,元素的金属性减弱,非金属性增强。
2、同主族从上至下,元素的金属性增强,非金属性减弱。
3、(1(2域;(312、主族元素化合价的判断。
(1)元素最高正化合价的数值=族的序数=最外电子层电子数(即价电子数)(2)非金属元素最低负化合价的绝对值=8-其最高正化合价三、元素周期律和元素周期表的意义1869年,门捷列夫发现了元素周期律,并编制了第一张元素周期表。
元素周期表是学习研究的一种重要工具。
门捷列夫用元素周期律预言了未知元素,为发现新元素提供了线索。
元素周期律与元素周期表可以指导工农业生产。
【典型例题】[例1] 对比下列两组元素性质:(1)下列各组元素最高价氧化物对应的水化物碱性逐渐减弱、酸性逐渐加强的是( )A. NaOH 、2)(OH Mg 、43PO H 、42SO HB. KOH 、NaOH 、42SO H 、4HClOC. 2)(OH Ca 、2)(OH Ba 、4HBrO 、4HClOD. 2)(OH Mg 、2)(OH Ba 、43PO H 、42SO H(2)下列各组气态氢化物稳定性由强到弱的顺序正确的是( )A. 4SiH 、3PH 、S H 2、HClB. HF 、HCl 、HBr 、HIC. 3PH 、S H 2HCl 、HFD. 3NH 、3PH 、3AsH 、HF精析:(1)A 项第三周期的Na 、Mg 、P 、S 四元素最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强。
2024版新教材高中化学第1章原子结构元素周期律第2节元素周期律和元素周期表第2课时元素周期表知识小

第2课时元素周期表知识点1 元素周期表1.元素周期表与元素周期律的关系:元素周期表是元素周期律的具体表现形式,是学习和研究化学科学的重要工具。
2.元素周期表方格中的信息:通过元素周期表可了解元素的信息。
例如:3.元素周期表的编排原则:(1)横行:________相同的元素,按原子序数递增的顺序从左到右排列。
(2)纵列:最外层电子数相同的元素,按________递增的顺序自上而下排列。
4.元素周期表的结构:(1)周期:元素周期表有________个横行,即有________个周期。
①短周期:第1、2、3周期,每周期所含元素的种类数分别为__________、__________、__________。
②长周期:第4、5、6、7周期,每周期所含元素的种类数分别为__________、__________、__________、__________。
列数 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18类别主族副族Ⅷ族副族主族0族名称ⅠAⅡAⅢBⅣBⅤBⅥBⅦBⅧ族ⅠBⅡBⅢAⅣAⅤAⅥAⅦA族②副族,共7个(只由长周期元素组成,族序数后标B)。
③第Ⅷ族,包括________、________、________三个纵行。
④0族,最外层电子数是8(He是2)。
(3)过渡元素元素周期表中从第3到12列共10个纵列,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为________元素,统称为过渡元素。
5.元素周期表结构巧记口诀横行叫周期,现有一至七,四长三个短,第七已排满。
纵列称为族,共有十六族,一八依次现,一零再一遍。
一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。
镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。
说明:“一八依次现”指ⅠA、ⅡA、ⅢB、ⅣB、VB、ⅥB、ⅦB、Ⅷ族;“一零再一遍”指ⅠB、ⅡB、ⅢA、ⅣA、VA、ⅥA、ⅦA、0族。
知识点2 原子结构与元素在周期表中的位置关系1.元素周期表中的部分重要元素:族元素性质存在ⅡA族元素(碱土金属元素) ____、____、____、锶(Sr)、钡(Ba)、镭(Ra)①物理共性:单质都呈____色,具有良好的____②化学共性:单质呈强还原性,R—2e-→____在自然界中都以____存在VA族____、____、____、锑(Sb)、铋(Bi)等________为非金属元素,________为金属元素在自然界中以化合态或游离态存在副族和Ⅷ族(过渡元素) 第________列全部为金属元素,具有良好的____性2.焰色试验:(1)定义:某些________________在灼烧时使火焰呈现特殊颜色的反应,如钠:黄色,钾:________色。
高一化学人教版2019必修第一册 4.2元素周期律 (知识点)
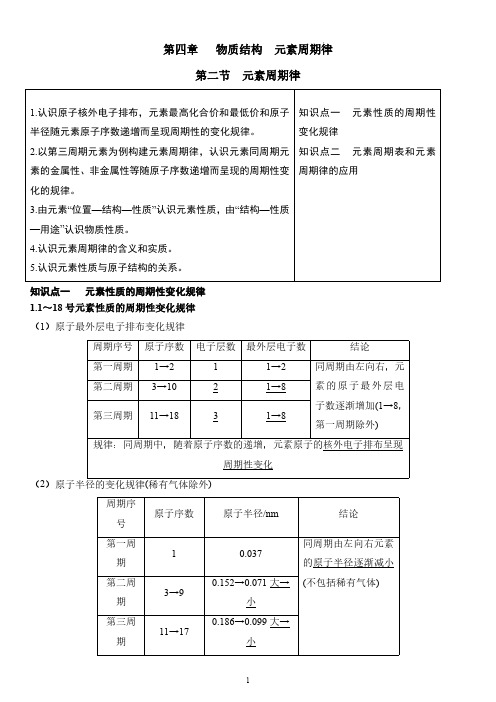
第四章物质结构元素周期律第二节元素周期律1.认识原子核外电子排布,元素最高化合价和最低价和原子半径随元素原子序数递增而呈现周期性的变化规律。
2.以第三周期元素为例构建元素周期律,认识元素同周期元素的金属性、非金属性等随原子序数递增而呈现的周期性变化的规律。
3.由元素“位置—结构—性质”认识元素性质,由“结构—性质—用途”认识物质性质。
4.认识元素周期律的含义和实质。
5.认识元素性质与原子结构的关系。
知识点一元素性质的周期性变化规律知识点二元素周期表和元素周期律的应用知识点一元素性质的周期性变化规律1.1~18号元素性质的周期性变化规律(1)原子最外层电子排布变化规律(2周期序号原子序数原子半径/nm结论第一周期10.037同周期由左向右元素的原子半径逐渐减小(不包括稀有气体)第二周期3→90.152→0.071大→小第三周期11→170.186→0.099大→小规律:同周期中,随着原子序数的递增,元素的原子半径呈现周期性变化3.元素的主要化合价周期序号原子序数主要化合价结论第一周期1→2+1→0①同周期由左向右,元素的最高正价逐渐升高(+1→+7,O和F无最高正价);②元素的最低负价由第ⅣA族的-4价逐渐升高至第ⅦA族的-1价;③最高正价+|最低负价|=8第二周期3→9最高价+1→+5(不含O、F)最低价-4→-1第三周期11→17最高价+1→+7最低价-4→-1规律:同周期中,随着原子序数的递增,元素的主要化合价呈现周期性变化4.实验探究:金属性的递变规律(1)Na、Mg元素金属性强弱比较原理金属与水反应置换出H2的难易程度操作现象镁条表面附着少量气泡剧烈反应,溶液变成浅红色化学反应-Mg+2H2OMg(OH)2+H2↑结论结合Na与水的反应的现象,Na与水反应置换H2比Mg 容易,则金属性:Na>Mg(2)Mg、Al元素金属性强弱比较原理金属的最高价氧化物对应水化物的碱性强弱物质Al(OH)3Mg(OH)2操作现象A 中沉淀溶解B 中沉淀溶解C 中沉淀溶解D 中沉淀不溶解A 、B 、C 、D 试管中的离子方程式A :Al(OH)3+3H +===Al 3++3H 2O B :Al(OH)3+OH -===AlO -2+2H 2OC :Mg(OH)2+2H +===Mg 2++2H 2OD :不反应结论Al(OH)3是两性氢氧化物,其碱性弱于Mg(OH)2(中强碱),更弱于NaOH(强碱),则金属性:Na>Mg>Al5.非金属性的递变规律6.元素周期律(1)内容:元素的性质随着原子序数的递增而呈周期性的变化。
高一化学知识点元素周期表

高一化学知识点元素周期表高一化学知识点:元素周期表元素周期表是化学中一项重要的工具,由化学家门捷列夫于1869年首次提出并发表。
它是将元素按照一定的规律组织和排列,使我们可以系统地了解元素的性质、原子结构、化合价和周期性规律等方面的知识。
本文将对元素周期表的基本结构、元素的周期性和分类进行介绍。
一、元素周期表的基本结构元素周期表通常采用长表式和简化式两种形式。
长表式将元素按照原子序数逐个排列,同时标注着元素的符号、相对原子质量和元素名。
而简化式则将元素按照一定的规律分组,以便更好地显示元素的周期性特征。
在元素周期表中,元素的横行称为周期,竖列称为族。
元素周期表中的水平行称为主周期,而在主周期下方的两行称为辅周期。
每个周期中的元素按照递增的原子序数排列,且性质呈现出周期性变化。
二、元素的周期性和分类元素周期表的主要价值在于揭示了元素之间的周期性规律。
根据这些规律,我们可以预测元素的性质和元素之间的化学反应。
元素周期表中,元素按照性质的周期性变化划分为不同的区域,如金属区、非金属区和类金属区等。
其中金属区域包括一至三族元素,具有良好的导电性和导热性。
而非金属区域包括氢、卤素和稀有气体等元素,具有不良的导电性和导热性。
类金属区则处于金属和非金属的过渡地带,具有介于两者之间的性质。
此外,元素周期表中还存在着一些特殊的元素,如稀有气体、过渡金属和内过渡金属等。
稀有气体位于元素周期表的最后一族,具有低反应性。
过渡金属位于元素周期表的四至十一族,具有多种化合价和复杂的反应性。
内过渡金属则位于元素周期表的下方两行,具有较强的金属性质。
三、元素周期表中的重要概念在学习元素周期表时,需要了解一些重要的概念,如周期性、原子半径、电子亲和力和电负性等。
周期性是指元素在元素周期表中性质随周期变化的规律。
例如,原子半径随周期增加而减小,电子亲和力随周期增加而增大。
而电负性是指元素对共价键中电子的吸引能力,是描述化学键极性差异的重要指标。
高中化学元素周期律知识点总结

高中化学元素周期律知识点总结-CAL-FENGHAI.-(YICAI)-Company One1第一节课时1元素周期表的结构一、元素周期表的发展历程二、现行元素周期表的编排与结构1.原子序数(1)含义:按照元素在元素周期表中的顺序给元素编号,得到原子序数。
(2)原子序数与原子结构的关系原子序数=核电荷数=质子数=核外电子数。
2.元素周期表的编排原则(1)原子核外电子层数目相同的元素,按原子序数递增的顺序从左到右排成横行,称为周期。
(2)原子核外最外层电子数相同的元素,按电子层数递增的顺序由上而下排成纵行,称为族。
3.元素周期表的结构(1)周期(横行)①个数:元素周期表中有7个周期。
②特点:每一周期中元素的电子层数相同。
③分类(3短4长)短周期:包括第一、二、三周期(3短)。
长周期:包括第四、五、六、七周期(4长)。
(2)族(纵行)①个数:元素周期表中有18个纵行,但只有16个族。
②特点:元素周期表中主族元素的族序数等于其最外层电子数。
③分类④常见族的特别名称 第ⅠA 族(除H):碱金属元素;第ⅦA 族:卤族元素;0族:稀有气体元素;ⅣA 族:碳族元素;ⅥA 族:氧族元素。
课时2 元素的性质与原子结构一、碱金属元素——锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr) 1.原子结构(1)相似性:最外层电子数都是__1__。
(2)递变性:Li ―→Cs ,核电荷数增加,电子层数增多,原子半径增大。
2.碱金属单质的物理性质3.碱金属元素单质化学性质的相似性和递变性 (1)相似性(用R 表示碱金属元素)单质R —⎩⎪⎨⎪⎧与非金属单质反应:如Cl 2+2R===2RCl 与水反应:如2R +2H 2O===2ROH +H 2↑与酸溶液反应:如2R +2H +===2R ++H 2↑化合物:最高价氧化物对应水化物的化学式为ROH ,且均呈碱性。
(2)递变性具体表现如下(按从Li→Cs 的顺序)①与O 2的反应越来越剧烈,产物越来越复杂,如Li 与O 2反应只能生成Li 2O ,Na 与O 2反应还可以生成Na 2O 2,而K 与O 2反应能够生成KO 2等。
化学元素周期表高一知识点

化学元素周期表高一知识点化学元素周期表是化学中基本的工具之一。
它按照元素的原子序数(也称为元素的序数)和元素的电子结构来排列元素。
每个元素都具有唯一的原子序数,而且每个元素都有一组特定的化学性质。
周期表的布局:周期表通常被划分为若干个主要部分,包括主族元素(也称为A族元素)和过渡元素(也称为B族元素)。
主族元素是周期表的左侧,包括1A族到8A族元素,过渡元素则位于周期表的中心部分。
此外,周期表还包括稀有气体元素(8A族的最后一列)和镧系和锕系元素(通常放在底部的两行)。
元素符号:每个元素都用一个或两个字母的符号来表示,这些符号通常是元素名称的缩写。
例如,氧元素的符号为O,氢元素的符号为H。
这种符号体系使元素名字的表达更加简洁和方便记忆。
原子序数和电子结构:元素的原子序数表示了元素中原子的数目。
根据元素的原子序数,可以知道元素在周期表中的位置。
每个元素的电子结构描述了其外层电子的排布方式。
电子结构对于确定元素的化学性质和反应行为非常重要。
周期表中的周期性:元素周期表的主要特点是周期性。
周期性表现在元素的化学性质以及与元素位置相关的一系列属性上。
周期表中相邻元素的电子结构和性质有相似之处,形成了垂直和水平上的周期性规律。
周期表中的元素分类:根据元素的一些特定属性,可以将元素进一步分类。
主要的分类包括金属(包括碱金属、碱土金属、过渡金属等)、非金属和类金属等。
这些分类有助于我们对元素的特征和性质有更清晰的认识。
周期表的拓展:随着科学的发展,科学家们继续发现新的元素。
新发现的元素被添加到现有的周期表中,丰富了我们对元素的认识。
周期表的拓展使我们能够更好地研究和理解元素以及它们之间的相互关系。
结语:化学元素周期表是化学研究中不可或缺的工具。
通过对周期表的学习,我们可以更好地理解元素的性质和行为规律。
同时,周期表也为我们提供了研究和应用各种元素的基础。
以上是关于化学元素周期表的一些高一知识点。
通过研究和掌握这些知识,我们可以更好地理解化学世界的奥秘。
高一化学元素周期律知识点

高一化学元素周期律知识点元素周期律是化学中重要的基础知识,它是按照原子核的电子结构和化学性质等规律性的变化,将元素有序地排列在一起的表格,可以为我们理解和记忆元素的性质提供便利。
下面将介绍高一化学中与元素周期律相关的几个重要知识点。
一、元素周期表的组成元素周期表是按照原子序数从小到大将元素排列在一起的表格。
它由横向的周期和纵向的族组成。
周期代表着元素原子核外层电子的能级,而族代表着元素原子核外层电子的数量。
二、元素周期表的周期规律1. 周期规律:元素周期表的横向周期呈现出一些规律性变化。
原子半径随周期增加而减小,电离能、电负性和原子的氧化态也呈现出周期性变化。
这些规律的存在,使我们能够根据元素在周期表中的位置推测其性质。
2. 原子半径的变化:从左到右,原子半径逐渐减小,原因是电子层不断填充,核电荷也逐渐增加,吸引外层电子的能力增强;从上到下,原子半径逐渐增大,原因是电子层增加,外层电子与原子核的吸引力减小。
3. 电离能的变化:从左到右,原子的电离能逐渐增加,即元素更难失去电子形成正离子;从上到下,原子的电离能逐渐减小,即元素较容易失去电子。
4. 电负性的变化:从左到右,原子的电负性逐渐增加,即元素更容易接受电子形成负离子;从上到下,原子的电负性逐渐降低,即元素较不容易接受电子。
三、元素周期表中的主要族元素周期表中的主要族包括:1. 碱金属族:位于周期表的第一组,具有非常活泼的金属性质,易与氧气和水反应。
2. 碱土金属族:位于周期表的第二组,比碱金属更活泼,但比较稳定。
3. 铁系过渡族:位于周期表中间,具有良好的导电性、机械性能和催化性能。
4. 卤素族:位于周期表的第七组,非常活泼,常以阴离子形式存在。
5. 惰性气体:位于周期表的第八组,具有极低的反应性,稳定性极高。
四、元素周期表的应用元素周期表的应用十分广泛,主要包括以下几个方面:1. 元素性质预测:根据元素在周期表中的位置,可以预测其一些基本性质,如电子亲和力、电离能等。
高一化学元素周期表知识精讲

高一化学元素周期表【本讲主要内容】元素周期表元素周期表中主族元素性质的递变规律、原子结构、元素性质及元素在周期表中位置三者的关系、元素周期表的结构及应用、元素的推断等。
其中元素周期表的结构及应用是学习的重点。
【知识掌握】【知识点精析】二. 原子结构、元素性质及元素在周期表中位置三者的关系主族序数质子数原子半径1.同周期左右:非金属性增强。
2.同主族上下:化学性质相似,但又有递变。
1. 原子结构与元素在周期表中的位置关系:(1)核外电子层数=周期数(2)主族元素的最外层电子数=价电子数=主族序数=最高正价数(3)质子数=原子序数=原子核外电子数=核电荷数(4)负价绝对值=8-主族数(限ⅣA~ⅦA)(5)原子半径越大,失电子越易,还原性越强,金属性越强,形成的最高价氧化物的相应水化物碱性越强,其离子的氧化性越弱。
(6)原子半径越小,得电子越易,氧化性越强,非金属性越强,形成的气态氢化物越稳定,形成最高价氧化物的相应水化物酸性越强,其离子的还原性越弱。
2. 周期表与电子排布(1)最外层电子数等于或大于3(小于8)的一定是主族元素。
(2)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素又可能是副族或零族元素氦。
(3)最外层电子数比次外层电子数多的元素一定位于第二周期。
(4)某元素阴离子最外层电子数与次外层相同,该元素位于第三周期。
(5)电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期。
3. 从元素周期表归纳元素化合价的规律(1)主族元素的最高正价数等于主族序数,等于主族元素原子的最外层电子数,其中氟无正价。
非金属元素除氢外,均不能形成简单阳离子,金属元素不能形成简单阴离子。
(2)主族元素的最高正价数与最低负价数的绝对值之和为8,绝对值之差为0、2、4、6的主族依次为ⅣA、ⅤA、ⅥA、ⅦA族。
(3)非金属元素的正价一般相差2,如氯元素正化合价有+7、+5、+3、+1等,某些金属也符合此规律,如锡元素正化合价有+4、+2价(4)短周期正价变化随原子序数递增,同周期有一个+1到+7价的变化(ⅠA~ⅦA);长周期有两个+1到+7价的变化(ⅠA~ⅦB,ⅠB~ⅦA)。
(完整版)高一化学元素周期表知识点总结,推荐文档

这五种元素的核电荷数之和可能是( C )
A 5Z+2
B 5Z+8 C 5Z+10 D 5Z+18
二、碱金属元素
⑴碱金属元素包括
;
⑵碱金属的化学性质:(由钠钾分别与氧气与水反应得出)
①相似性:碱金属元素原子的最外层都有
个电子,它们的化学性质相似,化合价都是
。
②递变性:随着核电荷数的增加,碱金属元素原子的电子层数逐渐
元素周期表结构
主族(1、2、13、14、15、16、17 列),族的序号一般用罗马数字+A 表示。
副族(3、4、5、6、7、11、12 列), 族的序号一般用罗马数字+B 表示。 族 零族(18 列)
第 VIII 族(8、9、10 列) 注意:①0 族不是主族,第 VIII 族不是副族
②主族:由短周期元素和长周期元素共同构成的族 副族:完全由长周期元素构成的族
四、元素、核素、同位素
(1)质量数:将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。
(1)颜色、状态:F2
Cl 2
Br 2
状态由气到固)
(2)熔沸点:逐渐
(3)密度:逐渐
3.卤素单质与氢气反应
名称
反应条件
(4)溶解性: 方程式
F2
H2+F2 2HF
Cl2
光照或点燃
H2+Cl2
1
C.钾与水反应比钠与水反应更剧烈
D.加热时,钾比钠更易汽化
四、卤族元素
1.卤素原子结构示意图:F
Cl
Br
I
最外层电子数均为
个,但电子层数逐渐增大,得电子能力
,非金属性
2.卤族元素单质的物理性质的变化规律。
高一化学《元素周期表-元素周期律》知识总结

高一化学《元素周期表 元素周期律》知识总结一、原子的结构1、原子的构成:。
2、原子结构中常见的微粒关系(1)原子:质量数=质子数+中子数;质子数=核电荷数=原子序数=核外电子数。
(2)离子的核外电子数:核外电子数⎩⎪⎨⎪⎧阳离子:质子数-电荷数阴离子:质子数+电荷数。
(3)符号baX +cd +e 中各数字的含义:。
二、元素、核素、同位素1、元素:具有相同核电荷数(即质子数)的同一类原子的总称。
2、核素:具有一定数目质子和一定数目中子的一种原子。
可用符号AZ X 表示。
3、同位素(1)概念:质子数相同而中子数不同的同一种元素的不同核素互称为同位素。
(2)特征:①具有相同存在形态的同位素,化学性质几乎完全相同。
②天然存在的同一元素各核素所占的原子百分数一般不变。
(3)有关同位素的四点说明①“同位”是指这几种核素的质子数(核电荷数)相同,在元素周期表中占据同一个位置。
②因许多元素存在同位素,故原子的种数多于元素的种数。
有多少种核素就有多少种原子。
但也并非所有元素都有同位素,如Na 、F 、Al 等就没有同位素。
③同位素分为稳定同位素和放射性同位素。
④同位素的中子数不同,质子数相同,化学性质几乎完全相同,物理性质差异较大。
三、核外电子排布1、排布方式:多电子原子核外的电子是分层排布的,即2、排布规律(1)电子一般总是首先排在能量最低的电子层里,即最先排在第1层,当第1层排满后,再排第2层,依次类推。
(2)每层最多容纳的电子数为2n2(n代表电子层数)。
(3)最外层电子数不超过8个(K层为最外层时,最多不超过2个),次外层不超过18个,倒数第3层不超过32个。
四、元素周期律1、定义:元素的性质随原子序数的递增而呈周期性变化的规律。
2、实质:元素原子核外电子排布周期性变化的结果。
3、元素周期表中元素的电子排布和化合价规律(1)从元素周期表归纳电子排布规律①最外层电子数等于或大于3(小于8)的一定是主族元素。
化学元素周期表精讲

化学元素周期表精讲引言:化学元素周期表是化学领域中最为重要的工具之一。
它以一种有序、系统的方式展示了所有已知的化学元素,为我们理解元素的性质和相互关系提供了基础。
本文将深入解析周期表的结构、元素的分类和周期规律,以及周期表在化学研究和应用中的重要性。
一、周期表的结构周期表的结构是由德国化学家门德莱夫于1869年首次提出的。
它由一系列水平排列的行和垂直排列的列组成。
每一行被称为一个周期,每一列被称为一个族或一个元素类别。
周期表的左侧是金属元素,右侧是非金属元素,而位于两者之间的是过渡金属元素。
二、元素的分类根据周期表的结构,我们可以将元素分为三大类:金属、非金属和半金属。
金属元素具有良好的导电性、热导性和延展性,常见的金属元素有铁、铜和铝等。
非金属元素则通常是不良导电体,如氧、氮和碳等。
半金属元素具有介于金属和非金属之间的特性,硅和锑就是典型的半金属元素。
三、周期规律周期表中的元素按照原子序数的增加顺序排列,这使得元素的周期性规律得以展现。
最为著名的周期规律是门德莱夫提出的原子半径和电子亲和能的周期性变化。
原子半径是指元素中心原子核到外层电子的平均距离,而电子亲和能则是指元素接受外层电子形成负离子时释放的能量。
这些规律的发现,为我们预测元素的性质和反应提供了重要线索。
四、周期表的应用周期表不仅仅是化学教育中的基础知识,它在化学研究和应用中也起着重要的作用。
首先,周期表为我们理解元素的周期性趋势提供了便利,帮助我们预测元素的性质和反应。
其次,周期表为元素的命名和符号提供了统一的规范,使得科学家们能够更好地交流和合作。
此外,周期表还为新元素的发现和研究提供了指导。
五、元素周期表的发展随着科学技术的不断进步,元素周期表也在不断发展和完善。
最初的周期表只包含了少数元素,随着新元素的发现,周期表的尺寸不断扩大。
目前,已经发现的元素有118个,这些元素都被纳入了现代周期表中。
此外,随着人们对元素性质的深入研究,有些元素的分类和性质也发生了变化,这促使周期表的更新和修订。
(新)高一化学必修一化学元素周期表(按章节归纳)

(新)高一化学必修一化学元素周期表(按章
节归纳)
第一章:绪论
- 科学研究的基本方法和手段
- 化学的定义和分类
- 化学元素及其符号的来源和命名
第二章:化学元素与元素周期表
- 原子的结构
- 元素的定义和分类
- 元素的周期性和周期表的构成
- 元素的分类和性质
第三章:周期律及元素周期表
- 元素周期律的发现
- 量子数和电子排布规律
- 元素的周期性规律和周期表的应用
- 周期表指标的解读和使用
第四章:原子结构与元素周期表
- 原子的结构和组成
- 原子半径的变化规律
- 原子的电离能和电子亲和能
第五章:化学键
- 化合价
- 共价键和离子键
- 价电子的变化
第六章:周期律与化学键
- 周期律与离子键能和晶体结构
- 周期律与共价键的极性和分子结构
第七章:离子及离子键
- 离子的定义和性质
- 离子键的性质和应用
第八章:元素周期表及化学键小结- 元素周期表的发展历程
- 难以归入现有分类的元素
- 化学键的研究方法和应用
这份文档按照《高一化学必修一》课本的章节归纳了化学元素周期表的相关内容。
通过学习这份文档,你将了解元素周期表的构成、元素的分类和性质、化学键的形成规律以及元素周期表在化学研究中的应用。
在学习化学的过程中,这份文档将会为你提供有关化学元素周期表的重要知识点和基本理论。
希望对你的学习有所帮助!。
[精]高中化学元素周期表知识点详解
![[精]高中化学元素周期表知识点详解](https://img.taocdn.com/s3/m/71e4f75527284b73f24250f0.png)
第一节元素周期表一.元素周期表的结构周期序数=核外电子层数主族序数=最外层电子数原子序数=核电荷数=质子数=核外电子数短周期(第1、2、3周期)周期:7个(共七个横行)周期表长周期(第4、5、6、7周期)主族7个:ⅠA-ⅦA族:16个(共18个纵行)副族7个:IB-ⅦB第Ⅷ族1个(3个纵行)零族(1个)稀有气体元素【练习】1.主族元素的次外层电子数(除氢)A.一定是8个B.一定是2个C.一定是18个D.是2个、8个或18个2.若某ⅡB族元素原子序数为x,那么原子序数为x+1的元素位于A.ⅢB族B.ⅢA族C.ⅠB族D.ⅠA族3.已知A元素原子的最外层电子数是次外层电子数的3倍,B元素原子的次外层电子数是最外层电子数的2倍,则A、B元素A.一定是第二周期元素B.一定是同一主族元素C.可能是二、三周期元素D.可以相互化合形成化合物二.元素的性质和原子结构(一)碱金属元素:1.原子结构相似性:最外层电子数相同,都为_______个递变性:从上到下,随着核电核数的增大,电子层数增多2.碱金属化学性质的相似性:点燃点燃4Li + O2 Li2O 2Na + O2 Na2O22 Na + 2H2O =2NaOH + H2↑ 2K + 2H2O =2KOH + H2↑2R + 2 H2O =2 ROH + H2 ↑产物中,碱金属元素的化合价都为+1价。
结论:碱金属元素原子的最外层上都只有_______个电子,因此,它们的化学性质相似。
3.碱金属化学性质的递变性:递变性:从上到下(从Li到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li到Cs的金属性逐渐增强。
结论:1)原子结构的递变性导致化学性质的递变性。
2)金属性强弱的判断依据:与水或酸反应越容易,金属性越强;最高价氧化物对应的水化物(氢氧化物)碱性越强,金属性越强。
高一化学必修一第一章第一节元素周期表

同种元素原子的原子核中质子数是相同的。 那么,中子数是否一定相同呢?
1 H 1 2 1
H
3 1H
氕 H 氢
氘 D 重氢
氚 T 超重氢
核素:具有一定数目的质子和一定数目的中子 的一种原子。 即一种原子就是一种核素。
1 H 1 2
1
H
3 H 各为一种核素 1
同位素:质子数相同而中子数不同的同一元素 的不同原子互称为同位素。 同一种元素的不同核素互称为同位素。
一、元素周期表
1. 编排原则: (1)按原子序数递增的顺序从左到右排成横行
(2)按电子层数递增的顺序从上而下排成纵行
一、元素周期表
2.元素周期表的结构:
第一周期:2 种元素 第二周期:8 种元素 第三周期:8 种元素 第四周期:18 种元素 第五周期:18 种元素 第六周期:32 种元素(含 镧系15种) 第七周期(不完全周期):26 种元素 (含 锕系15种)
★主族序数=最外层电子数
习题:
序号位置:
例1:试推测出第32号元素在周期表中的 位置。 分析:0族定位法。即根据与该元素原子 序数最接近的0族元素的位置来确定。
答案:第四周期 第ⅣA族。
原子结构示意图位置:
例2:写出下列元素在周期表的位置:
第 三 周期 第 ⅣA 族
第 二 周期 第 ⅥA 族
13 6 C-NMR(核磁共振)可以用于含碳化
元素相对原子质量的计算:
按各种同位素所占的一定百分 比算出的平均值
A=A1×a1%+A2×a2%+…
A1、A2: 同位素的相对原子质量 a1%、a2%: 同位素原子的个数分数 如
35Cl
——75% , 37Cl——25% 35×0.75+37×0.25=35.5 即:氯的原子量为35.5。(近似值)
高中化学元素周期表知识点详解

高中化学元素周期表知识点详解一、元素周期表概述1.1 元素周期表的定义元素周期表是根据元素的化学和物理性质,按照一定的规律将元素排列成表格状的一种定期系统,它是化学基础知识中最基本,最核心的内容之一。
1.2 元素周期表的历史元素周期表的历史可以追溯到1869年,当时俄国化学家门捷列夫根据元素的化学性质,提出了周期定律,并将元素按照周期性定律进行排列,从而形成了第一个元素周期表。
以后,随着科学技术的不断发展,元素周期表逐渐完善,不断更新。
1.3 元素周期表的基本结构现代元素周期表由7个水平排列的周期和18个垂直排列的族组成。
周期表中,从左至右,原子序数逐渐增加,元素的电子层数也逐渐增加;从上至下,主量子数逐渐增加,元素的原子半径也逐渐增加。
二、周期性规律2.1 周期性规律的概述周期性规律是指元素的物理和化学性质随着元素原子序数的增大而呈现出周期变化的规律。
周期性规律包括原子半径、电离能、电子亲和能、电负性等方面的规律。
2.2 原子半径的周期性规律原子半径是指原子中最外层电子所处的轨道半径。
原子半径的大小与原子核中质子数和电子数有关,原子半径随着电子层数的增大而逐渐增加。
另外,周期表中第一周期的原子半径最小。
2.3 电离能的周期性规律原子的电离能是指从原子中剥离一个电子所需要的最小能量。
电离能大小与原子核的质子数和电子云的结构有关,它随着电子层数的增大而逐渐减小。
周期表中第一周期的电离能最小。
2.4 电子亲和能的周期性规律电子亲和能是指向一个原子中引入一个电子时,所放出的能量。
电子亲和能大小与原子核的质子数和电子云的结构有关,它随着电子层数的增大而逐渐增加。
周期表中第一周期的电子亲和能最小。
2.5 电负性的周期性规律电负性是描述元素在化学反应中容易获得或失去电子的能力。
电负性大小与元素的原子结构有关,它随着电子的层数由内向外逐渐增加,即在周期表中,从左到右和从下到上电负性逐渐增大。
三、队列式周期表3.1 队列式周期表的概述队列式周期表是指按照元素的化学性质排列的周期表,多用于描述元素之间的化学反应。
高一化学知识点-元素周期表

高一化学知识点:元素周期表高一化学知识点:元素周期表一、元素周期表原子序数=核电荷数=质子数=核外电子数1、元素周期表的编排原则:①按照原子序数递增的顺序从左到右排列;②将电子层数相同的元素排成一个横行——周期;③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行——族2、周期序数=电子层数;主族序数=最外层电子数3、元素金属性和非金属性判断依据:①元素金属性强弱的判断依据:单质跟水或酸起反应置换出氢的难易;元素最高价氧化物的水化物——氢氧化物的碱性强弱;置换反应。
②元素非金属性强弱的判断依据:单质与氢气生成气态氢化物的难易及气态氢化物的稳定性;最高价氧化物对应的水化物的酸性强弱;置换反应。
4、核素:具有一定数目的质子和一定数目的中子的一种原子。
①质量数二二质子数+中子数:A==Z+N②同位素:质子数相同而中子数不同的同一元素的不同原子,互称同位素。
(同一元素的各种同位素物理性质不同,化学性质相同)二、元素周期律1、影响原子半径大小的因素:①电子层数:电子层数越多,原子半径越大(最主要因素)②核电荷数:核电荷数增多,吸引力增大,使原子半径有减小的趋向(次要因素)③核外电子数:电子数增多,增加了相互排斥,使原子半径有增大的倾向2、元素的化合价与最外层电子数的关系:最高正价等于最外层电子数(氟氧元素无正价)负化合价数=8—最外层电子数(金属元素无负化合价)3、同主族、同周期元素的结构、性质递变规律:同主族:从上到下,随电子层数的递增,原子半径增大,核对外层电子吸引能力减弱,失电子能力增强,还原性(金属性)逐渐增强,其离子的氧化性减弱。
七大方法助你告别化学“差生”一.尽快去找化学老师,让他告诉你以前学过的关键知识点,在短期内掌握,目的是能够大致跟上现在的教学进度,以听懂老师讲授的新知识。
要想进步,必须弄清楚导致化学成绩差的根本原因是什么?是常用的几个公式、概念没记住,还是很重要的几个基本解题方法不能熟练应用,或者是以前的一些重点知识没有理解透彻等等。
高一化学元素周期表

H 2
1
C 13
6
O 17
8
Cl 37
17
U 235
92
H 3
1
C 14 6
O 18 8
U 238 92
4、注意事项:
① 元素的种类由质子数决定,与中子数、核外电子数无关;
② 核素种类由质子数和中子数共同决定,与核外电子数无关;
③ 元素和核素只能论种类,不能论个数;而原子既论种类, 又能论个数;
④ 同一元素的各种核素虽然中子数(质量数)不同,但它们 的化学性质基本相同。
⑤ 天然存在的同位素,相互间保持一定的比率。元素的相对 原子质量,是按照该元素的各种核素原子所占的一定百分比 算出的平均值。
1、作核燃料:作制造核武器的动力性材料(235U) 2、金属探伤:利用γ射线的贯穿本领,可以检查金属内 部有没有沙眼和裂纹。 3、辐射育种:利用放射性同位素的射线对遗传物质产生 影响,提高基因突变频率,从而选育出优良品种。 4、临床治癌:利用放射性同位素的射线杀伤癌细胞或阻 止癌细胞分裂。 5、环保治污:利用放射性同位素的射线可消毒灭菌,杀 死各种病原体从而能保护环境是其少受污染。
2、核素:具有一定数目的质子和一定 数目的中子的一种原子。
3、同位素:质子数相同而中子数不同的 同一种元素的不同原子互称为同位素。 即:同一元素的不同核素之间互称为同位素
(1) Z同,N不同 (2)不同的原子
元素
核素1 … 核素n
同位素
H:
H1
1
C:
C 12
6
O:
O 16
8Байду номын сангаас
Cl:
Cl 35
17
U: U 234 92
精高中化学元素周期表知识点详解

第一节 元素周期表一.元素周期表的结构周期序数=核外电子层数 主族序数=最外层电子数原子序数 = 核电荷数 = 质子数 = 核外电子数短周期(第1、2、3周期)周期:7个(共七个横行)周期表 长周期(第4、5、6、7周期)主族7个:ⅠA-ⅦA族:16个(共18个纵行)副族7个:IB-ⅦB第Ⅷ族1个(3个纵行)零族(1个)稀有气体元素✓ 【练习】1.主族元素的次外层电子数(除氢)A .一定是8个B .一定是2个C .一定是18个D .是2个、8个或18个2.若某ⅡB 族元素原子序数为x ,那么原子序数为x +1的元素位于A .ⅢB 族 B .ⅢA 族C .ⅠB 族D .ⅠA 族3.已知A 元素原子的最外层电子数是次外层电子数的3倍,B 元素原子的次外层电子数是最外层电子数的2倍,则A 、B 元素A .一定是第二周期元素B .一定是同一主族元素C .可能是二、三周期元素D .可以相互化合形成化合物二.元素的性质和原子结构(一)碱金属元素:1.原子结构 相似性:最外层电子数相同,都为_______个递变性:从上到下,随着核电核数的增大,电子层数增多2.碱金属化学性质的相似性:4Li + O 2 Li 2O 2Na + O 2 Na 2O 22 Na + 2H 2O = 2NaOH + H 2↑ 2K + 2H 2O = 2KOH + H 2↑2R + 2 H 2O = 2 ROH + H 2 ↑产物中,碱金属元素的化合价都为+1价。
结论:碱金属元素原子的最外层上都只有_______个电子,因此,它们的化学性质相似。
3.碱金属化学性质的递变性:递变性:从上到下(从Li 到Cs ),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li 到Cs 的金属性逐渐增强。
结论:1)原子结构的递变性导致化学性质的递变性。
2)金属性强弱的判断依据:与水或酸反应越容易,金属性越强;最高价氧化物对应的水化物(氢氧化物)碱性越强,金属性越强。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高一化学元素周期表【本讲主要内容】元素周期表元素周期表中主族元素性质的递变规律、原子结构、元素性质及元素在周期表中位置三者的关系、元素周期表的结构及应用、元素的推断等。
其中元素周期表的结构及应用是学习的重点。
【知识掌握】【知识点精析】二. 原子结构、元素性质及元素在周期表中位置三者的关系主族序数原子半径1.同周期左右:非金属性增强。
2.同主族上下:化学性质相似,但又有递变。
1. 原子结构与元素在周期表中的位置关系:(1)核外电子层数=周期数(2)主族元素的最外层电子数=价电子数=主族序数=最高正价数(3)质子数=原子序数=原子核外电子数=核电荷数(4)负价绝对值=8-主族数(限ⅣA~ⅦA)(5)原子半径越大,失电子越易,还原性越强,金属性越强,形成的最高价氧化物的相应水化物碱性越强,其离子的氧化性越弱。
(6)原子半径越小,得电子越易,氧化性越强,非金属性越强,形成的气态氢化物越稳定,形成最高价氧化物的相应水化物酸性越强,其离子的还原性越弱。
2. 周期表与电子排布(1)最外层电子数等于或大于3(小于8)的一定是主族元素。
(2)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素又可能是副族或零族元素氦。
(3)最外层电子数比次外层电子数多的元素一定位于第二周期。
(4)某元素阴离子最外层电子数与次外层相同,该元素位于第三周期。
(5)电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期。
3. 从元素周期表归纳元素化合价的规律(1)主族元素的最高正价数等于主族序数,等于主族元素原子的最外层电子数,其中氟无正价。
非金属元素除氢外,均不能形成简单阳离子,金属元素不能形成简单阴离子。
(2)主族元素的最高正价数与最低负价数的绝对值之和为8,绝对值之差为0、2、4、6的主族依次为ⅣA、ⅤA、ⅥA、ⅦA族。
(3)非金属元素的正价一般相差2,如氯元素正化合价有+7、+5、+3、+1等,某些金属也符合此规律,如锡元素正化合价有+4、+2价(4)短周期正价变化随原子序数递增,同周期有一个+1到+7价的变化(ⅠA~ⅦA);长周期有两个+1到+7价的变化(ⅠA~ⅦB,ⅠB~ⅦA)。
三. 元素周期表的结构1. 周期元素周期表分7个周期,第一、二、三为短周期,元素种类依次为2、8、8;第四、五、六周期为长周期,元素种类依次为18,18,32;第七周期为不完全周期,目前有32种元素。
除第一周期外,每一周期的元素都是从碱金属开始,逐渐过渡到卤族元素,最后以稀有气体元素结束。
2. 族元素周期表中有18个纵行,分为16个族,其中7个主族、7个副族,还有1个零族和1个第Ⅷ族。
过渡元素包括全部副族和第Ⅷ族,都是金属,又称过渡金属。
除短周期外;族序数从左到右的顺序为:ⅠA→ⅡA→ⅢB→…ⅦB→Ⅷ→ⅠB→ⅡB→ⅢA →…→ⅦA→0族,前后从1→8更迭两次。
金属、非金属的分界线位于分界线附近的元素既能表现一定的金属性,又能表现出一定的非金属性。
如铝既能跟盐酸反应,也能跟NaOH溶液反应生成NaAlO2并放出H2。
周期表的左下方金属性最强的元素是(放射性元素除外)Cs,右上方非金属性最强的元素是F。
五. 元素、核素和同位素1. 概念辨析元素是具有相同核电荷数(即质子数)的同一类原子的总称。
元素的种类由质子数决定,与中子数、核外电子数无关。
如H和D+属于同种元素。
核素是核内具有确定数目质子和中子的原子。
核素的种类是由质子数和中子数共同决定的,与核外电子无关。
如Cl3517和-Cl3517是同种核素。
同位素是同种元素的不同核素。
如O168、O178、O188三种核素的质子数相同、同属氧元素,但中子数不同,是不同的核素和同位素。
因此,只有同种元素的不同核素才是同位素,不同元素的核素不是同位素。
元素只能论种类不能计个数,而原子既能论种类又能计个数。
2. 由不同同位素构成的物质的性质和特点(1)不同同位素的质子数相同,核外电子数也相同,只是中子数不同,因而其化学性质基本相同。
(2)不同同位素构成的单质(如H2和D2)是不相同的单质,但其化学性质基本相同。
(3)不同同位素构成的化合物(如D2O和T2O)是不同的化合物,其物理性质不同,但化学性质基本相同。
六. 元素周期表的应用1. 同周期元素从左到右金属性逐渐减弱,非金属性逐渐增强,元素最高价氧化物所对应的水化物碱性逐渐减弱,酸性逐渐增强。
以第三周期为例:2. 同一主族从上到下金属性逐渐增强,非金属性逐渐减弱。
如ⅠA族:从Li→Cs,最高价氧化物的水化物碱性增强,CsOH为最强碱;ⅦA:F→I,最高价含氧酸(F无含氧酸)酸性逐渐减弱,氢化物的稳定性逐渐减弱。
F2与H2结合最容易,生成的HF最稳定,非金属性最强。
3. 第ⅣA族所形成的化合物种类最多(多为有机物),第ⅢB族包括的元素种类最多(包括Sc、Y、镧系、锕系,其中Sc、Y、镧系为十七种稀土元素)。
4. 第ⅠA族与ⅦA族,第ⅡA族与ⅥA族所形成的化合物为AB型(NaCl、MgO),此外属于AB型的物质还有Na2O2、H2O2、C2H2、C6H6、CO、NO等;第ⅠA族与ⅥA族所形成的化合物为AB2型,N2O也是;ⅢA族与ⅦA族所形成的化合物为AB3型,此外NH3、PH3、PCl3、SO3、CH3—CH3也是;ⅢA族与ⅤA族所形成的化合物为A2B3型,此外N2O3也是;ⅣA与ⅦA族所形成的化合物为AB4型,如CCl4、CH4等。
5. 在元素周期表中,金属和非金属交界线附近的元素可作半导体材料;制特种合金、耐高温、耐腐蚀的合金,一般在过渡元素中找;制催化剂的元素一般也在过渡元素中找。
七. 元素的推断元素的推断多为文字叙述题。
考查该知识点的题型主要有选择题、填空题、推断题等涉及知识面广,常给出如下条件:结构特点,性质特点,定量计算。
推断题主要考查学生基础知识的掌握情况和运用基础知识的能力。
1. 定性推断第一:给出元素的某些性质特点:①短周期元素1~18号元素。
②在自然界含量最多的元素—氧。
③在自然界含量最多的金属元素—铝。
④最活泼的非金属—F。
⑤最活泼的金属—Cs。
⑥常温下呈液态的金属—Hg。
⑦常温下呈液态的非金属单质—Br2。
⑧焰色反应(K—紫,Na—黄,Ca—砖红)。
⑨单质气体最轻的—H 2。
⑩非金属单质的晶体硬度最大的—金刚石。
原子难于形成离子的—C、Si。
通常形成化合物种类最多的—C。
典型的变价金属—Fe(+2,+3)Cu(+1,+2)。
第二,给出元素原子的结构特点①最外层电子数是次外层电子数的2倍、3倍,说明其原子只有2个电子层分别为②最外层电子数等于最内层电子数,对主族元素而言,是第ⅡA主族元素Be、Mg、Ca、Sr、Ba。
③某元素的阴离子或阳离子和稀有气体原子的电子层结构相同。
阴离子的电子层结构和本周期稀有气体原子电子层结构相同。
阳离子的电子层结构和上周期稀有气体原子电子层结构相同。
如O2-、F-和同周期Ne电子层结构相同,Na+、Mg2+、Al3+电子层结构和上周期稀有气体Ne电子层结构相同。
④被推断的各元素原子电子层和电子数的关系。
2. 定量推断主要根据最高价氧化物中氧元素质量分数或气态氢化物中H的质量分数确定出元素的原子量,由此确定元素。
或由原子量确定质量数,再由质量数减去中子数求出质子数以确定元素。
如某元素最高价氧化物分子式为RO3,则氢化物分子式为H2R。
另外由金属和酸或和水作用产生的H2的量进行计算。
有如下量的关系:ⅠA2R~H2;ⅡAR~H2;ⅢA2R~3H2。
3. 元素推断的思维途径和方法①熟练掌握元素的性质特点,原子结构特点,充分运用“构”——“位”——“性”的相互关系。
②建立合理的思维模式。
4. 有关推断必备知识(1)主族元素在周期表中的特殊位置:①族序数等于周期数的元素:H、Be、Al。
②族序数等于周期数2倍的元素:C、S。
③族序数等于周期数3倍的元素:O。
④周期数是族序数2倍的元素:Li。
⑤周期数是族序数3倍的元素:Na。
⑥最高正价与最低负价代数和为零的短周期元素:C、Si。
⑦最高正价是最低负价绝对值3倍的短周期元素:S。
⑧除H外,原子半径最小的元素:F。
⑨短周期中其离子半径最大的元素:S。
⑩最高正价不等于族序数的元素:O、F。
(2)主族元素性质、存在、用途的特殊性。
①形成化合物最多的元素;或单质是自然界硬度最大的物质的元素;或气态氢化物中含氢质量分数最大的元素:C。
②空气中含量最多的元素;或气态氢化物的水溶液呈碱性的元素:N。
③地壳中含量最多的元素;或气态氢化物的沸点最高的元素;或氢化物在通常状况下呈液态的元素:O。
④地壳中含量最多的金属元素:Al。
⑤最活泼的非金属元素;或无正价的元素;或无含氧酸的非金属元素;或无氧酸可腐蚀玻璃的元素;或气态氢化物最稳定的元素;或阴离子的还原性最弱的元素:F。
⑥最活泼的金属元素;或最高价氧化物的水物碱性最强的元素;或阳离子氧化性最弱的元素:Cs。
⑦最易着火的非金属元素的单质,其元素是:P。
⑧最轻单质的元素:H,最轻的金属元素:Li。
单质中常温下呈液态的非金属元素:Br,金属元素:Hg。
⑩最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Be、Al。
○11元素的气态氢化物和它的最高价氧化物的水化物起化合反应的元素:N;能起氧化、还原反应的元素:S。
○12元素的气态氢化物能和它的氧化物在常温下反应生成该元素单质的元素:S。
○13元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
○14常见的能形成同素异形体的元素有C、P、O、S。
【解题方法指导】[例1] X元素的阳离子和Y元素的阴离子具有与氩元素相同的电子层结构。
下列叙述正确的是()A. X的核电荷数比YB. X的最高价氧化物一定是X2O,Y的气态氢化物为H2YC. X的离子半径比YD. X的最高正价比Y解析:由题给条件可知,X应比氩多一个电子层,而Y与氩有相同的电子层,从而判断出X的核电荷数比Y的大。
且X的最高正价要小于Y,由于X离子和Y离子具有相同的电子层数,而核电荷数X大于Y。
所以X的离子半径应小于X,而X的最高价氧化物可能是X2O,也可能是XO,而Y的氢化物不一定就是H2Y答案:D[例2] 两种短周期元素组成的化合物中,原子个数比为1∶2。
若两种元素的原子序数分别为p和q,则对下列p和q可能的关系概括得最完全的是()① p+q=15 ② p=q+5 ③ p=q-5 ④ p+q=22A. ①④B. ①③④C. ①②③④D. ①②④解析:①两种“短周期元素”,说明这两种元素的原子序数都小于18;②化合物中,原子个数比为1∶2,有两种形式:XY2或X2Y。
其中XY2型的化合物,常见的有CO2、SO2、NO2以及ⅡA和ⅦA族元素之间形成的化合物,如MgCl2、BeF2等。
