银杏叶提取物及其制剂的质量控制探析[3改]
银杏叶提取物泡腾片的研制及质量控制

银杏叶提取物泡腾片的研制及质量控制作者:于凯来源:《科学与财富》2015年第05期摘要:本实验研究银杏叶提取物泡腾片的制备方法并建立质量控制的方法。
性状、重量差异、崩解时限、微生物限度等均符合中国药典2010版有关规定。
含量测定方法:Waters XBridge C18液相色谱柱(150*4.6mm,5un),水-甲醇-乙腈-磷酸(72∶32∶12∶1),检测波长为254nm,流速为1.0ml/min。
结论:本制剂稳定、可靠,质量控制方法可行。
关键词:银杏叶;制备;质量银杏树为古老的树种,它是神奇的医疗之树,其叶、果实、种子均有较高的药用价值,其药理作用不断被认识,临床应用范围逐步扩大。
银杏叶提取物具有活血化瘀通络的功效。
银杏叶提取物用于中风、半身不遂、胃部疼痛、痢疾、高血压、舌强语蹇、冠心病稳定型心绞痛、脑梗塞、精神紧张、支气管炎等。
银杏叶提取物还能增加血液流向脑子和四肢,帮助改进记忆和精神敏锐感,包括记忆及警觉肾脏不适,老年人痴呆症,改善心脏心血管疾病或循环不佳造成的手脚冰冷,都有相当好的帮助。
槲皮素具有抗氧化及清除自由基、抗癌、抗炎、抗菌、抗病毒、降糖降压、免疫调节及心血管保护作用等[1]。
本实验研究银杏叶提取物泡腾片的制备方法并建立质量控制的方法。
1 仪器与试药1.1 仪器:安捷伦1100高效液相色谱仪、安捷伦色谱工作站、安捷伦1100可变波长检测器、SCQ-K001空气超声波清洗器(上海声彦超声仪器有限公司)、FA1204B电子分析天平(上海精科天美贸易有限公司)、CH-0108A手动压片机(东莞市创宏仪器设备有限公司)、UV4501双光束紫外可见分光光度计(天津港东科技发展股份有限公司)、pHS-2C型精密酸度计(上海精科雷磁厂)、XYF-H 帕恩特超低有机物型超纯水机(北京湘顺源科技有限公司)、德国优莱博TW20通用水浴槽(上海沃珑仪器有限公司)、RC-3药物溶出仪(天津大学无线电厂)。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定

注射用银杏叶提取物及其制剂中总银杏酸含量的测定引言银杏是一种珍贵的中草药,其叶子被广泛应用于医药制剂中。
银杏叶提取物中的总银杏酸是其主要活性成分之一,具有改善微循环、抗氧化、抗炎等多种作用。
监测和测定注射用银杏叶提取物及其制剂中总银杏酸含量是非常重要的。
材料与方法1. 实验仪器与试剂(1) 仪器: 离心机、紫外可见分光光度计、磁力搅拌器、研钵、磁力搅拌器、0.22μm微孔膜过滤器。
(2) 试剂: 甲醇、乙醇 (分析纯)、总银杏酸标准品。
2. 样品的制备粉碎银杏叶干燥物,取适量粉碎物加入甲醇与乙醇混合溶液浸泡,振荡60分钟后过滤,取滤液加入甲醇与乙醇混合液中,浸泡24小时后过滤,浓缩收集溶剂,干燥得到提取物。
3. 总银杏酸的测定(1) 样品溶液的制备: 取适量提取物加入甲醇与乙醇的混合溶液中,振荡溶解,通过0.22μm微孔膜过滤器过滤。
(2) 样品溶液的检测: 取适量样品溶液,用紫外可见分光光度计进行检测,以总银杏酸标准品为对照组。
数据处理通过测定样品中总银杏酸的浓度,得出样品中总银杏酸的含量,并与标准品进行对照,计算出样品中总银杏酸的含量。
讨论注射用银杏叶提取物及其制剂中总银杏酸含量的测定是十分重要的。
总银杏酸的含量不仅决定了银杏叶提取物的质量,也与其药效密切相关。
对总银杏酸含量进行精准的测定是保证药品质量和有效性的重要保障。
结论制作注射用银杏叶提取物及其制剂中总银杏酸含量的测定是十分关键的,通过合理选择仪器、试剂和标准操作流程,可以准确测定样品中总银杏酸的含量,并且得出科学准确的数据,为保障药品的质量和有效性提供了重要的支持。
这一研究也为银杏叶提取物及其制剂在临床上的应用提供了科学的参考依据。
银杏叶提取物质量标准

银杏叶提取物质量标准银杏叶提取物是一种常见的中药材,具有多种药用价值。
为了确保银杏叶提取物的质量和安全性,制定了一系列的质量标准,以便对其进行监管和控制。
本文将对银杏叶提取物的质量标准进行详细介绍,以便相关从业人员和消费者了解其质量标准的要求。
一、外观特征。
银杏叶提取物应为淡黄色至棕黄色的粉末,无异物、结块和霉变现象。
二、理化指标。
1. 含量测定。
银杏叶提取物中有效成分是银杏内酯类物质,其含量应不低于24%。
2. 溶剂残留。
银杏叶提取物中溶剂残留量应符合国家相关标准规定,丙酮残留不得超过0.5%。
3. 水分含量。
银杏叶提取物的水分含量不应超过5%。
三、微生物指标。
1. 细菌总数。
银杏叶提取物中细菌总数不得超过1000CFU/g。
2. 霉菌和酵母菌总数。
银杏叶提取物中霉菌和酵母菌总数不得超过100CFU/g。
3. 大肠菌群。
银杏叶提取物中大肠菌群不得检出。
四、重金属和有害物质限量。
1. 铅、汞、镉、砷含量。
银杏叶提取物中铅、汞、镉、砷含量应符合国家相关标准规定,不得超过规定限量。
五、贮存。
银杏叶提取物应贮存在阴凉干燥处,远离有害气体和阳光直射。
六、包装。
银杏叶提取物的包装应符合国家相关标准规定,标注清晰、完整,防潮、防尘、防虫。
七、其他。
银杏叶提取物的生产企业应具备相关的生产许可证和质量管理体系认证,确保生产过程的合规性和质量可控性。
总结,银杏叶提取物的质量标准是保障其质量和安全的重要依据,相关企业和从业人员应严格按照国家相关标准进行生产和监管,确保银杏叶提取物的质量安全,为消费者提供优质的产品。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定

注射用银杏叶提取物及其制剂中总银杏酸含量的测定引言
银杏叶提取物是一种常用的天然药物,被广泛应用于心脑血管疾病的治疗和预防。
其中的有效成分之一是银杏酸,它是银杏叶提取物中的主要成分之一,被认为具有抗缺血、抗缺氧、扩张血管、提高微循环等多种药理作用。
由于银杏酸具有一定的药理活性,在药物生产和质量监管过程中,对其含量进行准确测定十分重要。
对注射用银杏叶提取物及其制剂中总银杏酸含量进行测定具有重要的意义。
一、实验目的
本实验旨在建立一种准确测定注射用银杏叶提取物及其制剂中总银杏酸含量的方法,为其质量控制提供技术支持。
二、实验方法
1. 仪器与试剂
(1) 仪器:高效液相色谱仪(HPLC)、电子天平、恒温水浴仪等;
(2) 试剂:甲醇、乙腈、磷酸二氢钾等。
2. 样品制备
将注射用银杏叶提取物及其制剂样品取适量,粉碎至60目以下,称重备用。
3. 样品提取
取粉碎的样品0.5g,加入50ml甲醇中,用超声波提取30min,静置冷却,上清液置于50ml烧瓶中,加入甲醇至刻度,摇匀,过滤。
4. 色谱条件
色谱柱:C18色谱柱(4.6mm×250mm,5μm);
流动相:乙腈-0.05mol/L磷酸二氢钾溶液(30:70);
流速:1.0mL/min;
检测波长:275nm;
柱温:25℃。
5. 样品测定
将提取液取适量进行色谱分析,计算得到其总银杏酸含量。
三、结果与分析
经过上述实验方法进行实验测定,得到注射用银杏叶提取物及其制剂中总银杏酸含量的结果。
经统计分析,测定结果准确可靠。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定
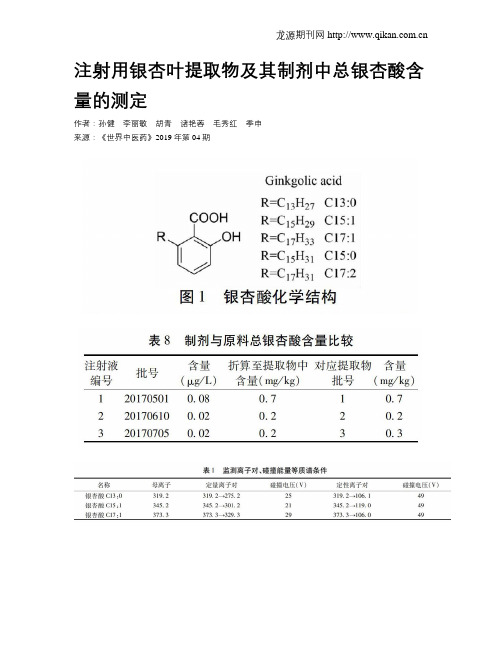
注射用银杏叶提取物及其制剂中总银杏酸含量的测定作者:孙健李丽敏胡青诸艳蓉毛秀红季申来源:《世界中医药》2019年第04期摘要;目的:建立超高效液相色谱串联三重四极杆质谱测定注射用银杏叶提取物及其制剂中总银杏酸的方法。
方法:采用HLB固相萃取净化制剂,Waters Cortecs T3色谱柱(50mm×2.1 mm,2.7 μm),以甲醇-1%冰醋酸溶液(90∶10)为流动相,在电喷雾离子化负离子模式下,以多反应监测方式(MRM)检测。
结果:银杏酸C13:0、C15:1、C17:1在0~50 ng/mL范围内成良好线性关系,相关系数均大于0.999;平均加样回收率为97.3%~115.2%,相对标准偏差(RSD)为0.3%~3.4%;检出限分别为0.03、0.06、0.04 mg/kg。
结论:本方法可应用于实际样品的测定。
关键词;银杏叶提取物;注射剂;银杏酸C13:0;银杏酸C15:1;银杏酸C17:1;超高效液相色谱-三重四极杆质谱;多重反应监测;固相萃取Determination of Ginkgolic Acids in the Ginkgo Biloba Extract for Injection and its Preparation Sun Jian,Li Limin,Hu Qing,Zhu Yanrong,Mao Xiuhong,Ji Shen(Shanghai Institute for Food and Drug Control,Shanghai 201203,China)Abstract;Objective:To develop an analytical method for determination of ginkgolic acids in the ginkgo biloba extract for injection and its preparation by ultra-high performance liquid chromatography-triple quadrupole mass spectrometry.Methods:The preparations were purified by HLB SPE.A chromatographic column,Waters Cortecs T3(50 mm×2.1 mm,2.7 μm),was used with methanol-1% acetic acid(90∶10)as the mobile phase.The ginkgo acids were detected by electrospray ionization mass spectrometry in negative mode with multiple reaction monitoring (MRM)mode.Results:Ginkgo Acid C13:0,C15:1 and C17:1 possessed good linear correlation in the mass concentration range from 0 to 50 ng/mL,with the correlation coefficients more than 0.999.The mean recoveries were in the range of 97.3%-115.2%,and the RSDs were 0.3%-3.4%.The limits of quantification were 0.03,0.06,0.04 mg/kg,respectively.Conclusion:The method could be applied to the analysis of ginkgolic acids in actual samples.Key Words;Ginkgo biloba extract; Injection; Ginkgolic acid C13:0; Ginkgolic acid C15:1; Ginkgolic acid C17:1; Ultra high performance liquid chromatography-tandem mass spectrometry; Multiple reaction monitor; Solid-phase extraction中圖分类号:R284.1文献标识码:Adoi:10.3969/j.issn.1673-7202.2019.04.006银杏叶提取物为银杏科植物银杏的干燥叶经加工制成的提取物,其主要功效为活血化瘀通络。
银杏叶提取物复方制剂的药效分析

银杏叶提取物复方制剂的药效分析作者:柴宝丽李桂红姜成忠来源:《健康必读·下旬刊》2011年第02期【中图分类号】R94 【文献标识码】A 【文章编号】1672-3783(2011)02-0176-01【摘要】文章通过观察银杏叶复方制剂对老龄小鼠的抗氧化作用。
得出银杏叶复方制剂具有抗氧化作用且呈现一定的量效关系,处方中的银杏叶提取物与野葛根提取物成分具有一定的协同药效作用。
【关键词】银杏叶;提取根据有关资料,银杏叶提取物能有效清除细胞内氧自由基,对胰岛细胞凋亡有保护作用;银杏叶提取物可以通过增强运动机体抗氧化酶的活性,提高机体的抗氧化功能,减轻大强度耐力训练对大鼠组织造成的脂质过氧化损伤,改善运动造成的自由基代谢紊乱,加快自由基的清除。
葛根提取物具有抗氧化应激的作用,可提高糖尿病大鼠血浆超氧化物歧化酶的活性,减少丙二醛的产生,有效防治糖尿病血管病变的发生;葛根提取物的抗氧化作用主要与其主要有效成分葛根素能提高SOD酶、+-+-ATP酶、+-ATP酶活性,降低MDA含量有关。
目前,有关银杏叶提取物和葛根提取物的配伍作用研究尚鲜见报道。
前文我们曾经报道了银杏叶提取物和葛根提取物的复方制剂的工艺研究及其质量标准研究。
为了进一步观察银杏叶提取物和葛根提取物组成复方新制剂的药效学作用,为临床研究提供实验依据,本文根据该复方制剂有效成分的药理作用及其功能主治主要针对心脑血管疾病、糖尿病和老年病的特点,对其进行小鼠抗氧化试验观察,旨在为后续的临床研究提供实验依据。
现报道如下。
1 材料与仪器1.1 药物与试剂银杏叶复方制剂(片剂),批号:20051030,由广西壮族自治区人民医院制剂室提供。
银杏叶单方制剂(片剂),广西某药业股份有限公司提供,批号:050418。
SOD 和MDA测定试剂盒均为南京建成生物技术工程研究所产品,批号分别为:20051129,20051128。
肾上腺素注射液,天津金耀氨基酸有限公司产品,批号:0503011。
银杏叶活性成分的提取制备及测定方法的研究进展

银杏叶活性成分的提取制备及测定方法的研究进展银杏叶提取物(GBE)具有独特的药理活性及巨大的临床应用价值,因此对银杏叶的药用、保健等综合价值的深入挖掘和开发日益受到重视。
本文就银杏叶的化学成分、提取分离及其质量控制方面的最新进展作一综述。
1银杏叶的化学成分银杏叶的化学成分较为复杂,迄今为止,已从银杏叶中分离出大量的极性和非极性化合物,其中主要为黄酮类化合物、萜类内酯,此外还有有机酸、烷基酚和烷基酚酸、甾体化合物及微量元素等。
1.1EGb761的化学组成GBE具有多种生理活性,目前国际上标准银杏叶提取物是按德国Schwabe专利工艺生产的EGb761,其中黄酮含量为24%,萜内酯为6%,白果酸小于0.0005%,原花青素类7.0%,羧酸类成分13.0%,儿茶素类2.0%,非黄酮苷类20%,高分子化合物4.0%,无机物5.0%,水分溶剂3.0%,其他3.0%。
提取物的各种成分是一个整体中有机的组成部分,EGb761的药理作用是各种相对固定组成的各组分共同作用的结果。
1.2化学成分的动态变化目前比较公认的GBE的有效成分为黄酮类化合物和萜类内酯,而它们在叶中的含量随季节变化和植株性别差异会有较大变化。
苑可武等[1]测定了北京地区银杏叶中黄酮含量的季节性变化,结果认为银杏叶总黄酮含量在4月份为最高,8月份时居次;同时发现大部分时期内以槲皮素为主而异鼠李素比例相对一直较小。
南京大学药物研究所对银杏叶中黄酮苷与萜类内酯含量分别进行研究[2,3],结果发现黄酮苷含量以5月份为最高,以后逐月降低,雄性植株叶中黄酮含量明显高于雌性植株;而同株银杏树叶中萜类内酯含量随季节变化规律与黄酮苷相异,同时发现雌性植株叶子中内酯含量明显高于雄性植株,分别为0.22%,0.09%。
这一发现为我们充分利用自然资源提供了有价值的参考。
比较各地测定的银杏叶总内酯及黄酮苷含量,结果相差较大,除各自测定的方法的准确度或系统误差外,银杏总内酯与黄酮苷是否与各地的土壤、气候、环境及银杏树的性别、树龄等因素相关,还需做大量实验研究和分析统计工作。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定

注射用银杏叶提取物及其制剂中总银杏酸含量的测定【摘要】本研究旨在开发一种测定注射用银杏叶提取物及其制剂中总银杏酸含量的方法。
样品经过制备后,通过色谱条件进行分析,采用定量方法测定银杏酸含量,并进行方法验证。
结果分析表明,该方法准确可靠,适用于银杏酸的测定。
结论指出,本研究为注射用银杏叶提取物及其制剂的质量控制提供了重要参考,具有一定的应用前景。
【关键词】注射用银杏叶提取物、总银杏酸含量、测定、样品制备、色谱条件、定量方法、方法验证、结果分析、总结、展望1. 引言1.1 研究背景目前,国内外对于银杏叶提取物中总银杏酸含量的测定方法主要有高效液相色谱法、气相色谱法、紫外分光光度法和色谱质谱联用法等。
这些方法在测定精度、灵敏度和准确性上各有优劣,但都需要进行方法的验证和结果的分析,以确保测定结果的可靠性和准确性。
本研究旨在建立一种简便、准确的方法,用于测定注射用银杏叶提取物及其制剂中总银杏酸的含量,并进行方法验证和结果分析,为其临床应用提供科学依据。
1.2 研究目的本研究旨在建立一种精确、快速、稳定的测定注射用银杏叶提取物及其制剂中总银杏酸含量的方法。
当前市面上对注射用银杏叶提取物及其制剂中总银杏酸含量的测定方法存在一定的局限性和不足,在一定程度上影响了产品质量的监控和控制。
本研究的目的是对现有的测定方法进行改进和优化,使其具有更高的灵敏度、准确度和稳定性,从而为相关企业提供更准确、可靠的产品质量控制手段。
通过该研究,也将为相关行业的技术研发和质量监管提供参考和借鉴,推动该领域的发展和进步。
2. 正文2.1 样品制备样品制备是该研究的关键步骤之一,其质量直接影响到后续的分析结果。
需要选择高质量的注射用银杏叶提取物作为样品。
样品的选择应该考虑到其来源、保存条件以及处理方式等因素,以确保样品的稳定性和纯度。
在实际操作中,可以选择市售的银杏叶提取物作为样品,也可以自行提取银杏叶提取物。
在样品制备过程中,需要注意保持样品的稳定性和一致性。
银杏叶中黄酮的提取及其抑菌性检测

目录第一章绪论 (3)1.1银杏叶功效成分简述 (3)1.2 银杏叶主要成分研究情况 (3)1.3黄酮类化合物 (3)(1)组成及结构 (3)(5)银杏黄酮类化合物的理化性质 (4)第二章理论分析 (5)2.1银杏叶采集分析 (5)2.2 提取分析 (5)第三章实验仪器及其材料 (6)第四章实验方法及其过程 (6)4.1银杏叶采集、干燥 (6)4.2银杏叶中黄酮等物质的提取 (6)4.3细菌培养 (7)4.4制作菌悬液 (8)4.5提取物的抑菌性检测实验 (8)第五章实验结果分析 .......................................................... 错误!未定义书签。
第六章结论. (9)银杏叶中黄酮的提取及其抑菌性检测摘要银杏是我国的特有植物,又称公孙树。
银杏叶为最古老的中生代孑遗植物银杏的干燥叶。
银杏有裸子植物活化石之称。
据《本草纲目》记载,银杏果具有敛肺平喘、止遗尿、白带的作用。
在医药上有很高的利用价值。
银杏所含黄酮类成分主要为银杏双黄酮、异银杏双黄酮,去甲基银杏双黄酮,其他还有二萜内酯、银杏内酯A、B、C等,其中黄酮类和二萜内酯类物质具有捕获游离基和抑制血小板活化因子、扩张脑血管、促进血液循环、抗氧化等功能,从而广泛用于治疗冠心病、心绞痛、治疗老年痴呆症和增强记忆功能、防治皮肤病、脱发等多种疾病,随着深入的研究银杏的开发和利用,银杏所特有的医药、经济价值逐步受到重视。
银杏叶的提取方法有有机溶剂萃取法、水提取法、碱性稀醇或碱性水提取法、超临界萃取法、超声波提取法、酶法等。
本文采用有机溶剂提取黄酮类化合物,结果表明实验证明提取银杏叶黄酮等物质用乙醚3小时提取70℃下2次回流最佳。
菌体浓度试验表明当实验用菌体浓度在OD值为0.557,稀释到10-5和10-6比较适合,涂布能够成为单菌落,便于以后进行试验。
提取抑菌性试验证明加入0.5ml 时对大肠杆菌就有明显抑制作用,其抑菌效果随着提取物浓度的增加而增强,当提取物加入2.0ml时具有完全抑菌效果。
银杏叶提取物及其制剂补充检验方法的建立
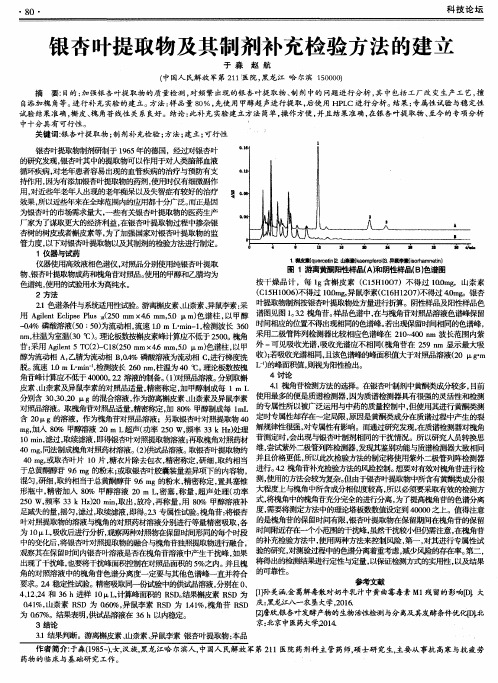
4讨论 角苷峰计算应不低于 4 0 0 0 0 。 2 . 2溶液的制备。 ( 1 ) 对照品溶液。 分别取槲 4 I 1槐角苷检澳 4 方法的选择。在银杏叶制剂中黄 赦多, 目前 皮素、 山柰素及异鼠李素的对照品适量, 精密称定, 加甲醇制成每 1 m L } 检i 贝 4 器, 因为质谱睑测器具有很强的灵活性和检测 分别含 3 0 、 3 0 、 2 0 g的混合溶液 , 作为游离槲皮素 、 山柰素及异鼠李素 使用最多的便是质谗 但使用其进行黄酮类测 对照品溶液。取槐角苷对照品适量 , 精密称定 , 加8 0 % 甲醇制成每 l m L 的专属性所以被广泛运用与中药的质量控制 中, 原因是黄酮类成分在质谱过程 中产生的裂 含 2 0 I X g的溶液,作为槐角苷对照品溶液 ;另取银杏叶对照提取物 4 0 定时专属性却存在一定局限, 圭 E 彳 艮 强, 对专属性有影响。而通过研究发现, 在质谱检测器列槐角 m g , 加入 8 % 甲醇溶液 2 0 0 m L 超声( 功率 2 5 0 W, 频率 3 3 k n z ) 处理 解规律I 苷测定时, 会 出现与银杏叶制剂相同的干扰腈况。所以研究 ^ 、 员转换思 1 0 m i n , 滤过, 取续滤液 , 即得银杏叶对照提取物溶液 ; 再取槐角对照药材 维 , 尝试紫外二极管列阵检 器, 发现其鉴别功能与质谱检测器大致相 同 4 0 m g , 同法制成槐角对照药材溶液。 ( 2 腆 试品溶液。 取银杏叶提取物约 并管列阵检测器 4 O m g , 或取杏叶片 l 0片, 糖衣片除去包衣, 精密称定 , 研细, 取约相当 4 2槐角苷补充检验方法的风险控制。 想要对有效对槐角苷进行检 于总黄酮醇苷 9 - 6 m g的粉末; 或取银杏叶胶囊装量差异项下的内容物 , 进行。 测 , 使用白 勺 = 胡去 会较为复杂。 但 由于银杏叶提取物中所 宁 黄酮类成分很 混匀 , 研细, 取约相当于总黄酮醇苷 9 . 6 mg的粉末 , 精密称定 , 置具塞锥 大程度上与槐角 中E 袷 成分相似度较高, 所以必须要采取有效的检测方 形瓶 中, 精密加入 8 % 甲醇溶液 2 0 0 m L , 密塞 , 称量 , 超声处理( 功率 将槐角中的魄角苷充分完全的进行分离 , 为了提高隗角苷的色谱分离 2 5 0 W, 频率 3 3 k Hz ) 2 0 ai r n , 取出, 放冷 , 再称量 , 用 8 % 甲醇溶液补 式 , 0 需要将测定方法中的理论塔板数数值设定到 4 0 0 0 0 之上。值得注意 足减失的量, 摇匀, 滤过 , 取续滤液 , 即得。 2 3专属 险 。 槐角苷: 将银杏 度 , 银杏叶提取物在保留期间在槐角苷的保 留 叶对照提取物的溶液与槐角的对照药材溶液分别进行等量精密吸取 , 各 的是槐角苷的保 留时间有限, . / J 、 范围的干扰峰 , 虽然干扰较小但仍需注意 , 在槐角苷 为l O L , 吸收后进行分析 , 观察两种对照物在保留时间形同的每个时段 时间附近存在—个 使用两种方法来控制风险, 第一 , 对其进行专属性试 中的变化后, 将银杏叶对照提取物的融合与槐角苷独照提取物进行融合 , 的补充检验方法 中, 对测验过程中的色谱分离着重考虑, 减少风险的存在率。 第二, 观察其在保留时间内银杏叶溶液是否在槐角苷溶液 中产生干扰峰 , 如果 验的研究, 将得出的检测结果进行定性与定量 , 以保证检测方式的实用性 , 以及结果 出现了干扰峰, 也要将干扰峰面积控制在对照品面积的5 %之 内。 并目 槐 角的对照溶液中的槐角苷色谱分离度一定要与其他色谱峰一直并符合 的可靠性。 参考文献 要求。 2 4 稳定 硷 。 精密吸 取同—份试验中的供试品 溶液, 分别在 0 、 [ 1 ] 孙美涵. 金葛解毒散对奶牛乳汁 中黄 曲霉毒素 M1 残 留的影响【 I ) l大 4 、 1 2 、 2 4和 3 6 h进样 1 0 L , 计算峰面积的 R S D 。 结果槲皮素 R S D为 庆 : 黑龙江八一农垦大学, 2 0 1 6 . 0 . 4 1 %, 山柰素 R S D为 0 . 6 %, 0 异 鼠李素 R S D为 1 . 4 1 %, 槐角苷 R S D c 2 】 詹欣 银杏叶发酵产物的生物活性检测与分 离及其发酵条件优化Ⅱ ) l 北 为0 . 6 7 %。结果表明, 侈 } 试品溶液在 3 6 h以内稳定 。 京: 北京中医药大学2 0 1 4 . 3结 论
《中国药典》银杏叶提取物质量标准与《美国药典》,《欧洲药典》的对比分析

《中国药典》银杏叶提取物质量标准与《美国药典》,《欧洲药典》的对比分析银杏叶在中医学中具有重要地位,它被称为神奇的草药,因为它具有多种药用作用。
我国《中国药典》对银杏叶提取物质量标准的要求苛刻而严格,而其他西方药典也有相关的规范。
本文详细分析了《中国药典》、《美国药典》和《欧洲药典》在银杏叶提取物质量标准方面的区别。
首先,该提取物在《中国药典》中的定义。
《中国药典》定义银杏树叶提取物为“芳皮苷、银杏内酯、柔毛甙苷、类固醇和多种植物黏液物质”,其总甾醇和有效性改善剂含量必须达到一定标准。
此外,《中国药典》要求所检测物质中植物黏液物质和一氧化氮含量达到一定标准。
其次,在《美国药典》中,银杏叶提取物的标准定义为“柔毛甙苷的总含量和有活性的改善剂的总量”,需达到规定的标准。
USP还规定,检测银杏叶提取物中的有效成分必须在一定范围之内,具体包括柔毛甙苷、类固醇、多糖类等。
最后,《欧洲药典》提取物质量标准主要是柔毛甙苷('G. K252a')含量和有活性的改善剂的总量,但在欧洲药典的检测程序中,还要考虑多糖类、黏液质等多种有效成分的含量。
总而言之,上述具体标准的不同反映出西方药典系统对银杏叶提取物的检测需求有明显的区别,主要由于检测程序、检测组成物和检测标准等因素。
具体来讲,《中国药典》检测程序更加苛刻,检测组成物更加细致全面,而欧洲药典和美国药典更加关注有效成分的检测和含量,而不怎么关注其他物质的含量。
综上所述,《中国药典》、《美国药典》和《欧洲药典》在银杏叶提取物质量标准方面有明显的区别,这主要是由于它们各自的检测和标准的不同而导致的。
这些差异在某种程度上表明,西方药典系统更多关注检测有效成分和有效成分的含量,而中国药典却把更多的重视力量投入到物质的细致检测上,旨在更有效地确保其有效性和标准。
银杏叶制剂的质量控制分析

银杏叶制剂的质量控制分析[摘要] 银杏叶是一种有着悠久历史的中药原材料,在临床上常用于冠心病、心绞痛和高脂血症等。
目前对于银杏叶的临床应用,最常用的方式是进行炮制,将其中的活性物质,如黄酮类化合物、萜内酯等提纯、加入辅料做成制剂。
由于制剂制作工艺、材料使用的差异,这类制剂的质量也存在各种相应的问题,本文拟通过分析银杏叶的生产工艺现状、制剂制作流程中的各种问题,围绕银杏叶制剂的质量控制现状及改进,进行探讨。
[关键词] 银杏叶制剂质量控制1.银杏叶的药用价值简介银杏叶为银杏的干燥树叶,它是一种重要的中药原材料。
具有敛肺、平喘、活血化瘀、止痛等作用。
目前对于银杏叶的化学成分研究结果认为:银杏叶及其制剂中,最重要的活性成分为黄酮类化合物和银杏内酯.其中,黄酮类化合物包括40余种,根据分子结构分为三大类:三羟基黄酮醇及其苷类、双黄酮类、儿茶素类化合物。
药理学分析指出,这三类化合物中,以前两类生物活性最显著。
这两类化合物均有抗组胺、抗炎症、扩张血管、消除自由基、防治动脉硬化等作用。
除了黄酮类外,银杏叶中还有一类自己独有的化合物:银杏内酯。
这类仅仅从银杏叶中提取的化合物中,大多具有二萜或半萜结构。
因此,属于萜类化合物。
这类化合物具有抗血小板活化因子、抗氧化、去除自由基的作用。
能够保护机体免受自由基的氧化损伤的作用。
目前银杏叶制剂在欧美国家的临床应用已经三十余年,从临床的经验数据来看,银杏叶制剂的主要用于脑部、外周血流的循环障碍患者,并可有改善患者脑缺血引起的记忆力减退功能。
在中医中,中国药典 2000 版登载:银杏叶制剂可用于“瘀血阻络引起的胸痹心痛、中风、半身不遂、舌强语謇”。
由此可见,银杏叶制剂在活化局部循环,改善重要脏器功能方面,有着重要药用价值。
2.银杏叶制剂的生产工艺探讨由于中药成分复杂,其制剂流程较多,每一步都可能对最终的制剂质量产生影响,因此,对于制剂的生产制作工艺,应该有比较严格的把关控制,严格按照GMP要求进行生产。
银杏叶提取物质量标准及检验操作规程
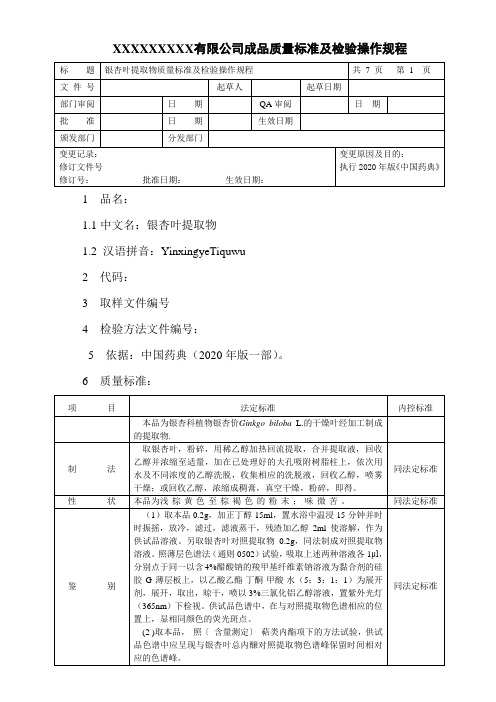
XXXXXXXXX有限公司成品质量标准及检验操作规程1 品名:1.1中文名:银杏叶提取物1.2 汉语拼音:YinxingyeTiquwu2 代码:3 取样文件编号4 检验方法文件编号:5 依据:中国药典(2020年版一部)。
6 质量标准:检查水分不得过5.0%(通则0832第二法)。
炽灼残渣不得过0.8%(通则0841)。
重金属取炽灼残渣项下遗留的残渣,依法检查(通则0821),不得过百万分之二十。
黄铜苷元峰面积比按〔含量测定〕项下的总黄铜醇苷色谱计算,槲皮素与山柰素的峰面积比应为0.8~1.2,异鼠李素与槲皮素的峰面积比值大于0.15。
总银杏酸照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验以十八烷基硅胶键合硅胶为填充剂;(柱长为150mm,柱内径为4.6mm,粒径为5M m );以含0.1%三氟乙酸的乙腈为流动相A ,含0.1%三氣乙酸的水为流动相B,按下表中的规定进行梯度洗脱;检测波长为310nm 。
理论板数按白果新酸峰计算应不低于4000。
对照品溶液的制备取白果新酸对照品适量,精密称定,加甲醇制成每1ml含1μg的溶液,作为对照品溶液。
另取总银杏酸对照品适量,加甲醇制成每1ml含20μg的溶液,作为定位用对照溶液。
供试品溶液的制备取本品粉末约2g,精密称定,置具塞锥形瓶中,精密加人甲醇l0ml,称定重量,超声使其溶解,放冷,用甲醉补足减失的重f,摇匀,滤过,取续滤液,即得。
测定法精密吸取供试品溶液、对照品溶液及定位用对照溶液各50μl,注入液相色谱仪,计算供试品溶液中与总银杏酸对照品相应色谱峰的总峰面积,以白果新酸对照品外标法计算总银杏酸含量,即得。
本品含总银杏酸不得过百万分之十。
同法定标准含量测定总黄酮醇苷照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验以十八烷基硅胶键合硅胶为填充剂;甲醇-0.4%磷酸溶液(50:50)为流动相;检测波长为360nm。
理论板数按槲皮素峰计算应不低于2500。
银杏叶提取物质量标准及检验操作规程

XXXXXXXXX有限企业成质量量标准及查验操作规程标题银杏叶提取物质量标准及查验操作规程共7 页第 1页文件号草拟人草拟日期部门批阅日期QA 批阅日期批准日期奏效日期颁发部门散发部门更改记录:订正文件号更改原由及目的:履行 2020 年版《中国药典》订正号:同意日期:奏效日期:1品名:1.1 中文名:银杏叶提取物1.2 汉语拼音: YinxingyeTiquwu2代码:3取样文件编号4查验方法文件编号:5依照:中国药典( 2020 年版一部)。
6质量标准:项目法定标准内控标准本品为银杏科植物银杏价Ginkgo biloba L.的干燥叶经加工制成的提取物 .取银杏叶,粉碎,用稀乙醇加热回流提取,归并提取液,回收制法乙醇并浓缩至适当,加在已办理好的大孔吸附树脂柱上,挨次用同法定标准水及不一样浓度的乙醇洗脱,采集相应的洗脱液,回收乙醇,喷雾干燥;或回收乙醇,浓缩成稠膏,真空干燥,粉碎,即得。
性状本品为浅棕黄色至棕褐色的粉末;味微苦。
同法定标准( 1)取本品 0.2g,加正丁醇 15ml,置水浴中温浸15 分钟并时时振摇,放冷,滤过,滤液蒸干,残渣加乙醇2ml使溶解,作为供试品溶液。
另取银杏叶比较提取物0.2g,同法制成比较提取物溶液。
照薄层色谱法(公则0502)试验,汲取上述两种溶液各 1μl,分别点于同一以含 4%醋酸钠的羧甲基纤维素钠溶液为黏合剂的硅鉴别胶 G 薄层板上,以乙酸乙酯-丁酮 -甲酸 -水( 5: 3: 1: 1)为睁开同法定标准剂,睁开,拿出,晾干,喷以3%三氯化铝乙醇溶液,置紫外光灯(365nm)下检视。
供试品色谱中,在与比较提取物色谱相应的地点上,显同样颜色的荧光斑点。
(2 )取本品,照〔含量测定〕萜类内酯项下的方法试验,供试品色谱中应体现与银杏叶总内醸比较提取物色谱峰保存时间相对应的色谱峰。
水分不得过 5.0%(公则 0832 第二法)。
炽灼残渣不得过 0.8% (公则 0841)。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定

注射用银杏叶提取物及其制剂中总银杏酸含量的测定1. 引言1.1 研究背景银杏叶提取物是一种常用的中药材,具有多种药理作用,被广泛用于治疗心脑血管疾病、抗衰老和改善记忆力等。
银杏叶中的主要有效成分是银杏内酯类物质,其中总银杏酸是银杏内酯的主要成分之一。
总银杏酸具有抗氧化、抗炎和抗肿瘤等多种药理作用,对人体健康具有重要意义。
随着银杏叶提取物在临床应用中的逐渐普及,对其质量进行准确测定变得尤为重要。
总银杏酸是银杏叶提取物中的主要活性成分,其含量直接影响着银杏叶提取物的药效和质量。
研究注射用银杏叶提取物及其制剂中总银杏酸含量的测定方法具有重要的理论和实践意义。
在这个背景下,本研究旨在探讨总银杏酸的测定方法,为提高注射用银杏叶提取物及其制剂的质量控制水平提供科学依据和技术支持。
通过本研究的开展,将为银杏叶提取物的质量标准制定和生产工艺优化提供参考依据,推动银杏叶提取物在临床应用中发挥更好的药效。
1.2 研究目的研究目的:通过对注射用银杏叶提取物及其制剂中总银杏酸含量的测定,探讨其质量控制方法,为该制剂的质量评价提供依据。
具体目的包括:1.建立一种快速、准确、稳定的测定方法,确保总银杏酸含量的准确性;2.分析不同提取工艺对总银杏酸含量的影响,指导生产过程中的优化和控制;3.评价不同制剂中总银杏酸含量的差异,为临床应用提供参考依据;4.促进注射用银杏叶提取物及其制剂的质量管理与监督,保障患者用药安全。
通过本研究,旨在为提高注射用银杏叶提取物及其制剂的质量水平,推动其在临床应用中的进一步推广和应用。
2. 正文2.1 银杏叶提取物的制备方法银杏叶提取物的制备方法可以分为传统提取法和现代生物技术法两种主要方法。
传统提取法主要包括水提取、酒精提取和超临界流体萃取等。
水提取是将银杏叶与水混合加热后去除悬浮颗粒,然后经过浸提、榨取、浓缩、干燥等工艺步骤制备而成。
酒精提取是将银杏叶与有机溶剂酒精混合后加热浸泡,再进行过滤、蒸发、冷凝等步骤得到银杏叶提取物。
注射用银杏叶提取物及其制剂中总银杏酸含量的测定

注射用银杏叶提取物及其制剂中总银杏酸含量的测定摘要:本研究旨在探讨注射用银杏叶提取物及其制剂中总银杏酸含量的测定方法。
采用高效液相色谱法(HPLC)来测定25个不同批次的银杏叶提取物和10个样品的制剂中总银杏酸含量。
结果表明,所有样品中总银杏酸的含量都在要求的范围内,且精密度和准确度均良好。
因此,所开发的方法可用于注射用银杏叶提取物及其制剂的质量控制。
关键词:银杏叶提取物;总银杏酸;HPLC;制剂;质量控制引言:银杏叶提取物是一种常用的草药提取物,广泛用于中药配方和保健品中。
银杏叶提取物中含有多种药理活性成分,其中总银杏酸是其中一个主要的成分。
银杏叶提取物的制剂一般会用作口服药物和注射用药物。
注射用银杏叶提取物对于治疗脑卒中和其他神经系统疾病有一定的疗效。
因此,对于银杏叶提取物及其制剂的质量控制十分重要,而总银杏酸的含量是一个主要的质量指标。
目的:材料与方法:仪器和设备:1. HPLC(高效液相色谱): Agilent 1200系列,相分离柱:C18,柱温:30℃;检测波长:254 nm。
2. 称量仪:Mettler-Toledo XPE 205。
3. 蒸馏水仪: Milli-Q水系统。
试验药品和试剂:1. 银杏叶提取物(25个样品):来自不同生产厂家,不同剂型(粉末、固体、液体)。
这些样品的保质期在4年以上。
2. 3,5-二硝基苯甲酸: Sigma-Aldrich。
3. 甲醇: Fisher Scientific。
6. 离子交换树脂:Dowex 50x8-200。
样品制备:银杏叶提取物样品:每个样品取2g,加入50 mL甲醇-水(1:1)混合液中,在温度为60℃下浸泡2小时,然后过滤,将过滤液浓缩到4 mL,用10%三氯乙酸溶液pH=3调节pH到5.5-6.5,蒸发至干燥。
最后添加1 mL甲醇-水(1:1)混合液,将溶液通过0.45 μm的微孔过滤器过滤后使用。
测定方法:1. 制备标准曲线:精确称量5 mg弱碱性银杏酸标准品,加入10 mL甲醇-水(1:1)混合液中,通过0.45 μm的微孔过滤器过滤。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
学科代码: 070301学号: 2009407003本科毕业论文(设计)题目:银杏叶提取物的生理活性及测定方法学院:化学与材料工程学院专业:__化学班级:09化本学号:2009407003学生姓名:黄飞指导教师:曹晖2013年3月8日目录目录.............................................................................................. 错误!未定义书签。
摘要. (Ⅱ)关键词 (Ⅱ)Abstract: (Ⅱ)Keywords (Ⅱ)1 引言.......................................................................................... 错误!未定义书签。
2 银杏叶化学成分...................................................................... 错误!未定义书签。
3 生理活性.................................................................................. 错误!未定义书签。
3.1 促进血液循环................................................................ 错误!未定义书签。
3.2 抗氧化作用.................................................................... 错误!未定义书签。
3.3 抗衰老功能.................................................................... 错误!未定义书签。
3.4 糖尿病的治疗................................................................ 错误!未定义书签。
3.5 高血压的治疗................................................................... 错误!未定义书签。
4 银杏叶活性成分提取.............................................................. 错误!未定义书签。
4.1 溶剂提取法.................................................................... 错误!未定义书签。
4.2 树脂法............................................................................ 错误!未定义书签。
4.3 超临界CO2提取法....................................................... 错误!未定义书签。
4.4 超声波提取法................................................................ 错误!未定义书签。
4.5 微波提取法.................................................................... 错误!未定义书签。
4.6 高速逆流色谱技术提取法............................................ 错误!未定义书签。
5 银杏叶提取物及其制剂的质量控制方法.............................. 错误!未定义书签。
5.1 银杏黄酮含量分析........................................................ 错误!未定义书签。
5.1.1 紫外分光光度(UV)法 ....................................... 错误!未定义书签。
5.1.2 HPLC法 .......................................................... 错误!未定义书签。
5.1.3 胶束电动毛细管电泳(MECC)法...................... 错误!未定义书签。
5.1.4 核磁共振(NMR)法.......................................... 错误!未定义书签。
5.2 银杏内酯含量分析........................................................ 错误!未定义书签。
5.2.1 RP-HPLC法 ....................................................... 错误!未定义书签。
5.2.2 LC-TSP-MS 法 ............................................... 错误!未定义书签。
5.2.3 GC-MS 法....................................................... 错误!未定义书签。
5.2.4 核磁共振法........................................................ 错误!未定义书签。
5.3 银杏酸的定量分析........................................................ 错误!未定义书签。
5.3.2 UV定量分析方法.............................................. 错误!未定义书签。
5.3.3 衍生化-GC定量分析方法................................ 错误!未定义书签。
6 结论及展望.............................................................................. 错误!未定义书签。
参考文献...................................................................................... 错误!未定义书签。
致谢 (10)银杏叶提取物的生理活性及质量控制方法黄飞(凯里学院化学与材料工程学院化学)摘要: 随着人们对银杏叶提取物药理和临床认识的不断深入以及银杏叶活性物质提取技术和质量控制手段的进步,银杏叶提取物的相关产业也获得了快速的发展。
本文通过参阅国内外的相关文献报道,对银杏叶提取物的生理活性及其相关活性物质的测定方法进行了归纳分析,以期为相关工作者提供参考。
关键词:银杏叶提取物,提取方法;制剂;质量控制Physiological activity of Ginkgo biloba extract and qualitycontrol methodsHuang Fei(Environment and life science, Kaili university)Abstract: Ginkgo biloba extract Ginkgo biloba extract matter pharmacological and clinical deeper understanding and active substances of Ginkgo biloba extract the continuous advancement of technology and quality control methods, industry also gained rapid development. Reported at home and abroad to participate in the physiological activity of the Ginkgo biloba extract and its related method for determination of active substances were summarized and analyzed in order to provide a reference for the relevant workers.(英文翻译改好)Keywords:Ginkgo biloba extract; extraction methods; preparations; quality control1 引言银杏叶为银杏科植物银杏(Ginkgo biloba L)的干燥叶,性甘、苦、涩、平,归心、肺经,具有敛肺、平喘、活血化瘀、止痛等作用,用于冠心病、心绞痛和高血脂症。
目前,《中国药典》已经收载了包括银杏叶在内的5种相关的品种。
《欧洲药典》规定了银杏叶及其银杏叶提取物的相关标准,《美国药典》也已经将银杏叶及其制剂作为了食品补充剂而收录。
经过20多年的发展,国内银杏叶提取物的厂家已成规模。
目前银杏叶提取物的质量控制已成为制约提取物制剂发展的重要因素,而影响银杏叶提取物质量的主要因素涉及到生产工艺和含量的检测方法,因此本文就银杏叶活性物质的提取及检测方法进行总结。
2 银杏叶化学成分银杏叶及其制剂的主要活性成分为黄酮类化合物和银杏内酯。
此外,也含有有机酸类、酚类以及原花青素类等。
目前国内外研究者从银杏叶中分离出来的黄酮类化合物已经有40多种,据分子结构的不同其可以分为黄酮、黄酮醇及其苷、双黄酮和儿茶素等几大类,其中黄酮(醇)苷类是主要的活性成分[1-2]。
银杏内酯为二萜类内酯,其主要分为银杏内酯A、B、C、J以及白果内酯。
银杏叶中的酚酸类成分属于羟基取代的水杨酸衍生物,主要有白果酸、白果新酸、白果酚、银杏酸等。
此外,银杏叶还含有氨基酸、蛋白质、糖类、维生素、矿物质、微量元素等成分[3]。
相关研究显示,银杏的酚酸具有一定的细胞毒性,其可以导致过敏和致突变,引起阵发性痉挛和神经麻痹等,因此应对其在制剂中的含量加以控制[4]。
但GBE(银杏叶提取物)的化学成分较为复杂,目前尚无统一质量标准,国际上公认的银杏叶制剂质量控制标准是德国Schwabe(舒培药厂)公司1991年的专利GBE761标准,即黄酮>24%,总内酯>6%(其中银杏2.5%~4.5%,白果内酯2.0%~4.0%),同时限定银杏酸水平在5 mg·kg-1以内[3]。
