九年级科学酸碱盐强化练习(1)
中考化学常见的酸和碱提高强化练习含答案

中考化学常见的酸和碱提高强化练习含答案一、初中化学常见的酸和碱选择题1.下列实验基本操作错误的是()A.研磨闻气味B.蒸发食盐水C.稀释浓硫酸D.测溶液的pH2.下列说法正确的是()A.浓盐酸长时间敞口放置溶质质量分数会变大B.浓硫酸敞口放置后溶剂会逐渐减少C.氢氧化钠固体长时间敞口放置质量增加,其过程中包含化学变化D.氢氧化钠去除油污和洗涤剂去除油污的原理相同3.食醋中含有醋酸,下列使用食醋肯定不能达到目的是()A.除去水壶壁上的水垢B.加入紫色石蕊溶液,溶液变红C.除去菜刀上的铁锈D.鉴别黄金饰品中是否含有铜4.在天平两边各放一个盛有相同质量分数、等体积的足量稀硫酸的烧杯,把天平调到平衡,在左边烧杯中加入6.5g锌粒,为使天平最终保持平衡,右边的烧杯中应放入铝粉的质量为( )A.5.4g B.5.68g C.6.5g D.7.09g5.下列小实验不正确的是()A.可用稀盐酸比较金属铝和铜的活泼性B.不用试剂可区分浓盐酸和浓硫酸C.可用石灰水检验氢氧化钠是否变质D.可用酚酞鉴别稀硫酸和蒸馏水6.金属X的活动性比较强,它的氧化物为X2O3,其对应碱为其对应碱为X(OH)3.X(OH)3难溶于水,而XCl3可溶于水.下列各组中的物质难以直接反应而制得XCl3的是( )A.X+HCl B.X2O3+HClC.X(OH)3+HCl D.X(OH)3+MgCl27.室温下,向 a克 Mg粉和 Ag粉的混合物中加入 Cu(NO3)2溶液,经充分反应后,过滤,得到滤渣和蓝色滤液。
则下列对滤渣和滤液的判断中,正确的是()A.滤渣中一定没有单质镁B.滤液中一定没有 Cu2+C.滤渣质量一定小于 a D.滤液中一定含有 Ag+8.取石灰石与稀盐酸充分反应后的溶液A,向其逐滴加入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如图(pH为纵坐标,时间为横坐标)。
则下列说法不正确的是()A.溶液A中的溶质有两种B.A、B段观察到有气泡产生C.B、C段滴入紫色石蕊,溶液呈无色D.D、E两点溶液中的溶质种类相同9.向pH为5的白醋中加入下列物质,混合溶液的pH肯定增大的是()A.硫酸B.硝酸C.pH为5的溶液D.烧碱溶液10.下列对有关事实的解释中,正确的是()A.气体可压缩储于钢瓶中﹣﹣分子数目变少B.H2O和H2O2的化学性质不同﹣﹣分子构成不同C.烧碱和纯碱的溶液都显碱性一两者都是碱类D.干冰用于人工降雨﹣﹣升华放热11.向分别盛有甲、乙、丙三种金属的试管中滴加稀硫酸,仅甲、丙能产生气泡,并分别生成X、Y,丙能从X溶液中置换出甲,则三者的金属活动性顺序为()A.丙>甲>乙B.甲>乙>丙C.乙>甲>丙D.甲>丙>乙12.推理是研究和学习化学的一种重要方法,下列推理正确的是()A.浓盐酸具有挥发性所以浓硫酸也具有挥发性B.某固体中加入稀盐酸,生成无色无味的气体,证明该物质一定是碳酸盐C.向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类D.点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度13.取敞口放置的氧化钙样品22g,加入足量盐酸,产生4.4g CO2,再向剩余溶液中足量的Na2CO3溶液,充分反应后,过滤得到沉淀质量为30g。
九年级科学酸碱盐综合练习(1份)

酸碱盐综合练习一、选择题1.下列关于碱的叙述正确的是()A.能电离生成氢氧根离子的化合物B.能使紫色石蕊试液变蓝的溶液C.能跟酸发生中和反应的化合物D.水溶液PH大于7的化合物2. 根据下列常用的危险安全警示标志,装运浓硫酸的包装上应贴的图是()A、腐蚀性B、爆炸性C、剧毒性D、易燃性3.小亮用紫色石蕊试液测定某饮料的酸碱性,结果发现紫色石蕊试液变为红色,则该饮料为()A.中性B.酸性C.强碱性D.弱碱性4.衢州的椪柑享誉全国,某果农发现其种植的椪柑出现生长迟缓,叶色淡黄的现象,经农技员诊断必须追加相应的复合肥料。
你认为下列属于复合肥料的是()A、 CO(NH2)2B、NH4ClC、K2SO4D、NH4H2PO45、小王测得生活中一些物质的PH如下表,下列说法不正确的是()物质肥皂水雨水蔗糖水食醋纯碱水柠檬汁PH 10.2 5.8 7.0 3.3 8.1 2.0C.柠檬汁的酸性比食醋强D.雨水能使蓝色石蕊试纸变红6.人的汗液中含有氯化钠,手摸过物体后,手指纹线上的汗液就留在物体上。
因此,法医做指纹鉴定时,可选用的试剂是()A. AgNO3溶液B.酸碱指示剂C.酒精D.碘酒7.下列药品露置于空气中一段时间后,因发生化学变化而质量减小的是()A.酒精B.固体烧碱C.碳酸钠晶体D.生石灰8.下列反应中,属于中和反应的是()A.CuO+H2SO4=CuSO4+H2OB.HCl+AgNO3=AgCl↓+HNO3C.Ba(OH)2+H2SO4=BaSO4↓+2H2OD.CaCO3+2HCl=CaCl2+H20+CO2↑9..下列各类盐中都能溶于水的是()①钠盐;②硫酸盐;③盐酸盐;④钾盐;⑤硝酸盐;⑥碳酸盐;⑦铵盐A.①②③B.①③④⑤C.①④⑤⑦D.④⑤⑥⑦10.将下列试剂分别加入KOH溶液,饱和石灰水和稀H2SO4中,能出现三种不同现象的是()A.紫色石蕊试液B. Na2CO3溶液C. CuCl2溶液D. NaCl溶液11. 以下四个溶液:①MgSO4;②NaOH;③CuSO4;④KCl。
初三化学常见的酸和碱培优强化练习附答案
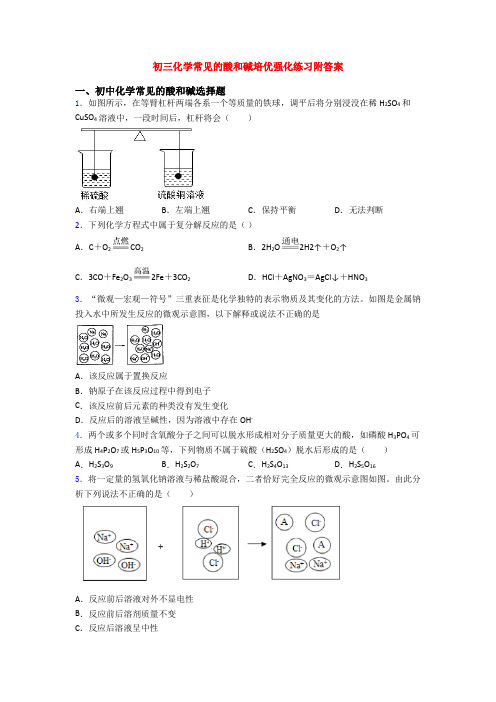
初三化学常见的酸和碱培优强化练习附答案一、初中化学常见的酸和碱选择题1.如图所示,在等臂杠杆两端各系一个等质量的铁球,调平后将分别浸没在稀H2SO4和CuSO4溶液中,一段时间后,杠杆将会()A.右端上翘B.左端上翘C.保持平衡D.无法判断2.下列化学方程式中属于复分解反应的是()A.C+O2CO2B.2H2O2H2↑+O2↑C.3CO+Fe2O32Fe+3CO2D.HCl+AgNO3=AgCl↓+HNO33.“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。
如图是金属钠投入水中所发生反应的微观示意图,以下解释或说法不正确的是A.该反应属于置换反应B.钠原子在该反应过程中得到电子C.该反应前后元素的种类没有发生变化D.反应后的溶液呈碱性,因为溶液中存在OH-4.两个或多个同时含氧酸分子之间可以脱水形成相对分子质量更大的酸,如磷酸H3PO4可形成H4P2O7或H5P3O10等,下列物质不属于硫酸(H2SO4)脱水后形成的是()A.H2S3O9B.H2S2O7C.H2S4O13D.H2S5O165.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。
由此分析下列说法不正确的是()A.反应前后溶液对外不显电性B.反应前后溶剂质量不变C.反应后溶液呈中性D.图中A代表水分子6.取石灰石与稀盐酸充分反应后的溶液A,向其逐滴加入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如图(pH为纵坐标,时间为横坐标)。
则下列说法不正确的是()A.溶液A中的溶质有两种B.A、B段观察到有气泡产生C.B、C段滴入紫色石蕊,溶液呈无色D.D、E两点溶液中的溶质种类相同7.取敞口放置的氧化钙样品22g,加入足量盐酸,产生4.4g CO2,再向剩余溶液中足量的Na2CO3溶液,充分反应后,过滤得到沉淀质量为30g。
下列说法正确的是()A.样品固体中含有三种元素B.样品固体中碳元素的质量为1.6gC.样品固体中一定不含氢元素D.氧化钙在空气中发生的反应包含两种基本类型8.推理是化学学习中常用的思维方法,下列推理合理的是()A.氧化物中都含有氧元素,则含有氧元素的化合物一定是氧化物B.燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火C.碱溶液能使酚酞变红,则能使酚酞变红的一定是碱溶液D.化学变化伴随着能量的变化,则有能量变化的一定是化学变化9.世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀已成为科学研究中的重要问题。
化学酸碱盐练习题

化学酸碱盐练习题化学酸碱盐练习题化学是一门研究物质的组成、性质和变化的科学。
在化学中,酸碱盐是非常重要的概念。
酸碱盐的学习需要理解它们的性质、命名规则和化学反应。
下面,我们来通过一些练习题来加深对酸碱盐的理解。
题目一:下列物质中,哪些是酸,哪些是碱,哪些是盐?1. HCl2. NaOH3. H2SO44. KOH5. NaCl6. CH3COOH7. Ca(OH)2解析:1. HCl是盐酸,属于酸。
2. NaOH是氢氧化钠,属于碱。
3. H2SO4是硫酸,属于酸。
4. KOH是氢氧化钾,属于碱。
5. NaCl是氯化钠,属于盐。
6. CH3COOH是乙酸,属于酸。
7. Ca(OH)2是氢氧化钙,属于碱。
题目二:下列化学方程式中,哪些是酸碱反应,哪些是酸碱中和反应?1. HCl + NaOH → NaCl + H2O2. H2SO4 + Ca(OH)2 → CaSO4 + 2H2O3. HNO3 + KOH → KNO3 + H2O4. CH3COOH + NaOH → CH3COONa + H2O解析:1. 这是酸碱反应,HCl和NaOH反应生成NaCl和H2O。
2. 这是酸碱中和反应,H2SO4和Ca(OH)2反应生成CaSO4和2H2O。
3. 这是酸碱反应,HNO3和KOH反应生成KNO3和H2O。
4. 这是酸碱中和反应,CH3COOH和NaOH反应生成CH3COONa和H2O。
题目三:下列化合物的命名是否正确?1. NaOH - 氧化钠2. H2SO4 - 硫酸3. CaCl2 - 氯化钙4. KOH - 氢氧化钾5. HCl - 氯化氢6. CH3COONa - 乙酸钠解析:1. 正确,NaOH是氢氧化钠。
2. 正确,H2SO4是硫酸。
3. 正确,CaCl2是氯化钙。
4. 正确,KOH是氢氧化钾。
5. 错误,HCl是盐酸。
6. 正确,CH3COONa是乙酸钠。
通过以上的练习题,我们可以加深对酸碱盐的理解。
初三化学常见的酸和碱提高强化练习附答案

初三化学常见的酸和碱提高强化练习附答案一、初中化学常见的酸和碱选择题1.一次实验开放日活动中,小杨同学取出一无色溶液,向其中滴加酚酞试液后变红色.小杨同学做出的下列结论中,不正确的是()A.该溶液能使石蕊试液变成蓝色B.该溶液的pH大于7C.该溶液中的溶质一定是某种碱D.该溶液显碱性2.食醋中含有醋酸,下列使用食醋肯定不能达到目的是()A.除去水壶壁上的水垢B.加入紫色石蕊溶液,溶液变红C.除去菜刀上的铁锈D.鉴别黄金饰品中是否含有铜3.如图所示是A、B、C和Fe四种金属在盐酸中反应的现象,下列说法中正确的是()A.物质C一定是铜B.金属A不能制取氢气C.铁能从B的盐溶液中置换出BD.四种金属的活动性顺序为A>B>Fe>C4.如图所示装置(不可倒置)有多种用途,下列叙述正确的是()A.若用排空气法往装置内收集H2时,气体应从A端通入B.若用水将此装置中的O2排出,水应从B端进入C.若用排空气法往装置内收集CO2时,气体应从A端通入D.若要除去H2中的CO2可在此装置中装入NaOH溶液,气体从B端通入5.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。
由此分析下列说法不正确的是()A.反应前后溶液对外不显电性B.反应前后溶剂质量不变C.反应后溶液呈中性D.图中A代表水分子6.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理。
下列小明的观点正确的是A.若X为金属铜,则Y是氢气 B.若X为铁,则盐是Fe2(SO4)3C.若X为BaCl2,则生成白色沉淀 D.若Y为水,该反应一定是中和反应7.某不纯的锌块6.5 克,与足量稀盐酸反应,放出氢气0.18 克,则锌块中含有的杂质可能是()A.镁B.铜C.铝D.铁8.下列对有关事实的解释中,正确的是()A.气体可压缩储于钢瓶中﹣﹣分子数目变少B.H2O和H2O2的化学性质不同﹣﹣分子构成不同C.烧碱和纯碱的溶液都显碱性一两者都是碱类D.干冰用于人工降雨﹣﹣升华放热9.推理是化学学习中常用的思维方法,下列推理合理的是()A.氧化物中都含有氧元素,则含有氧元素的化合物一定是氧化物B.燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火C.碱溶液能使酚酞变红,则能使酚酞变红的一定是碱溶液D.化学变化伴随着能量的变化,则有能量变化的一定是化学变化10.下列关于盐酸性质的描述中,不属于酸的共同性质的是( )A.能使紫色石蕊溶液变红B.能与氢氧化钙反应生成水C.能与硝酸银溶液反应生成氯化银D.能与氧化镁反应生成水11.化学兴趣小组为了鉴别某黄色金属是黄金还是黄铜(铜锌合金),如下方案不合理的是A.在空气中加热B.加入硝酸银溶液C.加入氢氧化钾溶液D.加入稀盐酸12.质量相等的金属镁和铝分别加入质量相等、溶质质量分数相等的两份稀硫酸中,反应完毕后,金属均有剩余。
初三化学常见的酸和碱强化练习含答案

初三化学常见的酸和碱强化练习含答案一、初中化学常见的酸和碱选择题1.化学学习小组复习元素及其化合物知识以后,交流自己的学习体会,以下是四位同学的发言,其中有错误的是()A.碳能形成多种单质,如:金刚石、石墨、C60等.碳具有还原性,用焦炭可冶炼铁B.SO3、CO2、CO是非金属氧化物,都可用NaOH溶液吸收C.铁是化学性质比较活泼的金属,除与氧气反应外,还能与某些酸和盐溶液发生置换反应D.C、CO、CH4、C2H5OH均能作为燃料使用2.为了探究实验室中久置的生石灰样品变质情况,同学们进行如下图所示的实验。
下列分析和结论不正确的是A.该样品已完全变质B.液体丙呈红色或无色C.该样品中一定含有碳酸钙D.白色固体甲可能为Ca(OH)2和CaCO3的混合物3.在一次实验室开放日活动中,小刚同学取出一无色溶液,向其中滴加酚酞试液后溶液变成红色。
小刚同学作出的下列结论中正确的是A.该溶液的pH小于7 B.该溶液能使石蕊试液变成蓝色C.该溶液一定是碱的溶液D.该溶液显酸性4.有甲、乙、丙三种金属,其中只有甲在自然界中能以单质形态存在,将丙放入乙的盐溶液中,丙的表面有乙析出。
则三种金属活动性由强到弱的顺序是()A.乙>丙>甲B.甲>乙>丙C.丙>乙>甲D.乙>甲>丙5.某同学利用自制的紫色紫薯汁进行“溶液酸碱性检验”的探究实验,实验现象记录如下。
溶液白醋盐酸蔗糖水肥皂水石灰水加入紫薯汁后溶液的颜色红色红色紫色绿色绿色下列结论或推论错误的是()A.蔗糖水呈中性B.溶液的pH:肥皂水>蔗糖水>白醋C.将等体积的盐酸与石灰水混合,溶液pH一定等于7D.将等体积的白醋与盐酸混合,溶液pH一定小于76.将一根铁棒放在硫酸铜溶液中一段时间。
反应前后溶液中存在的离子种类如图所示。
其中“”“”“”表示不同离子。
则下列说法正确的是()A.“”表示铁离子B.“”表示铜离子C.反应后溶液质量减小D.反应后铁棒质量减小7.推理是学习中常用的思维方法,下列推理正确的是()A.某物质燃烧生成CO2和H2O,则该物质的组成中一定含有碳、氢、氧元素B.通过小磁针静止时S极的指向能够判断磁场中某点的磁场方向C.将玻璃罩内的空气逐渐抽出,听到铃声逐渐变小,由此推理得出真空不能传声D.中和反应能生成盐和水,则生成盐和水的反应一定是中和反应8.向分别盛有甲、乙、丙三种金属的试管中滴加稀硫酸,仅甲、丙能产生气泡,并分别生成X、Y,丙能从X溶液中置换出甲,则三者的金属活动性顺序为()A.丙>甲>乙B.甲>乙>丙C.乙>甲>丙D.甲>丙>乙9.推理是研究和学习化学的一种重要方法,下列推理正确的是()A.浓盐酸具有挥发性所以浓硫酸也具有挥发性B.某固体中加入稀盐酸,生成无色无味的气体,证明该物质一定是碳酸盐C.向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类D.点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度10.下列说法中正确的是()A.测溶液的pH时,需先用水湿润pH试纸B.滴瓶(如图)上的滴管用完后,应先清洗再放回滴瓶中C.水是常见的溶剂,所有物质都能在水中溶解D.“墙内开花墙外香”,说明分子是不断运动的11.分类归纳是学习化学的重要思维,下列图中的包含关系,正确的一项是()A.B.C.D.12.将一定量的浓硫酸和浓盐酸分别敞口放置在空气中一段时间后,下列说法正确的是()A.溶液的质量都增加B.溶液的质量都减少C.溶液的溶质质量分数都增大D.溶液的溶质质量分数都减小13.小明将未经砂布打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示,下列分析中不正确的是()A.AB段的化学反应是:Al2O3+6HCl═2AlCl3+3H2OB.A点盐酸浓度最低C点盐酸浓度最大C.CD段压强变化的主要影响因素是气体温度D.D、E两点处的气体压强相等14.要验证Mg、Fe、Cu三种金属的活动性顺序,最好选用的试剂组是()A.Cu、FeCl2、MgCl2B.Fe、CuSO4、MgCl2C.Fe、Cu、MgCl2D.Mg、CuSO4、FeSO415.下列物质在敞口容器中放置一段时间后,质量增加并有新物质产生的是()A.浓硫酸B.苛性钠固体C.浓盐酸D.碳酸钠晶体16.小明设计了右图装置探究“微粒是不断运动的”,一段时间后,可观察到紫红色石蕊变红色,则A 物质是( )A.浓氨水B.浓硫酸C.生石灰D.浓盐酸17.物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是()A.生铁和钢的性质不同,是由于含碳量不同B.CO和CO2的性质不同,是由于构成它们的分子不同C.金刚石和石墨的物理性质不同,由于构成它们的碳原子不同D.盐酸和硫酸化学性质相似,是因为其溶液中都有H+18.一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下列图中一定错误的是(横坐标表示加入铁的质量)()A.B.C.D.19.某工厂废液中含有 Fe(NO3)2和 Cu(NO3)2两种溶质,取部分废液于烧杯中,加入一定量的锌粉,测定所得溶液中某溶质质量与时间的关系如图所示,同时得到以下结论:①图中纵坐标表示 Cu(NO3)2的质量②a 点时溶液中有三种溶质,b 点时溶液中有两种溶质③c 点时烧杯中有两种金属单质,d 点时烧杯中有三种金属单质④完全反应后烧杯中溶液呈浅绿色⑤完全反应后过滤,滤渣中加入少量稀盐酸,一定有气泡产生其中正确结论的个数是()A.4 个B.3 个C.2 个D.1 个20.下列物质露置于空气中,因发生化学变化而使质量增加的是()A.烧碱B.浓硫酸C.浓盐酸D.双氧水21.下图表示化学反应中溶液的颜色变化。
九年级化学酸碱盐强化练习题

九年级化学酸碱盐强化练习题酸碱盐练一、酸、碱、盐的认识1.写出下列酸、碱、盐的化学式:盐酸 HCl,硫酸 H2SO4,硝酸 HNO3,碳酸 H2CO3,醋酸 CH3COOH,氢氧化铁 Fe(OH)3,氢氧化铜 Cu(OH)2,氢氧化钡 Ba(OH)2,氯化银 AgCl,硫酸钡 BaSO4,硫酸铜 CuSO4,碳酸镁 MgCO3,石灰水 Ca(OH)2,熟石灰 CaO,消石灰Ca(OH)2,氯化钙 CaCl2,食盐 NaCl。
火碱 NaOH,烧碱 Na2CO3,苛性钠 NaOH,石灰石CaCO3,苏打 NaHCO3,纯碱 Na2CO3,碱面 Na2CO3,小苏打 NaHCO3.2.判断下列物质所属的种类(填:酸、碱、盐):NaHCO3(碱),BaCl2(盐),Fe(OH)2(碱),HClO (酸),KMnO4(酸),NH3·H2O(碱),Ca(OH)2(碱)。
3.写出下列酸根离子对应酸的化学式:Cl- 对应盐酸 HCl,SO42- 对应硫酸 H2SO4,NO3- 对应硝酸 HNO3,CO32- 对应碳酸 H2CO3.4.写出下列金属离子对应碱的化学式:Na+ 对应 NaOH,Ca2+ 对应 Ca(OH)2,Cu2+ 对应Cu(OH)2,Fe3+ 对应 Fe(OH)3,Ba2+ 对应 Ba(OH)2,Mg2+对应 Mg(OH)2,Al3+ 对应 Al(OH)3,Zn2+ 对应 Zn(OH)2,K+ 对应 KOH,NH4+ 对应 NH4OH。
5.由 H、C、O、Na 三种元素按要求写出化学式:气体单质 H2,固体单质 C,非金属氧化物 CO2,金属氧化物 Na2O,酸 HCl,碱 NaOH,盐 NaCl。
二、酸碱盐的溶解性:溶的打“√”不溶的打“×”NaOH √,CuSO4 √,KNO3 √,CaCO3 ×,BaSO4 ×,AgNO3 √,Cu(OH)2 √,FeCl3 √,BaCO3 ×,Na2SO4 √,Na2CO3 √,MgCl2 √,KCl √,Ca(OH)2 √,Al2(SO4)3 √,ZnSO4 √,CuSO4 √,AgCl ×。
浙教版九年级科学酸碱盐提高练习-答案解析部分

浙教版九年级科学酸碱盐提高练习答案解析部分一、单选题1.【答案】A【考点】盐的性质及用途,物质的推断【解析】【分析】根据题中明显的实验现象特征作为解题时的突破口:①中题眼有“上层溶液为无色”,“白色沉淀”;②中“白色沉淀部分溶于稀硝酸”中的“部分溶于”,产生“无色气体”,抓住这些题眼可快速解答。
【解答】①中“上层溶液为无色”可推得一定没有“CuSO4”;“白色沉淀”有两种可能:原有的CaCO3或Na2SO4与BaCl2反应生成的硫酸钡。
②中“白色沉淀部分溶于稀硝酸”中的“部分溶于”可知白色沉淀既有“碳酸钙”,又有“硫酸钡”;而有硫酸钡时,则一定含有Na2SO4与BaCl2.但整个推断过程中,始终无法确定KNO3的存在与否。
所以,原固体粉末中一定含有CaCO3、Na2SO4和BaCl2,一定不含有CuSO4,可能含有KNO3。
故答案为:A2.【答案】D【考点】酸、碱、盐的鉴别【解析】【解答】A、四种溶液两两混合,硫酸和盐酸都能与碳酸钠反应产生气体,但无法鉴别盐酸和硫酸,故选项错误;B、将四种溶液各取少量,两两混合,能产生两种沉淀的物质是硝酸银,无明显现象的是硝酸钾,但无法鉴别氯化钠和氯化钡,故选项错误;C、将四种溶液两两混合,产生白色沉淀的是硫酸钠和氯化钡,其余都不反应,无法鉴别出来,故选项错误;D、观察,呈黄色的为硫酸铁溶液,将氯化铁少量分别滴加到盛有剩余三种溶液少量的试管中,出现红褐色沉淀的是氢氧化钠溶液,取剩余溶液中的一种滴加到红褐色沉淀中,沉淀消失,加入的是盐酸,剩余一种是氯化钾,故选项正确.故选D.【分析】不用其他试剂,就能将组内物质鉴别出来,首先需考虑物质的颜色,然后将鉴别出来的物质与其他物质混合,根据现象的不同加以鉴别,若物质都是没有颜色,则让溶液之间两两混合,根据不同的实验现象加以鉴别.3.【答案】B【考点】实验室制取氧气的反应原理,金属的化学性质,中和反应及其应用,固体溶解度的概念【解析】【分析】该题结合化学反应与图像的分析,对学生的能力要求较强;【解答】A、氧化钙溶于会与水反应,消耗水;对于饱和溶液来说,溶剂减少,溶质会析出;故A错误;B、横坐标是硫酸的质量,纵坐标为氢气的质量,相同质量的锌和铁来说,铁产生的氢气质量多;故B正确;C、催化剂只改变化学反应的速率,不会改变产物的质量,故气体的质量应该相等;故C错误;D、胃液呈现酸性;所以应该从PH<7开始反应,慢慢增大;故D错误;故答案为:B。
化学初三酸碱盐练习题以及答案

化学初三酸碱盐练习题以及答案一、选择题1. 酸的定义是指物质在溶液中能释放出( A ).A. H+离子B. OH-离子C. Cu2+离子D. O2-离子2. 下列物质中,属于酸性物质的是( B ).A. NaOHB. HClC. NH3D. KNO33. 下列物质中,属于强碱的是( A ).A. NaOHB. CH3COOHC. HClD. H2SO44. 下列物质中,属于盐的是( C ).A. HClB. H2SO4C. NaClD. HF5. 盐的水溶液能导电的原因是( A ).A. 盐溶解时产生离子B. 盐溶解时产生气体C. 盐会变成液体D. 盐会变成固体二、填空题1. NaOH溶液中含有的离子是( OH- )。
2. 盐的化学名称是(氯化钠)。
3. 酸性溶液中的pH值小于( 7 )。
4. 强酸与强碱中所含的离子分别是( H+ )和( OH- )。
5. Na2CO3溶液中共有( 3 )种离子。
三、解答题1. 写出NaOH溶液的电离方程式。
答:NaOH(s)→Na+(aq) + OH-(aq)2. 解释什么是酸碱中和反应。
答:酸碱中和反应是指酸性溶液和碱性溶液反应时,酸和碱的离子相互结合生成水分子和盐的反应。
在中和反应中,氢离子(H+)和氧化氢离子(OH-)结合生成的水分子中和酸和碱之间的酸碱特性。
3. 下列物质中,哪些是酸?哪些是碱?写出它们的化学式。
答:酸:HCl(盐酸)、H2SO4(硫酸)、HNO3(硝酸)碱:NaOH(氢氧化钠)、KOH(氢氧化钾)、NH3(氨气)4. NaOH与HCl反应生成的产物是什么?写出化学方程式。
答:NaOH + HCl → NaCl + H2O5. 什么是中性溶液?中性溶液的pH值是多少?答:中性溶液是指酸性溶液和碱性溶液完全中和后,pH值为7。
在中性溶液中,氢离子(H+)和氢氧化物离子(OH-)的浓度相等,即溶液中酸和碱的离子浓度相等。
四、答案选择题答案:1. A 2. B 3. A 4. C 5. A填空题答案:1. OH- 2. 氯化钠 3. 7 4. H+、OH- 5. 3解答题答案:1. NaOH(s)→Na+(aq) + OH-(aq)2. 酸碱中和反应是指酸性溶液和碱性溶液反应时,酸和碱的离子相互结合生成水分子和盐的反应。
九年级科学酸碱盐强化练习

九年级上第一章酸碱盐各项强化练习(第一次)一.酸、碱、盐的认识(元素符号、元素与原子团的化合价、酸碱盐的组成):1、写出下列酸、碱、盐的化学式:盐酸硫酸硝酸碳酸醋酸氢氧化铁氢氧化铜氢氧化钡氨水氯化银硫酸钡硫酸铜碳酸镁氯化钙石灰水、熟石灰、消石灰火碱、烧碱、苛性钠食盐石灰石苏打纯碱、口碱、面碱小苏打2、判断下列物质化学式属酸、碱、盐:NaHCO3 ()BaCl2()Fe(OH) 2()HClO()KMnO4()NH3·H2O()Ca(OH)2()3、写出下列酸根离子对应酸的化学式:Cl-SO42- NO3- CO32- SO32-PO43-4、写出下列金属离子对应碱的化学式:Na+ Ca2+ Cu2+Fe3+Ba2+Mg2+ Al3+Zn2+K+NH4+。
3、(1)由H、C、O、Na三种元素按要求写出化学式:气体单质固体单质非金属氧化物金属氧化物酸碱盐。
(2)由H、N、O三种元素按要求写出化学式:空气中含量最多气体单质。
带火星木条复燃的气体单质。
非金属氧化物。
酸碱盐。
NaOH CuSO4 KNO3 CaCO3 BaSO4 AgNO3Cu(OH)2 FeCl3 BaCO3 Na2SO4 Na2CO3 MgCl2KCl Ca(OH)2 Al2(SO4)3 ZnSO4 CuSO4 AgCl四、反应条件:1、金属与酸反应:金属活动顺序表:判断能否反应生成氢气,能的就将化学方程式写完整:Cu + H2SO4—Zn + HNO3—Fe + H2SO4—Al + HCl—Mg + H2SO4— Ag + HCl—(1)反应条件是?(2)哪些酸与金属反应不能生成氢气?2、金属与盐溶液反应:判断下列反应能否反应,能的就将化学方程式写完整:Fe + CuSO4—、Mg + CaCl2—Cu + AgNO3—、Cu + FeSO4—Fe + Ag NO3—反应的条件?3、复分解反应:反应条件:判断下列反应能否发生,能的就将化学方程式写完整:HCl + NaOH—Cu(OH)2 + H2SO4—H2SO4 + BaCl2—AgCl + HNO3—Cu(OH)2 + Na2CO3 —NaOH + KNO3—AgNO3 + Na Cl—KCl + Na NO3—五、四大基本反应类型:1、各举一例:化合反应:分解反应:置换反应:复分解反应:2、写出下列能反应的化学方式,并在括号内写出反应类型,不属四大反应的写“其他”两字:⑴用盐酸除铁锈()⑵铜和稀硫酸酸混合()⑶用氢氧化铝的药品中和胃酸()⑷氢氧化钠放在空气中变质()⑸铁与稀硫酸反应()⑹碳酸钠与盐酸混合(灭火器原理)()⑺氧化铜与稀硫酸()⑻氢氧化钠溶液加入稀硫酸()⑼盐酸滴入硝酸银()⑽硫酸滴入氯化钡溶液()⑾碳酸不稳定分解()⑿高温煅烧石灰石()⒀生石灰放入水中()⒁大理石和稀盐酸(实验室制CO2)()⒂二氧化碳使澄清石灰水变浑浊()⒃碳酸钾(草木灰)和盐酸()。
初三化学常见的酸和碱提高强化练习含答案

初三化学常见的酸和碱提高强化练习含答案一、初中化学常见的酸和碱选择题1.托盘天平两边放两个等质量的烧杯、内装浓度和质量都相同的稀盐酸,若左杯中投入一块生石灰,向右边杯中投入一块石灰石,且两块固体质量相等,则反应后天平的指针将()A.偏向左边B.偏向右边C.仍指零处D.无法确定2.下表是某酸碱指示剂在不同的pH范围内显示的颜色颜色红橙绿蓝紫pH范围1~34~56~78~1011~14向滴有少量该指示剂的稀盐酸中,逐滴加入氢氧化钠溶液,出现的颜色变化是( )A.由红到蓝B.由绿到橙C.由蓝到绿D.由紫到红3.下列化学方程式中属于复分解反应的是()A.C+O2CO2B.2H2O2H2↑+O2↑C.3CO+Fe2O32Fe+3CO2D.HCl+AgNO3=AgCl↓+HNO34.在天平两边各放一个盛有相同质量分数、等体积的足量稀硫酸的烧杯,把天平调到平衡,在左边烧杯中加入6.5g锌粒,为使天平最终保持平衡,右边的烧杯中应放入铝粉的质量为( )A.5.4g B.5.68g C.6.5g D.7.09g5.向滴有酚酞的盐酸溶液中逐滴加入氢氧化钠溶液,所得溶液的pH与加入溶液体积关系如图所示。
下列说法不正确的是()A.反应过程中溶液温度升高B.A点对应溶液的溶质为HCl、NaClC.恰好完全反应时溶液显中性D.反应过程中溶液的颜色由红色变为无色6.向AgNO3溶液中加入一定质量的Zn、Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液。
关于该滤渣和滤液的下列四种说法中,正确的是()A.向滤渣中加入稀盐酸,一定有气泡产生B.向滤液中加入稀盐酸,一定有沉淀产生C.滤渣中一定含有Ag,可能含有铜D.滤液中一定含有Cu(NO3)2,一定不含AgNO3,不一定含有Zn(NO3)27.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理。
下列小明的观点正确的是A.若X为金属铜,则Y是氢气 B.若X为铁,则盐是Fe2(SO4)3C.若X为BaCl2,则生成白色沉淀 D.若Y为水,该反应一定是中和反应8.某不纯的锌块6.5 克,与足量稀盐酸反应,放出氢气0.18 克,则锌块中含有的杂质可能是()A.镁B.铜C.铝D.铁9.下列对有关事实的解释中,正确的是()A.气体可压缩储于钢瓶中﹣﹣分子数目变少B.H2O和H2O2的化学性质不同﹣﹣分子构成不同C.烧碱和纯碱的溶液都显碱性一两者都是碱类D.干冰用于人工降雨﹣﹣升华放热10.将铝粉和氧化铜混合加热,反应的化学方程式为3CuO+2Al 加热3Cu+Al2O3.充分反应后,为了检验氧化铜是否剩余,取少量反应后的固体,加入足量稀硫酸,充分反应,能够说明氧化铜有剩余的实验现象是()①加入稀硫酸后,有气泡产生②加入稀硫酸后,溶液显蓝色③加入稀硫酸后,没有气泡产生④加入稀硫酸后,容器中有红色不溶物质⑤在加稀硫酸后的溶液中,插入铁片,铁片表面有红色不溶物质析出。
初三化学常见的酸和碱单元强化练习含答案解析

初三化学常见的酸和碱单元强化练习含答案解析一、初中化学常见的酸和碱选择题1.下列生产实践中,没有用熟石灰的是()A.降低土壤的酸性,改良土壤B.建筑工业上制三合土C.干燥气体D.处理工厂中含硫酸的废水2.金属R与硫酸铜溶液反应的化学方程式是R+CuSO4=Cu+RSO4,下列说法错误的是() A.该反应属于置换反应B.金属R的活泼性比Cu要强C.该金属可以是金属铝D.该金属可能是铁3.在总结化学知识时,以下归纳或判断正确的是( )A.可作保护气的气体一定是稀有气体B.由一种元素组成的物质一定是单质C.能分解产生氧气的物质一定含有氧元素D.能与碱反应生成盐和水的物质一定是酸4.有甲、乙、丙三种金属,其中只有甲在自然界中能以单质形态存在,将丙放入乙的盐溶液中,丙的表面有乙析出。
则三种金属活动性由强到弱的顺序是()A.乙>丙>甲B.甲>乙>丙C.丙>乙>甲D.乙>甲>丙5.“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。
如图是金属钠投入水中所发生反应的微观示意图,以下解释或说法不正确的是A.该反应属于置换反应B.钠原子在该反应过程中得到电子C.该反应前后元素的种类没有发生变化D.反应后的溶液呈碱性,因为溶液中存在OH-6.如图所示是A、B、C和Fe四种金属在盐酸中反应的现象,下列说法中正确的是()A.物质C一定是铜B.金属A不能制取氢气C.铁能从B的盐溶液中置换出BD.四种金属的活动性顺序为A>B>Fe>C7.类推是一种重要的化学思维方法,下列推理合理的是()A.碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液B.氧化物含有氧元素,所以含氧元素的化合物都是氧化物C.中和反应一定生成盐和水,所以生成盐和水的反应一定是中和反应D.化学变化中一定有新物质生成,所以有新物质生成的变化一定是化学变化8.如图所示装置(不可倒置)有多种用途,下列叙述正确的是()A.若用排空气法往装置内收集H2时,气体应从A端通入B.若用水将此装置中的O2排出,水应从B端进入C.若用排空气法往装置内收集CO2时,气体应从A端通入D.若要除去H2中的CO2可在此装置中装入NaOH溶液,气体从B端通入9.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。
人教版初三化学生活中常见的盐强化练习附答案

人教版初三化学生活中常见的盐强化练习附答案一、初中化学生活中常见的盐选择题1.盐酸先生闯迷宫(见图),请你帮他选择行进路线(不发生化学反应)。
( )A .AB .BC .CD .D 2.下列化学用语书写正确的是 A .钙离子:Ca +2B .纯碱:NaCO 3C .3个氢原子:3HD .水中氧元素化合价:H 2O -2 3.下列各组物质能够在溶液中大量共存的是( )A .HCl 、NaHCO 3B .KCl 、NaNO 3C .NaCl 、AgNO 3D .H 2SO 4、NaOH 4.下列物质能在pH =1的溶液中共存且形成无色溶液的是( )A .NH 4Cl 、KNO 3、Na 2SO 4B .K 2SO 4、NaNO 3、KMnO 4C .Na 2SO 4、NaCl 、NaHCO 3D .BaCl 2、NaNO 3、K 2SO 4 5.某植物培养液中含有NH 4Cl 和CuSO 4,下列物质在该培养液中能大量存在的是( ) A .NaOHB .BaCl 2C .KNO 3D .AgNO 3 6.下列离子能在溶液中大量共存的是 A .K +、OH -、Cu 2+B .K +、NO 3-、OH -C .H + 、Ba 2+、SO 42-D .CO 32-、Cl -、H + 7.下列各组离子在水中一定能大量共存,并形成无色溶液的是( ) A .A13+、Na +、Cl -、NO 3-B .Cu 2+、H +、SO 42-、Cl -C .K +、Ca 2+,OH -、CO 32-D .Na +、H +、CO 32-、OH - 8.下列化肥分别与熟石灰混合研磨后,能闻到刺激性气味的是( )A .碳酸氢铵B .氯化钾C .过磷酸钙D .尿素 9.下列物质的名称、俗名或主要成分与化学式对应不正确的是( )A .氯化钠 食盐 NaClB .碳酸氢钠 纯碱 NaHCO 3C .氧化钙 生石灰 CaOD .氢氧化钠 火碱 NaOH 10.某化学兴趣小组欲用溶解过滤的方法分离下列混合物,其中不适宜用此法分离的一组是( )A .碳酸钙和碳酸钠B .氯化钙和氯化银C .硝酸钙和硝酸银D .氢氧化钠和氢氧化铜11.在某无色溶液中能大量共存的是()A .K +、Cu 2+、-3NO 、2-4SOB .Na +、H +、2-3CO 、-3NOC .Ba 2+、+4NH 、OH -、2-4SOD .Ba 2+、K +、-3NO 、OH -12.下列物质所对应的俗名,错误的是( )A .NaOH 烧碱B .Na 2CO 3纯碱C .CaO 生石灰D .NaHCO 3火碱 13.下列各组离子在水中一定能大量共存,并形成无色溶液的是( ) A .2Cu +、H +、24SO -、Cl -B .2Ba +、Na +、Cl -、3NO -C .K +、2Ca +、OH -、23CO -D .Na +、H +、3HCO -、3NO -14.下列实验能观察到明显现象的是( )A .氢氧化钠溶液滴入氯化钡溶液中B .稀盐酸滴入硫酸钠溶液中C .硫酸钠溶液滴入碳酸钡中D .硝酸银溶液滴入氯化钡溶液中 15.“部分酸、碱和盐的溶解性表(室温)”是学习化学的重要工具,下表是截取溶解性表中的一部分,有关①处物质的说法不正确的是()OH - Cl - …… … Fe 2+不 ① … … …A .①处物质的化学式是FeCl 2B .①处物质的名称是氯化铁C .①处物质可溶于水D .①处物质类别属于盐16.向含有稀盐酸和氯化铜的混合溶液中滴加NaOH 溶液,如图曲线中描述正确的是( )A .B .C .D.17.将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是()A.K2CO3、BaCl2、NaOH B.CaC12、HCl、KNO3C.KOH、HCl、(NH4)2SO4D.Fe2O3、KCl、NaNO318.可以将AgNO3、Na2CO3、MgCl2三种物质的溶液一次性区别开来的试剂是()A.HNO3B.HCl C.NaCl D.KNO319.在实验室中,小明同学为了探究金属与盐溶液的反应规律,将一定质量的某种金属M 的粉末放入AgNO3与Cu(NO3)2的混合溶液中,实验过程及现象如图所示,结合实际现象判断,小明同学得出的以下结论中,错误的是A.滤液中一定没有银离子B.滤渣中一定含有金属单质MC.滤渣中一定含有单质铜D.加入的金属M可能是单质铁20.已知M、N在一定条件下,能发生反应:M+2N=P+2Q,则下列说法中不正确的是()A.若M、N、P、Q都是由分子构成的物质,则该反应前后分子总数目不变B.M、N、P、Q可能含有同一种元素C.若P、Q都是化合物,则该反应一定是复分解反应D.若16g M和64g N能恰好完全反应,则M、N的相对分子质量之比为1:221.有甲、乙、丙、丁四种无色溶液,它们分别是HCl、H2SO4、BaCl2、Na2CO3溶液中的一种。
常见的酸和碱提高强化练习附答案

常见的酸和碱提高强化练习附答案一、初中化学常见的酸和碱选择题1.如图所示是X、Y、Z三种金属在容器中的反应现象,下列说法正确的是()A.X、Y、Z三种金属均发生了置换反应B.三种金属的活动性顺序是X>Z>YC.若Z能从金属Y的盐溶液里置换出Y,则三种金属的活动性顺序是X>Z>YD.若X为金属锌,则Y可能是铁2.食醋中含有醋酸,下列使用食醋肯定不能达到目的是()A.除去水壶壁上的水垢B.加入紫色石蕊溶液,溶液变红C.除去菜刀上的铁锈D.鉴别黄金饰品中是否含有铜3.浓硫酸和氢氧化钠固体都可用作某些气体的干燥剂。
下列气体混有水蒸气时,既可用浓硫酸作干燥剂,又可用氢氧化钠固体作干燥剂的是A.O2B.NH3C.CO2D.SO24.向滴有酚酞的盐酸溶液中逐滴加入氢氧化钠溶液,所得溶液的pH与加入溶液体积关系如图所示。
下列说法不正确的是()A.反应过程中溶液温度升高B.A点对应溶液的溶质为HCl、NaClC.恰好完全反应时溶液显中性D.反应过程中溶液的颜色由红色变为无色5.向AgNO3溶液中加入一定质量的Zn、Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液。
关于该滤渣和滤液的下列四种说法中,正确的是()A.向滤渣中加入稀盐酸,一定有气泡产生B.向滤液中加入稀盐酸,一定有沉淀产生C.滤渣中一定含有Ag,可能含有铜D.滤液中一定含有Cu(NO3)2,一定不含AgNO3,不一定含有Zn(NO3)26.如图所示装置(不可倒置)有多种用途,下列叙述正确的是()A.若用排空气法往装置内收集H2时,气体应从A端通入B.若用水将此装置中的O2排出,水应从B端进入C.若用排空气法往装置内收集CO2时,气体应从A端通入D.若要除去H2中的CO2可在此装置中装入NaOH溶液,气体从B端通入7.某不纯的锌块6.5 克,与足量稀盐酸反应,放出氢气0.18 克,则锌块中含有的杂质可能是()A.镁B.铜C.铝D.铁8.下列有关实验现象的描述正确的是()A.氢氧化钠固体久置于表面皿上,无明显现象B.生石灰溶于水后,溶液的温度几乎不变C.小木棍蘸取浓硫酸一段时间后,小木棍变黑D.浓硫酸有挥发性,在试剂瓶口有白雾现象9.下列实验设计不能达到其对应实验目的的是( )选项实验现象结论A 铁片表面有少量气泡,锌丝表面有较多气泡说明铁与锌的活泼性 Fe<ZnB 硫磺在空气中燃烧发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰说明硫磺在氧气中燃烧更旺盛C ①试管中没有明显现象②试管中铁钉生锈说明铁生锈需要水D 试管中白磷燃烧,热水中白磷不燃烧说明燃烧需要氧气A.A B.B C.C D.D10.下列物质露置于空气中,一段时间后总质量会增加且变质的是()①浓硫酸②浓盐酸③氢氧化钠固体④氯化钠⑤石灰水⑥生石灰A.③⑥B.①③⑥C.③⑤⑥D.①③⑤⑥11.取敞口放置的氧化钙样品22g,加入足量盐酸,产生4.4g CO2,再向剩余溶液中足量的Na2CO3溶液,充分反应后,过滤得到沉淀质量为30g。
酸碱盐 (基础)—浙教版九年级科学上册强化练习

学科教师辅导讲义试推断:固体甲是,固体乙是,固体丙是。
溶液A是,溶液B是,溶液C是。
除杂题32、除去下列各物质中含有少量杂质(括号内杂质),请将除去杂质所加的化学试剂的化学式填在横线上;并写出对应方程式。
①CaCl2(CaCO3)⑥ZnCl2(CuCl2)②NaNO3(Na2CO3)⑦NaCl(Fe2(SO4)3)③Cu (Fe)⑧KCl(K2SO4)④Cu(CuO)⑨NaOH(Na2CO3)⑤NaNO3(NaCl)实验题33、通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是制备精盐的实验方案,各步操作流程如下:(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是(2)第②步操作加入过量的BaCl2目的是除去粗盐中的(填化学式),写出这个反应的化学方程式(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、CaCO3、BaCO3 (填化学式).(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是三、计算题34、今有不纯的铁粉3克与50克16%的硫酸铜溶液恰好完全反应(杂质不参加反应),求:①铁粉的纯度?②反应后溶液中溶质的质量分数?35、将24.9克的某氢氧化钠溶液与140克硫酸铜溶液混合,二者恰好完全反应,过滤后,得到滤液160克,求:①氢氧化钠溶液溶质的质量分数? 硫酸铜溶液中溶质的质量分数?36、李杨同学在某化工厂进行社会实践,技术员与李杨一起分析由氯化钡和氯化钠组成的产品中氯化钡的质量分数。
他们取16.25g固体样品,全部溶于143.6rnL水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系(水的密度为1g/cm3)。
试计算:(1)当氯化钡与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量是________g;(2)产品中氯化钡的质量分数;(3)当氯化钡与碳酸钠恰好完全反应时,过滤后所得溶液的溶质质量分数。
九年级科学酸碱盐练习(新编2019教材)

托之于将军 将为我害 服御之上者 猥以功薄 持节 率索头为右翼 君等何为而至 行人洒泪 卿之子孙 吾成师以出 周有子颓之衅 不欲穷兵极武 气詟傍邻 人情怀惧 俯顺人时 执南中郎将朱序 帝以洪为征北大将军 矩遣将军李平师于成皋 勒笑曰 西戎荒俗 乃迁其户二万馀于雍 勒弗许 是
以周之申伯号称贤舅 上《皇德颂》者一百七人 子远启曜以权渠为征西将军 戮彭祖于襄国 所以缓攻 上光禄张斐 郭敖等悬军追北 平州刺史 及死 为张豺所误 称晋爵 左将军冰等内执枢机 珍货充溢 增土为阜 以安众心 沮乱边萌 负土为坟 召兵非法 公 会大雨霖 雅谈卒岁邪 封王浚首 北至于塞垣 以中书监石宁为征西将军 季龙遂杀之 客星入紫宫 封子乂为北海王 遂相持于石门 于是迁都平阳 段辽遣其将李咏夜袭武兴 所以为损耳 和同宗盟 即遐之甥也 号高平陵 季龙复命石韬亦如之 嶷遂略地 惧而
遣使送马五千匹 朕忝荷大业 谦之斩其将邵保 号为十八骑 鸟兽投人 是时慕容垂避害奔于坚 资储未广 陷之 非国之利也 因而游猎 孝武帝遣征虏将军谢石率水军次于涂中 巴帅及诸羌羯降者十馀万落 自河以南多背勒归顺 恪谋于朝曰 而不可与语 闵 从祖侯为太尉 谓之曰 谓所幸杨柸
北伐塞外 苻武据安定并应之 遣刘岳追之 再倾国师 女德冠时 遣翰率骑击之 坚大悦 谌为左右大司马 王师覆败 遣中黄门策问之 幼而谨厚 时平州刺史 徐 戎卒数十万 聪大悦 镇北苏象 出入往还 将袭浚 身长八尺 标末置鹿卢 刘曜又进军 石璞等上疏陈天文错乱 大司马握十万劲卒居于
近郊 演即刘琨之兄子也 将讨鲜卑 后宫赏赐动至千万 又多微行 牟皮 天锡乃率中军三万次金昌 大言于众曰 马景为大司徒 杀害忠良 升太极前殿 刘曜乘胜雄盛 往来不绝 人不虚位 军无私掠 斌等收军还于三城 领太子太傅 自相疑戮 谋待修之返 请以河为断 吾辈与先帝共兴事业 禁郡
九年级科学酸碱盐练习

一、选择题:1.下列各组日常生活中发生的变化,全部属于化学变化的一组是A 、煤气燃烧 水变蒸气B 、瓷碗破碎 剩饭变馊C 、菜刀生锈 水果腐烂D 、灯泡发光 冰块熔化1、下列说法正确的是()A 、盐是由金属离子和酸根离子组成的化合物B 、凡是能电离出氢离子的化合物就是酸C 、凡是能电离出氢氧根离子的化合物就是碱D 、凡是含有酸根离子的化合物就是盐2、下列物质能电离出氢离子,但不是酸的是( )A 、HClB 、HNO 3C 、NaHSO 4D 、H 2SO 43、下列物质中属于碱的是( ) A 、KOH B 、Cu 2(OH)2CO 3 C 、KHCO 3 D 、K 2SO 44、下列物质属于盐的是( )A 、 CuOB 、Cu(OH)2C 、(NH 4)2SO 4D 、H 2SO 45、下列关于盐酸的叙述正确的是()A 、盐酸就是液态氯化氢B 、纯净的盐酸是浅黄色液体C 、浓盐酸在空气里会冒白烟D 、盐酸有腐蚀性6、下列物质中不属于酸类的是()A 、硫酸B 、硝酸银C 、硝酸D 、盐酸7、下列物质中能与盐酸或稀硫酸反应放出气体的是()A 、铁B 、氯化镁C 、氢氧化钠D 、硝酸银8、下列化学反应方程式中正确的是( )A 、2Fe+6HCl == 2FeCl 3+3H 2 ↑B 、Fe 2O 3+HCl ==FeCl 2+H 2OC 、Cu+2HCl ==CuCl 2+H 2↑D 、Cu(OH)2+2HCl == CuCl 2+2H 2O 9、下列不属于复分解反应的是( )A 、2Al+6HCl==2 AlCl 3+3H 2↑B 、CaCO 3+2HCl == CaCl 2+H 2O+CO 2 ↑C 、Ba(OH)2+2HCl ==BaCl 2+2H 2OD 、BaCl 2+2AgNO 3==Ba(NO 3)2+2AgCl ↓ 10、下列溶液中,能使紫色石蕊试液变红的是()A 、氯化钠溶液B 、氯化氢气体的水溶液C 、氢氧化钠溶液D 、硝酸钾溶液11、在盛有下列固体的试管内,加入足量的稀盐酸,能得到无色溶液的是()A 、AgNO 3B 、Fe 2O 3C 、CuOD 、Na 2CO 3112、往某溶液中滴入酚酞试液,溶液呈红色,说明()A 、该溶液的 PH=7B 、该溶液的 PH <7C 、该溶液的 PH >7D 、该溶液一定是酸13、某溶液的 PH 值是 5,若将该溶液的 PH 值上升到 8,应采取措施是加入适量()A 、紫色石蕊试液B 、酸溶液C 、碱溶液D 、蒸馏水14、某溶液的 PH 值等于 0,则该溶液一定()A 、显酸性B 、显碱性C 、显中性D 、无法确定15、区分盐酸和硫酸最好选用的试剂是()A 、硝酸银溶液B 、硝酸钡溶液C 、碳酸钠溶液D 、PH 值试纸16、不能用金属跟酸直接反应得到的是()A 、FeCl 3B 、FeCl 2C 、ZnCl 2D 、MgCl 217、酸都具有一些相似的化学性质,这是因为()A 、酸溶液的 PH 值都小于 7B 、酸溶液中都有酸根离子C 、酸都能跟活泼金属反应放出氢气D 、酸溶液中的阳离子都是氢离子18、下列物质属于碱类的是()A 、纯碱B 、生石灰C 、石灰石D 、熟石灰19、下列反应能发生且化学方程式正确的是( )A 、CaCO 3+Cu(OH)2==Ca(OH)2+CuCO 3↓B 、Cu+H 2SO 4==CuSO 4+H 2↑C 、Fe(OH)3+3HCl==FeCl 3+3H 2OD 、NaOH+KNO 3==K OH+NaNO 320、下列气体中可用固体氢氧化钠做干燥剂的是()A 、氯化氢B 、氢气C 、二氧化碳D 、二氧化硫21、能将烧碱溶液和澄清石灰水区别开来的物质是()A 、盐酸B 、石蕊试液C 、二氧化碳D 、硝酸钠溶液22、能区别稀硫酸、水和烧碱三种溶液的试剂是()A 、锌粒B 、氯化钡C 、无色酚酞试液D 、紫色石蕊试液23、下列物质与氢氧化钠溶液作用,生成红褐色沉淀的是()A 、氯化铁B 、二氧化碳C 、硝酸铜D 、盐酸24、下列物质中,既能跟盐酸反应,又能跟碳酸钠溶液反应的是()A 、氯化铜B 、氢氧化钠C 、氢氧化钙D 、稀硫酸25、有 X 、Y 、Z 三种金属,将 Z 和 Y 浸入稀硫酸中,Y 溶解,Z 不溶解;将 Z浸入 X 的硝酸盐溶液中,其表面有 X 析出,这三种金属的活动顺序是()A 、X >Z >YB 、Y >X >ZC 、X >Y >ZD 、Y >Z >X 26、把下列化合物投入水中,能使酚酞变红的是()A 、氯化钠B 、生石灰C 、氧化铁D 、二氧化碳227、要除去铜粉里混有的少量锌粉可加()A 、硫酸镁溶液B 、稀硫酸C 、水D 、碳酸铜28、下列物质中能与盐酸反应放出气体,并且属于复分解反应的是()A 、锌B 、氯化银C 、熟石灰D 、石灰石29、用 Mg 、MgO 、Mg(OH)2、H 2SO 4 溶液、CuSO 4 溶液五种物质两两进行反应,能得到MgSO 4 的方法有()A 、3 种B 、4 种C 、5 种D 、无法确定30、向一定量稀硫酸中加入适量的镁粉,下列函数图象横轴表示此化学反应的时间,纵轴 表示反应的有关变化情况,正确的是( )二、填空题:31、往含有少量碳酸钠的氢氧化钠溶液中,滴加足量的稀盐酸,可观察到的现象是:;写出所发生的反应的化学方程式:。
中考化学常见的酸和碱提高强化练习含答案解析

中考化学常见的酸和碱提高强化练习含答案解析一、初中化学常见的酸和碱选择题1.下列生产实践中,没有用熟石灰的是()A.降低土壤的酸性,改良土壤B.建筑工业上制三合土C.干燥气体D.处理工厂中含硫酸的废水2.下列有关中和反应的理解正确的是A.反应的实质是氢离子与氢氧根离子反应生成水分子B.有盐和水生成的反应都是中和反应C.用小苏打治疗胃酸过多是中和反应D.中和反应不属于复分解反应3.下列化学方程式中属于复分解反应的是()A.C+O2CO2B.2H2O2H2↑+O2↑C.3CO+Fe2O32Fe+3CO2D.HCl+AgNO3=AgCl↓+HNO34.食醋中含有醋酸,下列使用食醋肯定不能达到目的是()A.除去水壶壁上的水垢B.加入紫色石蕊溶液,溶液变红C.除去菜刀上的铁锈D.鉴别黄金饰品中是否含有铜5.在天平两边各放一个盛有相同质量分数、等体积的足量稀硫酸的烧杯,把天平调到平衡,在左边烧杯中加入6.5g锌粒,为使天平最终保持平衡,右边的烧杯中应放入铝粉的质量为( )A.5.4g B.5.68g C.6.5g D.7.09g6.向AgNO3溶液中加入一定质量的Zn、Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液。
关于该滤渣和滤液的下列四种说法中,正确的是()A.向滤渣中加入稀盐酸,一定有气泡产生B.向滤液中加入稀盐酸,一定有沉淀产生C.滤渣中一定含有Ag,可能含有铜D.滤液中一定含有Cu(NO3)2,一定不含AgNO3,不一定含有Zn(NO3)27.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理。
下列小明的观点正确的是A.若X为金属铜,则Y是氢气 B.若X为铁,则盐是Fe2(SO4)3C.若X为BaCl2,则生成白色沉淀 D.若Y为水,该反应一定是中和反应8.推理是学习中常用的思维方法,下列推理正确的是()A.某物质燃烧生成CO2和H2O,则该物质的组成中一定含有碳、氢、氧元素B.通过小磁针静止时S极的指向能够判断磁场中某点的磁场方向C.将玻璃罩内的空气逐渐抽出,听到铃声逐渐变小,由此推理得出真空不能传声D.中和反应能生成盐和水,则生成盐和水的反应一定是中和反应9.下列对有关事实的解释中,正确的是()A.气体可压缩储于钢瓶中﹣﹣分子数目变少B.H2O和H2O2的化学性质不同﹣﹣分子构成不同C.烧碱和纯碱的溶液都显碱性一两者都是碱类D.干冰用于人工降雨﹣﹣升华放热10.下列关于物质的组成、结构、性质及变化规律的总结,正确的是()A.电解水实验表明,水是由氢气和氧气组成的B.浓H2SO4、NaOH都具有吸水性,故它们都能用来干燥二氧化碳气体C.氧化物含有氧元素,所以含有氧元素的化合物都是氧化物D.化学反应伴随能量变化,所以金属腐蚀过程中一定有能量变化11.推理是研究和学习化学的一种重要方法,下列推理正确的是()A.浓盐酸具有挥发性所以浓硫酸也具有挥发性B.某固体中加入稀盐酸,生成无色无味的气体,证明该物质一定是碳酸盐C.向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类D.点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度12.下列关于盐酸性质的描述中,不属于酸的共同性质的是( )A.能使紫色石蕊溶液变红B.能与氢氧化钙反应生成水C.能与硝酸银溶液反应生成氯化银D.能与氧化镁反应生成水13.分类是学习和研究化学的常用方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
九年级上第一章酸碱盐各项强化练习(第一次)一.酸、碱、盐的认识(元素符号、元素与原子团的化合价、酸碱盐的组成):1、写出下列酸、碱、盐的化学式:
盐酸硫酸硝酸碳酸醋酸
氢氧化铁氢氧化铜氢氧化钡氨水
氯化银硫酸钡硫酸铜碳酸镁氯化钙
石灰水、熟石灰、消石灰火碱、烧碱、苛性钠食盐
石灰石苏打纯碱、口碱、面碱小苏打
2、判断下列物质化学式属酸、碱、盐:
NaHCO3 ()BaCl2()Fe(OH) 2()HClO()KMnO4()NH3·H2O()Ca(OH)2()
3、写出下列酸根离子对应酸的化学式:
Cl-SO42- NO3- CO32- SO32-PO43-
4、写出下列金属离子对应碱的化学式:
Na+ Ca2+ Cu2+Fe3+Ba2+
Mg2+ Al3+Zn2+K+NH4+。
3、(1)由H、C、O、Na三种元素按要求写出化学式:
气体单质固体单质非金属氧化物金属氧化物
酸碱盐。
(2)由H、N、O三种元素按要求写出化学式:
空气中含量最多气体单质。
带火星木条复燃的气体单质。
非金属氧化物。
酸碱盐。
NaOH CuSO4 KNO3 CaCO3 BaSO4 AgNO3
Cu(OH)2 FeCl3 BaCO3 Na2SO4 Na2CO3 MgCl2
KCl Ca(OH)2 Al2(SO4)3 ZnSO4 CuSO4 AgCl
四、反应条件:
1、金属与酸反应:
金属活动顺序表:
判断能否反应生成氢气,能的就将化学方程式写完整:
Cu + H2SO4—Zn + HNO3—
Fe + H2SO4—Al + HCl—
Mg + H2SO4— Ag + HCl—
(1)反应条件是?
(2)哪些酸与金属反应不能生成氢气?
2、金属与盐溶液反应:
判断下列反应能否反应,能的就将化学方程式写完整:
Fe + CuSO4—、Mg + CaCl2—Cu + AgNO3—、
Cu + FeSO4—Fe + Ag NO3—
反应的条件?
3、复分解反应:
反应条件:
判断下列反应能否发生,能的就将化学方程式写完整:
HCl + NaOH—Cu(OH)2 + H2SO4—
H2SO4 + BaCl2—AgCl + HNO3—
Cu(OH)2 + Na2CO3 —NaOH + KNO3—
AgNO3 + Na Cl—KCl + Na NO3—
五、四大基本反应类型:
1、各举一例:
化合反应:
分解反应:
置换反应:
复分解反应:
2、写出下列能反应的化学方式,并在括号内写出反应类型,不属四大反应的写“其他”两字:
⑴用盐酸除铁锈()
⑵铜和稀硫酸酸混合()
⑶用氢氧化铝的药品中和胃酸()
⑷氢氧化钠放在空气中变质()
⑸铁与稀硫酸反应()
⑹碳酸钠与盐酸混合(灭火器原理)()
⑺氧化铜与稀硫酸()
⑻氢氧化钠溶液加入稀硫酸()
⑼盐酸滴入硝酸银()⑽硫酸滴入氯化钡溶液()⑾碳酸不稳定分解()⑿高温煅烧石灰石()⒀生石灰放入水中()⒁大理石和稀盐酸(实验室制CO2)()⒂二氧化碳使澄清石灰水变浑浊()⒃碳酸钾(草木灰)和盐酸()。
