3_氨基_4_甲基_6_甲氧基_7_羟基香豆素的合成研究
香豆素波谱解析

只有苯环上有取代基 的香豆素 如: 7-羟基香豆素
简单香豆素
取代基:
羟基、烷氧基、苯基、异戊烯基等。
HO O O
由于绝大多数香豆素在C7位都有含氧
官能团存在,因此,7-羟香豆素可以 认为是香豆素类成分的母体。
7-羟基香豆素
HO O O
HO
O
O
HO O O O
环 合 的 形 成 过 程
O HO
O
O
补骨脂内酯
O O O
白芷内酯
O
O
O
线型:补骨脂内酯型 6,7- 呋喃骈香豆素型
角型:异补骨脂内酯型 7,8- 呋喃骈香豆素型
呋喃香豆素(线型和角型)
• 直线型分子是由C-6异戊二烯与C-7位羟基环合而 4 5 成,三个环在一直线上。 6 10
274 nm——苯环
最大吸收向红位移。
311 nm——吡喃酮环
香豆素波谱解析
(二)红外光谱 3025 ~ 3175 cm-1—— C-H 伸缩振动 1700 ~ 1750 cm-1—— 羰基伸缩振动
1500 ~ 1600 cm-1—— 芳环吸收
1600 ~ 1650 cm-1—— 出现1-3个较强峰
香豆素波谱解析
(五)质谱 香豆素类化合物有如下特点:
有强的分子离子峰;
基峰是失去CO的苯骈呋喃离子;
主要裂解途径是:首先失去CO。
香豆素波谱举例
香豆素波谱举例
OR1 H H
RO H
O
O
C6-H d, J=2 Hz C8-H d, J=2 Hz C6-H 尖峰 区别 C8-H 与C4-H有远程偶合
7-羟基-4-甲基香豆素的合成

7-羟基-4-甲基香豆素的合成
7-羟基-4-甲基香豆素,也称为香豆素-4-酚,是一种重要的有机化合物,广泛应用于医药、化妆品、食品等领域。
本文将介绍7-羟基-4-甲基香豆素的合成方法。
1. 从天然产物中提取
7-羟基-4-甲基香豆素可以从植物中提取得到,如黄芩、桉树、莪术等。
但是,这种方法的产量较低,成本较高,不适合大规模生产。
2. 化学合成
目前,化学合成是7-羟基-4-甲基香豆素的主要生产方法。
以下是一种常用的合成方法:
首先,将苯甲醛和乙酸乙酯在碱性条件下反应,得到2-苯基-2-羟基乙酸乙酯。
然后,将2-苯基-2-羟基乙酸乙酯和丙酮在酸性条件下反应,得到7-羟基-4-甲基香豆素。
这种方法具有反应条件温和、产率高等优点,但需要使用一些有毒有害的试剂,对环境和人体健康有一定的危害。
3. 微生物发酵
近年来,微生物发酵合成7-羟基-4-甲基香豆素的方法也得到了广泛关注。
通过筛选和改良微生物菌株,可以实现高效、低成本的合成。
总的来说,7-羟基-4-甲基香豆素是一种重要的有机化合物,其合成方法多种多样,可以根据实际需要选择合适的方法进行生产。
7-羟基-4-甲基香豆素的合成研究

7-羟基-4-甲基香豆素的合成研究
陈闻起
【期刊名称】《化工时刊》
【年(卷),期】2011(025)006
【摘要】以间苯二酚和乙酰乙酸乙酯为原料,有机酸和固体超强酸作为催化剂,合成了7 -羟基-4-甲基香豆素.实验结果表明:间苯二酚、乙酰乙酸乙酯物质的量比为1:1,催化剂对甲苯磺酸用量为1.5%(物质的量百分比),85℃下反应2h,产率较高为85.1%.
【总页数】3页(P18-19,44)
【作者】陈闻起
【作者单位】常州工程职业技术学院制药系,江苏常州213164
【正文语种】中文
【相关文献】
1.7-羟基-4-甲基香豆素缩缬氨酸-邻菲咯啉-铜对乳腺癌MCF-7细胞增殖及凋亡的影响及其作用机制 [J], 虞浩;肖秀娣;徐雪松;李巧玉
2.7-羟基-4-甲基香豆素的合成及其荧光性质研究 [J], 陈爱乾;侯慧静;唐大梅;胡云
3.离子液体催化合成7-羟基-4-甲基香豆素的研究 [J], 陈昊;顾若楠;陈关虎;倪雨铃;蔡雯菁;汤小芳;张勤
4.氨肽酶底物L-丙氨酰-7-氨基-4-甲基香豆素的合成研究 [J], 寇沛浩;肖伟洪;肖强
5.n-Bu2SnO催化合成7-羟基-4-甲基香豆素 [J], 王银霞;王宏社
因版权原因,仅展示原文概要,查看原文内容请购买。
4-甲基-7-羟基香豆素的合成实验报告

4-甲基-7-羟基香豆素的合成实验报告
实验报告
合成4-甲基-7-羟基香豆素
一、实验目的
通过合成4-甲基-7-羟基香豆素,掌握相关有机合成技术和分离纯化方法。
二、实验原理
本实验采用人工合成方法合成4-甲基-7-羟基香豆素。
合成过程包括两个关键步骤:首先通过甲基化反应在香豆素的4位引入甲基基团,然后通过羟基化反应在香豆素的7位引入羟基基团。
三、实验步骤
1. 在干燥的三颈瓶中,加入香豆素(X g),甲基碘化碘(Y ml)和干燥的DMF(Z ml),并在惰性气氛下搅拌反应。
2. 将反应混合液转移至冷凝管连接的双颈瓶内,加入适量的干燥碳酸钠,并继续在惰性气氛下搅拌反应一段时间。
3. 将反应混合液转移至萃取瓶中,用氯仿进行萃取,并用浓盐酸调节pH值。
4. 过滤得到有机相,用旋转蒸发仪去除溶剂。
5. 将得到的产物溶于乙醚,并用冷冻结晶法结晶纯化产物。
6. 用旋转蒸发仪去除乙醚,得到纯化后的4-甲基-7-羟基香豆素。
四、实验结果与讨论
经红外光谱、质谱和核磁共振等分析手段鉴定,合成产物为4-甲基-7-羟基香豆素。
纯化后的产物形态良好,结晶度高。
五、结论
通过本次实验成功合成了4-甲基-7-羟基香豆素,并验证了合成产物的结构确认。
实验结果证明,经过合适的反应步骤和纯化方法,能够获得所需的目标产物。
7-羟基香豆素经二相代谢后产物

7-羟基香豆素经二相代谢后产物翻译:7-羟基香豆素经过二相代谢后产生多种代谢产物。
本文将以简体中文写,确保条理清晰。
首先,我们需要了解7-羟基香豆素的基本特性。
7-羟基香豆素,也称为7-羟基-4-甲氧基香豆素,是一种天然的化合物,广泛存在于植物中,如小米草、柚木等。
它具有抗氧化、抗炎和抗肿瘤等多种生物活性。
在二相代谢中,7-羟基香豆素首先会经过肝脏的代谢。
在肝脏中,7-羟基香豆素会被多种酶作用,最重要的是细胞色素P450酶。
细胞色素P450酶家族在人体中有多种成员,每个成员对7-羟基香豆素的代谢有不同的作用。
其中,CYP1A1和CYP1A2是两个重要的酶。
CYP1A1主要在肝脏中表达,它能将7-羟基香豆素代谢为7-羟基香豆素-4'-甲醚。
这是7-羟基香豆素的一个主要代谢产物。
而CYP1A2主要在肠道和肾上腺中表达,它能将7-羟基香豆素代谢为7-羟基香豆素-3'-甲醚和7-羟基香豆素-4'-甲醚的二甲基醚体。
这两种醚体也是7-羟基香豆素的重要代谢产物。
除了细胞色素P450酶,其他酶也参与了7-羟基香豆素的代谢。
例如,醛固酮和酮糖酶可以将7-羟基香豆素代谢为7-羟基香豆醇,进一步代谢为7-羟基香豆酸。
此外,甲基转移酶可以将7-羟基香豆素代谢为7-羟基香豆素-O-甲基化体。
在肝脏中,7-羟基香豆素的代谢产物还会与胆汁一起排出体外。
这些代谢产物进入肠道后,受到肠道菌群的进一步代谢。
肠道菌群中的β-葡萄糖苷酶可以将7-羟基香豆素糖苷水解为7-羟基香豆素。
此外,潜在的亚硝酰酸盐产生菌可以将7-羟基香豆素代谢为7-羟基香豆醛,这是一个具有潜在亚硝酸盐生成能力的代谢产物。
总结起来,在7-羟基香豆素的二相代谢中,主要产生了7-羟基香豆素-4'-甲醚、7-羟基香豆素-3'-甲醚、7-羟基香豆素-O-甲基化体、7-羟基香豆醇、7-羟基香豆酸等多种代谢产物。
这些代谢产物的形成提供了7-羟基香豆素多样化生物活性的基础,并且可能对其生物效应产生影响。
7-羟基-4-甲基香豆素的合成

7-羟基-4-甲基香豆素的合成
7-羟基-4-甲基香豆素(7-hydroxy-4-methylcoumarin)是一种具有香豆素结构的化合物,具有广泛的药理活性和生物活性,例如抗氧化、抗炎、抗菌等。
合成7-羟基-4-甲基香豆素的方法
有多种,以下是其中一种可能的合成路线。
合成路线如下:
第一步:氢氧化钠催化下的酮醛缩合反应
该反应中,用酮与醛进行缩合反应,生成α,β-不饱和酮。
反应
中的选择适当的醛和酮,可以控制合成目标化合物的结构和性质。
第二步:酮脱水反应
在酮脱水反应中,使用酸性催化剂(例如硫酸)促使酮分子内的α位氢氧离子化,并脱水生成α,β-不饱和酮。
该反应是生成
羟基香豆素的关键步骤。
第三步:砷酸催化下的Michael加成反应
在Michael加成反应中,使用砷酸作为催化剂,将亲电试剂
(例如醛或酮)加到α,β-不饱和酮上,生成带有羟基的化合物。
第四步:氧化反应
在氧化反应中,使用适当的氧化剂(例如邻苯二酚)将羟基化合物氧化为醌衍生物。
这一步骤会进一步改变目标化合物的结构和性质。
第五步:甲基化反应
在甲基化反应中,使用甲基化试剂(例如碘甲烷)引入甲基基团,生成最终的7-羟基-4-甲基香豆素。
综上所述,合成7-羟基-4-甲基香豆素可以通过酮醛缩合、酮
脱水、Michael加成、氧化和甲基化等反应步骤实现。
具体的
反应条件和试剂选择需要根据实际情况进行优化和调整。
此外,还可以考虑使用其他合成方法和路线,以提高合成效率和产率。
简单香豆素的药理作用与构效关系
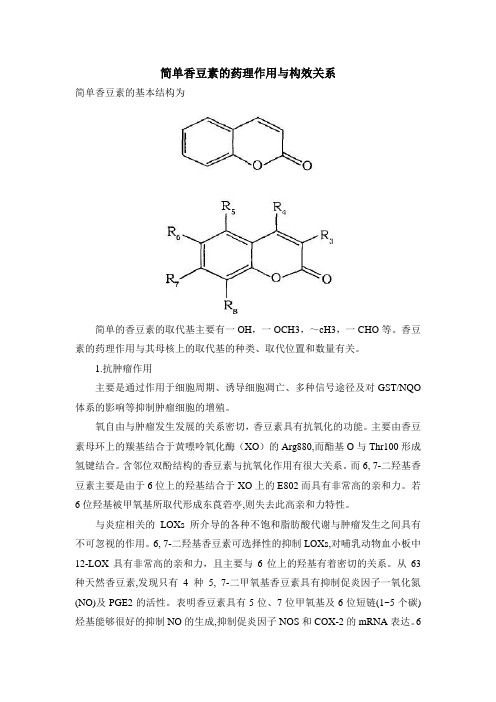
简单香豆素的药理作用与构效关系简单香豆素的基本结构为简单的香豆素的取代基主要有一OH,一OCH3,~cH3,一CHO等。
香豆素的药理作用与其母核上的取代基的种类、取代位置和数量有关。
1.抗肿瘤作用主要是通过作用于细胞周期、诱导细胞凋亡、多种信号途径及对GST/NQO 体系的影响等抑制肿瘤细胞的增殖。
氧自由与肿瘤发生发展的关系密切,香豆素具有抗氧化的功能。
主要由香豆素母环上的羰基结合于黄嘌呤氧化酶(XO)的Arg880,而酯基O与Thr100形成氢键结合。
含邻位双酚结构的香豆素与抗氧化作用有很大关系。
而6, 7-二羟基香豆素主要是由于6位上的羟基结合于XO上的E802而具有非常高的亲和力。
若6位羟基被甲氧基所取代形成东莨菪亭,则失去此高亲和力特性。
与炎症相关的LOXs所介导的各种不饱和脂肪酸代谢与肿瘤发生之间具有不可忽视的作用。
6, 7-二羟基香豆素可选择性的抑制LOXs,对哺乳动物血小板中12-LOX具有非常高的亲和力,且主要与6位上的羟基有着密切的关系。
从63种天然香豆素,发现只有4种5, 7-二甲氧基香豆素具有抑制促炎因子一氧化氮(NO)及PGE2的活性。
表明香豆素具有5位、7位甲氧基及6位短链(1~5个碳)烃基能够很好的抑制NO的生成,抑制促炎因子NOS和COX-2的mRNA表达。
6位取代对抑制肿瘤坏死因子α(TNF-α)的影响很大,如6位被卤素取代后,活性提高20~30倍,而供电基团甲氧基取代后,活性也能提高>3倍。
2.抗菌作用主要是抑制DNA拓扑异构酶、DNA旋转酶。
研究表明, 3-氨基-4, 7-二羟基香豆素(ADHC)部分及其7位上诺维糖基均为此类抗生素的抗菌活性所必需,且这两部分上的取代基不同将显著影响其抗菌活性。
3-O-氨基甲酰基诺维糖有一定活性,与3-乙酰氨基-7-羟基香豆素成苷后得到的衍生物活性比成苷前提高几十倍。
3位酰氨取代基团对此类抗生素的活性具有重要的意义。
3-乙氨香豆素类化合物的抗菌活性可随酰基基团链的延长而提高。
6-甲氧基-7-羟基香豆素

6-甲氧基-7-羟基香豆素
摘要:
1.介绍6-甲氧基-7-羟基香豆素的基本信息
2.探讨6-甲氧基-7-羟基香豆素的应用领域
3.分析6-甲氧基-7-羟基香豆素的合成方法
4.总结6-甲氧基-7-羟基香豆素的研究进展及前景
正文:
6-甲氧基-7-羟基香豆素是一种有机化合物,具有广泛的应用领域。
它的分子式为C10H6O4,是一种香豆素类化合物,具有较强的荧光性和抗氧化性。
6-甲氧基-7-羟基香豆素主要应用于医药、农药和染料等领域。
在医药领域,它可以用作抗炎、抗肿瘤和抗氧化剂等;在农药领域,它可以用作杀虫剂和植物生长调节剂等;在染料领域,它可以用作荧光染料和纺织染料等。
6-甲氧基-7-羟基香豆素的合成方法主要有以下几种:首先是通过香豆素的甲氧基化反应,然后再进行羟基化反应;其次是通过香豆素的硝化反应,然后再进行还原反应;最后是通过香豆素的磺化反应,然后再进行甲氧基化和羟基化反应。
随着科学技术的进步,6-甲氧基-7-羟基香豆素的研究不断深入,其应用领域也在不断扩大。
7-甲氧基香豆素的合成

7-甲氧基香豆素的合成
甲氧基香豆素(3’-O-Methylflavone)是一种重要的天
然二萜化合物,广泛存在于植物类中,被广泛应用于昆虫拓扑抑制剂、抗氧化剂、抗肿瘤剂、降血压剂等领域。
非天然甲氧基香豆素的合成借鉴了天然物的合成框架,经过一系列的有机合成步骤,即可以可控的合成出高收率的非天然甲氧基香豆素。
首先,甲醇脱去2,4-二氯苯酮的氯原子,溴以得到新的
基团——帕拉嘧啶氧化物,而对于带电惰性基团烯羰基,可以用活性氢气N-甲基化活性基团,活化基团形成AlCl3双硝酸
盐类化合物,再催化反应可以得到能排随氯出去的羰基,最终得到甲氧基香豆素。
其次,英国是合成甲氧基香豆素的另一种方法,它使用
氯甲烷亚磺酰胺,乙二胺,和有机氯化物的混合物,分子水平的Ritter反应以产生甲氧基香豆素,这种方法简单、快捷、
高纯度,但需要一定的环境保护,为了防止反应释放有害的产物,可以选择水溶性反应助剂。
最后,常温水分子束多步法也可以合成高纯度甲氧基香
豆素,在水中高能量水分子束作用下,内氧萜烯反应就会发生,最终可以通过催化有机反应得到所需的甲氧基香豆素。
甲氧基香豆素具有多重用途,天然和非天然的甲氧基香
豆素的合成已经成为研究的热点,为了满足不同行业和应用的需求,已经有多种合成方法可以供我们选择,这些方法可以有效地促进甲氧基香豆素在医药、农业和其他领域的应用。
6-甲基香豆素合成路线

6-甲基香豆素合成路线
6-甲基香豆素,也被称为香豆素-6-甲基醚,是一种重要的化学品和医药中间体,在医药、化妆品、香料等领域有着广泛的应用。
本文将探讨6-甲基香豆素的合成路线。
1. 红磷法合成路线
红磷法合成路线是6-甲基香豆素的传统合成方法,其原理是利用亚磷酸酯生成活性的亚磷酸盐,进而与苯酚反应得到6-甲基香豆素。
其具体反应步骤如下:
(1)将苯酚和亚磷酸酯反应生成亚磷酸盐。
(2)在加入亚磷酸盐后,通过加热、蒸馏、水解等步骤得到6-甲基香豆素。
其中该法的优点是反应条件温和,但缺点是产物纯度难以控制,且反应过程中生成的亚磷酸酯具有较高的毒性和易燃性,操作难度较大。
其中该法的优点是反应条件温和、产物纯度高,而且有利于固相反应,控制反应条件等操作。
(1)在离子液体中,利用离子液体中的阴阳离子互补性质,生成催化剂。
其中该法的优点是反应条件温和、产物纯度高,且具有较好的催化效果和重复使用性能。
总结:
以上介绍的3种合成路线,相比传统的红磷法合成路线而言,都有一定的优点,可以有效缓解红磷法合成所面临的环境污染和安全问题,同时从反应条件、操作难度、产物纯度等方面提高了合成效率及质量。
离子液体法合成路线有望成为未来6-甲基香豆素的主要合成方法。
7羟基香豆素葡萄糖醛酸结合物

7羟基香豆素葡萄糖醛酸结合物
近年来,7羟基香豆素葡萄糖醛酸结合物成为了医药化学领域研
究的热点。
其独特的生物链合结构以及良好的药理学特性,使得这种
分子具备了多种临床应用价值。
下面,我们将从分子结构、制备方法
和药理学特性等方面对7羟基香豆素葡萄糖醛酸结合物进行详细阐述。
一、分子结构
7羟基香豆素葡萄糖醛酸结合物,简称7-OH-PCI,分子式为
C23H24O11,相对分子质量为464.42。
其分子结构中含有丰富的香豆素及葡萄糖醛酸官能团,这种生物链合结构赋予了7-OH-PCI良好的药物
代谢和药效学特性。
二、制备方法
目前,7-OH-PCI的制备方法主要分为合成和提取两种方法。
其中,化学方法的合成利用硫酸作为催化剂,在DMSO中将4-甲氧基香豆素与苯甲醇酯和5-O-乙酰基-1,2-异丙基-3,6-二氧-4-二甲基苯基葡萄糖醛酸进行羟乙基化反应。
而提取法则是采用分离提取技术,从一系列植
物中分离出7-OH-PCI。
三、药理学特性
7-OH-PCI在多种疾病治疗中具有重要作用。
最为广泛的是,其抗炎与抗菌特性被广泛应用于感染性疾病治疗。
此外,7-OH-PCI还具有
抗凝、降糖、解痉和保肝等多种药理学特性,被广泛应用于多种常见
疾病的治疗。
四、结语
综上所述,7羟基香豆素葡萄糖醛酸结合物具有广泛的医学应用
前景。
作为药物领域的研究热点,研究人员们正在努力发现其更广泛
的应用场景。
未来也将持续关注7-OH-PCI在临床中的应用表现。
香豆素类化合物

⾹⾖素类化合物《天然产物化学》课程作业题⽬:⾹⾖素类化合物关键词:⾹⾖素结构性质制备吸收代谢应⽤⾷品学院2011级研究⽣农产品加⼯与储藏专业⾹⾖素类化合物1. 概述1.1 ⾹⾖素研究概况⾹⾖素(cornn arin)是具有苯骈a-吡喃酮母核的⼀类天然化合物的总称,在结构上可以看作是顺邻羟基桂⽪酸失⽔⽽成的内酯。
其具有芳甜⾹⽓的天然产物,是药⽤植物的主要活性成分之⼀。
在结构上应与异⾹⾖素类(isacoumarin)相区分,异⾹⾖素分⼦中虽也有苯并吡喃酮结构,但它可看做是邻羧基苯⼄烯醇所成的酯。
如下分⼦结构图所⽰:顺式邻羟基桂⽪酸⾹⾖素异⾹⾖素⾹⾖素类化合物可以游离态或成苷形式⼴泛的存在于植物界中,只有少数来⾃于动物和微⽣物,其中以双⼦叶植物中的伞形科(Umbelliferae),芸⾹科(Rutaceae)和桑科(Moraceae)含量最多,其他在⾖科(Leguminosae)、⽊犀科(Oleaeeae)、茄科(Solanaceae)、菊科(Compositae)和兰科(Orchidaeeae)中也较多。
研究表明,⾹⾖素类化合物具有明显的药理活性,如抗HIV、抗癌、对⼼⾎管的影响、抗炎及平滑肌松弛、抗凝⾎等。
,近年来,随着现代⾊谱和波潜技术的应⽤和发展,发现了不少新的结构类型,如⾊原酮⾹⾖素(chromonacoumarin),倍半萜类⾹⾖素(sesquiterpenyl coumarin),以及prenyl-furocoumarin型倍半萜衍⽣物等。
此外,也发现某些罕见的结构,如⾹⾖素的硫酸酯、⽆含氧取代如3, 4, 7-三甲基⾹⾖素和四氧取代的⾹⾖素。
在⾹⾖素的多聚体上,尚发现混合型⼆聚体,如由⾹⾖素与吖啶酮、喹诺酮或萘醌等组成的⼆聚体。
在分离和鉴定⼿段上,不少新⽅法、新技术近年也被应⽤。
例如,超临界流体被⽤于提取;多种制备型加压(低、中、⾼)和减压⾊潜被应⽤于分离;⽑细管电泳应⽤于分析;在结构鉴定上,2D-NMR被普遍采⽤及负离⼦质谱的使⽤等。
糖基化三氮唑香草酸衍生物的合成及酪氨酸酶抑制活性研究_景临林_范小飞_贾正平

4c
152. 3 ~ 50. 11 5. 12 11. 05 153. 1 ( 50. 39) ( 5. 02) ( 11. 02)
82 382[M + 1]
143. 5 ~ 50. 56 4. 91 10. 89 4d 145. 2 ( 50. 39) ( 5. 02) ( 11. 02) 85 382[M + 1]
第 36 卷第 1 期
景临林等: 糖基化三氮唑香草酸衍生物的合成及酪氨酸酶抑制活性研究
9
化学试剂,2014,36( 1) ,9 ~ 12; 92
糖基化三氮唑香草酸衍生物的合成及酪氨酸酶抑制活性研究
景临林1 ,范小飞1,2 ,贾正平* 1
( 1. 兰州军区兰州总医院 药剂科,甘肃 兰州 730050; 2. 兰州大学 药学院,甘肃 兰州 730000)
酪氨酸酶( EC 1. 14. 18. 1 ) 是一种在动植物 体内及微生物中广泛存在的含铜离子的氧化还原 酶,具有单酚酶和双酚酶的双重特性,是生物体内 黑色素合成 及 色 斑 产 生 的 关 键 酶[1]。 酪 氨 酸 酶 的过度表达会造成黑色素堆积,从而导致多种疾 病的发生,如老年斑、雀斑、黄褐斑以及恶性黑色 瘤等。酪氨酸酶抑制剂可以抑制黑色素生成,用 来预防和治疗色素沉着和黑色素瘤,还可用作防 止蔬菜水果褐变的保鲜剂和杀虫剂。因此,其在 医药、化妆品、食品工业和农业等领域都有着广阔 的应用前景[2]。
摘要: 以叠氮糖、炔丙基溴和香草醛为原料,通过醚化、“Click chemistry”、氧化、水解 4 步反应得到一系列标题化合物,产 物结构经1 HNMR、IR、EI-MS 和元素分析确认。通过对目标化合物进行酪氨酸酶抑制活性筛选,结果表明,所得目标化合 物均具有较强的酪氨酸酶抑制活性,其中 3-甲氧基-4-( ( 1-( ( 2R,3R,4S,5S,6R) -3,4,5-三羟基-6-( 羟基甲基) 四氢-2H-吡 喃-2-基) -1H-1,2,3-三唑-4-基) 甲氧基) 苯甲酸活性最佳,IC50 为 0. 12 ± 0. 04 mmol / L。 关键词: 香草酸衍生物; 点击化学; 糖基化三唑; 酪氨酸酶抑制剂 中图分类号: O629. 9 文献标识码: A 文章编号: 0258-3283( 2014) 01-0009-04
4-乙氧基-7-羟基香豆素及其衍生物的合成

4-乙氧基-7-羟基香豆素及其衍生物的合成
乙氧基-7-羟基香豆素是一种药物和化学品,具有多种生物活性,例如抗癌、抗炎、抗氧化、抗菌和光敏化等。
该化合物的合成通常包括两步反应:首先是苯甲酸的酯化,然后是巴尔-米格尔反应。
一、苯甲酸的酯化反应
苯甲酸的酯化反应是通过将苯甲酸与乙醇在硫酸的催化下反应得到乙酸苯酯。
反应方程式如下:
苯甲酸 + 乙醇→ 乙酸苯酯 + 水
该反应需要在高温下和强酸的催化下进行,其中硫酸充当催化剂。
二、巴尔-米格尔反应
巴尔-米格尔反应是一种经典的有机合成反应,它将芳香醛与乙烯基苯甲醚在碱性条件下反应得到目标产物乙氧基-7-羟基香豆素。
芳香醛 + 乙烯基苯甲醚→ β-氧杂环烷 + 水
β-氧杂环烷 + 碘化钠→ 乙氧基-7-羟基香豆素
在巴尔-米格尔反应中,碘化钠充当催化剂,反应需要在碱性条件下进行。
其他衍生物的合成方法:
该衍生物是通过巴尔-米格尔反应中所用的乙烯基苯甲醚换成甲基苯甲醚来实现。
6-甲氧基-7-羟基香豆素

6-甲氧基-7-羟基香豆素摘要:1.6-甲氧基-7-羟基香豆素的定义2.6-甲氧基-7-羟基香豆素在植物中的来源3.6-甲氧基-7-羟基香豆素的主要作用4.6-甲氧基-7-羟基香豆素在医药领域的应用5.6-甲氧基-7-羟基香豆素在食品工业中的应用6.6-甲氧基-7-羟基香豆素的安全性和副作用正文:6-甲氧基-7-羟基香豆素(6-Methoxy-7-hydroxycoumarin)是一种天然存在于植物中的化合物,具有多种生物活性和药理作用。
在植物中,它通常作为防御机制,以抵抗病虫害的侵袭。
近年来,6-甲氧基-7-羟基香豆素在医药和食品工业领域的应用越来越广泛,下面将详细介绍其作用和应用。
首先,6-甲氧基-7-羟基香豆素具有抗炎、抗肿瘤、抗病毒、抗氧化等多种生物学活性。
研究发现,它可以通过抑制肿瘤细胞的生长和增殖,从而达到抑制肿瘤发展的目的。
此外,6-甲氧基-7-羟基香豆素还具有抗病毒作用,对一些病毒性疾病有一定的预防和治疗作用。
同时,它还具有抗氧化作用,能清除体内的自由基,保护细胞免受氧化损伤。
其次,6-甲氧基-7-羟基香豆素在医药领域有广泛的应用。
由于其具有多种生物学活性,可作为一种辅助治疗药物,用于治疗肿瘤、病毒性疾病、炎症等疾病。
此外,6-甲氧基-7-羟基香豆素还可以用于制备新型药物,如抗肿瘤药物、抗病毒药物等。
再者,6-甲氧基-7-羟基香豆素在食品工业中也有广泛的应用。
由于其具有抗氧化作用,可用作食品添加剂,延长食品的保质期。
此外,它还可以用于制备功能性食品,如提高免疫力、抗疲劳等功能性饮料。
然而,尽管6-甲氧基-7-羟基香豆素具有多种生物学活性和药理作用,但过量使用也可能产生一定的副作用。
例如,长期大剂量使用可能对肝脏、肾脏等器官造成损害。
因此,在使用6-甲氧基-7-羟基香豆素时,应根据实际需要,遵循医生的建议和指导。
总之,6-甲氧基-7-羟基香豆素是一种具有多种生物学活性和药理作用的天然化合物,在医药和食品工业领域有广泛的应用。
7-甲氧基香豆素的合成的开题报告

7-甲氧基香豆素的合成的开题报告
甲氧基香豆素是一种植物中常见的化合物,具有多种生物活性,例如抗癌、抗氧化、
抗菌等。
因此,甲氧基香豆素的合成具有重要的药物应用前景。
本文将探讨甲氧基香
豆素的合成方法及其机理。
首先,我们介绍一种较为简单的合成方法,即石油醚萃取法。
首先将天然产物中含有
甲氧基香豆素的植物部位用石油醚进行提取,然后通过薄层层析或硅胶柱层析得到纯品。
这种方法较为简单,但纯化效果不够理想。
另一种常见的合成方法是酸性催化下的甲氧基香豆素合成。
首先通过甲酸酯和苯酚反
应制备出间甲氧基苯基甲酸酯,然后再将其加入到稀硫酸中进行酸催化。
水解后得到
甲氧基香豆素。
这种方法具有较高的收率和纯度,但使用的催化剂需要考虑对环境造
成的影响。
此外,还有一种采用核酸催化的合成方法,即采用DNA催化合成苯环上甲氧基苯环甲酸酯,然后通过酸水解得到甲氧基香豆素。
这种方法操作简单,且催化剂可重复使用,在药物制备中具有广泛应用前景。
总之,甲氧基香豆素的合成是一项有趣且具有挑战性的任务。
未来随着合成方法的不
断改进和优化,其应用前景将更加广阔。
3-氨基-4-甲氧基乙酰苯胺的绿色合成技术研究的开题报告

3-氨基-4-甲氧基乙酰苯胺的绿色合成技术研究的开
题报告
一、研究背景和意义
3-氨基-4-甲氧基乙酰苯胺是一种常用的碱性染料,具有良好的耐光、耐水性和色牢度,广泛应用于纺织、皮革、纸张等工业中。
然而,传统
的合成方法使用的化学试剂及条件往往存在着环境污染和健康危害等问题。
因此,研究一种绿色、环保的合成方法具有重要意义。
二、研究内容和方法
本研究旨在寻找一种简单、高效的绿色合成方法,通过实验考察不
同的催化剂、溶剂、温度、反应时间、反应物的比例等因素对反应的影响,并优化实验条件,最终完成3-氨基-4-甲氧基乙酰苯胺的绿色合成。
三、预期目标和意义
本研究将寻找一种低成本、环保的合成方法,避免环境污染和健康
危害等问题。
同时,实验的优化过程和方法可以推广到其他绿色合成的
研究中,促进化学品合成的绿色转型。
四、研究难点和解决方法
研究难点主要在于找到合适的催化剂和溶剂,以及确定最适合的反
应条件。
解决方法是通过试验调整反应的参数,寻找最佳组合,并运用
现代分析手段对合成产物进行分析,验证实验结果。
五、研究进度计划
第一年:文献调研,确定反应机理,设计实验方案,初步进行实验。
第二年:优化实验条件,分析产品结构和性质,改进合成方法。
第三年:深入研究反应机理,推广应用和进一步改进研究成果。
六、预期研究成果
预期通过研究合成3-氨基-4-甲氧基乙酰苯胺的新方法,能够在有一定工业应用价值的前提下,实现低成本、高效的绿色合成,为相关领域提供技术支持和经济效益。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
)。
HNMR( CDC l3, 400MH z) , : 1 32( , t 3H, J = 7 14 Hz , ! OCH 2 CH 3 ) ; 2 08 ( s , 3 H, 2 NH COCH 3 ); 2 40( s , 3H, 4 H ); 4 28 ( q , 2 H, J = 7 14 H z , ! OCH 2 CH 3 ) ; 5 26( d , 1H, J = 6 5 H z , 2 H ); 6 65 ( s, 1H, ! NH )。 [ 8] 1 2 2 4 甲氧基间苯二酚 ( 3) 的合成 将 5 44 g ( 35 78 mm o l) 异 香兰 素溶 于 100 mL CH 2 C l2 中, 依 次 加 入 12 mL H 2 O2 ( 30 % )、 0 41 g( 3 60 mm o l) SeO2, 室温搅拌 12 h 后 , 过滤 除去 SeO 2, N a H SO3 溶液洗滤液 , 至淀粉 K I 试纸
将 5 0 g( 38 mm o l) 乙酰乙酸乙酯溶于 15 mL
10
化
学
试
剂
2011 年 1 月
品红色 油 状 物。 粗 品 经 柱 层 析 : S ilica Gel H, V (石油醚 ) ∀V (乙酸乙酯 ) = 5∀1 , 得 4 23 g 淡黄 色油状物, 产率 85 % 。HNMR ( CDC l3, 400 MH z), : 3 67( s , 3 H, ! OCH 3 ); 6 17( d , J = 8 6 H z, 1H, 6 H ) ; 6 35( s , 1H, 2 H ) ; 6 67( d , J = 8 6 H z, 1H, 5 H ) ; 8 80( s , 1H, OH ) ; 8 77( s , 1H, OH )。 1 2 3 3 乙酰胺基 4 甲基 6 甲氧基 7 羟基香豆
+
1 2 4
3 氨基 4 甲基 6 甲 氧基 7 羟基 香豆 素
[ 10]
( 1) 的合成
将 2 0 g( 7 6 mm ol) 化合物 4 加入到 75 mL 2 m ol /L 盐酸中 , 搅拌回流 5 h 后, 停止反应。先 加入 8 5 g 固体碳酸钠 , 后加入少量 5 % 的碳酸氢 钠溶液调整反应液 p H 7 左右 , 析出大量固体, 抽 滤得 1 2 g 棕色固体粉末化合物 ( 1), 产率 71 %, m p 246~ 249 。HNMR ( DM SO d 6, 400 MH z),
[ 1] CU R I N I M, EP IFANO F, MALTESE F , et a. l Synthes is and anti inflamm atory of activ ity o f natura l and se m isyn the tic geranyloxycoum ar ins [ J ]. B ioorg. M ed. Chem. Lett . , 2004, 14 ( 9 ): 2 241 2 243 . [ 2] M ANOLOVL I , DAN CHEV N D. Synthesis , tox icolog ica l and phar m aco log ica l assessm ent o f so m e 4 hydroxycou m ar in der ivatives[ J]. Eur . J. M ed. Chem. , 1995, 30 ( 6 ): 531 535. [ 3] LEE S, SI VAKUM AR K, SH I NW S , et a. l Synthesis and anti ang iogenesis activ ity o f coum arin derivatives [ J ]. B ioorg. M ed. Che m. Lett . , 16 ( 17 ): 4 596 4 599. [ 4] THA ISR I VONGS S, W ATENPAUGH K D, HOW E W J , et a.l Structure based design o f nove lH I V protease inhib ito rs: carboxa m ide con taining 4 hydroxycouma rins and 4 hydroxy 2 pyrones as po ten t nonpeptid ic inh ib ito rs[ J]. J.M ed. Che m. , 1995 , 38 ( 18 ): 3 624 3 637 . [ 5] 智双 , 赵德 丰 , 李 海玉 , 等 . 香豆 素类 荧光染 料的 合成 及结构 表征 [ J]. 染料与染色 , 2004 , 41 ( 2) : 87 90. [ 6 ] DU FFY C F , O# KENNEDY R. D eter m ination of 7 hydroxycoum ar in and its g lucuronide and su lphate conju ga tes in live r slice incubates by capillary zone e lectropho res is[ J]. J. Pharm. B iomed. A nal. , 1998, 17 ( 8 ): 1 279 1 284.
收稿日期 : 2009 12 21 基金项目 : 国家自然科学基金资助项目 ( 30500631) 。 作者简介 : 邹昊 ( 1985 ) , 男 , 硕士, 湖南醴陵人 , 主要研究方 向为抗肿瘤药物的合成及生物活性研究。 联系作者 : 张倩 , E m ai: l zh angq ian511@ shmu. edu . cn。
香豆素类化合物是一类重要的有机杂环化合 物 , 具有显著的消炎、 抗凝结、 抗肿瘤及抗 H I V等 生物活性 泛的应用
[ 1 4]
冰醋酸中 , 冰水浴下, 逐滴滴入 亚硝酸钠水溶液 ( 3 1 g 亚硝酸钠 溶于 7 mL 水中 ) , 1 h 内加 完。 撤去冰水浴, 常温 搅拌 2 h 后, 向 反应液中 加入 10 g 冰及 8 mL 乙酸酐, 再次在冰水浴下 缓慢加 入 10 g 冰、 4 mL 乙酸酐和 10 g 锌粉的混合物, 保 持温度 < 20 搅拌 2 h 。 2 h后撤去冰水浴, 常温 搅拌 4 h 。过滤 , 滤渣用 50 mL 水分次洗涤 , 向滤 液中加入 100 mL冰水, 二氯甲烷萃取 ( 60mL 2), 合并有机相 , 依次用饱和 N aC l水溶液洗涤, 无水 N a2 SO 4 干燥 , 过滤 , 减压蒸除溶剂 , 粗品用石油醚 低温下 ( - 15 ) 重结晶得 3 2 g 淡黄色固体, 产 率 44 % , m p 43~ 46
1
: 2 18 ( s , 3H, 4 CH 3 ); 3 84 ( s , 3H, 6 OCH 3 ); 4 97( s , 2 H, ! NH 2 ); 6 73( s, 1 H, 8 H ) ; 6 96 ( s , 1H, 5 H ); 9 52( s , 1H, 7 OH ) 。 E I M S , m /z (% ): 221( M , 100); 206( 26 53) ; 178( 48 53) 。 2 结果与讨论 2 1 合成路线的探索 经典的香豆素环的合成方法主要包括两种, 一种是通过邻羟基苯酮类化合物与乙酸 ( 或者取 代乙酸 ) 衍生物的缩合反应 ( Perkin 法 ) 获得 , 另 一 种 是通 过 苯酚 与乙 酰 乙酸 乙 酯的 缩 合反 应 ( P echm ann 法 )生成。 3 位含有氨基 , 同时 4 位含有甲基的香豆素 类化合物, 极少见文献报道。 3 氨基香豆素多采 用水杨醛或者其衍生物与 取代乙酸衍生 物通过 P erk in 法合成, 而得到 4 位无取代的环系。作者 曾采用邻羟基苯乙酮类化合物与氨基保护的氨基
1
2 03( s, 3H, 4 CH 3 ) ; 2 25 ( s , 3 H, NHCOCH 3 ); 3 87( s , 3 H, 6 OCH 3 ) ; 6 79( s , 1H, 8 H ) ; 7 16( s , 1H, 5 H ) ; 9 35 ( s, 1 H, 7 OH ) ; 10 22 ( s , 1H, ! NH ) 。 E I M S , m /z (% ) : 263 ( M , 21 84) ; 221 ( 100); 206( 18 92) 。
第 33 卷第 1 期
邹昊等 : 3 氨基 4 甲基 6 甲氧基 7 羟基香豆素的合成研 究
9
化学试剂 , 2011 , 33( 1) , 9~ 10 ; 21
3 氨基 4 甲基 6 甲氧基 7 羟基香豆素的合成研究
邹昊 , 张倩
*
( 复旦大学 药学院 药物化学教研室 , 上海
201203)
摘要 : 以对甲苯磺酸为催化剂 , 采用操作简便、 绿色环保的无 溶剂合成 方法 , 通 过 Pechm ann 反应 成功合成 了未见 文献报 道的标题化合物 , 结构经 1 HNM R 及 M S 确证。 关键词 : 3 氨基 4 甲基 6 甲氧基 7 羟基香豆素 ; Pechm ann 缩合反 应 ; 无溶剂合成 中图分类号 : O 626 文献标识码 : A 文章编号 : 0258 3283( 2011) 01 0009 02
[ 9] 1
乙酸衍生物 , 尝试了多种环合条件下的缩合反应, 期望获得 4 位引入甲基 , 3 位引入氨基的香豆素 环系, 但均未能获得成功。此外 , 作者也企图通过 先合成香豆素母环, 再经硝化、 硝基还原成氨基的 [ 11 , 12 ] 合成路线, 引入 3 氨基 。但遗憾的是 , 由于 底物中存在 6 甲氧基和 7 羟基等活化苯 环的基 团 , 硝基均取代在苯环上而非内酯环上, 因而通过 该方法依然无法合成该目标化合物。 最后采用了 Pechm ann 合成法, 先在乙酰乙酸 乙酯上引入乙酰氨基, 与 4 甲氧基苯二酚在对甲 苯磺酸催化无溶剂条件下 , 成功合成了 3 乙酰氨 基 4 甲基 6 甲氧基 7 羟基香豆素, 再经水 解, 获 得目标化合物, 为未见文献报道的新化合物。 2 2 无溶剂合成 采用对甲 苯磺酸等有机酸 催化, 通 过 P ech [ 9] m ann法无溶剂合成香豆素 , 已有文献报道 。而 将该方法用于 3 氨基香豆素的合成 , 则未见文献 报道, 无溶剂合成方法的绿色环保、 产物易分离等 特性, 也为同类化合物的工业化生产 , 开辟了良好 的前景。 参考文献:
