人教版高中化学选修3物质结构与性质共价键共50页文档
【精品】人教版高中化学选修3 物质的结构与性质

第讲物质的结构与性质知识必备一、原子的结构与性质1、能层与能级能层:电子层能级:s、p、d、f、g能级交错:1s2、核外电子排布遵循原理(1)能量最低原理(2)泡利不相容原理(3)洪特规则3、前36号元素原子的基态电子排布式和电子排布图。
4、元素周期表(1)结构(2)分区①根据元素的金属性和非金属性,分为金属元素区和非金属元素区②根据核外电子排布分为s、p、d、ds、f区5、元素基本性质与元素周期律①原子半径:同周期元素从左往右,半径减小;同主族从上往下,半径增大。
②化合价③金属性和非金属性:同周期从左往右,金属性减弱,非金属性增强;同主族从上往下,金属性增强,非金属性减弱。
6、电离能:元素的第一电离能是气态原子失去一个电子所需要的能量。
①电离能越小,越容易失去电子②电离能比较:非金属性越强,电离能越大【特别提醒】半满和全满时,电离能要偏高。
7、电负性:描述原子对键合电子吸引力的大小。
电负性越大,对键合电子的吸引力越强。
①电负性越大,对电子对的吸引力越大②电负性比较:非金属性越强,电负性越大。
二、分子的结构与性质1、共价键(1)共价键的分类①按键的极性分为极性共价键和非极性共价键②按成建的形式可分为δ键和π键(2)共价键的参数:键长、键能、键角①成键原子的半径越小,键长越短,键能越大②键能越大,键越稳定2、物质的电子式(1)电子式的书写(2)判断共价物8电子稳定结构3、分子的结构(1)常见分子的构型(2)价层电子互斥模型预测分子的立体构型(3)分子的极性4、无机含氧酸分子的酸性规律:非羟基氧越多,酸性越强三、配合物1、配合物的形成2、配位数3、空间结构四、晶体1、晶体分类:离子晶体、金属晶体、分子晶体和原子晶体2、溶沸点的比较①不同类晶体:一般情况下,原子晶体>离子晶体>分子晶体②同种类型晶体a离子晶体:离子所带的电荷数越高,离子半径越小,则其熔沸点就越高。
b分子晶体:对于同类分子晶体,式量越大,则熔沸点越高。
高中化学第二章分子结构与性质第一节共价键课件新人教版选修3

课时1 共价键的特征与类型
刷基础
6.[陕西岐山2018高二期中]下列化合物分子中只有σ键的是( C )
A.CO2 C.H2O2
B.C2H2 D.COCl2
解析
二氧化碳分子为共价化合物,碳原子分别与两个氧原子形成2个C=O键,结构式为O=C=O,
则CO2中含有σ键和π键,A不符合题意;C2H2的结构式为H—C≡C—H,含有碳碳三键,
课时1 共价键的特征与类型
刷基础
9.根据氢原子和氟原子的核外电子排布,下列对F2和HF分子中形成的共价键描述正确的 是( C )
A.两者都为s-s σ 键 B.两者都为p-p σ 键 C.前者为p-p σ 键,后者为s-p σ 键 D.前者为s-s σ 键,后者为s-p σ 键
解析
H原子的核外电子排布式为1s1,F原子的核外电子排布式为1s22s22p5,形成共价键时,F为 2p电子参与成键,H为1s电子参与成键,则F2分子中形成的共价键为p-p σ键,HF分子中 形成的共价键为s-p σ键,C正确。
课时1 共价键的特征与类型
刷基础
题型2 σ键、π键的比较与判断
5.下列关于σ键和π键的理解不正确的是( D )
A.σ键能单独形成,而π键一定不能单独形成 B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转 C.双键中一定有一个σ键和一个π键,三键中一定有一个σ键和两个π键 D.气体单质中一定存在σ键,可能存在π键
解析
键能越大,分子越稳定,则越不容易受热分解,A错误,D正确;H—H键没有方向性,B错 误;形成共价键的两个原子之间的核间距叫键长,C错误。
课时2 共价键的键参数与等电子原理
刷基础
4.[宁夏石嘴山三中2018高三月考]下列分子或离子中键角由大到小的排列顺序是( B ) ①SO2 ②NH3 ③H2O ④CH4 ⑤CO2
人教版高中化学选修三 第二章 分子结构与性质2.1 共价键

1s 2s 2p
N ↑↓ ↑↓↑↓↑↓↑↓
1s 2s 2p
1.共价键的形成和分类 ——( π 键)
π键特点:两个原子轨道以 “肩并肩” 方式重 叠;原子重叠的部分分别位于两原子核构成平面的两 侧,如果以它们之间包含原子核的平面为镜面,它们 互为镜像,称为镜面对称
1.共价键的形成和分类 ——( π 键)
课堂练习
1.σ键的常见类型有(1)s-s, (2)s-px,
(3)px-px,请指出下列分子σ键所属类
型:
A. HF
s-px
B. NH3 C. F2
s-px px-px
D. H2
s-s
课堂练习
2. 下列关于共价键的说法不正确的是( D )
A.H2S分子中两个共价键的键角接近90°的原因是共 价键有方向性
3.π键:肩并肩、镜像对称、容易断裂。 4. 共价键类型规律:
单键:σ键; 双键:1个σ键 1个π键 三键:1个σ键 2个π键
作业布置
1、预习键参数、等电子原理 2、作业:学案:课堂练习、课后作业
达标检测
• 分析下列化学式中划有横线的元素,选出符合要求的物质。
• A.NH3 B.H2O
C.HCl
第二章 分子结构与性质
共价键
学习目标
1、理解共价键的特征 2.知道共价键的类型( σ键、 π键); 3.掌握共价键的成键类型。
问题展示
1.什么化学键?化学键的分类?
化学键:相邻原子之间强烈的相互作用
化学键
离子键 共价键 金属键
极性共价键 非极性共价键
化合物
离子化合物 共价化合物
一、共价键 1、概念:
共价键的形成和分类 ——( p-p σ 键)
高二化学-选修3-杂化类型及空间构型-物质结构与性质

中心原子最外层电子数 – 电荷数 + 配位数
2
价电子对
杂化类型
2
sp
3
sp2
单个 O / S = 0
CO32-
sp3
4
单个 氢原子 / 卤素 = 1
=
sp3d 不考
5
SO3 =
-
NO3 =
5+1+3╳0
2
=3
SO2 =
4 – (-2) + 3 ╳ 0
2
6+0+3╳0
2
6+0+2╳0
2
=3
=3
=3
二、杂化与空间构形
一、共价键
4. σ键和π键
N 1s22s22p3
下载后,图案可以编辑
N2的成键过程
z
σ键
z
π键
y
x
y
x
π键
一、共价键
4. σ键和π键
键类型
σ键
π键
原子轨道重叠方式
沿键轴方向“头碰头”重叠
沿键轴方向“肩并肩”重叠
原子轨道重叠部位
两原子核之间
键轴上方和下方
原子轨道重叠程度
键的强度
分类
化学活泼性
稳定性
3
sp2
2
1
平面三角形
V型
CO2
2
sp
2
0
直线形
直线形
甲烷 CH4
二、杂化与空间构形
1. 轨道杂化和杂化轨道
二、杂化与空间构形
C 1s22s22p2
甲烷 CH4
2s
相同
2p
sp3
二、杂化与空间构形
(完整word版)高中化学《《选修3物质结构与性质》》教材分析

高中化学vv选修3物质结构与性质>>教材分析
物质结构理论是现代化学的重要组成部分,也是医学、生命科学,材料科学、环境科学、能源科学、信息科学的重要基础。
它揭示了物质构成的奥秘。
物质结构与性质的关系,有助于人们理解物质变化的本质,预测物质的性质,为分子设计提供科学依据
在本课程模块中,我们将从原子、分子水平上认识物质构成的规律,以微粒之间不同的作用力为线索,侧重研究不同类型物质的有关性质,帮助高中学生进一步丰富物质结构的知识,提高分析问题和解决问题的能力。
一、模块的功能
高中化学选修3是在在必修课程基础上为满足学生的不同需要而设置的。
我省理工方向的学生必须选修本模块,它是学业水平考试和高考的内容。
本模块选修课程旨在让学生了解人类探索物质结构的重要意义和基本方法,研究物质构成的奥秘,认识物质结构与性质之间的关系,提高分析问题和解决问题的能力。
二、模块的课程目标
通过本课程模块的学习,学生应主要在以下几个方面得到发展:
1从科学家探索物质构成奥秘的史实中体会科学探究的过程和方法,增强学习化学的兴趣;
2•进一步形成有关物质结构的基本观念,初步认识物质的结构与性质之间的关系;
3 •能从物质结构决定性质的视角解释一些化学现象,预测物质的有关性质;
4•在理论分析和实验探究过程中学习辩证唯物主义的方法论,逐步形成科学的价值观。
三、模块的内容标准及学习要求
学习要求分为基本要求和发展要求:
基本要求:全体学生应在本节学习时掌握。
发展要求:有条件的学生可在选修3结束时掌握。
第二章分子结构与性质
第三章晶体结构与性质
节。
高中化学第2章分子结构与性质第1节共价键第1课时共价键课件新人教版选修3

B.当原子形成分子时,首先形成σ键,可能形成π 键
C.有些原子在与其他原子形成分子时只能形成σ 键,不能形成π键
答案 D 解析 在分子中,化学键可能只有σ键而没有π键, 若有π键,则必有σ键。
【变式3】 下列说法中,正确的是( )
A.在N2分子中,有三个π键 B.N2分子中有一个σ键、两个π键 C.N2分子中有两个σ键、一个π键 D.N2分子中存在一个σ键、一个π键 答案 B
解析 (2)氢气分子中含有1个σ键,A项错误;共价键 的本质就是高概率地出现在原子间的电子与原子间的电 性作用,B项正确;④已经达到稳定状态,C项正确; 氢气分子中含有一个非极性键,D项错误。
答案 (1)①⑤②③④ (2)BC
【变式1】 下列不属于共价键成键因素的是( ) A.共用电子对在两原子核之间高概率出现 B.共用的电子必须配对 C.成键后体系能量降低,趋于稳定 D.两原子体积大小要适中 答案 D
2.方向性 除s轨道是球形对称,其他的原子轨道在空间都具 有一定的分布特点。在形成共价键时,原子轨道重叠得 愈多,电子在核间出现的概率越大,所形成的共价键就 越牢固,因此共价键将尽可能沿着电子出现概率最大的 方向形成,所以共价键具有方向性。
【例题2】 下列说法正确的是( ) A.Cl2是双原子分子,H2S是三原子分子,这是由 共价键的方向性决定的
考点二 共价键的特征
1.饱和性 由于每个原子所能提供的未成对电子的数目是一定 的,因此在共价键的形成过程中,一个原子中的一个未 成对电子与另一个原子中的一个未成对电子配对成键 后,一般来说就不能再与其他原子的未成对电子配对成 键了。这就是共价键的饱和性。因此,不可能形成H3、 H2Cl、Cl3等分子。
人教版选修3物质结构与性质《共价键》说课稿

人教版选修3物质结构与性质《共价键》说课稿一、教学背景分析共价键作为化学知识的重要部分,对学生理解物质结构和性质具有重要意义。
本节课以人教版选修3中的《共价键》为教学内容,旨在帮助学生深入了解共价键的概念、特点及相关的物质性质。
二、教学目标1.知识目标:–了解共价键的概念与特点;–掌握共价键的形成过程;–理解共价键对物质性质的影响;–能够通过实际例子演示共价键的形成和影响。
2.能力目标:–运用共价键的概念解释物质性质的变化;–分析和比较不同共价键类型对物质性质的影响;–运用所学知识解决化学实际问题。
3.情感目标:–培养学生对化学知识的兴趣和好奇心;–提高学生的实验观察和实践动手能力;–培养学生合作学习和团队协作的意识。
三、教学重点和难点•教学重点:共价键的概念、特点、形成过程以及对物质性质的影响。
•教学难点:通过实例演示共价键的形成过程,启发学生的思维。
1. 导入新课•利用生活现象引入共价键的概念:例如,问学生为什么氧气和氮气是气体而不是液体或固体?2. 知识呈现与拓展•通过PPT展示共价键的概念和特点。
解释共价键的定义:共价键是两个非金属原子通过共享电子对而形成的化学键,并解释共享电子对的概念。
•简要介绍单、双和三共价键,并通过示意图展示不同类型的共价键。
3. 实例演示•利用实例演示共价键的形成过程。
例如,以氢气(H2)和氯气(Cl2)共价键的形成为例,通过动态模拟讲解原子间电子的共享过程,以帮助学生理解共价键的形成。
4. 实践探究•分组实验:学生分成小组,通过实验观察,探究不同共价键类型对物质性质的影响。
例如,比较氢气(H2)和氮气(N2)的燃烧性质。
5. 总结与归纳•引导学生总结所学内容,归纳共价键的特点和形成过程,并分析共价键对物质性质的影响。
6. 拓展应用•在实际应用中探究共价键的重要性。
例如,介绍共价键在有机化学合成、药物研发等领域的应用。
7. 课堂小结与作业布置•点名回答问题,对学生进行知识巩固和检查;•布置相关作业:阅读课后扩展材料、完成练习题。
人教版高中化学选修3-物质结构与性质:第一节 共价键

2.最大重叠原理
两原子各自提供1 个自旋方向相反 的电子彼此配对。
两个原子轨道重叠部分越大,两 核间电子的概率密度越大,形成 的共价键越牢固,分子越稳定。
2、共价键的形成
电子云在两个原子核间重叠,意味着电子 出现在核间的概率增大,电子带负电,因 而可以形象的说,核间电子好比在核间架 起一座带负电的桥梁,把带正电的两个原 子核“黏结”在一起了。
乙烷分子中由7个σ键组成;
乙烯分子中由5个σ键和1个π键组成;
乙烯分子中由3个σ键和2个π键组成。
课堂小结 第一节 共价键
1. σ键:以形成化学键的两原子核的连线为轴作旋 转操作,共价键电子云的图形不变,这种特征称为轴对 称。如H-H键。
类型:s—sσ、s—pσ、p—pσ等。 2. π键:由两个原子的p电子“肩并肩”重叠形成。 特点: 特点:肩并肩、两块组成、镜像对称、容易断裂。 3. 由原子轨道相互重叠形成的σ键和π键总称价键 轨道。 4. 判断共价键类型规律: 共价单键是σ键;而共价双键中有一个σ键,另一个 是π键;共价三键由一个σ键和两个π键组成.
人教版 选修三 第二章分子结构与性质
第一节 共价键
三维目标
知识与技能
1、复习化学键的概念,能用电子式表示常 见物质的离子键或共价键的形成
2、知道共价键的主要类型δ键和π键。 3、说出δ键和π键的明显差别和一般规律。
过程与方法
通过观察δ键和π键形成过程,理解δ键和π 键是 怎样形成的。
情感态度与价值观
ZZ X
归纳总结
项
键
目 型
成键方向
σ键
π键
沿轴方向“头碰头”平行方向“肩并肩”
电子云形状 牢固程度 成键判断规律
轴对称
人教版高中化学选修3 物质结构与性质 第二章 第一节 共价键(第2课时)

键参数
CO2 180°
2014年7月19日星期六 15
键参数
CH4 109°28’
2014年7月19日星期六 16
键参数
【观察】P32页中表2-3的数据
从表中可以看出,CO分子与N2分子在许多性 质上十分相似,这些相似性,可以归结为 它们具有相等的价电子数,导致它们具有 相似的化学结构。
表2-3 CO分子和N2分子的某些性质
ΔH=436.0kJ· mol-1 + 242.7kJ· mol-1 —2×431.8kJ· mol-1 = —184.9kJ
H2 + Br2 = 2HBr
ΔH=436.0kJ· mol-1 + 193.7kJ· mol-1 —2×366kJ· mol-1 = —102.7kJ 因为生成HCl放出的热量高于生成HBr放出的热量,所 某些共价键键能/kJ· mol-1
键能 157 键 N -O 键能 176 F-F
Cl-Cl
Br-Br I-I
242.7
193.7 152.7 347.7 615 812
N =O
O -O O =O C -H O -H N -H
607
142 497.3 413.4 462.8 390.8
2014年7月19日星期六 7
键参数
表2-2
键 H-H F-F Cl-Cl Br-Br I-I C-C C=C
某些共价键键能(kJ/mol)键长/pm (1pm=10-12m)
键能 436 157 242.7 193.7 152.7 347.7 615 键长 74 141 198 228 267 154 133 键 C≡C C -H O -H N -H N≡N Si-Si Si-O 键能 812 413.4 462.8 390.8 946 键长 120 109 96 101 110 235 162
化学人教选修三第2章第1节共价键

有些结构不会明确标出单双键,例如醛基-CHO(
)、羧基-COOH(
)、
酯基—COOR(
)、-CN(-C≡N)、CO(三键)、N(在有机物中多是三键)
E 每个原子的共价键数乘以原子数减去重复的数目。
例:如图,
C60 分子中每个碳都满足 8 电子稳定结构,σ键数目为
(2)π键 ①π键:形成共价键的未成对电子的原子轨道,采取“肩并肩”式重叠,这种共价 键叫π键。 ②如下图 p-pπ键的形成:
p-pπ键的形成
③π 键的特征: a.每个 π 键的电子云由两块组成,分别位于由两原子核构成平面的两侧,如果以它们之 间包含原子核的平面为镜面,它们互为镜像,这种特征称为镜像对称。 b.形成 π 键时电子云重叠程度比 σ 键小,π键没有 σ 键牢固。 ④π键的存在:π 键通常存在于双键或三键中。 ⑤π键不存在的理由:原子半径加大,很难形成肩并肩重叠或重叠程度很小,就很难形成 π键。
、C≡N 等均为极性
键,其电性情况为:δH+—δC-l、δC+ δO-、δC+≡δN-;H—H、OO、N≡N 等均为非极性键,原
子不显电性。
注意:①δ+、δ-表示带部分正电荷和部分负电荷,它不像离子键中的离子带完整的正、
负电荷,也不像非极性键中的原子不显电性。也就是说,极性键介于离子键和非极性键之间。 ②一般来说,成键原子的电负性相差越大,电子对偏移程度越大,键的极性越强,在化学
⑤判断存在:某个原子的价电子数小于共价键数目,该原子存在共价键
(2)配合物的性质 ①配合物中,中心原子在配位体的影响下,其价层轨道进行杂化,配位原子的孤对电子 进入中心原子的空轨道产生强的作用,因而配合物有较强的稳定性。配位键越强,配合 物越稳定。一般情况下,中心原子的半径越大,中心原子所带电荷越多,配位原子半径 越大,配位键越强。
人教版高中化学选修3物质结构与性质第二章第一节共价键第1课时

CH2=CH2分子结构
2019/9/26
18
共价键
CH≡CH分子结构
2019/9/26
19
共价键
【练习】
1、判断下列分子中,只含σ键的是
,既含σ键又含有π
键的是
。(填序号)
⑴ H2 ⑵ HCl ⑶ NH3 ⑷ H2O ⑸ CO2 ⑹ N2
⑺ C2H4 ⑻ C2H2 ⑼ F2
⑽ CH3CH3 ⑾ H2O2
【小结】
特征:①电子云结构为 轴对称 (头碰头) ②键能较大,较稳定
类型:有 s-s σ键,如 H2 有 s-p σ键,如 HCl 有 p-p σ键,如 Cl2
2019/9/26
8
共价键
一、共价键
2、 π键
p-pπ键的形成
2019/9/26
只是一个π 键
9
共价键
2P4轨道
↑↓
O2 中 p-pσ键和 p-pπ键的形成过程
只含σ键的是:1 2 3 4 9 10 11
既含σ键又含π键的是:5 6 7 8
2019/9/26
20
共价键
2、下列说法中正确的是( C)
A. p轨道之间以“肩并肩”重叠可形成σ键 B. p轨道之间以“头碰头”重叠可形成π键 C. s和p轨道以“头碰头”重叠可形成σ键 D. 共价键是两个原子轨道以“头碰头”重叠
电子云形状
ቤተ መጻሕፍቲ ባይዱσ键
沿键轴方向 头碰头 轴对称,可旋转
π键
沿键轴方向平行肩并 肩
镜像对称,不可旋转
原子轨道重叠程度
较大
较小
牢固程度 成键判断规律
σ键强度大,
π键强度较小,
不易断裂,不活泼。 容易断裂,活泼。
人教版高中化学选修3物质结构与性质共价键共50页文档

▪
29、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达·芬奇
▪
30、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华
谢谢!
50
人教版高中化学选修3物质结构与性质 共价键
1、战鼓一响,法律无声。——英国 2、任何法律的根本;不,不成文法本 身就是 讲道理 ……法 律,也 ----即 明示道 理。— —爱·科 克
3、法律是最保险的头盔。——爱·科 克 4、一个国家如果纲纪不正,其国风一 定颓败 。—— 塞内加 5、法律不能使人人平等,但是在法律 面前人 人是平 等的。 ——波 洛克
▪
26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭
▪
27、只有把抱怨环境的心情,化为上进的力量,才是成功的证。——罗曼·罗兰
▪
28、知之者不如好之者,好之者不如乐之者。——孔子
人教版高中化学选修3_《物质结构与性质》第二章共价键教案
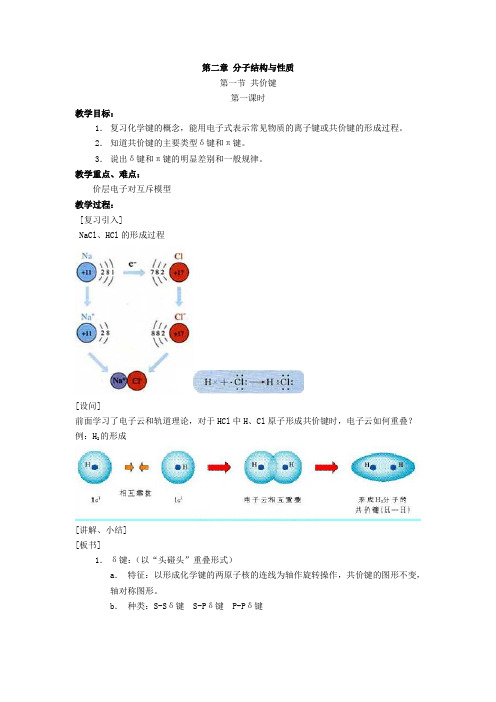
第二章分子结构与性质第一节共价键第一课时教学目标:1.复习化学键的概念,能用电子式表示常见物质的离子键或共价键的形成过程。
2.知道共价键的主要类型δ键和π键。
3.说出δ键和π键的明显差别和一般规律。
教学重点、难点:价层电子对互斥模型教学过程:[复习引入]NaCl、HCl的形成过程[设问]前面学习了电子云和轨道理论,对于HCl中H、Cl原子形成共价键时,电子云如何重叠?例:H2的形成[讲解、小结][板书]1.δ键:(以“头碰头”重叠形式)a.特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键的图形不变,轴对称图形。
b.种类:S-Sδ键 S-Pδ键 P-Pδ键[过渡]P电子和P电子除能形成δ键外,还能形成π键[板书]2.π键[讲解]a.特征:每个π键的电子云有两块组成,分别位于有两原子核构成平面的两侧,如果以它们之间包含原子核的平面镜面,它们互为镜像,这种特征称为镜像对称。
3.δ键和π键比较①重叠方式δ键:头碰头π键:肩并肩②δ键比π键的强度较大②成键电子:δ键 S-S S-P P-Pπ键 P-Pδ键成单键π键成双键、叁键4.共价键的特征饱和性、方向性[科学探究] 讲解[小结]生归纳本节重点,老师小结[补充练习]1.下列关于化学键的说法不正确的是()A.化学键是一种作用力B.化学键可以是原子间作用力,也可以是离子间作用力C.化学键存在于分子内部D.化学键存在于分子之间2.对δ键的认识不正确的是()A.δ键不属于共价键,是另一种化学键B.S-Sδ键与S-Pδ键的对称性相同C.分子中含有共价键,则至少含有一个δ键D.含有π键的化合物与只含δ键的化合物的化学性质不同3.下列物质中,属于共价化合物的是()A.I2 B.BaCl2 C.H2SO4 D.NaOH4.下列化合物中,属于离子化合物的是()A.KNO3 B.BeCl C.KO2 D.H2O25.写出下列物质的电子式。
H2、N2、HCl、H2O6.用电子式表示下列化合物的形成过程HCl、NaBr、MgF2、Na2S、CO2[答案]1.D 2.A3.C4.AC5.略6.略第二章分子结构与性质第一节共价键第二课时[教学目标]:1.认识键能、键长、键角等键参数的概念2.能用键参数――键能、键长、键角说明简单分子的某些性质3.知道等电子原理,结合实例说明“等电子原理的应用”[教学难点、重点]:键参数的概念,等电子原理[教学过程]:[创设问题情境]N2与H2在常温下很难反应,必须在高温下才能发生反应,而F2与H2在冷暗处就能发生化学反应,为什么?[学生讨论][小结]引入键能的定义[板书]二、键参数1.键能①概念:气态基态原子形成1mol化学键所释放出的最低能量。
专题3共价键

练习 从化合价可知,PCl5中 无 (有/无) 孤电子对,分子应为三角双锥 构型。
问题解决 共价键的键能与化学反应的反应热 归的纳热1m:量ol反反,H2应(应而g物)热1和m总(o1l键m△No2能(lHgC)大)l和2=,(g反1生)m反应o成l应物O物2(生总总g)成键键反能2能应H-C生小生l(成,成g)物吸2放N总热O出(键反g1)8能应却3k;需J 要吸收反18应0k物J的总热键量能,小请,根生据成以物上总数键据能计大算,说放明热并反归应纳。 化学键的键能与化学反应过程中能量变化的关系?
选修3物质结构与性质
专题3 共价键 原子晶体
WZZXLUOXIN
共价键
原子间通过共用电子对(电子云重叠)所形成 的化学键
用1.旧从电知原子回子式顾出描发述;共价键的形成: 2.哪每些个元单素电之子间配能成形1对成共共用价电键子?对,化合物中共用
电用子电对子数式等如于何原描子述化共合价价键数的;形成? 3.孤对电子保留。
排序为 H-F>H-O>H-N>H-C
。
练习 用电子式表示水合氢离子的形成并写出水合 氢离子结构式
配位键与普通共价键形成后没有任何区别
练习
1998年,卡尔·克里斯特合成了具有高能量的正离子N5+,有极
强爆炸性,被称为“盐粒炸弹”。在N5+中每个氮原子最外层都满
足“8电子稳定结构”,整个结构中含有两个N≡N键,写出N5+离
能说出共价键的三种键参数,知道键能与反应热的关 系,并能简单计算。能说出键能与键长的一般关系。 能根据键角判断分子的空间构型。
自学流程: ①阅读并完成书本上的:交流与讨论、问题解决、 你知道吗?等相关栏目。②小组讨论,答疑解惑。
人教版高中化学选修3物质结构与性质共价键共50页文档

谢谢!
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业,需 要决心 ,能力 ,组织 和责任 感。 ——易 卜 生 54、 唯 书 籍 不 朽。——乔 特
人教版高中化学选修3物质结构与性质共 价键
11、获得的成功越大,就越令人高兴 。野心 是使人 勤奋的 原因, 节制使 人枯萎 。 12、不问收获,只问耕耘。如同种树 ,先有 根茎, 再有枝 叶,尔 后花实 ,好好 劳动, 不要想 太多, 那样只 会使人 胆孝懒 惰,因 为不实 践,甚 至不接 触社会 ,难道 你是野 人。(名 言网) 13、不怕,不悔(虽然只有四个字,但 常看常 新。 14、我在心里默默地为每一个人祝福 。我爱 自己, 我用清 洁与节 制来珍 惜我的 身体, 我用智 慧和知 识充实 我的头 脑。 15、这世上的一切都借希望而完成。 农夫不 会播下 一粒玉 米,如 果他不 曾希望 它长成 种籽; 单身汉 不会娶 妻,如 果他不 曾希望 有小孩 ;商人 或手艺 人不会 工作, 如果他 不曾希 望因此 而有收 益。-- 马钉路 德。
55、 为 中 华
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
13、归去来兮,田蜀将芜胡不归。 14、酒能祛百虑,菊为制颓龄。 15、春蚕收长丝,秋熟靡王税。
▪
26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭
▪
27、只有把抱怨环境的心情,化为上进的力量,才是成功的保证。——罗曼·罗兰
▪
28、知之者不如好之者,好之者不如乐之者。——孔子
▪
29、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达·芬奇
▪
30、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华
谢谢!
50
