[最新]镁的提取与应用PPT
合集下载
镁的提取及应用PPT教学课件

神州六号
一、镁在自然界中的存在形式:
主要以化合态的形式存在于
煅烧 贝壳(CaCO3)
生石灰
水
海水 石灰乳
盐酸 Mg(OH)2
一定条件
MgCl2·6H2O
MgCl2
电解
Mg
海水
煅烧 贝壳(CaCO3)
生石灰
水
石灰乳
Mg(OH)2
盐酸 MgCl2·6H2O
色,有金属光泽;镁
条
燃烧,发出耀眼的
,生成
色粉末,
同时在瓶内壁有黑色物质生成
有
生成。
1.贝壳煅烧成石灰:
高温
CaCO3 = CaO + CO2 2.石灰制成石灰乳:
CaO + H2O = Ca(OH)2 (石灰乳) 3.石灰乳加入海水沉淀池中得到氢氧化镁沉淀:
Ca(OH)2 + MgCl2 = Mg (OH)2 + CaCl2 4.氢氧化镁与盐酸反应:
2.在氯化镁溶液中,分别投入下列各物质, 既有沉淀出现又有气体产生的是 ( B )
A.氢氧化钠
B.金属钠
C.碳酸钠
D.硫酸钠
实验操作
取一根镁条, 用砂纸将表面 的氧化膜擦去 在酒精灯上点 燃后,伸入 CO2的集气瓶 中
在一支试管中 放镁条,再加 稀硫酸。
实验现象
化学方程 式
镁条呈黑色,擦去氧化镁后呈
曹雪芹
香 菱 学 诗
香菱身世
“粉妆玉琢”
香菱,本名甄英莲 (偕音真应怜),是甄 世隐的女儿。小时候生 得极可爱,是父母的掌 上明珠,三岁那年元宵, 在看社火花灯时被骗子 拐走,过了几年,侥幸 遇到个“风流人品”的 冯公子冯渊(偕音逢冤) 真心正意地要买她,不 料又碰到了呆霸王薛蟠。 打死了冯渊,生拖死拽 地抢走香菱。
一、镁在自然界中的存在形式:
主要以化合态的形式存在于
煅烧 贝壳(CaCO3)
生石灰
水
海水 石灰乳
盐酸 Mg(OH)2
一定条件
MgCl2·6H2O
MgCl2
电解
Mg
海水
煅烧 贝壳(CaCO3)
生石灰
水
石灰乳
Mg(OH)2
盐酸 MgCl2·6H2O
色,有金属光泽;镁
条
燃烧,发出耀眼的
,生成
色粉末,
同时在瓶内壁有黑色物质生成
有
生成。
1.贝壳煅烧成石灰:
高温
CaCO3 = CaO + CO2 2.石灰制成石灰乳:
CaO + H2O = Ca(OH)2 (石灰乳) 3.石灰乳加入海水沉淀池中得到氢氧化镁沉淀:
Ca(OH)2 + MgCl2 = Mg (OH)2 + CaCl2 4.氢氧化镁与盐酸反应:
2.在氯化镁溶液中,分别投入下列各物质, 既有沉淀出现又有气体产生的是 ( B )
A.氢氧化钠
B.金属钠
C.碳酸钠
D.硫酸钠
实验操作
取一根镁条, 用砂纸将表面 的氧化膜擦去 在酒精灯上点 燃后,伸入 CO2的集气瓶 中
在一支试管中 放镁条,再加 稀硫酸。
实验现象
化学方程 式
镁条呈黑色,擦去氧化镁后呈
曹雪芹
香 菱 学 诗
香菱身世
“粉妆玉琢”
香菱,本名甄英莲 (偕音真应怜),是甄 世隐的女儿。小时候生 得极可爱,是父母的掌 上明珠,三岁那年元宵, 在看社火花灯时被骗子 拐走,过了几年,侥幸 遇到个“风流人品”的 冯公子冯渊(偕音逢冤) 真心正意地要买她,不 料又碰到了呆霸王薛蟠。 打死了冯渊,生拖死拽 地抢走香菱。
镁的提取及其应用ppt 苏教版优质课件

镁的物理性质和用途
银白色金属光泽,密度小,硬度小 合金特性:硬度、强度大于任一组分
熔点低于任一组分
主要用途: 1.制合金
2.信号弹、焰火 3.制耐火材料(MgO)熔点高
巩固练习:
1. 用于飞机制造业的重要材料 A.镁铝合金 B.铜锌合金 C.铝铁合金 D.不锈钢
2. 2.4g镁在空气中燃烧,反应转移的电子
数为
。
3. 将镁在SO2中燃烧后,生成的物质可能有
方程式为
。
(SO2与CO2性质类似,S与氧气的性质类似)
14 、心态安好,则幸福常存。有梦想,就要坚持扞卫它。人生是一场又一场离开,熟悉的陌生的,曾走近又走远的。当你真心相信一切都会好的时候,一切就会真的好了。你的目光所及,就是 你的人生境界。总是看到比自己优秀的人,说明你正在走上坡路;总是看到不如自己的人,说明你正在走下坡路。 2 、赢家总有一个计划,输家总有一个借口。 18 、成功就是在不断地克服困难,在困难中创造自己的价值。有心人会在困境中找出路,而无心的人只会在众多的机会中找借口。 16 、后悔是一种耗费精神的情绪。后悔是比损失更大的损失,比错误更大的错误。所以不要后悔。 19 、每个人都有潜在的能量,只是很容易:被习惯所掩盖,被时间所迷离,被惰性所消磨。 18 、金矿的山上还有着其他花朵,除了具备发现的眼睛外,还需要有着肯流汗的心。成功提示:金子常常就埋在身旁的泥土里,勤奋是最好的点金指。 15 、是战士就应该奋勇杀敌,是勇士就应该无所畏惧,要成功就得努力,去拼搏才能胜利,这里是你们驰骋的天地,勇士们,擦亮你们的眼睛,亮出你们的宝剑,活出属于你们的精彩吧! 11 、将欲歙之,必故张之;将欲弱之,必故强之;将欲废之,必故兴之;将欲取之,必故与之。是谓微明。 2 、发现自己的闪光点,挖掘自己的潜能,做你真正喜欢的事业。 12 、、老板只能给一个位置,不能给一个未来。舞台再大,人走茶凉。、下对注,赢一次;跟对人,赢一世。、不识货,半世苦;不识人,一世苦。、学识不如知识,知识不如做事,做事不如做人 。、重师者王,重友者霸,重己者亡。、人生三比:比才华;比财力;比境界。早安!送给自己的话。 19 、做任何事都要经受得挫折,要有恒心和毅力,满怀信心坚持到底。 10 、聆听不代表沉默,有时安静也是一种力量。 10 、如果你被幸运之神遗忘,请不要悲伤,相信阳光总会有一天会照耀在你的身上。 4 、天底下有享不了的福,没有遭不了的罪,多大的苦你要吃,多大的罪你要受,只要你吃苦受罪,好日子就会来了。 14 、人生没有不可逾越的天堑,只要一步步走过去,前方就是幸福的彼岸。 13 、时间是宝贵的,抓住了时间就抓住了成功。 17 、磨砺内心比油饰外表要难得多,世界上没有永恒的懦弱,也没有永恒的坚强,万事靠自己,但是一定要放下懦弱,活的有尊严,活出你的坚强,才真正的体现你的自信和力量,你的活才更 有价值! 11 、这个世界从不缺乏有才能的人,但缺少有精神的人。生活是没有路标的单程轮回,固守心的航向,需要非凡的勇气。以微笑驾驭人生之舟,愿你收获一路精彩! 6 、用乐观的心态迎接困难,因为能打败你的,只有你自己。 20 、想停下来深情地沉湎一番,怎奈行驶的船却没有铁锚;想回过头去重温旧梦,怎奈身后早已没有了归途。因为时间的钟摆一刻也不曾停顿过,所以生命便赋予我们将在汹涌的大潮之中不停地 颠簸。
镁的提取和应用(课件PPT)

解决:浓缩,
利用晒盐后的 母液(卤水)
二、海水提镁的工业流程
问题3:在海边如何获 得工业上氢氧化钙?
二、海水提镁的工业流程
问题3:在海边如何获 得工业上氢氧化钙?
解决:利用海
边的贝壳生产 石灰乳, 降 低成本。
贝壳(CaCO3) 煅烧 CaO 水
Ca(OH)2
二、海水提镁的工业流程
问题4:如何把Mg(OH)2转化 为单质镁?
过滤,加盐酸
特定条件
电解
Mg(OH)2
a
b
MgCl2 溶液
MgCl2·6H2O
浓缩
MgCl2 c Mg
石灰乳
a MgCl2+Ca(OH)2=Mg(OH)2 +CaCl2
b Mg(OH)2+2HCl=MgCl2+2H2O
通电
c MgCl2(熔融) = Mg+Cl2
氯气如何 处理?
镁的原子结构与性质
e- Mg 2 +12 2 82 易失去
课堂回顾
镁容易失去最外层的2个电子形成Mg2+,是一 种比较活泼的金属,可以和某些非金属单质、氧 化物、酸等反应。
2Mg+O2 点燃 2MgO
3Mg+N2 点燃 Mg3N2 2Mg+CO2 点燃 2MgO+C Mg+CuSO4 Cu + MgSO4 Mg+2HCl=MgCl2+H2↑
结构 决定 性质 决定 存在与用途
问题1:海水中含有较
大量的Na+、 K+ 、 Ca2+和Mg2+ 等阳离子,
解决:选择
如何把Mg2+从中分离 氢氧化钙沉
出来?
淀镁离子
二、海水提镁的工业流程
镁的提取及应用PPT课件

现象:迅速反应,生成大量气泡,且放 出热量,温度升高
Mg +2HCl =MgCl 2 + H2 ↑
镁的应用
镁 肥 镁铝焊丝
镁光灯
焰火金属
六、镁与人体健康的关系
1. 镁 关系: 缺镁,人体骨骼会变得疏松崩塌。
人体内有1300多种酶,其中有300多种必须有镁 的 参加,才会发挥催化作用。 镁的含量过低,冠心病的发病几率将大幅升高。
CaO H2O Ca(OH)2
思考3:从沉淀效果看,澄清石灰水比氢氧化钠 效果差得多,如何解决这一矛盾?
用石灰乳代替石灰水
思考4:是不是直接往海水中加沉淀剂?
不是,因为海水中的Mg2+ 的浓度很小,直 接加沉淀剂不利于Mg2+ 的沉淀,而且会增 大沉淀剂的用量,我们可以先将海水浓缩, 再加沉淀剂
四、镁的工业制法流程
Ca(OH)2 + MgCl2 = Mg (OH)2↓ + CaCl2 ④氢氧化镁与盐酸反应:
Mg(OH)2 + 2HCl = MgCl2 + 2H2O ⑤电解熔融的氯化镁可以得到金属镁:
电解
MgCl2 = = Mg + Cl2↑
【实验与探究】
【实验1】取一根打磨好的镁条,用坩埚钳夹 住,在酒精灯上点燃,观察现象。
演讲人:XXXXXX 时 间:XX年XX月XX日
Mg +2H2O =Mg(OH) 2 + H2 ↑
【实验与探究】
【实验5】对实验三的试管进行加热,观察 现象。
现象:加热后镁条表面有大量气泡产生, 加酚酞后溶液变红。
Mg +2H2O ==Mg(OH) 2 + H2 ↑
【实验与探究】
Mg +2HCl =MgCl 2 + H2 ↑
镁的应用
镁 肥 镁铝焊丝
镁光灯
焰火金属
六、镁与人体健康的关系
1. 镁 关系: 缺镁,人体骨骼会变得疏松崩塌。
人体内有1300多种酶,其中有300多种必须有镁 的 参加,才会发挥催化作用。 镁的含量过低,冠心病的发病几率将大幅升高。
CaO H2O Ca(OH)2
思考3:从沉淀效果看,澄清石灰水比氢氧化钠 效果差得多,如何解决这一矛盾?
用石灰乳代替石灰水
思考4:是不是直接往海水中加沉淀剂?
不是,因为海水中的Mg2+ 的浓度很小,直 接加沉淀剂不利于Mg2+ 的沉淀,而且会增 大沉淀剂的用量,我们可以先将海水浓缩, 再加沉淀剂
四、镁的工业制法流程
Ca(OH)2 + MgCl2 = Mg (OH)2↓ + CaCl2 ④氢氧化镁与盐酸反应:
Mg(OH)2 + 2HCl = MgCl2 + 2H2O ⑤电解熔融的氯化镁可以得到金属镁:
电解
MgCl2 = = Mg + Cl2↑
【实验与探究】
【实验1】取一根打磨好的镁条,用坩埚钳夹 住,在酒精灯上点燃,观察现象。
演讲人:XXXXXX 时 间:XX年XX月XX日
Mg +2H2O =Mg(OH) 2 + H2 ↑
【实验与探究】
【实验5】对实验三的试管进行加热,观察 现象。
现象:加热后镁条表面有大量气泡产生, 加酚酞后溶液变红。
Mg +2H2O ==Mg(OH) 2 + H2 ↑
【实验与探究】
镁的提取及应用(共17张)

CaO+CO2↑
生成的CaO属于氧化物,该反应为分解反应。 答案:(1)CaCO3 盐 氧化物 分解反应
(2)上述流程图中,由母液得到氢氧化镁的反应从形式上看属于 应,其离子方程式为 程式: 。
反
(3)上述流程图中,有没有氧化还原反应?
。
。若有,写出其化学方
解析:(2)由母液中获得 Mg(OH)2:MgCl2+Ca(OH)2 应。 离子方程式为 Mg2++Ca(OH)2
素能提升
1.某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程 图如图所示,下列说法错误的是( A )
盐卤 MgCl2 Mg Mg(OH)2 MgCl2 溶液 MgCl2·6H2O
A.若在实验室进行操作①,只需要漏斗和烧杯两种玻璃仪器 B.操作①发生的反应为非氧化还原反应 C.操作②是蒸发浓缩结晶 D.在整个制备过程中,未发生置换反应
Mg(OH)2↓+CaCl2,属于复分解反
Mg(OH)2↓+Ca2+,流程图中 Ca(OH)2 为石灰乳,不可
Mg+Cl2↑。
拆写为离子。 (3)电解熔融 MgCl2 为氧化还原反应,其化学方程式为 MgCl2
答案:(2)复分解 Mg2++Ca(OH)2
(3)有 MgCl2 Mg+Cl2↑
Mg(OH)2↓+Ca2+
)
A.O2
B.Cl2
Cl2、CO2均能反应,与Ar不反应。
4.海水的综合利用可以制备金属镁,其流程如图所示:
(1)贝壳的主要成分是 形式上分)。
,它属于
(填“盐”“氧化物”或 ,该反应的类型属于 (从
最新2.2.4-镁的提取及应用-课件1教学讲义PPT

2.2.4-镁的提取及应用-课 件1
一、镁的提取
1.镁的存在:自然界中的镁主要以 化合态 的形式存在于地壳和海水中。 海水中镁的总储量约为1.8×1015吨。
2.镁的提取
从海水中提取镁,步骤如下:
(1)煅烧海边贝壳(
石灰石
高温
),制成石灰乳。化学方程式:CaCO3
CaO
+CO2↑,CaO+ H2O ===Ca(OH)2↓。
导弹 和 飞机 的部件等。因此,镁被誉为“国防金属”。 (2)由于镁燃烧发出耀眼的 白光 ,因此常用来制造 信号弹 和 焰火 。 2.氧化镁的用途:氧化镁的熔点高达2 800 ℃,是优质的耐高温材料。
镁的提取过程中涉及哪些化学反应?请用化学方程式(离子方程
式)表示。
[学生交流] 【提示】 CaCO3 =高==温== CaO+CO2↑ CaO+H2O===Ca(OH)2 MgCl2+Ca(OH)2===CaCl2+Mg(OH)2↓ [Mg2++Ca(OH)2===Ca2++Mg(OH)2↓] 2HCl+Mg(OH)2===MgCl2+2H2O [Mg(OH)2+2H+===Mg2++2H2O]
是因为镁与酸所电离的H+发生氧化还原反应,把H+还原成氢气。化学方程式:
Mg+H2SO4(稀)===MgSO4+H2↑,离子方程式为 Mg+2H+===Mg2++H2↑ 。 (3)镁与某些氧化物的反应
将燃着的镁条伸入盛满二氧化碳的集气瓶中,镁条 剧烈
燃烧
,发生耀眼此法的优点之一是原料来源丰富 B.进行①②③步骤的目的是从海水中提取MgCl2 C.第④步电解时会产生氯气 D.以上提取镁的过程中涉及的反应有分解反应、化合反应和置换反应
【解析】 提取镁的过程中发生的反应有:CaCO3CaO+CO2↑;CaO+ H2O===Ca(OH)2;Ca(OH)2+MgCl2===Mg(OH)2↓+CaCl2;Mg(OH)2+ 2HCl===MgCl2+2H2O;MgCl2Mg+Cl2↑;此过程中不涉及置换反应。
一、镁的提取
1.镁的存在:自然界中的镁主要以 化合态 的形式存在于地壳和海水中。 海水中镁的总储量约为1.8×1015吨。
2.镁的提取
从海水中提取镁,步骤如下:
(1)煅烧海边贝壳(
石灰石
高温
),制成石灰乳。化学方程式:CaCO3
CaO
+CO2↑,CaO+ H2O ===Ca(OH)2↓。
导弹 和 飞机 的部件等。因此,镁被誉为“国防金属”。 (2)由于镁燃烧发出耀眼的 白光 ,因此常用来制造 信号弹 和 焰火 。 2.氧化镁的用途:氧化镁的熔点高达2 800 ℃,是优质的耐高温材料。
镁的提取过程中涉及哪些化学反应?请用化学方程式(离子方程
式)表示。
[学生交流] 【提示】 CaCO3 =高==温== CaO+CO2↑ CaO+H2O===Ca(OH)2 MgCl2+Ca(OH)2===CaCl2+Mg(OH)2↓ [Mg2++Ca(OH)2===Ca2++Mg(OH)2↓] 2HCl+Mg(OH)2===MgCl2+2H2O [Mg(OH)2+2H+===Mg2++2H2O]
是因为镁与酸所电离的H+发生氧化还原反应,把H+还原成氢气。化学方程式:
Mg+H2SO4(稀)===MgSO4+H2↑,离子方程式为 Mg+2H+===Mg2++H2↑ 。 (3)镁与某些氧化物的反应
将燃着的镁条伸入盛满二氧化碳的集气瓶中,镁条 剧烈
燃烧
,发生耀眼此法的优点之一是原料来源丰富 B.进行①②③步骤的目的是从海水中提取MgCl2 C.第④步电解时会产生氯气 D.以上提取镁的过程中涉及的反应有分解反应、化合反应和置换反应
【解析】 提取镁的过程中发生的反应有:CaCO3CaO+CO2↑;CaO+ H2O===Ca(OH)2;Ca(OH)2+MgCl2===Mg(OH)2↓+CaCl2;Mg(OH)2+ 2HCl===MgCl2+2H2O;MgCl2Mg+Cl2↑;此过程中不涉及置换反应。
镁的提取及应用ppt1
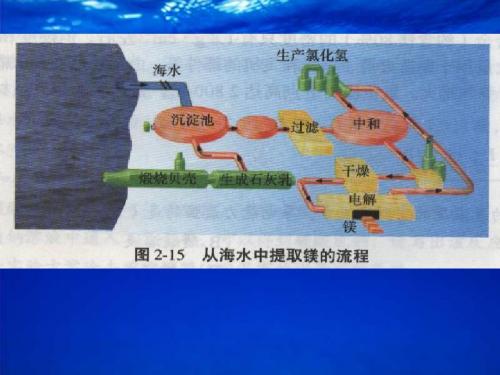
思考:如何由贝壳制得氢氧化钙?
贝壳 (CaCO3) 煅烧
CaO
Ca(OH)2
思考:
1、从沉淀效果看,澄清石灰水比 氢氧化钠效果差得多,如何解决这 一矛盾?
用石灰乳代替石灰水
2、请设计由Mg(OH)2到Mg的可能途径。
思考:
3、如何制得无水MgCl2 ?
先加盐酸反应,再浓缩得 MgCl2·6H2O晶体,然后再将 MgCl2·6H2O晶体在HCl气氛中加热脱 水即可得无水MgCl2
4、由MgCl2 到Mg究竟用还原法还是电 解法好? 由于镁本身比较活泼,用还原法比较 困难,工业上常使用电解熔融的氯化 镁得到镁
[练习]根据讨论,在下列方框中填入合适的物质 的化学式完成工业上用海水提镁的工艺流程,并 写出a、b、c三个步骤的化学方程式:
海水
浓缩
母液
过滤 a Mg(OH) b
加盐酸
主要用途: 彩1、制合金
2、信号弹、焰火 3、制耐火材料(MgO)熔点高
知 识 链 接
焰 火 金 属
镁光灯 烟花的制造
小结
一、镁的存在及提取 二、镁的化学性质 1、与非金属的反应 2、与二氧化碳的反应 3、与酸的反应 4、与水的反应 5、与盐溶液的反应 三、镁的物理性质及用途
决定
结构 性质
决定
拓展视野
镁的应用: 镁合金可用于汽车发动机、车身、车轮、 驾驶盘及盘轴、座椅架、仪表盘、变速 箱以及变速凸轮等部件的制造。典型镁 合金部件的重量仅为相同体积的铝合金 的64%,铁的23%。而每减轻100kg 的重量、燃料消耗就可以降低5%,这对 于节约能源、降低排放具有重大意义。
镁在航空航天和军事上的应用更加广泛,用它 可以设计制造飞行器机身和构件、火箭、导弹、 卫星和探测器等。太空飞船和卫星部件使用镁 合金后能适应太空运行的特殊环境。 在通读设备调研中,镁合金可以部分取代工程 塑料,用于电视机、数字投影仪、播放器、电 话机、像机、计算机部件及小型碟片的设计制 造等。
高中化学《镁的提取及应用》优质课PPT课件

2Mg+CO2 2MgO+C CO2不能用于扑灭由镁、钠活泼金属等引起的火灾。
三、镁的化学性质 (3)镁与水的反应
镁可与热水反应
Mg+2H2O==Mg(OH)2+H2↑ (4)镁与酸的反应
Mg+2H+==Mg2++H2↑
镁
合
四、镁的用途
金
制
品
镁型材、镁锭、镁合金、制
烟火、闪光粉、镁盐等。
氧化镁――熔点2800℃, 常被用做耐高温材料。
煅烧
CaCO3 === CaO+CO2↑ CaO+H2O==Ca(OH)2 。
电解
(3)写出电解饱和食盐水的离子方程式 2Cl‒+2H2O === 2OH‒+Cl2↑+H2 ,↑
若要保证电解后的溶液有恢复为原来的饱和食盐水,则可采取的方法是 通入HCl气体 。
三、镁的化学性质
(1)与非金属的反应 镁在O2中燃烧
镁的提取 及应用
镁的物理性质
从海水中提取镁的流程
镁的化学性质 镁的应用
与非金属反应 在二氧化碳中燃烧 与水反应 与酸反应
1. 镁粉在焰火、闪光粉、鞭炮中是不可缺少的原料,工业制造镁粉
是将镁蒸气在某冷却剂中冷却,下列可作为冷却剂的是( D )
①空气 ②O2 ③Ar ④H2
⑤N2 ⑥H2O
A. ①③④⑤ B. ①③④
镁的提取及应用
学习目标 了解镁的存在及物理性质 掌握镁的化学性质和工业制法
你知道轻盈起飞的舰载机的组成材料吗?
一、镁的物理性质 1. 银白色金属 2. 密度小 镁合金的密度小、硬度和强度大 镁合金大量用于制造火箭、导弹、飞机
三、镁的化学性质 (3)镁与水的反应
镁可与热水反应
Mg+2H2O==Mg(OH)2+H2↑ (4)镁与酸的反应
Mg+2H+==Mg2++H2↑
镁
合
四、镁的用途
金
制
品
镁型材、镁锭、镁合金、制
烟火、闪光粉、镁盐等。
氧化镁――熔点2800℃, 常被用做耐高温材料。
煅烧
CaCO3 === CaO+CO2↑ CaO+H2O==Ca(OH)2 。
电解
(3)写出电解饱和食盐水的离子方程式 2Cl‒+2H2O === 2OH‒+Cl2↑+H2 ,↑
若要保证电解后的溶液有恢复为原来的饱和食盐水,则可采取的方法是 通入HCl气体 。
三、镁的化学性质
(1)与非金属的反应 镁在O2中燃烧
镁的提取 及应用
镁的物理性质
从海水中提取镁的流程
镁的化学性质 镁的应用
与非金属反应 在二氧化碳中燃烧 与水反应 与酸反应
1. 镁粉在焰火、闪光粉、鞭炮中是不可缺少的原料,工业制造镁粉
是将镁蒸气在某冷却剂中冷却,下列可作为冷却剂的是( D )
①空气 ②O2 ③Ar ④H2
⑤N2 ⑥H2O
A. ①③④⑤ B. ①③④
镁的提取及应用
学习目标 了解镁的存在及物理性质 掌握镁的化学性质和工业制法
你知道轻盈起飞的舰载机的组成材料吗?
一、镁的物理性质 1. 银白色金属 2. 密度小 镁合金的密度小、硬度和强度大 镁合金大量用于制造火箭、导弹、飞机
镁的提取和应用 课件

2800℃
712 ℃
海水提取镁的工艺流程图
二、镁的性质与原子结构的关系
易失2e-
Mg
Mg2+
因此:镁很活泼,可与活泼的非金属、 酸等物质反应
1、与非金属的反应:如O2、N2等
请完成相应的化学方程式
实验1:把擦去氧化物保护膜的镁条点燃后伸入 二氧化碳中
现象: 剧烈燃烧,发出耀眼的白光,伴有白 烟,在瓶的内壁有黑色的固体生成
结论:
点燃
2Mg+CO2==2MgO+C
实验2:镁与稀硫酸反应 请完成相应的离子方程式
实验3:镁与水的反应
现象:
镁与冷水不反应,加热发生反应, 产生气泡,滴加酚酞溶液变为红色。
结论: Mg+2H2O=△Mg(OH)2+H2↑
中强碱,能使酚酞变红
三、镁的物性
银白色金属光泽,密度小,硬度小
合金特性:硬度、强度比其组分大
四、主要用途: 彩1、制合金
2、信号弹、焰火 3、制耐火材料(MgO)熔点高
焰火金属
烟花的制造
问题探究:镁粉在焰火、闪光粉、鞭
炮中是不可少的原料,工业制造镁粉
是将镁蒸气在某冷却剂中冷却。下列
可作为冷却剂的是 ③ ④
请说明理由
①空气 ②CO2
④N2
⑤H2
③氩气(Ar)
问题探究:等质量的镁条分别在O2、
CO2、N2中完全燃烧后,生成的固体的
质量的大小关系为
。
在空气中呢?
分离出来?
问题2:是直接往海水中加沉淀剂,还是 先浓缩再加沉淀剂?为什么?
不是,因为海水中的Mg2+的浓度很小,直接加沉 淀剂不利于Mg2+ 的沉淀,而且会增大沉淀剂的用 量,我们可以先将海水浓缩,再加沉淀剂
