克拉维酸钾杂质汇总
校准用标准物质稀释及对照品如何选择-克拉维酸钾杂质种类整理列表

中文名称
英文名称
CAS
提供规格
用途
结构式
克拉维酸钾EP杂质A
Clavulanate Potassium EP Impurity A
4744-51-8
10mg-25mg-50mg-100mg
更多规格请详询
研发分析与一致性评价
纯度≥95
克拉维酸钾EP杂质B
Clavulanate Potassium EP Impurity B
有代理中检院/EP/USP/TRC/TLC/MC/STD等多种品牌
96681-85-5
10mg-25mg-50mg-100mg
更多规格请详询
研发分析与一致性评价
纯度≥95
克拉维酸钾EP杂质C
Clavulanate Potassium EP Impurity C
86917-74-0
10mg-25mg-50mg-100mg
更多规格请详询
研发分析与一致性评价
纯度≥95
克拉维酸钾EP杂质D
3033-62-3
10mg-25mg-5ຫໍສະໝຸດ mg-100mg更多规格请详询
研发分析与一致性评价
纯度≥95
专业提供各种杂质对照品:奥司他韦杂质,克拉维酸钾杂质,利伐沙班杂质,沙库巴曲杂质,帕瑞昔布杂质,拉米地坦杂质等等,并随货提供COA,核磁,质谱,液相等相关图谱。为药物研发单位的第一助手,为其提供专业杂质对照品解决方案。
Clavulanate Potassium EP Impurity J
7677-21-6
10mg-25mg-50mg-100mg
更多规格请详询
研发分析与一致性评价
纯度≥95
克拉维酸钾EP杂质K
阿莫西林克拉维酸钾

阿莫西林克拉维酸钾
抗菌谱:革兰阳性菌中链球菌A、B、C、G族、咽峡炎链球菌、肺炎球菌、米氏链球菌、粪肠球菌、屎肠球菌、金黄色葡萄球菌MSSA、对本品敏感
革兰阴性菌中:淋病奈瑟球菌、脑膜炎球菌、卡他莫拉菌、流感嗜血军菌、大肠埃希菌、克雷伯菌、沙门菌、志贺菌、奇异变形杆菌、普通变形杆菌、普罗非登斯菌、气单胞菌、多杀巴斯德菌、杜克嗜血菌对本品敏感。
对衣原体和支原体效果不好。
厌氧菌中放线菌、脆弱拟杆菌、产黑素普雷澳菌、梭菌属(非艰难梭菌)、坏死梭杆菌、消化链球菌对本品敏感。
本品对耐甲氧西林葡萄糖球菌及肠杆菌属等产染色体介导I型酶的肠杆菌科细菌和假单胞杆菌属无作用。
头孢卡品酯Cefcapene Pivoxil杂质汇总列表

Impurity 3
N/A
25mg 50mg 100mg
项目报批 纯度高于98%
更大规格请咨询
Cefcapene Pivoxil 头孢卡品酯杂质4 Impurity 4 (Cefcapene) 135889-00-8
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
唐 1814- 扬信医药 代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉
Nபைடு நூலகம்A
Impurity 1
25mg 50mg 100mg
项目报批 纯度高于98%
更大规格请咨询
10mg
Cefcapene Pivoxil
头孢卡品酯杂质2
N/A
Impurity 2
25mg 50mg 100mg
项目报批 纯度高于98%
更大规格请咨询
10mg
Cefcapene Pivoxil
头孢卡品酯杂质3
头孢卡品酯Cefcapene Pivoxil杂质汇总列表
中文名称 头孢卡品酯
英文名称 Cefcapene Pivoxil
CAS 105889-45-0
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
10mg
头孢卡品酯杂质1 Cefcapene Pivoxil
志 -064- 维酸钾杂质,红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非;
康
-3157 瑞卢戈利杂质,艾康氟康唑杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢!
阿莫西林克拉维酸钾分散片说明书

成分本品为复方制剂,其组份为阿莫西林和克拉维酸钾。
性状本品为类白色至淡黄色片或薄膜衣片,除去包衣后显类白色至淡黄色。
适应症本品适用于敏感菌引起的各种感染,如:1、上呼吸道感染:鼻窦炎、扁桃体炎、咽炎、中耳炎等。
2、呼吸道感染:急性支气管炎、慢性支气管炎急性发作、肺炎、肺脓肿和支气管扩张合并感染等。
3、泌尿系统感染:膀胱炎、尿道炎、肾盂肾炎、前列腺炎、盆腔炎、淋球菌尿路感染及软性下疳等。
4、皮肤及软组织感染:疖、脓肿、蜂窝组织炎、伤口感染、腹内脓毒症等。
5、其它感染:骨髓炎、败血症、腹膜炎和手术后感染等。
规格0.2285g。
用法用量1、本品可直接用水吞服,也可放入适量水中搅拌至混悬状态后服用。
2、成人及大于12岁儿童,每次2片,一日三次。
3、7-12岁儿童,每次1.5片,一日三次。
4、1-7岁儿童,每次1片,一日三次。
5、3个月-1岁儿童,每次半片,一日三次。
6、严重感染时,剂量可加倍或遵医嘱。
未经重新检查,连续治疗期不超过14天。
不良反应1、少数患者可出现轻度的恶心、呕吐和腹泻等胃肠道副作用,如出现这些副作用,可在吃饭开始时服用就会恢复正常。
2、偶见荨麻疹和麻疹样皮疹,发生荨麻疹和严重的麻疹样皮疹时,应停止使用本品。
3、极少数患者可见暂时性的肝功能异常。
禁忌青霉素过敏者禁用。
注意事项1、用前需做青霉素钠的皮内敏感试验,阳性反应者禁用。
2、动物试验本品无致畸形作用,除非经过医生慎重研究,否则妊娠期内仍不建议使用本品。
3、严重肝功能障碍患者慎用。
4、中度或重度肾功能衰竭的病人使用本品应按医嘱调整剂量。
5、孕妇及哺乳期妇女用药:该药品对妊娠、分娩及哺乳期母婴的影响,未进行该项实验。
6、儿童用药:见本说明,用法用量项下有关儿童用量内容。
对儿童生长发育与成人的差异在药理、毒理或药代动力学方面未进行该项目实验。
7、老年用药:该药品在药理、毒理或药代动力学方面老人与成人的差异,未进行该项目实验。
8、药物过量:过量应用该药品在可能发生的毒性反应、剂量及处理方法方面,未进行该项目实验。
克拉维酸钾杂质总结分享

序号
名称
克拉维酸钾杂质总结分享
CAS
分子式
规格 用途
10mg
Clavulanate
25mg
1 Potassium EP 4744-51-8 C8H12N2O2
研发申报
50mg
Impurity A
100mg
结构式
10mg
Clavulanate
25mg
2 Potassium EP 96681-85-5 C11H16N2O4
研发申报
50mg
Impurity B
100mg
10mg
Clavulanate
25mg
3 Potassium EP 86917-74-0 C10H16N2O2
研发申报
50mg
Impurity C
100mg
10mg
Clavulanate
25mg
4 Potassium EP 404839-11-8 C7H9NO3
研发申报
50mg
Impurity D
100mg
ห้องสมุดไป่ตู้10mg
Clavulanate
1260617-10-
25mg
5 Potassium EP
C16H18N2O10
研发申报
4
50mg
Impurity E
100mg
湖北瑞诺医药---专注杂质对照品、标准品: ①二甲双胍杂质 ②茚达特罗杂质 ③艾司洛尔杂质 ④泊沙康唑杂质 ⑤帕罗西汀杂质 q:300⑥氨甲环酸杂质 ⑦伏立康唑杂质 ⑧文拉法辛杂质 ⑨奥司他韦杂质 ⑩西替利嗪杂质 -8058⑪利奈唑胺杂质 ⑫塞来昔布杂质 ⑬阿奇霉素杂质 ⑭普乐沙福杂质 ⑮卡巴拉汀杂质 -303 ⑯奥贝胆酸杂质 ......等更多项目品种 并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
阿莫西林克拉维酸钾片剂的关键质量属性与控制

阿莫西林克拉维酸钾片剂的关键质量属性与控制作者:吴宁来源:《科学与财富》2018年第32期摘要:阿莫西林克拉维酸钾片剂关键质量属性的有效落实,一方面能够为相关药品制备工作提供更加全面的质量保障前提,由此增强药品生产的可控性;另一方面能够凭借药品质量影响因素,制定更完善的药品产业链条,由此提升药品生产质量水准,以便为药品服用患者提供更全面的质量保障。
所以,本文将着重对片接关键质量属性因素进行着重分析,以便为药品产业提供新的发展思路。
关键词:阿莫西林克拉维酸钾;片剂制备;关键属性;质量控制1 阿莫西林克拉维酸钾片剂关键质量属性探讨的必要性我国药品安全管理体制随经济发展越发完善,传统的药品片剂制备技术早已无法满足现阶段市场药品市场需求,特别是药品质量管控这一方面,更需要完善的管理措施与制备流程,才能确保药品生产水准能够贴合药品经济市场可持续发展的需求。
期间,基于阿莫西林克拉维酸钾片剂药品的临床特性和以往的制备资料可知,此类药品生产质量水平的提升,需要从工艺路线、原辅料属性与工艺参数等多方面分析,才能为后续药品服用质量提供保障。
2 实验材料与方法2.1 仪器与样品材料实验仪器:真空烘箱、热重分析仪、射线衍射仪、元素分析软件、高效液相色谱仪、网络工作站、水分活度仪、统计学软件。
实验药品:阿莫西林三水合物原料、阿莫西林克拉维酸钾片剂、阿莫西林对照品、克拉维酸钾对照品、阿莫西林噻唑酸对照品、2',5'-二酮哌嗪-2阿莫西林对照品、2',5'-二酮哌嗪-2阿莫西林对照品、阿莫西林闭环二聚体对照品和阿莫西林闭环三聚体对照品;色谱纯为乙腈与磷酸二氢钾。
2.2 药品色谱条件色谱柱:C18(4.6mm×250mm,5μm);流动相:流动相A:0.01mol·L-1KH2PO4(用2mol·L-1NaOH调节pH至6.0),流动相B:0.01mol·L-1KH2PO4-CH3CN(20∶80);流速:1.0mL·min-1;检测器:紫外PDA;检测波长:230nm;柱温:30℃;进样器温度:4℃;进样体积:20μL;梯度洗脱[0min(98%A~2%B);20min(70%A~30%B);22min(98%A~2%B);32min(98%A~2%B)]。
克拉维酸钾杂质种类整理列表
项目报批 纯度高于98.89%
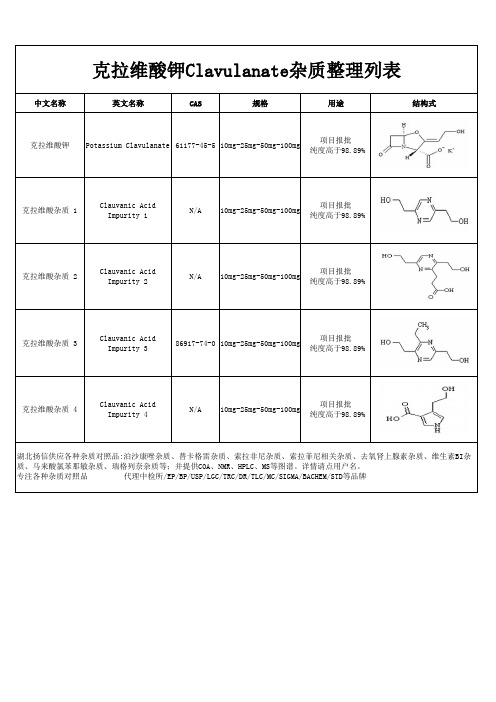
克拉维酸杂质 4
Clauvanic Acid Impurity 4
N/A
10mg-25mg-50mg-100mg
项目报批 纯度高于98.89%
湖北扬信供应各种杂质对照品:泊沙康唑杂质、替卡格雷杂质、索拉非尼杂质、索拉菲尼相关杂质、去氧肾上腺素杂质、维生素BI杂
质、马来酸氯苯那敏杂质、瑞格列奈杂质等;并提供COA、NMR、HPLC、MS等图谱。详情请点用户名。
克拉维酸钾Clavulanate杂质整理列表
中文名称
英文名称
CAS
规格
用途
结构式
克拉维酸钾
Potassium Clavulanate 61177-45-5 10mg-25mg-50mg-100mg
项目报批 纯度高于98.89%
克拉维酸杂质 1
Clauvanic Acid Impurity 1
N/A
10mg-25mg-50mg-100mg
专注各种杂质对照品
代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌
项目报批 纯度高于98.89%
克拉维酸杂质 2
Clauvanic mg-50mg-100mg
项目报批 纯度高于98.89%
克拉维酸杂质 3
Clauvanic Acid Impurity 3
86917-74-0 10mg-25mg-50mg-100mg
阿莫西林-克拉维酸钾

【阿莫西林-克拉维酸钾】<阿莫西林>日文名:アモキシシリン英文名:Amoxicillin 结构式:解离常数:pKa1 = 2.6pKa2 = 7.3pKa3 = 9.7在各溶出介质中的溶解度(37℃):pH1.2:30.7mg/ml pH4.0:3.8mg/mlpH 6.8:4.9mg/ml 水:3.6mg/ml在各溶出介质中的稳定性:水:未测定。
在各pH值溶出介质中:未测定。
光:未测定。
<克拉维酸钾>日文名:クラブラン酸カリウム英文名:Potassium Clavulanate 结构式:解离常数:pKa = 2.36在各溶出介质中的溶解度(37℃):pH1.2:2.5g/ml pH4.0:2.5g/mlpH 6.8:2.5g/ml 水:2.5g/ml在各溶出介质中的稳定性:●水溶液:主要降解为二氧化碳和碱性物质,随降解进行,溶液愈发呈碱性,再进一步促进降解。
由于粒子荷电效应,导致愈是高浓度、溶液愈发不稳定。
●在各pH值溶出介质中:在各pH值溶出介质中的降解速率,均以一级反应速率降解,并皆因缓冲盐的存在,对降解速率产生显著的催化作用。
使用三种缓冲盐测定了催化反应速率常数,结果速率常数kpH的pH依赖性皆与盐种类和浓度无关,仅与酸碱性相关——碱性溶液中降解速率是酸性溶液中的约10倍;并测得pH3.94、6.67、8.74溶液中的阿雷尼厄斯活化能分别为19.0、14.7、18.3kcl/mol。
将0.02%克拉维酸钾溶液【取克拉维酸钾,用pH4.0~9.0的伯瑞坦-罗比森缓冲溶液(Britton-Robinson Buffer Solution)制得】于25℃保存7天,对外观、吸光度、透过率、pH值和效价进行考察,结果酸度和碱度越强、溶液越不稳定,在pH6附近最稳定。
●光:未测定。
●其他:在30℃、相对湿度75%、开封状态下保存3个月,1个月时已吸湿显著,变为褐色粘稠液体。
《四条标准溶出曲线》【颗粒剂】溶出度试验条件:桨板法/50转、溶出介质中不添加表面活性剂。
阿莫西林克拉维酸钾研究资料

药学研究资料综述一、药品名称:通用名:阿莫西林克拉维酸钾(4:1)干混悬剂英文名:Amoxicillin and Clavulanate Potassium for Suspension汉语拼音: Amoxilin Kelaweisuanjia Ganhunxuanji本品为复方制剂,其组分为阿莫西林和克拉维酸钾,两者之比为4:1。
规格:156.25mg(阿莫西林125mg与克拉维酸31.25mg)二、处方工艺:根据《中国药典》2000年版二部及国家药品标准新药转正标准第32册152页“阿莫西林克拉维酸钾(4:1)干混悬剂”项下[WS1-(X-017)-2003Z],本品为阿莫西林钠克拉维酸钾(4:1)均匀混合制成的干混悬剂:1、处方:阿莫西林克拉维酸钾(4:1) 156.25g(阿莫西林125 g与克拉维酸31.25g)微粉硅胶 300g羧甲淀粉钠 100g微晶纤维素 62.5g草莓香精 20g干燥蔗糖粉加至2000 g制成 1000包2、详细制备工艺(1)蔗糖于65℃烘干,备用。
(2)将各原辅料粉碎过80目筛,备用。
(3)按处方量准确称取除蔗糖粉外的各原辅料,混合均匀后,按等量递加法再与处方量干燥蔗糖粉混合均匀。
(4)中间体送检含量,确定装量。
(5)药粉按装量分装于复合膜袋内。
(6)成品全检,包装,入库。
3、工艺处方研究:按《中国药典》2000年版二部及国家药品标准新药转正标准第32册152页阿莫西林克拉维酸钾(4:1)干混悬剂项下[WS1-(X-017)-2003Z],经对辅料的选择;以药粉流动性、装量差异、沉降体积比、粒度、再分散性、含量为目的指标,对本品进行处方筛选,并对含量与溶出度;样品微粉学试验的堆密度、休止角、测装量差异、粒度、沉降体积比、溶化性;临界相对湿度考察进行了考察,结果显示本处方组方合理,适合大生产要求。
影响因素试验:影响因素试验是在较为激烈的条件下进行的。
其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件以及运输建立质量控制方法提供科学依据。
超剂量用药致尿沉渣中出现阿莫西林-克拉维酸钾结晶1例

超剂量用药致尿沉渣中出现阿莫西林-克拉维酸钾结晶1例付 亮1,唐外姣2,吴海雄1(1.南方医科大学第五附属医院检验医学科,广东广州 510900;2.南方医科大学珠江医院药剂科,广东广州 510282)关键词:阿莫西林-克拉维酸钾;药物结晶;尿沉渣;相差显微镜;儿童尿路感染文章编号:1673-8640(2020)01-0092-03 中图分类号:R446.12 文献标志码:B DOI:10.3969/j.issn.1673-8640.2020.01.0221 病例资料患儿,女,10岁,于2018年7月27日至南方医科大学第五附属医院就诊。
患儿就诊7 h前无明显诱因出现尿频、尿急、尿痛,伴有1次全程血尿,伴腹痛(脐周为主,可自行缓解)。
入院查体:体温36.6 ℃,脉搏90 次/min,呼吸20 次/min,血压13.3/10.0 kPa(100/75 mmHg),体质量53 kg,咽部充血,双侧扁桃体无肿大。
心肺及腹部检查无异常。
2018年7月27日门诊血常规:白细胞计数23.63×109/L,中性粒细胞百分比77.6%,淋巴细胞百分比17.3%,血小板计数518×109/L,红细胞计数5.45×1012/L,血红蛋白148 g/L,高敏C反应蛋白3.3 mg/L。
尿常规:隐血“+++”,尿蛋白“+”,白细胞酯酶“++”,白细胞506个/μL,红细胞1 487个/μL。
入院诊断:(1)泌尿道感染;(2)疑急性胃炎。
入院完善相关检查后,当晚即给予阿莫西林-克拉维酸钾抗感染治疗,剂量为1 200 mg,3次/ d,静脉滴注。
2018年7月28日生化检测结果:钾3.83 mmol/L,钠140 m mol/L,氯化物103.6 m mol/L,总钙2.37 mmol/L,无机磷1.90 mmol/L,镁0.89 mmol/L,总蛋白75.2 g/L,白蛋白43.6 g/L,球蛋白31.6 g/L,白/球比值1.4,总胆红素9.5 μmol/L,未结合胆红素3.0 μmol/L,结合胆红素6.5 μmol/L,丙氨酸氨基转移酶28 U/L,天门冬氨酸氨基转移酶23 U/L,丙氨酸氨基转移酶/天门冬氨酸氨基转移酶比值0.8,总二氧化碳19.0 mmol/L,尿素4.13 m mol/L,肌酐38 μmol/L,葡萄糖5.05 m mol/L,尿酸365 μmol/L,降钙素原< 0.05 ng/mL。
克拉维酸钾工艺流程

克拉维酸钾工艺流程英文回答:Potassium clavulanate is an important pharmaceutical intermediate that is widely used in the production of antibiotics. The process of manufacturing potassium clavulanate involves several steps. Let me explain the process in detail.Firstly, the starting material for the synthesis of potassium clavulanate is 6-aminopenicillanic acid (6-APA). This compound is obtained through the fermentation of a specific strain of bacteria. Once the 6-APA is isolated, it undergoes a series of chemical reactions to convert it into clavulanic acid.The next step in the process is the esterification of clavulanic acid with potassium hydroxide to form potassium clavulanate. This reaction is typically carried out in a solvent such as methanol or ethanol. The reaction mixtureis heated and stirred for a specific period of time to ensure complete conversion of clavulanic acid to its potassium salt.After the esterification reaction, the solvent is removed through distillation or evaporation. The resulting crude product is then purified using techniques such as crystallization or chromatography. This helps to remove any impurities and obtain a high-purity potassium clavulanate.Once the purification is complete, the potassium clavulanate is typically dried and milled into a fine powder. It is then packaged and ready for use as a pharmaceutical intermediate.To illustrate the process, let's consider an example. Imagine I am working in a pharmaceutical company and my task is to produce potassium clavulanate. I start by obtaining the 6-APA from the fermentation process. I then set up the esterification reaction by adding clavulanic acid and potassium hydroxide to a reactor vessel. I heat and stir the mixture for a specific period of time,ensuring complete conversion of clavulanic acid topotassium clavulanate. After the reaction, I remove the solvent through distillation and obtain a crude product. I purify the crude product using crystallization, removing impurities and obtaining a high-purity potassium clavulanate. Finally, I dry and mill the product into afine powder, package it, and it is ready for use inantibiotic production.中文回答:克拉维酸钾是一种重要的药物中间体,广泛用于抗生素的生产。
克拉维酸钾生产工艺流程

克拉维酸钾生产工艺流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!克拉维酸钾生产工艺流程一、准备工作阶段。
在进行克拉维酸钾的生产之前,有诸多准备工作需要完成。
克拉维酸钾药品副作用介绍(克拉维酸钾副作用)

克拉维酸钾是一种广泛应用于临床的抗生素药品,常用于治疗呼吸道、泌尿道和皮肤软组织感染等疾病。
然而,就像其他药物一样,克拉维酸钾也存在一些副作用。
了解这些副作用对于患者和医生来说都非常重要。
首先,我们需要注意的是克拉维酸钾可能引起过敏反应。
有些人对克拉维酸钾成分敏感,一旦使用药物就可能出现过敏症状,如皮疹、荨麻疹、面部水肿、呼吸急促等。
如果出现任何过敏反应,请立即停止使用药物,并就医寻求帮助。
其次,克拉维酸钾还可能导致胃肠道不适。
一些常见的胃肠道副作用包括恶心、呕吐、腹泻、腹痛等。
这些副作用通常是暂时性的,随着药物的停用或治疗过程的进行会逐渐减轻。
然而,如果胃肠道不适严重或持续时间较长,应及时就医。
另外,克拉维酸钾也可能对肝脏产生一定的影响。
在使用药物期间,一些患者可能会出现肝功能异常的迹象,如黄疸、肝酶升高等。
这些情况通常是暂时的,但对于有肝病史的患者来说,应谨慎使用克拉维酸钾,并在使用过程中密切观察肝功能的变化。
此外,克拉维酸钾还可能对血液系统产生一定的影响。
一些患者在使用药物后可能会出现血小板减少、贫血等症状。
这种情况较为罕见,但如果出现不明原因的出血、乏力等症状,则应立即就医。
最后,我们需要注意的是克拉维酸钾抗生素的滥用可能导致耐药性的产生。
长期或不适当使用该药物,会使细菌逐渐对药物产生抵抗力,从而降低治疗效果。
因此,在使用克拉维酸钾时应遵循医生的建议,按照正确的剂量和疗程进行使用。
总结起来,克拉维酸钾是一种常用的抗生素药物,但也存在一些副作用。
过敏反应、胃肠道不适、肝脏影响、血液系统影响以及耐药性的产生都是需要重点关注的问题。
在使用药物时,患者应密切关注自身身体状况,并及时向医生汇报任何不适症状。
阿莫西林克拉维酸钾复方制剂中聚合物杂质的分析

药 物 分 析 杂 志 Chin J Pharm Anal 2017,37(8)
·1 4 3 1·
were detected in the amoxicillin clavulanate potassium systematic suitability standard by HPSEC method.It was proved by 2D-HPLC method that amoxicillin open ring dimer was co-eluted with clavulanic acid,and amoxicillin closed-loop dimer was eluted after amoxicillin peak.The polymer impurity peaks in real samples were broadened too severely to be analyzed quantitatively.It was verified that all the polymer impurities detected in the polymer mixed solutions by optimized RP-HPLC method could be eluted by the related substance method loaded in Part Ⅱ,Chinese pharmacopoeia 2015 version.The polymer impurity with the longest retention time was identified as amoxicillin tetrapolymer by column switching LC-MS method.Conclusion:HPSEC method is not suitable for the quality control of polymer impurities in amoxicillin and clavulanate potassium,while the RP-HPLC related substance method loaded in the Chinese pharmacopoeia 2015 edition is accurate and specific,which can effectively control the polymer impurities . Keywords:β-lactam antibiotics;co-amoxicillin and potassium clavulanate;polymer impurity;column-switch LC/MS;2D-HPLC;HPSEC
002 克拉维酸钾质量标准

克拉维酸钾质量标准制 定 人: 日 期:审 核 人: 日 期:批 准 人: 批准日期:生效日期:克拉维酸钾Kelaweisuan JiaClavulanate PotassiumC8H8KNO5 237.25 本品为(Z)-(2S,5R)-3-(2-羟亚乙基)-7-氧代-4-氧杂-1-氮杂双环[3.2.0]庚烷-2-羧酸钾。
按无水物计算,含克拉维酸(C8H9NO5)不得少于75.5%。
【性状】本品为白色或微黄色结晶性粉末;微臭;极易引湿。
本品在水中极易溶解,在甲醇中易溶,在乙醇中微溶,在乙醚中不溶。
比旋度取本品,精密称定,加水溶解并稀释成每1ml中含10mg的溶液,依法测定(附录Ⅵ E),比旋度为+55°至+60°。
【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与克拉维酸对照品峰的保留时间一致。
(2)本品的红外光吸收图谱应与克拉维酸对照品的图谱一致(附录Ⅳ C)。
(3)本品的水溶液显钾盐的鉴别反应(附录Ⅲ)。
【检查】酸碱度取本品200mg,加水20ml溶解后,依法测定(附录Ⅵ H),pH值应为6.0~8.0。
水分取本品,照水分测定法(附录Ⅷ M 第一法 A)测定,含水分不得过1.5%。
重金属取本品0.2g,加水23ml溶解后,加醋酸盐缓冲液(pH3.5)2ml,依法检查(附录ⅧH 第一法),含重金属不得过百万分之二十。
热源取本品,加灭菌注射用水制成每1ml中含10mg的溶液,依法检查(附录ⅪD),剂量按家兔体重每1kg注射1ml,应符合规定(供注射用)。
无菌取本品,分别加入100ml0.9%无菌氯化钠溶液中溶解,用薄膜过滤法处理后,依法检查(附录Ⅺ H),应符合规定(供注射用)。
【含量测定】照高效液相色谱法测定(附录Ⅴ D)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;以 0.1mol/L甲酸铵溶液-甲醇(9:1)为流动相;流速为每分钟0.7ml;检测波长为220nm。
阿莫西林克拉维酸钾制剂中有关物质超高效液相色谱分析方法的建立研究

阿莫西林克拉维酸钾制剂中有关物质超高效液相色谱分析方法的建立研究【摘要】目的:针对阿莫西林克拉维酸钾制剂中有关物质分析构建超高效液相色谱分析方法,并对其应用效果进行评价。
方法:参照高效液相色谱分析方法构建超高效液相色谱分析方法,行方法学研究。
结果:阿莫西林克拉维酸钾制剂中有关物质超高效液相色谱分析法精密度、耐用性、准确度较高,在0.0005mg/mL~2.2mg/mL范围内具有较好线性关系(R>0.999)。
超高效液相色谱分析法与高效液相色谱分析法检查结果差值较小,杂质之间达到基线分离。
结论:超高效液相色谱分析法对阿莫西林克拉维酸钾制剂中有关物质测定具有较好应用效果,能够快速、准确检出杂质,为阿莫西林克拉维酸钾制剂杂质控制提供指导。
【关键词】阿莫西林克拉维酸钾制剂;超高效液相色谱分析法;线性范围;有关物质阿莫西林克拉维酸钾制剂对上呼吸道感染、皮肤软组织感染、尿路系统感染等具有确切疗效,临床治疗总有效率达到70%以上[1]。
随着阿莫西林克拉维酸钾制剂研究的不断深入,形成多种剂型,出现2:1~8:1等多种配比。
在此背景下,如何保证各类型阿莫西林克拉维酸钾制剂质量,成为相关人员关注与思考的重点问题。
以往所用阿莫西林克拉维酸钾制剂有关物质分析方法,时效性较差,且对色谱柱性能具有较高要求,为提高阿莫西林克拉维酸钾制剂有关物质分析效果,本文建立了超高效液相色谱分析方法,现将研究结果报道如下。
1仪器与试剂1.1主要仪器特世科技(上海)有限公司ACQUITY UPLC超高效液相色谱系统:ACQUITY UPLC system型超高液相色谱仪,Waters Empower3.0工作站;安捷伦1260 Infinity柱温箱;特世科技(上海)有限公司E2695高效液相色谱系统:WatersE2695高效液相色谱仪,Waters Empower3.0工作站;美国Milli-Q AdvantageA10超纯水系统等。
1.2主要试剂阿莫西林克拉维酸系统适用性对照品(中国食品药品检定研究院,批号为130588-201603);色谱乙腈(天津市康科德科技有限公司);磷酸二氢钾(山东鼎欣生物科技有限公司,分析纯);氢氧化钠(国药集团化学试剂有限公司,分析纯);阿莫西林系统适用性对照品(中国食品药品检定研究院,批号为130608-202005);10批阿莫西林克拉维酸钾制剂见表1。
克拉维酸钾 ep标准

克拉维酸钾EP标准
克拉维酸钾的EP标准是指欧洲药典(European Pharmacopoeia)对克拉维酸钾的质量和测试方法的标准规定。
这些标准包括了对克拉维酸钾的化学、物理、微生物等方面的测试和要求,以确保其质量和安全性能符合欧洲药典的标准。
在化学方面,EP标准规定了克拉维酸钾的化学式、分子量、结构式等化学信息,以及对其纯度、杂质含量的测试方法和要求。
在物理方面,EP标准规定了克拉维酸钾的外观、颜色、熔点、密度等物理性质,以及对其粒度、流动性、稳定性等物理性能的要求。
在微生物方面,EP标准规定了克拉维酸钾的微生物限度标准,以确保其符合欧洲药典对药物微生物限度的要求。
此外,EP标准还规定了克拉维酸钾的药品包装、标签、储存、运输等方面的要求,以确保其在使用过程中的安全性和有效性。
总之,克拉维酸钾的EP标准是欧洲药典对克拉维酸钾的质量和测试方法的标准规定,旨在确保其质量和安全性能符合欧洲药典的标准,为医生和患者提供更安全、有效的药物选择。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C)
86917-74-0
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
项目报批 纯度高于98%
项目报批 纯度高于98%
结构式
克拉维酸钾杂质 4(克拉维酸钾EP杂
质D)
Clavulanate Potassium Impurity 4
质B)
Clavulanate Potassium Impurity 2
(Clavulanate Potassium EP Impurity
B)
96681-85-5
10mg 25mg 50mg 100mg 更大规格请咨询
克拉维酸钾杂质 3(克拉维酸钾EP杂
质C)
Clavulanate Potassium Impurity 3
克拉维酸钾杂质列表集
中文名称
英文名称
CAS
克拉维酸钾杂质 1(克拉维酸钾EP杂
质A)
Clavulanate Potassium Impurity 1
(Clavulanate Potassium EP ImpurityA)Biblioteka 4744-51-8规格
10mg 25mg 50mg 100mg 更大规格请咨询
克拉维酸钾杂质 2(克拉维酸钾EP杂
(Clavulanate Potassium EP Impurity
D)
404839-11-8
10mg 25mg 50mg 100mg 更大规格请咨询
克拉维酸钾杂质 5(克拉维酸钾EP杂
质E)
Clavulanate Potassium
Impurity 5
(Clavulanate
1260617-10-4
Potassium EP Impurity
E)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑 杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点用户名,谢谢! 专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。
