硅及硅的化合物
硅和硅的化合物

中学化学竞赛试题资源库——硅和硅的化合物A组1.下列属于纯净物的是A 蓝宝石B 钢化玻璃C 王水D 氮化硅2.科索沃战争中,北约部队使用了大量的石墨炸弹,石墨炸弹的主要目标是A 发电厂B 医院C 机械厂D 化学武器库3.下列关于硅和硅的化合物叙述不正确的是①硅晶体的结构和金刚石相似,都是原子晶体;②硅是地壳中含量最多的元素;③单晶硅是良好的半导体材料;④二氧化硅是制造光导纤维的重要原料;⑤二氧化硅分子是由两个氧原子和一个硅原子组成的;③二氧化硅是酸性氧化物,它不溶于任何酸。
A ①②③B ①⑤⑥C ③④⑤D ②⑤⑥4.生石灰中往往含有CaCO3和SiO2杂质,若检验是否存在这两种杂质,最适宜的试剂是A 氟化氢B 浓硫酸C 盐酸D 苛性钠5.某氧化物X难溶于水,能熔于熔融态的烧碱,生成易溶于水的化合物Y,将少量Y溶液滴入盐酸中,最终能生成一种白色的胶状沉淀,则X是A MgOB Al2O3C SiO2D P2O56.能与NaOH溶液反应的原子晶体是A 铝B 金刚石C 硅D 二氧化硅7.地壳中含量第一、第二两种元素之间形成的化合物,不具有的性质是A 可与碳酸钠反应B 熔点较高C 与水作用生成相应的酸D 与碳在电炉中共热可生成两种元素中的一种单质8.关于硅的下列叙述中,不正确的是A 在自然界中,硅既能以游离态形式存在,又能以化合态形式存在B 在硅晶体中,含有由共价键形成的硅原子环,其中最小的环上有6个硅原子C 常温下,硅可以与氟气、强碱溶液起反应D 在加热条件下,硅可与氧气、氯气、硝酸等物质反应9.下列叙述中错误的是:A 石灰石、高岭石、石英和水晶的主要成份都是SiO2B SiO2是通讯材料光导纤维的主要成份C 氧化铝陶瓷,氮化硅陶瓷都是主要的高温结构陶瓷D 含硅4%(质量分数)的钢,可制变压器铁芯10.下列关于硅和二氧化硅的叙述不正确的是A 晶体硅和二氧化硅晶体的结构都类似于金刚石B 晶体硅和二氧化硅晶体都常用来制造电子部件C 硅和二氧化硅都不与酸(氢氟酸除外)反应D 硅和二氧化硅都广泛存在于自然界中,天然单质硅叫硅石11.有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。
硅及硅的化合物相关化学知识点

高中化学:硅及硅的化合物考点一:硅的存在例1:下列叙述中,正确的是()A.自然界中存在大量的单质硅B.石英、水晶、硅石的主要成分都是二氧化硅C.二氧化硅的化学性质活泼,能跟酸或碱的溶液发生化学反应D.自然界中二氧化硅都存在于石英中解析:自然界中硅的含量很高,但都是以化合态形式存在,A选项错误;硅是亲氧元素,在自然界中主要以氧化物及硅酸盐形式存在,如石英、水晶、硅石等主要成分都是二氧化硅,C项正确,D项错误;二氧化硅的性质很稳定,C项错误。
答案:B点评:二氧化硅虽然能够和碱性氧化物、碱溶液反应,但不能说明二氧化硅的化学性质就活泼。
变式训练1:下列物质中,主要成分不是SiO2的是()A.刚玉B.玛瑙C.水晶D.石英考点二:SiO2的性质例2:下列叙述正确的是( )A.因为有反应Na2CO3+SiO2=高温=Na2SiO3+ CO2↑,所以硅酸的酸性比碳酸强B.碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似C.二氧化硅既溶于氢氧化钠溶液又能溶于氢氟酸,所以二氧化硅是两性氧化物D.二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不能和水反应生成硅酸解析:根据酸盐之间复分解反应进行的方向判断酸性强弱一般是在常温湿态下适用,在高温干态下不适用,事实上碳酸酸性比硅酸强,故A项错误;CO2和SiO2属不同类型晶体,在物理性质方面有很大差异,故B项错误;SiO2与氢氟酸反应,不属于酸性氧化物的通性,故C项错误;SiO2虽属于酸性氧化物,但不能直接与H2O反应生成H2SiO3,D项正确。
答案:D点评:Si02高温下能与碳酸盐反应,不能说明硅酸的酸性比碳酸强,而是遵循高沸点物质制低沸点物质的原理,又由于CO2是气体,生成后脱离反应体系,使反应向右进行彻底。
变式训练2-1:下列有关说法正确的是( )A.CO2与水反应生成碳酸,是酸性氧化物;SiO2不能与水反应生成相应的硅酸,不是酸性氧化物B.NaOH溶液不能用带磨口玻璃塞的玻璃瓶盛放C.除去二氧化硅中少量的碳酸钙杂质应选用水D.粗硅制备时,发生的反应为:SiO2+ C=Si + CO2↑例2-2:熔融烧碱应选用的器皿是()A.石英坩埚B.普通玻璃坩埚C.生铁坩埚D.刚玉坩埚解析:石英坩埚和普通玻璃坩埚中都含有SiO2,烧碱能与SiO2发生如下反应:SiO2+2NaOH=Na2SiO3+H2O;刚玉坩埚的主要成分是Al2O3,也能与NaOH 反应:Al2O3+2NaOH=2NaAlO2+H2O。
硅知识点总结

硅及其化合物年月日硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
硅的原子结构示意图为,硅元素位于元素周期表第三周期第ⅣA族,硅原子最外层有4个电子,既不易失去电子又不易得到电子,主要形成四价的化合物。
1、单质硅(Si):(1)物理性质:有金属光泽的灰黑色固体,熔点高,硬度大。
(2)化学性质:①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑②在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
Si+O2SiO2Si+2Cl2SiCl4(3)用途:太阳能电池、计算机芯片以及半导体材料等。
(4)硅的制备:工业上,用C在高温下还原SiO2可制得粗硅。
SiO2+2C=Si(粗)+2CO↑Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl2、二氧化硅(SiO2):(1)SiO2的空间结构:立体网状结构,SiO2直接由原子构成,不存在单个SiO2分子。
(2)物理性质:熔点高,硬度大,不溶于水。
(3)化学性质:SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应:①与强碱反应:SiO2+2NaOH=Na2SiO3+H2O(生成的硅酸钠具有粘性,所以不能用带磨口玻璃塞试剂瓶存放NaOH溶液和Na2SiO3溶液,避免Na2SiO3将瓶塞和试剂瓶粘住,打不开,应用橡皮塞)。
②与氢氟酸反应[SiO2的特性]:SiO2+4HF=SiF4↑+2H2O(利用此反应,氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放,应用塑料瓶)。
③高温下与碱性氧化物反应:SiO2+CaO CaSiO3(4)用途:光导纤维、玛瑙饰物、石英坩埚、水晶镜片、石英钟、仪器轴承、玻璃和建筑材料等。
高一硅及硅的化合物知识点

高一硅及硅的化合物知识点硅(Si)是元素周期表中的第14号元素,属于非金属元素。
硅及其化合物在日常生活和工业生产中具有重要的应用价值。
本文将介绍关于硅及其化合物的知识点。
一、硅的基本性质硅是一种无色、硬度较高、脆性较大的固体物质。
它具有较高的熔点和沸点,不溶于水和大多数常见的溶剂,但能溶于热的氢氟酸和碱性溶液。
硅是一种良好的导热材料,同时具有半导体特性,因此在电子行业中有广泛应用。
二、硅的化合物及应用1. 硅石(SiO2):也称为二氧化硅,是硅最常见的氧化物。
硅石在自然界中广泛存在,常见于石英、石英砂等形式。
它是制备硅金属的重要原料,也用于制备玻璃、陶瓷等材料。
2. 硅酸盐:是一类以硅酸根离子(SiO4^4-)为主的化合物。
硅酸盐在岩石、矿石和土壤中普遍存在,如长石、石英等。
它们具有重要的地质作用,也用于制备建筑材料、陶瓷等。
3. 二氧化硅凝胶:是一种由硅酸盐制备得到的多孔固体材料,具有很高的比表面积和孔隙度。
它被广泛应用于催化剂、吸附剂、保温材料等领域。
4. 硅油:是一种由聚硅氧烷链构成的有机硅化合物,具有良好的润滑性、绝缘性和耐热性。
硅油常用于机械设备的润滑、电子元器件的封装等。
5. 硅树脂:是一类由有机硅聚合物构成的高分子材料,常用于制备塑料、胶黏剂等。
硅树脂具有良好的耐高温性能和化学稳定性,广泛应用于航空航天、电子、汽车等领域。
6. 硅橡胶:是一种由聚硅氧烷和填充剂组成的弹性材料,具有优异的耐高温、耐候性和绝缘性。
硅橡胶常用于制备密封件、隔振垫等。
7. 硅材料在半导体工业中的应用:由于硅具有半导体特性,因此在半导体工业中,硅被广泛应用于制备集成电路、太阳能电池等。
三、硅及其化合物的重要性硅及其化合物在现代工业和科技领域具有重要的地位和应用价值。
硅材料的独特性能使其成为电子行业中不可或缺的材料,半导体工业的发展离不开硅材料。
此外,硅化合物在建筑材料、化工原料、橡胶和塑料等领域也起着重要作用。
最新高考化学专题复习硅及含硅化合物之间的相互转化关系
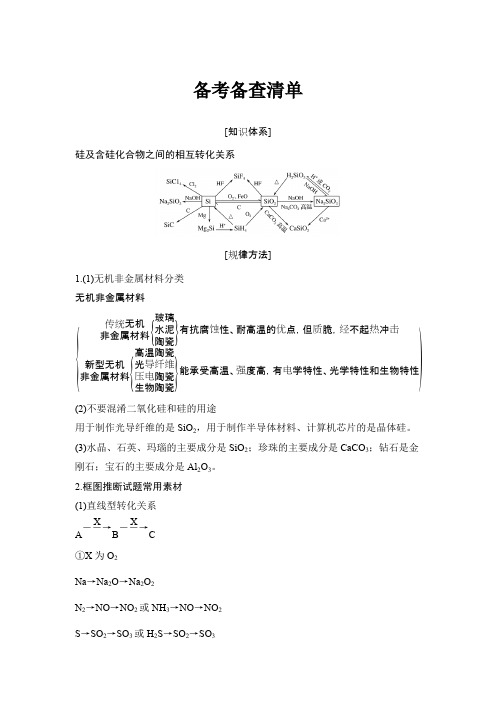
备考备查清单[知识体系]硅及含硅化合物之间的相互转化关系[规律方法]1.(1)无机非金属材料分类无机非金属材料{传统无机非金属材料{玻璃水泥陶瓷}有抗腐蚀性、耐高温的优点,但质脆,经不起热冲击新型无机非金属材料{高温陶瓷光导纤维压电陶瓷生物陶瓷}能承受高温、强度高,有电学特性、光学特性和生物特性)(2)不要混淆二氧化硅和硅的用途用于制作光导纤维的是SiO 2,用于制作半导体材料、计算机芯片的是晶体硅。
(3)水晶、石英、玛瑙的主要成分是SiO 2;珍珠的主要成分是CaCO 3;钻石是金刚石;宝石的主要成分是Al 2O 3。
2.框图推断试题常用素材(1)直线型转化关系A B C――→X ――→X ①X 为O 2Na →Na 2O →Na 2O 2N 2→NO →NO 2或NH 3→NO →NO 2S →SO 2→SO 3或H 2S →SO 2→SO 3C →CO →CO 2或CH 4→CO →CO 2醇→醛→羧酸②X 为CO 2NaOH Na 2CO 3NaHCO 3――→CO2 ――→CO2 ③X 为强酸,如HClNaAlO 2Al(OH)3AlCl 3――→HCl ――→HCl Na 2CO 3NaHCO 3CO 2――→HCl ――→HCl ④X 为强碱,如NaOHAlCl 3Al(OH)3NaAlO 2――→NaOH ――→NaOH (2)交叉型转化(3)三角型转化(4)注意反应形式与物质的关系,特别是置换反应①金属―→金属:金属+盐―→盐+金属,铝热反应。
②金属―→非金属:活泼金属+H 2O(或H +)―→H 2,2Mg +CO 22MgO +C 。
=====点燃 ③非金属―→非金属:2F 2+2H 2O===4HF +O 2,2C +SiO 2Si +2CO ↑,C +H 2O(g)=====高温CO +H 2,X 2+H 2S===2HX +S ↓。
=====高温 ④非金属―→金属,用H 2、C 冶炼金属。
硅及其化合物复习学案

硅及其化合物复习学案
一、硅的基本概述
硅是一种常见的非金属元素,化学符号为Si,原子序数为14,
属于碳族元素。
硅在自然界中广泛存在,主要以二氧化硅的形式存
在于石英、玛瑙、云母等矿石中。
硅是地壳中第二丰富的元素,其
化学性质与炭素相似,具有良好的热稳定性和机械性能。
二、硅的物理性质
1. 外观:硅是一种灰白色的固体,呈无定形或结晶形态。
2. 密度:硅的密度为2.33克/立方厘米,是地壳中密度较小的元素之一。
3. 熔点和沸点:硅的熔点为1414摄氏度,沸点为3265摄氏度,具有较高的熔点和沸点。
4. 导热性和导电性:硅具有良好的导热性和导电性,在室温下,硅的导电率约为铜的1/100。
5. 光学性质:硅具有透明或半透明的性质,能够在红外光谱范
围内传导和发射光线。
三、硅的化学性质
1. 稳定性:硅具有较高的化学稳定性,在常温下与大多数非金
属元素和化合物相对稳定。
2. 与氧的反应:硅与氧反应生成二氧化硅,是常见的氧化反应,如硅与氧气在高温下反应生成二氧化硅:
Si + O2 → SiO2
3. 与酸的反应:硅能够与酸反应生成硅酸盐,如硅与稀盐酸反
应生成氯化硅:
Si + 4HCl → SiCl4 + 2H2
4. 与碱的反应:硅能够与碱反应生成硅酸盐和硅化物,如硅与
氢氧化钠反应生成氢氧化硅和氢气:
Si + 2NaOH → Na2SiO3 + H2 ↑
四、硅的重要化合物。
硅及其化合物Si高中化学必修一知识点

硅及其化合物Si高中化学必修一知识点硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
小偏整理了硅及其化合物Si高中化学必修一知识点,感谢您的每一次阅读。
硅及其化合物Si高中化学必修一知识点硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
硅的原子结构示意图为硅元素位于元素周期表第三周期第ⅣA族,硅原子最外层有4个电子,既不易失去电子又不易得到电子,主要形成四价的化合物。
1、单质硅(Si):(1)物理性质:有金属光泽的灰黑色固体,熔点高,硬度大。
(2)化学性质:①常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑②在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
(3)用途:太阳能电池、计算机芯片以及半导体材料等。
(4)硅的制备:工业上,用C在高温下还原SiO2可制得粗硅。
SiO2+2C=Si(粗)+2CO↑Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl2、二氧化硅(SiO2):(1)SiO2的空间结构:立体网状结构,SiO2直接由原子构成,不存在单个SiO2分子。
(2)物理性质:熔点高,硬度大,不溶于水。
(3)化学性质:SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应。
①与强碱反应:SiO2+2NaOH=Na2SiO3+H2O(生成的硅酸钠具有粘性,所以不能用带磨口玻璃塞试剂瓶存放NaOH溶液和Na2SiO3溶液,避免Na2SiO3将瓶塞和试剂瓶粘住,打不开,应用橡皮塞)。
②与氢氟酸反应[SiO2的特性]:SiO2+4HF=SiF4↑+2H2O(利用此反应,氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放,应用塑料瓶)。
硅及其化合物

硅及其化合物TTA standardization office【TTA 5AB- TTAK 08- TTA 2C】硅及其化合物1、硅硅(Si)物理性质灰黑色,有金属光泽,硬而脆的固体,是半导体,具有较高的硬度和熔点。
化学性质与氟气反应Si+2F2=SiF4与氢氟酸反应Si + 4HF = SiF4↑+ 2H2↑与强碱溶液反应Si + 2NaOH + H2O = Na2SiO3 + 2H2↑与氧气反应Si + O2 SiO2粗硅工业制取SiO2 + 2C 高温Si + 2CO↑存在硅元素在地壳中的含量排第二,仅次于氧,是构成矿物和岩石的主要成分。
硅在地壳中全部以化合态形式存在,没有游离态的硅。
用途太阳能电池、计算机芯片以及良好的半导体材料等。
2、二氧化硅二氧化硅(SiO2)空间结构SiO2直接由原子构成,不存在单个SiO2分子。
一个硅连接四个氧原子,一个氧连接两个硅原子,硅、氧原子个数比为2:1.物理性质坚硬难熔的固体,硬度、熔点都很高。
纯净的晶体俗称水晶化学性质与碱性氧化物反应SiO2+ CO2高温 CaSiO3与强碱溶液反应SiO2 + 2NaOH = Na2SiO3 + H2O(碱溶液不能在使用磨口玻璃塞的试剂瓶中)与碳酸盐反应SiO2 + Na2CO3高温 Na2SiO3 + CO2↑ SiO2 + CaCO3高温CaSiO3 + CO2↑与氢氟酸反应SiO2 + 4HF = SiF4↑+ 2H2O(利用此反应,氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放,应用塑料瓶)存在石英、水晶、玛瑙、硅石、沙子用途光导纤维、玛瑙饰物、石英坩埚、石英钟、仪器轴承、玻璃和建筑材料等。
3、硅酸硅酸(H2SiO3)物理性质不溶于水的白色胶状物,能形成硅胶,吸附水分能力强。
化学性质与强碱溶液反应H2SiO3 + 2NaOH = Na2SiO3 +2H2O加热H2SiO3 H2O + SiO2实验室制取原理H2SiO3是一种弱酸,酸性比碳酸还要弱,但SiO2不溶于水,故不能直接由SiO2溶于水制得,而用可溶性硅酸盐与酸反应制取:(强酸制弱酸原理)Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3(此方程式证明酸性:H2SiO3<H2CO3)Na2SiO3 + 2HCl = H2SiO3↓+ 2NaCl用途硅胶作干燥剂、催化剂的载体。
硅及其化合物PPT课件

△ Si+2Cl2===SiCl4
.
5
与强碱的反应 Si+2NaOH+H2O===NaSiO3+H2
与HF的反应 Si+4HF===SiF4 +2H2
.
6
(3) 单质硅的制法
高温
SiO2+2C==SiCl4
△
SiCl4+2H2===Si+4HCl
化 学 性 质 常 温 下 化 学 性 质 都 不 活 泼。
物质类别 不
氧化物
单
质
物理性质 不 导 电 同
半导体
与HF反应 SiO2+4HF=SiF4↑+2H2O Si+4HF= SiF4↑+2H2↑ 点
与F2反应
不反应
Si+2F2= SiF4
与NaOH反应 SiO2+2NaOH=N.a2SiO3+H2O Si+2NaOH+H2O=Na2SiO3+2H12↑6
硅及其化合物
.
1
晶体硅
单质
无定形硅
硅
二氧化硅
化合物 硅酸
硅酸盐
.
2
1 单质硅
(1)物理性质
晶体硅为灰黑色黑色固体, 熔沸点高,硬度大。属原子 晶体
.
3
(2)硅的化学性质
常温下,化学性质不活泼, 不与强酸,强氧化剂反应, 可于一些非金属单质,氟化 氢,强碱反应
.
4
与非金属的反应
△ Si+O2===SiO2
个人观点供参考,欢迎讨论!
与盐反应 高温 SiO2+Na2CO3===Na2SIO3+CO2
硅、铝及其化合物

1、硅、铝及其化合物一、硅及其重要化合物(1)硅的存在:自然界中以化合态存在,含量仅次于氧,排第二位,是构成矿物和岩石的主要成分。
(2)硅的单质:有晶体硅和无定形硅两种同素异形体,晶体硅是原子晶体,类似于金刚石,熔沸点高、硬度大,是良好的半导体。
(3)硅的性质:性质稳定不易与其他物质发生化学反应①Si+O2=SiO2②Si+2NaOH+H2O=Na2SiO3+2H2↑(4)硅的制备及提纯:SiO2+2C=Si+CO↑,Si+2Cl2=SiCl4SiCl4+2H2=Si+4HCl(5)硅的氧化物SiO2:酸性氧化物:但不溶于水,也不与水反应SiO2+CaO CaSiO3SiO2+2NaOH=Na2SiO3+H2O与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O光导纤维的主要原抖,制造石英玻璃等。
(6)硅及其重要化合物二、镁、铝、铁及其化合物1.镁、铝在元素周期表中位置及原子结构镁(Mg):位于周期表第3周期第IIA原子结构铝(Al):位于周期表第3周期第IIIA,原子结构Mg、Al均为活泼金属,在化学反应中都易失电子,其性质有相似之处,但由于原子结构不同性质上也有差异。
2.镁、铝的物理性质①相同点:密度较小,熔点较低、硬度较小、均为银白色。
②不同点:铅的硬度比镁稍大,熔沸点比镁高,这是由于镁、铅的金属键的强弱不同。
3.镁、铝的化学性质比较:Mg Al暴露在空气中(与O2反应)常温下被O2氧化,形成致密氧化膜、因而具有一定抗腐蚀性很快与O2反应,形成致密氧化膜,抗腐蚀性比镁强燃烧空气中点燃,发出耀眼的白光2Mg + O2 2MgO在纯氧中或高温下可燃烧4Al + 3O2 2Al2O3与某些氧化物反应2Mg +CO2 2MgO+ C 4Al+3MnO22Al2O3+3Mn 2Al+Fe2O3Al2O3+2Fe与H2O反应Mg+2H2O Mg(OH)2↓+H2↑与沸水只有微弱反应与非金属反应3Mg + N2 Mg3N2 2Al+ 3Cl22AlCl3与非氧化性酸反应Mg + 2HCl = MgCl2 + H2↑2Al + 6HCl = 2AlCl3+ 3H2↑与氧化性酸反应能反应,无H2生成4.氧化铝和氢氧化铝A12O3和Al(OH)3是典型的两性化合物,既能与强酸反应。
硅及其化合物总结

⑴、n(Na2O)= 13/62=0.21(mol) n(CaO)= 11.7/56=0.21 (mol)
n(SiO2 )= 75.3/60=1.255 (mol)
普通玻璃的氧化物表示:
CaCO3-----CaO
106
62
100
56
m(Na2O)=10t×13﹪×31×106÷62÷95﹪=72.52(t) m(CaO)=10t×11.7﹪×31×100÷56÷80﹪=80.96(t)
硅是非金属元素,有无定形和晶体两种同素异形体,晶体硅具有金属光泽和某些金属特
性,因此常被称为准金属元素。硅是一种重要的半导体材料,掺微量杂质的硅单晶可用来制
造大功率晶体管、整流器和太阳能电池等。二氧化硅(硅石)是最普遍的化合物,在自然界
中分布极广,构成各种矿物和岩石。最重要的晶体硅石是石英。大而透明的石英晶体叫水晶,
HF能腐蚀玻璃,因此,盛 装氢氟酸不能用玻璃试剂瓶而 要用塑料瓶。
2、实验室盛 装NaOH溶液 的试剂瓶为 什么用橡胶 塞而不用玻 璃塞?
NaOH溶液能与玻璃中的 SiO2反应生成Na2SiO3,使瓶塞 部分粘结而无法打开。因此盛
装NaOH溶液的试剂瓶不能用 玻璃塞而要用橡胶塞。
实验4-1
2、硅酸(H2SiO3)
一、二氧化硅(SiO2)和硅酸
1.二氧化硅
天然的二氧化硅也叫硅石。石英晶 体是结晶的二氧化硅.砂、石英、水晶 的主要成分都是SiO2
1).物理性质: 坚硬难熔的固体,不溶于水。熔沸点高.
2).化学性质:
常温下,二氧化硅的化学
性质不活泼不与水、酸(HF
除外)反应,能与碱性氧化物
或强碱反应生成盐。
a、与氢氟酸反应: SiO2+4HF==SiF4 +2H2O
硅及其化合物

硅及其化合物知识梳理:硅元素在地壳中的含量排第二;在自然界中没有游离态的硅;只有以化合态存在的硅;常见的是二氧化硅、硅酸盐等.. 硅的原子结构示意图为;硅元素位于元素周期表;硅原子最外层有4个电子;既不易失去电子又不易得到电子;主要形成四价的化合物..1、单质硅Si⑴硅的物理性质单质硅是原子晶体;硬度大;熔沸点高;是一种灰黑色;有金属光泽的固体;是良好的半导体材料..(2)化学性质硅的化学性质不活泼;常温下除与F2、HF和NaOH溶液反应外;一般不与其他物质反应;加热时可与O2、Cl2等反应..Si +F2 =Si +HF =Si +NaOH +H2O =Si +O2 =Si +Cl2 =(3)硅的用途:太阳能电池、计算机芯片以及半导体材料等..(4)硅的制备:工业上;用C在高温下还原SiO2可制得粗硅..SiO2+2C=Si粗+2CO↑Si粗+2Cl2=SiCl4SiCl4+2H2=Si纯+4HCl2、二氧化硅SiO2:1SiO2空间结构:立体网状结构的原子晶体;不存在单个SiO2分子..2物理性质:熔点高;硬度大;不溶于水..3化学性质:SiO2常温下化学性质很不活泼;不与水、酸反应氢氟酸除外;能与强碱溶液、氢氟酸反应;高温条件下可以与碱性氧化物反应:NaOHCaOSiO2 + CaCO3HFC注意:①与强碱反应:SiO2与NaOH反应生成Na2SiO3生成的硅酸钠具有粘性;所以不能用带磨口玻璃塞试剂瓶存放NaOH溶液和Na2SiO3溶液;避免Na2SiO3将瓶塞和试剂瓶粘住;打不开;应用橡皮塞..②与氢氟酸反应SiO2的特性:利用此反应;氢氟酸能雕刻玻璃;氢氟酸不能用玻璃试剂瓶存放;应用塑料瓶..4用途:光导纤维、玛瑙饰物、石英坩埚、水晶镜片、石英钟、仪器轴承、玻璃和建筑材料等..3、硅酸H2SiO3:1物理性质:不溶于水的白色胶状物;能形成硅胶;吸附水分能力强..2化学性质:硅酸H2SiO3、原硅酸H4SiO4为不溶于水的弱酸;酸性比碳酸还要弱;其酸酐为SiO2;原硅酸不稳定;在空气中易失水形成硅酸..3硅酸的制备SiO2不溶于水;故不能直接由SiO2溶于水制得;而用可溶性硅酸盐与酸反应制取Na2SiO3 +HCl =Na2SiO3 +CO2 +H2O =4用途:硅胶作干燥剂、催化剂的载体4、硅酸盐1硅酸盐:硅酸盐是由硅、氧、金属元素组成的化合物的总称..大多数难溶于水;最常见的可溶性硅酸盐是Na2SiO3;Na2SiO3的水溶液俗称水玻璃;又称泡花碱;是一种无色粘稠的液体;可以作黏胶剂和木材防火剂..硅酸钠水溶液久置在空气中容易变质:Na2SiO3+CO2+H2O=2 硅酸盐由于组成比较复杂;常用氧化物的形式表示:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水..氧化物前系数配置原则:除氧元素外;其他元素按配置前后原子个数守恒原则配置系数..例如:硅酸钠:Na2SiO3Na2O·SiO2硅酸钙:CaSiO3CaO·SiO2高岭石AI2Si2O5OH4可表示为;正长石KAlSi3O8可表示为.. 5、传统硅酸盐工业三大产品有:玻璃、陶瓷、水泥泥设备水泥回转窑成分硅酸三钙3 CaO·SiO2、硅酸二钙2CaO·SiO2、铝酸三钙3 CaO·Al2O3陶瓷原料黏土陶瓷的优点抗氧化、抗酸碱腐蚀、耐高温、绝缘、易成型等..6、硅及其化合物的转化关系:当堂检测1.在实验室下列物质不与晶体硅反应的是A.F2 B.HF C.KOH溶液 D.Cl22.下列溶液可以盛放在玻璃瓶中;但不能用玻璃塞的是A.硅酸钠溶液B.氢氟酸C.氢氧化钠溶液D.氯化钠溶液3.下列关于硅的说法中不正确的是A.硅是非金属元素;它的单质是灰黑色有金属光泽的固体B.硅的导电性能介于金属和绝缘体之间;是良好的半导体材料C.硅的化学性质不活泼;常温下不与任何物质反应D.加热到一定温度时;硅能与氢气、氧气等反应4.光纤通信是一种现代的通信手段;光纤是光导纤维的简称;制造光导纤维的主要原料是A.铜B.铝C.石英砂D.水玻璃5.下列物质中;没有固定熔沸点的是A.石英B.Na2SiO3 C.固体SO3D.玻璃6.工业制造金刚砂SiC的化学方程式如下:SiO2 + 3C ====== SiC + 2CO ..在这个氧化还原反应中;氧化剂和还原剂的物质的量之比是A.1:2 B.2:1 C.1:1 D.3:57.在无色的强碱性溶液中;能大量共存的是A.Na+、AI3+、NO3-、CI-B.K+、Na+、CI-、SiO32-C.Fe2+、K+、SO42-、CI- D.Na+、HCO3-、K+、NO3-8.在一定条件下;下列物质不能和二氧化硅反应的是焦炭②纯碱③碳酸钙④氢氟酸⑤高氯酸⑥氢氧化钾⑦氧化钙⑧氮气A.③⑤⑦⑧B.⑤⑦⑧C.⑤⑧D.⑤9.下列物质放置在空气中不考虑水分蒸发和吸收空气中的水分变质;且能析出固体;加入盐酸时固体不溶解的是A.澄清石灰水.B.水玻璃C.氢硫酸D.氯化钙溶液10.下列说法正确的是A.陶瓷、玻璃、水泥都是硅酸盐产品B.水晶、玛瑙、光纤、硅胶的主要成分都是SiO2C.SiO2很稳定;与所有的酸都不反应D.将石棉CaMg3Si4O12化学式改写成氧化物的形式:3MgO·CaO·4SiO211.地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是A.熔点很高B.与水反应生成对应的酸C.可与烧碱反应生成盐D.坚硬12.要除去SiO2中混有的少量CaO杂质;最适宜的试剂是A.纯碱溶液B.盐酸C.硫酸D.苛性钠溶液13.能证明硅酸的酸性弱于碳酸酸性的实验事实是A.CO2溶于水形成碳酸;SiO2难溶于水B.CO2通入可溶性硅酸盐中析出硅酸沉淀C.高温下SiO2与碳酸盐反应生成CO2D.氯化氢通入可溶性碳酸盐溶液中放出气体;通入可溶性硅酸盐溶液中生成沉淀14.下列试剂能贮存在磨口玻璃塞的试剂瓶里的是A.HF溶液B.KOH溶液C.盐酸D.水玻璃15.能将Na2SiO3、CaCO3、SiO2三种白色粉末鉴别开来的试剂是A.NaOH溶液B.水C.氢氟酸D.稀盐酸16.下列物质的变化;不能通过一步化学反应完成的是A.CO2→H2CO3B.SiO2→Na2SiO3C.Na2O→Na2CO3D.SiO2→H2SiO3。
硅及其化合物知识总结

硅及其化合物知识总结1.硅单质(Si)(1)存在:硅是一种亲氧元素,在自然界中以化合态存在,在地壳中的含量仅次于氧。
(2)物理性质:晶体硅是灰黑色固体,硬度大,熔、沸点高,具有金属光泽。
(3)化学性质:常温下能与F 2、HF 、NaOH 反应;加热时能与H 2化合生成不稳定的氢化物SiH 4,还能与Cl 2、O 2化合分别生成SiCl 4、SiO 2。
涉及的化学方程式如下:2:Si +O 2=====△SiO 22:Si +2F 2===SiF 42:Si +2Cl 2=====△SiCl 4②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑(4)用途:①良好的半导体材料;②太阳能电池;③计算机芯片。
(5)高纯硅的制备①SiO 2+2C=====高温Si(粗)+2CO ↑(1800~2000℃)②③2.二氧化硅(SiO 2)(1)存在与形态SiO 2的存在形态有结晶形和无定形两大类。
自然界中的二氧化硅,存在于沙子、水晶、玛瑙,石英等中。
(2)结构SiO 2是由Si 原子和O 原子按个数比1∶2直接构成的立体网状结构的晶体。
(3)二氧化硅与二氧化碳都是酸性氧化物,二者的性质与用途比较性质与用途二氧化硅二氧化碳物理性质硬度大,熔、沸点高,不溶于水熔、沸点低,可溶于水化学性质与水反应不反应CO 2+H 2OH 2CO 3与酸反应(只与HF 反应)氢氟酸用于刻蚀玻璃:SiO 2+4HF===SiF 4↑+2H 2O不反应与碱反应(如NaOH)SiO 2+2NaOH===Na 2SiO 3+H 2O(盛碱液的试剂瓶不能用玻璃塞)CO 2+2NaOH===Na 2CO 3+H 2O 或CO 2+NaOH===NaHCO 3与盐反应(如Na 2CO 3)SiO 2+Na 2CO 3=====高温Na 2SiO 3+CO 2↑CO 2+Na 2CO 3+H 2O===2NaHCO 3与碱性氧化物反应与CaO 反应:SiO 2+CaO=====高温CaSiO 3与Na 2O 反应:CO 2+Na 2O===Na 2CO 3与碳反应2C +SiO 2=====高温Si +2CO ↑C +CO 2=====高温2CO 主要用途制光学仪器、石英玻璃;水晶和玛瑙可制作饰品;常用来制造通讯材料——光导纤维;以SiO 2为主要成分的沙子是基本的建筑材料化工原料、灭火剂;干冰用作制冷剂,人工降雨3.硅酸(H 2SiO 3)(1)物理性质:难溶于水的白色胶状物质。
化学硅的知识点

化学硅的知识点
1. 硅元素:硅是一种非金属元素,位于第14族,原子序数为14,化学符号为Si。
2. 硅的性质:硅是一种灰色的坚硬晶体,可以通过三种不同的形态(晶体硅,非晶硅和纳米晶硅)存在。
它是不可溶于水的,但可以溶解于大多数互不相容的溶剂中,如氢氟酸和密度大约为2.33 g/cm³的苛性钠。
3. 硅的用途:硅是一种广泛应用于电子和半导体领域的材料,其重要性体现在各种电子设备和计算机上。
硅在制造晶体管、半导体、太阳能电池板等方面应用广泛,它还用于制造玻璃、沙鼠、硅橡胶、硅油等。
4. 硅化合物:硅能形成许多不同的化合物,如SiO2,SiC,SiH4等。
SiO2也被称为二氧化硅,是地球上最常见的化合物之一。
SiC是一种具有高度耐腐蚀性和强度的陶瓷材料。
SiH4是一种高度易爆的气体,常用于制造半导体材料。
5. 硅的制备方法:硅可以通过多种方法制备,其中最常见的是从硅矿石中提取。
硅矿石通常是以SiO2的形式存在,通过熔融还原法或化学还原法可以得到纯硅。
在实验室中,还可以通过电化学方法或热分解的方法进行制备。
6. 硅烷:硅烷是最简单的硅化合物之一,其分子式为SiH4,属于非极性分子。
硅烷是一种高度易爆的气体,可以通过化学还原法制备。
它在半导体加工和纳米
技术等领域有广泛应用。
高中化学必修1第四章第一节硅及硅的化合物

• C.1∶2 D.2∶1
关于硅的说法不正确的( C )
A.晶体硅的导电性介于金属和绝缘体之间, 是良好的半导体材料
B.晶体硅具有较高的熔沸点,硬度也很大
C.单质硅的化学性质不活泼,常温下不与任 何物质反应,加热到一定温度时,硅能 与碳、氧气等非金属反应
D.硅是非金属元素,它的单质是灰黑色的有 金属光泽的固体
人教版高一化学必修1第四章非金属及其化合物
硅单质 人造石英 玛瑙
一、硅 1、存在 含量第二位 构成矿物和岩石的主要元素。 以二氧化硅和硅酸盐形式存在。 2、物理性质 灰黑色有金属光泽,硬而脆,良好的 半导体材料。
3、化学性质 • 化学性质不活泼,常温下只与氟气,
氢氟酸,强碱反应。
• Si + 2F2 = SiF4 • Si + 4HF = SiF4 + 2H2↑
二、二氧化硅
• 1,物理性质 • 坚硬不溶的固体,耐高温﹑耐腐蚀。 • 纯净的SiO2无色透明---水晶 • 常见:石英、沙石、硅石
• 2,化学性质 • 化学性质不活泼,通常不与强酸反应。 • 特殊:能和氢氟酸反应。
• SiO2 + 4HF==SiF4 + 2H2O • 酸性氧化物 • SiO2 + 2NaOH==Na2SiO3+H2O
高温下
• SiO2+CaO CaSiO3 • Na2CO3+SiO2 Na2SiO3+CO2↑ • CaCO3+SiO2 CaSiO3+CO2↑ • 3,用途:制光导纤维,石英坩埚。 • 优点:质轻、导光能力强、抗干扰性
好﹑耐腐蚀。
二氧化硅可用来做光导纤维;石英可用来做石英钟、石 英表,耐高温的石英玻璃;水晶可以用来制造电子工业中 的重要部件、光学仪器、工艺品、眼镜片等,玛瑙为含有 有色杂质的石英,可用于制造精密仪器轴承,耐磨器皿和 装饰品等。 但有时也会对人体造成危害,使人患硅肺病 。
一节硅和硅的化合物最新版最新版

(2)物理性质: 熔沸点高、硬度大、半导体
硅化的学用性途质::加常热温或能高与温F2能、与HFO、2、NCaOl2、H反C等应反; 应表现还原性
(5)硅的制法: SiO2+2C
高温
= Si +2CO
2、二氧化硅(SiO2):
存在: 用途:
(3)物理性质: 坚硬难熔的固体,不溶于水 化学性质: 不溶于水的酸性氧化物
硅酸原钠硅是酸一:种H4白Si色O4 的同固上体物质,易溶于水,其水溶液 俗称多水硅玻酸璃:,硅呈酸粘或稠多状硅,酸能缩与水盐后酸的等产强物酸反应, 能与CO2和H2O反应。
• 硅酸盐
• 硅酸钠:Na2SiO3 • 高岭石:
Na2O·SiO2
Al2(Si2O5)(OH)4 粘 土:高岭土
Al2O3 ·2SiO2 ·2H2O
能与CaO、NaOH、HF等反应
硅酸(H2SiO3): 不溶于水,酸性比碳酸弱
4、硅酸盐: Na2SiO3
晶体硅
二、硅
晶体硅是良好的半导体材料
无定形硅
晶体硅的结构
类似于金刚石
0. 硅的发现
硅石(硅的氧化物)、水晶早为古代人所认识, 古埃及就已经用石英砂为原料制造玻璃。由于硅石化 学性质稳定,除了氢氟酸外什么酸也不能侵蚀它、溶 解它,因此长期以来人们把它看成是不能再分的物质 大约在18世纪70年代,化学家们用萤石( CaF2 )与硫 酸作用发现氢氟酸以后,便打开了人们认识硅石复杂 组成的大门。尤其电池发明以后,化学家们利用电池 获得了活泼金属钾、钠,初步找到了把硅从它的化合 物中分离出来的途径。1823年,瑞典化学家贝采利乌 斯(1779~1848)用金属钾还原SiF4或用金属钾与氟硅 酸钾共热,首次制得粉状单质硅。
硅和硅的化合物

SiO2晶体的空间结构: 正四面体型,立体网状结构。SiO2直接由 原子构成,不存在单个SiO2分子。SiO2只是组 成简式,不是分子式。 每个Si原子周围结合 4个O原子,Si在中心,O在 4个顶角;许多这样的四面体又通过顶角的O原子相 连接,每个 为 个 面体所共有,即每个 与 个 相 合 连接,每个O为两个四面体所共有,即每个O与2个Si相结合。
2
用途: ① 氧 硅 制造高 能 ①二氧化硅是制造高性能通讯材料 材料——光导纤维的重要原料。 光 的 料 ②石英用来制造石英电子表、石英钟。较纯净的石英用来制造石英玻 璃 石英玻璃常用来制造耐高温的化学仪器 璃,石英玻璃常用来制造耐高温的化学仪器。 ③水晶常用来制造电子工业中的重要部件、光学仪器、工艺品和眼镜 片等。 ④玛瑙用于制造精密仪器轴承、耐磨器皿和装饰品。
用途: ①硅 ①硅可用来制造集成电路、晶体管、硅整流器等半导体器件,还可制成 来制造集成电路 体管 硅整 等半导体 件 制成 太阳能电池。 ②利用硅的合金 可用来制造变压器铁芯和耐酸设备等 ②利用硅的合金,可用来制造变压器铁芯和耐酸设备等。 制法 工业制法: 高温条件下
SiO2 + 2C → Si + 2CO↑ Si(粗硅) + 2Cl2 → SiCl4 SiCl4 + 2H2 → Si(精硅) + 4HCl
巩固与提升 固与 升 1.据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未 来的石油”的观点 来的石油 的观点。假如硅作为 假如硅作为一种普遍使用的新型能源被开发利用 种普遍使用的新型能源被开发利用 下列关于其有利因素的说法中,你认为不妥的是( ) A.便于运输、储存,从安全角度考虑,硅是最佳的燃料 于 存, 角 考虑, 最 料 B.自然界的含硅化合物易开采 C.硅燃烧放出的热量大,燃烧产物对环境污染程度低且容易有效控制 D.自然界中存在大量单质硅 自然界中存在 量单质硅
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
KAlSi3O8
钙沸石
正长石
硅酸盐在陶瓷中的应用
硅酸盐工业
1、玻璃: 原料:纯碱、石灰石和石英
Na2CO3+SiO2=Na2SiO3+CO2↑ CaCO3+SiO2==CaSiO3+CO2↑ 主要成分:Na2SiO3、CaSiO3、SiO2 (Na2O•CaO•6SiO2)
2、水泥:主要原料:粘土和石灰石
水晶
玛瑙
石英:耐高温化学仪器、石英电子表 石英钟
水晶:电子工业的重要部件、光学仪器、 高级工艺品和眼镜片
玛瑙:精密仪器轴承、耐磨器皿和装饰品
石英玻璃有许多特殊性质, 如能高度透过可见光和紫 外光,膨胀系数小,能经 受温度的剧变。因此可做 紫外灯和光学仪器。
二氧化硅的化学性质
与酸反应:
玻璃的主要成分是SiO2,化学性质不活泼, 不与水反应,不与除HF外的酸反应,所以在生 活中常用HF来雕刻玻璃。
• SiF4无色,刺激性气味,再水中强烈水解(气相产 物:F3SiOSiF3)
• 四氟化硅的制备: • CaF2+H2SO4----CaSO4+2HF • SiO2+4HF----SiF4+2H2O • SiF4与HF相互作用生成酸性较强的氟硅酸: • 2HF+ SiF4----H2(SiF6) • H2(SiF6)游离态易分解,水溶液稳定,具有强酸性
思考与交流:CO2+H2O=H2CO3,我们知道SiO2不 能(1直)接制和取水化合成H2SiO3,那怎样制原备理 H2SiO3呢?
Na2SiO3+2HCl=2NaCl+H2SiO3↓ 强酸制弱酸
现象 红色逐渐消失,且有白色胶状沉淀生成
结论
难溶于水的弱酸
方程式
Na2SiO3+2HCl=2NaCl+H2SiO3↓
硅的氧化物及硅酸盐构成了 地壳中大部分的岩石、沙子和土 壤、约占地壳总量的90%以上。
硅的氧化物
• 二氧化硅又称硅石
石英是天然的二氧化硅 原子晶体,其中每个硅 原子与4个氧原子以单键 相连,构成SiO4四面体 结构单元。Si原子位于 四面体的中心,4个氧原 子位于四面体的顶角。
天然硅石
纯净的石英又叫水晶,它是一种坚硬、脆性、 难溶的无色透明的固体,常用于制作光学仪 器等。
演示完毕谢谢。
我国现有水泥企业8000多家,上次许可证发证企业7400家左右,而20 万吨以上的企业不足10%,全国水泥企业平均规模不到10万吨,与世界其 它国家相经差距极大。
与碱反应:
SiO2+2NaOH---Na2SiO3+H2O
与盐反应:
SiO2+2Na2CO3---Na2SiO3+CO2
硅酸及其盐
硅酸(H2SiO3)
石膏—作用是调节水泥硬化速度
3、陶瓷:主要原料:粘土
4、特殊含硅化合物——碳化硅SiC,俗名金刚砂
(金刚石,二氧化硅),具有的空间网状结构,硬度 大,熔点高
硅酸盐在生活用具中的应用
酸碳 盐化
硅 零 件 及 硅
无机非金属材料 硅酸盐产品
陶瓷 水泥 玻璃
t
硅的卤化物
• 硅的卤化SiX4都是无色的,常温下SiF4是气体, SiCl4和SiBr4是液体,SiI4是固体
化学方程式: 。 SiO2+4HF=SiF4↑+2H2O
水泥 成分
硅酸三钙、硅酸二钙、铝酸三钙
原料 石灰石、粘土、辅助原料
水
设备 水 泥 回 转 窑
泥
工
反应 条件高温业来自生产 过程生料→熟料
水泥 应用
建筑粘合剂
水泥 工业 展望
中国水泥工业明天更美好
我国水泥工业已经历了100多年的历史。旧中国的水泥工业在漫长的 20世纪前50年内,步履维艰,发展缓慢,只有在新中国诞生以后,水泥工 业才走一了健康发展之路。
硅的氢化物
• 硅的氢化物又称硅烷(SinH2n+2) • 与碳烷不同:
1.硅烷数目有限 2.硅与氢不能生成烯烃,炔烃类似不饱和化合物. 最简单的硅烷:甲硅烷SiH4(无色无臭气体 ) 甲硅烷的制取 (1)Mg2Si+4HCl2MgCl2 +SiH4 (2)SiCl4+LiAlH4 SiH4+LiCl+AlCl3
我国水泥总产量虽高,但由于人口多,所以人你产量罗低。如在90年 代中期,意大利、西班牙、德国、法国、美国、日本、韩国人均产量(千 克)分别为584、630、434、320、339、654、1318,同期我国为412千克。 从1994年至1999年,我国人均消费(千克)分别为352、399、412、428、 435、472。
硅及硅的化合物
主讲人:袁小平、黎轩、张德 许伟瑜、赵志新
硅
美国硅谷
工业制粗硅:
高温
SiO2+2C===Si+2CO↑
粗硅提纯:
Si+2Cl高2==温=SiCl4 SiCl4+2H高2==温=Si+4HCl
+C SiO2高温粗硅
+Cl2 高温
SiCl4 精馏+H2 高温
Si
硅元素(silicon)在地壳中的含量
燃烧
无明火,不燃烧
Na2SiO3不易燃烧,可作防火剂
Na2SiO3溶液(水玻璃)— 木材防火、黏胶剂等
硅酸盐的改写:
硅酸盐是构成地壳岩石的主要成分(5%)
Na2SiO3 : Na2O·SiO2 Al2(Si2O5)(OH)4 : Al2O3·2SiO2·2H2O
高岭石
Ca(Al2Si3O10)·3H2O
-
SiH4的性质
• 化学性质活泼 SiH4+2O2-----SiO2+H2O
• 有强的还原性 SiH2+2K2MnO4----2MnO2+K2SiO3+H2O+H2
• 对碱十分敏感
SiH4+(n-2)H2O—SiO2 ·nH2O+H2 (需要催化剂)
• 热稳定性差 SiH4(g)-----Si(s)+2H2(g) (在500摄氏度)
① 白色胶状,难溶(白色胶状)
(2)性质: ② 弱酸性(酸性 H2SiO3 < H2CO3) Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
③ 脱水形成硅胶 用作干燥剂、吸咐剂
硅酸盐
硅酸盐是由硅、氧和金属组成的化合物的总称。
硅酸钠(Na2SiO3):
现象 结论
放入蒸馏水 放入Na2SiO3饱和溶液
建国后50年,水泥工业发生了翻天覆地的变化,尤其是1979年改革开 放以来,随着国民经济发展和人民生活水平的不断提高,水泥工业得到迅 速发展,产量和质量都有有了很大提高。
水泥产量自1979年到1999年增长了7.8倍,20年间我国水泥产量平均 增长达11.08%,水泥产量自1995年以来一直居全世界首位。其中1999年 我国水泥产量占世界的37.16%。
硼和硅的相似性
• 硼和硅在元素周期表中处于对角线的位置,它们 的化合物表现出相似性。
• 举例说明: • 1)单质与碱反应H2 • 2)氢化物:化学性质活泼,易挥发,与水反应生成
氢气 • 3)能生成玻璃态氧化物 • 4)氧化物显酸性与金属氧化物生成硅酸盐和硼酸
盐 • 5)硅酸和硼酸都是弱酸 • 6)卤化物水解都生成相应酸
