离子反应和离子共存练习题
高三化学离子共存试题(含答案)

离子共存1.在pH=1的溶液中能大量共存的一组离子或分子是 :A.Na+、Mg2+、ClO—、NO3—B. Al3+、 NH4+、 Br-、Cl-C. K+、Cr2O72-、CH3CHO、 SO42-D. Na+、K+、SiO32-、Cl-2..能在溶液中大量共存的一组离子是A.NH4+、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-C.K+、Na+、NO3-、MnO4- D.Al3+、Mg2+、SO42-、CO32-3.下列离子组一定能大量共存的是A.甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3-C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO-D.含大量OH一的溶液中:CO32-、Cl-、F-、K+4.(2011江苏高考4)常温下,下列各组离子在指定溶液中一定能大量共存的是A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl-C.pH=12的溶液:K+、Na+、CH3COO-、Br-D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-5.(2011安徽高考8)室温下,下列各组离子在指定溶液中能大量共存的是A.饱和氯水中 Cl-、NO3-、Na+、SO32-B.c(H+)=1.0×10-13mol/L溶液中 C6H5O-、K+、SO42-、Br-C.Na2S溶液中 SO42-、 K+、Cl-、Cu2+D.pH=12的溶液中 NO3-、I-、Na+、Al3+6. (2011广东高考8)能在水溶液中大量共存的一组离子是A. H+、I―、NO3―、SiO32-B. Ag+、Fe3+、Cl―、SO42―C.K+、SO42-、Cu2+、NO3―D.NH4+、OH-、Cl-、HCO3-7.(2011全国II卷11)将足量CO2通入下列各溶液中,所含离子还能大量共存的是A.K+、SiO32-、Cl-、NO3-B.H+、NH4+、Al3+、SO42-C.Na+、S2-、OH-、SO42-D.Na+、C6H5O-、CH3COO-、HCO3-8.(2011四川)甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。
高一化学离子方程式离子共存练习题(附答案)

高一化学离子方程式离子共存练习题一、单选题1.下列两种物质的溶液混合后不能发生离子反应的是( )A.3HNO 和23Na COB.NaCl 和3AgNOC.24K SO 和2BaClD.3HNO 和2BaCl2.下列反应不能用离子方程式2244Ba +SO BaSO +-=↓表示的是( )A .氢氧化钡与硫酸B .氯化钡与硫酸钠C .硝酸钡与硫酸钾D .氢氧化钡与硫酸钠 3.下列各选项中的反应①与反应②不能用同一离子方程式表示的是( )序号 反应①反应②A 向3AgNO 溶液中滴加稀盐酸 3AgNO 溶液与食盐水混合B 过量2CO 通入NaOH 溶液中 过量2CO 通入澄清石灰水中 C向烧碱溶液中滴加稀盐酸向24H SO 溶液中滴加KOH溶液D向2BaCl 溶液中滴加稀硫酸 向2Ba(OH)溶液中滴加4CuSO 溶液4.下列化学反应,能用离子方程式232CO H-++22CO H O ↑+来表示的是( )A.稀硝酸和碳酸钡的反应B.稀硝酸和碳酸钾溶液的反应C.石灰石和盐酸的反应D.盐酸和NaHCO 3溶液的反应5.下列离子方程式书写正确的是( ) A.碳酸钾与盐酸反应: 3CO -+2H+CO 2+H 2OB.硫酸和氯化钡溶液反应:Ba 2++24SO -BaSO 4↓C.铜插入硝酸银溶液中:Cu+Ag+Ag+Cu2+ D.铁放入硫酸铜溶液中:2Fe+3Cu 2+2Fe 3++3Cu6.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( ) A.氢氧化钠与盐酸;氢氧化钠与碳酸 B.石灰石与硝酸;石灰石与盐酸C.BaCl 2溶液与Na 2SO 4溶液;Ba(OH)2溶液与NaHSO 4溶液D.Na 2CO 3溶液与硝酸溶液;CaCO 3溶液与硝酸溶液 7.下列有关CuSO 4溶液的叙述正确的是( )A.该溶液中Na +、4NH +、3NO -、Mg 2+可以大量共存 B.通入CO 2气体产生蓝色沉淀 C.与H 2S 反应的离子方程式:Cu 2++S 2-CuS↓D.与过量浓氨水反应的离子方程式: 2+32Cu +2NH H O ⋅()+42Cu OH +2NH ↓8.下列离子方程式正确的是( )A.铁跟FeCl 3溶液反应:Fe+Fe 3+=2Fe 2+B.Fe 跟稀盐酸反应:2Fe+6H +=2Fe 3++3H 2↑ C.FeCl 2溶液跟Cl 2反应:Fe 2++Cl 2=Fe 3++2Cl - D.Fe(OH)3跟盐酸反应:Fe(OH)3+3H +=Fe 3++3H 2O9.离子方程式+2+322BaCO +2H =CO +H O+Ba ↑中的+H 不能代表的物质是( )①HCl ②24H SO ③3HNO ④4NaHSO ⑤3CH COOH A.①③ B.①④⑤ C.②④⑤ D.①⑤10.下列化学反应对应的离子方程式,书写正确的是( )A.氢氧化钡溶液与稀盐酸的反应:-+2OH +H =H OB.澄清石灰水与稀盐酸的反应:+2+22Ca(OH)+2H =Ca +2H OC.铜片插入硝酸汞溶液中:+2+Cu+Hg =Hg+CuD.碳酸钙溶于稀盐酸中:2-+322CO +2H =H O+CO ↑11.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示。
离子共存习题及解答

离子共存题型1:离子间因发生复分解反应(离子互换反应)而不能大量共存。
例1、下列各组离子在水溶液中能大量共存的是()(A)K+ HCO3— CO32— Br—(B)CO32— HCO3— OH— K+(C)Fe3+ Cu2+ NO3- SO42- (D)H+ Cl- Na+ SO32-题型2:在酸性(或碱性)溶液中不能大量共存。
例2、下列各组离子,在强碱性溶液中可以大量共存的是()(A)I- AlO2- Cl- S2- (B)Na+ K+ NH4+ Ba2+(C)Br- S2- Cl- HCO3- (D)SO32- NO3- SO42- HCO3-例3、室温时某溶液的pH为1,该溶液中可能大量共存的离子组是()(A)Zn2+ Cl- Ba2+ NO3-(B)Na+ NO3- K+ CO32-(C)K+ SO42- Na+ AlO2-(D)Cu2+ NO3- Al3+ SO42-题型3:离子间因发生氧化还原反应而不能大量共存。
例4下列离子在溶液中因发生氧化还原反应而不能大量共存的是()(A)H3O+、 NO3-、 Fe2+、 Na+ (B)Ag+、 NO3-、Cl-、 K+(C)K+、Ba2+、OH-、 SO42- (D)Cu2+、NH4+、Br-、OH-题型4:在无色透明的溶液中离子间能够大量共存。
例5、下列各组离子中,在碱性溶液里能大量共存,并且溶液为无色透明的是()(A)K+ MnO4- Cl- SO42- (B)Na+ AlO2- NO3- CO32-(C)Na+ H+ NO3- SO42- (D)Na+ SO42- S2- Cl-题型5:在强酸或强碱性溶液中均不能大量共存。
例6、若溶液中由水电离产生的C(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是()(A) Al3+ Na+ NO3- Cl- (B) K+ Na+ Cl- NO3-(C) K+ Na+ Cl- AlO2- (D) K+ NH4+ SO42- NO3-例7、某无色透明溶液,跟金属铝反应放出H2 ,试判断下列离子:Mg2+、Cu2+、 Ba2+、H+、Ag+、 SO42-、 SO32-、HCO3- 、OH-、NO3-,何者能存在于此溶液中?(1)当生成Al3+时,可能存在__________;(2)当生成AlO2-时,可能存在__________。
离子反应与离子共存习题

1-2 离子反应与离子共存习题(1)班级:_________姓名:_________一、选择题(每小题6分,共60分。
每小题有1~2个正确答案)1.下列反应的离子方程式正确的是A.铁跟稀硝酸反应:Fe+2H+===Fe2++H2↑B.铜跟浓硝酸反应:Cu+2NO-3+H+===Cu2++2NO2↑+2H2OC.碳酸钡跟盐酸反应:BaCO3+2H+===Ba2++CO2↑+H2OD.铜跟氯化铁反应:Cu+Fe3+===Cu2++Fe2+2.下列反应的离子方程式不正确的是A.向FeCl3溶液中滴入KSCN溶液:Fe3++SCN-===[Fe(SCN)]2+B.向明矾溶液中加入过量Ba(OH)2溶液:Al3++4OH-===AlO-2+2H2O C.向Fe2(SO4)3溶液中通入H2S:Fe3++H2S===S↓+Fe2++2H+D.澄清的石灰水中加入盐酸:OH-+H+===H2O3.下列反应的离子方程式不正确的是A.向亚硫酸中滴加溴水:Br2+H2SO3+H2O===SO-24+4H++2Br-B.硫氢化钠溶液与苛性钠溶液混合:HS-+OH-===S2-+H2OC.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-===3Cl-+ClO-+H2O D.硫化钠的水解:S2-+2H2O===H2S↑+2OH-4.下列反应的离子方程式正确的是A.在硫酸铁溶液中加入足量氢氧化钡溶液:Ba2++SO-24===BaSO4↓B.硫化钠水解:S2-+H2O HS-+OH-C.硫酸铜溶液中通入过量的硫化氢:Cu2++S2-===CuS↓D.溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2===2Fe3++6Cl-+2Br2 5.下列离子方程式书写正确的是A.过量氯气通入溴化亚铁溶液:3Cl2+2Fe2++4Br-===6Cl-+2Fe3++2Br2B.过量二氧化碳通入偏铝酸钠溶液中:CO2+2H2O+AlO-2===Al(OH)3↓+HCO-3C.在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合:NH+4+HSO-3+2OH-===SO-23+NH3↑+2H2OD.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO-3+Ca2++2OH-===CaCO3↓+2H2O+MgCO3↓6.下列反应的离子方程式正确的是A.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO B.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2OC.用氨水吸收少量二氧化硫:NH3·H2O+SO2===NH+4+HSO-3D.硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3↓+3NH+4 7.能正确表示下列反应的离子方程式是A.硫化亚铁跟盐酸反应:FeS+2H+===Fe2++H2S↑B.氯气跟水反应:Cl2+H2O===2H++Cl-+ClO-C.钠跟水反应:Na+2H2O===Na++2OH-+H2↑D.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO-2===BaSO4↓48.下列反应的离子方程式正确的是A.含3 mol FeBr2的溶液中通入1 mol Cl2:2Fe2++Cl2===2Fe3++2Cl-B.明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH-===AlO-+2H2O2+8H+===3Cu2++2NO↑+4H2O C.Cu与稀HNO3反应:3Cu+2NO-3D.实验室用CaCO3制取CO2:CO-2+2H+===CO2↑+H2O39.下列反应的离子方程式不正确的是A.mol Cl2通入到溶有1 mol FeBr2的溶液中:Cl2+2Fe2+===2Fe3++2Cl-+Ba2++OH-===BaSO4↓B.NaHSO4溶液中滴入少量的Ba(OH)2溶液:H++SO-24+H2O+CH3COOH===CO2↑+CH3COO-+H2O C.小苏打溶液中加醋酸溶液:HCO-3D.稀硫酸溶液中通入氨气:H++NH3===NH+410.下列反应的离子方程式正确的是A.硫氢化钠溶液与I2反应:HS-+I2===S↓+2I-+H++OH-===CaCO3↓+H2O B.向碳酸氢钙溶液中滴加石灰水:Ca2++HCO-3C.碳酸亚铁与足量稀硝酸反应:FeCO3+2H+===Fe2++CO2↑+H2O===BaSO4↓D.硫酸镁与氢氧化钡溶液反应:Ba2++SO-24二、填空题(20分)11.有甲、乙两相邻的工厂,排放的污水经初步处理后只溶有Ag+、Ba2+、Fe3+、Na+、Cl-、SO-24、NO-3、OH-中的各不相同的四种离子。
离子反应方程式与离子共存问题专题练习[1]
![离子反应方程式与离子共存问题专题练习[1]](https://img.taocdn.com/s3/m/f0cb9a641eb91a37f1115c94.png)
离子反应方程式与离子共存问题专题练习(一)、由于发生复分解反应,离子不能大量共存。
1、有气体产生。
如CO32- 、HCO3- 、S2-、HS- 、SO32-、HSO3- 、等易挥发的弱酸的酸根与H+不能大量共存,主要是由于发生CO32- + 2H+ → CO2↑+H2O 、HS- +H+ →H2S↑等。
2、有沉淀生成。
如Ba2+、Ca2+、Mg2+等不能与SO42-、CO32-等大量共存,主要是由于Ba2+ + CO32- →BaCO3↓、Ca2+ + SO42- →CaSO4↓(微溶);Mg2+ 、Al3+、Cu2+、Fe2+、Fe3+等不能与OH-打大量共存是因为Cu2+ +2OH- →Cu(OH)2↓,Fe3+ + 3 OH- →Fe(OH)3↓等;SiO32- 、AlO2- 、S2O32- 等不能与H+大量共存是因为SiO32- + 2H+ →H2SiO3↓、AlO2- + H+ +H2O →Al(OH)3↓、S2O32- + 2H+ →S↓+SO2↑+H2O3、有弱电解质生成。
如OH-、ClO- 、F-、CH3COO- 、HCOO- 、PO43-、HPO42-、H2PO4-等于不能与H+大量共存是因为OH- +H+ →H2O、CH3COO- +H+ →CH3COOH等;一些酸式弱酸根及NH4+不能与OH- 大量共存是因为HCO3- +OH- →CO32- +H2O 、HPO42- +OH- →PO43- +H2O、NH4+ +OH- →NH3·H2O等。
(二)审题时应注意题中给出的附加条件,如:(1)有色离子:MnO4-、Fe3+、Fe2+、Cu2+,使溶液呈现一定的颜色。
(2)注意题目要求“一定大量共存”、“可能大量共存”还是“不能大量共存”等要求。
(3)注意挖掘题目中的隐含的信息,排除干扰信息,克服非智力因素成分。
离子方程式及离子共存强化练习一、选择题(每小题有一个或两个选项符合题意)1. 在pH=1的无色透明溶液中,不能大量共存的离子组是:A. Al3+ 、Ag+、NO3-、I-B. Mg2+、NH4+、NO3-、Cl-C. NH4+、K+、S2-、Br-D. Zn2+、Na+、NO3-、SO42-2、下列各组离子,在强碱性溶液中可以大量共存的是:A. K+、Na+、HSO3- 、Cl-B. Na+、Ba2+、AlO2- 、NO3-C. NH4+、K+、Cl-、NO3-D. K+ 、Na+、ClO- 、S2-4.(2001全国卷13)下列各族离子,在强碱性溶液中可以大量共存的是A. I- 、AlO2-、Cl-、S2-B. K+、Na+、NH4+、Ba2+C. CO32-、Cl-、S2- 、Br-D. SO32-、HCO3-、NO3-、SO42-5.(2001上海卷12)下列离子在溶液中因发生氧化还原反应而不能大量共存的是A. H30+、NO3-、Fe2+、Na+B. K+、Ag+、NO3-、Cl-C. K+、Ba2+、OH-、SO42-D. Cu2+、NH4+、Br-、OH-6.(2003江苏卷11)若溶液中有水电离产生的c(OH-) = 1×10-14 mol·L-1 ,满足此条件的溶液中一定可以大量共存的离子组是A. Al3+、Na+、NO3-、Cl-B. K+、Na+、Cl- 、NO3-C. K+、Na+、Cl- 、AlO2-D. K+ 、NH4+、SO42- 、NO3-7.(2003江苏卷12)对某酸性溶液(可能含有Br-、SO42- 、H2SO3 、NH4+)分别进行如下实验:①加热释放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;③加入氯水石,溶液略显黄色,再加入BaCl2 溶液时,产生的白色沉淀不溶于稀硝酸,对于下列物质不能确认其在溶液中是否存在的是A. Br-B. SO42-C. H2SO3D. NH4+8.(2003南通市高三一模13)在含有I- 且能使酚酞变红的无色溶液中,可大量存在的离子组是A. Cu2+、Na+、Br-、Cl-B. K+、Na+、NH4+ 、AlO2-C. K+、Na+、NO3- 、H+D. K+ 、S2-、SO42- 、OH-9.(2003南通市高三二模10)某溶液由水电离出的c(H+) = 1×10-12 mol∕L,则此溶液中可能大量存在的离子组是A. HCO3-、NH4+、Mg2+、Cl-B. K+、Na+、Cl- 、NO3-C. K+、Ba2+、I- 、NO3-D. Ba2+ 、Na+、Cl-、SO42-10. 下列各组离子在溶液中不能大量共存,且加入过量NaOH 溶液或过量稀盐酸均能得到澄清溶液的是A. SO42-、Cl-、Fe3+、Na+B. Na+、Cl-、NO3-、CO32-C. Ag+、NO3-、Na+、SO42-D. AlO2-、CO32-、K+、Na+11. 某能使石蕊试液变红的溶液中,能大量存在的离子是A. Al3+、NH4+、SO42-、Cl-B. Mg2+、Na+、HCO3- 、NO3-C. K+、Na+、Cl- 、AlO2-D. K+ 、Fe2+、Cl- 、NO3-12. 在pH=0 的无色透明溶液中,因发生氧化还原反应而不能大量共存的离子组是A. K+、Na+、MnO4- 、Cl-B. Cl-、S2O32-、K+、Na+C. Na+、K+、Cl-、CHCOO-D. K+ 、Na+、I- 、ClO-13. 常温下测得某无色溶液中有水电离出c(H+) = 1×10-13 mol∕L,又知该溶液中还有NO3- 、Na+、Cl- ,那么该溶液中还一定存在的例子是A. AlO2-、ClO-B. Mg2+、SO42-C. Fe2+ 、Cu2+D.Ba2+ 、K+14. 下列离子方程式正确的是A. AlCl3 溶液中加入过量氨水:Al3+ +3NH3··H2O → Al(OH)3↓ + 3NH4+;B. 氢氧化铁与氢碘酸中和:Fe(OH)3 + 3H+→ Fe3+ + 3H2OC.Mg(HCO3)2溶液中加入足量NaOH 溶液:Mg2+ + 2HCO3- →Mg(OH)2↓+ 2CO32-+2H2OD. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液,至完全沉淀:2H+ + SO42- + Ba2+ + 2OH-→BaSO4 ↓ + 2H2O15. (2003上海卷18)下列离子方程式中正确的是A. 过量NaHSO4与Ba(OH)2溶液反应:Ba2+ +2H++ 2OH-+ SO42- →BaSO4 ↓ + 2H2OB. NH4HCO3溶液与过量氢氧化钠溶液反应:NH4+ + OH-→ NH3 ↑ + H2OC. 苯酚钠溶液中通入少量CO2: —O- + CO2+H2O → —OH+ HCO3-D. FeCl2溶液中通入过量Cl2:2Fe2+ + 2Br- + 2Cl2→2Fe3+ + Br2 + 4Cl-16. 下列离子方程式正确的是A. 等物质的量浓度的Ba(OH)2溶液与明矾溶液以体积比3比2混合:3Ba2+ +6OH- +2Al3+ + 3SO42-→ 2Al(OH)3↓ + 3BaSO4↓;B. 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+ 3H+→ Fe2+ + 3H2OC. H218O中投入Na2O2固体:2H218O + 2O22- →4OH- + 18O2↑D. CuCl2 溶液中加入Na2S溶液:Cu2+ + S2- +2H2O →Cu(OH)2↓+H2S ↑17. 下列离子方程式的书写正确的是A. FeS固体与稀硝酸溶液混合:FeS +2H+→ 2Fe2+ +H2S ↑B. NH4HSO4溶液中加入足量Ba(OH)2 溶液:H+ + SO42-+Ba2++OH-→BaSO4↓+ H2OC. Ca(ClO)2溶液中加入足量CO2气体:Ca2++2ClO- +CO2 +H2O→CaCO3↓+2HClOD. 等浓度等体积的Ca(H2PO4)2溶液与NaOH溶液混合:Ca2++ H2PO4- + OH-→CaHPO4 ↓ +H2O18. 下列离子方程式书写正确的是A. 将少量SO2气体通入NaClO溶液中:SO2 +2ClO- +H2O → SO32- +2HClOB. 向KHSO4溶液中加入足量Ba(OH)2 溶液至所得溶液的pH=7:Ba2++2OH- +2H+ +SO42-→BaSO4↓+2H2OC. 向Ca(HCO3)2溶液中滴入过量的NaOH溶液:Ca2++2HCO3- +2OH-→ CaCO3 ↓+CO32- +2H2OD. 112mL(S.T.P)Cl2通入10mL 1mol/L 的FeBr2溶液中:2Fe2+ + 4Br- + 3Cl2→2Fe3+ + 6Cl- + 2Br219. 下列反应的离子方程式中不正确的是A. 向烧碱溶液中滴加少量氯化铝溶液:Al3+ +4OH-→AlO2- + 2H2OB. 物质的量相等的溴化亚铁和氯气反应:2Fe2+ + 2Br- +2Cl2→2Fe3+ + Br2 + 4Cl-C. 硫化钾晶体溶于水:S2- + 2H2O 2OH- + H2SD. 向碳酸钠溶液中滴加过量的稀硫酸:CO32- + 2H+→ CO2↑+ H2O20. 下列反应的离子方程式书写正确的是A. Fe粉与稀硝酸反应:Fe +2H+ (稀) →Fe2++ H2↑B. Cl2与水的反应:H2O + Cl2→2H+ +Cl- + ClO-C. Na与盐酸的反应:2Na +2H+→ 2Na+ + H2↑D. HAc 和KOH 溶液的反应:HAc + OH-→ Ac-+ H2O21. 下列离子方程式正确的是A. FeBr2溶液中加入过量氯水:2Fe2+ +Cl2→ 2Fe3++2Cl-B. 铁粉和FeCl3溶液反应:Fe + Fe3+→ 2Fe2+C. 铁粉和过量的稀硝酸反应:Fe + NO3- + 4H+→ Fe3++NO↑+ 2H2OD. Mg(HCO3)2溶液与过量NaOH反应:Mg2+ + 2HCO3- + 2OH-→MgCO3 ↓+CO32- +2H2O22. 下列离子方程式正确的是A. 先Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2+ + 2OH- + NH4+ + H+ + SO42-→BaSO4↓+ NH3··H2O + H2O电解B. 用Pt电极电解饱和MgCl2 溶液:2Cl- + 2H2O 2OH- +H2↑+Cl2↑C. 向漂白粉溶液中通入SO2:Ca2+ + 2ClO- + SO2 +H2O → CaSO3↓+2HClOD. 向碳酸氢钠溶液中滴加少量氢氧化钡溶液:2HCO3- + Ba2+ + 2OH-→BaCO3↓+2H2O + CO32-23. 下列反应的离子方程式正确的是A. 将H2S 气体通入FeCl3溶液:2Fe3+ + S2-→ 2Fe2++S↓B. 将少量的NaHSO4溶液跟Ba(OH)2溶液混合反应:H++ Ba2+ +SO42- +OH- →BaSO4↓+ H2OC. 将少量的(NH4)2HPO4溶液加入过量的澄清石灰水中:Ca(OH)2 +2NH4+ +HPO42-→ 2NH3↑+ CaHPO4↓+ 2H2OD. 硫化钠溶于水:S2- + 2H2O H2S + 2OH-24. 下列反应的离子方程式书写正确的是A. 鸡蛋壳在醋酸中溶解中有气泡产生:CaCO3 +2H+ →Ca2+ +H2O +CO2↑B. 偏铝酸钠溶液中加入过量盐酸:AlO2- + 4H+→Al3+ +2H2OC. 溴化亚铁溶液中通入少量Cl2:Cl2 +2Fe2+→ 2Fe3+ + 2Cl-↑D. CuSO4 溶液中加入少量Ba(OH)2溶液:Ba2+ +SO42- → BaSO4↓25. (2001上海卷13)下列反应的离子方程式错误的是A. 向碳酸氢钙溶液中加入过量氢氧化钠:Ca2+ + 2HCO3- + 2OH-→CaCO3↓+CO32- + 2H2OB. 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2+ +2OH- +NH4+ +HCO3-→ BaCO3↓+ NH3··H2O + H2OC. 氢氧化铝与足量盐酸反应:Al(OH)3 + 3H+→ Al3+ +3H2OD. 过量CO2通入氢氧化钠溶液中:CO2 + 2OH-→ CO32- + H2O26. (2002全国卷9)下列离子方程式书写正确的是A. 向碳酸氢钙溶液中加入过量氢氧化钠:HCO3- + OH-→ CO32- + H2OB. 氯化铁溶液中通入硫化氢气体:2Fe3+ + S2-→2Fe2++ S↓C. 次氯酸钙溶液中通入过量二氧化碳:Ca2+ + 2ClO- +H2O + CO2→ CaCO3↓+ 2 HClOD. 氯化亚铁溶液中加入硝酸:3Fe2+ + 4H+ +NO3- → 3Fe3+ + 2H2O + NO↑27. (2007上海卷)下列反应的离子方程式正确的是A. 氢氧化钠溶液中通入少量二氧化硫:SO2 + OH-→ HSO3-B. 碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3- + Ba2+ + OH-→ BaCO3↓+H2OC. 盐酸滴入氨水中:OH- + H+ → H2OD. 碳酸钙溶解于稀硝酸中:CO32- + 2H+→ CO2↑ + H2O28. (2003江苏卷13)能正确表示下列反应的离子方程式是A. 用碳酸氢钠溶液吸收少量二氧化硫:2CO32- + SO2+ H2O → 2HCO3- + SO32-B. 金属铝溶液盐酸中:Al + 2H+→ Al3+ +H2↑C. 硫化钠溶于水中:S2- + 2H2O H2S ↑+ 2OH-D. 碳酸镁溶解于硝酸中:CO32- + 2H+→ CO2↑ + H2O29. (2008上海卷)下列离子方程式书写正确的是A. AgNO3溶液中滴入少量Na2S 溶液:2Ag+ + S2-→ Ag2SB. 过量CO2通入Ca(ClO)2溶液中:ClO- +H2O + CO2 →HCO3- + HClOC. Na2CO3溶液中加入过量CH3COOH溶液:CO32- + 2H+→CO2↑ + H2OD. 向Ba(OH)2溶液加入少量NaHSO3溶液:2HSO3- + Ba2+ + 2OH-→ BaSO3↓+ SO32- + 2H2O30. (2009上海卷)下列离子方程式正确的是A. H2SO4与Ba(OH)2溶液反应:Ba2+ + OH- +H+ SO42-→BaSO4↓ + H2OB. CuSO4溶液吸收H2S 气体:Cu + H2S → CuS↓ +2H+C. AlCl3溶液加入过量的浓氨水:Al3+ + 4 NH3··H2O →AlO2- + 4NH4+ + 2H2OD. 等体积等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2+ + 2OH- + NH4+ HCO3-→ BaCO3↓ + NH3··H2O + H2O二、填空简答31. 按要求写出下列离子方程式:将NH4Cl加入到重水中。
离子反应-高考题汇总

高考题汇总--离子反应一.离子共存1.下列离子在溶液中因发生氧化还原反应而不能大量共存的是()A. H3O+、NO-3、Fe2+、Na+ B. Ag+、NO-3、Cl-、K+C. K+、Ba2+、OH-、SO-24D. Cu2+、NH+4、Br-、OH-2.在pH=1的无色溶液中能大量共存的离子组是()A.NH4+、Mg2+、SO42-、Cl-B.Ba2+、K+、OH-、NO3-C.Al3+、Cu2+、SO42-、Cl-D.Na+、Ca2+、Cl-、AlO2-3.下列各组离子在溶液中能大量共存的是()A.酸性溶液Na+、K+、MnO4-、Br-B.酸性溶液Fe3+、NH4+、SCN-、NO3-C.碱性溶液Na+、K+、AlO2-、SO42-D.碱性溶液Ba2+、Na+、CO32-、Cl-4.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的是离子组是()A.K+、Na+、HCO3-、NO3-B.Na+、SO42-、Cl-、ClO-C.H+、Mg2+、SO42-、NO3-D.Ag+、K+、NO3-、Na+5.下列各组离子一定能大量共存的是()A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-B.在强碱溶液中:Na+、K+、AlO2-、CO32-C.在c(H+)=10-13mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3-D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3-6.在pH=1的溶液中,可以大量共存的离子是()A.K+Na+SO42—S2O32—B.NH4+Mg2+SO42—Cl—C.Na+K+HCO3—Cl—D.K+Na+AlO2—NO3—7.已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是()A.A13+、CH3COO-、C1-B.Na+、NH4+、C1-C.Mg2+、C1-、Fe2+ D.Mg2+、Ba2+、Br-8.室温下,在强酸性和强碱性溶液中都不能..大量共存的离子组是()A.NH4+、Cu2+、Cl-、NO3-B.K+、Na+、SO32-、S2-C.K+、Na+、AlO2-、SO42-D.Ba2+、Fe2+、NO3-、Br-9.一定能在下列溶液中大量共存的离子组是()A.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-B.c(H+)=1×10—13mol·L—1的溶液:Na+、Ca2+、SO42-、CO32-C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-D.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-10.在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是( )① K+、Cl-、NO3-、S2-② K+、Fe2+、I-、SO42-③ Na+、Cl-、NO3-、SO42-④Na+、Ca2+、Cl-、HCO3-⑤ K+、Ba2+、Cl-、NO3-A.①③B.③⑤C.③④D.②⑤11.在pH=1时,可大量共存且形成无色溶液的一组离子或分子是()A.Ca2+、CH3COOH、Br-、Na+B.NO3-、Fe3+、Mg2+、SO42-C.ClO-、Ba2+、Na+、Cl-D.K+、Cl-、Al3+、SO32-12.向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是()A.K+、Br-、CO32-B.Al3+、H+、MnO4-C.NH4+、Fe3+、SO42-D.Ag+、Cu2+、NO3-13.在溶液中加入足量Na2O2后仍能大量共存的离子组是()A.NH4+、Ba2+、Cl—、NO3—B.K+、AlO2-、Cl-、SO42—C.Ca2+、Mg2+、NO3—、HCO3—D.Na+、Cl-、CO32—、SO32—14.在下列溶液中,各组离子一定能够大量共存的是()A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+B .使紫色石蕊试液变红的溶液:Fe 2+、Mg 2+、NO 3-、Cl -C . c (H +)=10-12 mol·L -1的溶液:K +、Ba 2+、Cl -、Br -D .碳酸氢钠溶液:K +、SO 42-、Cl -、H +15.将足量CO 2通入下列各溶液中,所含离子还能大量共存的是( )A .K +、SiO 32-、Cl -、NO 3-B .H +、NH 4+、Al 3+、SO 42-C .Na +、S 2- 、OH -、SO 42-D .Na +、C 6H 5O -、CH 3COO -、HCO 3-16.下列各组离子在指定溶液中能大量共存的是( )A .饱和氯水中Cl -、NO -3、Na +、SO -23、B .c(H +)=1.0×10-13mol ·L 溶液中C 6H 5O -、K +、SO 42-、Br - C .Na 2S 溶液中 SO 42-、K +、Cl -、Cu 2+D .pH=12的溶液中NO -3、I -、Na +、Al 3+17. 能在水溶液中大量共存的一组离子是( )A. H +、I -、NO 3-、SiO 32-B. Ag +、Fe 3+、Cl -、SO 42-C.K +、SO 42-、Cu 2+、NO 3-D.NH 4+、OH -、Cl -、HCO 3-18.常温下,下列各组离子在制定溶液中一定能大量共存的是( )A.1.0mol ▪L -1的KNO 3溶液:H +、Fe 2+、Cl -、SO 42-B.甲基橙呈红色的溶液:NH 4+、Ba 2+、AlO 2-、Cl -C.pH=12的溶液:K +、Na +、CH 3COO -、Br -D.与铝反应产生大量氢气的溶液:Na +、K +、CO 32-、NO 3-19.在pH =1的溶液中,能大量共存的一组离子或分子是( )A .Mg 2+、Na +、ClO -、NO 3-B .Al 3+、NH 4+、Br -、Cl -C .K +、Cr 2O 27-、CH 3CHO 、SO 24-D .Na +、K +、SiO 23-、Cl -20. 下列离子组一定能大量共存的是( )A .甲基橙呈黄色的溶液中:I -、Cl -、NO 3-、Na +B .石蕊呈蓝色的溶液中:Na +、AlO 2-、NO 3-、HCO 3-C .含大量Al 3+的溶液中:K +、Na +、NO 3-、ClO -D .含大量OH -的溶液中:CO 32-、Cl -、F -、K +21.能在溶液中大量共存的一组离子是( )A . NH 4+ 、Ag + 、PO 43-、Cl - B.Fe 3+、H +、I -、 HCO 3- C. K +、 Na +、 NO 3- 、 MnO 4- D.Al 3+ 、Mg 2+、SO 42- 、CO 32- 22. 在溶液中能大量共存的一组离子或分子是( )A. NH 4+ 、H +、NO 3-、HCO 3-B.K + 、Al 3+、SO 42- 、NH 3·H 2OC.Na +、K +、SO 32-、Cl 2D.Na + 、CH 3COO -、CO 32-、OH - 23.下列各组离子,在溶液中能大量共存、加入NaOH 溶液后加热既有气体放出又有沉淀生成的一组是( )A.Ba 2+ 、NO 3-、NH 4+、Cl -B. Ca 2+、HCO 3-、 NH 4+、AlO 2-C. K +、Ba 2+、Cl -、HSO 3-D. Mg 2+ 、NH 4+、SO 42-、K + 24.下列各组离子,能在溶液中大量共存的是( )A .Na +、Mg 2+ 、AlO 2-、Al 3+B . H +、Fe 2+、SO 42-、NO 3-C .K +、NH 4+、CO 32-、OH -D .Ca 2+、Al 3+ 、NO 3-、Cl -25.在下列给定条件的溶液中,一定能大量共存的离子组是( ) A.无色溶液:Ca 2+、H +、Cl -、HSO 3-B.能使pH 试纸呈红色的溶液:Na +、NH +4、I -、NO 3-C.FeCl 2溶液:K +、Na +、SO 42-、AlO 2-D.Kw/c(H +)=0.1 mol/L 的溶液:Na +、K +、SiO 32-、NO 3-26.在下列各溶液中,离子一定能大量共存的是( ) A.强碱性溶液中:K +、、Al 3+、Cl -、SO 42-B.含有0.1 mol ·L -1 Fe 3+的溶液中:K +、Mg 2+、I -、NO -3C.含有0.1 mol ·L -1Ca 2+的溶液中:Na +、K +、CO 32-、Cl -D.室温下,PH=1的溶液中:Na +、Fe 3+、NO -3、SO 42-27.在溶液中加入过量Na 2O 2后仍能大量共存的离子组是( ) A.NH 4+、Ba 2+、Cl -、NO 3- B.K +、AlO 2-、Cl -、SO 42- C.Ca 2+、Mg 2+、NO 3-、HCO 3- D.Na +、Cl -、CO 32-、SO 32- 28.下列各组离子在给定条件下能大量共存的是( ) A.在pH=1的溶液中:NH 4+、K +、ClO -、Cl -B .有SO 42-存在的溶液中:Na + 、Mg 2+、Ca 2+、I -C .有NO 3-存在的强酸性溶液中:NH 4+、Ba 2+、Fe 2+、Br -D.在c(H +)=1.0×10-13mol ·L -1的溶液中:Na +、S 2-、AlO 2-、SO 32-29.下列各组离子一定能大量共存的是( )A .在含有大量AlO 2-的溶液中:NH 4+、Na +、Cl -、H +B .在强碱溶液中:Na +、K +、CO 32-、NO 3-C .在pH =12的溶液中:NH 4+、Na +、SO 42-、Cl -D .在c(H +)=0.1mol ·L -1的溶液中:K +、I -、Cl -、NO 3- 30.在下列溶液中,各组离子一定能够大量共存的是( ) A .使酚酞试液变红的溶液: Na +、Cl -、SO 42-、Fe 3+ B .使紫色石蕊试液变红的溶液:Fe 2+、Mg 2+、NO 3-、Cl - C .c(H +)=10-12 mol ·L -1的溶液:K +、Ba 2+、Cl -、Br - D .碳酸氢钠溶液:K +、SO 42-、Cl -、H +二、离子方程式的正误判断1、下列离子方程式正确的是( )A .碳酸氢钠溶液与少量石灰水反应 HCO -3+ Ca 2+ + OH — = CaCO 3↓ + H 2OB .氯化铵与氢氧化钠两种浓溶液混合加热OH — + NH +4 △ H 2O + NH 3↑ C .氢氧化镁与稀硫酸反应 H + + OH — = H 2OD .单质铜与稀硝酸反应 Cu + 2H ++ 2NO -3 = Cu 2+ + 2NO↑+H 2O2、列反应的离子方程式错误的是( ) A .铁跟稀硫酸反应Fe+2H +=Fe 2++H 2↑B .铜跟浓硝酸反应Cu+2N03-+4H +=Cu 2++2N02↑+2H 2OC .碳酸钙跟稀盐酸反应CO 32-+2H +=CO 2↑+H 2OD .铁跟氯化铁溶液反应Fe+2Fe 3+=3Fe 2+ 3、下列反应的离子方程式书写正确的是( )A. 氯化铝溶液中加入过量氨水:Al 3+ + 4NH 3•H 2O AlO 2- + 4NH 4+ + 2H 2OB. 澄清石灰水与少量苏打溶液混合:Ca 2+ + OH -+HCO 3 CaCO 3↓ + H 2OC. 碳酸钙溶于醋酸CaCO 3 + 2H + Ca 2++ CO 2↑ + H 2OD. 氯化亚铁溶液中通入氯气:2Fe 2+ + Cl 2 2Fe 3++ 2Cl - 4、下列反应的离子方程式正确的是( )A.向沸水中滴加FeCl 3溶液制备Fe(OH)3胶体:Fe 3++3H 2O _____3↓+3H +B.用小苏打治疗胃酸过多:HCO 3-+H +===CO 2↑+H 2OC.实验室用浓盐酸与MnO 2反应制Cl 2:MnO 2+2H ++2Cl -_____Cl 2↑+Mn 2++H 2OD.用FeCl 3溶液腐蚀印刷电路板:Fe 3++Cu===Fe 2++Cu 2+ 5.下列化学反应的离子方程式正确的是( )A.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2OB.往碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑+H2OC.往氨水中滴加氯化铝溶液:Al3++4OH-=AlO2-+2H2OD.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O 6.能正确表示下列反应的离子方程式是( )A.碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-= CO32-+H2OB.醋酸钠溶液和盐酸混合:CH3COONa+H+= CH3COOH+Na+C.少量金属钠放入冷水中:Na+2H2O = Na++2OH-+H2↑D.硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-= Cu(OH)2↓+BaSO4↓7.能正确表示下列反应的离子方程式是( )A .醋酸钠的水解反应CH3COO-+H3O+= CH3COOH+H2OB. 碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-= CaCO3↓+2H2O+CO32-C.苯酚钠溶液与二氧化碳反应C6H5O-+CO2+H2O = C6H5OH+CO32-D .稀硝酸与过量的铁屑反应3Fe+8H++2NO3-= 3Fe3++2NO↑+4H2O8.下列反应的离子方程式正确的是( )A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-= HSO3-B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-= BaCO3↓+H2OC.盐酸滴入氨水中:H++OH-= H2OD.碳酸钙溶解于稀硝酸中:CO32-+2H+= CO2↑+H2O9.下列反应的离子方程式正确的是( )A.锌片插入硝酸银溶液中:Zn+Ag+= Zn2++AgB.碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH = Ca2++2CH3COO-+2CO2↑+2H2OC.少量金属钠加到冷水中:Na+2H2O = Na++OH-+H2↑D.氢氧化铜加到盐酸中:Cu(OH)2+2H+= Cu2++2H2O10.下列文字表述与反应方程式对应且正确的是()A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑C.利用腐蚀法制作印刷线路板:Fe3+ + Cu == Fe2+ + Cu2+D.实验室用液溴和苯在催化剂作用下制溴苯:11.下列反应的离子方程式正确的是()A.钠与水的反应:Na+H2O=Na++OH-+H2↑B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-C.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2OD.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+12.下列离方程式书写正确的是()A.石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3B.NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-NH3•+SO32-+2H2OC.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH-D.AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH∙+NH4+13.能正确表示下列反应的离子方程式是( )A.足量的硫酸铝与纯碱反应:2Al3++3CO32-+3H2O===2Al(OH)3↓+3CO2↑B.硫酸铜与烧碱反应:CuSO4+2OH-===Cu(OH)2↓+SO42-C.苯酚与碳酸钠反应:2C6H5OH+CO32-===2C6H5O-+CO2↑+H2OD.碳酸钡与硫酸反应:Ba2++SO42-===BaSO4↓14.下列表示对应化学反应的离子方程式正确的是( ) A.用KIO 3氧化酸性溶液中的KI :5I -+IO 3-+3H 2O =3I 2+6OH - B.向NH 4HCO 3溶液中加过量NaOH 溶液并加热:NH 4++6OH -NH 3↑+H 2OC.将过量二氧化硫气体入冷氨水中:SO 2+NH 3·H 2O =HSO 3-+NH 4+D.用稀硝酸洗涤试管内壁的银镜:Ag +2H ++3NO 3-=Ag ++NO ↑+H 2O15.向10mL 0.1mol ·1-L 244)(SO Al NH 溶液中,滴加等浓度2)(OH Ba 溶液x mL ,下列叙述正确的是( )A.x=10时,溶液中有+4NH 、+3Al 、-24SO ,且)()(34++>Al c NH c B.x=10时,溶液中有+4NH 、-2AlO 、-24SO ,且)()(244-+>SO c NH c C.x=30时,溶液中有+2Ba 、-2AlO 、-OH ,且)()(2--<AlO c OH cD.x=30时,溶液中有+2Ba 、+3Al 、-OH ,且)()(2+-=Ba c OH c16.下列离子方程式正确的是( )A .钠与水反应:Na+2H 2O=Na ++2OH -+H 2↑B .硅酸钠溶液与醋酸溶液混合:SiO 32-+2H +=H 2SiO 3↓C .0.01mol ·L -1NH 4Al(SO 4)2溶液与0.02mol ·L -1Ba(OH)2溶液等体积混合:NH 4++Al 3++2SO 42-+2Ba 2++4OH -=2BaSO 4↓+Al(OH)3↓+NH 3·H 2OD .浓硝酸中加入过量铁粉并加热:Fe+3NO 3-+6H+错误!未找到引用源。
高考真题化学分项详解专题九 离子反应与离子共存 (含参考答案与解析)
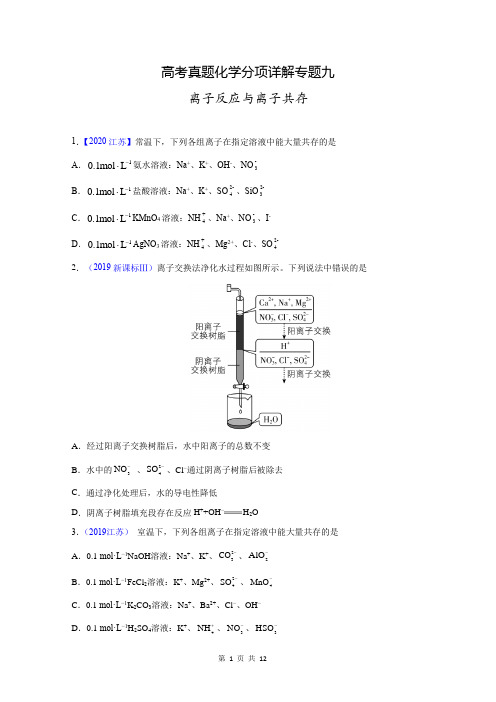
高考真题化学分项详解专题九离子反应与离子共存1.【2020江苏】常温下,下列各组离子在指定溶液中能大量共存的是A .10.1mol L -⋅氨水溶液:Na +、K +、OH -、NO -3B .10.1mol L -⋅盐酸溶液:Na +、K +、SO 2-4、SiO 2-3C .10.1mol L -⋅KMnO 4溶液:NH +4、Na +、NO -3、I -D .10.1mol L -⋅AgNO 3溶液:NH +4、Mg 2+、Cl -、SO 2-42.(2019新课标Ⅲ)离子交换法净化水过程如图所示。
下列说法中错误的是A .经过阳离子交换树脂后,水中阳离子的总数不变B .水中的3NO - 、24SO -、Cl −通过阴离子树脂后被除去C .通过净化处理后,水的导电性降低D .阴离子树脂填充段存在反应H ++OH −H 2O 3.(2019江苏) 室温下,下列各组离子在指定溶液中能大量共存的是A .0.1 mol·L −1NaOH 溶液:Na +、K +、23CO -、2AlO -B .0.1 mol·L −1FeCl 2溶液:K +、Mg 2+、24SO -、4MnO -C .0.1 mol·L −1K 2CO 3溶液:Na +、Ba 2+、Cl −、OH −D .0.1 mol·L −1H 2SO 4溶液:K +、4NH +、3NO -、3HSO -4.(2018江苏)室温下,下列各组离子在指定溶液中能大量共存的是A .0.1 mol·L −1 KI 溶液:Na +、K +、ClO − 、OH −B .0.1 mol·L −1 Fe 2(SO 4)3溶液:Cu 2+、NH 4+ 、NO 3−、SO 42−C .0.1 mol·L −1 HCl 溶液:Ba 2+、K +、CH 3COO −、NO 3−D .0.1 mol·L −1 NaOH 溶液:Mg 2+、Na +、SO 42−、HCO 3−5.(2017江苏)常温下,下列各组离子在指定溶液中能大量共存的是A .无色透明的溶液中:Fe 3+、Mg 2+、SCN –、Cl –B .()()–H OH c c +=1×10 −12的溶液中:K +、Na +、23CO -、3NO -C .c (Fe 2+) =1 mol·L −1的溶液中:K +、+4NH 、4MnO -、24SO -D .能使甲基橙变红的溶液中:Na +、+4NH 、24SO -、3HCO -6.(2017·11月浙江选考)取某固体样品,进行如下实验①取一定量的样品,加足量水充分溶解,过滤得到滤液和滤渣;②取少量滤液,加入BaCl 2溶液,有白色沉淀产生;③取少量滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.某无色溶液中只含有下列8种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HC、OH-、N,已知该溶液能与铝反应放出氢气。
试回答下列问题:(1)若反应后生成Al3+,则溶液中可能存在的离子有,一定存在的离子有,一定不存在的离子有,反应的离子方程式为。
(2)若反应后生成Al,则溶液中可能存在的离子有,一定存在的离子有,一定不存在的离子有,反应的离子方程式为。
【答案】(1)Mg2+、Na+H+、Cl-Ag+、HC、N、OH-2Al+6H+====2Al3++3H2↑(2)N、Cl-OH-、Na+H+、Mg2+、Ag+、HC2Al+2OH-+2H2O====2Al+3H2↑【解析】(1)若反应后生成Al3+,则说明该溶液显酸性,则HC、OH-不存在,若有HNO3则不能生成H2,所以也不存在N,则酸只能为HCl,故也不存在Ag+;一定存在H+、Cl-,Mg2+、Na+可能存在。
(2)反应后生成Al,说明溶液呈碱性,则H+、Mg2+、Ag+、HC一定不存在,一定存在OH-、Na+,N、Cl-可能存在。
【考点】铝及铝合金2.水溶液中能大量共存的一组离子是A.Na+、Ca2+、Cl-、SO42-B.Fe2+、H+、SO32-、ClO-C.Mg2+、NH4+、Cl-、SO42-D.K+、Fe3+、NO3-、SCN-【答案】C【解析】A、水溶液中发生反应:Ca2++SO42- CaSO4↓,不能大量共存,错误;B、酸性条件下ClO-与Fe2+、SO32-发生氧化还原反应,不能大量共存,错误;C、水溶液中,组内离子间不反应,能大量共存,正确;D、水溶液中发生络合反应:Fe3++3SCN- Fe(SCN)3,不能大量共存,错误。
【考点】考查离子共存问题。
3.下列各组离子中,在强碱性溶液中能大量共存是A.Na+、HCO3-、CO32-、K+B.K+、Ba2+、Cl-、NO3-C.Na+、NO3-、K+、S2-D.K+、NH4+、SO42-、Cl-【答案】BC【解析】审题“强碱性溶液”说明溶液中有大量的OH-,所以,A. HCO3-与OH-不能共存,错误;B.可以共存,正确;C.可以共存,正确;D. OH-与NH4+不能共存,错误。
高三二轮复习 专题03 离子反应方程式和离子共存(练)解析版

专题03 离子反应方程式和离子共存1.(2021·四川省成都市第一次诊断)对下列实验,一定能正确描述其反应过程的离子方程式是( ) A .向稀硝酸中加入过量铁粉:Fe +4H ++ NO -3 =Fe 3++NO↑+2H 2OB .向饱和Na 2CO 3溶液中滴入几滴稀AlCl 3溶液:2A13++3CO 2-3+3H 2O=2Al(OH)3↓+3CO 2↑C .乙酸乙酯与稀NaOH 溶液共热:CH 3COOC 2H 5+OH -→ CH 3COO -+C 2H 5OHD .向长期露置于空气的酸性KI 溶液先后滴入几滴FeCl 3溶液和淀粉溶液,立即出现蓝色2Fe 3++2I -=2Fe 2++I 2【答案】C【解析】铁粉过量生成Fe 2+,离子方程式为+-2+323Fe +8H + 2NO =3Fe +2NO +4H O ↑,故A 错误;AlCl 3少量2-3CO 过量,只发生第一步水解生成-3HCO ,离子方程式为()3+2--3233A1+3CO +3H O=Al OH +3HCO ↓,故B 错误;乙酸乙酯在碱性条件下水解生成CH 3COO -和C 2H 5OH ,故C 正确;长期露置于空气的KI 被氧气氧化,生成I 2,遇到淀粉立即出现变蓝,离子方程式为+-222O +4I =+4H +I 2H 2O ,故D 错误;故选C 。
2.(2021·云南省红河州统一检测)常温下,下列各组离子在有关限定条件下一定能大量共存的是( ) A .酸性溶液中:K +、Na +、Fe 2+、NO 3-、Cl -B .中性溶液中:K +、Fe 3+ 、Cl -、CO 23-、HCO 3-C .常温下,C(H +)/C(OH -)=1×10-12的溶液:K +、AlO 2-、CO 23-、Na +、Cl -D .pH =13的溶液中:AlO 2-、Cl -、HCO 3-、SO 24-【答案】C【解析】酸性溶液中:H +、Fe 2+、NO 3-能发生氧化还原反应,不能大量共存,A 与题意不符;中性溶液中:Fe 3+和CO 23-或HCO 3-发生双水解反应,不能大量共存,B 与题意不符;常温下,C(H +)/C(OH -)=1×10-12的溶液呈碱性,K +、AlO 2-、CO 23-、Na +、Cl -、OH -之间不反应,能大量共存,C 符合题意;pH =13的溶液呈碱性, HCO 3-、OH -反应生成碳酸根离子和水,不能大量共存,D 与题意不符;答案为C 。
离子方程式正误判断及离子共存问题专题训练

离子方程式的书写及离子共存问题班级姓名一、离子方程式的书写练习1.向复盐明矾溶液中滴加Ba(OH)2溶液,使SO42-恰好完全沉淀,反应的离子方程式正确的是( )A、Ba2+ + SO42- = BaSO4↓B、2Al3+ + 3SO42- + 3Ba2+ + 6OH- = 3BaSO4↓+ 2Al(OH)3↓C、Al3+ + 2SO42- +2Ba2+ + 3OH- = 2BaSO4↓+ Al(OH)3↓D、Al3+ + 2SO42- +2Ba2+ +4OH- = 2BaSO4↓+ AlO2- + 2H2O2.下列离子方程式中不正确的是( )A、等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合:2HCO3- + Ba2+ + 2OH- = BaCO3↓+ CO32- + 2H2OB、氯气通入氯化亚铁溶液中:2Fe2+ + Cl2 = 2Fe3+ + 2Cl-C、石灰水中通入过量的氟化氢:Ca2+ + 2OH- + 2HF = CaF2↓+ 2H2O电解D、电解饱和氯化镁溶液:2Cl- + 2H2O 2OH- + H2↑+ Cl2↑3.下列离子方程式中正确的是( )A、溴化亚铁溶液中通入过量氯气:3Cl2 + 2Fe2+ + 4Br- = 6Cl- + 2Fe3+ + 2Br2B、过量CO2通入偏铝酸钠溶液中:CO2 + 2H2O + AlO2- = Al(OH)3↓+ HCO3-C、在溶液中亚硫酸氢铵与等物质的量的氢氧化钠混合:NH4+ + HSO3- +2OH- = SO32- + NH3↑+2H2OD、碳酸氢镁溶液中加入过量石灰水:Mg2+ +2HCO3- +Ca2+ +2OH- =CaCO3↓+2H2O +MgCO3↓4.下列离子方程式中,正确的是( )A、在氯化铝溶液中加入过量氨水Al3++3OH- =Al(OH)3↓B、在硫酸铜溶液中加入过量氢氧化钡溶液Ba2++SO42- = BaSO4↓C、在澄清石灰水中通入过量二氧化碳OH- +CO2=HCO3-D、在碳酸氢钙溶液中加入过量氢氧化钠溶液Ca2++HCO3- +OH- =CaCO3↓+H2O5.下列反应的离子方程式错误的是( )A、氯化铝溶液中加入过量的氨水Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2OB、用氨水吸收过量的二氧化硫NH3·H2O + SO2 = NH4+ + HSO3-C、碳酸钠溶液中加入过量的苯酚C6H5-OH + CO32- = C6H5O- + HCO3-D、次氯酸钙溶液中通入过量的二氧化碳ClO- + CO2 + H2O = HCO3- + HClO6.下列反应的离子方程式错误的是( )A、向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2OC、氢氧化铝与足量盐酸反应:Al(OH)3+3H+= Al3++3H2OD、过量CO2通入氢氧化钠溶液中:CO2+2OH-= CO32-+H2O7.下列离子方程式书写正确的是( )A、FeBr2溶液中通入少量Cl2:Fe2+ + Cl2 = Fe3+ + 2Cl-B、澄清石灰水与少量小苏打溶液混合:Ca2+ +OH- +HCO3- = CaCO3↓+ H2OC、FeS固体放入稀硝酸溶液中:FeS + 2H+ = Fe2+ + H2S↑D、饱和石灰水中加入饱和碳酸氢钙溶液:Ca2+ + OH- + HCO3- = CaCO3↓+ H2O8.下列离子方程式中正确的是()(A)碳酸氢钙溶液中加入过量的氢氧化钠溶液: HCO3- + OH-═CO32-+ H2O(B)氯化铁溶液中通入硫化氢气体: 2Fe3+ + S2-═ 2Fe2++ S↓(C)次氯酸钙溶液中通入过量二氧化碳: Ca2+ + 2ClO- + H2O + CO2 ═ CaCO3↓+ 2HClO (D)氯化亚铁溶液中加入硝酸: 3Fe2+ + 4H+ + NO3-═ 3Fe3+ + 2H2O + NO9.下列离子方程式中正确的是()(A)氨气通入醋酸溶液中CH3COOH+NH3=CH3COONH4(B)澄清的石灰水跟盐酸反应 H++OH-=H2O(C)碳酸钡溶于醋酸 BaCO3+2H+=Ba2++H2O+CO2↑(D)金属钠跟水反应2Na+2H2O=2Na++2OH-+H2↑10.下列离子方程式中正确的是()A、向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全Ba2+ + 2OH- + NH4+ +H+ + SO42- = BaSO4↓+ NH3·H2O + H2OB、碳酸氢钠的水解:HCO3- + H2O = H3+O + CO32-C、硫酸铝加过量氨水:Al3+ + 4OH- = AlO2- + 2H2OD、漂白粉溶液中通入少量的SO2:Ca2+ + 2ClO- + SO2 + H2O = CaSO3↓+ 2HClO11.下列反应的离子程式正确的是( )A、硫酸亚铁酸性溶液中加入过氧化氢:4Fe2+ + 2H2O2 + 4H+ = 4Fe3+ + 4H2OB、氯化铝溶液通入过量氨气:Al3+ + 4OH- = AlO2- + 2H2OC、大理石溶于醋酸:CaCO3 + 2CH3COOH = Ca2+ + 2CH3COO- + H2O + CO2↑D、次氯酸钙溶液中通入过量CO2:Ca2+ + 2ClO- + H2O + CO2 = CaCO3↓+ 2HClO12.下列反应的离子反应方程式正确的是( )A、二氧化碳通入少量漂白粉溶液中:CO2 + ClO- + H2O = HClO + HCO3-B、氯气通入冷的氢氧化钠溶液中:2Cl2 + 2OH- = 3Cl- + ClO- + H2OC、硫酸亚铁溶液中加入过氧化氢溶液:Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2OD、硫代硫酸钠溶液中滴入稀盐酸:S2O32- + 2H+ = S↓+ SO2↑+ H2O13.下列离子方程式正确的是( )A、在氢氧化钡溶液中加入过量小苏打:Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2OB、在氢氧化钾的稀溶液中通入过量SO2:SO2 + OH- = HSO3-C、氯化铁水解:Fe3+ +3H2O = Fe(OH)3↓+ 3H+D、氯气通入水中:Cl2 + H2O = 2H+ + Cl- + ClO-14.下列离子方程式中正确的是( )A、氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+ = Fe2+ + 2H2O电解B、用惰性电极电解饱和食盐水:2Cl- + 2H2O 2OH- + H2↑+ Cl2↑C、湿润的醋酸铅试纸检验H2S气体的存在:Pb2+ + H2S = PbS↓+ 2H+D、在苯酚钠溶液中通入过量的CO2气体:2C6H5O- + CO2 + H2O →2C6H5OH↓+ CO32-15下列物质间反应的离子方程式正确的是()A.向苯酚溶液中加入碳酸氢钠溶液B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba2++2OH-+NH4+ +H++SO42-=BaSO4↓+NH3·H2O+H2OC .向沸水中没加饱和氯化铁溶液Fe 3++3H 2OFe(OH)3↓+3H + D .过量的NaOH 溶液与碳酸氢钙溶液Ca 2++2HCO 3-+2OH -=CaCO 3↓+2H 2O+CO 3-16.下列离子方程式正确的是( )A .醋酸铵和盐酸反应CH 3COONH 4+H + CH 3COOH+NH 4+B .氢氧化钡与碳酸氢镁反应Ba 2++OH -+HCO - BaCO 3↓+H 2OC .偏铝酸钠和过量盐酸AlO 2-+4H + Al 3++2H 2OD .钠跟水反应Na+2H 2O Na ++2OH -+H 2↑ 17.下列离子方程式不正确的是 ( ).A.碳酸氢钙溶液中加入等物质的量溶质的NaOH 溶液:Ca 2++HCO 3-+OH -= CaCO 3↓+H 2OB.2SO 通入溴水中:--+++++24222SO 2Br 4H O2H Br SO C .Cu 片插入3AgNO 溶液中:Ag Cu Ag Cu ++++D .FeO 与稀3HNO 反应:O H Fe 2H FeO 22++++18.下列各组在溶液中的反应,不管反应物量的多少,都只能用同一个离程式来表示的是A.FeBr 2与Cl 2B.Ba(OH)2与H 2SO 4 ( )C.HCl 与Na 2CO 3D.Ca(HCO 3)2与NaOH19.下列离子方程式书写正确的是A.过量二氧化硫气通入到漂白粉溶液中Ca 2++2ClO -+SO 2+H 2O == CaSO 3↓+2HClOB.Ba(OH)2溶液中滴入几滴硫酸铜溶液 Cu 2++2HO - == Cu(OH)2↓C.用湿润的醋酸铅试纸检验硫化氢 P b 2++H 2S == PbS ↓+2H +D.碳酸镁溶液中加入过量的澄清石灰水Mg 2++2HCO 3-+2Ca 2++4OH - == Mg(OH)2↓+2CaCO 3↓+2H 2O20. 下列反应的离子方程式正确的是A.氟气通入水中:2F 2+2H 2O == 4F -+4H ++O 2B.向小苏打溶液中加入过量的石灰水:Ca 2++2OH -+2HCO 3- == CaCO 3↓+CO 32-+2H 2OC.硫氢化钠溶液与盐酸反应:S 2-+2H +==H 2S ↑D.FeBr 2溶液与等摩Cl 2反应:2Fe 2++2Br -+2Cl 2== 2Fe 3++4Cl -+Br 221.下列反应的离子方程式正确的是 ( )A.氨气通入醋酸溶液 CH 3COOH+NH 3 == CH 3COONH 4B.澄清的石灰水跟盐酸反应 H ++OH - == H 2OC.碳酸钡溶于醋酸 BaCO 3+2H + == Ba 2++H 2O+CO 2↑D.金属钠跟水反应 2Na+2H 2O == 2Na ++2OH -+H 2↑22. 下列离子方程式正确的是 ( )A 、银氨溶液中加入足量盐酸产生沉淀[Ag(NH 3)2]++OH -+3H ++Cl -=AgCl ↓+2NH 4++H 2OB 、在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解3BaSO 3+2H ++2NO 3-=3BaSO 4↓+2NO ↑+H 2OC 、孔雀石可溶于盐酸 CO 32-+2H +=CO 2↑+H 2OD 、氧化铁可溶于氢碘酸 Fe 2O 3+6H +=2Fe 3++3H 2O二、离子共存问题的练习1.室温下,已知某溶液中由水电离生成的H +和OH -的物质的量浓度的乘积为10-24,则在该溶液中,一定不能大量存在的离子是 ( )A 、S 2O 32-B 、NH 4+C 、NO 3-D 、HCO 3-2.下列各组离子在水溶液中能大量共存的是 () A 、H + 、Fe 2+ 、NO 3- 、Cl - B 、S - 、Na + 、OH - 、K +C 、K + 、CO 32-、Br - 、AlO 2-D 、H + 、Cl - 、Na + 、S 2O 32-3.下列各组离子在溶液中能大量共存的是 () A 、Ca 2+ 、HCO 3-、Cl -、K + B 、Al 3+、AlO 2-、HCO 3-、Na +C 、Fe 2+、NH 4+、SO 42-、S 2-D 、Fe 3+、SCN -、Na +、CO 32-4.下列离子在溶液中因发生氧化还原反应而不能大量共存的是 () A 、H 3O +、NO 3-、Fe 2+、Na + B 、Fe 3+、NO -3、I -、K +C 、K +、Ba 2+、OH -、SO 42-D 、Cu 2+、NH 4+、Br -、OH -5.在pH=1的无色溶液中能大量共存的离子组是 () A 、NH 4+、Mg 2+、SO 42-、Cl - B 、Ba 2+、K +、S 2O 32-、NO 3-C 、Al 3+、Fe 2+、SO 42-、Cl -D 、Na +、Ca 2+、Cl -、AlO 2-6.下列各组离子,在强碱性溶液中可以大量共存的是 () A 、I -、AlO 2-、Cl -、S 2- B 、Na +、K +、NH 4+、Ba 2+C 、Br -、S 2-、Cl -、CO 32-D 、SO 32-、NO 3-、SO 42-、HCO 3-7.某溶液滴入酚酞显红色,加入铝粉产生氢气,则在此溶液中能大量共存的离子组是() A 、Mg 2+、K +、NO 3-、SO 42- B 、AlO 2-、NH 4+、Na +、Br -C 、SO 42-、Cl -、AlO 2-、Na +D 、NH 4+、I -、Fe 3+、Cl -8.下列各组离子,在指定环境中一定能大量共存的是 () A 、pH=7的溶液中:Al 3+、K +、SO 42-、HCO 3-B 、加入铝粉能放出氢气的溶液中:CO 32-、AlO 2-、I -、NO 3-C 、能使pH 试纸变深蓝色的溶液中:S 2-、SO 32-、S 2O 32-、SO 42-D 、由水电离出的[OH -]=10-13mol/L 的溶液中:Fe 3+、NH 4+、ClO -、Cl -9.下列各组离子在溶液中能大量共存的、且此溶液既能与盐酸反应又能与烧碱反应的是() A 、Na +、K +、SO 42-、HCO 3- B 、AlO 2-、OH -、Na +、K +C 、K +、NH 4+、NO 3-、Cl -D 、NH 4+、Fe 2+、HSO 4-、OH -10.在无色的酸性溶液中可以大量共存的离子组是 () A 、Na +、OH -、S 2O 32-、K + B 、Cu 2+、SO 42-、Al 3+、Na +C 、Na +、Al 3+、Mg 2+、NO 3-D 、K + Fe 2+、Cl - 、NO 3-11.下列各组离子中,在碱性溶液中共存,且加入盐酸过程中会产生气体和沉淀的是() A. Na + 、 NO 3- 、 AlO 2--、 SO 42- B. Na + 、CO 32-、、K + 、 SiO 32-C 、、K + 、 Cl -、 AlO 2--、 CO 32-D 、Na + 、Cl -、HCO 3- 、Ca 2+三、简答1.(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:2.写出下列反应的离子方程式:(1)向NaAlO2溶液中通入CO2气体(2)将NaHCO3与Ba(OH)2溶液混和(3)Mg(HCO3)2溶液与石灰水反应(4)明矾溶液与Ba(OH)2溶液反应四、参考答案一、D, D, AB,C,A; D,B,D,BD,A; C,AD,AB,BC,BD; C,CD,B,CD,CD; BD,AB二、D,BC,A,AB,A; AC,C,C,A,C; BC三、1 (1)2H++SO4-+Ba2++2OH- =BaSO4↓+H2O (2) SO4-+Ba2+= BaSO4↓2 (1)CO2不足时:2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32-CO2过量时: AlO2-+2H2O+CO2 = Al(OH)3↓+HCO3-(2)当Ba(OH)2过量时:HCO3-+Ba2++OH- = BaCO3↑+H2O当NaHCO3过量时: 2HCO3-+Ba2++2OH- = BaCO3↓+2H2O+CO32-(3) Mg(HCO3)2过量时: Ca2++2HCO3-+2OH-+Mg2+ = MgCO3↓+CaCO3↓+2H2O;当石灰水过量时:2Ca2++2HCO3-+4OH-+Mg2+ = Mg(OH)2↓+2CaCO3↓+2H2O(4)2Al3++3SO42-+3Ba2++6OH- = 3BaSO4↓+2Al(OH)3↓或Al3++2SO42-+2Ba2++4OH- = 2BaSO4↓+AlO2-+2H2O。
(完整版)离子反应与离子共存练习题及答案

离子反应与离子共存习题一、选择题:每小题只有一个选项正确. 1.下列反应的离子方程式不正确的是( )A .向烧碱溶液中滴加少量氯化铝溶液O 2H AlO 4OH Al 223+=+--+B .物质的量相等的溴化亚铁跟氯气反应-+-+++=++4Cl Br 2Fe 2Cl 2Br 2Fe 2322C .硫化钾晶体溶于水O2H S 22+-S H 2OH 2+-D .向碳酸钠溶液中滴加过量的稀硫酸O H CO 2H CO 2223+↑=++-2.某无色透明的溶液,在pH =0和pH =14的条件下都能大量共存的是( )A .+2Fe +K -24SO -3NOB .+2Mg +4NH -24SO -Cl C .+Na +K -24SO -3NO D .+2Ba +Na -4MnO -24SO3.下列离子方程式书写正确的是( )A .碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液---+++↓=++232332CO O 2H CaCO 2OH 2HCO CaB .碳酸钠溶液中加入等物质的量的乙酸 --++↑=+COO 2CH O H CO COOH 2CH CO 322323C .2)Ca(ClO 溶液中通入过量的二氧化硫气体2HClO CaSO SO O H 2ClO Ca 3222+↑=+++-+D .用碳棒作电极电解氯化钠饱和溶液4.下列离子反应方程式正确的是( )A .小苏打溶液中加入过量石灰水 O 2H CO CaCO 2OH Ca 2HCO 223323++↓=++--+- B .氯化铝溶液中加入过量氨水 +++↓=+⋅432333NH Al(OH)O H 3NH Al C .氯化亚铁溶液中通入氯气 -+++=+2Cl Fe Cl Fe 322 D .苛性钾溶液中加入稀醋酸 O H OH H 2=+-+ 5.下列反应的离子方程式书写正确的是( )A .金属钠跟水反应: ↑+++-+22H 2OH Na O2H NaB .向偏铝酸钠溶液中加入少量硫酸氢钠溶液 ↓=+++-322)Al(OH O H H AlOC .澄清石灰水中滴入少量的NaHCO 3溶液O 2H CO CaCO 2HCO 2OH Ca 223332++↓=++---+ D .浓盐酸跟二氧化锰混合共热 ↑+++++-+22222Cl O 2H Mn Δ4Cl 4H MnO二、选择题:每小题有一个或二个选项符合题意.6.下列各组离子,在所给条件下能够大量共存的是( )A .pH =0的溶液中,+3Fe 、+2Mg 、-Cl 、-24SOB .水电离出的18L m ol 101][H --+⋅⨯=的溶液中,+K 、-3HCO 、-Cl 、-2SC .使pH 试纸显深蓝色的溶液中,+2Cu 、+3Fe 、-3NO 、-24SOD .在3AlCl 溶液中+Na 、-2AlO 、-24SO 、-3NO7.下列离子方程式的书写正确的是( )A .过量二氧化碳通入偏铝酸钠溶液中: --+↓=++33222HCO Al(OH)AlO O 2H COB .在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合O 2H NH SO 2OH HSO NH 232334+↑+=++---+C .氯气通入冷的烧碱溶液中: O H ClO 3Cl 2OH 2Cl 22++=+---D .硫酸氢钠溶液中加入碳酸氢钠溶液:O H CO HCO H 223+↑=+-+ 8.某溶液中由水电离出的+H 浓度为114L mo1101--⋅⨯,在此溶液中可能大量共存的离子是( )A .+3Al 、-24SO 、+4NH 、-ClB .+K 、+2Fe 、-Cl 、-4MnO C .+K 、+Na 、-2AlO 、-24SO D .+Na 、+K 、-3NO 、-3HCO9.下列离子方程式书写正确的是( )A .在碘化亚铁溶液中通入足量氯气:-+-+++=++4Cl I 2Fe 2Cl 2I 2Fe 2322B .用铂电极电解氯化钠饱和溶液:--+↑+↑+2OH H Cl O2H 2Cl 222电解C .向硫酸亚铁溶液中通入S H 2气体:+++↓=+2H FeS S H Fe 22D .氯化铵溶于水:O2H NH 24++O H NH O H 233⋅++10.下列反应的离子方程式正确的是( )A .硫酸亚铁酸性溶液中加入过氧化氢 O 4H 4Fe 4H O 2H 4Fe 23222+=+++++B .氯化铝溶液通入过量氨水 O 2H AlO 4OH Al 223+=+--C .碳酸钙溶于醋酸 ↑+++=+-+223233CO O H COO 2CH Ca COOH 2CH CaCOD .次氯酸钙溶液中通入过量二氧化碳2HClO CaCO CO O H 2ClO Ca 3222+↓=+++-+11.下列各组离子能大量共存于同一溶液中,且加入过量NaOH 溶液或少量稀42SO H 时,都能产生白色沉淀的是( )A .+2Ba 、+2Mg 、-3NO 、-23COB .+Na 、+3Al 、-Cl 、-2AlOC .+K 、+2Ba 、-Cl 、-3HCOD .+4NH 、+2Ba、+3Fe 、-Cl 12.向等物质的量浓度的NaA 和A Na '溶液中分别通入适量的2CO ,发生如下反应:322NaHCO HA O H CO NaA +=++ 3222CO Na A 2H O H CO A 2Na +'=++'现有等物质的量浓度的NaA 、A Na '、32CO Na 、3NaHCO 四种溶液,其溶液pH 的关系正确的是( )A .332NaHCO CO Na A Na NaA >>'>B .332NaHCO CO Na NaA A Na >>>'C .NaA A Na NaHCO CO Na 332>'>>D .332NaHCO NaA CO Na A Na >>>' 13.下列离子方程式写正确的是( )A .过量二氧化碳通入偏铝酸钠溶液中 --+↓=++33222HCO )Al(OH AlO O 2H COB .用湿润的醋酸铅试纸检验硫化氢气 +++↓=+2H PbS Pb S H 22C .氯化铵溶于水 O2H NH 24++++⋅O H O H NH 323D .用烧碱溶液吸收尾气中少量二氧化硫 --=+32HSO SO OH 三、选择题:每小题3分,9小题共27分.每小题只有一个选项正确14.1L 10m11mol -⋅的O H NH 23⋅与1L mol 12 5m -⋅的盐酸恰好完全中和,最后溶液中所含离子的浓度大小顺序是( )A .][OH ][Cl ][NH ][H 4--++>>>B .][OH ][H ][Cl ][NH 4-+-+>>= C .][H ][OH ][NH ][Cl 4+-+->>> D .][OH ][H ][NH ][Cl 4-++->>> 15.下列离子方程式正确的是( )A .漂白粉溶于盐酸:2HClO Ca 2H )Ca(ClO 22+=+++B .磷酸二钠溶液中加入足量的氢氧化钡溶液O 4H )(PO Ba 4OH 3BaPO 2H 2243242+↓=++-+- C .铝溶于氢氧化钠溶液中:↑+=++--2223H AlO 2O 2H 2OH 2Al D .饱和氯化铁溶液滴加沸水中:+++↓=+3H )Fe(OH O 3H Fe 32316.某二元弱酸的酸式盐NaHA 溶液,若pH >7时,测混合液中各离子的浓度大小关系不正确的是( ) A .][A ][H ][OH ][HA ][Na 2-+--+>>>> B .][OH ]2[A ][HA ][H ][Na 2---++++=+ C .][A ][OH A][H ][H 22--++=+ D .][H ][OH ][A ][HA ][Na 2+---+>>>> 17.在指定的条件下,下列各组离子能大量共存的是( ) A .强碱性溶液中:+K 、+Na 、-ClO 、-2S B .pH =1的溶液中:+2Fe 、+Na 、-I 、+4NHC .与Al 反应产生2H 的溶液中:+H 、-Cl 、-3NO 、+KD .由O H 2电离出的mol/L 10][H 11-+=溶液中:+Na 、-3HCO 、-2AlO 、-24SO18.下列离子方程式书写正确的是( ) A .向4NaHSO 溶液中滴加2)Ba(OH 溶液显中性O H BaSO OH BaSO H 24224+↓=+++-+-+ B .向2NaAlO 溶液中加盐酸至呈酸性 O 2H Al 4H AlO 232+=+++- C .碳酸氢铵溶液中加入过量 O H CO OH HCO NaOH 2233+=+--- D .向苯酚钠溶液中通入过量CO 219.下列离子方程式正确的是( )A .NaHS 水解反应:O H HS 2+--+OH S H 2B .石灰石溶于醋酸:O H CO Ca 2H CaCO 2223+↑+=+++C .Al 投入2FeCl 溶液中:Fe Al Fe Al 32+=+++D .往2)Ba(OH 溶液中滴入42SO H 溶液:↓=+-+4242BaSO SO Ba20.下列各组离子中能在水溶液中大量共存,且溶液显酸性的是( )A .+Na 、+K 、-3HCO 、-3NOB .+H 、+Na 、-Cl 、C .+3Fe 、+K 、-2S 、-ClD .+2Cu 、-3NO 、+2Mg 、-24SO21.下列反应的离子方程式正确的是( ) A .碳酸氢钠溶液跟过量的饱和石灰水反应O 2H CO CaCO 2OH Ca 2HCO 223323++↓=++--+- B .向氢氧化钠溶液中加入稀醋酸 O H H OH 2=++- C .向氯化铁溶液中加入铁粉 -++=+3Cl 2Fe FeCl Fe 23D .向硝酸镁溶液中加过量氨水 +++↓=+⋅422322NH )Mg(OH O H 2NH Mg 22.下列反应的离子方程式正确的是( )A .用氨水吸收少量二氧化硫:-++=+⋅34223HSO NH SO O H NH B .碳酸氢钠溶液中加入少量烧碱:O H CO OH HCO 2233+=+--- C .碳酸亚铁固体加入稀硝酸:O H CO Fe 2H FeCO 2223+↑+=+++ D .2Cl 溶解在水中:--+++=+ClO Cl 2H O H Cl 22 四、本题包括2小题共14分23.(7分)(1)硝酸铅的稀溶液中,滴入几滴稀42SO Na 生成白色4PbSO 沉淀,再滴入数滴饱和醋酸钠溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式______________,试推测第二步离子反应发生原因是________ ______.(2)边微热边向铵明矾O]12H )Al(SO [NH 2244⋅溶液中逐滴加入2)Ba(OH 溶液至中性.①此时发生反应的离子方程式为______________.②向以上所得中性溶液中继续滴加2)Ba(OH 溶液,这一步离子反应的离子方程式是______________. 24.(7分)42HPO Na 溶液呈弱碱性,42PO NaH 溶液呈弱酸性,在42HPO Na 溶液中加入3AgNO 溶液,有黄色沉淀生成,且溶液由弱碱性转变为弱酸性.(1)42HPO Na 溶液呈弱碱性的原因是_____________; (2)42PO NaH 溶液呈弱酸性的原因是_____________;(3)42HPO Na 与3AgNO 反应生成43PO Ag 黄色沉淀的离子方程式是____________.五、本题包括2小题共13分25.(9分)现有A 、B 、C 、D 、E 五种盐溶液,分别由+K 、+4NH 、+Ag 、+2Ba 、+3Al 、-Cl 、-Br 、-23CO 、-24SO 、-3NO 中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同).已知:①A +B →白↓ ②A+D →白↓ ③B +C →白↓ ④D +C →白↓ ⑤A 溶液中][OH ][H -+= ⑥B 溶液中112L mol 101][H --+⋅⨯= ⑦C 、D 、E 三种溶液的pH <7,根据以上实验事实可以推出(用分子式表示)A 为___________________;B 为__________________;C 为___________________;D 为__________________;E 为___________________. 写出以上各步反应的离子方程式:①__________________________________ ②_______________________________ ③______________________________________④_____________________________________26.(5分)在含有+Na 、+2Mg 、-3HCO 、-24SO 的稀溶液中,各离子的物质的量之比为:1212)(SO )(HCO )(Ng )(Na ::::::2432=--++n n n n(1)向该溶液中滴加酚酞试液数滴,溶液呈________色.有关反应的离子方程式为:___________________________.(2)充分加热(1)步所得的溶液,加热的过程中观察到的现象有_________________;完全反应后,溶液呈_________________色,有关反应的离子方程式为:_________________. 六、本题包括2小题共12分27.(4分)(1)在酸性介质中,往4MnSO 溶液里滴加8224O S )(NH (连二硫酸铵)溶液会发生如下离子反应:+---+++→++H SO MnO O H O S Mn 24422822该反应常用于检验+2Mn 的存在,其特征现象是________________.若反应中有0.1 mol 还原剂参加反应,则消耗氧化剂的物质的量为________________mol .。
离子共存练习题

离子共存练习题离子共存是化学学科中的一个重要内容,涉及到离子间的相互作用和离子的稳定性等问题。
下面是一些离子共存的练习题,帮助你巩固相关知识。
题目一:根据以下反应方程式,回答问题1. NaOH + HCl → NaCl + H2O2. AgNO3 + NaCl → AgCl + NaNO31) 请问在反应中发生了哪些离子的共存?它们是以什么形式共存的?答案:在第一反应中,发生了氢离子和氯离子的共存,它们以氯化钠的形式共存。
在第二反应中,发生了银离子和氯离子的共存,它们以氯化银的形式共存。
2) 分别写出上述两个反应中生成物的离子方程式。
答案:第一反应中,产生了Na+离子和Cl-离子。
第二反应中,产生了Ag+离子和Cl-离子。
题目二:根据以下描述,判断离子间的共存情况1) 某化学试验中,向溶液中依次滴加了Ba2+离子和SO42-离子,观察发现产生了白色沉淀。
问题:根据观察结果,判断Ba2+离子和SO42-离子的共存情况。
答案:观察结果表明,Ba2+离子和SO42-离子以硫酸钡的形式共存。
2) 在一次实验中,H2SO4溶液与NaOH溶液混合,产生了Na+、SO42-和H2O。
问题:根据实验结果,判断Na+离子、SO42-离子和H2O的共存情况。
答案:实验结果表明,Na+离子、SO42-离子和H2O以硫酸钠和水的形式共存。
题目三:对以下离子配对进行判断1) Mg2+和CO32-问题:根据Mg2+和CO32-离子的化学性质,判断它们能否以碳酸镁的形式共存。
答案:根据Mg2+和CO32-离子的化学性质,它们能够以碳酸镁的形式共存。
2) Al3+和OH-问题:根据Al3+和OH-离子的化学性质,判断它们能否以氢氧化铝的形式共存。
答案:根据Al3+和OH-离子的化学性质,它们能够以氢氧化铝的形式共存。
题目四:综合判断在实验中,向溶液中加入了Ag+离子和Br-离子,观察到在溶液中形成了黄色沉淀。
问题:根据观察结果,判断Ag+离子和Br-离子能否以溴化银的形式共存。
新教材高考化学微专题小练习专练6离子反应与离子共存
专练6 离子反应与离子共存一、单项选择题 1.[2021·北京卷]使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现“亮→暗(或灭)→亮”现象的是( )2.[2021·湖南卷]对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )3.[2020·江苏卷]常温下,下列各组离子在指定溶液中能大量共存的是( )A.0.1 mol ·L -1氨水:Na +、K +、OH -、NO -3B.0.1 mol ·L -1盐酸:Na +、K +、SO 2-4 、SiO 2-3C.0.1 mol ·L -1KMnO 4溶液:NH +4 、Na +、NO -3 、I -D.0.1 mol ·L -1AgNO 3溶液:NH +4 、Mg 2+、Cl -、SO 2-4 4.下列实验操作、现象与结论均正确的是( )换法净化水过程如图所示。
下列说法中错误的是( )A .经过阳离子交换树脂后,水中阳离子的总数不变B .水中的NO -3 、SO 2-4 、Cl -通过阴离子树脂后被除去 C .通过净化处理后,水的导电性降低 D .阴离子树脂填充段存在反应H ++OH -===H 2O6.[2022·哈尔滨师大附中高三月考]常温下,下列各组离子在指定溶液中能大量共存的是( )A .无色透明的溶液中:Fe 3+、Mg 2+、SCN -、Cl -B .c (H +)c (OH -)=1×10-12的溶液中:K +、Na +、CO 2-3 、NO -3 C .c (Fe 2+)=1 mol ·L -1的溶液中:K +、NH +4 、MnO -4 、SO 2-4D .能使甲基橙变红的溶液中:Na +、NH +4 、SO 2-4 、HCO -37.下列有关NaClO 和NaCl 混合溶液(已知该混合溶液呈碱性)的叙述正确的是( )A.该溶液中, H +、NH +4 、SO 2-4 、Br -可以大量共存B.该溶液中, Ag +、K +、NO -3 可以大量共存C .向该溶液中滴入少量FeSO 4溶液,反应的离子方程式为:2Fe 2++ClO -+2H +===Cl -+2Fe 3++H 2OD .向该溶液中加入浓盐酸,每产生1 mol Cl 2×1023个 二、不定项选择题8.制备(NH 4)2Fe(SO 4)2·6H 2O 的实验中,需对过滤出产品的母液(pH <1)进行处理。
离子反应练习题及答案

离子反应练习题及答案一、选择题1. 在离子反应中,哪些离子是不可能共存的?A. Na+ 和 Cl-B. Fe3+ 和 SCN-C. OH- 和 H+D. K+ 和 NO3-2. 以下哪个反应是离子反应?A. 2H2 + O2 → 2H2OB. 2H+ + CO3^2- → CO2 + H2OC. 2H2O → 2H2 + O2D. 2Na + Cl2 → 2NaCl3. 离子反应的实质是什么?A. 电子的转移B. 原子的重新排列C. 离子的重新排列D. 能量的释放4. 以下哪个离子方程式书写正确?A. Ag+ + Cl- → AgCl↓B. 2H+ + CO3^2- → CO2↑ + H2OC. 2H2O → 2H2 + O2D. Ca2+ + CO3^2- → CaCO35. 离子反应中,哪些条件会导致离子不能共存?A. 离子间发生氧化还原反应B. 离子间生成弱电解质C. 离子间生成沉淀D. 所有上述条件二、填空题6. 离子反应的条件包括________、________和________。
7. 离子方程式中,如果反应物或生成物是可溶性的,通常写成________形式,如果是难溶性的,则写成________形式。
8. 在离子反应中,如果生成物中有气体或沉淀,需要用符号________或________表示。
9. 离子反应中,如果生成物中有弱电解质,通常用化学式表示,并且用符号________表示。
10. 离子反应中,如果反应物或生成物中有水生成,通常用化学式________表示。
三、简答题11. 请简述离子反应的特点。
12. 请解释为什么在离子反应中,某些离子不能共存。
四、计算题13. 已知在25°C时,Ksp(Ag2CrO4) = 5.36 × 10^-12。
如果向含有0.01 mol/L Ag+的溶液中加入CrO4^2-,求CrO4^2-的浓度至少为多少才能使Ag2CrO4沉淀完全形成?五、实验题14. 实验室中进行离子反应实验时,如何验证离子反应是否发生?请列举实验步骤和预期观察结果。
专题二:离子反应与共存--解析版

△△专题二 离子反应与共存1.不能正确表示下列变化的离子方程式的是A.在漂白液中滴加少量稀硫酸以增强漂白性:ClO -+H + = HClOB.少量铁粉溶解在稀硝酸中::Fe+4H ++NO 3−=Fe 3++NO↑+2H 2O C.向硫酸铝溶液中加入少量的氢氧化钡溶液:2Al 3++3SO 42−+3Ba 2++6OH -=2Al(OH)3↓+3BaSO 4↓D.自来水长期煮沸时生成水垢:xCa 2++yMg 2++(2x+2y) HCO 3−=xCaCO 3↓+yMgCO 3↓+(x+y)CO 2↑+ (x+y)H 2O D D 项:水垢的主要成分为CaCO 3和Mg(OH)2 2.下列解释事实的方程式不正确的是 A.泡沫灭火器的反应原理:2Al 3++3CO 32−+3H 2O =2Al(OH)3↓+3CO 2↑B.氧化亚铁在空气中加热:6FeO+O 2=2Fe 3O 4C.漂白液中加少量白醋可以增强消毒效果:ClO -+ CH 3COOH = HClO+ CH 3COO -D.用Na 2S 2O 3做碘量法实验时,溶液pH 不可太低:S 2O 32− +2H +=SO2↑+S↓+H 2O A A 项泡沫灭火器是Al 2(SO 4)3溶液和NaHCO 3溶液反应3.宏观辨识与微观探析是化学学科核心素养之一。
下列变化对应的离子方程式正确的是A.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe 3++3MgO+3H 20=2Fe(OH)3↓+3Mg 2+B.向碘化亚铁溶液中滴加少量稀硝酸:2NO 3−+3Fe 2++4H +=3Fe 3++2NO↑+2H 2OC.碳酸钙溶于醋酸:CaCO 3+2H +=Ca 2++CO 2↑+H 2OD.铅蓄电池放电时正极上的反应:PbO 2+2e -+4H +=Pb 2++2H 2O A 【解析】B 项I -先被 HNO 3氧化 C 项酷酸是弱电解质,不能拆为H + D 项生成的 P b 2+以PbSO 4固体的形式存在4.下列分子或离子在指定的分散系中能大量共存的一组是 A.银氨溶液:Na +、K +、NO 3−、NH 3·H 2O B.中性溶液中:Fe 3+、K +、Cl -、SO 42− C.氢氧化铁胶体:H +、K +、S 2-、Br - D.高锰酸钾溶液:H +、Na +、SO 42−、葡萄糖分子 A 【解析】B 项 Fe 3+只存在于pH<3的酸性溶液中 C 项H +不能与S 2-大量共存 D 项高锰酸钾会将葡萄糖氧化5. 25℃时,下列各组离子在指定溶液中一定能大量共存的是A.pH=1的溶液中:K +、NH 4+、[Ag(NH 3)2]+、NO 3−B.与Al 反应可以放出氢气的溶液中:Mg 2+、NH 4+、SO 42−、Br -C.澄清透明的溶液中:Fe 3+、Na +、SO 42−、Cl -D.能使甲基橙变为红色的溶液中:Fe 2+、Na +、Cl -、NO 3− C 【解析】A 项,[Ag(NH 3)2]+无法在酸性溶液中大量存在B项,若溶液为强碱性,则NH4+无法大量存在D项,酸性溶液中,NO3−会氧化Fe2+6.下列反应方程式表达正确的是A.用饱和Na2CO3溶液除去乙酸乙酯中的少量乙酸:2CH3COOH+CO32−=2CH3COO-+CO2↑+H2OB.明矾溶液与过量氨水混合:A13++4NH3+2H2O=AlO2−+4NH4+C.稀硫酸与稀氢氧化钾溶液发生反应:H 2SO4(l)+2KOH(1)=K2SO4(1)+2H2O(1) ΔH=-57.3 kJ/molD.将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1:2混合:Ba2++20H-+2H++SO42−=BaSO4↓+2H2OD【解析】A项应该生成HCO3−,B项应该生成Al(OH)3,C项H2O的系数应为1,且除水外其它的物质状态应为aq7.某溶液可能含有Na+、NH4+、Fe2+、A13+、I-、AlO2−、SiO32−、SO32−、CO32−、SO42−。
初中离子共存问题完整版

初中离子共存问题
解题准备信息:
1、离子在溶液中能大量共存的基本条件是:彼此间任意结合不会产生沉淀、气体或水。
下面横线链接的
离子不能共存。
2、在解决离子
共存时还应
注意以下条
件:
(1)若题
目强
调溶
液无
色,则溶液中不能含Cu离子、Fe离子和亚Fe离子。
(2)若题目强调溶液的pH=0(或1,2,)则溶液呈强酸性,此时一定不含
CO3离子、HCO3离子、OH离子等。
(3)若题目强调溶液的pH=14(或12,13)则溶液呈强碱性,此时一定不含
H离子、HCO3离子、NH4离子等。
初中化学—离子共存问题30题
1.(
、、
、OH﹣、、
)
)
12.(2012?防城港)下列各组物质在水溶液中能够共存,而且加入紫色石蕊试液后显蓝色的
)
22.(2011?南京)下列各组离子在水中一定能大量共存,并形成无色透明溶液的是()
)。
i离子反应和离子共存

三、离子方程式:
离子反应:有离子参加或生成的化学反应。 (1)概念:用实际参加反应的离子符号来表示离子反应的式子。
(2)意义:A.反映物质(微粒)在水中主要状态; B.揭示反应实质;C.表示同一类型反应 (3)离子方程式的类型 A.在溶液中进行的复分解反应 B.在溶液中进行的络合反应 E.盐类的水解
(4)NaHSO4溶液与Ba(OH)2溶液混合
Ba(OH)2溶液中加入NaHSO4溶液至中性
Ba2++ 2OH- +SO42-+2H+ = BaSO4↓+2H2O
Ba(OH)2溶液中加入NaHSO4溶液至沉淀完全
SO42-+H++ Ba2++OH- =BaSO4 ↓ +H2O
注意: Ca(OH)2溶液中加入少量的Ca(HCO3)2溶液 Ca(OH)2溶液中加入足量的Ca(HCO3)2溶液
现象:先无明显现象,然后生成白色沉淀。
盐酸
Na2CO3 溶液
① CO32-+2H+ = CO2↑+H2O
H2SO4 溶液 现象:有大量气体生成
H2SO4 溶液
Na2CO3 溶液
① CO32-+H+ = HCO3② HCO3-+H+ = CO2↑+H2O 现象:开始时无明显气体,稍后有大量气体 产生
: 讨论2:(2010· 江苏)常温下,下列各组离子在指定溶液中能大 、 量共存的是( ) A.pH=1的溶液中: Fe2+ NO3 、SO2 Na 4 、 B.由水电离的 c H 1 1014 mol L1 的溶液中: 2+ K Cl HCO3 Ca c C. H / c OH 1012 的溶液中: NH Al3 NO3 4
高二化学离子共存试题

高二化学离子共存试题1.在指定的条件下,下列各组离子能大量共存的是()A.使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+B.强碱性溶液中:K+、Na+、ClO-、S2-C.0.1 mol·L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42-D.由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42-【答案】A【解析】A、给定条件下,组内离子间不反应,能大量共存,正确;B、强碱性溶液中,ClO-和S2-间发生氧化还原反应,不能大量共存,错误;C、0.1 mol·L-1 NaAlO2溶液中,H+和AlO2-之间发生反应:AlO2- + H+ + H2O ====Al(OH)3↓ 或AlO2- + 4H+ ====Al3+ + 2H2O,不能大量共存,错误;D、由H2O电离出的c(H+)=10-11mol/L溶液既可能为强酸溶液,又可能为强碱溶液,强酸性条件下,发生反应: HCO3- + H+ ="===" CO2↑ + H2O,强碱性条件下发生反应:HCO3- +OH- ="===" CO32- + H2O,不能大量共存,错误。
【考点】考查离子反应、离子大量共存问题。
2.在下列各溶液中,离子一定能大量共存的是A.强酸性溶液中:K+、Al3+、CH3COO-、SO42-B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO、Br-、Ba2+C.室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl-D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42-【答案】C【解析】A、在强酸性溶液中,醋酸根离子要与氢离子生成弱电解质醋酸,不能共存,错误;B、水电离出来的c(H+)=10-13mol/L的溶液,表明水的电离受到了抑制,不能共存,错误;C、正确;D、硝酸根离子在酸性条件下,可以氧化二价铁离子,不有共存,错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
离子反应和离子共存练
习题
集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)
离子反应综合练习:离子方程式+离子共存 1.下列反应中符合H+ + OH-=H2O 离子反应的是
A. 稀硫酸与稀氨水
B.稀硫酸与氢氧化钡溶液
C. 浓硝酸与氢氧化钡溶液
D.盐酸与氢氧化铁胶体反应 2.下列属于强电解质的是
A.醋酸
B.酒精
C.铜
D.小苏打 3.下列各组离子能在呈酸性的无色溶液中大量共存的是
A.Ba 2+、Na +、NO 3-、MnO 4-
B.Mg 2+、Cl -、Al 3+、SO 42-
C.K +、OH -、HCO 3-、NO 3-
D.Ca 2+、Na +、Fe 3+、SO 32- 4
44溶液之间的反应 ②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应 ③稀硫酸与可溶性钡盐溶液之间的反应 ④氢氧化钡溶液与稀硫酸反应( )
A .①②
B .①②④
C .②③
D .①②③ 6. 下列离子方程式中,不正确的是
A.稀硫酸滴在铁片上:Fe +2H +=2Fe 2++H 2↑
B .硫酸铜溶液与氯化钡溶液反应:SO 42-+Ba 2+=BaSO 4↓ C.盐酸滴在石灰石上:CaCO 3+2H +=Ca 2++CO 2↑+H 2O D.氧化铜与稀硫酸混合:CuO +2H +=Cu 2++H 2O
7. 下列离子方程式改写成化学方程式正确的是( )
A .Cu 2+ + 2OH - = Cu(OH)2? CuCO 3+2NaOH= Cu(OH)2? +Na 2CO 3
B .CO 32- + 2H + = CO 2? + H 2O BaCO 3 + 2HCl =BaCl 2+ CO 2? + H 2O
C .Ca 2+ + CO 32- = CaCO 3 ? Ca(NO 3)2+NaCO 3 = CaCO 3 ?+2NaNO 3
D .H + +OH - = H 2O 2KOH+H 2SO 4 = K 2SO 4 +2H 2O 8. 下列无色..溶液中离子可大量共存的是 A.Cu 2+、SO 42-、Fe 3+、Cl - B.Ba 2+、Na +、NO 3-、CO 32-
C.MnO 4- 、Fe 2+ 、Na + 、SO 42- D .Na + 、NO 3-、K + 、SO 42- 9. 下列离子可大量共存的
A.K + 、NH 4+、、 HCO 3- 、OH -
B.SO 32- 、SO 42- 、H + 、Na +
C.Fe 3+ 、Cu 2+ 、SO 42- 、OH -
D.Cu 2+ 、Fe 2+、SO 42- 、NO 3 10.对四种无色..溶液进行离子检验,实验结果如下,其中明显错误..的是( ) A .K +、Na +、Cl -、NO 3- B .Cu 2+、NO 3-、OH -、HCO 3-
C .Na +、OH -、Cl -、NO 3-
D .MnO 4-、K +、S 2-、Na +
11.分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂
( )
A .CH 3COOH 与NaOH 在相同条件下电离程度相等
B .NaCl 溶液能导电是因为溶液中有Na +和Cl -
C .H 2SO 4在电流作用下在水中电离出H + 和SO 42-
D .检验CO 32-或HCO 3-离子的方法是取少许样品加入盐酸,将产生的气体通入澄清石灰水
13.下列离子方程式书写正确的是 ( )
A .碳酸钙与盐酸反应 CO 32-+2H +=CO 2↑+H 2O
B .硫酸和氯化钡溶液反应 Ba 2++SO 42-=BaSO 4↓
C .氢氧化钠和少量氢硫酸反应 2OH -+H 2S=S 2-+H 2O
D .铁钉放入硫酸铜溶液中 Fe+3Cu 2+=2Fe 3++3Cu
14.在碱性溶液中能大量共存且为无色透明的溶液是 ( )
A .K 、Cl -、MnO 4-、SO 42-
B .Na +、SiO 32-、NO 3-、CO 32-
C .Na +、NO 3-、SO 42-、HCO 3-
D .Na +、SO 42-、S 2-、Cl - 15.向CuSO 4溶液中滴加NaOH 溶液,溶液中 离子的量减少,
离子的量增加, 离子的量没有变化,反应的离子方程式是 。
16.写出符合以下离子方程式的化学方程式各1个 (1)HCO 3-+H +=CO 2↑+H 2O
_________________________________________ (2)CaCO 3+2H +=Ca 2++CO 2↑+H 20
_________________________________________ (3)CO 2+2OH -=CO 32-+H 2O
__________________________________________
17.下列各组离子在水溶液中能大量共存的是
( )
A .Na +
、Ba 2+
、Cl ?
、SO 42-
B . Ca 2+、HCO 3?、C1?、K +
C .Mg 2+
、Ag +
、NO 3?
、Cl ?
D . H +
、Cl ?
、Na +
、CO 32?
18.在某无色透明的酸性溶液中,能共存的离子组是
( )
A .Na + 、K +、SO 42-、HCO 3?
B .Cu 2+、K +、SO 42-、NO 3?
C .Na +、 K +、Cl ?、 NO 3?
D .Fe 3+、K +、SO 42-、Cl ?
19.已知某酸性溶液中含有Ba 2+、Fe 3+,则下述离子组中能与上述离子共存的是
( )
A .CO 32-、Cl -
B .NO 3-、Cl -
C .NO 3-、SO 42-
D .OH -、NO 3-
20.能正确表示下列化学反应的离子方程式的是 ( )
A .氢氧化钡溶液与盐酸的反应 OH ?+H + = H 2O
B .澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H + = Ca 2+ + 2H 2O
C .铜片插入硝酸银溶液中 Cu + Ag + = Cu 2+ + Ag
D .碳酸钙溶于稀盐酸中 CaCO 3+2H +
=Ca 2+
+H 2O +CO 2?
21.在下列化学方程式中,能够用离子方程式Ba 2++SO 42-=BaSO 4↓表示的是
( )
A .BaCl 2+K 2SO 4=BaSO 4↓+2KCl
B .BaCO 3+H 2SO 4 = BaSO 4↓+CO 2↑+H 2O
C .Ba(NO 3)2+ H 2SO 4= BaSO 4↓+2H NO 3
D .Ba(OH)2+ 2KHSO 4 = BaSO 4↓+K 2SO 4+2H 2O
22.重金属离子具有毒性。
实验室中有甲、乙两种重金属离子的废液,甲废
液经化验呈碱性,主要为有毒离子为Ba 2+,如将甲、乙两废液按一定比例混合,毒性明显降低。
则乙废液中可能含有的离子是
A . Cu 2+和SO 42-
B . Cu 2+和Cl ?
C . K +和
SO 42-
D . Ag +和NO 3?
23.下列溶液的溶质都是强电解质,这些溶液中的Cl ?浓度与50 mL 1
mol ·L -1 MgCl 2溶液中的Cl ?浓度相等的是
( )
A.150 mL 1 mol·L-1 NaCl溶液B.75 mL 1 mol·L-1 溶液
CaCl
2
C.150 mL 2 mol·L-1 KCl溶液D.75 mL 1 mol ·L -1 AlCl
溶液
3。
