2011年暨南大学硕士研究生考试大纲818有机化学B
暨南大学有机化学第九章-1

R O
H
O R H O
H
由于形成氢键,要使醇液体变成蒸汽而沸腾, 由于形成氢键,要使醇液体变成蒸汽而沸腾,必 须打开这些氢键,因此醇的沸点比较高。 须打开这些氢键,因此醇的沸点比较高。
醇的结构与物理性质
另外,由于醇中的羟基 另外, 可以同水形成氢键: 可以同水形成氢键:
R H O O H O R H H O H
-OH 是一个邻对位定位基,且对苯环有致活作用,这也是由 是一个邻对位定位基,且对苯环有致活作用, 于上面所讲的p-π共轭导致苯环上电子云密度增加之故。 共轭导致苯环上电子云密度增加之故。 于上面所讲的 共轭导致苯环上电子云密度增加之故
α−碳上的亲核取代 碳上的亲核取代
机理
邻基参与效应
邻基参与效应
邻基参与效应
例:芥子气的水解速度比一般伯氯代烷快,动力学为 芥子气的水解速度比一般伯氯代烷快, 一级。 一级。
邻基参与效应
机理
邻基参与效应
邻基参与效应
例:下面反应的速率ktrans: kcis= 800 : 1,为什么?
与卤化磷的反应
酚的酸性 与FeCl3显色反应 芳环上的取代反应
酚的酸性
酚具有酸性,而醇是中性的, 酚具有酸性,而醇是中性的,苯酚的酸性比一般的有机酸 甚至比碳酸还弱,但能与NaOH等强碱成盐: NaOH等强碱成盐 弱,甚至比碳酸还弱,但能与NaOH等强碱成盐:
O H O N a O H + + N a H 2 O
与强碱反应
羟基氧的性质
作为碱: 作为碱:醇羟基的取代反应
Brönsted碱 碱
羟基氧的性质
作为碱: 作为碱:醇羟基的取代反应
Lewis碱 碱
作为亲核试剂
硕士研究生(有机化学专业初试)入学考试大纲

硕士研究生(有机化学专业初试)入学考试大纲第一篇:硕士研究生(有机化学专业初试)入学考试大纲硕士研究生(有机化学专业初试)入学考试大纲课程名称:化学基础一、考试的总体要求1、掌握无机化学的基本概念和基本原理;掌握对一般无机化学问题进行理论分析和计算。
2、掌握分析化学中各类分析方法的特点、应用范围及局限性,正确处理分析数据与信息,并具有选择分析化学方法、正确判断和表达分析结果的能力。
3、掌握物理化学课程中重要的基本概念与基本原理并掌握其含义及适用范围。
掌握物理化学的公式应用及应用条件,概念要明确,计算题要求思路正确,步骤简明。
二、考试内容及复习范围无机、分析化学部分1.物质结构简介1)了解微观粒子运动的特殊性:能量的量子化、波粒二象性。
2)了解原子轨道、波函数、概率、概率密度、电子云的概念,了解原子轨道和电子云的角度分布特征。
重点掌握描述电子运动状态的四个量子数(n、l、m、ms)的物理意义、取值规律和合理组合。
3)根据电子排布的三个原则和能级组概念,掌握多电子原子核外电子排布规律,并根据电子排布的价电子构型,判断元素在周期表中的位置(周期、族、区)及有关性质。
4)了解电离能、电子亲和能和电负性等概念及其一般递变规律。
5)了解离子键、共价键的理论要点。
重点掌握杂化轨道理论与分子空间构型及分子极性的关系。
6)了解分子间力和氢键的性质。
7)熟悉和掌握晶体的内部结构和基本类型,以及离子键和离子晶体,金属键和金属晶体。
2.滴定分析概述1)了解有关误差的几个基本概念:系统误差、随机误差、准确度、精密度等。
2)了解误差的来源、特点、消除及减免、提高测定准确度的措施和方法,掌握各种误差的计算(绝对误差、相对误差、绝对偏差、相对偏差、平均偏差、相对平均偏差、标准偏差、变动系数)。
3)掌握有效数字及运算规则,了解置信区间与置信度的概念及计算。
4)掌握可疑值的取舍方法(Q检验法、G检验法)。
了解显著性检验方法(F检验法、t检验法)。
暨南大学考研真题有机化学无机化学

20XX 年招收攻读硕士学位研究生入学考试试题********************************************************************************************学科、专业名称:化学(无机化学、分析化学、有机化学、物理化学、高分子化学与物理) 研究方向:考试科目名称:610无机化学一、选择题 (选择一个正确答案,每小题3分,20题共60分)1. H 2(g) +21O 2(g)H 2O(l) 的Q p 与Q V 之差(kJ ·mol -1)是………………………( ) (A) -3.7 (B) 3.7 (C) 1.2 (D) -1.22. 下列分子形状不属直线形的是……………………………………………………… ( )(A) C 2H 2 (B) H 2S (C) CO 2 (D) HF3. 在某种酸化的黄色溶液中,加入锌粒,溶液颜色从黄经过蓝、绿直到变为紫色,该溶液中含有…………………………………………………………………………………………( ) (A) Fe 3+(B) +2VO (C)-24CrO(D) Fe (CN)-464. 某化学反应的速率常数的单位是(时间)-1,则反应是……………………………… ( ) (A) 零级反应 (B) 三级反应 (C) 二级反应 (D) 一级反应5. 弱酸性水溶液中的氢离子浓度可表示为…………………………………………… ( )(A) 14 - pOH (B) K w /pOH (C) 10 - (14- pOH) (D) 10 - pOH6. 反应 Na 2O(s) + I 2(g)−→−2NaI(s) +21O 2(g) 的m r H ∆为………………………… ( ) (A) 2 m f H ∆(NaI, s) –m f H ∆(Na 2O, s)(B) m f H ∆(NaI, s) – m f H ∆(Na 2O, s) – m f H ∆(I 2, g) (C) 2 m f H ∆(NaI, s) – m f H ∆(Na 2O, s) – m f H ∆(I 2, g)(D) m f H ∆(NaI, s) – m f H ∆(Na 2O, s)7. 当一个化学反应处于平衡时,则………………………………………………………( ) (A) 平衡混合物中各种物质的浓度都相等 (B) 正反应和逆反应速率都是零(C) 反应混合物的组成不随时间而改变 (D) 反应的焓变是零8. 下列各组双原子分子中,均具有顺磁性的是…………………………………………( ) (A) O 2,B 2 (B) C 2,O 2 (C) B 2,Be 2 (D) Be 2,O 29. 关于催化剂的作用,下述中不正确的是………………………………………………( ) (A) 能够加快反应的进行(B) 在几个反应中,能选择性地加快其中一、二个反应 (C) 能改变某一反应的正逆向速率的比值(D) 能缩短到达平衡的时间,但不能改变某一反应物的转化率考试科目:无机化学 共4页,第1页10. 0.40 mol ·dm -3丙酸溶液的pH 是 (K a = 1.3 ⨯ 10-5)……………………………………( ) (A) 0.40 (B) 2.64 (C) 5.28 (D) 4.8811. 第二周期元素双原子分子中有未成对电子的分子有……………………………… ( ) (A) O 2、Be 2两种 (B) C 2、N 2两种 (C) B 2、O 2两种 (D) Be 2、C 2两种12. 欲除去CuSO 4酸性溶液中少量Fe 3+,加入下列试剂效果最好的是…………………( ) (A) 氨水 (B) NaOH (C) H 2S 水 (D) Cu 2(OH)2CO 313. 反应A + B −→−C ,就每种反应物而言,反应级数均为1,在一定的起始浓度下, 25℃ 时的反应速率是15℃ 时的三倍,问35℃ 时的反应速率是15℃ 时的多少倍…( ) (A) 31/2 (B) 3 (C) 9 (D) 1814. 在[Co(en)(C 2O 4)2]配离子中,中心离子的配位数为…………………………………( ) (A) 3 (B) 4 (C) 5 (D) 6 15. 已知 N 2(g) + 3H 2(g)2NH 3(g);N 2(g) +21H 2(g)NH 3(g) 和N 2(g) + H 2(g)2/3NH 3(g) 的平衡常数分别为K 1、K 2和K 3,则它们的关系是…( )(A) K 1 = K 2 = K 3 (B) K 1 = (K 2)2 = (K 3)3(C) K 1 =21K 2 =31K 3 (D) K 1 = (K 2)1/2 = (K 3)1/316. 将下列物种按键能大小排列成序,正确的是…………………………………………( )(A) NO 2-< N 2;NO > NO +;O 2+>O 2-(B) N 2+< N 2;NO < NO +;O 2+>O 2- (C) N 2+> N 2;NO > NO +;O 2+>O 2- (D) N 2+< N 2;NO > NO +;O 2+<O 2-17. 下列离子的电子构型可以用[Ar]3d 6表示的是………………………………………( ) (A) Mn 2+ (B) Fe 3+ (C) Co 3+ (D) Ni 2+18. 某一反应的活化能为65 kJ ·mol -1,则其逆反应的活化能为………………………( ) (A) 65 kJ ·mol -1 (B) -65 kJ ·mol -1(C) 0.0154 kJ ·mol -1 (D) 无法确定19. 下列各对含氧酸盐热稳定性的大小顺序,正确的是…………………………………( ) (A) BaCO 3 > K 2CO 3 (B) CaCO 3 < CdCO 3 (C) BeCO 3 > MgCO 3 (D) Na 2SO 3 > NaHSO 320. AgCl 在纯水中的溶解度比在0.10 mol ·dm -3 NaCl 溶液中的溶解度大:…………( ) (AgCl :K sp = 1.77 ⨯ 10-10)(A) 约7.5 ⨯ 103倍 (B) 约7.5 ⨯ 102倍 (C) 约75倍 (D) 不是以上数据考试科目:无机化学 共4页,第2页考试科目:无机化学共4页,第3页考试科目:无机化学共4页,第4页20XX年招收攻读硕士学位研究生入学考试试题(副题)******************************************************************************************** 学科、专业名称:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、应用化学研究方向:各个方向考试科目名称:812有机化学A考试科目:812有机化学A 共4页,第1 页考试科目:812有机化学A 共4 页,第2 页考试科目:812有机化学A 共4 页,第3 页五、机理题(10分)写出下面反应的反应机理六、合成题(共35分)1、由乙烯为原料合成(15分)2、(10分)3、(10分)考试科目:812有机化学A 共4 页,第4 页。
暨南大学有机化学机理题期末考试试卷(含答案)

暨南大学有机化学机理题期末考试试卷(含答案)一、有机化学机理题1. 解释卤原子接在桥头碳原子上的桥环卤代烃不易发生亲核取代反应。
解:+如果起S N 1反应,得到中间体碳正离子平面型结构,而桥环卤代烃存在刚性结构,桥头碳不易形成sp 2杂化的平面构型;如果起S N 2 反应, 要求亲核试剂从桥头碳背后进攻,高度空间障碍又妨碍了这一点。
所以不论S N 1、S N 2反应都不容易,也就是不易起亲核取代反应。
2.O解OH OH - H+3.OH24解OH2+- HOH- H+ 4.BrH解:OHOH- Cl-++..5.OO2CH3解OHOMeO这是二苯羟乙酸重排。
6.螺戊烷在光照条件下与氯气反应是制备氯代螺戊烷的最好方法。
Cl解释在该反应条件下,为什么氯化是制备这一化合物的如此有用的方法并写出反应历程。
解:H.该反应条件下螺戊烷氯化是自由基反应, 形成图示的平面型或近似于平面型的自由基中间体,中心碳原子为sp2杂化, 未参与杂化的p轨道只有一个未配对电子,垂直于三个sp2杂化轨道,并被另一个环丙烷的弯曲键所稳定,活化能低,反应速度快,是制备该化合物有效的方法。
链引发:Cl2链传递:Cl链终止:ClCl2..7.Cl解 碳正离子1发生重排。
不重排的产物是1-异丙基-1-氯环己烷。
本题碳正离子重排由氢迁移造成。
ClCl++8.4R - 甲基己烯与HBr 反应后生成不等量的2S ,4R -2-溴-4-甲基己烷和2R ,4R -2-溴-4-甲基己烷。
解:Et CH 3H CH 2EtCH 3H CH 2H 3H 3+溴负离子进攻平面三角形碳正离子, 从位阻小的氢原子一侧容易些,所以得到产物以A 占优势。
9.NMe 2OHN HNMe 222+ 苯肼与丁酮在Fischer 吲哚合成法条件下反应,生成两个吲哚异构体,给出它们的结构并解释原因。
解:丁酮羰基两侧都有α–氢,在Fischer吲哚合成法中都可用于成环,所以产物有两种异构体1和2。
暨南大学有机化学1-14

第二章烷烃一、选择题1、下列自由基最稳定的是,最不稳定的是。
提交答案A. B.C. D.2、在光照条件下与反应,可能的一氯产物有几种提交答案A.3B.4C.5D.63、下列化合物含有伯、仲、叔、季碳原子的是提交答案,2,3—三甲基丁烷,2,3—三甲基戊烷,3,4—三甲基戊烷,3—二甲基戊烷4、下列化合物含有伯、仲、叔氢的是提交答案,2,4,4—四甲基戊烷,3,4—三甲基戊烷,2,4—三甲基戊烷 D.正庚烷5、2—甲基丁烷在室温下光照溴代,相对含量最高的是提交答案A.B.C.D.二、判断下列各组构象是否相同1.相 同不相同和2.相 同不相同和3.相 同和不相同4.相同不相同三、写出下列反应的机理。
解答四、某烷烃的相对分子质量为72。
氯化时(1)只得一种一氯代产物,(2)得三种一氯代产物,(3)得四种一氯代产物,(4)只得二种二氯衍生物。
分别写出这些烷烃的构造式。
解答第三章烯烃一、选择题1、下列烯烃,相对稳定性最大的是提交答案,3—二甲基—2—丁烯—甲基—2—戊烯C.反—3—已烯D.顺—2—已烯2、下列化合物既是顺式,又是E型的是提交答案A. B.C. D.3、下列化合物既是反式、又是Z型的是提交答案A. B.C. D.4、下列试剂与环已烯反应得到顺式二醇的是提交答案A. B.C. D.5、下列反应为碳正离子机理的是提交答案A.B.C.D.6、下列化合物与加成的相对速度顺序最快的是提交答案A. B.C. D.7、下列化合物中有顺反异构体的是提交答案A. 2—甲基—1—丁烯—甲基—2—丁烯C. 2—甲基—2—戊烯—甲基—2—戊烯8、在过氧化物存在下,与反应,得不到反马氏物的提交是答案—甲基—2—丁烯—戊烯—甲基—1—丁烯 D.环已烯提交9、下列碳正离子最稳定的是,最不稳定的是答案A. B.C. D.二、完成下列反应式.1.答案2.答案3.答案4.答案5.答案6.答案1. 2.7.( )答案 1. 2.8.答案9.答案10.()( )答案1.2 .11.答案三、写出下列反应可能机理。
暨南大学硕士研究生考考试参考书目
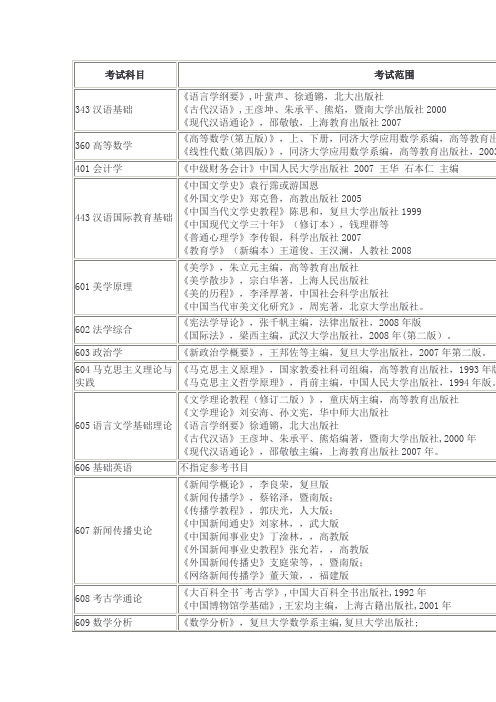
601美学原理
《美学》,朱立元主编,高等教育出版社
《美学散步》,宗白华著,上海人民出版社
《美的历程》,李泽厚著,中国社会科学出版社
《中国当代审美文化研究》,周宪著,北京大学出版社。
602法学综合
《宪法学导论》,张千帆主编,法律出版社,2008年版
《国际法》,梁西主编,武汉大学出版社,2008年(第二版)。
《文学理论》刘安海、孙文宪,华中师大出版社
《语言学纲要》徐通锵,北大出版社
《古代汉语》王彦坤、朱承平、熊焰编著,暨南大学出版社,2000年
《现代汉语通论》,邵敬敏主编,上海教育出版社2007年。
606基础英语
不指定参考书目
607新闻传播史论
《新闻学概论》,李良荣,复旦版
《新闻传播学》,蔡铭泽,暨南版;
401会计学
《中级财务会计》中国人民大学出版社2007王华石本仁主编
443汉语国际教育基础
《中国文学史》袁行霈或游国恩
《外国文学史》郑克鲁,高教出版社2005
《中国当代文学史教程》陈思和,复旦大学出版社1999
《中国现代文学三十年》(修订本),钱理群等
《普通心理学》李传银,科学出版社2007
《教育学》(新编本)王道俊、王汉澜,人教社2008
《新闻公关广告之互动研究》,董天策等,暨南版
810高等代数
《高等代数》,北京大学编著,高等教育出版社
811普通物理
《物理学》,马文蔚编,高等教育出版社,(第四版电磁学、光学和量子物理部分),1999版
812有机化学A
《有机化学》,胡宏纹编,南京大学出版社,第二版
813病理生理学
2013年暨南大学有机化学B考研真题

2013年暨南大学招收攻读硕士学位研究生入学考试试题(B 卷)********************************************************************************************学科、专业名称:药学学科药物化学、药剂学、生药学、药物分析学、微生物与生化药学、药理学专业、中药学专业研究方向:考试科目名称:有机化学B考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、写出结构式或根据结构式命名(10小题,每题2分,共20分)1.化合物为含C 数少于10的伯醇,其中70.4%C 和13.9%H 。
2.与分子式C 3H 4相匹配的所有可能结构。
3.油脂水解,提取脂肪酸后余下的化合物。
4.SMeBrCO 2H5.N OHBr6.COOHH 2N7.8.9.OO t -BuEt Me Br H ClHCOOH10.反-1-甲基-3-异丙基环己烷最稳定的构象。
二、用化学方法区别下列各组化合物(4小题,每小题2分,共8分)1.环丙烷、丙烯、丙炔和丙烷。
2.苯酚和邻二甲苯。
3.D-葡萄糖和D-果糖。
4.乙醇、叔丁醇和异丙醇。
三、选择题,可能不只一个答案(16小题,每小题2分,共32分)1、下列化合物中,哪一个最容易发生亲电加成反应()A.(CH 3)2C=CH-CH 3B.(CH 3)2C=CH 2C.CH 3-CH=CH-CHOD.CH 2=CH-Cl2、由大到小排列以下化合物与1,3-丁二烯发生Diels-Alder 反应的活性次序()I.CH 2=CHCH 2Cl;II.CH 2=CHCH 2CN;III.CH 2=CHCH 2CH 3;IV.CH 2=CHCHOA.I >II >IV >III;B.IV >II >I >III;C.III >II >I >IV;D.IV >I >III >II 3、丁烷的构象中,能量最低的是()A.邻位交叉式 B.对位交叉式 C.部分重叠式 D.全重叠式4、与AgNO 3水溶液反应速度最快的是()A.氯仿 B.氯苯 C.氯化苄 D.氯乙烷5、下列化合物在低温下和亚硝酸反应能得到重氮盐的是()A.伯脂肪胺 B.仲脂肪胺 C.伯芳香胺 D.仲芳香胺6、下列化合物那些具有旋光性()C 2H 5CH 3Br ClH BrCH 3H H H N H 3C C 3H 7C 2H 5O CH 3Br H Br H CH 3A. B.C.D.7、就碱性而言,下列化合物那个最大()NN HN HNH 2A.B.C.D.8、下列化合物中沸点最高的是()A.CH 3CH 2CH 2CHO B.CH 3CH 2CH 2CH 2OH C.CH 3CH 2OCH 2CH 3 D.CH 3CH 2CH 2CH 39、可用红外光谱鉴别的化合物是()A.CH 3CH 2CH 3/B.CHOOH/C.OCH 3COOH/D./10、下列化合物中,pH 值最小的是()A.CH 3CH 2OH B.CH 3OCH 3 C.对甲苯酚 D.H 2O 11、下列化合物中,哪一个最容易发生S N 2反应()FClBrIA.B.C.D.12、下列化合物与饱和NaHSO 3溶液反应,活性最大的是()A.乙醛 B.丙酮 C.2-戊酮 D.苯甲醛13、光照条件下烯丙位的卤代反应是通过哪种中间体进行的()A.正碳离子 B.负碳离子 C.协同过渡态 D.自由基14、下列化合物不能使KMnO4水溶液褪色而能使溴水褪色的是()A.环戊烷 B.环戊烯 C.环己烯 D.环丙烷15、下列溶剂可用于制备格氏试剂的是()A.EtOEt B.THF C.EtOH D.AcOH 16、保护醛基常用的反应是()A.氧化反应 B.还原反应 C.羟醛缩合反应 D.缩醛反应四、完成下列反应,并注明主次产物和立体化学(14小题,每空格2分,共40分)OCH 3Zn(Hg)/HCl1.2.CH 3 CH = C CH 2 CH 3CH 3+ HBr过氧化合物COOHNH 23.NaNO 2/H 2SO 44.COCH 3+HCHO+N HHClO5.O(1) 2CH 3MgI (2) H +/H 2O 6.+CH 2=CHCHO7.CH 3Cl 2FeCl 2lightN CH 3CH 3IAg 2O H 2O8.9.CH=CHBrCH 2Cl+NaCN10.HCH 3HOC 6H 5SOCl 2Et 2OCH 3COONa PTC/DCM11.Ph CH 2NH 2CH 3OH NaNO 2/HCl12.OC 6H 5CO 3HOO过量CH 2I 2Zn(Cu)13.Ph 3P=CH 2COOHCH 3(1) SOCl 2(2) NH 3Br 2/OH -14.五、综合问答题(4小题,共30分)1、(6分)顺-1,2-环戊二醇和丙酮及少量酸的混合物进行回流,用分水器不断除水,获得分子式为C 8H 14O 2的产物(A ),(A )对碱稳定,遇稀酸生成原料(即顺-1,2-环戊二醇)。
高分子专业有机化学期中测试题

)
4、下列氯化物与 AgNO3 乙醇溶液按 SN1 反应历程最快的是 (
)
A、H2C CHCH2Cl
B、H3CHC CHCl
CH3 C、 CH3CHCl
D、CH3CH2CH2Cl
5、下列碳正离子稳定性由大到小排列正确的是(
)。
(a) CH3CHCH=CH2
(b)
CH3
(c) (CH3)2CH (d) Cl3CCH2
七、合成题。用指定有机物为合成起始原料(无机物、溶剂、催化剂任
选),合成下列各化合物 :(每小题 6 分,共 24 分)
1、以甲苯及其它必要的试剂为原料,合成
2、由环己酮和乙烯为原料合成
CH3
以甲苯为原料,合成
3、以苯为原料合成
Cl 。
以苯、三聚甲醛、乙烯为原料,合成
4、以苯、三聚甲醛、乙烯为原料,合成
8、羧酸衍生物中下列离去基团的离去活性由大到小排列正确的是( B )。
(a) NH2 (b) RO (c) RCOO (d) Cl A、a >b >c >d B、d >c >b >a C、b >c >d >a
D、d >a >c >b
9、下列化合物按亲核加成反应活性由大到小排列正确的是( D ):
O
O
6、下列卤代物中哪一种可用于制备 Grignard 试剂?( D )
A、 HOCH2CH2Br
B、 CH3CHCOOH Br
C、 BrCH2CH2Br
D、 (CH3O)2CHCH2Br
《 有机化学 》试卷第 2 页 共 9 页
7、下列的表述哪个是错误的? ( C、D ) A、 外消旋体的旋光度为 0;B、 内消旋体的旋光度为 0; C、 内消旋体是混合物;D、 含有 2 个手性碳原子的化合物一定具有手性.
暨南大学生物化学B 2010-2018年考研真题及答案解析

目录Ⅰ历年真题试卷 (2)暨南大学2010年招收攻读硕士学位研究生入学考试试题 (2)暨南大学2011年招收攻读硕士学位研究生入学考试试题 (6)暨南大学2012年招收攻读硕士学位研究生入学考试试题 (10)暨南大学2013年招收攻读硕士学位研究生入学考试试题 (11)暨南大学2014年招收攻读硕士学位研究生入学考试试题 (15)暨南大学2015年招收攻读硕士学位研究生入学考试试题 (18)暨南大学2016年招收攻读硕士学位研究生入学考试试题 (22)暨南大学2017年招收攻读硕士学位研究生入学考试试题 (27)暨南大学2018年招收攻读硕士学位研究生入学考试试题 (31)Ⅱ历年真题试卷答案解析 (35)暨南大学2010年招收攻读硕士学位研究生入学考试试题答案解析 (35)暨南大学2011年招收攻读硕士学位研究生入学考试试题答案解析 (52)暨南大学2012年招收攻读硕士学位研究生入学考试试题答案解析 (68)暨南大学2013年招收攻读硕士学位研究生入学考试试题答案解析 (72)暨南大学2014年招收攻读硕士学位研究生入学考试试题答案解析 (85)暨南大学2015年招收攻读硕士学位研究生入学考试试题答案解析 (101)暨南大学2016年招收攻读硕士学位研究生入学考试试题答案解析 (117)暨南大学2017年招收攻读硕士学位研究生入学考试试题答案解析 (132)Ⅰ历年真题试卷暨南大学2010年招收攻读硕士学位研究生入学考试试题学科、专业名称:药物化学、药剂学、药物分析学、微生物与生化药学、药理学、中药学专业考试科目名称:713生物化学B考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、名词解释(5*4=20分)1.蛋白质二级结构2.信使核糖核酸3.全酶4.流动镶嵌模型5.内含子二、是非判断(20*1=20分)1.肽键中相关的六个原子无论在二级或三级结构中,一般都处在一个刚性平面内。
[暨南大学考研复试资料]分析化学简答题
![[暨南大学考研复试资料]分析化学简答题](https://img.taocdn.com/s3/m/998ee5bcd5bbfd0a795673c2.png)
1.正确理解准确度和精密度,误差和偏差的概念。
答:准确度是测定平均值与真值接近的程度,常用误差大小来表示,误差越小,准确度越高。
精密度是指在确定条件下,将测试方法实施多次,所得结果之间的一致程度。
精密度的大小常用偏差来表示。
误差是指测定值与真值之差,其大小可用绝对误差和相对误差来表示。
偏差是指个别测定结果与几次测定结果的平均值之间的差别,其大小可用绝对偏差和相对偏差表示,也可以用标准偏差表示。
2.下列情况分别引起什么误差?如果是系统误差,应如何消除?(1)砝码被腐蚀;(2)天平两臂不等长;(3)容量瓶和吸管不配套;(4)重量分析中杂质被共沉淀;(5)天平称量时最后一位读数估计不准;(6)以含量为99%的邻苯二甲酸氢钾作基准物标定碱溶液。
答:(1)引起系统误差,校正砝码;(2)引起系统误差,校正仪器;(3)引起系统误差,校正仪器;(4)引起系统误差,做对照试验;(5)引起偶然误差;(6)引起系统误差,做对照试验或提纯试剂。
3.用标准偏差和算术平均偏差表示结果,哪一种更合理?答:用标准偏差表示更合理。
因为将单次测定值的偏差平方后,能将较大的偏差显著地表现出来。
4.如何减少偶然误差?如何减少系统误差?答:在一定测定次数范围内,适当增加测定次数,可以减少偶然误差。
针对系统误差产生的原因不同,可采用选择标准方法、进行试剂的提纯和使用校正值等办法加以消除。
如选择一种标准方法与所采用的方法作对照试验或选择与试样组成接近的标准试样做对照试验,找出校正值加以校正。
对试剂或实验用水是否带入被测成分,或所含杂质是否有干扰,可通过空白试验扣除空白值加以校正。
5. 质子理论和电离理论的最主要不同点是什么?答:质子理论和电离理论对酸碱的定义不同;电离理论只适用于水溶液,不适用于非水溶液,而质子理论适用于水溶液和非水溶液。
6. 可以采用哪些方法确定酸碱滴定的终点?试简要地进行比较。
答:可以用酸碱指示剂法和电位滴定法确定酸碱滴定的终点。
暨南大学有机化学1-14

第二章烷烃一、选择题1、下列自由基最稳定的是,最不稳定的是。
提交答案A. B.C. D.2、在光照条件下与反应,可能的一氯产物有几种? 提交答案A. 3B. 4C. 5D. 63、下列化合物含有伯、仲、叔、季碳原子的是提交答案A.2,2,3—三甲基丁烷B.2,2,3—三甲基戊烷C.2,3,4—三甲基戊烷D.3,3—二甲基戊烷4、下列化合物含有伯、仲、叔氢的是提交答案A.2,2,4,4—四甲基戊烷B.2,3,4—三甲基戊烷C.2,2,4—三甲基戊烷D.正庚烷5、2—甲基丁烷在室温下光照溴代,相对含量最高的是提交答案A. B.C.D.二、判断下列各组构象是否相同?1.相 同不相同和2.相 同不相同和3.相 同不相同和4.相同不相同三、写出下列反应的机理。
解答四、某烷烃的相对分子质量为72。
氯化时(1)只得一种一氯代产物,(2)得三种一氯代产物,(3)得四种一氯代产物,(4)只得二种二氯衍生物。
分别写出这些烷烃的构造式。
解答第三章烯烃一、选择题1、下列烯烃,相对稳定性最大的是提交答案A.2,3—二甲基—2—丁烯 B.2—甲基—2—戊烯C.反—3—已烯D.顺—2—已烯2、下列化合物既是顺式,又是E型的是? 提交答案A. B.C. D.3、下列化合物既是反式、又是Z型的是?提交答案A. B.C. D.4、下列试剂与环已烯反应得到顺式二醇的是?提交答案A. B.C. D.5、下列反应为碳正离子机理的是提交答案A.B.C.D.6、下列化合物与加成的相对速度顺序最快的是? 提交答案A. B.C. D.7、下列化合物中有顺反异构体的是?提交答案A. 2—甲基—1—丁烯 B.2—甲基—2—丁烯C. 2—甲基—2—戊烯D.3—甲基—2—戊烯8、在过氧化物存在下,与反应,得不到反马氏物的是?提交答案A.2—甲基—2—丁烯 B.1—戊烯C.2—甲基—1—丁烯D.环已烯9、下列碳正离子最稳定的是,最不稳定的是?提交答案A. B.C. D.二、完成下列反应式.1.答案2.答案3.答案4.答案5.答案6.答案1. 2.7.( )答案 1. 2.8.答案9.答案10.()( )答案1.2.11.答案三、写出下列反应可能机理。
硕士研究生考研专业课复习资料

性,(4)本身。
二、单项选择题(每小题2分,共30分)
1.碳原子数相同时,烃类分子的凝点:()
A、异构烷烃〉环状烃〉正构烷烃
B、正构烷烃〉环状烃〉异构烷烃
C、环状烃〉正构烷烃〉异构烷烃
D、环状烃〉异构烷烃〉正构烷烃
2.油品加热到某一温度时,引火后所生成的火焰5秒钟内不再熄灭,这时油品的最低温度称为:()
C、沉降水D、游离水
7.通常认为液体燃料电导率的最低安全值是()。
A、30pS/mB、50pS/m
C、80 pS/mD、100 pS/m
9.油品的粘压系数( ),弹性流体动压润滑越易实现。
A、越高C、不确定
B、越低D、以上都不是
10.流体动力润滑实现的条件不包括( )
A、一定的相对运动速度
B、流体(液体润滑油)有合适的粘性
2.新鲜催化剂的活性高,平衡剂的活性就高。()
3.催化裂化的气体产品中,烷烃的含量比烯烃高。()
4.喷气燃料中的中性胶质不会引起变色( )
5.金属钝化剂通过与氧化生成的活性中心结合起到抗氧化作用。( )
6.柴油机混合气形成应采用空间雾化混合,不能采用油膜蒸发混合方式。( )
7.喷气燃料银片腐蚀合格,可以认为不含活性硫。( )
7、腐蚀试验是用__________检查液体燃料对金属有无腐蚀性的试
验方法,目的是检查燃料中有无____________,我国标准方法中
的腐蚀试验包括____________和____________。
8、.影响粘着磨损的因素较多,概括起来主要有两个大的方面:一
是;二是。
9、润滑油单剂包括:、抗氧抗腐剂、极压抗磨剂、
C、两摩擦表面形成一定的收敛型间隙
暨南大学814普通生物学2010--2021年考研专业课初试真题

2021年招收攻读硕士学位研究生入学考试试题(A卷)******************************************************************************************** 招生专业与代码:考试科目名称及代码:普通生物学814考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、填空题(每空2分,共20分)1.PCR的一个循环由______、______、______三个基本反应组成。
2.植物细胞中,和是主要的转换能量的细胞器。
3.有氧条件下,细胞呼吸的反应可归纳为3个阶段:、和。
4.传统的分类学是根据来考量物种之间的共祖近度的。
5.事实证明,是推动形成群体间表型分化的一个重要因素。
二、名词解释(每题5分,共30分)1.转录2.细胞凋亡3.第二信使4.光周期5.种子休眠6.实际生态位三、简答题(每题10分,共40分)1.简述动物的多层次结构。
2.试以简图描述细胞的DNA损伤修复系统的切除修复的过程。
3.简述秋水仙素诱导多倍体细胞的原理。
4.什么是生态系统?生态系统包括哪些成分?四、论述题(每题20分,共60分)1.在真核细胞有丝分裂的不同阶段,详述染色体的主要行为和形态改变。
2.什么叫植物细胞全能性?在生产上有何意义?3.地球上有哪些主要的陆地群落类型?其所处环境各有什么特点?2020年招收攻读硕士学位研究生入学考试试题(B卷)******************************************************************************************** 招生专业与代码:考试科目名称及代码:普通生物学814考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
二、填空题(每空2分,共20分)1.真核细胞中,是生物氧化、产生能量的场所,是光合作用的场所,是蛋白质合成的场所。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2011年暨南大学硕士研究生入学考试有机化学考试大纲I、考试目标II、考试形式和试卷结构III、考查范围IV、试题样板I、考试目标暨南大学《有机化学》考试的目标,重点在于考查考生如下几个方面的内容:1、各类有机化合物的命名法、异构现象、结构特征、主要性质、重要的合成方法,以及它们之间的关系。
2、对现代价键理论基本概念的理解,并应用于解释有机化合物基本结构的能力;通过电子效应和立体效应,进一步掌握有机化合物结构与性能的关系。
3、重要的反应历程,如:亲电和亲核取代反应、亲电和亲核加成反应、游离基反应、消除反应等历程。
4、对立体化学的基本知识和基本理论的理解,并能用于解释一些反应的选择性问题。
5、各类重要有机化合物的来源、制法及其主要用途。
II、考试形式和试卷结构一、试卷分数满分为150分二、答题方式答题方式为闭卷、笔试,考生独立完成考试内容。
三、试卷结构有机化合物结构30%结构理论关系30%有机反应30%有机合成设计10%四、试卷题型结构1.命名题(10%)2.写结构式(10%)3.选择题(10%)4.填空题(10%)5.完成反应式(30%)6.简答题(20%)7.设计合成题(10%)III、考查范围【考查目标】一、各类有机化合物的命名法、异构现象、结构特征、主要性质、重要的合成方法,以及它们之间的关系。
二、对现代价键理论的基本概念,并应用于理解有机化合物的基本结构的能力;通过电子效应和立体效应,进一步掌握有机化合物结构与性能的关系。
三、重要的反应历程,如:亲电和亲核取代反应、亲电和亲核加成反应、游离基反应、消除反应等历程。
四、对立体化学的基本知识和基本理论的理解,并能用于理解一些反应的选择性问题。
五、各类重要有机化合物的来源、制法及其主要用途。
第一章绪论【基本内容】一、有机化合物和有机化学二、有机化合物的结构:凯库勒结构式、离子键和共价键、现代共价键理论、共价键的属性三、有机化合物的分类四、有机酸碱的概念:勃朗斯德酸碱理论、路易斯酸碱理论【基本要求】一、了解(理解):有机化合物的分类二、掌握:有机酸碱的概念三、重点掌握:有机化合物和有机化学;有机化合物的结构第二章烷烃和环烷烃【基本内容】第一节烷烃一、同系列和构造异构:同系列和同系物、构造异构二、命名:普通命名法、系统命名法三、结构四、构象:乙烷的构象、丁烷的构象五、物理性质:分之间的作用力、沸点、熔点、密度、溶解度六、化学性质:氧化和燃烧、热裂反应、卤化反应第二节脂环烃一、脂环烃的分类、构造异构和命名二、物理性质三、化学性质:与开链烷烃相似的化学性质、环丙烷和环丁烷的开环反应四、拜尔张力学说五、环烷烃的构象:环丙烷和环丁烷的构象、环戊烷的构象、环己烷的构象【基本要求】一、了解(理解)烷烃的物理性质二、掌握:烷烃的氧化、燃烧和热裂反应三、重点掌握:烷烃的命名、结构、构象和卤代反应及机理;自由基的概念。
四、了解(理解):环烷烃的物理性质五、掌握:脂环烃的分类、环烷烃的化学反应;环丙烷、环丁烷、环戊烷和六元环的环烷烃构象六、重点掌握:环烷烃、桥环和螺环的命名;脂环烃的构造异物;环己烷的构象、a键和e键的概念;环烷烃的化学性质第三章立体化学基础【基本内容】一、对映异构:平面偏振光和比旋光度、对映异构体和手性、对映异构体的表示方法、构型的命名、对映异构体的物理性质、外消旋体、非对映异构体和内消旋体、构象异构和构型异构二、环烷烃的立体异构:几何异构和对映异构、一取代环己烷的构象、二取代环己烷的构象三、聚集二烯烃的立体异构四、十氢萘的立体异构五、对映异构体的合成及化学:手性中心的产生、外消旋体的拆分、对映异构体与手性试剂的反应、手性分子在反应中的立体化学【基本要求】一、了解(理解):偏振光的有关概念;外消旋体拆分;手性分子在反应中的立体化学二、掌握:手性中心的产生三、重点掌握:对映异构体和手性的概念;对映异构体的表示方法及构型的命名;对映异构体的物理性质;外消旋体、内消旋体的概念;构象异构和构型异构第四章卤代烷亲核取代反应【基本内容】一、分类和命名二、结构三、物理性质四、化学性质:亲核取代反应、消除反应、还原反应、有机金属化合物的形成五、乙烯型和烯丙型卤代烃六、多卤烷和氟代烷【基本要求】一、了解(理解):物理性质;多卤代烷和氟代烷二、掌握:卤代烷的分类;亲和取代和消除反应的竞争;卤代烷的还原反应三、重点掌握:卤代烷的分类、命名、结构;亲核取代反映、机理及影响因素;消除反应及消除反应的Saytzeff规则;消除反应机理;E2消除的立体化学第五章醇和醚【基本内容】第一节醇一、分类和命名二、结构和物理性质三、化学性质:一元醇的化学性质、二元醇的化学性质(氧化反应、频哪醇重排)四、制备:由烯烃制备、卤烃水解、格氏试剂与醛、酮加成、水解制备1º、2 º、3 º醇第二节醚和环氧化合物一、醚的分类和命名二、醚的结构和物理性质三、醚的化学性质:详盐的形成、醚键的断裂、自动氧化四、醚的制备:醇分子间脱水、威廉姆逊合成法五、冠醚六、环氧化合物:环氧化合物的结构、环氧化合物的反应七、硫醇和硫醚:命名、硫醇的性质、硫醚的性质【基本要求】一、了解(理解):硫醚二、掌握:物理性质;醇与HX反应机理;取代酚酸性的解释;Claisen重排机理;酚的氧化反应;醚的自动氧化、冠醚三、重点掌握:醇、酚、醚的命名、结构;氢键的概念;一元醇与Na的反应;取代反应、脱水反应,生成硫酸酯,醇的氧化(Sarrett试剂、Jones试剂、活性MnO2、Oppenauer氧化、KMnO4、K2Cr2O7/H2SO4);二元醇的氧化反应和频哪醇重排;酚的酸性;酚芳环上的取代反应;酚酯的形成和Fries重排;酚醚的形成和Claisen重排;醚键的断裂和详盐的形成;环氧化合物的开环反应及方向。
醇、酚、醚的制备方法;硫醇和硫醚的性质。
第六章烯烃【基本内容】一、结构二、同分异构:构造异构、顺反异构三、命名四、物理性质五、化学性质:催化加氢、亲电性加成反应、自由基加成反应、硼氢化反应、氧化反应、a氢的卤代反应、聚合反应六、制备:炔烃还原、醇脱水、卤代烷脱卤代氢【基本要求】一、了解(理解):烯烃的物理性质、聚合反应二、掌握:过酸氧化、硼氢化反应机理、自由基加成反应机理三、重点掌握:烯烃的结构、命名;顺反异构体及其构型标记法、烯烃的催化加氢;亲电加成反应(加HX,加X2,加H2SO4,加HOX,硼氢化反应);亲电加成反应机理(加X2,加HX);亲电加成反应的马氏(Markovnikov)规则;烯烃的氧化反应(被KMnO4氧化,臭氧化);a-氢的卤代反应第七章烯炔烃和二烯烃【基本内容】一、炔烃:结构、同分异构和命名;物理性质、化学性质、制备二、二烯烃:分类和命名、公轭二烯烃【基本要求】一、了解(理解):超共轭效应的概念二、掌握:二烯烃的分类;物理性质三、重点掌握:炔烃、共轭二烯烃的结构、命名;炔烃的化学性质(炔氢的反应,碳碳键的还原反应,亲电加成反应);共轭二烯烃的1,2和1,4加成;乙烯型卤烃和烯丙型卤烃;p-π共轭第八章芳烃【基本内容】一、苯及其同系物:苯的结构;苯衍生物的同分异构、命名和物理性质;苯的亲电取代反应及其机理;一取代苯的亲电取代反应的活性和定位规律;苯的其他反应;烷基苯侧链的反应;卤代芳烃二、多环芳烃和非苯芳烃:稠环芳烃、联苯、非苯芳烃及休克尔规则【基本要求】一、了解(理解):苯的分子轨道模型,蒽和菲的反应二、掌握:苯的加成、氧化反应;共振论对亲电取代反应定位规律的解释;物理性质;萘的氧化反应三、重点掌握:芳香性的概念;苯的结构;苯的同分异构及命名;苯的亲电取代反应(卤代、硝化、磺化、F.C反应);亲电取代反应机理;芳环上亲电取代反应定位规律;萘的结构、命名;萘的亲电取代反应;联苯的立体化学;修克尔规则第九章醛和酮【基本内容】一、醛和酮的结构和命名二、醛和酮的物理性质三、醛和酮的化学性质:亲核加成反应、a活泼氢的反应、氧化和还原反应、其它反应四、醛和酮的制备:官能团转化法、向分子中直接引入羰基五、不饱和醛、酮:α,β-不饱和醛、酮的反应、烯酮六、醌类化合物:双键的加成反应、羰基与氨衍生物的反应、1,4-加成反应、1,6-加成反应【基本要求】一、了解(理解):醛、酮与水的加成,羟醛缩合反应的酸催化机理,醌的1,6加成;聚合反应二、掌握:碱催化卤仿反应机理;醌的性质;烯酮的反应;醌的命名三、重点掌握:醛、酮的结构、命名、亲核加成反应及活性(与HCN、NaHSO3、RMgX、氨的衍生物的加成);亲核加成反应的机理;羟醛缩合反应(分子间,分子内及交叉羟醛缩合)及碱催化机理;氧化反应(KMnO4/H+;Tollens试剂,Fehing试剂)和还原反应(Clemmensen还原,Wolff-kishner-黄鸣龙还原,催化氢化,Meewein-Ponndorf还原;金属氢化物还原及立体化学;酮的双分子还原);Witting反应;醛酮的制备方法;a b不饱和醛酮的1,4和1,2加成;Michael加成;Diels-Alder反应。
第十章酚和醌[基本内容]一、酚的结构、命名、物理性质、化学性质以及制备二、醌的分类、命名、制备以及对苯醌的反应[基本要求]一、了解酚和醌的制备二、熟悉酚和醌的结构、命名、物理性质以及对苯醌的反应三、掌握酚和醌的化学性质第十一章羧酸和取代羧酸【基本内容】一、分类和命名二、物理性质三、结构和酸性及电性效应小节四、化学性质:成盐反应、羧基中羟基的取代反应、还原反应、a氢的反应、脱羧反应、二元酸的热解反应五、制备:氧化法、腈水解法、格氏试剂的羧化、丙二酸酯合成法、不饱和羧酸的制备六、取代羧酸:卤代酸和羟基酸的化学反应、羟基酸的制备、酚酸、氨基酸、多肽和蛋白质【基本要求】一、了解(理解):a-H被卤代反应机理;氨基酸的显色机理,多肽及蛋白质;二、掌握:取代芳酸酸性的解释,物理性质三、重点掌握:羧酸及取代羧酸的命名;羧基的结构;影响羧酸酸性的因素;羧酸衍生物的形成反应,酯化反应机理;卤代酸、羟基酸、氨基酸的化学反应;b-羰基酸的脱羧;二元酸受热时的变化规律;羧酸的制备方法;Kolbe-Schmitt的反应第十二章羧酸衍生物【基本内容】一、结构和命名二、物理性质三、化学性质:水解反应、醇解反应、氨解反应、与有机金属化合物的反应、还原反应、酯羧合反应、达参反应、酰胺的特性四、制备:由羧酸制备、由羧酸的衍生物间相互转化制备、由酮肟重排制备N-取代酰胺【基本要求】一、了解(理解):Darzen反应机理;油脂、原酸酯二、掌握:物理性质;碳酸衍生物;酯的酸性水解机理三、重点掌握:羧酸的衍生物的结构、命名;羧酸的衍生物的水解、醇解、氨解反应及反应活性;酯碱性水解反应机理;酯与格氏试剂的加成;羧酸的衍生物的还原反应(氢化锂铝还原,Rosenmund还原,Bouveault-Blanc还原);第十三章碳负离子反应【基本内容】一、α-氢的酸性和互变异构二、缩合反应:羟醛缩合型反应,酯缩合反应三、β-二羰基化合物的烷基化、酰基化及在合成中的应用:乙酰乙酸乙酯,丙二酸二乙酯四、烯胺的烷基化和酰基化反应【基本要求】一、掌握羰基α–取代反应及反应机理。
