化学专业III期修改版
臭氧氧化活性染料及其降解产物毒性研究

Y 8 作图, 结果得到直线关系 ( $& W #K FJ& ) , 由直线 ,% 如图 % 所 斜率可求得速率常数 3 为 #K #%JF DMN , 示。由此可见, 臭氧氧化染料可以看作一级反应动 力学反应, 这就从实验上验证了式 (&) 所表达的动 力学模型。
!" 实验
! 0 !" 试剂 活性艳蓝 *1 , 2 和活性黑 活性艳红 *+ , "-、 *1 , - 均购自德国巴斯夫 ( -345, 现 67489: ) , 质量 )#$ , ;($ 。用二甲基甲酰胺 < 丙 分数分别为 )&$ , /ABC 级) 提纯染料。染料的质量浓度 酮法 ( =>:?@, 为 &## DE < B, 所有染料均在 F( G 回流 " H 进行水 解。发光菌 ,)-.)/ 0)1’2%.) 购自德国 6:0 B31I+ 公 司。所有溶液均用超纯水 ( %JK & =!・?D) 配制。 ! 0 #" 仪器 实验装置由臭氧发生器 ( 德国, +:LMN 49NO>: ) 、 反应管、 尾气吸收装置、 臭氧分析仪及流量计组成, 所有连接管线均采用聚四氟乙烯管。 P9:M9N C9:7 % 分光光度计 ( P9:M9N, Q43 ) ,BQ=R48ST "## 测光 仪 ( 德国, 6:0 B31I+ ) 。 ! 0 $" 发光菌毒性检测 将冷冻的海洋性菌种 ,)-.)/ 0)1’2%.)R 按照 6R1 待测样 R4U +1 %%"’J —& 标准方法配制成菌悬液, 品用浓度为 % DSV < B 的 19U/ 和 % DSV < B 的 /CV 调 节 ./ W ;K # 左右, 按 6R1 "J’%& B"’ < "’% 标准稀释 成所需质量浓度。本实验的温度控制在 %( G 左右。 由于染料本身带有一定的颜色, 对发光菌毒性测试 有干扰, 因此, 在实验之前须进行颜色校正。作者采 用发光菌发光强度抑制值来评价溶液毒性大小。
化工专业调研报告

化工专业调研报告目录一、内容综述 (2)1. 调研背景与意义 (3)2. 研究目的与问题 (3)3. 研究方法与数据来源 (4)二、国内外化工行业发展现状 (5)1. 国际化工市场概况 (7)2. 国内化工行业发展趋势 (9)3. 化工产业结构分析 (10)4. 技术创新与环保政策影响 (11)三、化工专业人才培养现状 (12)1. 专业设置与课程体系 (14)2. 教育资源投入情况 (15)3. 学生就业情况与职业发展 (17)4. 师资队伍建设与教学水平 (18)四、化工专业教育质量评估 (18)1. 教学质量评价标准与方法 (19)2. 校内实践教学环节实施情况 (20)3. 学生实习实训效果分析 (22)4. 学位论文质量与科研成果 (23)五、化工专业教育改革与发展建议 (24)1. 明确专业定位与培养目标 (25)2. 优化课程体系与教学内容 (26)3. 加强实践教学与创新能力培养 (27)4. 提升师资队伍水平与教学研究能力 (28)5. 深化产教融合与社会服务能力 (29)六、结论与展望 (30)1. 调研总结 (30)2. 发展前景与挑战分析 (32)3. 对未来研究的建议 (33)一、内容综述本次化工专业调研报告旨在全面分析化工行业的现状、发展趋势以及面临的挑战,为相关企业和政策制定者提供决策依据。
报告首先概述了化工行业的整体规模、主要产品及市场分布,然后深入探讨了化工行业的产业结构、技术创新、节能减排等方面的情况。
在行业规模方面,随着全球经济的复苏和新兴市场的崛起,化工行业正迎来前所未有的发展机遇。
行业内的竞争也日趋激烈,企业需要不断提升自身的竞争力以适应市场变化。
在产业结构方面,报告分析了化工产品的种类、质量和附加值等方面。
未来化工行业的发展将更加注重绿色、低碳、高附加值的新型材料和产品,以满足市场需求。
在技术创新方面,报告强调了科技创新在化工行业发展中的核心地位。
企业应加大研发投入,积极引进国内外先进技术,提高自主创新能力,以实现产业升级和可持续发展。
化学工程与工艺专业培养方案-北京理工大学化学与化工学院

化学工程与工艺专业培养方案前言北京理工大学化学工程与工艺专业自2013级学生开始执行“2013版北京理工大学化学工程与工艺专业本科教学培养方案”。
根据学校安排,于2015年10月启动2016版培养方案制订工作,通过调研和广泛征求意见,于2016年8月在化学与化工学院本科培养方案研讨会上通过,从2016级开始执行2016版培养方案。
这一培养方案对2013修订版本科教学培养方案的基本框架进行了修改,新增了毕业要求对专业培养目标的支撑矩阵和每个培养环节与毕业要求的对应关系。
一、培养目标化学工程与工艺专业培养具有良好的人文素质和工程职业道德,具有扎实的数学、物理、化学及化工知识基础,具有分析和解决复杂化学工程问题的基本能力,了解化学工程与工艺专业及相关领域国内外发展现状及趋势,具有研究开发和设计化工特别是精细化工领域新产品、新工艺的能力,具有良好的团队协作和组织管理能力的工程技术人才。
毕业后5年左右在化工及相关专业领域具备独立从事:1)化工产品特别是精细化学品的设计与开发;2)化工生产工艺设计;3)生产技术管理,技术文件制定;4)生产过程模拟优化、革新改造。
二、毕业生基本要求能够将数学、物理、化学等专业基础知识用于分析和解决复杂化学工程问题,以及能够应用上述专业知识的基本原理,识别、表达、并通过文献查询分析复杂化学工程问题,以获得有效结论。
能够设计针对复杂化学工程问题的解决方案,设计满足特定需求的化工系统、化工单元操作或工艺流程,并能够在设计环节中体现创新理念,考虑社会、法律、环境等因素。
具备能够根据化学和化工基本原理并采用科学方法对工程实践活动中涉及的复杂化学工程问题进行研究的能力,并能够对研究结果进行分析与解释数据,通过综合得到合理有效的结论。
能够针对复杂化学工程技术问题,开发、选择与使用恰当的技术、资源、现代工程工具和信息技术工具,包括对复杂工程问题的预测与模拟,并能够理解其局限性。
能够基于化学工程与技术专业相关背景知识进行合理分析,评价工程设计与复杂技术问题解决方案对社会、健康、安全、法律以及文化的影响,并理解应承担的责任。
化学专业教学培养方案

化学专业教学培养方案一、专业特色化学专业依托华东理工大学国家一流学科—化学学科,在化学及相关学科前沿领域的科学研究、化学产品合成和配方设计、化学产品检验分析和性能测试等方面形成特色,学生毕业后可在教育、科研院所、医药、材料、能源、生物、环境、化工、食品和日用化学、金融贸易等领域的各类企事业单位就业,或进入化学及相关学科深造,成为研究型专业人才。
二、培养目标化学专业以培养一流的化学及相关领域的复合型专业人才为目标,毕业学生应具有扎实的化学基础理论知识和专业知识,以及数、理、外语和计算机等公共基础知识和技能,具备一定的科学研究、产品开发和实践创新能力,拥有坚实的家国情怀、良好的人文素养、强烈的社会责任感、高尚的道德情操、广阔的国际视野和流畅的国际交流能力。
要求五年以上的毕业生:➢能够从事化学及相关领域科学研究、技术开发、经营管理等工作,适应独立和团队工作环境。
➢以社会责任感、法律、道德修养、安全与环境意识和经济等方面的视角理解和解决多学科的问题。
➢在终身学习、专业发展、竞争能力和领导能力上表现出担当和进步,在化学及相关领域具有职场竞争力。
三、毕业要求本专业学生毕业时应当达到普通高等学校本科专业认证标准规定的能力,共有9条:1. 具有人文底蕴、科学精神、职业素养和社会责任感,了解国情社情民情,践行社会主义核心价值观;2. 具有扎实的基础知识和化学专业知识,掌握必备的化学研究方法,了解化学及相关领域最新动态和发展趋势;3. 具有批判性思维和创新能力。
能够发现、辨析、质疑、评价化学及相关领域现象和问题,表达个人见解;4. 有解决复杂问题的能力。
能够对化学及相关领域复杂问题进行综合分析和研究,并提出相应对策或解决方案;5. 有信息技术应用能力。
能够恰当应用现代信息技术手段和工具解决实际问题;6. 具有较强的沟通表达能力。
能够通过口头和书面表达方式与同行、社会公众进行有效沟通;7. 具有良好的团队合作能力。
能够与团队成员和谐相处,协作共事,并作为成员或领导者在团队活动中发挥积极作用;8. 具有国际视野和国际理解能力。
定量化学分析简明教程第3版答案

⎛1 ⎞ n⎜ KHC 2 O 4 ⋅ H 2 C 2 O 4 ⎟ = n( NaOH) ⎝3 ⎠
氧化还原反应中:
V (KMnO 4 ) =
第 2 章 习题参考答案
2.2 测定试样中 CaO 的质量分数时,得到如下结果:35.65%、35.69%、35.72%、35.60%。问: (1)统计处理后的分析结果应如何表示? (2)比较 95%和 90%置信度下总体平均值的置信区间。 答案: (1) 结果表示为:n=4, x = 35.66% ,s=0.052% (2) 1 − α = 0.95 ,则 α = 0.05 , t 0.05 (3) = 3.18
4
答
案
2.1 测定某样品中氮的质量分数时,六次平行测定的结果是 20.48%、20.55%、20.58%、20.60%、 20.53%、20.50%。 (1) 计算这组数据的平均值、 中位数、 平均偏差、 标准差、 变异系数和平均值的标准差; (20.54%, 20.54%, 0.12%, 0.037%, 0.046%, 0.22%, 0.019%) (2)若此样品是标准样品,其中氮的质量分数为 20.45%,计算以上测定结果的绝对误差和相对 误差。(+0.09%, 0.44%)
∴σ1 与σ2 无显著差异。 (2)用 t 检验法检验μ1 是否等于μ2 假设μ1=μ2
课 后
(1)用 F 检验法检验σ1=σ2 是否成立(α =0.10) 假设σ1=σ2
F计算
2 s大 0.9 2 = 2 = = 2.2 < F表 = F0.05 (4,3) = 9.12 s小 0.6 2
度(c)的 Na2C2O4 溶液?要配制 100mL 溶液,应称取 Na2C2O4 多少克?
2019年《5年高考3年模拟》B版化学课标III精编教师用书:专题二十三 有机化学基础PDF版含解析

新制
Cu( OH) 2 悬 浊 液、 O2 等
������������
氧化
���O���������
羧
O
能电离产 ①具有酸的通性
������
R C OH
酸
CH3 C OH
生 H+
②酯化反应
������������������������������
������������������������ ������������������������
三、四 等———指 相 同 取 代 基 或 官 能 团 的 个 数; ③ 甲、 乙、 丙、
丁———指主链碳原子个数分别为 1、2、3、4;④烯、炔、醛、酮、酸、
酯———指物质类别。
2.相对分子质量的测定———质谱法
质荷比( 分子离子、碎片离子的相对质量 与其电 荷的比 值)
最大值即为该有机物的相对分子质量。
3.分子结构的鉴定
(1) 化学方法:利用特征反应鉴定出官能团,再制备它的衍
生物进一步确认。
( 2) 物理方法
①红外光谱:分子中化学键或官能团对红外线发生振动吸
收,不同化学键或官能团吸收频率不同,在红外光谱图上处于不
同的位置,从而获得分子中含有何种化学键或官能团的信息。
②核磁共振氢谱:吸收峰个数等于不同化学环境的氢原子
对应学生用书起始页码 P259
续表
类 通式 / 官能团
别
代表物
分子结 构特点
主要化学性质
������
������ ������������
酚
������
������������ O���H���
������
������
������������
化学专业英语---化合物的命名

24
5. Acids
(1). Per-, hydro-,normal acid (its salt-ate,-ide)
Acid = Central element’s root -ic + acid
举例: PH3: phosphine或phosphane SbH3: stibine或stibane CH4: methane B2H6: diborane
AsH3: arsine或arsane BiH3: bismuthane SiH4: silane
17
无氧酸
命名规则:hydro-词根-ic acid 举例: HCl: hydrochloric acid H2S : hydrosulfuric acid
VIA
VIIA
0
He Helium
O Oxygen
F Fluorine
Ne Neon
S Sulfur
Cl Chlorine
Ar Argon
Se Selenium Br Bromine
Kr Krypton
Te Tellurium
I Iodine
Xe Xenon
Po Polonium At Astatine
7
2.Multivalence ions
Cation’s name = Element(N)
For example:
Fe2+ Iron(II)
or Ferrous
Fe3+ Iron(III)
or Ferric
化学专业英语译文

化学专业英语(修订版)译文目录:1、THE ELEMENTS AND THE PERIODIC TABLE(元素和周期表)........................................6、THE CLASSIFICATION OF INORGANIC COMPOUNDS(无机化合物的分类).................................................................................................................................................................................7、The Nomenclature of Inorganic Compounds(无机化合物的命名) ....................................................9、The coordination complex(配位化合物) ...........................................................................................10、Alkanes(烷烃) ..............................................................................................................................................11、Unsaturated Compounds不饱和化合物...............................................................................................12、The Nomenclature of Cyclic Hydrocarbons(环烃的命名) ...........................................................13、Subsitutive Nomencalture(取代基命名法)......................................................................................14、The Compounds Containing Oxygen(含氧化合物).......................................................................15、Preparation of A Carboxylic Acid by the Grignard Method (格式法制备羧酸) .....................................................................................................................................................18、Synthesis of alcohols and design of organic synthesis (醇的合成及有机合成的设计)........................................................................................................................................22、Polymers(聚合物).................................................................................................................................1、THE ELEMENTS AND THE PERIODIC TABLE(元素和周期表)在原子核中质子的数目被称为原子序数,或质子数,Z。
_化生丨广东省广东实验中学2023届高三下学期第三次阶段考试化生试卷及答案

广东实验中学2023届高三级第三次阶段考试化学本试卷分选择题和非选择题两部分,共10页,满分100分,考试用时75分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.选择题每小题选出答案后,用2B铅笔把答题卷上对应题目的答案标号涂黑:如需改动,用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液,不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将答题卷收回。
相对原子质量H=1O=16C1=35.5Co=59Zn=65第一部分选择题(共44分)一、选择题:本题共16小题,共44分。
第1~10小题,每小题2分;第11~16小题,每小题4分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.广东人爱“饮茶”,毛泽东有“饮茶粤海未能忘”诗句。
下列说法错误的是A.茶饼浸泡前要掰成小块,可使之更快浸出茶香B.使用沸水泡茶,可加速茶叶中物质的溶解C.茶叶封装时常附带一包铁粉,可减慢茶叶的氧化D.某温度下测得茶水的pH=6.6,则该茶水一定呈酸性2.化学与生活息息相关。
下列叙述错误的是A.热的碳酸钠溶液可用于去除餐具的油污B.明矾和二氧化氯均可作净水剂,且净水原理相同C.硫酸钡可用于胃肠X射线造影检查D.电热水器用镁棒防止内胆腐蚀,采用的是牺牲阳极保护法3.化学与生活、科技及环境密切相关。
下列说法正确的是A.温室气体是形成酸雨的主要物质B.过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO3溶液的方法解毒C.食品袋中放置的CaO可直接防止食品氧化变质D.太阳能电池阵使用的材料是半导体,其主要成分是SiO24.设N A为阿伏加德罗常数的值。
下列说法不正确的是A.标准状况下,22.4L CCl4中,原子数大于5N AB.71g Cl2与足量烧碱溶液反应制备漂白液,转移的电子数为N AC.1L0.1mol/L Na[Ag(CN)2]溶液中CN-的数目为0.2N AD.1mol C2H6O中含碳氢单键数可能为5N A5.下列方案能达到实验目的是A.用水萃取CCl4中的溴B.用排饱和石灰水集气法收集Cl2C.用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体D.用饱和的Na2CO3溶液除去Cl2中混有的HCl6.下列反应的离子方程式正确的是A.Na与水反应:Na+H2O=Na++OH-+H2↑B.硫化钠水解反应:S2-+H3O+HS-+H2OC.稀醋酸滴入NaOH溶液中:H++OH-=H2OD.氯氧化钠溶液中通入足量二氧化碳:CO2+OH-=HCO3-。
化学专业本科人才培养方案

★化学专业本科人才培养方案化学专业本科人才培养方案一、专业培养目标及基本要求培养目标:本专业培养掌握化学学科以及教师教育的基本理论、基本知识和基本技能,具备良好的人文与科学素质,强烈的社会责任感,具有创新意识、终身学习、实践与研究的能力,乐教、懂教和善教的服务于基础教育的化学教师。
基本要求:1.热爱祖国,遵纪守法,诚实守信;努力学习和掌握科学的世界观和方法论;2.学习和掌握本专业所需的通识课程数学、物理、计算机等相关学科的基本知识;3.学习和掌握化学专业课程和教师教育课程的基本理论、基本知识和基本技能,了解熟悉本学科的研究前沿、应用前景和相关学科的知识;4.学习教育创新理论,掌握“以生为本”和“促进学生全面发展”的先进的教学理念和教学方法,具有创新意识和终身学习的能力;5.掌握一门外国语和现代教育技术,具有信息的获取与处理能力,从事科学研究与教学研究的能力;6.具有健康的体魄、良好的心理素质,激励自己向研究型、学者型、专家型教师的方向发展。
二、主要课程普通化学原理、无机化学、分析化学、有机化学、物理化学、结构化学、仪器分析、化工基础、化学信息学及上述课程的实验课程、教育学、心理学、化学教学论等课程。
三、学制4年四、授予学位理学学士五、教学时间分配表项目周数学分各学期分配情况(周数)备注一二三四五六七八军事训练 3 3 3 0 0 0 0 0 0 0 学年论文0 0 0 0 0 0 0 0 0 0 教育实习或毕业实习8 8 0 0 0 0 0 0 8 0 见习 4 4 0 1 1 1 1 0 0 0 毕业论文(设计)16 16 0 0 0 0 0 0 8 8 复习考试12 0 2 1.5 2 1.5 2 1.5 1 0.5 入学及毕业教育 2 0 0.5 0 0 0 0 0 0 1.5 学年总结 1.5 0 0 0.5 0 0.5 0 0.5 0 0 机动 4.5 0 0.5 0 1 0 1 1 1 0 课程教学113 157 15 17 17 17 17 17 3 10 小计164 188 21 20 21 20 21 20 21 20 六、课程教学学时、学分分布表类别学期课类一二三四五六七八总计百分比%学时通识教育必修课213 201 136 153 0 0 0 0 703 24 专业类必修课188 356 442 225 272 118 0 0 1601 54.6 专业类选修课计划开设0 0 0 136 359 655 102 187 1439学生应修0 0 0 34 85 238 0 68 425 14.5 通识教育选修课0 0 0 51 51 51 0 51 204 7 小计401 557 578 463 408 407 0 119 2933 100学分通识教育必修课13 11 8 11 0 0 0 0 43 27.4 专业类必修课10.5 17.5 21.5 11 13 4 0 0 77.5 49.4 专业类选修课计划开设0 0 0 8 20 37 6 11 82学生应修0 0 0 2 5 13.5 0 4 24.5 15.6 通识教育选修课0 0 0 3 3 3 0 3 12 7.6小计23.5 28.5 29.5 27 21 20.5 0 7 157 100 注:专业类必修课指学科基础必修课与专业必修课;专业类选修课指学科基础选修课与专业选修课七、课程计划表课程类别课程号课程名称开课学期学分学时分配表周学时先行课考试方式双学位课素质课程课程课类授课实验课外通识教育课必修课31001001 计算机基础 1 3 51 0 34 4 1 理31004001 高等语文 1 3 51 0 0 4 1 文33001100 大学体育1 1 1 30 0 0 2 1 体34000021 思想道德修养与法律基础 1 3 48 0 0 3 1 文35000011 大学英语阅读与写作1 1 2 42 0 0 3 1 文35000012 大学英语听力与口语1 1 2 15 0 15 1 1 文31001003 高级程序语言设计 2 3 51 0 24 3 1 理33002100 大学体育2 2 1 34 0 0 2 33001100 1 体34000022 中国近现代史纲要 2 2 24 0 10 3 1 文35000021 大学英语阅读与写作2 2 2 51 0 0 3 35000011 1 文35000022 大学英语听力与口语2 2 2 17 0 17 1 35000012 1 文33003100 大学体育3 3 1 34 0 0 2 33002100 1 体34000023 马克思主义基本原理 3 3 34 0 17 2 1 文35000031 大学英语阅读与写作3 3 2 51 0 0 3 35000021 1 文35000032 大学英语听力与口语3 3 2 17 0 17 1 35000022 1 文33004100 大学体育4 4 1 34 0 0 2 33003100 1 体34000025毛泽东思想和中国特色社会主义理论体系概论4 6 51 0 51 3 1 文35000041 大学英语阅读与写作4 4 2 51 0 0 3 35000031 1 文35000042 大学英语听力与口语4 4 2 17 0 17 1 35000032 1 文选修课学生至少修取12个学分,其中:线性代数B(第二学期开设)2学分、概率统计B(第三学期开设)2个学分、文科类的课程4个学分、艺体类课程2个学分、其余2个学分由学生自主决定选择。
石大远程奥鹏-化工设计概论-第三阶段在线作业正确答案

B、浮头式换热器
C、板壳式换热器
D、套管式换热器
E、蛇管式换热器
正确答案:C
6. 哪个是卧式容器的支座
A、支承式支座
B、悬挂式支座
C、裙式支座
D、鞍式支座
正确答案:D
7. 哪个不是车间装置布置的发展趋势
A、露天化
B、大型化
C、集中化
D、定型化
E、露天化
正确答案:B
8. 哪个不是管件的连接方式
A、能量基准
B、时间基准
C、质量基准
D、体积基准
E、干湿基准
正确答案:BCDE
21. 气体标准状态的温度和压力是
A、T=273.15 K
B、T=275.15 K
C、P=0.1013 MPa
D、P=1.013 MPa
E、P=0.2013 MPa
正确答案:AC
22. 过程物料平衡时对系统的分析内容有
A、确定物料平衡方程式
B、确定物流约束式
C、确定设备约束式
D、确定变量
E、确定设计变量
正确答案:ABCDE
23. 反应过程物料衡算方法有
A、节点衡算法
B、元素平衡法
C、组分质量衡算法
D、反应速率衡算法
E、直接计算法
正确答案:ABDE
24. 简单过程物料衡算是指哪些过程
A、混合单元
B、循环过程
C、精馏单元
D、弛放过程
E、旁路
18. 化工过程整合的要求有
A、过程的安全性
B、过程的可靠性
C、过程的环保性
D、过程的经济性
E、过程的多样性
正确答案:ABCD
19. 在物理过程中,存在哪些物料衡算式
实验5 三草酸合铁(III)酸钾的制备和组成测定(1)

齐齐哈尔大学实验报告题目:三草酸合铁酸钾的制备和组成测定学院:_化学与化学工程学院__专业班级:__化学091班__学生姓名:_____李锦娟_同组者姓名徐智丽成绩:___________2012年11 月20日实验5三草酸合铁酸钾的制备和组成测定实验目的:掌握合成K3Fe[(C2O4)3].3H2O的基本原理和操作技巧加深对铁(Ⅲ)和铁(Ⅱ)化合物性质的了解掌握容量分析等基本操作。
实验原理:以硫酸亚铁铵为原料,与草酸在酸性溶液中先制得草酸亚铁沉淀,然后再用草酸亚铁在草酸溶钾和草酸存在下,以过氧化氢为氧化剂,得到铁草酸配合物。
主要反应为(NH4Fe(SO4)2+H2C2O4+2H2O=FeC2O4•2H2O+(NH4)2SO4+H2SO42FeC2O4.2H2O+H2O2+3K2C2O4+H2C2O4=2K3[Fe(C2O4)3]•3H2O改变溶剂极性并加少量盐析剂,可析出绿色单斜晶体纯的三草酸合铁酸钾,通过化学分析确定配离子的组成。
用KMnO4标准溶液在酸性介质滴定测得草酸根的含量。
Fe3+含量可先用过量锌粉将其还原为Fe2+,然后再用KMnO4标准溶液滴定而测定,其反应式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O2MnO4-+5C2O42-+16H+=2Mn2++10CO2+8H2O实验步骤:1.2 草酸亚铁的制备1.2.1 称取5g硫酸亚铁铵固体放在250ml烧杯中,然后加15ml蒸馏水和5~6滴1mol/LH2SO4。
1.2.2 加热溶解后,再加入25ml饱和草酸溶液(150g/L),加热搅拌至沸,同时不断搅拌,防止飞溅。
1.2.3 维持微沸4min后,停止加热,取少量清液于试管中,煮沸,根据是否还有沉淀产生判断是否还需加热,证实反应基本完全后,将溶液静置。
1.2.4 待黄色晶体FeC2O4•2H2O沉淀后倾析,弃去上层清液,用总量20mL蒸馏水分三次用倾泻法洗涤晶体,搅拌并温热,静置,弃去上层清液,即得黄色晶体草酸亚铁。
无机化学(化学工程)课程教学大纲

无机化学课程教学大纲课程名称:无机化学英文名称:Inorganic Chemistry课程编号:x2030471学时数:56其中实践学时数:0 课外学时数:0学分数:3.5适用专业:化学工程一、课程简介本课程是化学工程专业学生的专业基础课。
本课程讲授了化学反应原理、物质结构的基础理论、元素、单质及无机化合物的基本知识;是后续化学课程及相关专业课程学习的基础。
通过对本课程的学习,学生掌握化学反应原理、物质结构的基础理论、元素、单质及化合物的基本知识;培养学生自学能力,使之具有自学无机化学书刊的能力;培养学生学以致用的能力,使之具有解决一般无机化学问题的能力。
二、课程目标与毕业要求关系表三、课程教学内容、基本要求、重点和难点(一)气体及热化学基础1.要求学生熟练掌握理想气体状态方程式及其应用、气体分压定律及其应用、盖斯定律及其应用;了解分压、体系、环境、状态、功、热及热力学能等概念;理解热力学第一定律,理解焓、焓变的概念,掌握状态函数和标准摩尔生成焓的概念。
2.重点:状态函数的概念及特点,标准生成焓的概念,理想气体状态方程式和分压定律的应用,运用盖斯定律和标准生成焓计算反应热。
3.难点:状态函数、焓及标准生成焓的理解。
(二)化学反应速率和化学平衡1.要求学生了解化学反应速率,基元反应和反应级数的概念,理解浓度对反应速率的影响和温度对反应速率的影响,熟练掌握质量作用定律,了解速率理论,并能用活化能和活化分子的概念说明浓度、温度和催化剂对反应速率的影响,了解影响反应速率的因素。
要求学生理解可逆反应与化学平衡的概念,掌握标准平衡常数ΘK 及其应用,掌握化学平衡的移动的规律,掌握热力学第二定律及热力学第三定律,掌握有关化学平衡组成的计算。
要求学生熟练掌握标准摩尔反应焓变、标准摩尔反应熵变和标准摩尔反应吉布斯函数变的关系,熟练掌握ΘK 与Θ∆m r G 的关系,熟练掌握Θ∆mr G 和m r G ∆的计算方法,熟练掌握转变温度的计算方法,熟练掌握吉布斯函数判据,熟练掌握通过计算判断反应方向和反应程度的方法。
化学版科目三-概念解析以及定义

化学版科目三-概述说明以及解释1.引言1.1 概述概述:化学是一门研究物质的性质、组成、结构、变化规律以及物质之间相互作用的科学。
它在我们生活中随处可见,无论是食品、药品、化妆品还是日常用品,都离不开化学的应用。
化学作为一门学科,不仅仅是理论知识的学习,更重要的是实际操作和实验技能的掌握。
本文将介绍化学知识的概述、实验技能的培养以及化学安全常识的重要性,帮助读者更加全面地了解化学,提高化学实验技能,培养安全意识,为今后的学习和工作打下坚实的基础。
1.2 文章结构文章结构部分的内容应该是对整篇文章的章节安排和内容概述,引导读者了解全文结构和主题内容。
具体内容可以包括每个章节的标题和简要描述,以及文章的主要论点或讨论重点。
例如:"文章结构部分将包括引言、正文和结论三个部分。
在引言部分,我们将简要介绍化学版科目三的背景和重要性;在正文部分,我们将分别讨论化学知识概述、化学实验技能以及化学安全常识的内容;最后,在结论部分,我们将总结本文的主要观点,并给出学习建议和未来的发展展望。
"1.3 目的本文旨在通过对化学知识的概述、化学实验技能和化学安全常识的介绍,帮助读者全面了解化学科目,提升学习效率和实践能力。
同时,通过对化学知识的总结和学习建议,引导读者更好地掌握化学知识,提高学习成绩。
此外,还展望未来,在化学科目学习的过程中,能够更好地运用所学知识,探索化学领域的更深层次,为未来的学习和工作打下坚实的基础。
2.正文2.1 化学知识概述在化学知识概述部分,我们将学习化学的基本概念和原理。
化学是一门研究物质的性质、结构、组成、变化规律以及与能量的关系的自然科学。
在化学知识概述中,我们将涉及原子结构、化学键、化学反应、物质的分类和特性等基本概念。
通过学习化学知识概述,我们可以更好地理解物质间的相互作用和变化规律,为后续的化学学习打下坚实的基础。
同时,也能够帮助我们更好地理解和应用化学知识于日常生活和实际工作中。
齐齐哈尔大学化学专业实验三草酸合铁(III)酸钾的制备和组成测定

齐齐哈尔大学实验报告题目:三草酸合铁(III)酸钾的制备和组成测定学校:_齐齐哈尔大学___专业班级:___化学072____学生姓名:__________同组者姓名:__________成绩:___________[实验目的]1 掌握合成32432K [Fe(C O )]3H O 的基本原理和操作技术;2 加深对铁(III )和铁(II )化合物性质的了解;3 掌握容量分析等基本操作。
[实验原理]三草酸合铁(III )酸钾(含三个结晶水)为翠绿色单斜晶体,易溶于水且难溶于乙醇,受光易分解。
本实验以硫酸亚铁铵为原料,与草酸在酸性溶液中先制得草酸亚铁沉淀,然后再用草酸亚铁在草酸钾和草酸的存在下,以过氧化氢为氧化剂,得到铁(III )草酸配合物。
主要反应为4242224224242424(NH )Fe(SO )H C O 2H O FeC O 2H O (NH )SO H SO ++==↓++24222224224324322FeC O 2H O H O 3K C O H C O 2K [Fe(C O )]3H O +++==改变溶剂极性并加少量盐析剂,可析出绿色单斜晶体纯的三草酸合铁(III )酸钾,通过化学分析确定配离子的组成。
用高锰酸钾标准溶液在酸性介质中滴定测得草酸根的含量。
3Fe +含量可先用过量镁粉将其还原为2Fe +,然后再用高锰酸钾标准溶液滴定而测得,其反应式为232425Fe MnO 8H 5Fe Mn 4H O +-+++++==++ 22424222MnO 5C O 16H 2Mn10CO 8H O --++++==++ [仪器与实验药品]托盘天平;分析天平;抽滤装置;烧杯;电炉;移液管;容量瓶;锥形瓶;量筒;试管;表面皿;玻璃棒;滤纸;点滴板;恒温水浴槽;恒温干燥箱。
24H SO (3mol/L);24H SO (1mol/L);224H C O (饱和);224K C O (饱和);3KNO (300g/L );乙醇(95%);36K [Fe(CN)](5%);22H O (3%);镁粉;224Na C O ;高锰酸钾。
化学反应工程三级项目

Aspen plus模拟RCSTR和RStoic反应器的操作与计算学院:环境与化学工程学院专业: 11化工工艺学生姓名:苏亮学号: 110110010026指导教师:李建军I化学反应工程三级项目任务书学院:环境与化工学院系级教学单位:化工系学号110110010026学生姓名苏亮专业班级11化工工艺题目题目名称Aspen plus模拟RCSTR和RStoic反应器的操作与计算题目性质理论研究主要内容1.反应器的选型;2.输入输出物料参数的设定;3.物性方法的选择;4.计算收敛过程优化;5.计算结果输出;6.项目报告基本要求写出2000字的报告;报告主体应有反应器基本原理、参数设定、计算过程及计算结果输出、结果与讨论。
参考资料1.《化学反应工程》第三版陈甘棠化学工业出版社2.《化工流程模拟实训--Aspen Plus教程》孙兰义化学工业出版社指导教师:李建军职称:副教授系级教学单位审批:年月日说明:如计算机输入,表题黑体小三号字,内容五号字。
II前言:Aspen Plus是一个生产装置设计、稳态模拟和优化的大型通用流程模拟系统。
Aspen Plus在整个工艺装置的从研发、工程到生产生命周期中,提供了经过验证的巨大的经济效益。
它将稳态模型的功能带到工程桌面,传递着无与伦比的模型功能和方便使用的组合。
利用Aspen Plus可以设计、模拟、故障诊断和管理有效益的生产装置。
Aspen Plus具有最先进的流程收敛方法。
Aspen Plus具有最先进的数值计算方法,能使循环物流和设计规定迅速而准确地收敛。
这些方法包括直接迭代法(Wegstein)、正割法(Secant)、拟牛顿法、Broyden法等。
这些方法均经AspenTech进行了修正。
例如,修正后Secant法可以处理非单调的设计规定。
Aspen Plus可以同时收敛多股撕裂(Tear)物流、多个设计规定,甚至收敛有设计规定的撕裂物流。
这些特点对解决高度交互影响的问题时特别重要。
02 化学专业英语络合物的命名
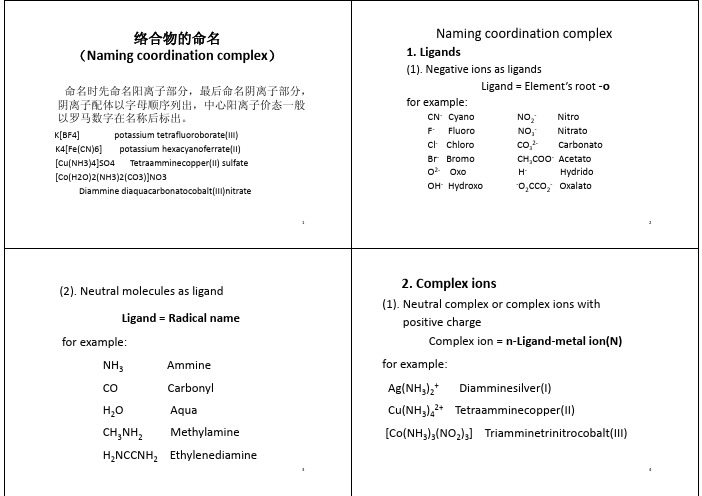
2. Complex ions p
(1). Neutral complex or complex iห้องสมุดไป่ตู้ns with positive charge Complex ion n‐Ligand‐metal ion(N) Complex ion = n Ligand metal ion(N) for example: Ag(NH3)2+ Diamminesilver(I)
5
molecules H2O NH3 CO CH3NH2 aqua ammine carbonyl methylamine
(2).Complex ions with negative charge Complex ion =n‐Ligand‐metal’s root‐ate(N) for example: f l [Fe(CN)6]4‐ Hexacyanoferrate(II) [ [BF4]‐ [AlF6]3‐ [AuCl4]‐ Tetrafluoroborate(III) ( ) Hexafluoroaluminate(III) Tetrachloroaurate(III)
Cu(NH3)42+ Tetraamminecopper(II) [Co(NH3)3(NO2)3] Triamminetrinitrocobalt(III)
4
H2NCCNH2 Eth l Ethylenediamine di i
常见配体的名称 ions CNOHCH3COONO3NO2FClBrCO32cyano hydroxo acetato nitrato nitro fluoro chloro bromo carbonato
6
3.Naming complex
Complex = Cation + anion = Cation + anion for example: p
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
7.9 化学水部分
7.9.1 工程概况
本期工程为新建1×130t/h次高温次高压循环流化床锅炉+新建1台背压B15MW 排汽机组。
7.9.2 水源与水质
7.9.2.1 水源及水质资料
本期工程水源为预处理后的河水(地下水)。
水量和水质均能满足本期工程需要。
由业主提供的水质分析报告见下表。
水质全分析报告
7.9.2.2 原锅炉补给水处理系统概述
原锅炉补给水处理系统工艺流程为:原水→自清洗过滤器→加热器→超滤→超滤水泵→保安过滤器→反渗透装置→淡水箱→淡水泵→弱阳床→强阳床→除碳器→中间水箱→中间水泵→弱阴床→强阴床→混床→除盐水箱→除盐水泵→主厂房。
原有的主要水处理设备有:¢2200一套、¢2000二套弱阴、弱阳、强阴、强阳交换器,¢1600一套、¢1600一套、¢1500二套混合离子交换器,正常出力120T/h.,新增3×120T/h超滤与3×90T/h反渗透预脱盐后,三套离子交换器全投运不考虑备用最大出力190T/h。
7.9.3 锅炉补给水处理系统出力
本期工程扩建后机组的外供汽量最大为268+50t/h,外供蒸汽凝结水不回收,所以本期工程外供汽损失为268+50t/h。
根据《小型火力发电厂设计规范》,可计算化学水处理系统出力:
1.厂内汽水损失 3%×(3×75+1×130+1×130)=14.55t/h
2.锅炉排污损失 2%×(3×75+1×130+1×130)=9.7t/h
3.机组启动或事故增加的损失 10%×130=13t/h
4.外供汽损失 268+50t/h
5.其它汽水损失 10.75t/h
本期工程扩建后锅炉补给水处理系统设计总出力应为:366t/h
而原有锅炉补给水处理系统正常出力为:120t/h,所以本期工程新增锅炉补给水处理系统出力应为:366-120=246t/h。
本期工程锅炉补给水处理系统设计出力取:250t/h。
(化学专业修改)
7.9.4 设计依据
汽水标准按照<<火力发电机组及蒸汽动力设备水汽质量标准>> GB/T 12145-2008
1)蒸汽质量标准
铁(Fe)≤15μg/L
铜 (Cu) ≤3μg/L
钠 (Na) ≤5μg/L
二氧化硅≤20μg/L
电导率(25℃) ≤0.15μS/cm
2)锅炉给水质量标准
PH(25℃) 9.1~9.4
溶解氧≤7μg/L
铁≤30μg/L
铜≤5μg/L
电导率(25℃) ≤0.3μS/cm
二氧化硅(SiO2 )保证蒸汽的二氧化硅符合标准
3)汽轮机凝结水质量标准
硬度≤1μmol/L
溶解氧≤50μg/L
电导率(25℃) ≤0.3μS/cm
4)锅炉炉水质量标准
磷酸根 2~10mg/L
PH(25℃) 9~10.5
二氧化硅≤2.00mg/L
电导率(25℃) ≤150μS/cm
5)化学除盐水
硬度 0μmol/L
二氧化硅≤20μg/L
电导率(25℃) ≤0.2μS/cm
7.9.5 锅炉补给水处理系统的选择
因地表水随季节水质变化较大,本期扩建工程延用原锅炉补给水处理系统工艺流程,即:原水→自清洗过滤器→加热器→超滤→超滤水泵→保安过滤器→反
渗透装置→淡水箱→淡水泵→弱阳床→强阳床→除二氧化碳器→中间水箱→中间水泵→弱阴床→强阴床→混床→除盐水箱→除盐水泵→主厂房。
因前期工程自清洗过滤器、加热器、弱阳床、强阳床、除二氧化碳器、弱阴床、强阴床、混床和水泵等化水设备均在前期工程中已经一次性上齐,本期工程只需新上一套超滤和反渗透装置。
7.9.5.1 主要设备选择
化水主要设备表
7.9.5.2 化水车间室外设备布置
化水车间室外布置水箱和水池均利用原有水箱和水池。
7.9.6炉水、给水校正处理系统
在原锅炉间运转层已设置有加药间,并已经安装了磷酸盐加药装置和给水加氨装置,所以本期工程不再新上。
7.9.6 汽水取样系统
为使热力系统连续、正常、安全的运行,设置了一套完整的汽水取样系统,集中取样,取样项目及化验标准应遵循《火力发电厂水汽化学监督导则》及《火力发电机组及蒸气动力设备水汽质量》(GB/T12145-2008)的规定。
按照《火力发电厂化学设计技术规程》的要求设置了以下的人工分析项目:
除氧器出口给水含氧量
省煤器入口给水电导率
炉水电导率
饱和蒸气电导率
过热蒸气电导率
凝结水电导率、含氧量
供热回水电导率
7.9.6.1 取样点的设置
锅炉上各取样点由厂家设置取样头,每台炉4项6点(炉水、饱和蒸汽各2点,过热蒸汽1点,给水1点)。
其余4项共6点(给水取样1点,除氧器共2点、凝结水取样2点,供热回水1点)均在安装时设置。
人工取样的取样冷却器由锅炉厂成套供应,每台锅炉设1套取样冷却器,分别为过热蒸汽、饱和蒸汽、给水、炉水取样。
7.9.7 化学水处理系统防腐措施
1、酸、碱罐采用钢制品内衬胶。
2、中间水箱、除盐水箱等钢制品内衬玻璃钢。
3、除盐水管采用不锈钢管。
4、酸、碱运输采用罐车购成品。
