chap.5 手性分子(有机化学)
手性分子与手性药物

有机化学手性分子与手性药物材料与化学工程系12级应化(1)班左旋海螺的螺壳都是右旋的,出现左旋螺壳的概率是百万分之。
我们吃的如甘蔗汁制的或甜莱汁制的糖,它们的分子都是右旋的。
人体内氨基酸分子都是左旋的,而淀粉的分子都是右旋的,传递遗传信息的脱氧核糖 核酸(DNA),95%以上呈右旋。
星系的运动都呈圆形、椭圆形或涡旋形运动,多是左旋。
多数藤本植物如牵牛花、扁豆等的茎蔓是右旋的。
然界中的手性 右旋长瓣兜兰花两侧长瓣的螺旋是左右对称的,右侧是左旋,左侧是右旋。
《科学》化学概念中的手性镜象不能重合的现象。
称为手性分子,手性分子都具有旋光性;不具有手性的分子称为非手性分子,无旋光性。
由于含一个不对称碳原子的化合物具有手性,这与其呈现手性特征的中心碳原子有关,因此这个中心碳原子称为手性中心,称其不对称碳原子为手性碳原子。
手性碳不不手性分子的特征所谓手性碳原子,是指饱和碳原子上连有四个完全不同的原子或原子团,常用火号予以 标注。
* H_C_Cl非手性分子两者可以重合什么是手性 手互为手性碳标记2.含有一个手性碳原子的分子往往具有手性。
含有多个手性碳原子的分子 不一定都具有手性。
例如:2,3-丁二醇的三种立体结构III 的结构具有对称中心,为非手性分子,与I 和n 均不成镜像,互为非对映异构体。
互为镜像,不能重合,均为手性分子。
I 和n 互为对映异构体 小结:手性分子与非手性分子不能与镜象叠合的分子叫手性分子,而能叠合的叫非手性分子。
综上所述:物质分子凡在结构上具有对称面或对称中心的,均不具有手性,则无旋光性;反之,在结构上既不具有对称面,也不具对称中心的,在这种分子具有手性,它与镜像互为对映异构体,不能重叠,故具有旋光性。
除了含有一个手性碳原子的化合物具有手性,还有含其他手性因素的化合物如含手性氮原子等化合物,以及某些不含手性碳原子但具有手性的化合物。
CH 33H ——OHHO ——H CH 3 HO-U-H H —OHC H 3II翻转180°,完全重合 帆川,明 III对映体的表示方法两种方法:1.透视法直观,但书写麻烦,不适用于复杂化合物2.Fischer投影式使用方便,适用于简单和复杂化合物1.透视法实线纸面上的键虚线伸向纸后方的键锲形线伸向纸前方的键COOHCOOHO2、Fischer投影式①碳链竖置,且编号小者置于上端;②上下朝里,左右朝外;COOH观察COOH■HC OH OHC H.3COOHHOHY透视式CH3Fische r投影式命名规则:R、S标记法的规则①找出手性C原子②C原子上的基团依从大到小次序排列③若为顺时针排列,叫做R-构型;若为逆时针排列,叫做S-构型。
有机化学基础知识手性与不对称合成

有机化学基础知识手性与不对称合成有机化学基础知识:手性与不对称合成在有机化学中,手性和不对称合成是两个重要的概念。
手性是指分子或化合物具有非重叠的镜像对称结构,分为左旋(S)和右旋(R)两种构型。
不对称合成则是指通过反应使得手性化合物生成的过程。
手性与不对称合成的重要性在于它们在生物学、药物学和有机合成领域具有广泛应用。
手性分子在生物体中扮演重要的角色,药物分子的手性性质直接影响其在体内的活性和毒性。
此外,许多有机合成过程中需要获得高立体选择性的产物,这就需要使用不对称合成方法。
一、手性的定义与属性手性(chirality)是指分子或化合物不能与其镜像完全重合的性质。
简单来说,手性分子就像是左右手,无法完全重叠,这是由于手性分子的立体结构具有非对称性。
手性的性质包括以下几个方面:1. 手性分子无旋转轴或镜面反射面:旋转或镜面反射一个手性分子,无法使其和源分子完全重合,这就是左旋和右旋构型的来源。
2. 左旋(S)和右旋(R)构型:对于手性分子,以手的方式分别沿顺时针和逆时针方向围绕分子中心生成立体结构,可得到左旋(S)和右旋(R)构型,确定手性分子的构型是有机化学的重要内容。
3. 光学活性:左旋和右旋构型的手性分子之间可以通过手性光学活性来区分,其中旋光(optical rotation)是一种常用的手性分析方法。
二、手性分子的来源手性分子的来源多种多样,包括以下几种常见的方式:1. 手性衍生物:通过对不对称化合物的反应进行处理,引入手性基团,从而生成手性产物。
2. 手性诱导:在合成过程中,通过使用手性诱导剂,使得产物具有手性结构。
3. 手性模板:在有机合成中,通过使用手性模板,使得反应生成具有手性结构的产物。
4. 生物来源:许多生物体内产生的分子都是手性的,因此通过利用生物体提取或合成方式,可以获得手性分子。
三、不对称合成方法不对称合成是指通过有选择性地控制反应条件、底物结构或合成步骤,使得手性化合物生成的合成方法。
有机化学基础知识点手性化合物的分离与合成

有机化学基础知识点手性化合物的分离与合成有机化学基础知识点:手性化合物的分离与合成手性化合物在有机化学领域中扮演着重要的角色,它们具有两种非对称的镜像异构体,即左旋和右旋。
手性化合物的分离与合成是有机化学中的一项重要技术和研究内容。
本文将探讨手性化合物的分离与合成的基础知识点。
一、手性化合物的分离方法1. 基于手性配体的手性柱层析法手性柱层析法是一种基于手性配体与目标分子之间的亲和性进行分离的方法。
通过选择适当的手性配体,可以实现对手性化合物的分离纯化。
例如,利用氨基酸衍生物作为手性配体,可以成功地分离出手性氨基酸和手性药物等。
2. 经典拆分结晶法经典拆分结晶法是一种通过晶体生长的方式分离手性化合物的方法。
通过合适的溶剂和配体选择,可以在晶体生长过程中实现手性化合物的拆分和纯化。
这种方法适用于一些具有较高拆分度的手性化合物。
3. 手性萃取法手性萃取法是一种利用手性选择性较大的手性萃取剂对手性化合物进行分离的方法。
通常通过控制温度、pH值和萃取剂浓度等条件,实现对手性化合物的选择性萃取。
手性萃取法在手性酮、手性醇以及手性药物等的分离中得到了广泛应用。
二、手性化合物的合成方法1. 左旋-右旋互换法左旋-右旋互换法是一种将一种手性化合物转化为其对映异构体的方法。
通常可通过二氧化硫气体的作用,将左旋手性化合物转化为右旋手性化合物,或者通过酸碱反应进行互换。
这种方法在手性药物和手性农药的合成中得到了广泛应用。
2. 手性催化剂的应用手性催化剂是一种能够选择性地促使手性化合物发生反应的催化剂。
通过催化剂的选择,可以实现手性化合物的不对称合成。
例如,手性金属配合物催化剂在不对称氢化和不对称还原反应中起到了关键作用。
3. 有机合成中的修饰法有机合成中的修饰法是一种通过对已有手性分子进行化学修饰,合成新的手性分子的方法。
通过对已有手性分子的保留或改变官能团,可以得到一系列具有不同手性的化合物。
这种方法在新药开发和杂环合成中得到了广泛应用。
有机化学:第五章 手性分子与旋光异构

一、旋光活性
1. 平面偏振光 ( plane-polarized light )
--- 普通光在通过尼克尔棱镜后形成的只在一个方向传播的 平面光。
3
一、旋光活性
2. 光学活性 ( optical activity ) --- 物质能使偏振光发生偏转的性质。
4
旋光仪(polarimeter) l
5
一、旋光活性
3. 右旋和左旋 ( dextrorotatory and levorotatory ) --- 使偏振光振动平面向右旋转称右旋,“ + ” --- 使偏振光振动平面向左旋转称左旋,“ - ”
4. 旋光度(observed rotation) --- 旋光活性物质使偏振光振动平面旋转的角度:与两个或两个以上相同基团相连的碳原子。
18
H
CH
H
H
6个对称面
Cl
CH
H
H
3个对称面
Cl
CH
F
H
1个对称面
Cl
CH
F
CH3
无对称面
手性碳:连接了四个不同基团的碳原子
19
不对称分子(手性分子) 如果分子中不存在对称面、对称中心和四重象转轴,则这个分子
具有手性,其实物与镜影不能完全重叠。
22
(2) 手性分子在生理活性上存在差异
“反应停事件” 20世纪60年代,名为“反应停” 的药物在欧洲用作治疗孕 妇的妊娠反应,它的副作用曾经使一些服用此药物的孕妇产 下了1.2万名畸型婴儿。
惨痛的教训!
23
小资料:
经过34年的慎重研究,1998年FDA批 准“反应停”作为治疗麻风结节性红斑的 药物在美国上市。美国成为第一个将“反 应停”重新上市的国家。 “反应停”还被发现有可能用于治疗多 种癌症。现在90% “反应停”被用于治疗 癌症病人,在美国的销售额每年约两亿 美元。 活性更强且没有致畸性的“反应停”衍 生物也已被批准上市。
大学有机化学立体化学基础手性分子讲义

大学有机化学立体化学基础手性分子讲义一、教学内容1. 手性碳原子:介绍手性碳原子的定义、判断方法以及手性碳原子的性质。
2. 手性分子:介绍手性分子的定义、分类以及手性分子的性质。
3. 手性分子的光谱性质:介绍手性分子在不同光谱范围内的表现形式,如红外光谱、紫外光谱等。
4. 手性分子的化学反应:介绍手性分子在化学反应中的特性,如不对称催化、手性分子的选择性反应等。
5. 手性分子的应用:介绍手性分子在医药、农药、材料科学等领域的应用。
二、教学目标1. 了解手性碳原子的定义和判断方法,掌握手性碳原子的性质。
2. 掌握手性分子的定义和分类,了解手性分子的性质。
3. 了解手性分子的光谱性质,认识手性分子在不同光谱范围内的表现形式。
4. 理解手性分子在化学反应中的特性,如不对称催化、手性分子的选择性反应等。
5. 了解手性分子在医药、农药、材料科学等领域的应用。
三、教学难点与重点重点:手性碳原子的判断方法、手性分子的性质、手性分子的光谱性质、手性分子的化学反应。
难点:手性分子的分类、手性分子在不同光谱范围内的表现形式、手性分子在化学反应中的特性。
四、教具与学具准备教具:PPT、黑板、粉笔。
学具:笔记本、彩色笔、课本。
五、教学过程1. 实践情景引入:通过展示一些日常生活中常见的的手性分子,如氨基酸、糖类等,引发学生对手性分子的兴趣。
2. 手性碳原子的定义和判断方法:通过PPT讲解手性碳原子的定义和判断方法,让学生掌握手性碳原子的性质。
3. 手性分子的定义和分类:通过PPT讲解手性分子的定义和分类,让学生了解手性分子的性质。
4. 手性分子的光谱性质:通过PPT讲解手性分子在不同光谱范围内的表现形式,让学生认识手性分子的光谱性质。
5. 手性分子的化学反应:通过PPT讲解手性分子在化学反应中的特性,让学生理解手性分子的化学反应。
6. 手性分子的应用:通过PPT讲解手性分子在医药、农药、材料科学等领域的应用,让学生了解手性分子的实际应用价值。
手性分子专业知识讲座

Cl Cl
HOOC C消旋体旳拆分 (1)机械拆分法 (3)选择吸附拆分法 (5)化学拆分法
(2)微生物拆分法 (4)诱导结晶拆分法
小结: 1、了解手性、旋光性、对映异构旳概念 2、熟练掌握构型旳标识措施 3、熟练掌握构型式旳透视式和菲舍尔投影式之间旳 相互转化。
注:
①但凡手性分子,都有旋光性; 非手性分子无旋光性
②一对对映体对偏振光旳作用恰好相反,一种使偏 振光左旋,一种使之右旋,旋光度数值相等。
3)旋光性旳测量 用旋光仪进行测量。
A
A
B
D'
C
D
B'
A'
A'
起偏镜
乳酸
旋光性物质
盛液管
α
目镜(亮)
检偏镜
4)比旋光度
t
l C
α旋光仪中读到旳旋光度; l 盛液管旳长度;(dm) C 溶液旳浓度;(g/ml)
H
H
Br
Br
H
H
CH3 Cl
CH3 Cl CH3
H
Cl
Br H
CH3 CH3
Br H
CH3
CCHH33
H
Br
Cl
H
CH3
五、含一种手性碳原子化合物旳对映异构
1、手性碳:常用“*”表达
CH3C*HCOOH OH
具有一种手性碳原子旳化合物,一定是手性分子。 有一对对映体,其中一种是左旋,一种是右旋。 如乳酸:
作业:1、 (2) (4) (6);2 、(2) (5) ; 4、 (2) (4) ;7
对映体非对映体 对映体
分子中具有n个手性碳旳化合物,最多有 2n 个对映异构 体,有2n-1对对映异构体。
有机化学基础知识分子的立体化学

有机化学基础知识分子的立体化学有机化学是研究含碳的化合物的分子结构、性质、合成、反应以及它们在生物体系中的作用的科学。
其中,分子的立体化学是有机化学中至关重要的一部分。
本文将介绍有机化学中分子的立体化学基础知识,包括手性,立体异构体及其命名以及手性分子的光学活性。
一、手性分子的手性是指其镜像不能重合的特性。
由于碳原子可以形成四个互不相同的键,大部分有机化合物都可以具有手性。
手性分子包括两种类型:手性中心和轴手性。
1. 手性中心手性中心是指分子中的一个碳原子,它与四个不同的基团连接。
手性中心的碳原子通常以S(拉丁语 sinister )和R(拉丁语 rectus)表示,分别代表左旋和右旋的空间构型。
2. 轴手性轴手性是指分子中存在一个对称轴,该对称轴可以将分子分为两个不可重合的镜像体。
轴手性是由于分子的非完全对称所导致的,在立体异构体中较为常见。
二、立体异构体及其命名立体异构体是指分子在空间排列上存在不同的构型,从而导致其化学性质和生物活性的差异。
立体异构体包括构象异构体和对映异构体。
1. 构象异构体构象异构体是指分子在空间上能够互相转换,但又不能通过化学反应相互转化的异构体。
最常见的构象异构体是旋转受限的双键环状化合物,如环烯烃和环烷烃。
2. 对映异构体对映异构体是指分子的镜像体,在化学和物理性质上没有差异,但与其他手性物质的相互作用不同。
对映异构体是由于分子的手性中心或轴手性所引起的。
对映异构体的命名通常使用R/S命名法或者D/L命名法,其中R/S命名法适用于手性中心,而D/L命名法适用于糖类和氨基酸等化合物。
这些方法可以准确地描述分子在空间中的立体排列。
三、手性分子的光学活性手性分子的光学活性是指它们对平面偏振光有选择性地旋转偏振面的性质。
手性分子旋光的方向可以是顺时针旋光(右旋)或逆时针旋光(左旋),分别用(+)和(-)表示。
对于含有手性中心的分子,不对称的环境可以导致光学活性。
手性分子的光学活性在药物、农药、香料等领域具有重要的应用价值。
大学有机化学立体化学基础:手性分子资料

d
d a
(R)
b
(基团的顺序 为a>b>c>d)
(2) 小竖同。
a
b c d
(R)
d b c
(S)
a
CN H2N H , C6H5
C H2S H HO O C NH2 , H
C HO OH H C H2O H
上页 下页 首页
第五章 立体化学基础 第四节 构型标记法 (R/S构型标记法)
R-S标记法应用较广泛,当分子中含有多个 手性碳原子时,它能标记出每一个手性碳原 子的构型。 目前D-L构型标记法仍在使用,特别是糖类 化合物和氨基酸。 D/ L 与R/S无对应关系
上页 下页 首页
第五章 立体化学基础 第四节 构型标记法 (R/S构型标记法)
二、R/S 构型标记法 —— 绝对构型
根据基团的顺序规则,确定与手性碳原子相连的 4 个基团 优先顺序的大小,假设顺序为a>b>c>d。将优先顺序最小的 基团d处于眼睛对面最远的位置上,然后再看a→b→c的排列顺 序,如顺时针方向的定为 R 构型 ( 拉丁文 Rectus 的缩写 ) ,假若 a→b→c是逆时针方向的则定为S构型(拉丁文Sinister的缩写).
问题:下列化合物哪些含手性碳原子?
1. CH2Cl2 2. CHCl3
3.CH3CHClCH2CH3
4. CH3-CH-CH2CH3
CH2CH3
5. CH3-CH-CH-CH2CH3 OH OH
H
6.
CH3
7.
CH3
8.
H3C
CH3
CH3
O
CH3
上页 下页 首页
第五章 立体化学基础 第一节 手性分子和对映体(四、判断对映体的方法)
化学手性有机化合物的合成和应用研究

化学手性有机化合物的合成和应用研究一、手性有机化合物的概念手性有机化合物是指分子中含有手性碳原子(即一个碳原子连接着四个不同的原子或原子团)的有机分子。
手性碳原子使得分子具有非对称的空间结构,因此手性有机化合物具有镜像异构体,称为手性异构体。
二、手性有机化合物的合成方法1.逆合成法:逆合成法是一种根据目标产物设计合成路径的方法。
首先确定目标产物的结构,然后逆向推导出合成该产物的步骤。
这种方法在有机合成中具有广泛的应用。
2.手性催化剂:手性催化剂是指在化学反应中能够诱导出手性选择性的催化剂。
利用手性催化剂可以实现对手性有机化合物的合成,从而获得特定的手性异构体。
3.手性助剂:手性助剂是指在化学反应中与反应物发生作用,从而影响反应选择性的化合物。
手性助剂可以提高手性有机化合物的合成效率和选择性。
4.立体选择性合成:立体选择性合成是指在化学反应中,通过控制反应条件,使反应物分子中的不同基团在空间上发生选择性反应,从而获得特定手性异构体的方法。
三、手性有机化合物的应用1.药物化学:手性有机化合物在药物化学领域具有重要意义。
许多药物分子具有手性异构体,这些异构体在药效、药代动力学和毒副作用方面可能存在显著差异。
因此,研究手性有机化合物的合成和应用,有助于开发新药和优化药物结构。
2.材料科学:手性有机化合物在材料科学领域也有广泛应用。
例如,手性有机分子可以用于制备手性光学材料、手性液晶和手性传感器等。
3.催化领域:手性有机化合物在催化领域具有重要作用。
手性催化剂和手性助剂可以提高化学反应的选择性,从而实现高效、绿色的化学合成。
4.分析化学:手性有机化合物在分析化学领域也有应用。
手性异构体之间的相互作用差异,可以用于检测和分析生物分子、环境污染物等。
综上所述,化学手性有机化合物的合成和应用研究是一个涉及有机合成、手性化学、药物化学、材料科学等多个领域的复杂课题。
通过对手性有机化合物的合成方法及其应用的研究,可以为我国化学工业、医药事业和材料科学的发展提供理论支持和实践指导。
有机化学基础知识点整理有机分子的手性中心和对映体生成的条件

有机化学基础知识点整理有机分子的手性中心和对映体生成的条件有机化学基础知识点整理:有机分子的手性中心和对映体生成的条件在有机化学中,手性中心和对映体是非常重要的概念。
手性中心指的是一个分子中的碳原子,它与四个不同基团连接,导致该碳原子存在两种互为镜像的立体异构体,即对映体。
本文将对有机分子的手性中心和对映体生成的条件进行整理。
手性中心的定义手性中心是指一个分子中的碳原子或其他有机官能团,其与不同基团或官能团的连接方式不相同,从而使得该碳原子或官能团存在两个非重叠的镜像异构体。
一般来说,一个分子中需要有手性中心才能形成对映体。
对映体的定义对映体是指具有相同分子式和结构式,但无法通过旋转重叠叠加的方式使其重合的两个异构体。
对映体具有相同的物理化学性质,如熔点、沸点等,但在光学活性和化学反应性上有明显的差异。
对映体生成的条件1. 手性中心的存在如前所述,对映体的生成需要分子中存在手性中心。
常见的手性中心是由四个不同基团连接的碳原子,简称R/S中心。
2. 空间异构对映体的生成要求分子在三维空间中存在非重叠的镜像异构体。
这要求分子的结构具有立体异构性,即存在非平面性或空间构型限制。
3. 不可旋转键对映体的生成还需要分子中存在不可旋转的化学键。
典型的不可旋转键是双键、环状结构和含有重原子的键(如C-Cl键)等。
4. 化学键的空间构型当分子中含有不可旋转键时,键的空间构型将决定对映体的生成。
常见的键空间构型包括顺式和反式构型、立体异构的卤代烷烃和手性环状化合物等。
应用和研究对映体广泛存在于生物大分子、药物和农药等有机化合物中。
由于对映体在光学活性、药理学和生物学方面的差异,对映体的鉴定和分离成为有机化学和药学领域的重要研究内容。
此外,对映体的制备也是有机合成中的一项重要任务。
常见的对映体合成方法包括手性拆分、手性诱导和手性催化等。
结论有机分子的手性中心和对映体生成的条件是有机化学中的基础知识点之一。
手性中心是导致分子存在对映体的原因,而对映体则在光学活性、药理学和生物学等方面具有重要的应用和研究价值。
有机化学基础教案:手性化合物

有机化学基础教案:手性化合物手性化合物一、基本概念手性化合物,又称为光学异构体,是指一类分子具有非对称的空间结构的化合物,与它们的镜像图像称为对映异构体。
左右手是最为普遍的手性,所以分子的对映异构体也被称为左旋异构体和右旋异构体。
手性化合物在化学领域中占据着重要的地位,因为它们和它们的对映异构体在化学和生物学上表现出截然不同的性质。
一些手性分子被用于味道和气味,如L-和D-型氨基酸和L-和D-型半乳糖等,其对映异构体的话味道、气味也是有很大的差别的。
二、分子手性手性化学的重点在于分子的手性性质,这需要涉及到“不对称中心”的概念。
所谓不对称中心,是指分子中存在一个原子或原子团,它与其他原子或原子团不同,具有不对称性。
当原子或原子团的四个键上的原子或原子团不同时,则该不对称中心对应两个对映异构体。
手性分子相互作用具有非对称性,因此可以与环境中的手性分子有选择性的反应,因此具有广泛的应用。
如下图所示,对于一个分子来说,其手性一般是由其空间构型所决定的。
如上图所示的化合物,由于其中碳上结合有四种不同的基团,可以形成一个不对称中心,使得该分子存在两种对称性不同的构型。
这两种构型之间没有旋转、平移或翻转等操作可以相互转化,因此是两种独立的存在,分别称为对映异构体。
三、手性分子的制备手性分子的制备是化学工业中的重要难题之一。
目前,制备手性化合物的主要方法包括对称合成法、非对称合成法和拆分法三种。
对称合成法是通过利用对称性不同的化合物反应产生手性物质。
这种方法具有化学反应研究的重要价值,但现在不再是制备非常手性化合物的主要方法。
非对称合成法是通过将对映异构体的反应性差异进行利用,直接合成具有一定手性的化合物,从而逐步调节其手性化合物的方法。
这是制备手性化合物最为直接和有效的方法。
拆分法是指以具有不对称结果的手性物质为原料,从中分离出其对映异构体的方法。
该法要求手性物质必须是有光学活性的化合物,如在分子中有不对称碳原子、手性杂环、含手性杂原子等,否则就无法使用此法。
14-5手性分子
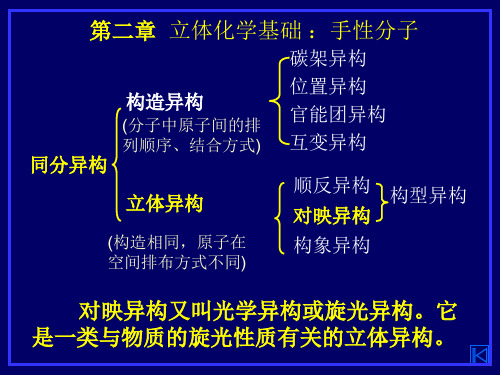
[α]D20 =
+3.2o
1× 0.05
= +64o (C, 0.05, H2O)
第一节
一、手 性
手性分子和对映体
观察自己的双手, 左手与右手有什么联系和区别?
左手的镜像是右手
右手的镜像是左手
左右手互为镜像与实物关系(称为对映关系),彼此 又不能重合的现象称为手性。
问题:脚, 耳朵, 鼻子, 螺丝钉是否具有手性?
COOH H OH
COOH H CH3 OH
OH
COOH H
COOH OH CH3 H
C CH3
C CH3
课堂练习:试根据模型写出Fischer投影式。
(+)-甘油醛
在符合“横前竖后”规则的前提下,亦可得到不同Fischer投影式。
CHO H OH HOCH2 CH2OH
OH CHO HO H
CH2OH H OHC CHO
一个手性碳原子所连的4个不同原子或基团位 于四面体的四个顶角,在空间具有2种不同的排列 方式(也称两种构型), 它们彼此构成一对对映体。
* CH3CHCOOH
OH
乳酸
COOH HO C CH3 H
COOH H C OH CH3
有一个手性碳的化合物必定 是手性化合物,只有一对对映体。
1.手性分子 有对映异构体的分子称为手性分子(Chiral molecule),或称分子具有手性(chirality). 乙醇没有 对映体,因此是非手性分子。 2.手性碳与4个不同基团相连的碳原子称为手性碳原子 ( 常用 *C表示 ), 正是这种碳原子使乳酸分子产生了手性。 *C只是手性原子(又称手性中心)的一种。 OH C H H CH3 H H3C CO2H C* OH HO CO2H *C H CH3
手性分子
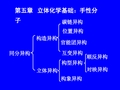
把主链竖 立,编号 最小碳放 在上端
划十字线, 交点代表手性 碳,横键向前,竖键向 。
含有两个手性碳的手性分子的投影
CH3 HO
HO C C OH CH3 H
H OH CH3
H
H H3C
CH3 HO H H CH3
HO C C
CH3 H
HO C C
CH3 H
HO
H H3C
OH HO
CH3 H
二、使用Fischer 投影式应注意的几个问题 1、 Fischer 投影式只能在纸面上旋转180°, 而不能旋转90°或270 °
1、掌握对映体、非对映体、内消旋体、外消旋体、 手性、手性分子等概念,了解旋光性、旋光度、比旋光度、 等概念。 2、掌握构型命名、 Fischer 投影式的写法及使用 应注意的几个问题、 Fischer 投影式与锯架式(或纽曼 投影式)之间的转换关系。 3、正确判断分子有无手性(含一个手性碳、两个手性 碳、无手性碳、及环状化合物),用D/L和R/S表示构型的原
COOH H2N CH 3 H = H3C H COOH NH 2 = H NH 2 COOH CH 3 = H CH 3 NH 2 COOH
4、Fischer 投影式中手性碳原子所连原子或 基团,可以两两交换偶数次。但不能交换奇数 次。
对映异构体的Fischer 投影式
COOH H CH3 OH OH
a c d b
R 构型 优先顺序:a>b>c>d
1、确定C*abcd分子,优先顺序a>b>c>d; 2、若最小基d在垂直方向,ab c顺时针时为R 构型; 反之,为S构型。 3、若最小基d在水平方向,ab c顺时针时为 S构型; 反之,为R构型。
05-立体化学基础:手性分子PPT课件

2021/6/4
30
课堂练习:试根据模型写出Fischer投影式。
(+)-甘油醛
在符合“横前竖后”规则的前提下,亦可得到不同Fischer投影式。
H
C H O
O H
C H 2O H
H O HH O C H 2 C H OH O HO H C C H 2O H
羧基与H交换位置 羟基与甲基交换位置
2021/6/4
36
Fischer 式中同一个手性碳上所连原子或基 团两两交换奇数次,其构型改变为其对映体。
基团互换
2021/6/4
37
Fischer式的平移或纸平面内旋转或180的 整数倍,其构型不变。 但Fischer式不能离开 纸面翻转或沿纸面旋转90 (或270)。
公式中的c换成液体的密度d即可。
最常用的光源是钠光(D),λ=589.3nm。 所用溶剂不同也会影响物质的旋光度。因此
在不用水为溶剂时,需注明溶剂的名称,例如,
右旋的酒石酸在5%的乙醇中其比旋光度为:
[α2 D]0 +3.79(乙醇,5%)
2021/6/4
26
旋光仪(polarimeter)
2021/6/4
2021/6/4
23
能使偏振光振动平面向右旋转的物质称右 旋体,能使偏振光振动平面向左旋转的物质称 左旋体。
旋光性物质使偏振光旋转的角度,称为旋
光度,以“”表示。
顺 时 针 右 旋 , 以 “ d ” 或 “ + ” 表 示 。 其 旋 光 方 向
逆 时 针 左 旋 , 以 “ l ” 或 “ ” 表 示 。
手性分子的性质

什么是手性分子英文名:chiral molecules我们知道,生命是由碳元素组成的,碳原子在形成有机分子的时候,4个原子或基团可以通过4根共价键形成三维的空间结构。
由于相连的原子或基团不同,它会形成两种分子结构。
这两种分子拥有完全一样的物理、化学性质。
比如它们的沸点一样,溶解度和光谱也一样。
但是从分子的组成形状来看,它们依然是两种分子。
这种情形像是镜子里和镜子外的物体那样,看上去互为对应。
由于是三维结构,它们不管怎样旋转都不会重合,就像我们的左手和右手那样,所以又叫手性分子。
对于非碳原子手性中心的分子,只要没有对称面和对称中心即为手性分子。
手性分子的基本标志一个化合物的分子与其镜像不能互相叠合,则必然存在一个与镜像相应的化合物,这两个化合物之间的关系,相当于左手和右手的关系,即互相对映。
这种互相对应的两个化合物成为对映异构体(enantiomers)。
这类化合物分子成为手性分子(chiral molecule)。
不具有对称面和对称中心的分子有一个重要的特点,就是实体和镜象不能重叠,镜面不对称性是识别手性分子与非手性分子的基本标志。
生物分子手性原则是什么生物分子都有手性,即分子形式的右撇子和左撇子(或左旋、右旋)。
在法国生物学家巴斯德发现酒石酸晶体的镜像后就更激起了科学家的兴趣。
然而,手性分子是如何形成的却一直让人迷惑不解。
过去,生物化学领域趋向于认为,单一手性形式的分子合成通常从一开始就要利用手性本体,也就是说生物分子自身在催化着手性形式的形成。
而且在一些化学反应中手性产物的形成进一步扩大了。
2006年6月16日出版的英国《自然》刊发文章称,最近,美国研究人员发现,物质的固(体)-液(体)相平衡可能参与了生物分子手性的形成。
比如,氨基酸固(体)-液(体)相的平衡,可以由刚开始时的小小的不平衡导致严重偏向一种手性形式,即左旋或右旋。
而这种现象出现在水溶液中,因而也可以解释生命起源以前的左手性和右手性,即为何左右手性数量相当的分子为何会转变成生物分子偏爱一种手性。
有机化学第6章手性分析

H3C H
CH3 CH3
2019/10/21
23
As a rule, an activation energy barrier of 16 to 19 kcal/mole is required to prevent spontaneous room temperature racemization of substituted biphenyls
3.Double and trip bond
CH2CH2CH3
CH2CH2CH3
CH2SH H
CH2SCH3 H
HH R
H CH CR
O H
OC CO H
CC
R
R
CC
O OH
OC CO OH
2019/10/21
10
4. 取代基互为对映异构体时, R 构型优先于S 构型 取代基对几何异构体时,顺式 (Z) 优先于反式 (E)
H
H Cl
Cl H
CH3
CH3
H3C
H Cl
Br H CH3
(2s,3R)-2-Bromo-3-chlorobutane
(2R,3S)-2-Bromo-3-chlorobutane
2019/10/21
14
2019/10/21
15
COOH
H
OH
HO
H
COOH
I
(2R,3R)-(+)-
COOH
HO
H
CH3
CH3
Enantiomers Br
H
H Cl
CH3
H3C
Cl H
Br H 2 3CH3
(2s,3s)-2-Bromo-3-chlorobutane Diastereomers (2R,3R)-2-Bromo-3-chlorobutane
手性分子优秀课件

的碳原子。
三、对称面和非手性分子
.
5
四、判断对映体(手性分子)的方法
第一 建造一个分子和它的镜像的模型。如果两 者不能重合,就是手性分子。
第二 寻找有无对称面、或对称中心。有对称面 或对称中心它就不存在对映体,为非手性分子。
第三 寻找手性碳原子(或手性中心)。只要有一个 手性碳原子,就是手性分子,有一对对映体 (两个以上C﹡有例外。见内消旋体)
如图是一 对互为镜 像关系的 乳酸分子 的立体结 构式(透 视式):
.
3
a和b 两个立体结构式之间有何种关系?它们代表 相同的分子?还是代表不同的分子?不妨观察上 述乳酸分子的两个立体结构式的球棍模型图示
图3-3-1乳酸球棍模型
图3-3-2乳酸球棍模型
.
4
小结:手性分子:不能与其镜像重合的分子。 对映体:彼此成镜像关系,又不能重合
.
6
手性分子
.
1
一、手性 产生对映异构现象的结构依据是手性(Chirality)。 什么叫手性呢?
Hale Waihona Puke 这种左右手互为镜像与实物关系,彼此又
不能重合的现象称为手性。自然界中有许多手
性物,例如:足球、剪刀、螺丝钉等都是手性
物。微观世界的分子中同样存在着手性现象。
有许多化合物分子具有手. 性。
2
二、手性分子和对映体
