工程热力学 第一章 基本概念.ppt
合集下载
高等工程热力学第1章
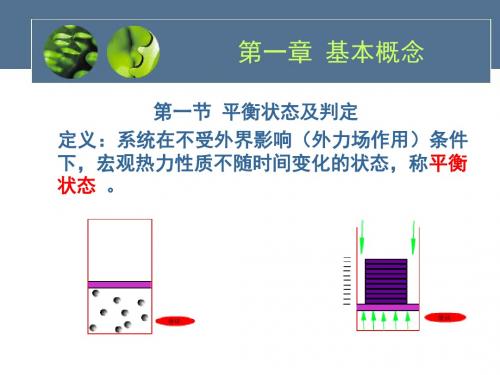
附: 华氏温标和摄氏温标
t
( C) =5 t(F ) 32 9
° °
33
☻ 压力
绝对压力 p;
表压力 pe(pg); 真空度 pv;
p=
F A
p = pb + pe ( p > pb )
p = pb - pv ( p < pb )
动压力、静压力、滞止压力和绝对压力 ?
☻ 热力学能
Uch
G = G( p, T , n1 , n2 , , nr )
热力平衡系统
其中
是驱使第i 种组分变化的势,即化学势:
12
用A表示的化学势
改变约束条件,化学势还可有其它的表达式、但是 无论如何表示,其实质都相同:
据化学势概念,定温、定容和定压、定温系统的 平衡判据:
13
四. 稳定平衡判据
力学中平衡的稳定性
+
+
1
b2
1
C)状态参数分类: 广延量 强度量 (广延量的比性质,具有强度量特性)32
► 系统两个状态相同的充要条件: 所有状参一一对应相等 简单可压缩系两状态相同的充要条件: 两个独立的状态参数对应相等
► 基本状态参数
☻ 温度
测温的基础—热力学零定律 热力学温标和国际摄氏温标
{t } C = {T }K 273.15
δ AT ,V = 0
1
δ AT , V > 0
2
定温定压系统,平衡与稳定的条件
δ GT , p = 0
1
δ GT , p > 0
2
16
过程
不同形式能量之间的转换必须通过工质的状态变化过程才 能完成。 一切过程都是平衡被破坏的结果,工质和外界有了热的、力的 或化学的不平衡才促使工质向新的状态变化,故实际过程都是不 平衡的。
t
( C) =5 t(F ) 32 9
° °
33
☻ 压力
绝对压力 p;
表压力 pe(pg); 真空度 pv;
p=
F A
p = pb + pe ( p > pb )
p = pb - pv ( p < pb )
动压力、静压力、滞止压力和绝对压力 ?
☻ 热力学能
Uch
G = G( p, T , n1 , n2 , , nr )
热力平衡系统
其中
是驱使第i 种组分变化的势,即化学势:
12
用A表示的化学势
改变约束条件,化学势还可有其它的表达式、但是 无论如何表示,其实质都相同:
据化学势概念,定温、定容和定压、定温系统的 平衡判据:
13
四. 稳定平衡判据
力学中平衡的稳定性
+
+
1
b2
1
C)状态参数分类: 广延量 强度量 (广延量的比性质,具有强度量特性)32
► 系统两个状态相同的充要条件: 所有状参一一对应相等 简单可压缩系两状态相同的充要条件: 两个独立的状态参数对应相等
► 基本状态参数
☻ 温度
测温的基础—热力学零定律 热力学温标和国际摄氏温标
{t } C = {T }K 273.15
δ AT ,V = 0
1
δ AT , V > 0
2
定温定压系统,平衡与稳定的条件
δ GT , p = 0
1
δ GT , p > 0
2
16
过程
不同形式能量之间的转换必须通过工质的状态变化过程才 能完成。 一切过程都是平衡被破坏的结果,工质和外界有了热的、力的 或化学的不平衡才促使工质向新的状态变化,故实际过程都是不 平衡的。
工程热力学-01 基本概念及定义

平衡状态1
p1 v1
p
p2
2
压容图 p-v图
平衡状态2
p1
1
p2 v2
O
v2
v1
v
12
1-4 状态方程式
在平衡状态下,由气态物质组成的系统,只要知道两个独立的 状态参数,系统的状态就完全确定,即所有的状态参数的数值随之 确定。这说明状态参数间存在某种确定的函数关系,状态参数之间 存在着确定的函数关系,这种函数关系就称为热力学函数。
(2)当系统处于热力学平衡状态时,只要没有外界的影响, 系统的状态就不会发生变化。
(3)整个系统可用一组具有确定数值的温度、压力及其他参
? 数来描述其状态。
10
经验表明,确定热力学系统所处平衡状态所需的独立状 态参数的数目,就等于系统和外界间进行能量传递方式的数 目。对于工程上常见的气态物质组成的系统,系统和外界间传递 的能量只限于热量和系统容积变化所作的功两种形式,因此只需 要两个独立的状态参数即可描述一个平衡状态。
3、平衡状态、稳定状态、均匀状态
(1)关于稳定状态与平衡状态
稳定状态时,状态参数虽不随时间改 变,但它是依靠外界影响来维持的。而平 衡状态是不受外界影响时,参数不随时间 变化的状态。
85℃ 20℃
90℃
15℃
铜棒
平衡必稳定,稳定未必平衡。
(2)关于均匀状态与平衡 水
质统称为外界。 通常选取工质作为热力学系统,把高温热源、低温热源
等其他物体取作外界。
3、边界 ——热力学系统和外界之间的分界面称为边界。
边界可以是固定的,也可以是移动的; 边界可以是实际的,也可以是假想的。
3
二、热力学系统的分类 依据——有无物质或能量的交换
工程热力学.ppt课件

.
1.1 工质及热力系
工 质:实现热能和机械能相互转化的媒介物质
热源(高温热源) :工质从中吸取热能的物系
冷源(低温热源) :接受工质放出热能的物系
为了研究问题方便,热力学中常把分析对象从周围 物体中分割出来,研究它与周围物体之间的能量和物 质的传递。
.
热力系统(热力系):人为分割出来作为热 力学分析对象的有限物质系统。 外 界:热力系统以外的部分。 边 界:系统与外界之间的分界面。
四. 平衡状态
如果在不受外界影响的条件下,系统的状 态能够始终保持不变,则系统的这种状态称为 平衡状态。
.
实现平衡的充要条件: 系统内部及系统与外界之间的一切不平衡
势差(力差、温差、化学势差)消失是系统实 现热力平衡状态的充要条件。
.
热力平衡状态满足:
热平衡:组成热力系统的各部分之间没有热量的 传递。
由于压力计的测压元件处于某种环境压力 的作用下,因此压力计所测得的压力是工质的真 实压力 p (或称绝对压力)与环境压力 p b 之差,叫做表压力 p e斯卡(简称帕) 符
号: p a ,
1pa 1N/m2
工程单位:
标准大气压(atm , 也称物理大气压) 巴 (bar) 工程大气压(at) 毫米汞柱(mmHg) 毫米水柱(mmH2O)
压
气 燃机
燃 气 轮
料
机
空
气
.
压缩制冷装置系统简图
.
地源热泵
.
本课程的主要内容
基本概念 热力学第一定律 理想气体的性质 理想气体的热力过程 热力学第二定律 水蒸汽 湿空气 制冷循环
.
第一章 热力学基本概念 1.1 工质及热力系 1.2 热力系的宏观描述 1.3 基本状态参数 1.4 热力过程及热力循环
1.1 工质及热力系
工 质:实现热能和机械能相互转化的媒介物质
热源(高温热源) :工质从中吸取热能的物系
冷源(低温热源) :接受工质放出热能的物系
为了研究问题方便,热力学中常把分析对象从周围 物体中分割出来,研究它与周围物体之间的能量和物 质的传递。
.
热力系统(热力系):人为分割出来作为热 力学分析对象的有限物质系统。 外 界:热力系统以外的部分。 边 界:系统与外界之间的分界面。
四. 平衡状态
如果在不受外界影响的条件下,系统的状 态能够始终保持不变,则系统的这种状态称为 平衡状态。
.
实现平衡的充要条件: 系统内部及系统与外界之间的一切不平衡
势差(力差、温差、化学势差)消失是系统实 现热力平衡状态的充要条件。
.
热力平衡状态满足:
热平衡:组成热力系统的各部分之间没有热量的 传递。
由于压力计的测压元件处于某种环境压力 的作用下,因此压力计所测得的压力是工质的真 实压力 p (或称绝对压力)与环境压力 p b 之差,叫做表压力 p e斯卡(简称帕) 符
号: p a ,
1pa 1N/m2
工程单位:
标准大气压(atm , 也称物理大气压) 巴 (bar) 工程大气压(at) 毫米汞柱(mmHg) 毫米水柱(mmH2O)
压
气 燃机
燃 气 轮
料
机
空
气
.
压缩制冷装置系统简图
.
地源热泵
.
本课程的主要内容
基本概念 热力学第一定律 理想气体的性质 理想气体的热力过程 热力学第二定律 水蒸汽 湿空气 制冷循环
.
第一章 热力学基本概念 1.1 工质及热力系 1.2 热力系的宏观描述 1.3 基本状态参数 1.4 热力过程及热力循环
工程热力学(基本概念)
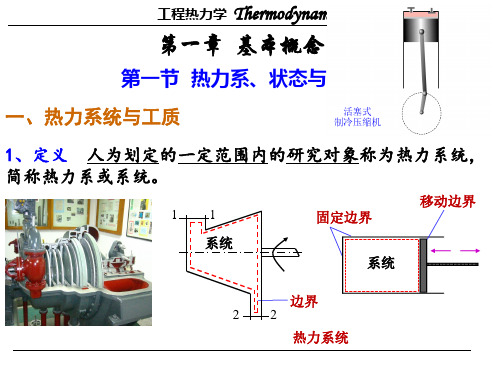
国际实用温标的固定点
平衡状态
平衡氢三相点 平衡氢沸点 氖沸点 氧三相点 氧冷凝点
国际实用温标指定
值
T,K
t,℃
13.81 -259.34
20.28 -252.87
20.102 -246.048
54.361 -218.789
90.183 -182.962
平衡状态
水三相点 水沸点
锌凝固点 银凝固点 金凝固点
一、热力过程
定义:热力系从一个状态向另一个状态变化时所经 历的全部状态的总和。
二、准平衡(准静态)过程
准平衡过程的实现
工程热力学 Thermodynamics
二、准平衡(准静态)过程
定义:由一系列平衡态组成的热力过程 实现条件:破坏平衡态存在的不平衡势差(温差、
力差、化学势差)应为无限小。 即Δp→0 ΔT→0 (Δμ→0)
工程热力学 Thermodynamics
三、可逆过程
力学例子:
定义: 当系统完成某一热力过程后,如果有可能使系统再
沿相同的路径逆行而恢复到原来状态,并使相互中所涉 及到的外界亦恢复到原来状态,而不留下任何变化,则 这一过程称为可逆过程。
实现条件:准平衡过程加无耗散效应的热力过程 才是可逆过程。
工程热力学 Thermodynamics
用来实现能量相互转换的媒介物质称为工质。
理想气体
工 质
实际气体
蒸气
工程热力学 Thermodynamics
二、平衡状态
(一)热力状态:热力系在某一瞬间所呈现的宏观
物理状况。(简称状态)
(二)平衡状态 1、定义:一个热力系统,如果在不受外界影响的条件下,
系统的状态能够始终保持不变,则系统的这种状态称为平衡 状态。
热工基础 1 第一章 基本概念

平衡不一定均匀,单相平衡态则一定是均匀的
平衡:时间上 均匀:空间上
Fundamentals of thermal engineering
热 工 基 础
1-2 平衡状态和状态参数
2、基本状态参数 热力学中常用的状态参数有压力、温度、比体 积、比热力学能、比焓、比熵等,其中可以直接测 量的状态参数如压力、温度、比体积,称为基本状 态参数。 (1)压力 单位面积上所受到的垂直作用力(即压强)
ds 0 , q 0 , 系统吸热; ds 0 , q 0 , 系统放热。 ds 0 , q 0 ,系统绝热,定熵过程。
比体积和密度二者相关,通常以比体积作为状态参数 。
Fundamentals of thermal engineering
热 工 基 础
1-3 状态方程与状态参数坐标图 1 状态公理 对于和外界只有热量和体积变化功(膨胀功或 压缩功)的简单可压缩系统,只需两个独立的参数 (如p、v;p、T 或v、T)便可确定它的平衡状态。
温度相等
热平衡
Fundamentals of thermal engineering
热
工基Βιβλιοθήκη 础1-2 平衡状态和状态参数
② 热力学温标(绝对温标) 英国物理学家开尔文(Kelvin)在热力学第二定 律基础上建立,也称开尔文温标。用符号 T 表示, 单位为 K(开)。
热力学温标取水的三相点为基准点,并定义其 温度为273.16 K。温差1K相当于水的三相点温度的 1/273.16.。
规定:系统对外界作功“+”,外界对系统作功“-”
膨胀:dv > 0 , w > 0
Fundamentals of thermal engineering
热力学基本概念

热源
吸热
热机
作功
放热
冷源
A
9
§1-2 热力系统
1 系统与边界
热力系统(热力系): 人为分割出来作为热力学分析对象的有限物质
系统
外界:热力系统以外的部分 边界:系统与外界之间的分界面
边界可以是实在的,也可以是假想的; 可以是固定的,也可以是移动的
A
10
§1-2 热力系统 热力系统选取的人为性
过热器
热力过程:吸热、膨胀A 作功和排热。
7
名词定义:
工质: 实现热能和机械能相互转化的媒介物质。
热源(高温热源) : 工质从中吸取热能的物系。
冷源(低温热源) : 接受工质排出热能的物系。
A
8
热能动力装置的工作过程可概括成:
工质从高温热源吸热,将其中一部分转 化为机械能而作功,并把余下部分传给低温 热源。
A
41
§1-5 状态方程、状态参数坐标图
2、状态方程
• 温度、压力和比体积这三个基本状态参
数之间的函数关系是最基本的热力学函数
关系,称为状态方程
vf(p,T) f(p,v,T)0
状态方程式是平衡状态下基本状态参数p、 v、T之间的关系
状态方程式的具体形式取决于工质的性质
A
42
§1-5 状态方程、状态参数坐标图
•••
★ ★★ ★
★ ★ ★
★★
★
★
★
★
★
48
§1-7 过程功和热量
功的定义
1、力学定义: 力 在力方向上的位移 2、热力学定义
a、当热力系与外界发生能量传递时,如果对外界 的唯一效果可归结为取起重物,此即为热力系对 外作功。
《工程热力学》第一章 基本概念

9
1.3.1、基本术语-状态、状态参数
1、状态:工质在热力变化过程中某一瞬间所呈现的宏观 物理状况称状态
2、状态参数:表示状态特征的物理量称为状态参数
状态与状态参数是一一对应的
3、状态参数特点
数学特征为点函数: 微元变化的微增量具全微分性质
4、热力学基本状态参数为三个:比容、压力、 温度
10
1.3.2、基本状态参数--比容及密度
C 1 2 B B A
16
1-4
平衡状态、状态方程式、坐标图
1.4.1 平衡状态与非平衡态 平衡状态:系统在不受外界影响的条件下, 如果宏观热力性质不随时间而变化,系统 内、外同时建立了热平衡、力平衡(及 化学平衡),此时系统所处状态为平衡态 非平衡态: 系统与外界,系统内部各部分间 存在能量传递及相对位移,状态将随时间 变化,称系统处于非平衡态
受逐渐变化的压力作用下的活塞的移动过程 发生系统状态变化 (力作用)(NEXT)
受变化的恒温热源缓慢加热的活塞系统发生 系统状态变化(热的作用) (NEXT)
26
P3 P2
P1
工质 工 质
工质
受逐渐变化压力作用下的活塞移动过程发生系 统状态变化(P、V、T变化) (力作用)
27
工质
工质
工质
热源T
31
1-6
过程功与热量
1.6.1 功的定义: 1、功的力学定义: 将物体间通过力的作用而传递的能量称为功并 定义:功等于力F与物体在力作用方向上的位移X 的乘积(点积) dW = F ·dX 2、功的热力学定义: 热力学系统和外界通过边界而传递的能量, 其效果可表现为举起重物
区别:功与系统动能、重力位能等“储存能”变化传递 的机械能的本质区别
工程热力学基本概念

= 收获/代价
炉
热效率: t
w net q1
顺 时 针
汽轮机
发电机 凝 汽 器
逆向循环 又称制冷循环或热泵循环
高温热源
或 制 Q1
逆 时
热冷 泵机
W
针
Q2
低温热源
制冷循环的经济性用制冷系数衡量:
2
1
1,a,2
1,b,2
b
2
状态参数的变化只与初终态相关,
1 dxx2 x1 与路径无关。
状态参数都有以上特性。
状态参数的循环 dx 0 积分等于零。
反之,有以上特性之一, 即为状态参数。
1-3 平衡状态、状态方程式、坐标图
一、平衡状态
热力系在没有外界作用的情况下〔重力场除 外〕,宏观性质不随时间变化的状态。
热力过程:工质由一个状态变化到另一状态所经历 的全部状态的总和。
实际过程由一系列非 平衡状态组成
例:
非平衡状态
无法简单描述
平衡状态
宏观静止
能量不能转换
“平衡〞意味着宏观静止, 引入 理想模型:
“过程〞意味着变化,意味着
准平衡过程
平衡被破坏。二者如何统一?
一、准平衡过程 热力系从一个平衡态连续经历一系列
系统与外界 通过边界进 展相互作用
热力系的选取主要决定于研究任务 。
选取热力系时注意:
❖热力系可以很大,但不能大到无限。
❖热力系可以很小,但不能小到只包含少量分子, 以致不能遵守统计平均规律。
❖ 边界可以是实际存在的, 也可以是假想的。
❖ 边界可以是固定的, 也可以是变动的。
系统与外界通过边界进展相互作用。
平衡的中间态过渡到另一个平衡态
《工程热力学》PPT课件

n从到0,放热→0 →吸热;等温线右内能增加,左内能减少。 例如压缩机压缩过程:K>n>1
第五节 热力学第二定律
重点掌握:
1、热力学第二定律的表述; 2、热力循环的热效率; 3、卡诺循环的热效率。
一、热力学第二定律的表述
1、热量不可能自发的、不付任何代价的由一个低温物 体传至高温物体。—热量不可能自发地从冷物体转移到
K= cp/cν:绝热指数
3、参数间的关系: 由 Pvk=常数 →P1v1k=P2v2k →P1/P2=(v2/v1)k 又 Pv=RT →P=RT/v →Tvk-1=常数 →T1/T2=(v2/v1)k-1 →T2=T1(v1/v2)k-1 =T1εk-1 4、过程量的计算: 推出: w=-u q=w+ u q=0
一、定容过程
1、定义:过程进行中系统的容积(比容)保持不变
的过程。
2、过程方程式:ν =常数 3、参数间的关系: 由 PV=RT 知,P/T=常数, 所以: P1/P2=T1/T2, P1/T1=P2/T2 4、过程量的计算: 又 q=Δ u+w, 由 W=∫PdV, 且 dV=0
→ w=0
→ q=Δ u
热力系统从一个平衡状 态到另一个平衡状态的变 化历程。
力过程。
二、膨胀功W(J)
气体在热力过程中由于体 积发生变化所做的功(又 称为容积功)
规定:热力系统对外界做功为正,外界对热
力系统做功为负。 由δ W=PdV得: dV>0,膨胀,δ W>0, 系统对外界做功; dV<0,压缩,δ W<0, 外界对系统做功; dV=0,δ W=0, 系统与外界之间无功量 传递。
四、课程的特点、要求、学时分配、考核
特点:本课程理论性较强,无多少实物供参照,课堂上的 讲授以理论分析和推导为主。
工程热力学(第五版)第一章课件

1.2.5 基本状态参数
U形管式压力计示意图
pb
U形管式压力计示意图
pb
p pb
p pb
p
pg
p pb pg
p
pv
p pb pv
真空度
当工质是处于负压工作状态时,工质的真实压力p低于环境压力pb,
其测量得到的相对压力称为真空度 p v 。
第1章 基本概念
1.2 热力系统的状态和状态参数
1.2.5 基本状态参数
例1-2某刚性容器被分隔为两部分,在容器壁上分别装有三个压力表,表B的 读数为80kPa,表C的读数为100kPa,试问压力表A的读数是多少? 设当地大气压为770mmHg。 已知: pgB 80kPa, pgC 100kPa, pb 770mmHg。 求 : pgA ? 解 由图示依据真实压力、参考压力和 相对压力之间的关系,可写出如下3 个关系式,从中整理出所求量。
物质 (水蒸气)
热力系统
物质 (凝结水)
蒸汽放热给冷却1.2 热力系统的分类
第1章 基本概念
1.1 热力系统 1.1.2 热力系统的分类
开口热力系(水泵示意图)
开口热力系统(水泵示意图)
锅炉给水 来自冷凝器的水
电动机
水 泵
水泵的简化热力学分析模型
水泵的简化热力学分析模型
边 界的特性 可以是真实的,也可以是假想的;可以是固定的,也可以是
运动的。
第1章 基本概念
1.1 热力系统
1.1.1 热力系统的定义
热力系统、界面、外界
热力系、界面、 外界例Ⅳ
界面
系
统
界面是真实的、固定不动的
第1章 基本概念
1.1 热力系统
工程热力学全部课件pptx

与外界没有物质和能量交 换的系统。
孤立系统
封闭系统
开放系统
热力学基本定律
热力学第零定律
如果两个系统分别与第三个系统处于热平衡状态,那么这两个系统也必定处于热平衡状态。
热力学第一定律
热量可以从一个物体传递到另一个物体,也可以与机械能或其他能量互相转换,但是在转换过程中,能量的总值保持 不变。
热力学第二定律
热力学循环
由一系列热力学过程组成的闭合路径,如卡诺循环、布雷顿循环 等。
02 热力学第一定律
能量守恒原理
1
能量不能自发地产生或消失,只能从一种形式转 换为另一种形式。
2
在一个孤立系统中,总能量始终保持不变。
3
能量转换过程中,各种形式的能量在数量上保持 平衡。
热力学第一定律表达式
Q = ΔU + W
其中,Δ(mv^2)/2表示系 统动能的变化量;
开口系统能量方程可表示 为:Q = ΔU + Δ(mv^2)/2 + Δ(mgh) + Δ(mΦ)。
Δ(mgh)表示系统势能的 变化量;
03 热力学第二定律
热力学第二定律表述
不可能从单一热源取热,使之完全转 换为有用的功而不产生其他影响。
热力学系统内的不可逆过程总是朝着 熵增加的方向进行。
具有加和性
理想气体基本过程
01
等温过程
温度保持不变的过程,如等温膨胀 和等温压缩
等容过程
体积保持不变的过程,如等容加热 和等容冷却
03
02
等压过程
压力保持不变的过程,如等压加热 和等压冷却
绝热过程
系统与外界没有热量交换的过程, 如绝热膨胀和绝热压缩
04
《工程热力学》 第一章—基本概念

状态参数的分类
★ 基本状态参数:可以直接测量的状态参数。 如压力p、温度T、比体积v。 ★ 导出状态参数:由基本状态参数间接求得的 参数。 如内能U、焓H、熵S等。
1. 压力
● 压力的定义
◆ 沿垂直方向作用在单位面积上的力称为压
力(即物理中压强)。
◆ 对于容器内的气态工质来说,压力是大量 气 体分子作不规则运动时对器壁单位面积撞 击 作用力的宏观统计结果。
压力的单位
压力的单位是N/m2 ,符号是帕(Pa)
常用压力单位的换算见附表1(222页)
1 atm = 760 mmHg = 1.013105 Pa
1 at = 1 kgf/ cm2 = 9.8067 104 Pa
1 MPa = 106Pa= 103kPa= 10bar
压力的表示方法
◆ 绝对压力(p)、表压力(pg)、
如果系统的宏观状态不随时间变化,则该系
统处于平衡状态。
● 不能把平衡态简单地说成不随时间而改变的状态, 也不能说成外界条件不变的状态。
平衡态是指系统的宏观性质不随时间变化的状态。 ● 平衡与均匀:均匀系统一定处于平衡状态,
反之则不然。
● 实现平衡的条件
◆ 热平衡 ◆ 力平衡 ◆ 相平衡 ◆ 化学平衡 温度相等 压力相等 各相间化学位相等 反应物与生成物化学 位相等
2. 温度
◆ 传统:温度是物体冷热程度的标志。
◆ 微观:温度是衡量分子平均动能的量度。
T 0.5 m c2 T=0 0.5 m c2=0 分子一切运动停止,零动能。
● 热力学第零定律
◆ 热平衡:不同物体的冷热程度相同,则它们处于热平衡。 ◆ 热力学第零定律(热力学中的一个基本实验结果): 若两个热力系分别与第三个热力系处于热平衡,那么这 两个热力系也处于热平衡。
第1章 工程热力学基础

44
喷管出口流速计算:
根据稳定流动开口系统能量方程:
1 2 q h c gz ws 2
简化得到:
c2 2(h1 h2 ) c12
喷管出口流速c2 ,取决于喷管入口压力p1与喷管 出口环境压力pb(背压)之比; 进出口压力之比越大,喷管出口流速越高。
45
喷管是一种能量转换部件,通过截面的变化把 系统的储存能变成动能(提高流速)。
第1章 工程热力学基础
1-1 热能与机械能的转换过程 1-2 基本概念 1-3 热力学基本定律 1-4 热力过程与热力循环 1-5 热力学的工程应用
1
1-1 热能与机械能的转换过程
一、工程热力学
定义:工程热力学是研究热能与机械能的转换规律、 条件、方法,以及工程应用的一门学科。 燃料能源的利用方式: 燃料(化学能) →热能 →机械能 →电能
与热力学能相关的能量传递和转化过程,都 具有方向性,如传热、自由膨胀等。 自发过程:能够自动进行,不需要附加条件; 非自发过程:自发过程的反方向过程,需要在 一定的附加条件才能进行;
热力学第二定律研究内容: 研究能量传递和转换的方向、条件与转换限度。为非自发过程。 在制冷循环中,通过消耗机械能,实现热量从低温 热源传导高温热源。消耗机械能就是附加条件。 能量转换分析:
热力学能组成:
内动能+内位能、化学能、原子能…..(内能)
一般不涉及化学、原子反应时: U= Uk+Up
比热力学能u:单位质量工质的热力学能:
u=U/m,kJ/kg
内动能Uk:主要取决于系统温度T; 内位能Up:主要取决于系统压力p。
25
(五)焓H
概念:流体的热力学能与推动功之和,kJ;
喷管出口流速计算:
根据稳定流动开口系统能量方程:
1 2 q h c gz ws 2
简化得到:
c2 2(h1 h2 ) c12
喷管出口流速c2 ,取决于喷管入口压力p1与喷管 出口环境压力pb(背压)之比; 进出口压力之比越大,喷管出口流速越高。
45
喷管是一种能量转换部件,通过截面的变化把 系统的储存能变成动能(提高流速)。
第1章 工程热力学基础
1-1 热能与机械能的转换过程 1-2 基本概念 1-3 热力学基本定律 1-4 热力过程与热力循环 1-5 热力学的工程应用
1
1-1 热能与机械能的转换过程
一、工程热力学
定义:工程热力学是研究热能与机械能的转换规律、 条件、方法,以及工程应用的一门学科。 燃料能源的利用方式: 燃料(化学能) →热能 →机械能 →电能
与热力学能相关的能量传递和转化过程,都 具有方向性,如传热、自由膨胀等。 自发过程:能够自动进行,不需要附加条件; 非自发过程:自发过程的反方向过程,需要在 一定的附加条件才能进行;
热力学第二定律研究内容: 研究能量传递和转换的方向、条件与转换限度。为非自发过程。 在制冷循环中,通过消耗机械能,实现热量从低温 热源传导高温热源。消耗机械能就是附加条件。 能量转换分析:
热力学能组成:
内动能+内位能、化学能、原子能…..(内能)
一般不涉及化学、原子反应时: U= Uk+Up
比热力学能u:单位质量工质的热力学能:
u=U/m,kJ/kg
内动能Uk:主要取决于系统温度T; 内位能Up:主要取决于系统压力p。
25
(五)焓H
概念:流体的热力学能与推动功之和,kJ;
工程热力学-1第一章 基本概念

例1-2 P23 可逆过程功的计算关键:找到p和v之间的关系
三、过程热量
系统与外界之间依靠温差传递的能量称为热量。 符号:Q ;单位:J 或kJ。
单位质量工质所传递的热量用q 表示,单位为 J/kg 或 kJ/kg。
热量正负的规定: 系统吸热:q > 0 系统放热:q < 0
热量和功量都是系统与外界在相互作用的过程 中所传递的能量,都是过程量而不是状态量
热量如何表达?
热量是否可以用类似于功的
? 式子表示?
Entropy
引入“熵”
清华大学刘仙洲教授 命名为“熵”
在可逆过程中,系统与外界交换的热量与功量
的计算公式具有相的形式。
功量:
热量:
w pdv
qqTTds?
2
w 1 pdv
2
q 1 Tds
条件 准静态或可逆
可逆
s 称为比熵。比熵同比体积 v 一样是工质的状态 参数。
比熵的定义式:ds q
T
(可逆过程)
比熵的单位为J/ (kg·K) 或 kJ/ (kg·K)
对于质量为m的工质,
Q TdS
2
Q 1 TdS
S为质量为 m 的工质的熵,单位是 J/K。
示热图
2
w 1 pdv
2
q 1 Tds
在可逆过程中单位 质量工质与外界交换 的 热 量 可 以 用 T-s 图 (温熵图)上过程曲 线下的面积来表示。
消除一种 不平衡势差
达到某一 方面平衡
消除一种能量 传递方式
状态公理 对于组成一定的物质系统,该系统平衡态的
独立状态参数有 n +1
n-表示系统与外界进行准静功交换的数目
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
各压力单位之间的换算关系:
Pa bar
Pa
bar atm at
mmHg mmH2O
1 1×105
1×10-5 1
0.98692 0.10197 7.5006 0.101971 ×10-5 ×10-4 ×10-2 2
0.98692 1.01972 750.062 10197.2
atm 101325 1.01325 1
外),如果系统的状态参数不随时间变化, 则该系统处于平衡状态。
温差 — 热不平衡势 压差 — 力不平衡势 化学反应 — 化学不平衡势
平衡的本质:不存在不平衡势
平衡与稳定
稳定:参数不随时间变化
稳定但存在不平衡势差 去掉外界影响,
则状态变化 若以(热源+铜棒+冷源) 为系统,又如何?
稳定不一定平衡,但平衡一定稳定
破坏平衡所需时间
恢复平衡所需时间
(外部作用时间) >> (驰豫时间)
有足够时间恢复新平衡 准静态过程
准静态过程的工程应用
例:活塞式内燃机 2000转/分 曲柄 2冲程/转,0.15米/冲程
活塞运动速度=20002 0.15/60=10 m/s 压力波恢复平衡速度(声速)350 m/s
破坏平衡所需时间 (外部作用时间)
热平衡,则两个系统彼此必然处于热平衡。
温度测量的 理论基础 B 温度计
温度的热力学定义
处于同一热平衡状态的各个热力系, 必定有某一宏观特征彼此相同,用于描述 此宏观特征的物理量 温度。
温度是确定一个系统是否与其它系 统处于热平衡的物理量
温度的测量
温度计
物质 (水银,铂电阻) 特性 (体积膨胀,阻值) 基准点 刻度
工质种类
单元系 多元系
单相 相态
多相
简单可压缩系统
最重要的系统 简单可压缩系统 只交换热量和一种准静态的容积变化功
容积变化功
压缩功 膨胀功
§1-3 工质的热力学状态及其基本状态参数
状态 热力系统在某一个瞬间所呈现的宏观
物理状况称为系统的状态。
平衡状态
定义: 在不受外界影响的条件下(重力场除
§1-1 热能在热机中转变成机械能的过程
热能动力装置:
从燃料燃烧中得到热能,并利用热能得到动 力的设备。
化学能
热能
机械能
热能动力装置分为两大类: 燃气动力装置(内燃机、燃气轮机) 蒸汽动力装置(蒸汽轮机)
内燃机(汽油机)
工作过程:
吸气
排气
压缩
燃烧、膨胀
能量转换:
燃料 化学能
燃气 热能
机械能
大气
平衡与均匀
平衡:时间上 均匀:空间上
平衡不一定均匀,单相平衡态则一定是均匀的
为什么引入平衡概念?
如果系统平衡,可用一组确切 的参数(压力、温度)描述
状态参数
描述系统所处平衡状态的宏观物理量称为状态 参数。如温度、压力等。
基本状态参数: 压力、温度、比体积 不可测参数: 热力学能、焓、熵等 复合参数: 吉布斯函数、亥姆霍兹函数
华氏温标与摄氏温标的换算关系为:
t(℃)= 5 [tF(o F ) 32] 9
0℃ = 32 °F 100 ℃ = 212°F
二、压力
定义: 单位面积上所受的垂直作用力称为压力(即压强)
分子运动学说认为压力是大量气体分子撞击器 壁的平均结果。
压力计 测量工质压力的仪器。常见的压力计有压力表
存在能提供热能的能量源; 余下的热能排向环境介质。
结论:
各种形式的热机都存在以下几个相同的热力过 程:吸热、膨胀作功和排热。
名词定义:
工质: 实现热能和机械能相互转化的媒介物质。
热源(高温热源): 工质从中吸取热能的物系。
冷源(低温热源) : 接受工质排出热能的物系。
热能动力装置的工作过程可概括成:
状态参数的特性:
(1) 状态参数的积分特征
状态参数变化量与路径无关,只与 初终态有关。
数学上: 点函数、态函数
2
2
2
1
a
2
dz dz dz z2 z1
1 1,a 1,b
b
dz 0
例:温度变化 山高度变化
(2) 状态参数的微分特征
设 z =z (x , y)
1
735.559 ×10-4
13.5951 1
比体积(比容)v
vV m
[m3/kg]
工质聚集的疏密程度
物理上常用密度 [kg/m3]
v 1
§1-4 状态方程、坐标图
平衡状态可用一组状态参数描述其状态
想确切描述某个热力系,是 否需要所有状态参数?
状态公理:对组元一定的闭口系, 独立状态参数个数 N=n+1
T2 = T0
p
1.
.
2
p,T
v
准静态过程
p1 = p0+重物 T1 = T0
p0
假如重物有无限多层 每次只去掉无限薄一层 系统随时接近于平衡态
p
1.
p,T
. .
2
v
准静态过程有实际意义吗?
既是平衡,又是变化
既可以用状态参数描述,又可进行热功转换
疑问:理论上准静态应无限 缓慢,工程上怎样处理?
准静态过程的工程条件
有
是否传质
开口系
是否传热
非绝热系
是否传功
非绝功系
是否传热、功、质 非孤立系
无 闭口系 绝热系 绝功系 孤立系
1
m
Q W
4
1 开口系 1+2 闭口系
2 1+2+3 绝热闭口系
1+2+3+4 孤立系
3
非孤立系+相关外界
=孤立系
热力系统其它分类方式
其它分类方式
均匀系 物理化学性质
非均匀系
绝热简单可压缩系统 N = ?
状态方程 基本状态参数(p,v,T)之间 的关系
v f ( p,T) f ( p,v,T) 0
状态方程的具体形式
状态方程的具体形式取决于工质的性质 理想气体的状态方程
pv RT pV mRT
实际工质的状态方程???
座标图
简单可压缩系 N=2,平面坐标图
p 1
说明:
1)系统任何平衡态可 表示在坐标图上
2
v 常见p-v图和T-s图
2)过程线中任意一点 为平衡态
3)不平衡态无法在图 上用实线表示
§1-6 热力过程
平衡状态
状态不变化
能量不能转换
非平衡状态
无法简单描述
热力学引入准静态(准平衡)过程
一般过程
p1 = p0+重物 T1 = T0
p0
突然去掉重物 最终 p2 = p0
蒸汽动力装置
1-炉子 2-炉墙 3-沸水管 4-汽锅 5-过热器
6-汽轮机 7-喷嘴 8-叶片 9-叶轮 10-轴 11-发电机 12-冷凝器 13、14、16-泵 15-蓄水池
比较上述两种热机
不同点:构造和工作特性不同。
相同点:
存在某一种媒介物质以获得能量;(如内 燃机中混合气,蒸汽机中的水)
温标
定义:温标是指温度的数值表示法
温标三要素: 测温物质及其测温属性 基准点 分度方法
任选一种物质的某一测温属性,采用以上温标的规定 所得到的温标称为经验温标,经验温标依赖于测温物 质的物理性质。热力学理论指出可以建立一种不依赖 于测温物质的性质的温标,即热力学绝对温标。
常用温标
绝对K 摄氏℃
dz是全微分
dz
z x
y
dx
z y
x
dy
充要条件:
2z 2z xy yx
可判断是否 是状态参数
(3)常用的状态参数有:
压力P、温度T、体积V、热力学能U、 焓H和熵S,其中压力、温度和体积可直 接用仪器测量,称为基本状态参数。其 余状态参数可根据基本状态参数间接算 得。
第一章 基本概念
本章基本要求:
掌握工程热力学中一些基本术语和概念:热力系、 平衡态、准平衡过程、可逆过程等。
掌握状态参数的特征,基本状态参数p、v、T 的
定义和单位等。掌握热量和功量这些过程量的特 征,并会用系统的状态参数对可逆过程的热量、 功量进行计算。
了解工程热力学分析问题的特点、方法和步骤。
工质从高温热源吸热,将其中一部分转 化为机械能而作功,并把余下部分传给低温 热源。
热源
吸热
热机
作功
放热
冷源
§1-2 热力系统
系统:选取一定的工质或空间作为研究对象 外界:与系统发生质、能交换的物体统称外界 边界:系统和外界之间的分界面
边界特性
固定、活动 真实、虚构
热力系统分类
以系统与外界关系划分:
w =pdv
准静态过程的容积变化功
mkg工质:W =pdV
2
W pdV
1
1kg工质:w =pdv
2
w 1 pdv
p
p外
注意: 上式仅适用于
1
2
准静态过程
p
1.
p 1
示功图
W
mkg工质:
0℃=273.15K,t(℃)=T(K)-273.15
华氏温标:
1724年由德国人华氏(cabridl D Fahrenheit) 提出。他把水、冰和氯化铵的混合物作为制冷剂而获 得的当时可得到的最低温度作为0度,把人体的温度 作为96度,中间等分,这样的数字是由于当时广泛使 用12进位法。符号tF ,单位 °F。
