原子的构成
《原子的构成》参考教案

《原子的构成》参考教案一、教学目标知识与技能:1. 了解原子的定义和构成;2. 掌握原子核和核外电子的组成;3. 能够描述原子的电子排布。
过程与方法:1. 通过模型和图片,直观地展示原子结构;2. 利用实验和观察,探究原子内部构成;3. 运用思维导图,总结原子的构成。
情感态度价值观:1. 培养对科学探究的兴趣和热情;2. 增强对原子世界的认识和好奇心;3. 培养合作意识和团队精神。
二、教学重点与难点重点:1. 原子的定义和构成;2. 原子核和核外电子的组成;3. 原子的电子排布。
难点:1. 原子核和核外电子的相互作用;2. 电子排布的规律和原理。
三、教学准备教具:1. 模型和图片;2. 实验器材;3. 思维导图软件。
学具:1. 笔记本;2. 彩色笔。
四、教学过程1. 导入:通过展示原子模型图片,引导学生思考原子的构成;2. 新课导入:介绍原子的定义和构成,讲解原子核和核外电子的组成;3. 实验探究:分组进行实验,观察原子内部结构,引导学生总结原子核和核外电子的特点;4. 知识拓展:介绍电子排布的规律和原理;5. 课堂小结:让学生用自己的话总结原子的构成;6. 作业布置:布置相关的练习题,巩固所学知识。
五、教学反思通过本节课的教学,学生应该能够掌握原子的定义和构成,了解原子核和核外电子的组成,以及原子的电子排布。
在教学过程中,要注意引导学生参与实验和观察,培养学生的实践操作能力。
要关注学生的学习情况,及时解答学生的疑问,确保教学效果。
六、教学评价评价目标:1. 学生对原子构成的理解程度;2. 学生对原子核和核外电子的认识;3. 学生对电子排布的应用能力。
评价方法:1. 课堂提问和回答;2. 实验报告和观察记录;3. 作业完成情况和练习题的正确率;4. 思维导图的制作和展示。
七、教学拓展1. 介绍原子的同位素和原子序数的概念;2. 探讨原子内部结构与元素化学性质的关系;3. 引入原子核物理学的研究内容和最新进展。
原子的结构
原子: Na Mg Fe C(金刚石,石墨, 木炭) Si P He Ne等
离子: CuSO4 NaCl KMnO4 Na2CO3
2016/10/6
MgCl2
NaOH
等
22
由离子构成的物质
NaCl 由Na+和Cl-构成 CuSO4 由Cu2+和SO42-构成 MgCl2 由Mg2+和Cl-构成 KMnO4 由K+和MnO4-构成 Na2CO3 由Na+和CO32-构成 NaOH 由Na+和OH-构成
Fe3+ Cl﹣、OH-、CO32-、SO422016/10/6 14
(2)离子的分类: 阳离子:带正电的离子叫阳离子。 如 Na﹢ 、Mg2+、 Fe2+ 阴离子:带负电的离子叫阴离子。
如 Cl﹣、OH-、CO32-、SO42-
阴、阳离子由于静电作用而形 成不带电的化合物。如:Na﹢与 Cl﹣由于静电作用而结合成化合物 氯化钠NaCl(请看以下图示)
2016/10/6 3
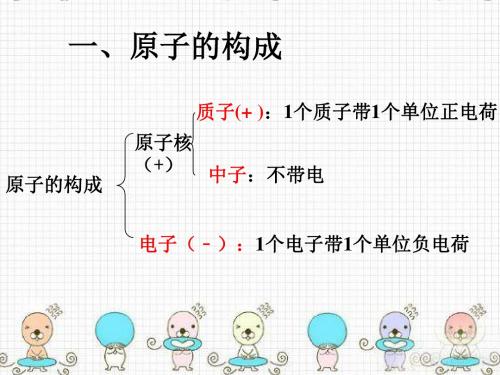
1、原子的构成: (核电荷数)
质子
(+)
1个质子带一个 单位正电荷
原子核
(+)
中子 不带电
原子
( 电中性 ) (-) 2、原子不显电性:因为原子中:
2016/10/6
核外电子
一个电子带一个单位 负电荷
核电荷数=质子数=核外电子数
4
例5:填空
在分子、原子、原子核、质子、中子、电子等 微粒中,找出符合下列条件的微粒,填空。 • 能直接构成物质的是( 分子、原子 ) • 能保持物质化学性质的是( • 带正电荷的是( • 带负电荷的是(
2016/10/6
构成原子的三种粒子

构成原子的三种粒子
“原子的构成是什么?”这是科学家探索宇宙的最终目标,从20世纪以来,关于原子的研究一直受到关注。
原子由三种基本粒子构成:电子,中子和质子。
电子是最著名的原子粒子之一,它是原子结构中最轻,最小的粒子。
电子有极少的质量,它们在原子的外层中围绕着原子核运行。
这些电子的外壳可分为若干能层,每个能层都有一定数量的能量水平。
当电子跃迁到较高的能量水平时,原子就会发出光谱,从而显示出原子的状态。
中子也是原子的组成部分,它们与电子一样,但他们的质量比电子要大得多。
中子质量非常大,比电子质量大20多倍,但它们的电荷为零,它们不会吸引或排斥电子,因而不会对原子结构产生影响。
质子是原子结构中最重要的粒子,它们有极大的质量,质量是电子的1800多倍,它们是原子核的主要组成部分。
质子有正电荷,它们吸引电子,使其围绕原子核运行并产生原子结构。
总而言之,原子由三种基本粒子构成:电子,中子和质子。
电子在原子的外层中围绕着原子核,中子的质量比电子大得多,而质子则有正电荷,用于吸引电子,使其形成原子结构。
各种分子的性质,如弹性,硬度,熔点和溶解性等,都决定于原子的组成。
因此,研究原子的组成对于我们了解宇宙是非常重要的。
- 1 -。
3.2.2原子的构成

F→F- S → S2- Cl→Cl-
+ Na→Na
+ Li→Li
K→K+ 2+ Ca→Ca
Mg→Mg2+ 3+ Al→Al
原子和离子的联系和区别
联系:
阳离子
区 别
失电子
原子 得电子
得电子
阴离子 失电子
原子中:质子数=电子数(原子不带电) 阳离子中:质子数>电子数(带正电) 阴离子中:质子数<电子数(带负电)
化合物由分子或离子构成。
一般情况下,有金属阳离子(或铵 + 根离子NH4 )的化合物由离子构成, 否则由分子构成。
本节课小节
1、离子形成、书写、意义
2、离子与原子的区别和联系
3、物质与其粒子的关系
同一类原子的总称
宏观 组成
微观 构成
只论种类 不论个数
既论种类 又论个数
【基础练习】
1.要能够分清原子结构示意图、离子结构示意图 2.要能够根据示意图写出对应的符号 Na
3.2.2原子的结构
一.原子的结构:
质子
原子核
每个质子带一个单 位的正电荷
1. 原 子 核外电子
中子
不带电
每个电子带一个单位的 负电荷
(一个原子只有一个原子核)
核外电子占 据 原 子 的 绝 大 部 分 体 积.
2.原子构成的规律:
⑴、核电荷数 = 质子数 = 核外电子数
(原子核所带的电荷数简称为核电荷数)
• 一个氢原子的质量是:1.67×10-27㎏, • 一个氧原子的质量是:2.657×10-26㎏, • 一个铁原子的质量是:9.288×10-26㎏。
这样小的数字,书写、记忆和使用起来都很 不方便,就像用吨做单位来表示一粒稻谷或小 麦的质量一样,能不能用一种好写、好记、好 用的方法来表示原子的质量呢?
原子的构成PPT课件(30)

原子的构成示意图
一、原子的结构
质子(每个质子带一个单位正电荷)
原子核
不
(居于原子中心)
原
(带正电) 中子(不带电)
子
显 电 性
电子 (每个电子带一个单位负电荷)
(原子核外)
原子核所带的正电荷数叫核电荷数
对于原子来说:核电荷数=核内质子数=核外电子数
观察表格
原子种类 氢 碳 氧 钠 氯 铁
标准碳原子质量的1/12
注意点:
1 相对原子质量不是原子的实际质量,是一个比值 2 相对原子质量的单位是1(略去不写)
找规律:相对原子质量的近似值与该原子的质子数,中子数的关系
原子种类
氢 碳 氧 钠 氯 铁
质子数
1 6 8 11 17 26
中子数 核外电子数
0
1
6
6
8
8
12
11
18
17
30
26
相对原子质量 (近似值)
身体健康,学习进步!
原子的质量绝大部分集中在原子核上,核外 电子的质量忽略不计
归纳:原子是由居于原子中心带正 电的原子核和核外带负电的绕核 作高速运动的电子构成的;原子核 在原子中只占很小的体积,但集 中了原子的绝大部分的质量;原 子中质子数等于核外电子的数, 它们数量相同电性相反,所以原 子不带电
二、相对原子质量
4、阳离子:带正电荷的原子叫做阳离子。 如: H+ 、Na+、 Mg2+ 、Al3+
氯化钠的形成
Na
Cl
Na+
Cl-
NaCl
化学反应中的离子:
NaCl
元素的性质与原子核外最外层电子数的关系
课题2 原子的构成

原子的构成知识点一:原子的构成1.原子是由下列粒子构成的:原子由原子核和核外电子(带负电荷)构成,原子核由质子(带正电荷)以及中子(不带电)构成,但并不是所有的原子都是由这三种粒子构成的。
例如:普通的氢原子核内没有中子。
2.原子中的等量关系:核电荷数=质子数=核外电子数在原子中,原子核所带的正电荷数(核电荷数)就是质子所带的电荷数(中子不带电),每个质子带1个单位正电荷,每个电子带一个单位负电荷,原子整体是呈电中性的粒子。
3.原子内部结构揭秘—散射实验(如下图所示):1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时,发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。
实验结论:(1)原子核体积很小,原子内部有很大空间,所以大多数α粒子能穿透金箔;(2)原子核带正电,α粒子途经原子核附近时,受到斥力而改变了运动方向;(3)金原子核的质量比α粒子大得多,当α粒子碰到体积很小的金原子核被弹了回来。
【要点诠释】1.原子是由居于原子中心带正电的原子核和核外带负电的电子构成,原子核又是由质子和中子构成,质子带正电,中子不带电;原子核所带正电荷(核电荷数)和核外电子所带负电荷相等,但电性相反,所以整个原子不显电性。
2.区分原子的种类,依据的是原子的质子数(核电荷数),因为不同种类的原子,核内的质子数不同。
知识点二:相对原子质量1.概念:以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比,就是这种原子的相对原子质量(符号为Ar)。
根据这个标准,氢的相对原子质量约为1,氧的相对原子质量约为16。
2.计算式:【要点诠释】1.相对原子质量只是一个比值,单位是“1”(一般不读也不写),不是原子的实际质量。
2.每个质子和每个中子的质量都约等于1个电子质量的1836倍,即电子质量很小,跟质子和中子相比可以忽略不计。
初三化学:原子的构成

第 1 页 共 1 页 初三化学:原子的构成
一、原子的构成
1. 原子的构成
原子由原子核和电子构成,原子核由质子和中子构成。
2. 每个质子带一个单位正电荷,每一个电子带一个单位负电荷,中子不带电。
原子核所带的正电荷数为核电荷数。
电子的质量很小,可忽略不计,原子的质量主要集中在原子核上。
3. 构成原子的粒子一般是质子、中子、电子。
构成原子的必要粒子是质子和电子,决定原子种类的是质子。
4. 原子核所带正电荷数(核电荷数)和核外电子所带负电荷数相等,但电性相反,所以整个原子不显电性。
5. 在原子中
核电荷数=质子数=电子数,
原子核内质子数不一定等于中子数。
二、相对原子量
国际上以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子量(A r )。
注意:相对原子量只是一个比,不是原子的实际质量。
相对原子量的计算公式:
12
112r ⨯=原子的质量碳一个原子的质量A 电子的质量很小,跟质子和中子相比可以忽略不计,所以
A r ≈质子数+中子数。
课题2 原子的构成

≥ 4个
得失电子
化学性质
稀有气体元素 =8个(He为2个)
金属元素 非金属元素
稳定 易失电子 易得电子
稳定 不稳定 不稳定
总结:
元素的化学性质主要是由最外层电子数决定的。 最外层电子数相等,化学性质就相似。 注意: He最外层2个电子,属于稳定结构。
例1、下列各组原子结构示意图中,所表示的两种元 素具有相似化学性质的是( A )
+1 1
氢(H)
1~18号元素原子 结构示意图
+2 2
氦(He)
+10
+3 2 1 +4 2 2 +5 2 3 +6 2 4 +7 2 5 +8 2 6 +9 2 7
28
锂(Li) 铍(Be) 硼(B) 碳(C) 氮(N) 氧(O) 氟(F) 氖(Ne)
+11 2 8 1 +12 2 8 2 +13 2 8 3 +14 2 8 4 +15 2 8 5 +16 2 8 6 +17 2 8 7 +18 2 8 8
1、六种粒子结构示意图分别为:
+8 2 6 +8 2 8
+10
28
+11
28
+12
28
+16
286
结论: 原子是由居于原子中心的体积很小,质
量很大,带正电的原子核和核外很大的 空间构成的。
结论: 原子是由居于原子中心的体积很小,质
量很大,带正电的原子核和核外很大的 空间构成的。 电子在核外作高速运动。
一、原子的构成
质子 原子核
(+) (0)
《原子的构成》板书设计【优秀8篇】

《原子的构成》板书设计【优秀8篇】(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如计划报告、合同协议、心得体会、演讲致辞、条据文书、策划方案、规章制度、教学资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of classic sample essays, such as plan reports, contract agreements, insights, speeches, policy documents, planning plans, rules and regulations, teaching materials, complete essays, and other sample essays. If you would like to learn about different sample formats and writing methods, please stay tuned!《原子的构成》板书设计【优秀8篇】化学是我们常考的科目之一、化学中有哪些知识点需要我们掌握?它山之石可以攻玉,下面本店铺为您精心整理了8篇《《原子的构成》板书设计》,如果能帮助到亲,我们的一切努力都是值得的。
原子的构成

4.1原子的构成【学习目标】1.了解原子的构成.2.了解相对原子质量.3.理解核电荷数、质子数、核外电子数的关系.【基础知识精讲】※课文全解一、原子的构成原子是由居于原子中心带正电的原子核和核外带负电的电子构成的.原子核是由质子和中子构成的.位置电性特点原子核居原子中心带正电体积小质量大(原子的主要质量都集中在核上) 核外电子居于核外带负电绕核按一定规律高速运动原子核为什么带正电呢?是因为原子核是由带正电的质子和不带电的中子构成.原子核所带的正电荷数(又称核电荷数)等于核内的质子数,质子数与核外电子数相等,原子核所带的电量与核外电子的电量相等,电性相反,所以原子作为一个整体不显电性.电性电量相对质量质子带正电一个单位正电荷 1中子不带电不带电 1电子带负电一个单位负电荷1/1836原子是很小的微粒,原子核更小,它的半径约为原子半径的万分之一.质子的质量与中子的质量大致相等,电子的质量约为质子质量的1/1836,原子的质量主要集中在原子核上.电子在原子核外空间里围绕着原子核作高速运动.二、相对原子质量原子的质量极小,不同的原子质量又不同,如何衡量原子的质量呢?为了书写和使用方便,国际上采用相对质量.以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得的比值,就作为这种原子的相对原子质量(符号为A r),根据这个标准氢的相对原子质量约为1,氧的相对原子质量约为16,碳的相对原子质量为12.跟质子、中子相比,电子质量很小,可以忽略不计,所以,原子的质量主要集中在原子核上,质子和中子的相对质量均为1,所以原子的相对质量又近似等于质子数和中子数之和.原子种类质子数中子数核外电子数相对原子质量氢 1 0 1 1碳 6 6 6 12氧8 8 8 16钠11 12 11 23硫16 16 16 32※问题全解1.什么是12C原子?答:12C原子是指含有6个质子和6个中子的碳原子,它的质量的1/12 等于1.66×10-27 kg.2.原子的构成是怎样的?核电荷数=质子数=核外电子数3.为什么原子不显电性?答:因为在原子内核电荷数=质子数=核外电子数,所带电量相等,但电性相反,所以原子不显电性.4.如何计算相对原子质量,它与原子质量有何区别?相对原子质量是原子质量的相对质量,它是一个比值,国际上规定它的单位为“一”,而原子质量是原子的实际质量,国际单位为“kg”.【学习方法指导】原子的构成是微观世界中的一个现象,肉眼看不到,因此让人觉得很抽象,但是如果同学们在学习的时候将微观世界宏观化,参考恰当的比喻,直观的图象,相信你一定能学好.[例]下列说法是否正确?1.原子是构成物质的一种粒子.2.因为二氧化碳里含有氧分子,所以二氧化碳也具有氧气的化学性质.3.一切原子核都是由质子和中子构成.4.原子的质量主要集中在原子核上.5.原子中质子和电子所带电量相等,电性相反,所以整个原子不显电性.答案:1.对2.错3.错4.对5.对点拨:1.构成物质的微粒有多种,有的物质是由分子构成的,如氧气、水等,有些物质是由原子直接构成的,如铁、氦气等,所以此说法正确.2.二氧化碳属于纯净物,它是由同一种分子——二氧化碳分子构成,每个二氧化碳分子又是由一个碳原子和两个氧原子构成,其中并不含氧分子,也就不具有氧气的化学性质,所以此说法是错误的.3.绝大多数原子核都是由质子和中子构成,但是有一种最常见的氢原子核却只有一个质子,而没有中子,所以“一切”的提法是不正确的.4.原子是由原子核和核外电子构成,原子核又是由质子和中子构成,由于原子质量很小,一个电子的质量只约等于一个质子(或一个中子)质量的1/1836,所以原子的质量主要集中在原子核上.5.原子是由带正电的原子核和核外带负电的电子构成,而且原子的核外电子数等于质子数即核电荷数,这样正负电荷的电量相等而且互相抵消,所以原子是显电中性的.[例2]原子R 核外有26个电子,核内有30个中子,它的质子数为_________,相对原子质量约为_________.解:已知R 原子核外有26个电子,则核内有26个质子,又因核内有30个中子,所以相对原子质量约为56.答案:26,56.点拨:此题是应用了两个相等关系,即原子内核电荷数=质子数=核外电子数,相对原子质量≈质子数+中子数.[例3]碳—12原子的质量为1.993×10-26kg ,某原子的相对原子质量是80,则该原子的质量是_________ kg .解:碳—12原子质量的121为12kg 10993.126-⨯≈1.66×10-27 kg 则该原子的质量为:1.66×10-27kg ×80=1.328×10-25kg .答案:1.328×10-25点拨:本题考查的是原子的质量和相对原子质量关系的计算,解题的关键是要搞清原子的质量和相对原子质量二者的区别和联系.(1)相对原子质量不是原子的实际质量,而是一个比值. (2)相对原子质量=121C 12⨯原子质量该原子质量【拓展训练】 一、道尔顿道尔顿(1766~1844),英国科学家,近代原子学说的奠基人.道尔顿与法拉第、布朗、歌德等属同一时代的人.他从15岁起就开始了边教课,边自学,边研究,边写作的道路,他的科学启蒙老师是一位双目失明的学者.道尔顿的第一部科学著作是《气象观测论文集》.他曾经连续亲自记录气象数据达56年之久,全部观测记录超过22万条.这对他日后提出并用实验证明他的原子学说起到了有益的作用.道尔顿一生勤奋、坚韧,他患有色盲症,但却从不妥协,而且把色盲症作为自己的一个研究课题.道尔顿原子学说的主要观点是:一切物质都是由分子组成的,各种分子又是由更小的粒子——原子构成的.道尔顿利用化学分析法进行研究,发现了著名的倍比定律,也正是这一定律的发现,确立了原子论的实验基础,从而使道尔顿成为近代原子论的奠基人.道尔顿一生著书50多部,其中最重要的是《化学哲学新体系》(中国科学院藏有此书).为了纪念他,英国曼彻斯特大学于1853年设立了道尔顿奖学金.二、扫描隧道显微镜扫描隧道显微镜是80年代初期发展起来的新型显微仪器,能达到原子级的超高分辨率.扫描隧道显微镜不仅作为观察物质表面结构的重要手段,而且可以作为在极其细微的尺度——即纳米尺度(1 nm=10-9m)上实现对物质表面精细加工的新奇工具.目前科学家已经可以随心所欲地操纵某些原子.一门新兴的学科——纳米科学技术已经应运而生.中国科学院化学研究所隧道显微学研究室的科学家正奋力投入纳米科学技术的研究,运用扫描隧道显微学方法.1993年,中国科学院北京真空物理实验室的研究人员,在常温下以超真空扫描隧道显微镜为手段,通过用探针拨出硅晶体表面的硅原子的方法,在硅晶体的表面形成了一定规整的图形(见图4—2).这种在晶体表面开展的操纵原子的研究,达到了世界水平.图中的“中国”两字就是这样形成,并经放大约180万倍在计算机屏幕上显示出来的.这两个字的“笔画”宽度约2 nm,是目前已知的最小的汉字.。
原子的构成及元素

原子结构和元素【知识点】:一、原子的构成1. 原子结构示意图的认识注:1) 在原子中 核电荷数=质子数=核外电子数决定元素种类: 质子数(核电荷数)三决定 决定元素化学性质 :最外层电子数决定原子的质量 :原子核2) 原子的质量主要集中在 原子核 上 ,近似相对原子质量=质子数+中子数。
3) 最外层电子数决定元素的化学性质。
一般金属元素的原子最外层电子数小于4,在化 学反应中易失 去电子;非金属元素的原子最外层电子数大于4,在化学反应中易得到电子;稀有气体元素的原子既不易失去电子,也不易得到电子,化学性质稳定,最外层电子数为8(当只有1个电子层时,电子数为2的结构是稳定结构)。
4)最外层电子数相同其化学性质不一定都相同(Mg ,He 最外层电子数为2)最外层电子数不同其化学性质有可能相似(He ,Ne 均为稳定结构)2. 相对原子质量:碳12原子质量的112作为标准,其他原子的质量跟它的比值。
相对原子质量的单位是1。
相对原子质量=某种原子的质量(kg)/一个碳原子质量的1/12(kg )相对原子质量越大,原子的实际质量越大;两种原子的相对原子质量之比等于两种原子的质量之比。
相对原子质量≈质子数+中子数3. 分子、原子化学变化的实质:在化学变化中分子分裂为原子,原子重新合成新的分子(或原子重新组合)例题1 (2010·河北)右图是钠元素的原子结构示意图,下列叙述不正确...的是( )A .钠原子的质子数为11B .钠原子的最外层电子数为1C .钠原子易失去电子形成阳离子D .钠元素为非金属元素例题2 下列有关分子、原子和离子的说法正确的是( )A .分子是保持物质性质的一种粒子B .物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变C .分子、原子、离子都可以直接构成物质D .在化学反应中,任何离子都不能再分二.元素1.元素:具有相同核电荷数(即质子数)的一类原子的总称。
元素是组成物质的基本成分,是宏观概念,只讲种类不讲个数。
原子的构成

原子的构成1、原子的构成情况:2、电性关系不带电的微粒:中子、原子(分子);带负电荷的微粒:电子;带正电荷的微粒:原子核、质子3、电量关系:核电荷数=质子数(原因是中子不带电);质子数=电子数(原因是原子不带电)所以在原子中:核电荷数=质子数=电子数4、质量关系:m(原子)=m(原子核)+m(电子)≈m(原子核)[原因是一个电子的质量很小,可以忽略]由于一个原子的真实质量很小,使用不方便,提出一个相对原子质量的概念相对原子质量:一种碳原子(质子数为6,中子数为6的碳原子)的质量的1/12作为基准,其他原子的质量与这个基准的比值。
公式表达式:Ar(原子)=引申:相对分子质量:构成分子的各原子的相对原子质量的总和。
Mr(分子)=∑Ar(构成微粒的原子)例题:求出水的相对分子质量Mr(H2O)=2Ar(H)+Ar(O)=2×1+16=18第三节、原子的构成复习题1、关于相对原子质量的说法正确的是()A、相对原子质量是一个比值,没有单位B、相对原子质量不是原子实际质量,相对原子质量是原子的相对质量C、相对原子质量是碳原子质量的1/12作为标准,其他原子的质量跟它比较所得的值D、以上说法都不对2、下列关于原子核的说法正确的是()A、所有的原子核都是由质子和中子构成的B、原子核在原子中所占的体积很小C、原子核居于原子中心,带正电荷D、原子的质量主要集中在原子核上3、在原子里,质子数等于()A、核外电子数B、中子数C、最外层电子数D、电子层数4、原子核外电子总数,等于原子核内的()A、中子数B、质子数与中子数之和C、质子数与中子数之差D、质子数5、根据相对原子质量的定义,判断溴原子的相对原子质量为()A、79.9gB、1.325×10-25gC、159.8gD、79.96、若一个碳12原子的实际质量为mg,则实际质量为ng的原子的相对原子质量为()A、12n/mB、12m/nC、n/12mD、m/12n7、某原子R,相对原子质量为a,核内中子数为b,则其核外电子数为()A、a-bB、a+bC、b-aD、无法确定8、甲原子与乙原子的质量比为a:b,而乙原子与碳12原子的质量比为c:d,则甲原子的相对原子质量为() A、12ac/bd B、bc/12ad C、12bd/ac D、ad/12bc9、钠原子核由11个质子和12个中子构成,下列说法错误的是()A、钠原子的核电荷数为11B、钠的相对原子质量为23C、钠原子核外电子数为12D、钠的相对原子质量为23g10、一个碳原子的质量为5.4akg,R的相对原子质量为b/3,则一个R原子的质量应该是()A、5.4abkg B、0.15abkg C、1.8a/bkg D、b/3akg11、一个水分子中,含有的质子数为()A、3B、8C、10D、1812、R元素的一个原子质量是一个碳原子质量的12倍,则一个R原子的质量约为一个氧原子质量的() A、8倍 B、9倍 C、16倍 D、18倍13、美英联军在伊拉克战场上,不顾全世界人民的反对,使用了后患无穷的贫油弹,其中含有238U,它的相对原子质量为238,质子数为92,则238U中含有的中子数为()A、238B、92C、146D、33014、下列有关分子原子和离子的说法中错误的是()A、带电的原子或原子团叫离子B、分子是保持物质性质的最小粒子C、原子是不能再分的最小粒子D、原子、分子、离子都是构成物质的微粒15、具有相同质子数和相同核外电子数的两种微粒,它们不可能是()A、两种不同的离子B、两种不同的分子C、一种分子和一种离子D、一种分子和一种原子16、非金属元素的原子得到电子后发生变化的是()A、核外电子层数B、化学性质C、元素种类D、核内中子数A、a+m+nB、a-m-nC、a-m+nD、a+m-n17、有两种不同的原子,一种原子核内有18个中子和17个质子,另一种原子核内有20个中子和17个质子,则它们不相等的是()A、核电荷数B、核外电子数C、原子的质量D、原子的带电量18.如果一个碳12原子的相对原子质量为24,则不会改变的是()(A)氧的相对原子质量(B)一个碳12原子的实际质量(C)硫酸的相对分子质量(D)都不变19、在分子、原子、原子核、质子、中子、电子等微粒中找出符合下列条件的微粒填空:①能直接构成纯净物的是________②能保持化学性质的最小粒子是_______③化学变化中的最小粒子是________ ④带正电荷的是_____________⑤带负电荷的是_______ ⑥不显电性的是________⑦质量与氢原子质量大约相等的是___________⑧在同一原子中数目相等的是_______________ ⑨决定相对原子质量大小的是______数和________数⑩氢原子中不含有的是____________。
原子的构成 元素 离子

)定义:具有相同核电荷数(即核内质子数)的一类原子的总称。
氧元素最多,其次是碳元素和氢元素。
如果第一个字母相同,还必须附加一个小写字母以示区别
”中的数字表示一个水分子中含有两个氢原子。
按原子序数递增的顺序从左到右排列。
②将电子层数相同的元素排成一个横行。
按照最外层电子数递增的顺序从左到右排列;元素周期表是元素性质的周期性
:
非金属元素的原子易得到电子形成阴离子。
,共价化合物是由分子构成的。
五、物质的构成与组成:
纯净物是由同种或不同种组成的。
大多数纯净物是由分子构成的,如氧气、水……
少数物质是由原子构成的,如铁、氖气等。
还有少数物质是由离子构成的。
如NaCl是由Na+和Cl-构成
氯、钠两元素的原子结构示意图分别为。
填“原子”、“阳离子”或“阴离子”
(1)在元素周期表中,原子序数为12的元素符号是___________,其原子结构示意图为,在化学反应中该原子易________(填“得到”或“失去”)电子。
(2)写出原子序数为1、6、8、11四种元素所组成化合物的化学式。
《原子的构成》 知识清单

《原子的构成》知识清单一、原子的发现历程在人类探索物质世界的漫长历史中,对于原子的认识经历了一个逐步深入的过程。
早在古希腊时期,哲学家德谟克利特就提出了“原子”的概念,他认为万物是由不可分割的原子组成。
然而,这只是一种哲学上的思辨,缺乏科学的实验依据。
到了 19 世纪初,英国科学家道尔顿基于大量的实验研究,正式提出了近代原子学说。
他认为原子是不可再分的实心球体,同种元素的原子性质和质量都相同。
随着科学技术的不断进步,人们发现了更多关于原子的奥秘。
1897 年,英国物理学家汤姆生发现了电子,这一发现打破了原子不可再分的观念。
他提出了“葡萄干布丁”模型,认为原子是一个带正电的球体,电子像葡萄干一样镶嵌在其中。
1911 年,卢瑟福通过α粒子散射实验,提出了原子的核式结构模型。
该实验表明,原子的中心有一个很小的原子核,电子在原子核外绕核高速运动。
二、原子的构成原子是化学变化中的最小粒子,但原子并不是一个实心球体,它由居于原子中心的原子核和核外电子构成。
原子核由质子和中子组成。
质子带正电荷,中子不带电。
一个质子所带的电荷量与一个电子所带的电荷量相等,但电性相反。
核外电子带负电荷,它们在原子核外的一定区域内高速运动。
不同元素的原子,核外电子的排布不同。
原子中,质子数等于核外电子数,因此整个原子呈电中性。
原子的质量主要集中在原子核上。
质子和中子的质量大约相等,而电子的质量很小,几乎可以忽略不计。
以一个普通的氢原子为例,它只有一个质子和一个电子,没有中子。
而对于质量较大的原子,如碳原子,它有 6 个质子、6 个中子和 6 个电子。
三、质子数、中子数、核外电子数的关系在原子中,质子数等于核外电子数,这是保持原子电中性的关键。
质子数决定了元素的种类。
不同元素的原子,质子数不同。
中子数则不是固定不变的,同种元素的原子可能具有不同的中子数,这些原子互为同位素。
例如,氢元素有三种同位素,分别是氕(没有中子)、氘(一个中子)和氚(两个中子)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原子的构成【导学目标】1.了解原子是由质子、中子和电子构成的;初步了解相对原子质量的概念,并会查相对原子质量表。
2.通过阅读分析、比较归纳的方法来学习有关知识,培养学生观察能力、分析综合能力和抽象思维能力。
3.通过对原子结构及粒子间关系的学习,进行世界是物质的、物质是运动的等辨证唯物主义观点教育【导学难点】原子和相对原子质量概念的形成【导学重点】原子的构成【导学方法】以创设情境活动为核心的活动元教学【复习导入】同学们,在第三单元的学习中我们知道了分子、原子都是同同学们,在第三单元的学习中我们知道了分子、原子都是构成物质的微观粒子。
在理解了分子和原子概念的基础上,你能说出化学变化的实质是什么吗?(过渡启发)在化学反应里分子可以为原子,原子在化学反应里不能再分。
用其他方法能不能再分呢?创设情景:(图片展示)这是原子弹爆炸时的蘑菇云的图片。
1964年10月16日下午3时,在我国西部地区新疆罗布泊上空,一个的巨大火球和蘑菇云升上了戈壁荒漠,中国第一颗原子弹爆炸成功了,为什么原子弹有那么大的威力呢? 导入新课:这节课我们就学习原子的构成介绍原子结构认识的发展简史:(1) 汤姆生的西瓜子模型(2) 卢瑟福的行星模型引导得出:【导研】为什么原子不显电性?(原子核和核外电子所带的电量相等,但电性相反,所以不显电性。
)得到规律:核电荷数=核外电子数投影展示、评判讨论(介绍)1897年,在英国科学家汤姆生发现电子以后,人们开始揭示了原子内部的秘密。
(得到:核电荷数=核内质子数由于中子不带电,一个质子带个单位的正电荷,一个电子带1个单位的负电荷,又由于整个原子不显电性,所以得到:核外电子数=核内质子数(指导阅读)表4-2,你能发现什么规律?(指导阅读)P70页第一段,想像一下原子和原子核的大小,并谈一谈自己的感受。
[介绍]我们可以看到原子分为原子核和核外电子(教师引导)原子核很小,科学家经过研究证明原子核还可再分,引导学生动手用大括号的形式将原子的结构表示出来。
引导学生动手用大括号的形式将原子的结构表示出来。
知识巩固1.观察表4-2,以碳原子为例说明构成原子的粒子有几种?2.它们是怎样构成原子的?指导学生阅读教材P68的表4-2;引导学生根据表格内容比较和讨论。
阅读讨论、归纳小结:质子数=核外电子数核电荷数=质子数计算:1个钠原子的质量过渡(思考)原子那么小,有没有质量呢?原子虽然很小,但也有一定的质量。
通过现代科学仪器可精确地测出原子的实际质量。
这样小的数字,无论书写、读数、记忆和使用都极不方便。
正像以吨为单位来表示一粒小麦的质量一样不方便。
所以国际上采用原子的相对质量——相对原子质量来表示。
(阅读)课文相对原子质量概念内容及旁白课文附录国际相对原子质量表。
查出氮、氯、钠、铁四种原子的相对原子质量。
某原子的相对原子质量=一种碳原子的质量×1/12单位:一,符号:1,但不写出〔思考与讨论〕通过这段课文的阅读,你能初步弄清相对原子质量与原子结构之间的关系吗?〔巩固提问〕相对原子质量就是原子的实际质量?对吗?为什么?学生读表4-2,思考:相对原子质量数值和质子数、中子数的关系?学生小结:导评:原子的结构与相对原子质量作业:补充习题附:一、电子的发现电子的发现和阴极射线的实验研究联系在一起的,而阴极射线的发现和研究又是以真空管放电现象开始的.早在1858年,德国物理学家普吕克在利用放电管研究气体放电时发现了阴极射线.普吕克利用真空泵,发现随着玻璃管内空气稀薄到一定程度时,管内放电逐渐消失,这时在阴极对面的玻璃管壁上出现了绿色荧光.当改变管外所加的磁场时,荧光的位置也会发生变化,可见,这种荧光是从阴极所发出的射线撞击玻璃管壁所产生的。
阴极射线究竟是什么呢?在19世纪后30年中,许多物理学家投入了研究.当时英国物理学家克鲁克斯等人已经根据阴极射线在磁场中偏转的事实,提出阴极射线是带负电的微粒,根据偏转算出阴极射线粒子的荷质比(e/m),要比氢离子的荷质比大1000倍之多.当时,赫兹和他的学生勒纳德,在阴极射线管中加了一个垂直于阴极射线的电场,企图观察它在电场中的偏转,为此他们认为阴极射线不带电.实际上当时是由于真空度还不高,建立不起静电场.J.J.汤姆生设计了新的阴极射线管(图1),在电场作用下由阴极C发出的阴极射线,通过Α和B聚焦,从另一对电极D和E间的电场中穿过.右侧管壁上贴有供侧量偏转用的标尺.他重复了赫兹的电场偏转实验,开始也没有看见任何偏转.但他分析了不发生偏转的原因可能是电场建立不起来。
于是,他利用当时最先进的真空技术获得高真空,终于使阴极射线在电场中发生了稳定的电偏转,从偏转方向也明确表明阴极射线是带负电的粒子.他还在管外加上了一个与电场和射线速度都垂直的磁场(此磁场由管外线圈产生),当电场力eE与磁场的洛仑兹力evB相等时,可以使射线不发生偏转而打到管壁中央。
经过推算可知,阴极射线粒子的荷质比e/m≈1011C/kg.通过进一步的实验,汤姆生发现用不同的物质材料或改变管内气体种类,测得射线粒子的荷质比e/m保持不变.可见这种粒子是各种材料中的普适成分。
1898年,汤姆生又和他的学生们继续做直接测量带电粒子电量的研究.其中之一就是用威尔逊云室,测得了电子电荷是1.1x10-19C,并证明了电子的质量约是氢离子的千分之一.于是,汤姆生最终解开了阴极射线之谜.这以后不少科学家较精确地测量了电子的电荷值,其中有代表性的是美国科学家密立根,在1906年第一次测得电子电荷量e=l.34X10-19C,1913年最后测得e=1.59x10-19C.在当时条件下,这是一个高精度的测量值.近代精确的电子电荷量e=1.60217733(49)x10-19C(括号中的值是测量误差).二、原子结构的模型20世纪初汤姆生提出了原子的枣糕式模型:原子是一个球体,正电荷均匀分布在整个球内,而电子却象枣糕里的枣子那样镶嵌在原子里面.其缺陷是只能说明了原子中有电子的存在和电子带负电,不能正确表示原子的结构.葡萄干蛋糕模型1909-1911年,英国物理学家卢瑟福做了α粒子散射实验,否定了汤姆生模型,提出了原子的核式结构模型.汤姆逊(Joseph John Thomson,1856-1940)(右图)继续进行更有系统的研究,尝试来描绘原子结构。
汤姆逊以为原子含有一个均匀的阳电球,若干阴性电子在这个球体内运行。
他按照迈耶尔(Alfred Mayer)关于浮置磁体平衡的研究证明,如果电子的数目不超过某一限度,则这些运行的电子所成的一个环必能稳定。
如果电子的数目超过这一限度,则将列成两环,如此类捱以至多环。
这样,电子的增多就造成了结构上呈周期的相似性,而门得列耶夫周期表中物理性质和化学性质的重复再现,或许也可得着解释了。
汤姆逊提出的这个模型,电子分布在球体中很有点像葡萄干点缀在一块蛋糕里,很多人把汤姆逊的原子模型称为“葡萄干蛋糕模型”。
它不仅能解释原子为什么是电中性的,电子在原子里是怎样分布的,而且还能解释阴极射线现象和金属在紫外线的照射下能发出电子的现象。
而且根据这个模型还能估算出原子的大小约10-8厘米,这是件了不起的事情,正由于汤姆逊模型能解释当时很多的实验事实,所以很容易被许多物理学家所接受。
太阳系模型——有核原子模型英国物理学家欧内斯特·卢瑟福(Ernest Rutherford,1871~1937)1895年来到英国卡文迪许实验室,跟随汤姆逊学习,成为汤姆逊第一位来自海外的研究生。
卢瑟福好学勤奋,在汤姆逊的指导下,卢瑟福在做他的第一个实验——放射性吸收实验时发现了α射线。
卢瑟福设计的巧妙的实验,他把铀、镭等放射性元素放在一个铅制的容器里,在铅容器上只留一个小孔。
由于铅能挡住放射线,所以只有一小部分射线从小孔中射出来,成一束很窄的放射线。
卢瑟福在放射线束附近放了一块很强的磁铁,结果发现有一种射线不受磁铁的影响,保持直线行进。
第二种射线受磁铁的影响,偏向一边,但偏转得不厉害。
第三种射线偏转得很厉害。
卢瑟福在放射线的前进方向放不同厚度的材料,观察射线被吸收的情况。
第一种射线不受磁场的影响,说明它是不带电的,而且有很强的穿透力,一般的材料如纸、木片之类的东西都挡不住射线的前进,只有比较厚的铅板才可以把它完全挡住,称为γ射线。
第二种射线会受到磁场的影响而偏向一边,从磁场的方向可判断出这种射线是带正电的,这种射线的穿透力很弱,只要用一张纸就可以完全挡住它。
这就是卢瑟福发现的α射线。
第三种射线由偏转方向断定是带负电的,性质同快速运动的电子一样,称为β射线。
卢瑟福对他自己发现的α射线特别感兴趣。
他经过深入细致的研究后指出,α射线是带正电的粒子流,这些粒子是氦原子的离子,即少掉两个电子的氦原子。
“计数管”是来自德国的学生汉斯·盖革(Hans Geiger,1882-1945))发明的,可用来测量肉眼看不见的带电微粒。
当带电微粒穿过计数管时,计数管就发出一个电讯号,将这个电讯号连到报警器上,仪器就会发出“咔嚓”一响,指示灯也会亮一下。
看不见摸不着的射线就可以用非常简单的仪器记录测量了。
人们把这个仪器称为盖革计数管。
藉助于盖革计数管,卢瑟福所领导的曼彻斯特实验室对α粒子性质的研究得到了迅速的发展。
1910年马斯登(E.Marsden,1889-1970)来到曼彻斯特大学,卢瑟福让他用α粒子去轰击金箔,做练习实验,利用荧光屏记录那些穿过金箔的α粒子。
按照汤姆逊的葡萄干蛋糕模型,质量微小的电子分布在均匀的带正电的物质中,而α粒子是失去两个电子的氮原子,它的质量要比电子大几千倍。
当这样一颗重型炮弹轰击原子时,小小的电子是抵挡不住的。
而金原子中的正物质均匀分布在整个原子体积中,也不可能抵挡住α粒子的轰击。
也就是说,α粒子将很容易地穿过金箔,即使受到一点阻挡的话,也仅仅是α粒子穿过金箔后稍微改变一下前进的方向而已。
这类实验,卢瑟福和盖革已经做过多次,他们的观测结果和汤姆逊的葡萄干蛋糕模型符合得很好。
α粒子受金原子的影响稍微改变了方向,它的散射角度极小。
马斯登(左图)和盖革又重复着这个已经做过多次的实验,奇迹出现了!他们不仅观察到了散射的α粒子,而且观察到了被金箔反射回来的α粒子。
在卢瑟福晚年的一次演讲中曾描述过当时的情景,他说:“我记得两三天后,盖革非常激动地来到我这里,说:‘我们得到了一些反射回来的α粒子......’,这是我一生中最不可思议的事件。
这就像你对着卷烟纸射出一颗15英寸的炮弹,却被反射回来的炮弹击中一样地不可思议。
经过思考之后,我认识到这种反向散射只能是单次碰撞的结果。
经过计算我看到,如果不考虑原子质量绝大部分都集中在一个很小的核中,那是不可能得到这个数量级的。
”卢瑟福所说的“经过思考以后”,不是思考一天、二天,而是思考了整整一、二年的时间。
