原子的构成练习题2
经典初中化学原子结构(练习题)

经典初中化学原子结构(练习题)
下面是一些关于经典初中化学原子结构的练题,希望能帮助您巩固和提高对这一知识领域的理解。
1. 原子是物质的最小单位,它由什么组成?
答案:原子由质子、中子和电子组成。
2. 请问原子核中质子和中子的区别是什么?
答案:质子带有正电荷,中子不带电荷。
3. 原子核的质量是由质子和中子的质量之和决定的,请问原子核外的电子贡献了什么?
答案:原子核外的电子贡献了负电荷,使得原子整体处于电中性状态。
4. 请问在原子模型中,电子是如何排布的?
答案:根据原子模型,电子是按能级分布在原子的不同轨道上。
5. 在氢原子中,质子数和电子数相等吗?
答案:是的,氢原子中质子数和电子数相等,都是1。
6. 原子团和化合物中的原子是如何结合的?
答案:原子团和化合物中的原子通过化学键结合在一起。
7. 请问原子的核外电子是如何参与化学反应的?
答案:原子的核外电子通过与其他原子的核外电子进行共享、
转移或接受电子等方式参与化学反应。
这些练习题旨在帮助您回顾和巩固对经典初中化学原子结构的
理解,希望对您有所帮助。
如果您还有其他问题,请随时提问。
最新鲁教版九年级化学上册《第三节 原子的构成》习题2(精品同步练习)

《第三节原子的构成》习题一、选择题1.关于钠离子和钠原子的认识不正确的是()A.它们的质子数相同B.它们的电子层数不同C.Na比Na+少一个电子D.Na+的最外层是稳定结构2.下列粒子结构示意图中,表示阳离子的是()3.Ca2+右上角的数字表示的意义是()A.钙原子最外层上有2个电子B.钙原子有2个电子层C.钙离子带两个单位正电荷D.2个钙离子4.原子失去最外层电子或在最外层得到电子后,不发生变化的是()(1)元素种类(2)化学性质(3)相对原子质量(4)原子的电性(5)原子核(6)电子层数(7)最外层电子数A.(1)(3)(5)B.(2)(4)(6)(8)C.(2)(5)D.(1)(5)5.结构示意图所表示的粒子是()A.分子B.原子C.阳离子D.阴离子6.某元素R的原子核带x个正电荷,则R2+的核外电子总数为()A.x-2B.x+2C.xD.无法确定7.朝核问题引发了国际关注,核问题的关键是核能的如何利用。
已知某种核原料的原子核中含有1个质子和2个中子,那么()A.该原子是一种氢原子B.该元素是金属元素C.该原子核外有3个电子D.该原子核带2个单位的正电荷8.质子、中子、电子三种微粒,在原子内部的分布情况为()A.三种粒子均匀地分布于原子内B.质子和中子构成原子核,电子绕核高速旋转C.质子和电子构成原子核,中子绕核高速旋转D.质子和中子构成原子核,电子在原子核外一定空间内做高速运动9.有下面两句话:“若两种微粒属于同一种元素,则它们所含质子数一定相同”;“若两种微粒质子数相同,则它们一定属于同一种元素。
”对这两句话可做出的判断是()A.前者正确,后者错误B.前者错误,后者正确C.两者均正确D.两者均错误10.下列粒子中,最外电子层不是稳定结构的是()A.氖原子B.氯原子C.钠离子D.硫离子11.某元素原子的核外电子排由时,第二层电子数是第一层与第三层电子数之和,则该元素属于()A.金属元素B.非金属元素C.稀有气体元素D.不能确定二、填空题1.原子是________中的最小粒子,是指在________中不可再分,不等于原子不可再分。
初中化学《原子的结构》精品练习2

《原子的结构》精品练习1·锂电池可用作心脏起搏器的电源。
已知一种锂原子核内含有3个质子和4个中子,则该锂原子的核外电子数为()A. 1B. 3C. 4D. 7【答案】B【解答】在原子中,质子数=电子数,故选B。
2·原子不显电性的原因是()A.原子中不含带电荷的粒子B.原子太小了C.原子核和核外电子带等量的异种电荷D.原因至今不明【答案】C【解答】A、原子核内的质子带正电荷,原子核外的电子带负电荷,故A错;B、原子的体积大小与是否不显电性无关,电子比原子小得多,但带负电荷,故B错;C、原子核带正电荷,原子核外的电子带负电荷,且电量相等,电性相反,所以整个原子不显电性,故C正确;D、因为原子内所带的正负电荷数相等造成不显电性,故D错。
故选C。
3·氧的相对原子质量为16,表示的意义是()A.氧原子核中有16个质子B.一个氧原子的质量为l6C.氧原子的质量是一个碳原子质量的1/12D.氧原子的质量是一个碳原子质量的1/12的16倍【答案】D【解答】A、相对原子质量近似的等于原子中质子数+中子数,所以氧原子的相对原子质量为16不能反应其原子核内质子数为16,故A说法错误;B、原子质量是单位的,其单位为g,故B说法错误;C、相对原子质量是一个原子的真实质量跟一个碳-12原子质量的1/12的比值,而不是一个碳原子质量的1/12,故C说法错误;D、相对原子质量是一个原子的真实质量跟一个碳-12原子质量的1/12的比值,故一个氧原子的质量是一个碳原子质量的1/12的16倍,故D说法正确。
故选D。
4·知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、c对应的是()A.原子核、核外电子B.原子、核外电子C.原子、原子核D.核外电子、原子【答案】B【解答】分子是由原子构成的,故a是原子,原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,故b是原子核,c是核外电子,观察选项,故选B。
九年级化学原子的构成习题精选

九年级化学原子的构成习题精选习题精选(一)1.化学变化中的最小粒子是( )。
A.分子B.原子C.质子D.电子2.原子的质量主要集中在( )。
A.质子B.中子C.电子D.原子核3.据报道,上海某医院正在研究用放射性碘治疗肿瘤。
这种碘原子的核电荷数为53,相对原子质量为125。
下列关于这种原子的说法中,错误的是( )。
A.中子数为72B.质子数为72C.电子数为53D.质子数和中子数之和为1254.下列关于原子核的叙述中,正确的是( )。
①通常由中子和电子构成②通常由质子和中子构成③带负电荷④不显电性⑤不能再分⑥体积大约相当于原子⑦质量大约相当于原子A.①⑤B.②⑦C.③④D.②⑥⑦5.用其质量的1/12作为相对原子质量的标准的碳原子相对原子的质量是( )。
A.12gB.12C.1/12gD.1/126.下列叙述中,正确的是( )。
A.相对原子质量就是原子质量的简称B.相对原子质量可用千克或克作单位C.相对原子质量是一个没有单位的比值D.原子质量约等于原子核内质子质量和中子质量之和7.下列粒子中带正电荷的是。
(填序号)①电子②质子③中子④原子核⑤原子⑥分子8.我国著名化学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕、铈、铒、锗、锌、镝等元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量新值为152,则该元素的原子中质子数为,中子数为,核外电子数为。
9.北约轰炸南联盟时,广泛使用了美制贫铀弹,造成了严重的生态灾难。
已知贫铀弹中含有铀236(236为相对原子质量),它具有放射性,其质子数为92,则这种铀原子里中子数与核外电子数之差为。
10.已知一个碳12原子的质量为1.993×10-26kg,一个氧原子的质量为2.657×10-26kg,求氧原子的相对原子质量。
参考答案:1.B 2.D 3.B 4.B 5.B 6.D 7.②④ 8.63 89 63 9.5210.26-262.65710kgAr(O)161.99310kg(1/12)-⨯=≈⨯⨯习题精选(二)1.下列叙述中错误的是()。
原子结构练习题(含参考答案)

原子结构练习题(含参考答案)题目一1. 原子核由哪两种粒子组成?2. 电子的属性是什么?3. 原子的质量数由什么决定?4. 如何计算一个原子的电子数?5. 请列举五种不同元素的符号和原子序数。
参考答案:1. 原子核由质子和中子组成。
2. 电子具有负电荷和质量很小的特性。
3. 原子的质量数由其质子数和中子数之和决定。
4. 一个原子的电子数等于其质子数。
5. 例如:氢(H) - 1,氧(O) - 8,氮(N) - 7,铜(Cu) - 29,铁(Fe) - 26.题目二1. 什么是元素周期表?2. 哪个元素是元素周期表中的第一元素?3. 元素周期表是如何组织的?4. 元素的周期性特点是什么?5. 元素周期表中有多少个主要分组?参考答案:1. 元素周期表是一种排列化学元素的表格,按照一定规则组织元素信息。
2. 氢元素是元素周期表中的第一元素。
3. 元素周期表按元素的原子序数和化学性质进行组织,相似化学性质的元素分在同一垂直列(组)中。
4. 元素周期表中的元素周期性特点表现为周期性变化的原子半径、电离能和电负性等。
5. 元素周期表中有18个主要分组。
题目三1. 排列下列元素按原子升序:铜、氧、铁、钠。
2. 哪个元素的电子云最靠近原子核?3. 一个元素的原子序数是其原子中有多少个什么?4. 请列举两种气体元素。
5. 化合物是由什么组成的?参考答案:1. 氧、钠、铁、铜。
2. 电子云最靠近原子核的元素是氧。
3. 一个元素的原子序数是其原子中有多少个质子。
4. 例如:氢(H)和氧(O)。
5. 化合物是由两种或更多不同元素结合而成的。
原子的构成练习题。doc

原子的构成练习题1、下列粒子中,质量最小的是()A.分子B.原子C.中子D.电子2.分子和原子的主要区别是()A.分子大原子小 B.是否能构成物质C.在化学变化中本身是否发生了变化 D.是否在不断地运动3.原子的质量主要集中在()A.质子上 B.中子上 C.电子上 D.原子核上4、2002年初,美国制成了第一台磁冰箱,其效率比普通冰箱效率高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的一种原子的相对原子质量为157,核电荷数为64,则其原子中子数为()A.64B.57C. 93D.1285.有一个原子核内有8个中子和8个质子,另一个原子的核内有10个中子,核外有8个电子,则它们不相同的是()A.核电荷数B.核外电子数C.质子数D.相对原子质量6. 决定元素化学性质的是()A.质子数B.核外电子数C.最外层电子数D.核电荷数7.下列粒子在化学反应中容易得到电子的是().D.A B C D8.据报道,上海某医院正研究用放射性碘治疗肿瘤,这种碘原子的质子数是53,相对原子质量是125,下列关于这种原子的说法错误的是()A.核电荷数是53 B.核外电子数是53C.中子数是53 D.质子数与中子数之和是1259.2007年10月24日,“嫦娥一号”发射成功。
其主要任务之一是探测月球上的氦(He-3),其原子核内的质子数为2,中子数为1,每一百吨氦(He-3)核聚变所释放的能量相当于目前人类一年消耗的能量。
下列关于氦(He-3)元素的说法正确的是()A.原子核外电子数为3B.相对原子质量为2C. 原子结构示意图为D. 原子结构示意图为10.一个氧分子是由两个氧原子构成的,则一个氧分子内含有的质子数是()A.8B.16C.32D.6411.由分子参加的化学反应,反应前后一定发生变化的是()。
A.分子种类B.分子数目C.原子种类D.原子数目12.关于分子、原子、离子的叙述中,正确的是()A.只有带电的粒子才叫离子B.原子是最小的粒子C.分子是化学变化中的最小微粒 D.分子、原子、离子都是构成物质的粒子13.下列关于相对原子质量的说法中正确的是()A、它是原子的实际质量B、它可以用千克作单位C、它是以碳12原子质量为标准D、它约等于质子数与中子数之和。
《原子的构成》配套练习 2022年九年级化学附答案
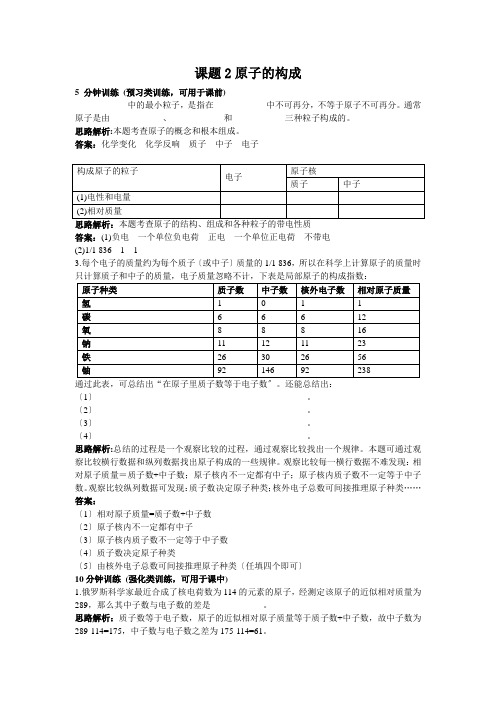
课题2原子的构成5 分钟训练(预习类训练,可用于课前)____________中的最小粒子,是指在____________中不可再分,不等于原子不可再分。
通常原子是由____________、____________和____________三种粒子构成的。
思路解析:本题考查原子的概念和根本组成。
答案:化学变化化学反响质子中子电子思路解析:本题考查原子的结构、组成和各种粒子的带电性质答案:(1)负电一个单位负电荷正电一个单位正电荷不带电(2)1/1 8361 13.每个电子的质量约为每个质子〔或中子〕质量的1/1 836,所以在科学上计算原子的质量时只计算质子和中子的质量,电子质量忽略不计,下表是局部原子的构成指数:通过此表,可总结出“在原子里质子数等于电子数〞。
还能总结出:〔1〕________________________________________________。
〔2〕________________________________________________。
〔3〕________________________________________________。
〔4〕________________________________________________。
思路解析:总结的过程是一个观察比较的过程,通过观察比较找出一个规律。
本题可通过观察比较横行数据和纵列数据找出原子构成的一些规律。
观察比较每一横行数据不难发现:相对原子质量=质子数+中子数;原子核内不一定都有中子;原子核内质子数不一定等于中子数。
观察比较纵列数据可发现:质子数决定原子种类;核外电子总数可间接推理原子种类……答案:〔1〕相对原子质量=质子数+中子数〔2〕原子核内不一定都有中子〔3〕原子核内质子数不一定等于中子数〔4〕质子数决定原子种类〔5〕由核外电子总数可间接推理原子种类〔任填四个即可〕10分钟训练(强化类训练,可用于课中)1.俄罗斯科学家最近合成了核电荷数为114的元素的原子,经测定该原子的近似相对质量为289,那么其中子数与电子数的差是____________。
九年级化学原子的构成练习题2

原子的构成我夯基我达标1.某些花岗岩石材中含有放射性元素氡。
一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为()A.50B.86C.136D.222思路解析:此题考查对原子结构以及原子结构中粒子数之间等量关系的理解水准,解此题的关键在于掌握原子结构中的等量关系。
即核电荷数=质子数=电子数(电荷等量关系),相对原子质量=质子数+中子数(质量等量关系)。
由题意,氡元素的质子数为86,则原子核外电子数为86;又因为中子数为136,则相对原子质量为222。
答案:B2.下列说法准确的是()A.原子不能再分B.原子核都是由质子和中子构成的思路解析:本题主要考查原子不能再分是指在化学反应中,而在原子核变化中,原子能够再分,故A不准确。
除有一种氢原子核是由一个质子而无中子构成之外,其他原子的原子核都由质子和中子构成,B不准确。
相对原子质量有单位,单位为1,一般不写,C不准确。
物质能够由分子、原子等粒子构成,而分子则由原子构成,故D准确。
答案:D3.有两种原子,一种原子核内有17个质子和18个中子,另一种原子核内有17个质子和19个中子,则它们不相等的是()A.核电荷数B.核外电子数C.原子质量D.原子的带电荷量思路解析:中子数的不同使得相对原子质量不等,也就是原子的质量不等。
这种原子数相同、中子数不同的原子互称同位素。
答案:C4.“神舟”五号不但将杨利伟送上太空,实现了亿万中国人的梦想,同时还承担着其他的科研任务。
比如探索宇宙中可能存有完全由反粒子构成的物质——反物质。
物质与反物质相遇会发生“湮灭”现象,释放出巨大的能量,在能源研究领域中前景可观。
正电子、负质子等都是反粒子。
它们与通常所说的电子、质子相比较,质量相等但电性相反。
请你推测,反氢原子的结构可能是()A.由一个带正电荷的质子与一个带负电荷的电子构成B.由一个带负电荷的质子与一个带正电荷的电子构成C.由一个带正电荷的质子与一个带正电荷的电子构成D.由一个带负电荷的质子与一个带负电荷的电子构成思路解析:根据所给信息,反氢原子是由1个反质子和反电子构成的,反质子带一个单位负电荷,反电子带一个单位正电荷。
化学人教版九年级上册原子结构课后习题.2 原子的构成

新人教版九年级上册《3.2 原子的构成》同步练习卷一、填空题(共5小题,每小题3分,满分15分)1.原子很小,原子核更小,电子在原子核外很大的空间里作的运动.科学研究表明,在含有多个电子的原子中,核外电子具有不同的,离核近的电子,离核越远,电子.2.核外电子的分层运动又叫做.到目前为止,人们发现元素原子核外电子的排布中,最少的只有层,最多的有层.最外层电子数最多不超过个(只有1层的,电子不超过个).3.原子结构示意图表示的意义:以镁原子为例:表示镁原子的核电荷数(质子数)为,核外共有个电子层,第一层上有个电子,最外层上有个电子.4.稀有气体的原子最外层有个电子(氦为个电子),是一种的结构,氦、氩等化学性质比较;钠、镁等金属的原子最外层电子数一般都于4个,在化学反应中易电子;氯、氧等非金属原子的最外层电子数一般都4个,在化学反应中易电子,都趋于达到的结构.5.叫做离子,原子失去电子会带上电,叫做离子,原子得到电子会带上电,叫做离子.像氯化钠这种由阴、阳离子相互作用形成的化合物叫做离子化合物.二、基础训练6.某原子的结构示意图为:,下列说法正确的是()A.该原子中所含的质子数为16B.该原子属于金属元素的原子C.该原子属于非金属元素的原子D.该原子的核外电子数为67.根据钠原子结构示意图不能确定的是()A.质子数B.电子层数C.相对原子质量D.元素种类8.下列陈述不正确的是()A.分子可以分解成原子B.原子由原子核和电子构成C.阳离子得到电子变成原子D.原子失去电子变成阴离子9.某元素负二价阴离子的结构示意图为,则该元素原子所含的质子数为()A.6 B.8 C.10 D.1210.下表列出了一些生活中常见元素的原子结构示意图.下列叙述错误的是()A.上表中,8种元素原子的核外电子层数相同B.S、Cl、Ar的原子在化学反应中都易得到电子,形成带负电荷的阴离子C.上表中,非金属元素原子的最外层电子数都大于4个D.从Na到Ar,随着核电荷数的递增,原子核外最外层电子数从1个递增到8个三、能力训练11.据科学家预测,月球的土壤中吸附着百万吨的氦(He﹣3),其原子核中质子数为2、中子数为1,每百吨氦(He﹣3)核聚变所释放出的能量相当于目前人类一年消耗的能量.下列关于氦(He﹣3)元素的说法正确的是()A.原子核外电子数为3 B.相对原子质量为2C .原子结构示意图为D .原子结构示意图为12.某粒子结构示意图为,下列对该粒子的说法中不正确的是( )A .核内一定有10个质子B .核外电子是分层排布的C .具有稳定结构D .可能是阳离子或阴离子或稀有气体原子13.下列结构示意图,表示阴离子的是( )A .B .C .D .14.下列结构示意图中表示阳离子的是( )A .B .C .D .15.原子失去最外层电子或最外层得到电子之后,一定不会引起的改变是( )①核外电子总数 ②化学性质③相对原子质量④粒子的电性 ⑤原子核 ⑥电子层数 ⑦最外层电子数.A .①⑤B .②⑤C .③⑤D .②④⑥16.对于Fe 、Fe 2+、Fe 3+三种粒子的判断正确的是( )①核电荷数相同 ②核外电子数相同 ③电子层结构完全相同 ④相对原子质量几乎相等.A .①②③④B .①③C .①④D .②③四、解答题(共3小题,满分0分)17.(1)用数字和化学符号表示:2个氧原子 ,3个钠离子 .(2)镁的原子结构示意图为.Mg原子再化学反应中容易(填“得到”或“失去”)2个电子.18.Na与Na+的比较:(1)Na与Na+的化学性质不同,是因为;(2)Na与Na+的质量几乎相等,是因为;(3)Na与Na+属于粒子,是因为.19.在一个水分子中(H2O),共有个质子,个电子.在一个氢氧根离子中(OH﹣),共有个质子,个电子.五、迁移拓展20.根据下列几种粒子的结构示意图,回答问题:(1)其中属于阴离子的是.(填序号,下同)(2)属于金属原子的是.(3)具有相似化学性质的粒子是.21.(2016•湘桥区模拟)如图1为某粒子的结构示意图,则(1)该粒子有个电子层,X的值为;(2)该粒子的化学性质与下列(如图2)(填序号)元素的化学性质最相似.。
原子的构成练习题
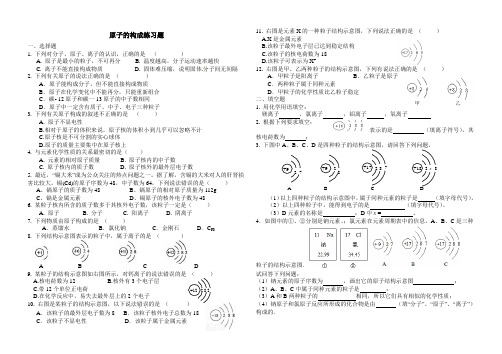
原子的构成练习题一、选择题 1. 下列对分子、原子、离子的认识,正确的是 ( ) A. 原子是最小的粒子,不可再分 B. 温度越高,分子运动速率越快 C. 离子不能直接构成物质 D. 固体难压缩,说明固体分子间无间隔 2. 下列有关原子的说法正确的是 ( ) A .原子能构成分子,但不能直接构成物质 B .原子在化学变化中不能再分,只能重新组合 C .碳- 12原子和碳一13原子的中子数相同 D .原子中一定含有质子、中子、电子三种粒子 3. 下列有关原子构成的叙述不正确的是 ( ) A. 原子不显电性 B.相对于原子的体积来说,原子核的体积小到几乎可以忽略不计 C.原子核是不可分割的实心球体 D.原子的质量主要集中在原子核上 4. 与元素化学性质的关系最密切的是( ) A. 元素的相对原子质量 B. 原子核内的中子数 C. 原子核内的质子数 D. 原子核外的最外层电子数 5. 最近,“镉大米”成为公众关注的热点问题之一。
据了解,含镉的大米对人的肝肾损害比较大。
镉(Cd)的原子序数为48,中子数为64,下列说法错误的是( ) A 、镉原子的质子数为48 B 、镉原子的相对原子质量为112g C 、镉是金属元素 D 、镉原子的核外电子数为48 6. 某粒子核内所含的质子数多于其核外电子数,该粒子一定是( ) A. 原子 B. 分子 C. 阳离子 D. 阴离子 7. 下列物质由原子构成的是 ( ) A .蒸馏水 B .氯化钠 C .金刚石 D .C 60 8. 下列结构示意图表示的粒子中,属于离子的是 ( )A B C D9. 某粒子的结构示意图如右图所示,对钙离子的说法错误的是A.核电荷数为12B.核外有3个电子层C.带12个单位正电荷D.在化学反应中,易失去最外层上的2个电子 10. 右图是某粒子的结构示意图,以下说法错误..的是 ( A .该粒子的最外层电子数为8 B .该粒子核外电子总数为18C .该粒子不显电性D .该粒子属于金属元素11. 右图是元素X 的一种粒子结构示意图,下列说法正确的是 ( ) A.X 是金属元素B.该粒子最外电子层已达到稳定结构C.该粒子的核电荷数为18D.该粒子可表示为X + 12. 右图是甲、乙两种粒子的结构示意图,下列有说法正确的是 ( ) A .甲粒子是阳离子 B .乙粒子是原子 C .两种粒子属于同种元素 D .甲粒子的化学性质比乙粒子稳定 二、填空题1. 用化学用语填空: 镁离子 ,氯离子 ,铝离子 ,氧离子2. 根据下列要求填空: 表示的是 (填离子符号),其 核电荷数为 ;3. 下图中A 、B 、C 、D(1)以上四种粒子的结构示意图中,属于同种元素的粒子是 (填字母代号)。
原子的结构练习题

原子的结构练习题题目一:选择题1. 原子的基本组成部分是:a) 电子b) 质子和中子c) 中子d) 电子和质子2. 质子的电荷为:a) 正电荷b) 负电荷c) 中性d) 都有可能3. 一个原子的中子数目等于:a) 质子数目b) 电子数目c) 原子核数目d) 都有可能4. 具有相同质子数,但中子数不同的原子称为:a) 同位素b) 异位素c) 同位中子d) 异位质子5. 具有相同中子数,但质子数不同的原子称为:a) 同位素b) 异位素c) 同位质子d) 异位中子题目二:判断题1. 原子核由质子和中子组成,质子带正电荷,中子带负电荷。
()2. 元素的化学性质由其质子数决定。
()3. 同位素具有相同的原子序数和质子数。
()4. 电子的质量约为质子和中子的1/1836。
()5. 原子的直径大约为10^-10米。
()题目三:简答题请简要介绍原子的结构。
题目四:填空题1. 具有相同原子序数但不同质子数的原子称为_____________。
2. 一个原子的质子数等于其原子核中_____________的数目。
3. 具有相同中子数但不同质子数的原子称为_____________。
4. 原子核由_____________和_____________组成。
5. 在原子结构中,电子以_____________的形式存在。
题目五:解答题1. 解释同位素和异位素的概念,并给出一个例子。
2. 为什么原子的直径通常用10^-10米来表示?3. 为什么电子的质量可以忽略不计?题目六:应用题1. 根据以下数据回答问题:元素X的原子核中有16个质子和18个中子,请回答以下问题:a) X元素的原子序数是多少?b) X元素的质量数是多少?c) X元素的核外电子数为多少?2. 通过填写下面的填空题,来画出氧原子的示意图:a) 原子序数:8b) 质子:8c) 中子:8答案及解析:题目一:选择题1. b) 质子和中子解析:原子的基本组成部分包括了质子和中子构成的原子核,以及环绕原子核的电子。
原子的构成练习题

原子的构成练习题一、选择题;1、在化学变化中可分的微粒是()A、原子B、分子C、质子D、电子2、下列关于原子的叙述,错误的是()A、能构成物质,也能构成分子B、一定含有质子、中子和电子C、原子不显电性D、是比分子小的粒子3、下列说法正确的是()A、在化学反应中,发生改变的只是原子核外的电子,而原子核没有改变B、在化学反应中,金属元素的原子容易失去电子变为带正电荷的阴离子C、在化学反应中,氯原子易失去1个电子,形成带1个单位负电荷的氯离子D、原子失去电子或得到电子后,一定会变成离子4、钠原子由11个质子和12个中子构成,下列说法错误的是()A、钠原子核所带电荷数为11B、钠的相对原子质量为23gC、钠原子核外电子数为11D、钠的相对原子质量为235、原子中,一定含有的微粒是()A、质子、中子、电子B、质子、中子C、中子、电子D、质子、电子6、碳的相对原子质量为()A、1.66×10-27kgB、 1.993×10-26kgC、12 kgD、127、构成氯化钠的粒子是()A、氯化钠分子B、钠原子和氯原子C、钠离子和氯离子D、氯化钠离子8、已知镁原子核内质子数为12,而且质子数与中子数相等,则该原子核内所含粒子总数为()A、12B、24C、36D、 489、下列关于原子核的叙述:①通常是由中子和电子构成②通常是由质子和中子构成③带正电荷④不显电性⑤不能再分⑥跟原子比较体积很小,但却集中了原子的主要质量。
其中正确的是()A、①③⑥B、②③⑥C、②③⑤D、①④⑥10、某原子中共有34个粒子,其中12个粒子不带电,则它的相对原子质量约为()A、34B、46C、23D、1211、某元素一个单位负电荷的阴离子结构示意图为,则x、y的值分别为()A、18和8B、17和8C、19和8D、14和412、某种氧原子的原子核内有8个质子和8个中子,另一种氧原子的原子核内有8个质子和10个中子,则这两种氧原子中不同的是()A、核电荷数B、核外电子数C、原子的质量D、原子的带电量13、美国“9.11事件”发生以后,美国政府扬言要用中子弹攻击恐怖分子,中子弹爆炸是()A、分子分解成原子B、原子得失电子C、原子核破裂D、中子运动或变化14、根据下列原子结构示意图判断,化学性质最稳定的是()15、根据粒子结构示意图:下列判断正确的是()A、它们都带有电荷B、它们原子的核外电子数相同C、它们都具有稳定结构D、它们表示同一种元素16、下列各组粒子的结构示意图中所表示的元素的化学性质相似的一组是()17、某粒子的结构示意图为,则它所带电荷数可能是()A、8-nB、n-8C、10-nD、n-1018、已知原子核内有6个质子和6个中子的碳原子质量为a克,若另一种原子的质量为b 克,则另一种原子的相对原子质量为()A、a/bB、b/aC、12b/aD、12a/b19、已知一种锶原子的相对原子质量为88,其质子数为38,则这种锶原子的核外电子数为()A、38B、50C、88D、12620、居里夫妇在1898年从几吨铀盐废料中提炼0.3%镭。
原子的构成习题精选及答案

原子的构成习题精选及答案一、选择题1、原子和分子的区别是:( )A、分子在化学反应中分成原子,但在化学反应中原子不可再分B、分子一定比原子大C、分子能构成物质,而原子只能构成分子D、在化学反应中分子和原子都可以变成另一种分子和原子,区别在于它们发生的是不同的变化2、已知一个质子数和中子数都是6的碳原子的质量是千克,则一个氧原子的质量是:( )A、16克B、16C、千克D、千克3、在原子中,质子数等于:( )A、中子数B、核外电子总数C、相对原子质量D、中子数和电子数之和4、下列原子各1克,所含原子个数最多的是:( )A、氧原子B、铁原子C、氢原子D、氯原子5、一滴水能分成许许多多个水分子,分子又可分成原子,原子又由中子、质子、电子等构成,这些微粒中,一定能保持水的化学性质的是()。
A、水分子B、构成水分子的原子C、中子和质子D、电子6、原子和分子的根本区别是()A、是否能直接构成物质B、是否能保持物质的化学性质C、是否在化学反应中发生种类的变化D、是否能构成单质7、下列关于原子的说法错误的是()A、原子是化学变化中的最小微粒B、原子是最小的微粒C、原子核带正电荷,但原子不显电性D、分子能直接构成物质而原子不能8、原子中决定相对原子质量大小的是()A、质子数和中子数B、质子数和电子数C、中子数和电子数D、核电荷数和电子数9、下列各种原子各1克,所含原子个数最多的是()A、氧原子B、铁原子C、氢原子D、氯原子10、下列各式中,表示两个氢原子的是()A、2HB、C、D、11、碳的原子量是()A、12克B、12C、千克D、1/12克12、在原子中()A、质子数一定等于中子数B、质子数一定等于电子数C、质子数、中子数、电子数三者都相等D、原子核所带电量跟核外电子的电量相等13、下列关于原子的叙述正确的是()A、物质都是由原子直接构成的B、原子是由质子和电子构成的C、原子是由质子和中子构成的D、原子是由原子核和核外电子构成的二、填空题1、硫原子的相对原子质量(原子量)为32,质子数是16,则中子数是______,电子数是______,核电荷数是______。
鲁教版五四制化学八年级全册3.1《原子的构成》同步练习2

第一节原子的构造同步练习2一、选择题2.A元素的原子核外排布是:第一层有2个电子,第二层上有7个电子,第三层上没有电子,那么A元素属于A.金属元素B.非金属元素3.原子核外有19个电子的某种原子,假设它失去一个电子后,剩余局部4.氧的相对原子质量为16,它获得两个电子后,发生改变的是6.核外有11个质子,12个中子,核外有10个电子的粒子,一定是8.某离子构造示意图为假设要表示阳离子,可表示的种数为9.某金属原子次外层为8个电子,原子最外层上的电子数是m个,在化学反响中,该金属原子最多能失去电子数目为m mm m10.A元素原子电子层数为3,其原子的最外层有2个电子,A离子的核外电子数为m,那么A的核电荷数为A.mB.m-2C.m+2二、填空题1.某元素的原子构造示意图为请答复:〔1〕该元素的原子最外层电子数是;〔2〕表示的含义是;〔3〕该元素原子核外有个电子层;〔4〕该元素在化学反响中是容易〔得或失〕电子。
〔1〕A~E共表示种元素;〔2〕表示阳离子的粒子是;〔3〕表示阴离子的是;〔4〕表示相对稳定构造的粒子是;〔5〕在化学反响中易获得电子的粒子是。
3.某粒子构造示意图为按以下要求答复各问题:〔1〕假设该粒子为中性原子,那么x = ;〔2〕假设该粒子带1个单位正电荷,那么x = ,假设带2个单位负电荷,那么x = 。
4.构成物质的粒子除原子、分子外,还有。
离子是由于原子形成的。
如果要使硫离子变成硫原子,每个硫离子需要失去个电子。
〔1〕带2个单位负电荷的阴离子,核外电子排布与氩原子一样;〔2〕核外有10个电子且带2个单位正电荷的阳离子;〔3〕相对原子质量为31,中子数为16的原子;〔4〕核外有三个电子层,最外层为稳定构造的原子;〔5〕第二层电子数是第一层电子数2倍的原子;〔6〕失去一个电子后剩一个原子核的离子。
7.俄罗斯科学家最近合成了核电荷数为114的元素的原子,经测定该原子的相对原子质量为289,那么其中子数和电子数之差是。
原子的构成习题精选及答案

原子的构成习题精选及答案原子的构成习题精选及答案一、选择题1、原子和分子的区别是:( )A、分子在化学反应中分成原子,但在化学反应中原子不可再分B、分子一定比原子大C、分子能构成物质,而原子只能构成分子D、在化学反应中分子和原子都可以变成另一种分子和原子,区别在于它们发生的是不同的变化2、已知一个质子数和中子数都是6的碳原子的质量是千克,则一个氧原子的质量是:( )A、16克B、16C、千克D、千克3、在原子中,质子数等于:( )A、中子数B、核外电子总数C、相对原子质量D、中子数和电子数之和4、下列原子各1克,所含原子个数最多的是:( )A、氧原子B、铁原子C、氢原子D、氯原子5、一滴水能分成许许多多个水分子,分子又可分成原子,原子又由中子、质子、电子等构成,这些微粒中,一定能保持水的化学性质的是()。
A、水分子B、构成水分子的原子C、中子和质子D、电子6、原子和分子的根本区别是()A、是否能直接构成物质B、是否能保持物质的化学性质C、是否在化学反应中发生种类的变化D、是否能构成单质7、下列关于原子的说法错误的是()A、原子是化学变化中的最小微粒B、原子是最小的微粒C、原子核带正电荷,但原子不显电性D、分子能直接构成物质而原子不能8、原子中决定相对原子质量大小的是()A、质子数和中子数B、质子数和电子数C、中子数和电子数D、核电荷数和电子数9、下列各种原子各1克,所含原子个数最多的是()A、氧原子B、铁原子C、氢原子D、氯原子10、下列各式中,表示两个氢原子的是()A、2HB、C、D、11、碳的原子量是()A、12克B、12C、千克D、1/12克12、在原子中()A、质子数一定等于中子数B、质子数一定等于电子数C、质子数、中子数、电子数三者都相等D、原子核所带电量跟核外电子的电量相等13、下列关于原子的叙述正确的是()A、物质都是由原子直接构成的B、原子是由质子和电子构成的C、原子是由质子和中子构成的D、原子是由原子核和核外电子构成的二、填空题1、硫原子的相对原子质量(原子量)为32,质子数是16,则中子数是______,电子数是______,核电荷数是______。
鲁教五四制版化学八年级全一册原子的构成课时练习

3.1原子的构成同步卷2一.选择题(共10小题)1.已知某粒子的结构示意图如图,且x﹣y=9.该粒子符号可能为()A.K+B.Cl﹣C.Cl D.Ar2.有三种粒子:①、②、③,关于这些粒子的说法正确的是()A.它们都是原子B.它们都是离子C.它们表示同一种元素D.它们都具有相对稳定结构3.如图为某原子结构模型图,其中a、b、c是构成该原子的三种不同粒子。
下列说法中正确的是()A.原子核由a和c构成B.原子中a与c的数目一定相等C.原子中b与c的数目一定相等D.原子的质量主要集中在a和b上4.核辐射污染物主要有铯﹣134,铯﹣137和碘﹣131,它们与作为相对原子质量标准的碳﹣12一样,属于()A.原子B.离子C.单质D.分子5.极光是一种绚丽多彩的发光现象,其发生是由于太阳带电粒子流进入地球磁场。
下列这些微粒中,不会引起极光的是()A.α粒子(氦的原子核)B.电子C.质子D.中子6.2021年4月,日本决定将福岛核污水排入大海。
核污水中的氚、碳﹣14等难以去除的放射性物质,通过环境循环进入食物链影响人类安全,已知氚原子中质子数为1,中子数为2,下列示意图能正确表示氚原子结构的是()A.A B.B C.C D.D7.氘和氚是制造氢弹的原料。
氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是()A.该变化不属于化学变化范畴B.氚、氦两种原子的质子数相同C.该变化涉及的元素有三种D.氘原子和氚原子的相对原子质量相等8.丹麦物理学家阿格•玻尔与莫特森及雷恩沃特共同提出了关于原子核的集体模型而共同获得了1975年诺贝尔物理学奖。
关于原子核的下列叙述中正确的是()①原子的质量主要集中在原子核上②原子核居于原子中心,带正电,所占体积很小③构成原子核的质子、中子是不能再分的粒子④原子核的核电荷数等于核内中子数⑤所有的原子都是由质子、中子和电子构成的⑥原子核具有很高的密度A.①②⑤B.①②⑥C.③④⑤D.③⑤⑥9.原子数相同、电子数也相同的分子或离子叫等电子体,等电子体具有相似的结构和某些相似的性质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原子的构成练习题(2)
1、下列粒子中,质量最小的是( )
A.分子B.原子 C.中子D.电子
2.分子和原子的主要区别是( )
A.分子大原子小 B.是否能构成物质
C.在化学变化中本身是否发生了变化 D.是否在不断地运动
3.原子的质量主要集中在( )
A.质子上
B.中子上C.电子上 D.原子核上
4、2002年初,美国制成了第一台磁冰箱,其效率比普通冰箱效率高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的一种原子的相对原子质量为157,核电荷数为64,则其原子中子数为()
A.64
B.57
C. 93D. 128
5.有一个原子核内有8个中子和8个质子,另一个原子的核内有10个中子,核外有8个电子,则它们不相同的是( )
A.核电荷数 B.核外电子数 C.质子数ﻩD.相对原子质量
6. 决定元素化学性质的是( )
A.质子数B.核外电子数 C.最外层电子数D.核电荷数
7.下列粒子在化学反应中容易得到电子的是( )
A B C D
8.据报道,上海某医院正研究用放射性碘治疗肿瘤,这种碘原子的质子数是53,相对原子质量是125,下列关于这种原子的说法错误的是()
A.核电荷数是53 B.核外电子数是53
C.中子数是53 D.质子数与中子数之和是125
9. 2007年10月24日,“嫦娥一号”发射成功。
其主要任务之一是探测月球上的氦(He-3),其原子核内的质子数为2,中子数为1,每一百吨氦(He-3)核聚变所释放的能量相当于目前人类一年消耗的能量。
下列关于氦(He-3)元素的说法正确的是()
A.原子核外电子数为3
B.相对原子质量为2
C. 原子结构示意图为D.原子结构示意图为
10.一个氧分子是由两个氧原子构成的,则一个氧分子内含有的质子数是()
A.8 ﻩB.16ﻩC.32 D.64
11.由分子参加的化学反应,反应前后一定发生变化的是( )。
A.分子种类
B.分子数目C.原子种类D.原子数目
12.关于分子、原子、离子的叙述中,正确的是( )
A.只有带电的粒子才叫离子ﻩB.原子是最小的粒子
C.分子是化学变化中的最小微粒D.分子、原子、离子都是构成物质的粒子
13.下列关于相对原子质量的说法中正确的是()
A、它是原子的实际质量B、它可以用千克作单位
C、它是以碳12原子质量为标准
D、它约等于质子数与中子数之和。
14.下列关于原子核的叙述中,正确的是( )。
①通常由中子和电子构成②通常由质子和中子构成③带负电荷④不显电性⑤不能再分⑥集中了原子绝大部分的体积⑦集中了原子绝大部分的质量A.①⑤B.②⑦C.③④D.②⑥⑦
15.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通信,其要发射的卫星的数目相等,下列关于铱元素的各种说法中正确的是()
A、铱原子的核电荷数为77
B、铱原子的相对原子质量为77
C、铱原子的质子数为70 D、铱元素是非金属元素
16、下列叙述中错误的是()。
①原子是化学变化中的最小粒子②原子是不能再分的粒子③一切物质都是由原子直接构成的④一切原子核都是由质子和中子构成的⑤原子不显电性⑥原子之间有间隔
A.①和②
B.②③和④
C.③和⑤
D.③和⑥
17.下列关于原子的叙述正确的是( )
A. 物质都是由原子直接构成的B.原子是由质子和电子构成的
C. 原子是由质子和中子构成的
D. 原子是由原子核和核外电子构成的
18. 原子核外有19个电子的某种原子,假如它失去一个电子后,剩余部分( )
A. 不显电性ﻩB. 显正电性ﻩC.显负电性D. 原子的带电量
19. 下列说法中正确的是( )
A.所有原子的原子核都是由质子和中子构成的B. 原子的质量主要集中在原子核上C.在化学变化中某一原子变成了另一原子 D. 碳原子在原子核内有12个质子20.下列说法中正确的是( )
A. 所有原子的原子核都是由质子和电子构成的B. 原子的质量主要集中在原子核上
C. 在化学变化中某一原子变成了另一原子D.碳原子在原子核内有12个质子
二、填空题
1、已知钠原子核内有11个质子,12个中子,则钠原子的核电荷数是 ,核外的电
子数是。
2.已知铁原子的相对原子质量是56,核电荷数是26,则铁原子的核内质子数是,核外电子数是 ,核内中子数是。
3.分子是由结合而成的,如每个水分子是由两个原子和一个原子
构成的。
4.相同质量的钠、锂、铁(相对原子质量分别为23、7、56)三种金属,含有原子数由多
到少排列的顺序为:__________________________
5.已知“○”、“●”表示质子数不同的原子。
(1)下列表示的气体物质中,属于化合物的是
(2)下列表示的气体物质中,属于混合物的是
6.某元素的原子结构示意图如右图所示,则该原子的核电荷数x
+x 2 8 1 为,核外共有个电子,分为个电子层,
第二层上有个电子,最外电子层上有个电子,在
化学反应中,该原子易电子,变成 (用符号
表示)。
7.某原子的结构示意图为最外层电子数n=_______,核外共有______个电子。
8.在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。
已知氢、碳、氧、钠、氯五种元素的核电荷数分别为1,6,8,11,17。
试按下列要求,写出微观
需满足的条件粒子的化学符号
(1)质子数为11的同种元素
....的原子和离子
(2)质子数之和均为10的两种不同
..的分子
(3)质子数为1的阳离子和质子数为9的阴离
子
三、简答题
1.原子由哪些微粒构成,这些微粒分别带什么电?原子为什么显电中性?
2、1911年著名物理学家卢瑟福和他的研究团队做了著名的α粒子轰击金箔的实验。
实验现象有哪些?应该如何解释这些现象?。
