高中化学第三章第1节第1课时碳单质的多样性及含碳化合物练习鲁科版必修1
化学鲁科版必修1第3章第1节碳的多样性作业1

课后训练1.下列有关CO 2的实验中,只能证明CO 2的物理性质的实验是( )2.比较归纳是学习化学常用的一种方法。
对以下三种物质的转化关系: ①C →CO 2 ②CH 4→CO 2 ③CO →CO 2比较归纳正确的是( )A .三种转化关系中发生的反应都属于化合反应B .三种转化关系中所有的生成物在常温下都是气体C .三种物质都只能跟氧气反应转化为二氧化碳D .三种物质都能在点燃条件下转化为二氧化碳3.下列物质中,既能跟强酸溶液反应、又能跟强碱溶液反应的是( )A .Na 2CO 3溶液B .CaCO 3C .NaHCO 3溶液D .Na 2SO 4溶液4.下列各溶液与强酸溶液反应,不能用离子方程式3HCO -+H +===CO 2↑+H 2O 表示的是( )A .碳酸氢钾溶液B .纯碱溶液C .碳酸氢钙溶液D .小苏打溶液5.用1 L 1.0 mol·L -1 NaOH 溶液吸收0.8 mol CO 2,所得溶液中的23CO -和3HCO -的物质的量浓度之比约是( )A .1∶3B .2∶1C .2∶3D .3∶26.将足量CO 2通入KOH 和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n )和通入CO 2体积(V )的关系正确的是( )7.由一气体甲开始,可发生如下四个变化: 甲气体通过灼热的碳层乙气体通过灼热的碳层丙气体通过灼热的氧化铜乙气体通过石灰水丁固体则甲、乙、丙、丁分别为( )A .CO 2、CO 、O 2、CaOB .O 2、CO 、CO 2、CaCO 3C .O 2、CO 2、CO 、CaCO 3D .CO 、CO 2、O 2、Ca(OH)28.把CO 2通入含NaOH 0.8 g 的碱溶液中,将产物在减压条件下蒸干后,得固体1.37 g ,则通入CO 2的质量是( )A .0.44 gB .0.66 gC .0.88 gD .都不是9.二氧化碳的过量排放,严重影响人类的生存环境,处理和利用二氧化碳是全球关注的重大问题。
高中化学第3章自然界中的元素第1节第1课时多种多样的碳单质和广泛存在的含碳化合物课后练习鲁科版必修1

第1课时多种多样的碳单质和广泛存在的含碳化合物课后篇巩固提升A组基础巩固1.航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一,其化学性质与CO相似。
下列有关C2O3的说法正确的是( )A.C2O3和CO2是同素异形体B.C2O3和CO的燃烧产物都是CO2C.C2O3和CO都是酸性氧化物D.C2O3和CO2都是碳酸的酸酐A项错;由于C2O3、CO中的碳分别为+3价、+2价,均没有对应价态的碳的含氧酸,故都不是酸性氧化物;碳酸的酸酐只有CO2;而C2O3、CO化学性质相似,燃烧均生成碳的最高价氧化物CO2。
2.下列关于金刚石、石墨和C60的说法中,正确的是( )A.它们为同一种物质B.互为同素异形体C.具有相同的结构D.金刚石和石墨的相互转化是物理变化C60是碳元素的三种不同的单质,互为同素异形体。
3.当分别向下列物质中滴加醋酸时,会产生相同气体的是( )①大理石②钟乳石③贝壳④水垢⑤白云石A.①②③B.②④⑤C.①③④⑤D.①②③④⑤CaCO3,分别滴加醋酸时,均产生CO2气体。
4.中国科学家以CO2为碳源,钠为还原剂,在470 ℃、80 MPa下合成金刚石,具有深远意义。
下列说法不正确的是( )A.由CO2合成金刚石是化学变化B.金刚石是氧化产物C.金刚石是碳的一种同素异形体D.钠元素发生氧化反应,CO2与Na反应时+4价的碳被还原为金刚石(0价),故金刚石是还原产物,B项错误。
5.有A、B两个完全相同的装置,某学生分别在它们的侧管中装入一定量的Na2CO3和NaHCO3,A、B中分别装有足量的相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )A.侧管中装入Na2CO3的气球膨胀速率大B.若加入等质量的Na2CO3和NaHCO3,最终两气球体积不同C.最终两试管中Na+、Cl-的物质的量一定相同D.反应完全后两溶液中溶质种类不同,先生成碳酸氢钠,然后碳酸氢钠和盐酸反应生成二氧化碳,所以A装置的气球膨胀速率慢,故A错误;若加入等质量的Na2CO3和NaHCO3,则碳酸钠的物质的量小于碳酸氢钠,最终碳酸氢钠对应的气球体积大,故B正确;由于Na2CO3和NaHCO3的物质的量不确定,所以Na2CO3和NaHCO3中钠离子的物质的量不一定相同,故C错误;由于盐酸足量,所以完全反应后两溶液中的溶质都是NaCl和HCl,故D错误。
鲁科版 高中化学必修一 3.1.1 多种多样的碳单质 广泛存在的含碳化合物 同步练习
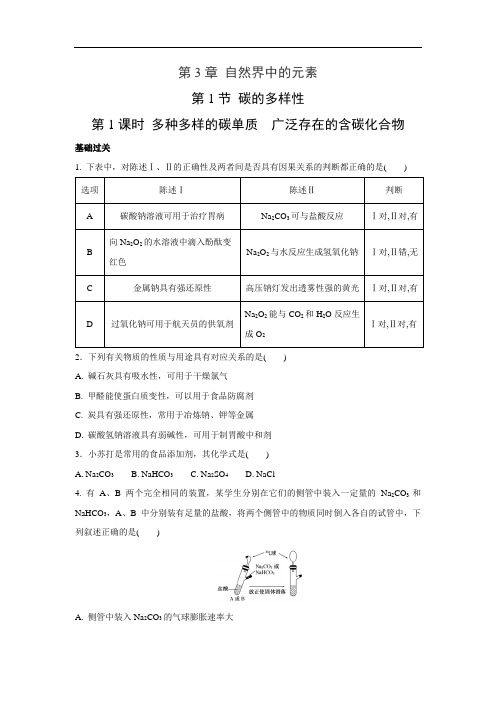
第3章自然界中的元素第1节碳的多样性第1课时多种多样的碳单质广泛存在的含碳化合物基础过关1. 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是()2.下列有关物质的性质与用途具有对应关系的是()A. 碱石灰具有吸水性,可用于干燥氯气B. 甲醛能使蛋白质变性,可以用于食品防腐剂C. 炭具有强还原性,常用于冶炼钠、钾等金属D. 碳酸氢钠溶液具有弱碱性,可用于制胃酸中和剂3.小苏打是常用的食品添加剂,其化学式是()A. Na2CO3B. NaHCO3C. Na2SO4D. NaCl4. 有A、B两个完全相同的装置,某学生分别在它们的侧管中装入一定量的Na2CO3和NaHCO3,A、B中分别装有足量的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是()A. 侧管中装入Na2CO3的气球膨胀速率大B. 若加入等质量的Na2CO3和NaHCO3 ,最终两气球体积不同C. 最终两试管中Na+、Cl-的物质的量一定相同D. 热稳定性:Na2CO3 < NaHCO35.常温下,向下列溶液中通入足量的CO2有明显变化的是()A. NaOH稀溶液B. NaAlO2溶液C. 饱和NaHCO3溶液D. CaCl2溶液6.下列有关物质用途的说法正确的是()A. 碳酸钠用于治疗胃酸过多B. 稀硫酸用于除铁锈C. 晶体硅用于制造光导纤维D. 硫酸钡用于制作石膏绷带7.根据下列实验操作预测的实验现象正确的是()8.下列说法正确的是()A. 向碳酸氢钠溶液中加入氢氧化钙溶液时,溶液没有浑浊B. 夏日的傍晚常常看到万丈霞光,该现象属于胶体的丁达尔效应C. 过氧化钠是一种强氧化剂,不可作为氧气来源D. 胶体和浊液的分散质都不能通过滤纸的孔隙9.下列关于Na2CO3、NaHCO3说法正确的是()A. 受热时Na2CO3较NaHCO3更不稳定,更易分解产生CO2B. 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多C. 常温下相同物质的量浓度的Na2CO3、NaHCO3溶液,前者碱性更强D. 向Na2CO3、NaHCO3溶液中分别滴加澄清石灰水,前者产生白色沉淀,后者无沉淀能力提升10. 根据反应现象填空。
高中化学 3.1.1 多种多样的碳单质 广泛存在的含碳化合物(精讲优练课型) 鲁科版必修1

【解析】选C。NaHCO3受热容易分解,A项错误。放出1 mol CO2消耗
Na2CO3106 g,消耗NaHCO384 g,B项错误。NaHCO3与盐酸反应的速
率比
Na2CO3要快,这是因为HO C3
CO2
O
3
+H+====H2O+COO2↑32 ,而C
与H+结合生成
分两步进行,先要生成HC ,然后再生成CO2,C项正确。1 mol Na2CO3
第3章 自然界中的元素 第1节 碳的多样性
第1课时 多种多样的碳单质 广泛存在的含碳化合物
一、多种多样的碳单质
单质
1.同素异形体:由同一种元素组成的性质不同的几种_____。
2.碳元素的同素异形体: 金刚石、石墨和C60
(1)常见的同素异形体主要有_________________。
(2)性质不同的原因:碳原子的_排__列__方__式__不同。
C.O2和O3
D.Na和Na+
【解析】选C。由同种元素组成的性质不同的单质是同素异形体。
3.(LK必纯净物 B.金刚石、石墨和C60都是由碳元素组成的 C.石墨转化为金刚石不属于化学变化 D.C60是新发现的一种碳的化合物
【微点拨】C60是由60个碳原子形成的分子。
二、广泛存在的含碳化合物 1.含碳化合物: (1)有机物:如CH4、蛋白质、淀粉等。 (2)无机物:氧化物,如CO、CO2等;碳酸盐,如正盐,如方解石(CaCO3), 白云石[CaMg(CO3)2],菱镁矿(MgCO3),菱铁矿(FeCO3),纯碱或苏打 (Na2CO3),小苏打(NaHCO3)等。 【微点拨】纯碱溶液显碱性,但不是碱。
消耗2 mol HCl,而1 mol NaHCO3消耗1 mol HCl,D项错误。
鲁科版高一化学必修1 第3章第1节 碳的多样性(第1课时) 作业

第3章自然界中的元素第1节碳的多样性第1课时多种多样的碳单质广泛存在的含碳化合物基础过关1. 关于Na2CO3和NaHCO3性质的说法正确的是()A. 25 ℃时,在水中的溶解度NaHCO3大于Na2CO3B. 用Ba(OH)2溶液能鉴别碳酸钠和碳酸氢钠溶液C. 受热时,NaHCO3比Na2CO3容易分解D. NaHCO3和Na2CO3各1 mol分别与过量盐酸充分反应,产生CO2的质量不同2.我国医学家通过研究发现小苏打可去除肿瘤内的氢离子,从而快速有效地杀死处于葡萄糖饥饿或缺乏状态的肿瘤细胞,为治疗原发性肝癌开辟了新路径。
下列有关小苏打的说法错误的是()A. 可用于制备苏打B. 可用于糕点生产中C. 与H+作用易产生CO2D. 可用饱和食盐水与CO2反应制得3.下列各物质混合后,不能生成NaOH的是()A. Na和H2OB. Na2O2和H2OC. Na2CO3和Ca(OH)2D. NaCl和Ca(OH)24.下列实验能成功的是()①用MgCl2溶液鉴别Na2CO3和NaOH溶液②用稀盐酸鉴别Na2CO3溶液和NaHCO3溶液③用观察法区别Na2O和Na2O2④用澄清石灰水鉴别Na2CO3和NaHCO3固体A. ①②③④B. ③④C. ②③D. ②③④5.下列各组中的两种物质作用时,反应条件(温度、反应物用量等)改变,不会引起产物改变的是()A. Na2O2和CO2B. NaOH和CO2C. Na和O2D. Na2CO3和HCl6.碳素墨水是一种以炭黑为颜料的黑色墨水,签署需要长时间保存的重要文件时,通常要求使用碳素墨水。
这是利用了碳的()A. 导电性B. 水溶性C. 氧化性D. 化学稳定性7.下列相关家庭实验能达到预期目的的是()8.向NaOH和Na2CO3混合溶液中滴加0.1 mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是()A. a点时溶液中存在c(Na+)=c(HCO-3)+c(CO2-3)+c(H2CO3)B. 0~a段溶液中水电离出的OH-浓度先增大后减小C. a=0.2D. ab段发生反应的离子方程式为CO2-3+2H+===H2O+CO2↑9.下列试剂不能把等物质的量浓度的Na2CO3溶液、NaHCO3溶液鉴别开的是()A. CaCl2溶液B. 澄清石灰水C. 稀盐酸D. pH试纸能力提升10. 化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
学年鲁科版必修1第3章第1节碳的多样性(第1课时)作业

学年鲁科版必修1第3章第1节碳的多样性(第1课时)作业第1课时 多种多样的碳单质 普遍存在的含碳化合物一、选择题1.假设国际社会可以就温室效应气体减排达成«后京都议定书»,到2020年兴旺国度全体上会减排30%。
大气中CO 2的含量添加会惹起〝温室效应〞,自然界消耗CO 2的反响主要是( )A .CO 2+2NaOH===Na 2CO 3+H 2OB .CaCO 3+CO 2+H 2O===Ca(HCO 3)2C .6CO 2+6H 2O ――→光叶绿素C 6H 12O 6(葡萄糖)+6O 2D .CO 2+C=====高温2CO 2.以下各组物质,不属于同素异形体的是( )A .金刚石和石墨B .白磷和红磷C .Na 2O 和Na 2O 2D .氧气和臭氧3.以下各组物质不用任何外加试剂,只用胶头滴管和试管就能鉴别的是( )A .AgNO 3溶液和NaCl 溶液B .BaCl 2溶液和KHSO 4溶液C .CaCl 2溶液和Na 2CO 3溶液D .Na 2CO 3溶液和盐酸4.以下离子组在溶液中能少量共存的是( )A .Na +、Ca 2+、HCO -3、CO 2-3B .K +、H +、CO 2-3、HCO -3C .Na +、Ba 2+、HCO -3、OH -D .Ca 2+、Ba 2+、Cl -、HCO -35.[双选]关于Na 2CO 3和NaHCO 3的说法中,正确的选项是( )A .Na 2CO 3的溶解度在相反条件下比NaHCO 3的溶解度大,NaHCO 3比Na 2CO 3动摇B .Na 2CO 3既可与CaCl 2溶液反响,也可与石灰水反响C .NaHCO 3既可与CaCl 2溶液反响,也可与石灰水反响D .等物质的量的Na 2CO 3和NaHCO 3与足量盐酸反响,消耗HCl 的物质的量之比为2∶1,而放出的气体的物质的量之比为1∶16.向碳酸钠浓溶液中逐滴参与稀盐酸直到不再发生二氧化碳气体为止,那么在此进程中,溶液中碳酸氢根离子浓度变化趋向能够是( )A .逐渐减小B .逐渐增大C .先逐渐增大,然后减小D .先逐渐减小,然后增大7.为了检验某含有NaHCO 3杂质的Na 2CO 3样品的纯度,现将w 1 g 样品加热,其质质变为w 2 g ,那么该样品的纯度(质量分数)是( )A.84w 2-53w 131w 1B.84(w 1-w 2)31w 1C.73w 2-42w 131w 1D.115w 2-84w 131w 18.不用任何试剂就能鉴别的一组物质是( )A .Na 2CO 3和NaHCO 3B .Na 2CO 3和NaClC .Na 2CO 3和盐酸D .NaHCO 3和盐酸9.关于Na 2CO 3和NaHCO 3性质的说法不正确的选项是( )A .热动摇性:NaHCO 3<Na 2CO 3B .在水中的溶解性:NaHCO 3<Na 2CO 3C .与盐酸反响的速率:NaHCO 3<Na 2CO 3D .等物质的量的Na 2CO 3、NaHCO 3区分与足量盐酸反响发生的CO 2质量相反10.为除去括号内的大批杂质,所选用的试剂或方法不正确的选项是( )A .Na 2CO 3溶液(NaHCO 3),参与过量的NaOH 溶液B .NaHCO 3溶液(Na 2CO 3),通入过量的CO 2气体C .Na 2O 2粉末(Na 2O),将混合物在空气中加热D .Na 2CO 3溶液(Na 2SO 4),参与过量的Ba(OH)2溶液,过滤11.现加热5 g 碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量增加了0.31 g ,那么原混合物中碳酸钠的质量为( )A .3.38 gB .4.58 gC .4.16 gD .4.41 g12.在10 mL 0.01 mol·L -1的Na 2CO 3溶液中,不时搅拌下逐滴参与1.2 mL 0.05 mol·L-1的盐酸,完全反响后,在规范状况下生成CO 2的体积为( ) A .1.34 mL B .2.24 mLC .0.672 mLD .0二、非选择题13.某同窗拟用50 mL NaOH 溶液吸收CO 2气体制备Na 2CO 3溶液。
2019高中化学 第3章第1节第1课时 多种多样的碳单质和广泛存在的含碳化合物作业 鲁科版必修1

第1课时 多种多样的碳单质和广泛存在的含碳化合物知能演练 轻松闯关[学生用书单独成册][基础温故]1.下列各组物质,不属于同素异形体的是( )A .金刚石和石墨B .白磷和红磷C .Na 2O 和Na 2O 2D .氧气和臭氧答案:C2.除去混在碳酸钠粉末中的少量碳酸氢钠,最合理的方法是( )A .加热B .加NaOH 溶液C .加盐酸D .加CaCl 2溶液解析:选A 。
除杂要注意四个原则:不增、不减、不变、易分离,根据Na 2CO 3和NaHCO 3的性质及状态应选择加热的方法除去NaHCO 3。
3.可以用来判定碳酸氢钠粉末中混有碳酸钠的实验方法是( )A .加热时有无色气体放出B .溶于水,滴加CaCl 2溶液,有白色沉淀生成C .滴加盐酸有气泡产生D .溶于水,滴加澄清石灰水,有白色沉淀生成解析:选B 。
NaHCO 3受热易分解,Na 2CO 3不分解,加热时有气体放出,无法判定混有Na 2CO 3,A 项错误;CaCl 2+Na 2CO 3===CaCO 3↓+2NaCl ,NaHCO 3与CaCl 2不反应,滴加CaCl 2溶液有白色沉淀生成,说明该粉末中有Na 2CO 3,B 项正确;NaHCO 3、Na 2CO 3均能与盐酸反应产生气泡,故无法判定Na 2CO 3的存在,C 项错误;Na 2CO 3与Ca(OH)2反应:Na 2CO 3+Ca(OH)2===CaCO 3↓+2NaOH ,产生白色沉淀,NaHCO 3与Ca(OH)2反应也能产生CaCO 3白色沉淀,故无法判定Na 2CO 3的存在,D 项错误。
4.下列关于Na 2CO 3和NaHCO 3的说法中,正确的是( )A .在加热条件下,Na 2CO 3、NaHCO 3都能分解产生CO 2气体B .饱和Na 2CO 3溶液中通入足量CO 2,溶液中无明显现象C .石灰水与Na 2CO 3反应产生沉淀,与NaHCO 3反应不产生沉淀D .可用稀盐酸来区分Na 2CO 3溶液和NaHCO 3溶液解析:选D 。
2021-2021学年高中化学 第3章 第1节 碳的多样性(第1课时)课时作业 鲁科版必修1(1)

2021-2021学年高中化学 第3章 第1节 碳的多样性(第1课时)课时作业 鲁科版必修11.具有可燃性和还原性的固体单质是( ) A .H 2 B .C C .Fe D .CO【解析】 上述四种物质都具有还原性,可是A 项为气体;C 项不可燃;D 项是化合物。
【答案】 B2.柴炭、一氧化碳在必然条件下都能与CuO 发生反映,以下表达正确的选项是 ( )A .反映中C 、CO 都取得氧,发生还原反映B .反映前后C 、Cu 、O 三种元素的化合价都发生了转变 C .反映都必需在加热或高温的条件下才能进行D .反映导出的气体都有毒,需进行处置以避免空气污染【解析】 C +CuO=====△Cu +CO↑,CO +CuO=====△Cu +CO 2,上述两反映中只有C 、Cu 两种元素化合价发生转变;C 和CO 均发生氧化反映。
【答案】 CD3.(2021·厦门高一检测)在炼铁高炉中,要紧发生了以下反映:①C+O 2=====点燃CO 2,②C+CO 2=====高温2CO ,③3CO+Fe 2O 3=====高温3CO 2+2Fe ,④CaCO 3=====高温CaO +CO 2↑,⑤CaO+SiO 2=====高温CaSiO 3,其中既属于化合反映又属于氧化还原反映的有( )A .1个B .2个C .3个D .4个【解析】化合反映是①②⑤,而氧化还原反映中反映前后均有化合价发生转变,那么只有①②符合。
【答案】B4.以下各溶液与强酸溶液反映,不能用离子方程式HCO-3+H+===CO2↑+H2O表示的是( )A.碳酸氢钾溶液B.纯碱溶液C.碳酸氢钙溶液D.小苏打溶液【解析】纯碱(Na2CO3)与强酸反映的离子方程式为CO2-3+2H+===CO2↑+H2O或CO2-3+H+===HCO-3。
【答案】B5.(2021·黑龙江北安第一中学高一月考)以下各组物质彼此作用,生成物不随反映条件或反映物的用量转变而转变的是( )A.Na和O2B.NaOH和CO2C.Ca(HCO3)2和Ca(OH)2D.Na2CO3和HCl【解析】Na与O2在常温下反映生成Na2O,在点燃或加热条件下反映生成Na2O2,A不正确;NaOH与少量CO2反映时生成Na2CO3,与足量CO2反映时生成NaHCO3,B 不正确;Na2CO3与少量盐酸反映时生成NaHCO3和NaCl,与足量盐酸反映时生成NaCl、CO2和H2O,D不正确。
鲁科版高一化学必修1 第3章第1节 碳的多样性 作业

第1节碳的多样性1.下列叙述中,正确的是()A.由碳元素的单质组成的物质一定是纯净物B.金刚石和石墨具有相同的化学组成C.金刚石与石墨之间的转化不属于化学变化D.C60是新发现的一种碳的化合物答案:B2.一天,小影惊奇地发现妈妈蒸馒头时用的不是纯碱,而是小苏打,她好奇地问:“为什么不用纯碱而用小苏打?”妈妈说:“面团没发酵,不能用纯碱。
”通过查阅资料小影发现小苏打的化学式为NaHCO3,是一种常用的膨松剂,加热可转化为纯碱。
下列相关的推断不合理的是() A.小苏打可作膨松剂是因为能产生二氧化碳气体B.小苏打受热转化为纯碱是分解反应C.小苏打属于酸D.小苏打对人体无害解析:小苏打是NaHCO3,NaHCO3属于盐而不属于酸,C选项错误。
答案:C3.下列说法中不正确的是()A.Na2CO3比NaHCO3易溶于水B.Na2CO3比NaHCO3稳定C.Na2CO3和NaHCO3都能跟石灰水反应得到白色沉淀D.物质的量相等的Na2CO3和NaHCO3分别与盐酸反应得CO2的物质的量之比为2∶1解析:物质的量相等的Na 2CO 3和NaHCO 3分别与盐酸反应得CO 2的物质的量之比为1∶1。
答案:D4.除去混在Na 2CO 3粉末中的少量NaHCO 3,最合理的方法是( )A .加热B .加氢氧化钠溶液C .加盐酸D .加氢氧化钙解析:2NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O ↑,因此用加热法除NaHCO 3便于操作。
答案:A5.下列离子方程式正确的是( )A .钠与水反应:2Na +H 2O===2Na ++OH -+H 2↑B .氧化钠与盐酸反应:O 2-+2H +===H 2OC .碳酸氢钠与稀硫酸反应:HCO -3+H +===CO 2↑+H 2OD .Ba(OH)2溶液与小苏打溶液反应:HCO -3+OH -===CO 2-3+H 2O解析:A 项,电荷不守恒;B 项,Na 2O 不能拆写;D 项应该生成BaCO 3沉淀。
高中化学 第3章 第1节 碳的多样性(第1课时)课时作业

2013-2014学年高中化学 第3章 第1节 碳的多样性(第1课时)课时作业 鲁科版必修11.具有可燃性和还原性的固体单质是( ) A .H 2 B .C C .Fe D .CO【解析】 上述四种物质都具有还原性,但是A 项为气体;C 项不可燃;D 项是化合物。
【答案】 B2.木炭、一氧化碳在一定条件下都能与CuO 发生反应,下列叙述正确的是( )A .反应中C 、CO 都得到氧,发生还原反应B .反应前后C 、Cu 、O 三种元素的化合价都发生了变化 C .反应都必须在加热或高温的条件下才能进行D .反应导出的气体都有毒,需进行处理以防止空气污染【解析】 C +CuO=====△Cu +CO↑,CO +CuO=====△Cu +CO 2,上述两反应中只有C 、Cu 两种元素化合价发生变化;C 和CO 均发生氧化反应。
【答案】 CD3.(2012·厦门高一检测)在炼铁高炉中,主要发生了下列反应:①C+O 2=====点燃CO 2,②C +CO 2=====高温2CO ,③3CO+Fe 2O 3=====高温3CO 2+2Fe ,④CaCO 3=====高温CaO +CO 2↑,⑤CaO+SiO 2=====高温CaSiO 3,其中既属于化合反应又属于氧化还原反应的有( )A .1个B .2个C .3个D .4个【解析】 化合反应是①②⑤,而氧化还原反应中反应前后均有化合价发生变化,则只有①②符合。
【答案】 B4.下列各溶液与强酸溶液反应,不能用离子方程式HCO -3+H +===CO 2↑+H 2O 表示的是( )A .碳酸氢钾溶液B .纯碱溶液C .碳酸氢钙溶液D .小苏打溶液【解析】 纯碱(Na 2CO 3)与强酸反应的离子方程式为CO 2-3+2H +===CO 2↑+H 2O 或CO 2-3+H+===HCO -3。
【答案】 B5.(2012·黑龙江北安第一中学高一月考)下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是( )A .Na 和O 2B .NaOH 和CO 2C .Ca(HCO 3)2和Ca(OH)2D .Na 2CO 3和HCl【解析】 Na 与O 2在常温下反应生成Na 2O ,在点燃或加热条件下反应生成Na 2O 2,A 不正确;NaOH 与少量CO 2反应时生成Na 2CO 3,与足量CO 2反应时生成NaHCO 3,B 不正确;Na 2CO 3与少量盐酸反应时生成NaHCO 3和NaCl ,与足量盐酸反应时生成NaCl 、CO 2和H 2O ,D 不正确。
鲁科版高一化学必修1 第3章第1节 碳的多样性 作业 (1)

第1节碳的多样性学校:__________姓名:__________班级:__________考号:__________1、中国诗词中常蕴含着一些自然科学知识,针对下列一些诗词,从化学角度解读正确的是()A. “落红不是无情物,化作春泥更护花”蕴藏着自然界中碳、氮的循环B. “纷纷灿烂如星陨,赫赫喧豗似火攻”描述了显色反应的现象C. “独忆飞絮鹅毛下,非复青丝马尾垂”中的“飞絮”与“马尾”化学成分相同D. “日照香炉生紫烟,遥看瀑布挂前川”中的“紫烟”是碘的升华现象2、下列用于解释事实的化学用语中,不正确的是()A. Na2S溶液显碱性: S2-+ 2H2O H2S + 2OH-B. K2Cr2O7溶液中含有CrO42-:Cr2O72- + H2O2CrO42- + 2H+C. 盛放NaOH 溶液的试剂瓶不能用玻璃塞: 2OH-+ SiO2=SiO32-+ H2OD. 红热木炭遇浓硫酸产生刺激性气味气体: 2H2SO4( 浓)+C CO2↑+2SO2↑+2H2O3、平昌冬奥会“北京8 分钟”主创团队用石墨烯制作了-20℃能发热4 h 的智能服饰; 用铝合金管材和碳纤维制作了高2.35m、重量仅为10kg 的熊猫木偶,向世界展现了新时代的中国形象。
下列说法中,不正确的是()A. 石墨烯是能导热的金属材料B. 铝合金是密度较低的金属材料C. 碳纤维是耐低温的无机非金属材料D. 新型材料种类多、用途广4、近年来,我国在航空航天事业上取得了令人瞩目的成就,科学家在能量的转化,航天器的零排放作出了很大的努力,其中为了达到零排放的要求,循环利用人体呼出的CO2并提供O2,设计了一种装置(如图)实现了能量的转化,总反应方程式为2CO2=2CO+O2。
关于该装置下列说法正确的是()A. 装置中离子交换膜为阳离子交换膜B. CO2参与X电极的反应方程式:CO2+2eˉ+H2O=CO+2OHˉC. N型半导体为正极,P型半导体为负极D. 外电路每转移2mol电子,Y极生成气体22.4L(标准状况)5、为测定石灰石样品中碳酸钙(含SiO2杂质)的含量。
鲁科版高中化学必修一:第三章第一节《碳的多样性》练习.docx

高中化学学习材料唐玲出品一.多种多样的碳单质:1.同素异形体:由组成的性质几种。
如:氧元素的同素异形体有和,碳元素的同素异形体有、和。
2.碳元素的三种重要的单质:石墨是一种色、、、的片状固体。
金刚石是极高、色的晶体。
C60是色的固体。
3. 不同,决定了碳的各种单质有着不同的性质。
二.广泛存在的含碳化合物:注意:下表中是离子反应的写出离子方程式,不能反应的用“——”表示:一、选择题:1.关于金刚石和石墨的说法中,不正确的是()A.它们都是由碳元素组成的单质B.它们都是电的良导体C.它们里面的碳原子排列不同D.金刚石质硬,石墨质软知识梳理2.下列属于同素异形体的是()①金刚石与C60②O2与O3 ③FeO与Fe2O3 ④红磷与白磷⑤CO2与干冰A.只有①②B.①②④C.①②④⑤D.全部都是3.近年来,科学家研制的一种新的分子,具有空心的类似足球的结构,分子式为C60,下列说法中正确的是()A.C60是一种新型的化合物B.C60在纯氧中燃烧只生成唯一产物CO2C.C60和石墨都是碳的同素异形体D.C60的摩尔质量是720g4.下列物质中,与Na2CO3、NaHCO3都能发生反应的是(双选题)()A.盐酸B.石灰水C.氢氧化钠D.氯化钙溶液5.下列各组离子在水溶液中能大量共存的是()A.Ba2+、HCO3-、Na+、Cl-B.Ca2+、Cl-、CO32-、Na+C. HCO3-、Na+、NO3-、H+D. OH-、Na+、HCO3-、Cl-6.为制备纯净干燥的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入()A.水;无水CaCl2固体B. 饱和NaHCO3溶液;浓硫酸C.浓硫酸;饱和NaHCO3溶液D. 饱和NaHCO3溶液;稀硫酸7. 关于NaHCO3和Na2CO3的下列说法中正确的是()A. Na2CO3比NaHCO3更难溶于水B. 石灰水能和NaHCO3反应,不与Na2CO3反应C. NaHCO3比Na2CO3稳定D.等物质的量的Na2CO3和NaHCO3与盐酸反应,消耗盐酸的物质的量之比为2:18.将石墨在一定条件下转化为金刚石的变化说法正确的是()A.不是化学变化B.金刚石和石墨性质相同C.是氧化还原反应D.是化学变化但不是氧化还原反应9.取两份质量相同的小苏打,一份直接与稀盐酸反应,另一份先加热至恒重,再与稀盐酸反应,下列说法正确的是( )A.消耗相同浓度的盐酸一样多B.消耗同浓度的盐酸后者多C.与盐酸反应后相同条件下收集的气体一样多(不包括加热生成的)D.与盐酸反应后相同条件下收集的气体后者多。
高中化学 第1节 碳的多样性 第1课时 碳单质的多样性及含碳化合物课时训练 鲁科版必修1

【金版学案】2014-2015学年高中化学第1节碳的多样性第1课时碳单质的多样性及含碳化合物课时训练鲁科版必修1水平测试1.将珍珠放入稀盐酸中,有气泡产生,生成的气体能使澄清的石灰水变浑浊,则珍珠中含有下列离子中的( )A.氯离子 B.硫酸根离子C.碳酸根离子 D.氢氧根离子解析:由于生成的气体能使澄清的石灰水变浑浊,故该种气体为CO2,则珍珠中应该含有碳酸根离子。
答案:C2.下列叙述中,正确的是( )A.由碳元素的单质组成的物质一定是纯净物B.金刚石和石墨具有相同的化学组成C.金刚石与石墨之间的转化不属于化学变化D.C60是新发现的一种碳的化合物解析:碳元素形成的单质有多种,不同的单质组成的物质是混合物,金刚石、石墨、C60都是碳元素的单质,它们之间的转化属于化学变化,故B项正确。
答案:B3.为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )A.水;无水CaCl2固体B.饱和NaHCO3溶液;浓H2SO4C.浓H2SO4;饱和Na2CO3溶液D.饱和Na2CO3溶液;稀H2SO4解析: CO2中通常混有HCl、H2O(g),而室温1体积水溶解1体积CO2,故A项错;气体最后通过盛有水溶液的装置时得到的CO2是潮湿的,故C、D两项均错;气体先通过饱和NaHCO3溶液,HCl被吸收且放出CO2,再通过浓H2SO4得以干燥,故B项正确。
答案:B4. 下列物质中分别滴入醋酸,会产生相同气体的是( )①大理石②钟乳石③锅垢④贝壳⑤蛋壳A.①② B.④⑤C.①②③ D.①②③④⑤解析:五种物质的主要成分都是CaCO3,与醋酸反应都会产生CO2气体。
答案:D5.(双选题)关于Na2CO3和NaHCO3的说法中,正确的是( )A.Na2CO3的溶解度在相同条件下比NaHCO3的溶解度大,NaHCO3比Na2CO3稳定B.Na2CO3既可与CaCl2溶液反应,也可与石灰水反应C.NaHCO3既可与CaCl2溶液反应,也可与石灰水反应D.等物质的量的Na2CO3和NaHCO3与足量盐酸反应,消耗HCl的物质的量之比为2∶1,而放出的气体的物质的量之比为1∶1解析:稳定性与溶解性无关,故A项不正确;Na2CO3+CaCl2===CaCO3↓+2NaCl,Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,故B项正确;NaHCO3与CaCl2溶液不反应,与石灰水反应生成CaCO3沉淀,故C项不正确;Na2CO3+2HCl===2NaCl+H2O+CO2↑,NaHCO3+HCl===NaCl+H2O +CO2↑,当n(Na2CO3)=n(NaHCO3)时,消耗n(HCl)之比为2∶1,放出CO2气体物质的量相等,故D项正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章 自然界中的元素 第1节 碳的多样性 第1课时 碳单质的多样性及含碳化合物1.了解同素异形体的概念。
2.了解碳元素的多种存在形态及碳的多种同素异形体。
3.掌握碳酸钠与碳酸氢钠的主要性质以及二者的相互转化、区别与鉴定。
知识清单一、多种多样的碳单质 1.同素异形体。
由同一种元素组成的性质不同的几种单质,如氧元素的同素异形体有O 2和O 3,碳元素的同素异形体有石墨、金刚石和C 60等。
片状固体1.金刚石、石墨和C 60均是由碳元素组成的单质,为什么物理性质不同?答案:物质的结构决定物质的性质。
金刚石、石墨和C 60内部碳原子的排列方式不同,决定了其性质的不同。
2.如何证明石墨、金刚石、C 60是同素异形体?答案:在一定条件下,使金刚石、石墨、C 60分别与氧气反应都生成CO 2气体就可以说明三者是同素异形体。
二、广泛存在的含碳化合物 1.种类繁多的含碳化合物。
碳的化合物⎩⎪⎨⎪⎧有机物:如甲烷、淀粉等无机物⎩⎪⎨⎪⎧氧化物:如CO 、CO 2等碳酸盐:如方解石CaCO 3,白云石CaMg (CO 3)2,菱铁矿MgCO 3,菱铁矿FeCO 3等2.碳酸钠和碳酸氢钠。
相同条件下比=====Na2HCl===Na2CO3 H2O+CO2△或加NaOH NaHCO33.碳酸钠固体中混有碳酸氢钠杂质,如何除去?答案:可用加热的方法。
碳酸氢钠受热不稳定可分解生成碳酸钠、水和二氧化碳。
活学活用1.下列各组物质,不属于同素异形体的是(C)A.金刚石和石墨B.白磷和红磷C.Na2O和Na2O2D.氧气和臭氧解析:同素异形体的研究对象是单质。
2.下列物质的化学名称、化学式和俗名一致的是(C)A.碳酸钙、CaCO3、生石灰B.氢氧化钠、NaOH、纯碱C.碳酸钠、Na2CO3、苏打D.碳酸氢钠、NaHCO3、苏打解析:A项中生石灰是CaO;B项中纯碱是Na2CO3;D项中苏打是Na2CO3。
3.(双选)关于Na2CO3和NaHCO3的说法中,正确的是(BD)A.Na2CO3的溶解度在相同条件下比NaHCO3的溶解度大,NaHCO3比Na2CO3稳定B.Na2CO3既可与CaCl2溶液反应,也可与石灰水反应C.NaHCO3既可与CaCl2溶液反应,也可与石灰水反应D.等物质的量的Na2CO3和NaHCO3与足量盐酸反应,消耗HCl的物质的量之比为2∶1,而放出的气体的物质的量之比为1∶1解析:稳定性与溶解性无关,A不对;Na2CO3+CaCl2===CaCO3↓+2NaCl,Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,B对。
NaHCO3与CaCl2溶液不反应,与石灰水反应生成CaCO3沉淀,C不对。
Na2CO3+2HCl===2NaCl+2H2O+CO2↑,NaHCO3+HCl===NaCl+H2O+CO2↑,当n(Na2CO3)=n(NaHCO3)时,消耗n(HCl)之比为2∶1,放出CO2气体物质的量相等,D对。
水平测试1.下列叙述中,正确的是(B)A.由碳元素的单质组成的物质一定是纯净物B.金刚石和石墨具有相同的化学组成C.金刚石与石墨之间的转化不属于化学变化D.C60是新发现的一种碳的化合物解析:碳元素形成的单质有多种,不同的单质组成的物质是混合物,金刚石、石墨、C60都是碳元素的单质,它们之间的转化属于化学变化。
2.不用任何试剂就能鉴别的一组物质是(C)A.Na2CO3和NaH CO3 B.Na2CO3和NaClC.Na2CO3和盐酸 D.NaHCO3和盐酸解析:将盐酸逐滴滴加到Na2CO3溶液中,开始时无气体生成,而将Na2CO3溶液滴加到盐酸中时,开始便有气体生成,滴加顺序不同,现象不同,不用其他试剂就能鉴别。
3.除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是(A)A.通入二氧化碳气体 B.加入氢氧化钡溶液C.加入澄清石灰水 D.加入稀盐酸解析:Na2CO3+CO2+H2O===2NaHCO3,CO2与NaHCO3不再反应,A对。
Ba(OH)2、Ca(OH)2和稀盐酸都能与NaHCO3和Na2CO3反应,故B、C、D错。
4.向碳酸钠浓溶液中逐滴加入稀盐酸直到不再产生二氧化碳气体为止,则在此过程中,溶液中碳酸氢根离子浓度变化趋势可能是(C)A.逐渐减小 B.逐渐增大C.先逐渐增大,而后减小 D.先逐渐减小,而后增大解析:反应过程可表示为:先:CO2-3+H+===HCO-3;后:HCO-3+H+===H2O+CO2↑。
所以c(HCO-3)先增大后减小。
5.下列关于碳酸钠和碳酸氢钠的比较中正确的是(C)A.碳酸氢钠的溶解度大于碳酸钠B.与盐酸反应放出等量的二氧化碳消耗碳酸钠的质量小于碳酸氢钠C.与等浓度的盐酸反应,碳酸氢钠反应的速率快D.与等质量的碳酸钠和碳酸氢钠反应,碳酸钠消耗盐酸少解析:NaHCO3的溶解性较小,A项错误。
放出1 mol CO2消耗Na2CO3106 g ,消耗NaHCO3 84 g, B项错误。
NaHCO3与盐酸反应的速率比Na2CO3要快,这是因为HCO-3+H+===H2O+CO2↑,而CO2-3与H+结合生成CO2分两步进行,先要生成HCO-3,后再生成CO2,C项正确。
106 g Na2CO3耗73 g HCl,而106 g NaHCO3耗HCl少于73 g,D项不正确。
6.可以说明溶液中大量存在CO2-3的理由是(C)A.加入AgNO3溶液有白色沉淀产生B.加入盐酸有无色无味气体产生C.加入MgCl2时有白色沉淀产生,再加稀盐酸沉淀全部溶解,且产生可以使澄清石灰水变浑浊的无色无味气体D.加入Ba(OH)2溶液有白色沉淀产生,再加稀盐酸,反应现象如选项C所述解析:A项不可说明,与AgNO3作用生成白色沉淀的还有Cl-等;B项不可说明,与盐酸作用产生无色无味气体的还有NaHCO3等;D项不可说明,NaHCO3等物质亦会有此现象。
7.现有A、B、C、D四种化合物都含钾元素,A、B、C和足量的盐酸反应后,均可生成D;若将固体C加热后可生成A和无色无毒的气体E,该气体能使澄清石灰水变浑浊;若在A溶液中通入足量E,可生成C;若B与C的溶液混合可生成A。
请回答下列问题。
(1)推断A、B、C、D的化学式。
A________;B________;C________;D________。
(2)A溶液中通入足量E反应的离子方程式为________________________________________________________________________ ________________________________________________________________________。
(3)B溶液与C溶液反应的离子方程式为________________________________________________________________________ ________________________________________________________________________。
(4)仅凭有气体E生成,______选填“能”或“否”断定A、C的组成。
解析:气体E无色无味且能使澄清石灰水变浑浊,为CO2,C为KHCO3,A为K2CO3;B与KHCO3溶液混合可生成K2CO3,B为KOH,A、B、C和足量的盐酸反应后,均可生成D,D为KCl。
HCO-3和CO2-3都可与盐酸反应生成CO2气体,所以不能仅凭有CO2气体生成,断定哪个是K2CO3,哪个是KHCO3。
答案:(1)K2CO3KOH KHCO3KCl(2)CO2-3+CO2+H2O===2HCO-3(3)OH-+HCO-3===H2O+CO2-3(4)否8.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做以下实验,如图所示。
(1)写出Ⅰ中与盐酸发生反应的化学方程式。
①Na 2CO 3时________________________________________________________________________,②NaHCO 3时________________________________________________________________________,③由此可知此装置________(填“能”或“不能”)鉴别Na 2CO 3和NaHCO 3。
(2)Ⅱ装置能鉴别Na 2CO 3和NaHCO 3的现象是________________________________________________________________________________________________________________________________________________。
(3)Ⅲ、Ⅳ装置均利用了Na 2CO 3和NaHCO 3________性的区别。
有关化学方程式为________________________________________________________________________。
(4)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B 中装入的固体最好是________(填化学式)。
有的同学在盛Na 2CO 3的导管口观察到开始加热时也有气泡产生,据此认为Na 2CO 3加热也能分解。
你认为此观点________(填“正确”或“错误”)。
分析此现象的原因为________________________________________________________________________。
________________________________________________________________________。
(5)除了以上方法,请你再举出一例鉴别二者的方法________________________________________________________________________________________________________________________________________________。
解析:鉴别Na 2CO 3和NaHCO 3是利用二者性质的差别,Ⅰ中二者均能与盐酸反应产生CO 2,现象相同,不能鉴别;Ⅱ中Na 2CO 3、NaHCO 3加入等浓度的盐酸中,NaHCO 3反应剧烈,产生的气体多,气球膨胀的快;NaHCO 3不稳定,受热分解,而Na 2CO 3稳定,受热不分解,Ⅳ中的试管B 在试管A 内部,不能直接接触到火焰,温度相对较低,故试管B 中装入的固体是易分解的NaHCO 3,NaHCO 3受热分解产生的CO 2使澄清石灰水变浑浊;鉴别Na 2CO 3和NaHCO 3还可利用其在溶液中电离出的阴离子的不同选择试剂,CO 2-3与Ba 2+或Ca 2+反应生成白色沉淀,HCO -3不反应。
