关于肌红肌钙室间质控问题说明
2002年全国心肌标志物测定室间质量评价

方法学编码
2002年全国心肌标志物测定项目:肌酸激酶-MB、肌红蛋白、肌钙蛋白I、肌钙蛋白T的方法学编码如下:
方法学编码方法学名称
2501速率法
2502免疫抑制法
2503免疫比浊法
2504琼脂糖凝胶电泳法
2505离子交换柱层析
2506免疫化学测定法
2507免疫学沉淀法
Friedewald公式计算
电泳
超速离心
沉淀-磁分离
其它沉淀方法
均匀性–消除法
均匀性–液体选择性洗涤剂
ApoA1
免疫透射比浊法
免疫火箭电泳法
速率散射比浊法
酶法ApoBLeabharlann 速率散射比浊法酶法
免疫火箭电泳法
脂蛋白(a)ELISA法
2508微粒子酶免疫分析法
2509化学发光法
2510放射免疫法
2511荧光酶免疫法
2512电化学发光法
2599其它
肌酸激酶-MB
速率法、酶法、
免疫抑制法
发光免疫分析法
化学发光法
荧光酶免疫法
免疫比浊法
琼脂糖凝胶电泳法
离子交换柱层析
免疫化学测定法(结果ng/mL)
电泳(结果%)
免疫化学抑制法
免疫学沉淀法
电泳(结果U/L)
柱层析
其它
微粒子酶免疫分析法
化学发光法
放射免疫法
荧光酶免疫法
电化学发光法
肌红蛋白
微粒子酶免疫分析法
化学发光法
放射免疫法
荧光酶免疫法
电化学发光法
肌钙蛋白I
金标
发光免疫分析法
微粒子酶免疫分析法
化学发光法
室间质量评价结果分析及整改

临床化学检验及临床尿液室间质量评价结果分析一、临床化学:1 、方法监测项目为钾、钠、氯、钙、磷、血糖、尿素、尿酸、肌酐、总蛋白、白蛋白、胆固醇、甘油三酯、总胆红素、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、碱性磷酸酶、淀粉酶、肌酸激酶及胆固醇,共20个项目。
2 结果我院使用临床化学标本批号为201602,我院开展并提供的六项数据血糖3.56为(预期检测结果为3.65),白蛋白为26.3(预期检测结果为23.2),胆固醇为2.3(预期检测结果为2.2),甘油三酯为0.84(预期检测结果为0.71),丙氨酸氨基转移酶为38(预期检测结果为36),天门冬氨酸氨基转移酶为32(预期检测结果为31.8)。
3不合格原因分析能力比对检验(PT)不合格数最多的项目白蛋白(Alb),原因为质控物的基质效应和测定方法的固有特征所导致的;其他项目不合格的原因是由于这些项目都是使用电极法测定,由于电极法检测原理特性而导致的。
二、临床尿液质评:1 、方法监测项目为PH值、比重、蛋白、葡萄糖、隐血、酮体、胆红素、亚硝酸盐、尿胆原、白细胞、维生素C,共11个项目。
2 结果我院使用临床尿液标本批号为201602,我院提供的数据为PH值5.0(预期检测结果为5.6)、比重1.010(预期检测结果为1.021)、蛋白阴性(预期检测结果为+)、葡萄糖阴性(预期检测结果为++)、隐血阴性(预期检测结果为+++)、酮体+(预期检测结果为+++)、胆红素+++(预期检测结果为++)、亚硝酸盐阴性(预期检测结果为+)、尿胆原阴性(预期检测结果为++)、白细胞阴性(预期检测结果为阴性)、维生素C为0(预期检测结果为++)。
3不合格原因分析经推断认为,我院尿液分析仪存在设备老化,误差较大的情况。
临床化学检验及临床尿液室间质量评价情况整改报告根据济宁市临床检验中心反馈的《2016年度检验医学室间评价第一次质评结果》,我院认真查找不合格原因,依据查找出的原因,做出了以下几点改进措施:一、加强对医护人员的培训,要求检验科室的工作人员均熟练掌握相关知识,使工作人员能够提高对标本质量影响因素的防范意识。
室内质控问题及思考

比对实验:与校准系统或封闭系统比较 室间质评:同组仪器比较
设定控制限
通过重复试验,得到SD,与质量目标比较 过大:说明检测系统不能满足质量要求 过小:
下限,通常以标准差的倍数表示。
基本概念
准确度 (Accuracy):待测物的测定值与
其真值的一致性程度。准确度不能直接以 数值表示,通常以不准确度来间接衡量。 对一分析物重复多次测定,所得均值与其 真值或参考靶值之间的差异亦即偏差即为 测定的不准确度。
偏倚 (Bias): 待测物的测定值与真值之
是否必须对“定值”控制品建立均值和范围?
• CLIA – 只要靶值,只适用于使用的方法和仪器。必须通过重复检测 确定均值与标准差
• CLSI – 定值仅供参考,必须通过重复检测建立自己的值 • 临床实验室定量测定室内质量控制指南 –若使用定值质控品,使用
说明书上的原有标定值只能作参考。必须由实验室作重复测定来确 定实际的均值和标准差。
室内质控存在的 问题及思考
室内质控的目的
提高常规测定工作中检测结果的 一致性。
检测、控制本实验室测定工作的 精密度,并检测其准确度的改变。
室内质控的基本方法
临床标本检测的特点是每个标 本仅检测一次,无法了解其精 密度
方法:每天使用同一质控物, 采用一系列统计学的方法,连 续地评价本实验室测定工作的 可靠程度。
的质控品作平行检测,最好在不同天内至少作20瓶的检测。若无法从20天内得到 20个数值,至少在5天内获得。
同种控制品更换批号 • CLSI – 至少需要20批的结果 • CLSI– 开始使用新批号前,与老批号进行20批的比对 • 临床实验室定量测定室内质量控制指南 – 新批号质控品的每个
室间质量评价结果分析及整改

室间质量评价结果分析及整改一、临床化学:1 、方法监测项目为钾、钠、氯、钙、磷、血糖、尿素、尿酸、肌酐、总蛋白、白蛋白、胆固醇、甘油三酯、总胆红素、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、碱性磷酸酶、淀粉酶、肌酸激酶及胆固醇,共20个项目。
2 结果我院使用临床化学标本批号为,我院开展并提供的六项数据血糖3、56为(预期检测结果为3、65),白蛋白为26、3(预期检测结果为23、2),胆固醇为2、3(预期检测结果为2、2),甘油三酯为0、84(预期检测结果为0、71),丙氨酸氨基转移酶为38(预期检测结果为36),天门冬氨酸氨基转移酶为32(预期检测结果为31、8)。
3不合格原因分析能力比对检验(PT)不合格数最多的项目白蛋白(Alb),原因为质控物的基质效应和测定方法的固有特征所导致的;其他项目不合格的原因是由于这些项目都是使用电极法测定,由于电极法检测原理特性而导致的。
2、临床尿液质评:1 、方法监测项目为PH值、比重、蛋白、葡萄糖、隐血、酮体、胆红素、亚硝酸盐、尿胆原、白细胞、维生素C,共11个项目。
2 结果我院使用临床尿液标本批号为,我院提供的数据为PH值5、0(预期检测结果为5、6)、比重1、010(预期检测结果为1、021)、蛋白阴性(预期检测结果为+)、葡萄糖阴性(预期检测结果为++)、隐血阴性(预期检测结果为+++)、酮体+(预期检测结果为+++)、胆红素+++(预期检测结果为++)、亚硝酸盐阴性(预期检测结果为+)、尿胆原阴性(预期检测结果为++)、白细胞阴性(预期检测结果为阴性)、维生素C为0(预期检测结果为++)。
3不合格原因分析经推断认为,我院尿液分析仪存在设备老化,误差较大的情况。
临床化学检验及临床尿液室间质量评价情况整改报告根据济宁市临床检验中心反馈的《xx年度检验医学室间评价第一次质评结果》,我院认真查找不合格原因,依据查找出的原因,做出了以下几点改进措施:1、加强对医护人员的培训,要求检验科室的工作人员均熟练掌握相关知识,使工作人员能够提高对标本质量影响因素的防范意识。
卫生部临床检验中心室间质量评价标准

2017年卫生部临床检验中心室间质量评价标准临床化学(NCCL-C-01)2017年2016年钾靶值±6%靶值±L钠靶值±4%靶值±4mmol/L氯靶值±5%靶值±5%钙靶值±5%靶值±LdL)磷靶值±10%靶值±L或靶值±%(取大者)葡萄糖靶值±7%靶值±L(6mg/dL)或±10%(取大者)尿素靶值±8%靶值±L或±9%(取大者)尿酸靶值±12%靶值±17%肌酐靶值±12%靶值±L(dL)或±15%(取大者)总蛋白靶值±5%靶值±10%白蛋白靶值±6%靶值±10%总胆固醇靶值±9%靶值±10%甘油三酯靶值±14%靶值±25%高密度脂蛋白胆固醇靶值±30%总胆红素靶值±15%靶值±L(dL)或±20%(取大者)丙氨酸氨基转移酶靶值±16%靶值±20%天门冬氨酸氨基转移酶靶值±15%靶值±20%碱性磷酸酶靶值±18%靶值±30%淀粉酶靶值±15%靶值±30%肌酸激酶靶值±15%靶值±30%乳酸脱氢酶靶值±11%靶值±20%直接胆红素靶值±2s靶值±2s铁靶值±15%靶值±20%总铁结合力靶值±2s镁靶值±15%靶值±25%锂靶值±L 或±20%(取大者)铜靶值±2s锌靶值±2s酸性磷酸酶靶值±30%γ-谷氨酰基转移酶靶值±11%靶值±20%α-羟丁酸脱氢酶靶值±30%靶值±30%胆碱酯酶靶值±20%靶值±20%脂肪酶靶值±20%靶值±20%心肌标志物肌酸激酶-MB(ug/L)靶值±30%靶值±30%肌红蛋白靶值±30%靶值±30%肌钙蛋白-I靶值±30%靶值±30%肌钙蛋白-T靶值±30%靶值±30%肌酸激酶-MB(U/L)靶值±30%超敏CRP靶值±30%靶值±30%同型半胱氨酸靶值±μmol/L 或±20%(取大者)脂类胆固醇靶值±9%靶值±10%甘油三酯靶值±14%靶值±25%高密度脂蛋白胆固醇靶值±30%靶值±30%低密度脂蛋白胆固醇靶值±30%靶值±30%载脂蛋白A1靶值±30%靶值±30%载脂蛋白B靶值±30%靶值±30%脂蛋白(a)靶值±30%血气分析pH靶值±靶值±靶值±5mmHg 或±8%(取大者)靶值±5mmHg或±8%(取大者)pO2靶值±8%靶值±2SNa+靶值±4%靶值±4mmol/LK+靶值±6%靶值±LCa2+靶值±5%靶值±LCl-靶值±4%靶值±5%特殊蛋白IgG、IgA、IgE、IgM、C3、C4、C-反应蛋白(CRP)、类风湿因子(RF)、抗链球菌溶血素O(ASO)、转铁蛋白(TRF)、前白蛋白(PA)靶值±25%靶值±25%内分泌总T4靶值±20%靶值±20%叶酸靶值±30%靶值±30%皮质醇、雌二醇、FSH、LH、孕酮、催乳素、睾酮、C-肽、FT3、TT3、FT4、胰岛素、维生素B12、25-OH-VD2、25-OH-VD3、总25-OH-VD靶值±25%靶值±25%肿瘤标志物CEA、AFP、HCG、PSA、CA199、CA125、CA153、β2-微球蛋白、铁蛋白、总β-HCG、游离PSA靶值±25%全血治疗药物监测环孢霉素A、他克莫司、西罗莫司靶值±25%血清治疗药物监测卡马西平靶值±25%地高辛靶值±20% 或±μg/L苯妥英靶值±25%茶碱靶值±25%丙戊酸靶值±25%糖化血红蛋白HbA1c靶值±8%脑钠肽/N末端前脑钠肽BNP、NT-proBNP靶值±30%尿液定量生化钾靶值±29%钠靶值±26%氯靶值±26%钙靶值±31%镁靶值±25%磷靶值±23%葡萄糖靶值±20%尿素靶值±21%尿酸靶值±24%肌酐靶值±17%总蛋白靶值±44%白蛋白靶值±30%淀粉酶靶值±30%微量白蛋白靶值±30%半胱氨酸蛋白酶抑制剂C半胱氨酸蛋白酶抑制剂C靶值±25%代谢物、总蛋白正确度验证葡萄糖靶值±%尿素靶值±%尿酸靶值±6%肌酐靶值±6%总蛋白靶值±%脂类正确度验证总胆固醇靶值±%甘油三酯靶值±%高密度脂蛋白胆固醇靶值±%酶学正确度验证ALT(含磷酸吡哆醛)靶值±6%AST(含磷酸吡哆醛)靶值±5%GGT靶值±%LDH靶值±4%CK靶值±%AMY靶值±%ALP靶值±10%糖化血红蛋白正确度验证HbA1c靶值±6%电解质正确度验证钠靶值±%钾靶值±2%钙靶值±2%镁靶值±%一般免疫学抗核抗体反应性或阴性抗-HIV反应性或阴性肝炎(HBsAg,anti-HBc,HBeAg)反应性或阴性风疹反应性或阴性全血细胞计数白细胞计数靶值±15%红细胞计数靶值±6%血红蛋白测定靶值±6%血细胞比容靶值±9%血小板计数靶值±20%MCV靶值±7%MCH靶值±7%MCHC靶值±8%凝血试验PT靶值±15%INR靶值±20%APTT靶值±15%Fbg靶值±20%尿液化学分析比重靶值±1等级PH靶值±1等级蛋白、葡萄糖、胆红素、酮体、红细胞、尿胆原、白细胞阳性时:靶值±1等级亚硝酸盐阴性或阳性红细胞沉降率测定红细胞沉降率靶值±(≤10时)或靶值±30%(>10时)流式细胞分析CD3+、CD3+CD4+、CD3+CD8+、CD3-CD16+CD56+、CD3-CD19+ 靶值±2s血液粘度检测切变率为1/S下的粘度()靶值±2s切变率为50/S下的粘度()靶值±2s切变率为200/S下的粘度()靶值±2s网织红细胞计数网织红细胞百分比(%)靶值±2s全血细胞计数正确度验证白细胞计数靶值±15%红细胞计数靶值±6%血红蛋白测定靶值±6%血细胞比容靶值±9%血小板计数靶值±20%MCV靶值±7%MCH靶值±7%MCHC靶值±8%凝血因子检测FⅧ、FⅨ靶值±30%D-二聚体检测D-Dimer靶值±2s新生儿遗传代谢病筛查-Phe、TSH苯丙氨酸靶值±30% 或±1mg/dL(取大值)促甲状腺素靶值±30%中孕期母血清产前筛查AFP 靶值±30% 或±5μg/L(取大值)hCG 靶值±30%β-hCG靶值±30%Free-β-hCG 靶值±30%游离雌三醇靶值±30%血铅血铅靶值±40μg/L 或±10%(取大值)便携式血糖检测仪葡萄糖靶值±20% 或±1mmol/L(取大值)脑脊液生化白蛋白靶值±10% 或±L(取大值)总蛋白靶值±10% 或±L(取大值)氯化物靶值±5%葡萄糖靶值±10% 或±L(取大值)乳酸脱氢酶靶值±20%IgA靶值±25%IgG靶值±25%IgM靶值±25%乳酸靶值±20% 或±L(取大值)全血五元素铜靶值±2s锌靶值±2s钙靶值±L镁靶值±25%铁靶值±20%新生儿遗传代谢病筛查-G6PDG6PD靶值±30%新生儿遗传代谢病筛查-17羟孕酮17-羟孕酮靶值±30% 新生儿遗传代谢病串联质谱筛查-氨基酸和酰基肉碱瓜氨酸靶值±25%亮氨酸靶值±25%甲硫氨酸靶值±25%苯丙氨酸靶值±25%酪氨酸靶值±25%缬氨酸靶值±25%游离肉碱靶值±30%丙酰肉碱靶值±30%异戊酰肉碱靶值±30%辛酰肉碱靶值±30%月桂酰肉碱靶值±30%棕榈酰肉碱靶值±30%十八碳酰肉碱靶值±30%血红蛋白A2和血红蛋白F血红蛋白A2 靶值±20%血红蛋白F 靶值±20%早孕期母血清产前筛查PAPP-A(μg/L) 靶值±30%PAPP-A(mU/L) 靶值±30%Free-β-HCG(μg/L) 靶值±30% Free-β-HCG(mIU/mL)靶值±30%。
室间质量评价结果分析及整改

一、临床化学:1、方法监测项目为钾、钠、氯、钙、磷、血糖、尿素、尿酸、肌酊•、总蛋白、白蛋白、胆固醇、甘油三酷、总胆红素、丙氛酸氨基转移酶、天门冬氨酸氨基转移酶、碱性磷酸酶、淀粉酶、肌酸激酶及胆固醇,共20个项目。
2结果我院使用临床化学标本批号为201602,我院开展并提供的六项数据血糖3. 56为(预期检测结果为3. 65),白蛋白为26.3 (预期检测结果为23. 2),胆固醇为2. 3 (预期检测结果为2.2),甘油三酯为0.84 (预期检测结果为0.71),丙氨酸氨基转移酶为38 (预期检测结果为36),天门冬氨酸氨基转移酶为32 (预期检测结果为31. 8)。
3不合格原因分析能力比对检验(PT)不合格数最多的项目白蛋白(Alb),原因为质控物的基质效应和测定方法的固有特征所导致的;其他项目不合格的原因是由于这些项目都是使用电极法测定,由于电极法检测原理特性而导致的。
二、临床尿液质评:1、方法监测项目为PH值、比重、蛋白、葡萄糖、隐血、酮体、胆红素、亚硝酸盐、尿胆原、白细胞、维生素C,共11个项目。
2结果我院使用临床尿液标本批号为201602,我院提供的数据为PH值5.0 (预期检测结果为5. 6)、比重1.010 (预期检测结果为1.021)、蛋白阴性(预期检测结果为+)、葡萄糖阴性(预期检测结果为++)、隐血阴性(预期检测结果为+++)、酮体+ (预期检测结果为+++)、胆红素+++ (预期检测结果为++)、亚硝酸盐阴性(预期检测结果为+)、尿胆原阴性(预期检测结果为++)、白细胞阴性(预期检测结果为阴性)、维生素C为0(预期检测结果为++)。
3不合格原因分析经推断认为,我院尿液分析仪存在设备老化,误差较大的情况。
根据济宁市临床检验中心反馈的《2016年度检验医学室间评价第一次质评结果》,我院认真查找不合格原因,依据查找出的原因,做出了以下几点改进措施:一、加强对医护人员的培训,要求检验科室的工作人员均熟练掌握相关知识,使工作人员能够提高对标本质量影响因素的防范意识。
急诊生化检验室内质控存在的问题及对策

T e s t s I n d o o r Qu a H t y Co n t r o l
LIHo n g yeXi n g ya n g Ci t y T he Pe o pl e Ho s pi t a l i n He’ n an Pr o v i nc e .
验结 果具 直接 性影 响 。
2 急诊 生化 检验 室 内质控 的对 策 2 . 1 建 立健 全质 控制 度
p r o bl e ms a n d t h us pr o p o s e a p pr o pr i a t e me a s ur e s t o p r o mo t e e fe c t i v e l y r e d u c e he t i n c i d e n c e o f p r o bl e ms ,i n o r d e r t o pl a y t o i mpr ov e e me r g e n c y
The Co unt e r me a s ur e s a nd Pr o bl e ms o f Em e r ge n c y Bi o c he mi c a l
ห้องสมุดไป่ตู้
及发 现 、 处 理 问题 的能力 均弱 于常规检 验人员 , 致使检 验质量 低下 园 。
1 . 4 标本 采集 送检 及处 理 的不规 范 常 规 生化 检验 时常 因 标本 采 集送 检 及处 理 的不 规范 ,从 而 导 致 实验 出现误 差 ;由于 上 述 问题 的 处理 不 当 ,所 产生 的误差 占实 验 总误 差 的 8 7 %;此类 误 差在 急 诊 生化 检 验 时应 更 加 明显 ,急 诊 本 就具 有 紧急 性 特 征 ,护 理人 员 在采 集 标本 时 常 出现 抽 血位 置 不
心肌标志物室内质控品使用说明

心肌标志物室内质控品使用说明
1.预期用途:心肌标志物室内质控品用于特定蛋白测定的室内质量控制。
该质控品为低
值和高值两个水平,可开展质控的项目包括:CK_MB、D二聚体、地高辛、同型半胱氨酸、高敏CRP、肌红蛋白、NT-ProNBP、肌钙蛋白I、肌钙蛋白T。
2.规格与保存要求:质控品为液体多项质控品3ml/瓶。
贮存条件为2-8℃。
开瓶稳定期为
30天(2-8℃、不可冻存)。
未开封的质控品,其稳定性可保持到保质期。
每次使用时计算好当次需要的量,打开瓶盖,取出所需量后,盖好瓶盖,将剩余质控品放回冰箱。
建议将每次的使用量吸至所用仪器的样品杯中,勿将质控品管直接上机检测。
每次使用后剩余的质控品不宜倒回原来的容器中,以防污染。
3.检测要求:质控调查品应与临床标本同步检测,请用实验室常用的诊断试剂或方法,
严格按照试剂使用说明书操作。
4.质控统计要求:在本中心的质控软件中累积≥20 次的室内质控调查品测定数据,完成
质控数据的初始化,使用Levey-Jennings质控图开展室内质量控制(具体方法参见软件应用说明)。
每月通过计算机网络向本中心上报结果,可提供回报数据项目包括:CK_MB、肌红蛋白、肌钙蛋白I、肌钙蛋白T。
5.注意事项:该调查品以人血清为基质,已经过病毒灭活。
使用中请仍视同传染性样本对
待。
BNP单位换算:pmol/L*8.5=pg/ml 。
上海临床检验质量控制中心
2014年1月2日。
卫生部临床检验中心常规化学第次室间质评不及格原
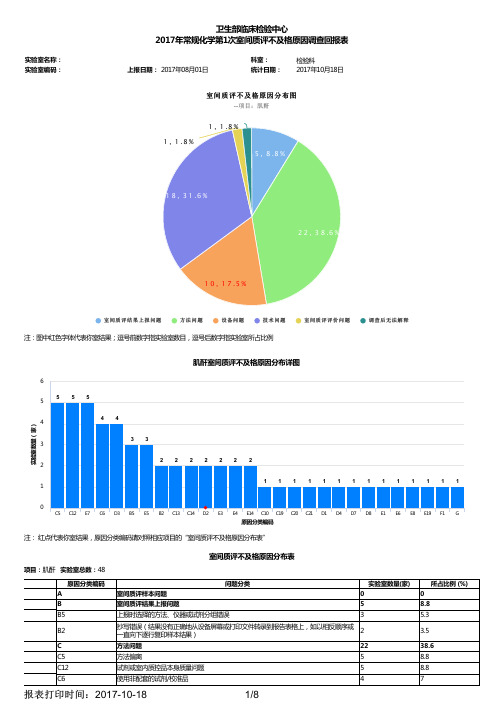
卫生部临床检验中心2017年常规化学第1次室间质评不及格原因调查回报表实验室名称:科室:检验科实验室编码:上报日期:2017年08月01日统计日期:2017年10月18日室间质评不及格原因分布表项目:肌酐 实验室总数:48原因分类编码问题分类实验室数量(家)所占比例 (%) A室间质评样本问题00B室间质评结果上报问题58.8B5上报时选择的方法、仪器或试剂分组错误3 5.3B2抄写错误(结果没有正确地从设备屏幕或打印文件转录到报告表格上,如以相反顺序或一直向下逐行复印样本结果)2 3.5 C方法问题2238.6C5方法偏离58.8C12试剂或室内质控品本身质量问题58.8C6使用非配套的试剂/校准品47C13试剂批间差异引起的不准确2 3.5 C14未使用最新换代的试剂2 3.5 C10校准品本身质量问题(如校准品赋值不正确、校准品不稳定)1 1.8 C19样本中可能包含干扰因素(这可能具有方法特异性)1 1.8 C20环境改变(如装修等)1 1.8C21室内质控方面问题(如不适当的质控方法或未做室内质控;质控品浓度与分析物浓度无关;质控规则或界限值不适当)11.8D设备问题1017.5D3设备功能故障(如仪器老化;零件故障)47D2设备加样不准2 3.5 D1设备管道或孔被堵塞1 1.8 D4纯水机或去离子水设备功能障碍1 1.8 D7未定期执行设备维护1 1.8 D8其他设备问题1 1.8 E技术问题1831.6 E7校准问题(如校准曲线过期,校准品浓度输入错误、校准品过期)58.8 E5试剂过期、超过开瓶稳定时间段、失效或污染3 5.3 E3质控品、校准品或试剂使用前处理不正确(包括复溶、配制、未混匀等)2 3.5 E4质控品、校准品或试剂储存不适当2 3.5 E14室间质评样本检测前未混匀2 3.5 E1未遵循建议对环境或设备进行监测(如温度、湿度等)1 1.8 E6不同批号试剂混加1 1.8 E8对室内质控失控未采取措施1 1.8 E19计算错误1 1.8 F室间质评评价问题1 1.8 F1由于参加实验室数量不够导致不适当的分组1 1.8 G调查后无法解释(调查后仍不能确定质评结果不合格的原因,请选择此项)1 1.8H 其他00说明:表中标注的代表你室结果纠正措施汇总表室间质评不及格原因分布表项目:白蛋白 实验室总数:107原因分类编码问题分类实验室数量(家)所占比例 (%) A室间质评样本问题74A3室间质评样本未在适当的温度下接收3 1.7A2室间质评样本未在规定的时间内接收(如一直放在收发室没有接收)2 1.1A1样本在运送时变质(污染;溶血;无活性;不均匀)10.6A4室间质评样本标签贴错10.6B室间质评结果上报问题1810.3B2抄写错误(结果没有正确地从设备屏幕或打印文件转录到报告表格上,如以相反顺序或一直向下逐行复印样本结果)6 3.4 B5上报时选择的方法、仪器或试剂分组错误5 2.9B3单位报告不正确或单位换算错误2 1.1B8上报数据不是原始数据,对数据进行了校正2 1.1B1室间质评结果未提交(如未检测、未及时提交)10.6B6上报项目错误(如将钠和钾的结果报反了)10.6B7其他结果上报问题10.6C方法问题5732.6C13试剂批间差异引起的不准确148C21室内质控方面问题(如不适当的质控方法或未做室内质控;质控品浓度与分析物浓度无关;质控规则或界限值不适当)9 5.1 C6使用非配套的试剂/校准品8 4.6C10校准品本身质量问题(如校准品赋值不正确、校准品不稳定)6 3.4C12试剂或室内质控品本身质量问题6 3.4C5方法偏离5 2.9C14未使用最新换代的试剂3 1.7C1未编写相应项目的标准操作规程(SOP)10.6C4未对员工进行培训和考核10.6C9不适当的温育条件(如时间、温度和/或空气)10.6C15结果接近方法检测限导致的不准确10.6C17基质效应引起的室间质评样本与患者样品的差异10.6C19样本中可能包含干扰因素(这可能具有方法特异性)10.6D设备问题2514.3D3设备功能故障(如仪器老化;零件故障)10 5.7D4纯水机或去离子水设备功能障碍6 3.4D7未定期执行设备维护3 1.7D2设备加样不准2 1.1D6设备软件应用编程错误或遗漏2 1.1D1设备管道或孔被堵塞10.6D8其他设备问题10.6E技术问题5531.4E7校准问题(如校准曲线过期,校准品浓度输入错误、校准品过期)2112E5试剂过期、超过开瓶稳定时间段、失效或污染10 5.7E6不同批号试剂混加74E3质控品、校准品或试剂使用前处理不正确(包括复溶、配制、未混匀等)3 1.7E2设备参数、检测模块或标本类型等设置未更改或错误2 1.1E4质控品、校准品或试剂储存不适当2 1.1E8对室内质控失控未采取措施2 1.1E15室间质评样本复溶后未在规定时间内检测2 1.1E9检测了错误的样本(如在第一次EQA活动中错误地检测了第二次EQA活动的样本)10.6E11未遵循室间质评使用说明书10.6E14室间质评样本检测前未混匀10.6E16室间质评样本处理时被污染10.6E18加样或稀释错误10.6E19计算错误10.6F室间质评评价问题10 5.7F1由于参加实验室数量不够导致不适当的分组4 2.3F3评价区间不适当3 1.7F2由于数据统计方法不当导致的不适当的靶值2 1.1F4室间质评组织者数据输入不正确10.6G调查后无法解释(调查后仍不能确定质评结果不合格的原因,请选择此项)2 1.1H其他10.6说明:表中标注的代表你室结果纠正措施汇总表室间质评不及格原因分布表项目:总铁结合力 实验室总数:15原因分类编码问题分类实验室数量(家)所占比例 (%)A 室间质评样本问题00B室间质评结果上报问题420B2抄写错误(结果没有正确地从设备屏幕或打印文件转录到报告表格上,如以相反顺序或一直向下逐行复印样本结果)210B3单位报告不正确或单位换算错误15B5上报时选择的方法、仪器或试剂分组错误15C方法问题735C12试剂或室内质控品本身质量问题210C13试剂批间差异引起的不准确210C5方法偏离15C14未使用最新换代的试剂15C21室内质控方面问题(如不适当的质控方法或未做室内质控;质控品浓度与分析物浓度无关;质控规则或界限值不适当)15D设备问题315D3设备功能故障(如仪器老化;零件故障)210D7未定期执行设备维护15 E技术问题525 E5试剂过期、超过开瓶稳定时间段、失效或污染210 E7校准问题(如校准曲线过期,校准品浓度输入错误、校准品过期)210 E4质控品、校准品或试剂储存不适当15 F室间质评评价问题00 G调查后无法解释(调查后仍不能确定质评结果不合格的原因,请选择此项)15 H其他00说明:表中标注的代表你室结果纠正措施汇总表。
加强临床实验室室内质控和室间质控评价

加强临床实验室室内质控和室间质控评价,提高检验质量柳州市人民医院检验科余洪立检查前要准备的基本资料1 工作人员基本情况表2 检验科分组室情况3 检验科检测仪器清单4 开展检验项目清单39-01实验室集中设置,统一管理1 要求在检验科之外不能再设置实验室。
各临床科室的实验室要统一到检验科。
(没做到扣3分)查有无小实验室:查医院有关文件2 实验室布局及流程要符合感控及生物安全的要求。
查看:实验室的设置布局及流程39-01建立完善临床实验室质量保证体系(1)成立检验科质控管理小组(2)检验科质量控制方案(3)有年度质控计划及质控总结(4)检验科有室内质控程序或方法。
(5)参加省级以上临检中心室间质评。
(三级医院参加卫生部)(6)有检验项目操作规程。
(7)有检验仪器操作规程。
(8)仪器设备定期校验标准检测。
(9)检验试剂使用管理符合规定。
39-02检验科的各项规章制度(部分)1 各级人员职责2 工作制度3 质量管理制度4 教育培训制度5 安全制度6 急诊检验制度7 检验仪器管理制度8 值班制度9 剧毒药品安全管理制度和意外事件预案10 消毒工作制度11 档案管理制度12 试剂采购及使用制度13 感染管理制度14 差错事故登记报告制度15网络管理制度39-02检测项目的标准操作规程标准操作程规(SOP文件)的主要内容是:1项目名称2适用仪器3方法及原理4样本要求(种类、保存、预处理、样本量)5试剂及配套品6校准7质控8操作程序9参考值范围10 临床意义11 参考文献39-02检测项目的标准操作规程检查:SOP文件的内容。
SOP文件的数量(要求所有检测项目)(不能用试剂使用说明书来代替)39-02仪器设备的标准操作规程标准操作程规(SOP文件)的主要内容:1概述:适用范围,产品持点2基本资料:生产厂家、型号、购进及使用日期。
3主要技术指标4基本工作原理5操作6校准7维护39-02仪器设备的标准操作规程检查:1 SOP文件的内容2 所用的仪器设备都要有SOP文件①包括:离心机,分光光度计等②相同仪器有多台的,要有多份SOP文件(打印多份)。
心肌肌钙蛋白校准

心肌肌钙蛋白校准
心肌肌钙蛋白是一种检测心肌损伤的标志物,用于诊断心肌梗死、心肌炎等心脏疾病。
为确保心肌肌钙蛋白的准确性,需要进行校准。
校准的方法有以下几种:
1. 内部质控。
在实验过程中加入内部质控样本,比较实验结果与已知的质控值,评估检测结果的准确性。
2. 外部质量控制。
参加外部质量控制项目,将自己的检测结果与其他实验室的结果进行比较,评估自己的检测准确性。
3. 标准曲线法。
用不同浓度的标准物质制作标准曲线,根据待测样品的信号强度在标准曲线上找到相应的浓度值。
总之,校准能够保证心肌肌钙蛋白检测结果的准确性,为准确诊断心脏疾病提供支持。
肌钙蛋白肌红蛋白肌酸激酶同工酶三合一

肌钙蛋白/肌红蛋白/肌酸激酶同工酶三合一测定(胶体金法)的标准程序【目的】体外肌钙蛋白/肌红蛋白/肌酸激酶同工酶的检测【适用仪器】干化学法【该SOP变动程序】本标准操作程序的修改可有使用本SOP文件的工作人员提出,并报请专业主管及科主任签字生效。
【检验原理】本法采用胶体金免疫层析技术,将金标抗-Myoglobin(Ab1、金标抗VK-MB和金标抗2nI(Ab1预先包被玻璃纤维上,膜上测试区固定抗-cTnI(Ab2)抗-CK-dM、抗Myoglobin (Ab2和质控区的相应抗体,测试时,标本中如含有肌红蛋白或肌酸激酶同工酶或心肌肌钙蛋白I时,分别与预先包被的金标抗体结合,结合物在毛细效应下向上层析,随后会被固定在膜上相应测试区的抗体捕获,从而在相应测试区出现紫红色条带。
如果是阴性标本,则测试区内无紫红色条带,质控区内所显示条带是判定是否有足够标本,层析过程是否正常的标准,同时也作为试剂的内控标准。
【操作步骤】1、使用前将试剂和血样标本恢复至室温。
2、从原包装试剂袋中取出试剂盒,在1小时内应尽快地使用,特别是在室温高于30C,并且在高度潮湿的环境中,打开包装后应立即使用。
3、将试剂盒放在干净的水平的台面上:血清或血浆标本:用滴管垂直滴入3滴血清或血浆标本(约120ul )于试剂盒样本孔中,开始计时。
静脉血标本:用滴管垂直滴入3滴静脉全血(约120ul )于试剂盒样本孔中,开始计时。
指尖血标本:用玻璃毛细管吸取或直接滴加3滴指尖血于试剂盒样本孔中,滴加1滴缓冲液,开始计时。
4、等待紫红色条带出现,测试结果应在10-20分钟读取,20分钟后读取的结果无效。
【检验结果的解释】阳性(+ ):四条紫红色条带出现。
三条位于测试区(T1)、(T2 )和(T3 )内,另一条位于质控区(C)。
阳性结果表明:标本中只含有三种心肌标志物。
若只有三条紫红色条带出现。
二条位于测试区(T1)、(T2)和33)任何两个区内,另一条位于质控区(C)。
室间质量评价标准

检验项目 常 规临 床化学 白蛋白 碱性磷酸 酶 淀粉酶 天门冬氨 酸氨基 转移酶 胆红素 总钙 氯 胆固醇 高密度脂 蛋白胆 固醇 肌酸激酶 肌酐 葡萄糖 铁 乳酸脱氢 酶 镁 钾 钠 总蛋白 甘油三酯 尿素 尿酸 磷 -谷 氨酰基 转肽酶
可接受范 围
靶值±10% 靶值±30% 靶值±30% 靶值±20% 靶值±6.84mmol/L(0.4mg/dL)或±20%(取大者) 靶值±0.250mmo l/ L(1.0mg/d L) 靶值±5% 靶值±10% 靶值±30% 靶值±30% 靶值±26.5mo l/ L(0.3mg/dL)或±15%(取大者) 靶值±0.33mmol/L(6mg/dL) 或±10%(取大者) 靶值±20% 靶值±20% 靶值±25% 靶值±0.5mmo l/ L 靶值±4mmo l/ L 靶值±10% 靶值±25% 靶值±0.71mmol/L 或±9%(取大者) 靶值±17% 靶值± 0.097mmol/L 或靶值±10.7%(取大者) 靶值±20%
靶值 ± 40mg/L 或 ± 10% (取大值)
同 型半 胱氨酸
靶值 ± 2.5μ mol/L 或 20% (取大值)
脑 脊液
白蛋白
靶值 ± 10% 或 ± 0.1g/L (取大值)
总蛋白
靶值 ± 10%或 ± 0.1g/L (取大值)
氯化物
靶值 ± 5%
葡萄糖
靶值 ± 10% 或 ± 1.0mmol/L (取大值)
乳酸脱氢 酶
靶值 ± 20%
IgA
靶值 ± 25%
Ig G
靶值 ± 25%
IgM
靶值 ± 25%
乳酸
靶值 ± 20% 或 ± 0.1mmol/L (取大值)
临床生化检验室内质控与室间质控存在的问题与对策

临床生化检验室内质控与室间质控存在的问题与对策目的:探讨临床生化检验室内质控与室间质控的情况并研究相关对策。
方法:在同样条件下,通过采用全自动生化分析仪对卫生部室间质控标本进行测试,并对临床生化室间质评结果进行统计。
结果:2008年的变异指数得分高于80分,其他年份的变异指数均低于80分,总MVIS分为57.50分。
结论:通过对临床生化检验室内质控与室间进行有效的控制,采取有效的措施,对其进行评价,能够确保检验质量,良好的质量控制们能够为临床提供准确的诊断、治疗和预后观察的依据。
标签:临床生化检验;室内质控;室间质控;存在的问题;对策临床生化检验质量控制主要通过对检测分析过程中出现的误差进行分析,对各个环节进行分析和控制,并在此基础上提高实验结果的准确度。
室内质控主要对常规工作的精密度和准确度进行检测和控制[1]。
室间质量评价主要建立在室内质量控制的基础上,对各个实验室结果得准确性进行观察,并采取相应的措施将各实验室结果渐趋一致。
1 资料与方法1.1 一般资料将我市临床检验中心统一发放的冻干质控血清作为研究对象。
1.2 方法主要选择仪器是日立7080全自动生化分析仪,及离子分析仪DSI-903。
主要选用的试验试剂是电解质试剂,由全自动生化分析仪对四川迈克公司提高的试剂。
采用离子选择电极法对K+、Na+、Cl-,采用日立7080全自动生化分析仪对AST、ALT、TP、ALB、Ca+进行测定。
1.3 观察指标[2]在对本组研究数据的临床评价过程中,主要使用VIS和PT 2种计分方式。
在对卫生部临检中心统一选定方面,主要使用变异指数CV和生化质评VI计算公式,主要的表达方式是MVIS,其中MVIS高于80分者为优秀,MVIS低于150分为及格,其中MVIS高于150分者为不及格,定为失控。
1.4 统计学分析在对本组数据进行统计学分析的过程中,主要运用SPSS17.0软件,计数资料以百分率(%)表示,采用X2检验,差异P<0.05,差异具有统计学意义。
医学实验室室内质控室间质评管理制度

医学实验室室内质控室间质评管理制度1 Women and Children ’s Hospital1. 目的:1.1. 室内质控的目的是检测、控制本实验室测定工作的精密度,并检测其准确度的改变,提高常规测定工作的批间、批内标本检测结果的一致性。
1.2. 室间质量控制是利用实验室间的比对来确定实验室的能力,评价各实验室测定结果的正确性,是否保持在临床所能接受的误差范围内,即借助外部力量进行回顾性检查。
2. 范围:各实验室3. 定义 :3.1. 质量控制(质控):为达到质量要求所采取的作业技术和活动。
3.1.1. 质量控制包括作业技术和活动,其目的在 文件名称 医学实验室室内质控、室间质评管理制度版本号 2016-10-A 文件编号 QFE/JCI-M-2016-076总页数 共4页 制定部门检验科 生效日期于监视过程,并排除质量环中所有阶段中导致不满意的原因,以取得经济效益。
3.1.2.质量控制和质量保证的某些活动是相互联系的(GB/T 6583 1994)。
3.2.室内质控:实验室内为达到质量要求的操作技术和活动。
3.2.1.在医学实验室,室内质控的目的在于监测过程,以评价检验结果是否可靠,以及排除质量环节中所有阶段中导致不满意的的原因。
3.2.2.广义上室内质控适用于得出检验结果所有步骤的活动,从临床需要考虑,从收集标本,检测直至报告测定结果。
3.3.室间质量评价:由第三方机构采用一系列的办法连续地、客观地评价各实验室的试验结果,并发现实验室本身不易发现的不准确性,了解各实验室之间结果的差异,帮助其校正,使其结果在具有可比性。
这种评价是一种回顾性评价,旨在建立实验室间结果的可比性。
4.内容:4.1.室内质控管理制度4.1.1.质量负责人负责管理检验过程全面质量控制程序;各组组长负责本组检验过程的质量控制程序;各岗位人员负责执行检验过程的质量控制程序和对本岗位室内质控进行分析和处理;质量监督员监督本专业组是否按照程序文件和作业指导书相关质量控制程序工作。
室内质控失控情况处理及原因分析

室内质控失控情况处理及原因分析室内质控的目的是要控制标本检测的精密度,并检测其准确度改变情况,提高检测结果一致性,要求检验人员在实际工作中不断进行培训提高,并按严格规范进行质控操作,仪器定期用配套校准物进行校准,实验室要根据自身情况选择定值质控物和非定值质控物,要求质控物要与患者标本在同样条件下进行测定,严格按照质控物说明书要求进行保存,并在保质期内使用,并认真对质控结果进行分析。
(一)失控情况处理发生失控情况应立即报告小组、科室及质控负责人;当天的该项目化验报告不可填发;并应尽速查清原因、采取纠正措施,必要时复测部分甚至全部化验标本,然后方可填发报告。
因为按统计学原理,由随机误差引起结果超出±3s范围的可能性为0。
3%。
对于几十次测定而言,实际上是不可能发生的。
一旦发生,提示可能存在非随机误差或特殊的情况。
而且这样大的误差,势必影响临床诊断和治疗工作,造成不良后果。
(二)失控原因分析失控原因的查找过程并无固定模式。
一般原则是由易到难,由近到远地查找。
1、对具体检测过程进行回顾分析失控后,应对该批检测的全过程进行迅速仔细的回顾,分析有无特殊情况,如电压波动仪、器不稳试、剂瓶标签脱落试、剂放置位置不符合要求质、控品瓶盖松动复、溶过程异常等.并应检查使用的容器、量器是否正确、仪器有无变动(如波长旋钮移动了位置)校准品或试剂有无变更生产厂家批号或接近失效期等,同时复查计算结果,对于认为上述“失控原因初步估计"中可能性较大的方面,在回顾分析过程中应特别加以注意。
2、通过选择性复查分析判断失控原因和决定处理方法。
为了验证上述的初步分析,并进一步查清失控原因,对标本作出妥善处理.—般应进行选择性复测.复查时,应包括下述样品,以便尽量一次找出原因,及时发出患者标本的化验报告a 失控时使用的质控品;b 重新打开一瓶相同批号的质控品;c 失控时使用的校准品;d 重新打开一支相同批号的校准品;e少数几个患者标本,最好包括已知病情,近期曾做过该项目检测的患者标本;f 如有条件,加测一瓶定值质控品多数情况下,通过上面的分析和复查可以查出原因,并能对患者标本提出较妥善的处理措施。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
关于肌钙蛋白、肌红蛋白检测试剂盒室间质
评不合格的原因分析
肌红蛋白检测试剂盒:目前我司的肌红蛋白检测试剂盒参加卫生部室间质评时,结果偏高,主要由于肌红蛋白eqa于2018年第二次开始,统计方法改为所有方法学统一靶值,受发光免疫及层析部分厂家测定结果非常低的影响,靶值下降很厉害,导致胶乳比浊方法学测定结果显得普遍偏高。
目前我司也在寻找一个适合的点,来迎合卫生部室间质评。
肌钙蛋白检测试剂盒:目前我司的肌钙蛋白检测试剂盒参加卫生部质评时,结果也是基本偏高,主要是该项目的靶值是通过较大数量的参加单位所报吿的值,应该说属于正态分布,用数学统法获得其平均值,当然要删除3s以外离差的值再行计算,此法须要一定数量,当然越多越好,用此平均值应该说也接近于真值,目前国内只有采取这个办法,这个办法常受参加单位数量不多的影响;也受参加单位水平的影响,如果水平差的单位越多,此平均值偏差就大。
在我司参加的卫生部室间质评里,目前相对来说肌红蛋白、肌钙蛋白、超敏-CRP这三个项目由于不同方法学的参与,导致靶值受某些方法学的影响,波动较大。
