工程热力学概念公式
工程热力学的公式大全

工程热力学公式大全1.梅耶公式:R c c v p =- R c c v p 0''ρ=-0R MR Mc Mc v p ==-2.比热比: vp vp vp Mc Mc c c c c ===''κ1-=κκRc v 1-=κnR c p 外储存能:1.宏观动能:221mc E k =2.重力位能:mgz E p =式中g —重力加速度。
系统总储存能:1.p k E E U E ++= 或mgz mc U E ++=2212.gz c u e ++=221 3.U E = 或u e =(没有宏观运动,并且高度为零)热力学能变化:1.dT c du v =,⎰=∆21dT c u v适用于理想气体一切过程或者实际气体定容过程 2.)(12T T c u v -=∆适用于理想气体一切过程或者实际气体定容过程(用定值比热计算)3.1020121221t c t c dt c dt c dt c u t vmt vmt v t v t t v ⋅-⋅=-==∆⎰⎰⎰适用于理想气体一切过程或者实际气体定容过程(用平均比热计算) 4.把()T f c v =的经验公式代入⎰=∆21dT c u v 积分。
适用于理想气体一切过程或者实际气体定容过程(用真实比热公式计算) 5.∑∑====+++=ni i i ni i n u m U U U U U 1121由理想气体组成的混合气体的热力学能等于各组成气体热力学能之与,各组成气体热力学能又可表示为单位质量热力学能与其质量的乘积。
6.⎰-=∆21pdv q u适用于任何工质,可逆过程。
7.q u =∆适用于任何工质,可逆定容过程8.⎰=∆21pdv u适用于任何工质,可逆绝热过程。
9.0=∆U适用于闭口系统任何工质绝热、对外不作功的热力过程等热力学能或理想气体定温过程。
10.W Q U -=∆适用于mkg 质量工质,开口、闭口,任何工质,可逆、不可逆过程。
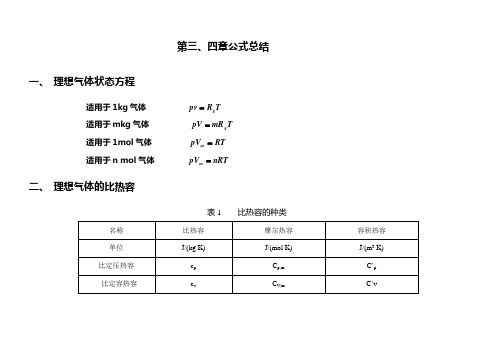
工程热力学-第三、四章公式总结
pvk=c
pvn=c
初终态p、v、T的关系式
热力学能变化Δu
0
焓变化Δh
0
熵变化Δs
0
定容过程
定压过程
定温过程
定熵过程
多变过程
过程功
0
技术功
0
过程热量
q
0
过程比热容
∞
0
第三、四章公式总结
一、理想气体状态方程
适用于1kg气体
适用于mkg气体
适用于1mol气体
适用于n mol气体
二、理想气体的比热容
表1比热容的种类
名称
比热容
摩尔热容
容积热容
单位
J/(kg K)
J/(mol K)
J/(m3K)
比定压热容
cp
Cp,m
C’p
比定容热容
cv
CV,m
C’v
迈耶方程 或
;
真实比热容
平均比热容
定值比热容
三、理想气体的热力学能、焓、熵
表2理想气体的热力学能、焓、熵
类型
热力学能
焓
熵
微元变化
有限变化
(真实比热容)
有限容)
四、理想气体的热力过程
表3理想气体的各种热力过程
定容过程
定压过程
定温过程
定熵过程
多变过程
多变指数n
±∞
0
1
k
n
过程方程式
v=c
p=c
工程热力学公式

工程热力学公式一、基本状态参数相关公式1.温度(T):-热力学温度(开尔文温度,K)与摄氏温度(℃)的关系:T(K)= t(℃)+273.15。
2.压力(p):-绝对压力、表压力和真空度的关系:-绝对压力= 大气压力+ 表压力;-绝对压力-大气压力= 真空度。
3.比体积(v):-质量为m 的物质,体积为V,则比体积v = V/m。
二、热力学第一定律相关公式1.闭口系统能量方程:- ΔU = Q - W,其中ΔU 是系统内能的变化,Q 是系统吸收的热量,W 是系统对外所做的功。
2.开口系统稳定流动能量方程:- ΔH + Δ(1/2mc²)+ gΔz = Q - Ws,其中ΔH 是焓的变化,m 是质量流量,c 是流体流速,g 是重力加速度,z 是高度,Q 是系统吸收的热量,Ws 是轴功。
三、热力学第二定律相关公式1.克劳修斯不等式:- ℃(dQ/T)≤0,对于可逆循环取等号,对于不可逆循环取小于号。
其中dQ 是微元热量,T 是热力学温度。
2.熵的定义式:- dS = dQ/T,其中dS 是熵的微元变化,dQ 是可逆过程中的微元热量,T 是热力学温度。
3.孤立系统熵增原理:- ΔSiso≥0,孤立系统的熵永不减少,对于可逆过程熵不变,对于不可逆过程熵增加。
四、理想气体状态方程及相关公式1.理想气体状态方程:- pV = nRT,其中p 是压力,V 是体积,n 是物质的量,R 是通用气体常数,T 是热力学温度。
2.比焓(h)、比内能(u)和比熵(s)的计算:-对于理想气体,比焓h = u + pv,其中u 是比内能,p 是压力,v 是比体积。
-比内能u = CvT,其中Cv 是定容比热,T 是热力学温度。
-比熵s = Cvln(T/T0) + Rln(v/v0),其中T0 和v0 是参考状态的温度和比体积,Cv 是定容比热,R 是通用气体常数。
五、卡诺循环相关公式1.卡诺循环热效率:- ηc = 1 - T2/T1,其中ηc 是卡诺循环热效率,T1 是高温热源温度,T2 是低温热源温度。
工程热力学基本概念

工程热力学基本概念及基本公式1.准静态过程(Quasi-static Process )过程中热力学系统经历的是一系列平衡状态并在每次状态变化时仅无限小地偏离平衡状态。
A quasi-static process is one in which the departure from thermodynamic equilibrium is at most infinitesimal.2.外界(Surroundings ):系统之外的一切其它物质。
边界(Boundary ):系统与外界之间的分界面。
闭口系统(Closed System ) ←→控制质量(Control Mass ):系统与外界之间没有物质交换,但有能量交换。
0;0≠=E m δδ开口系统(Open System )←→控制体积(Control Volume ):系统与外界之间不仅有物质交换,还有能量交换。
0;0≠≠E m δδ 孤立系统(Isolated System ):系统与外界之间既无质量交换又无能量交换。
0;0==E m δδ 3.热力学第一定律(First Law of Thermodynamics ):在系统两个状态之间的所有绝热过程的净功是一样的,也就是说,闭口系统在经历给定两点的绝热过程对环境所作的净功仅与系统初态和终态有关,而与绝热过程的具体路径无关。
It is found by experiment that for all adiabatic processes between two states the value of the net work done by or on the system is the same. That is, the value of the net work done by or on a closed system undergoing an adiabatic process between two given states depends solely on the end states and not on the details of the adiabatic process.dE Q W δδ=-→dE QW dt=- 4.第二定律的陈述(Statements of the Second Law )克劳修斯陈述: ① 热能不可能单独地从低温物体传向高温物体。
工程热力学基本概念及重要公式

工程热力学基本概念及重要公式1.热力学系统和热力学过程:热力学系统是指一定空间区域内被观察的物质或物体,它可以是一个封闭系统、开放系统或隔离系统。
热力学过程是指系统经历的状态变化过程,可以分为等温过程、绝热过程、等容过程和等焓过程等。
2.热力学第一定律:热力学第一定律是能量守恒定律在热力学中的表述,即能量守恒原则。
它可以表示为:ΔU=Q-W,其中ΔU表示系统内能的变化,Q表示系统吸收的热量,W表示系统对外做功。
该定律说明了系统内能的变化等于系统吸收的热量减去系统对外做的功。
3.热力学第二定律:热力学第二定律是热力学中的基本定律之一,也被称为熵增定律。
它可以表述为系统总熵永不减小,即所有自然界的过程和现象都遵循熵增的趋势。
根据熵的定义,dS≥Q/T,其中dS表示系统熵的增量,Q表示吸收的热量,T表示温度。
这个公式说明了系统的熵增量等于吸收的热量除以温度。
4.等温过程和绝热过程:在等温过程中,系统与外界保持温度不变,即温度恒定。
根据理想气体状态方程,PV=常数,即在等温过程中,气体的压强与体积呈反比关系。
在绝热过程中,系统与外界在热量交换上完全隔绝,即吸收或放出的热量为零。
根据理想气体状态方程,PV^γ=常数,其中γ为绝热指数,指的是在绝热过程中,气体压强与体积的幂指数之积的常数。
5.卡诺循环:卡诺循环是热力学中一种完美的热机循环,它由两个等温过程和两个绝热过程组成。
卡诺循环是理想的热机循环,它在可逆过程中实现了最大的功效率。
卡诺循环的功效率可表示为η=(T1-T2)/T1,其中T1表示高温热源的温度,T2表示低温热源的温度。
6.热力学第三定律:热力学第三定律是热力学中的基本定律之一,它表明在温度等于绝对零度时,所有系统的熵都将趋于零。
这个定律的提出为研究低温物理学和凝聚态物理学提供了重要的基础。
这些是工程热力学中的一些基本概念和重要公式。
工程热力学作为能源工程和热力工程等领域的基础学科,对于能量转换和热力设备的设计与运行具有重要作用。
工程热力学基本概念

工质:实现热能和机械能之间转换的媒介物质。
系统:热设备中分离出来作为热力学研究对象的物体。
状态参数:描述系统宏观特性的物理量。
热力学平衡态:在无外界影响的条件下,如果系统的状态不随时间发生变化,则系统所处的状态称为热力学平衡态。
压力:系统表面单位面积上的垂直作用力.温度:反映物体冷热程度的物理量。
温标:温度的数值表示法。
状态公理:对于一定组元的闭口系统,当其处于平衡状态时,可以用与该系统有关的准静态功形式的数量n加上一个象征传热方式的独立状态参数,即(n+1)个独立状态参数来确定.热力过程:系统从初始平衡态到终了平衡态所经历的全部状态。
准静态过程:如过程进行的足够缓慢,则封闭系统经历的每一中间状态足够接近平衡态,这样的过程称为准静态过程。
可逆过程:系统经历一个过程后如果系统和外界都能恢复到各自的初态,这样的过程称为可逆过程。
无任何不可逆因素的准静态过程是可逆过程.循环:工质从初态出发,经过一系列过程有回到初态,这种闭合的过程称为循环.可逆循环:全由可逆过程粘组成的循环。
不可逆循环:含有不可逆过程的循环.第二章热力学能:物质分子运动具有的平均动能和分子间相互作用而具有的分子势能称为物质的热力学能.体积功:工质体积改变所做的功。
热量:除功以外,通过系统边界和外界之间传递的能量。
焓:引进或排出工质输入或输出系统的总能量。
技术功:工程技术上将可以直接利用的动能差、位能差和轴功三项之和称为技术功。
功:物质间通过宏观运动发生相互作用传递的能量。
轴功:外界通过旋转轴对流动工质所做的功。
流动功:外界对流入系统工质所做的功。
热力学第二定律:克劳修斯说法:不可能使热量从低温物体传到高温物体而不引起其他变化.开尔文说法:不可能从单一热源吸热使之完全转化为有用功而不引起其他变化.卡诺循环:两热源间的可逆循环,由定温吸热、绝热膨胀、定温放热、绝热压缩四个可逆过程组成。
卡诺定理:在温度为T1的高温热源和温度为T2的低温热源之间工作的一切可逆热机,其热效率相等,与工质的性质无关;在温度为T1的高温热源和温度为T2的低温热源之间工作的热机循环,以卡诺循环的热效率为最高.熵:沿可逆过程的克劳修斯积分,与路径无关,由初、终状态决定。
工程热力学的公式大全

工程热力学的公式大全1.热力学第一定律:ΔU=Q-W其中,ΔU表示系统内能的变化,Q表示系统所吸收的热量,W表示系统所做的功。
2.理想气体状态方程:PV=nRT其中,P表示气体的压力,V表示气体的体积,n表示气体的物质的分子数,R表示气体常数,T表示气体的温度。
3.等温过程:Q=W在等温过程中,系统所吸收的热量等于所做的功。
4.绝热过程:P1V1^γ=P2V2^γ在绝热过程中,气体的压强与体积之积的γ次方是一个常数,γ为气体的绝热指数。
5.等容过程:ΔU=Qv在等容过程中,系统内能的变化等于吸收的热量。
6.等压过程:Q=ΔH在等压过程中,系统所吸收的热量等于焓的变化。
7.等焓过程:ΔH=Qp在等焓过程中,焓的变化等于吸收的热量。
8.热机效率:η=1-,Qc,/,Qh热机效率表示热机从高温热源吸收的热量减去放出的低温热量占高温热量的比例。
9.士温定理:η=1-(Tc/Th)士温定理是热力学第二定律的一种表述,表示热机效率与高温热源温度和低温热源温度的比值有关。
10.开尔文恒等式:η=1-(Tc/Th)=1-(,Qc,/,Qh,)开尔文恒等式是士温定理的另一种形式,表示任何热机的效率都不可能达到100%。
11.准静态过程:ΔS=∫(dQ/T)准静态过程中,系统的熵变等于系统吸收的微小热量除以系统的温度积分得到。
12.绝热可逆过程:ΔS=0在绝热可逆过程中,系统的熵不发生变化。
13.熵的增加原理:ΔS总=ΔS系统+ΔS环境≥0根据熵的增加原理,系统与环境的熵的变化之和大于等于0。
14.卡诺循环效率:η=1-(Tc/Th)卡诺循环是理想热机,其效率由高温热源温度和低温热源温度决定。
15.等温膨胀系数:β=(1/V)*(∂V/∂T)p等温膨胀系数表示单位温度升高时体积的变化与体积的比值。
16.等压热容量:Cp=(∂Q/∂T)p等压热容量表示在等压条件下单位温度升高吸收的热量与温度的比值。
17.等容热容量:Cv=(∂Q/∂T)v等容热容量表示在等容条件下单位温度升高吸收的热量与温度的比值。
工程热力学公式大全

工程热力学公式大全1.理想气体状态方程:理想气体状态方程描述了理想气体的状态。
其中,P为气体的压力,V为气体的体积,n为气体的物质量,R为气体的气体常数,T为气体的温度。
方程如下所示:PV=nRT2.热力学第一定律:热力学第一定律是能量守恒定律,描述了能量的转化与传递过程。
其中,Q为系统吸收的热量,W为系统对外作功,ΔE为系统内能的变化。
方程如下所示:Q=ΔE+W3.热力学第二定律-卡诺循环效率:卡诺循环是一个理想的热能转化循环,其效率最高。
其中,Th为高温热源的温度,Tc为低温热源的温度。
卡诺循环效率可以通过以下公式计算:η=1-(Tc/Th)4.热力学第二定律-卡诺热泵效率:卡诺热泵是一个理想的热能转换装置,其性能最佳。
其中,Th为高温热源的温度,Tc为低温热源的温度。
卡诺热泵效率可以通过以下公式计算:η=1-(Tc/Th)5.热力学第二定律-克劳修斯不等式:克劳修斯不等式给出了系统内能转化为功所能达到的最大效率的限制。
其中,η为系统内能转化为功的效率,T1为高温热源的温度,T2为低温热源的温度。
不等式如下所示:η≤1-(T2/T1)6.准静态过程:准静态过程是指系统在整个过程中处于平衡状态的近似过程。
在准静态过程中,系统的每个状态与下一个状态之间的温度、压力等参数都非常接近,因此可以使用热力学公式来描述其变化过程。
7.等温过程:等温过程是指系统在与外界保持恒温接触的条件下发生的过程。
在等温过程中,温度保持不变,因此可以使用以下公式计算其功和热量的变化:Q=W8.绝热过程:绝热过程是指在没有热量传递的情况下进行的过程。
在绝热过程中,可以使用以下公式计算其功和内能的变化:Q=0,ΔE=-W这些是工程热力学中的一些常见公式,它们用于描述热能转化与传递过程、能量守恒和热力学第二定律等内容。
这些公式在工程实践和学术研究中都有着广泛的应用。
工程热力学的公式大全

工程热力学的公式大全工程热力学公式大全1(梅耶公式:c,c,Rpvc',c',,Rpv0Mc,Mc,MR,Rpv02(比热比:cc'Mcppp,,, ,cc'Mcvvv,nRR ,,ccvp,,1,,1外储存能:1( 宏观动能:12 Emc,k22( 重力位能:E,mgzp式中 g—重力加速度。
系统总储存能:1( E,U,E,Ekp12或 E,U,mc,mgz212 2( e,u,c,gz23( 或(没有宏观运动,并且高度为零) e,uE,U热力学能变化:21(, du,cdT,u,cdT,vv1适用于理想气体一切过程或者实际气体定容过程2( ,u,c(T,T)v21适用于理想气体一切过程或者实际气体定容过程(用定值比热计算)ttt221tt213( ,u,cdt,cdt,cdt,c,t,c,t,,,2100vvvvmvm00t1适用于理想气体一切过程或者实际气体定容过程(用平均比热计算)24(把的经验公式代入积分。
,,c,fT,u,cdT,vv1适用于理想气体一切过程或者实际气体定容过程(用真实比热公式计算) nn5( U,U,U,?,U,U,mu,,12niii,1,1ii由理想气体组成的混合气体的热力学能等于各组成气体热力学能之和,各组成气体热力学能又可表示为单位质量热力学能与其质量的乘积。
2 6( ,u,q,pdv,1适用于任何工质,可逆过程。
7( ,u,q适用于任何工质,可逆定容过程2 8( ,u,pdv,1适用于任何工质,可逆绝热过程。
9( ,U,0适用于闭口系统任何工质绝热、对外不作功的热力过程等热力学能或理想气体定温过程。
10( ,U,Q,W适用于mkg质量工质,开口、闭口,任何工质,可逆、不可逆过程。
11. ,u,q,w适用于1kg质量工质,开口、闭口,任何工质,可逆、不可逆过程12. du,,q,pdv适用于微元,任何工质可逆过程13( ,u,,h,,pv热力学能的变化等于焓的变化与流动功的差值。
工程热力学基本概念及重要公式

称为热力系统,简称系统。
简称控制体,其界面称为控制界面。
称为工质的热力状态,简称为状态。
如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
( T)、压力(P)、比容(υ)或者密度(ρ)、内能(u)、焓(h)、熵(s)、自由能 (f)、自由焓(g) 等。
其中温度、压力、比容或者密度可以直接或者间接地用仪表测量出来,称为基本状态参数。
其物理实质是物质内部大量微观份子热运动的强弱程度的宏观反映。
则它们彼此之间也必然处于热平衡。
如工程上常用测压仪表测定系统中工质的压力即为相对压力。
与质量多少无关,没有可加性,如温度、压力等。
在热力过程中,强度性参数起着推动力作用,称为广义力或者势。
如系统的容积、内能、焓、熵等。
在热力过程中,广延性参数的变化起着类似力学中位移的作用,称为广义位移。
使过程中系统内部被破坏了的平衡有足够的时间恢复到新的平衡态,从而使过程的每一瞬间系统内部的状态都非常接近平衡状态,整个过程可看做是由一系列非常接近平衡态的状态所组成,并称之为准静态过程。
系统与外界均能彻底回复到初始状态,这样的过程称为可逆过程。
(增大或者缩小) 而通过界面向外界传递的机械功称为膨胀功,也称容积功。
经历一系列状态变化,最后又回复到初始状态的全部过程称为热力循环,简称循环。
(引力和斥力)、不占有体积的质点所构成。
1K (1℃)所吸收或者放出的热量,称为该物体的比热。
单位物量的物体,温度变化1K(1℃) 所吸收或者放出的热量,称为该物体的定容比热。
单位物量的物体,温度变化1K(1℃) 所吸收或者放出的热量,称为该物体的定压比热。
1K (1℃)时,物体和外界交换的热量,称为该物体的定压质量比热。
1K (1℃)时,物体和外界交换的热量,称为该物体的定压容积比热。
1K (1℃)时,物体和外界交换的热量,称为该物体的定压摩尔比热。
1K (1℃)时,物体和外界交换的热量,称为该物体的定容质量比热。
工程热力学公式知识点总结

工程热力学公式知识点总结热力学是研究热现象和能量转化的一门物理学科。
它不仅适用于工程领域,也适用于物理、化学、地质等领域。
热力学公式是热力学知识的重要组成部分,掌握好热力学公式可以帮助工程师更好地理解和应用热力学知识。
本文将对工程热力学公式知识点进行总结,并进行详细解释。
1. 热力学基本公式1.1 第一定律:热力学第一定律也称为能量守恒定律,它表明了能量在物质之间的转化和传递过程中的基本规律。
数学表达式为:\[dU = \delta Q - \delta W\]其中,dU表示系统内能的变化量,\(\delta Q\) 表示系统吸收的热量,\(\delta W\) 表示系统对外做功的量。
1.2 第二定律:热力学第二定律指出了自然界不可逆过程的特性,也就是热量永远不能自发地由低温物体传递到高温物体。
热力学第二定律的数学表达式有多种形式,其中最常见的是开尔文表述和克劳修斯表述。
开尔文表述表示为:\[\oint \frac{dQ}{T} \leq 0\]即,对于任何经过完整循环的过程而言,系统吸收的热量与温度的比值总是小于等于零。
而克劳修斯表述表示为:\[\text{不可能使得热量从低温物体自发地转移到高温物体,而不引入外界作用。
}\]1.3 熵增原理:熵是描述系统混乱程度或者无序性的物理量,熵增原理指出了自然界中系统总是朝着熵增长的方向发展。
数学表达式为:\[\Delta S \geq \frac{\delta Q}{T}\]其中,\(\Delta S\)代表系统的熵增量,\(\frac{\delta Q}{T}\)表示系统的对外吸收的热量与温度的比值。
2. 热力学循环公式2.1 卡诺循环公式:卡诺循环是一个理想的热力学循环,它包括两个绝热过程和两个等温过程。
卡诺循环可以用来评价热能机械的性能,其热效率被称为卡诺热效率。
卡诺热效率的数学表达式为:\[\eta_{\text{Carnot}} = 1 - \frac{T_c}{T_h}\]其中,\(\eta_{\text{Carnot}}\)表示卡诺热效率,\(T_c\)表示循环的低温端温度,\(T_h\)表示循环的高温端温度。
工程热力学的公式大全

工程热力学的公式大全1.热力学第一定律:ΔU=Q-W其中,ΔU代表内能的变化,Q代表系统吸收的热量,W代表系统对外界做功。
2.热力学第二定律:dS≥δQ/T其中,dS代表系统的熵变,δQ代表系统吸收的热量,T代表系统的绝对温度。
该定律表明在孤立系统中熵永不减少。
3.等容过程(内能不变):Q=ΔU在等容过程中,系统发生的任何热量变化都会完全转化为内能的变化。
4.等压过程(体积不变):W=PΔV在等压过程中,系统对外界所做的功等于系统内能的变化。
5.等温过程(温度不变):W = Q = nRT ln(V2/V1)在等温过程中,系统对外界所做的功等于系统从初始状态到最终状态所吸收的热量。
6.等熵过程(熵不变):Q=-W在等熵过程中,热量变化与对外界的功相等,系统的熵保持不变。
7.热机效率:η=1-(T2/T1)其中,η代表热机的效率,T2和T1分别代表工作物质的工作温度和热源的温度。
8.热泵效率:η=1-(T1/T2)其中,η代表热泵的效率,T1和T2分别代表热源的温度和工作物质的工作温度。
9.卡诺循环热机的效率上限:η=1-(T2/T1)卡诺循环是具有最高效率的热力循环,其效率仅取决于热源和冷源的温度。
10.纯物质气体的理想气体状态方程:PV=nRT其中,P代表压力,V代表体积,n代表物质的摩尔数,R为气体常数,T代表温度。
11.热力学温标:T(K)=T(°C)+273.15将摄氏温度转化为开尔文温标。
这只是一部分常用的工程热力学公式,还有其他更多的公式和关系式在工程热力学中发挥重要作用。
理解和应用这些公式可以帮助我们分析和解决实际工程问题,提高能源利用效率,促进工程技术的发展。
工程热力学 基 本 概 念

第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
工程热力学公式大全

第一章基本概念1.基本概念热力系统:用界面将所要研究的对象与周围环境分隔开来,这种人为分隔的研究对象,称为热力系统,简称系统。
边界:分隔系统与外界的分界面,称为边界。
外界:边界以外与系统相互作用的物体,称为外界或环境。
闭口系统:没有物质穿过边界的系统称为闭口系统,也称控制质量。
开口系统:有物质流穿过边界的系统称为开口系统,又称控制体积,简称控制体,其界面称为控制界面。
绝热系统:系统与外界之间没有热量传递,称为绝热系统。
孤立系统:系统与外界之间不发生任何能量传递和物质交换,称为孤立系统。
单相系:系统中工质的物理、化学性质都均匀一致的系统称为单相系。
复相系:由两个相以上组成的系统称为复相系,如固、液、气组成的三相系统。
单元系:由一种化学成分组成的系统称为单元系。
多元系:由两种以上不同化学成分组成的系统称为多元系。
均匀系:成分和相在整个系统空间呈均匀分布的为均匀系。
非均匀系:成分和相在整个系统空间呈非均匀分布,称非均匀系。
热力状态:系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
平衡状态:系统在不受外界影响的条件下,如果宏观热力性质不随时间而变化,系统内外同时建立了热的和力的平衡,这时系统的状态称为热力平衡状态,简称为平衡状态。
状态参数:描述工质状态特性的各种物理量称为工质的状态参数。
如温度(T)、压力(P)、比容(υ)或密度(ρ)、内能(u)、焓(h)、熵(s)、自由能(f)、自由焓(g)等。
基本状态参数:在工质的状态参数中,其中温度、压力、比容或密度可以直接或间接地用仪表测量出来,称为基本状态参数。
温度:是描述系统热力平衡状况时冷热程度的物理量,其物理实质是物质内部大量微观分子热运动的强弱程度的宏观反映。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
相对压力:相对于大气环境所测得的压力。
工程热力学的公式大全

工程热力学的公式大全1.理想气体状态方程:PV=nRT其中,P为气体的压强,V为气体的体积,n为气体的摩尔数,R为气体常数,T为气体的温度。
2.纯物质的热力学性质:(1)热容量:C=Q/ΔT其中,C为热容量,Q为吸热或放热的热量,ΔT为温度的变化。
(2)比热容量:c=Q/(m*ΔT)其中,c为比热容量,m为物质的质量。
(3)比熵:s=Q/T其中,s为比熵,Q为吸热或放热的热量,T为温度。
(4)比焓:h=Q/m其中,h为比焓,Q为吸热或放热的热量,m为物质的质量。
(5)等熵过程中的比热容量:Cp-Cv=R其中,Cp为等压比热容量,Cv为等容比热容量,R为气体常数。
3.热功定理:对于封闭系统,其热功等于系统内热能的减少。
W=Q-ΔU其中,W为热功,Q为吸热或放热的热量,ΔU为系统内能的变化。
4. 理想气体的Carnot热机效率:η=1-(Tc/Th)其中,η为Carnot热机的效率,Tc为冷源的温度,Th为热源的温度。
5.热流量:Q=U*A*ΔT其中,Q为热流量,U为热传导系数,A为传热面积,ΔT为温度的差异。
6.常见的传热方式:(1)对流传热:Q=h*A*ΔT其中,Q为对流传热量,h为传热系数,A为传热面积,ΔT为温度差异。
(2)辐射传热:Q=ε*σ*A*(T1^4-T2^4)其中,Q为辐射传热量,ε为发射率,σ为辐射常数,A为辐射面积,T1和T2为两个温度。
7.熵的守恒原理:对于封闭系统,熵的增加等于吸热过程中的热量除以绝对温度。
ΔS=Q/T其中,ΔS为熵的变化,Q为吸热或放热的热量,T为温度。
8.凝聚相变和汽化相变的热量计算:Q=mL其中,Q为相变的热量,m为物质的质量,L为潜热。
9.理想气体的质量分数计算:y=n/N其中,y为质量分数,n为其中一种气体的摩尔数,N为所有气体的总摩尔数。
工程热力学的公式大全

5.梅耶公式:R c c v p =- R c c v p 0''ρ=-0R MR Mc Mc v p ==-6.比热比: vp vp vp Mc Mc c c c c ===''κ1-=κκRc v 1-=κnR c p 外储存能:1. 宏观动能:221mc E k =2.重力位能:mgz E p =式中g —重力加速度。
系统总储存能:1.p k E E U E ++=或mgz mc U E ++=2212.gz c u e ++=2213.U E = 或u e =(没有宏观运动,并且高度为零)热力学能变化:1.dT c du v =,⎰=∆21dT c u v适用于理想气体一切过程或者实际气体定容过程 2.)(12T T c u v -=∆适用于理想气体一切过程或者实际气体定容过程(用定值比热计算) 3.1020121221t c t c dt c dt c dt c u t vmt vmt v t v t t v ⋅-⋅=-==∆⎰⎰⎰适用于理想气体一切过程或者实际气体定容过程(用平均比热计算) 4.把()T f c v =的经验公式代入⎰=∆21dT c u v 积分。
适用于理想气体一切过程或者实际气体定容过程(用真实比热公式计算) 5.∑∑====+++=ni i i ni i n u m U U U U U 1121Λ由理想气体组成的混合气体的热力学能等于各组成气体热力学能之和,各组成气体热力学能又可表示为单位质量热力学能与其质量的乘积。
6.⎰-=∆21pdv q u适用于任何工质,可逆过程。
7.q u =∆适用于任何工质,可逆定容过程8.⎰=∆21pdv u适用于任何工质,可逆绝热过程。
9.0=∆U适用于闭口系统任何工质绝热、对外不作功的热力过程等热力学能或理想气体定温过程。
10.W Q U -=∆适用于mkg 质量工质,开口、闭口,任何工质,可逆、不可逆过程。
工程热力学的公式大全

工程热力学的公式大全5.梅耶公式:R c c v p =-R c c v p 0''ρ=-0R MR Mc Mc v p ==-6.比热比:vp vp vp Mc Mc c c c c ===''κ1-=κκRc v 1-=κnR c p 外储存能:1.宏观动能:221mc E k =2.重力位能:mgzE p =式中g —重力加速度。
系统总储存能:1.pk E E U E ++=或mgz mc U E ++=2212.gzc u e ++=2213.U E =或u e =(没有宏观运动,并且高度为零)热力学能变化:1.dT c du v =,⎰=∆21dTc u v 适用于理想气体一切过程或者实际气体定容过程2.)(12T T c u v -=∆适用于理想气体一切过程或者实际气体定容过程(用定值比热计算)3.120121221t c t c dt c dt c dt c u t vmt vmt v t v t t v ⋅-⋅=-==∆⎰⎰⎰适用于理想气体一切过程或者实际气体定容过程(用平均比热计算)4.把()T f c v =的经验公式代入⎰=∆21dT c u v 积分。
适用于理想气体一切过程或者实际气体定容过程(用真实比热公式计算)5.∑∑====+++=ni ii ni i n u m U U U U U 1121 由理想气体组成的混合气体的热力学能等于各组成气体热力学能之和,各组成气体热力学能又可表示为单位质量热力学能与其质量的乘积。
6.⎰-=∆21pdvq u 适用于任何工质,可逆过程。
7.qu =∆适用于任何工质,可逆定容过程8.⎰=∆21pdvu 适用于任何工质,可逆绝热过程。
9.0=∆U 适用于闭口系统任何工质绝热、对外不作功的热力过程等热力学能或理想气体定温过程。
10.WQ U -=∆适用于mkg 质量工质,开口、闭口,任何工质,可逆、不可逆过程。
工程热力学概念公式

第一部分(第一章~第五章)一、概念(一)基本概念、基本术语1、工程热力学:工程热力学是从工程的观点出发,研究物质的热力性质、能量转换以及热能的直接利用等问题。
2、热力系统:通常根据所研究问题的需要,人为地划定一个或多个任意几何面所围成的空间作为热力学研究对象。
这种空间内的物质的总和称为热力系统,简称系统。
3、闭口系统:没有物质穿过边界的系统称为闭口系统。
系统内包含的物质质量为一不变的常量,所以有时又称为控制质量系统。
4、开口系统:有物质流穿过边界的系统称为开口系统。
开口系统总是一种相对固定的空间,故又称开口系统为控制体积系统,简称控制体.5、绝热系统:系统与外界之间没有热量传递的系统,称为绝热系统。
6、孤立系统:系统与外界之间不发生任何能量传递和物质交换的系统,称为孤立系统。
7、热力状态:我们把系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
8、状态参数:我们把描述工质状态特性的各种物理量称为工质的状态参数。
9、强度性状态参数:在给定的状态下,凡系统中单元体的参数值与整个系统的参数值相同,与质量多少无关,没有可加性的状态参数称为强度性参数.10、广延性状态参数:在给定的状态下,凡与系统内所含物质的数量有关的状态参数称为广延性参数.11、平衡状态:在不受外界影响(重力场除外)的条件下,如果系统的状态参数不随时间变化,则该系统所处的状态称为平衡状态。
12、热力过程:把工质从某一状态过渡到另一状态所经历的全部状态变化称为热力过程.13、准静态过程:理论研究可以设想一种过程,这种过程进行得非常缓慢,使过程中系统内部被破坏了的平衡有足够的时间恢复到新的平衡态,从而使过程的每一瞬间系统内部的状态都非常接近平衡状态,于是整个过程就可看作是由一系列非常接近平衡态的状态所组成,并称之为准静态过程。
14、可逆过程:当系统进行正、反两个过程后,系统与外界均能完全回复到初始状态,而不留下任何痕迹,这样的过程称为可逆过程.15、热力循环:把工质从某一初态开始,经历一系列状态变化,最后又回复到初始状态的全部过程称为热力循环,简称循环。
工程热力学(热力学第一定律)
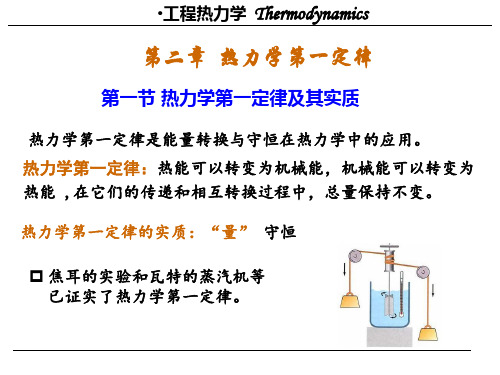
e u 1 c2 gz 2
三、闭口系的能量方程——热力学第一定律基本表达式
Q U W
q u w
可逆: 微元:
2
Q U pdV 1
或
2
q u pdv 1
Q dU W 或 q du w
可逆: Q dU pdV 或 q du pdv
•工程热力学 Thermodynamics
五、 焓
•工程热力学 Thermodynamics
定义式 H U pV
比焓 h H u pv
m
物理意义: 焓是开口系统中流入(或流出)系统工质所携带
的取决于热力学状态的总能量。
•工程热力学 Thermodynamics
第六节 能量方程的应用
一 叶轮式机械 1、动力机(汽轮机,燃气轮机)
气,带动此压气机要用多大功率的电动机?
解(1)系统为闭口系,能量方程为:
q u w
则
w q u 50 150 200 kJ kg
•工程热力学 Thermodynamics
(2)系统 可视为稳定流动系统(如图所示)则能量方程为:
q
h
1 2
c
2
g
z
wsh
由: c2 0, gz 0
得: wsh q h q [u ( pv)] (q u) ( pv)
—热力学第一定律基本表达式
一、能量方程:
Esy U
(e2 m2 e1 m1) 0
Q U W 或
Wtot W
q u w
Q Esy (e2m2 e1m1) Wtot
二、分析 :
Q U W
外热能
内热能
热能
体积变化功
机械能
工程热力学知识点总结 工程热力学公式总结

《工程热力学知识点总结工程热力学公式总结》摘要:功W0(0),△T0(0),△Q0(0)工程热力学知识点很多,同学们需要多进行归纳1、边界边界有一个特点(可变性):可以是固定的、假想的、移动的、变形的。
2、六种系统(重要!)六种系统分别是:开(闭)口系统、绝热(非绝热)系统、孤立(非孤立)系统。
a.系统与外界通过边界:功交换、热交换和物质交换.b.闭口系统不一定绝热,但开口系统可以绝热。
c.系统的取法不同只影响解决问题的难易,不影响结果。
3、三参数方程a.P=B+Pgb.P=B-H这两个方程的使用,首先要判断表盘的压力读数是正压还是负压,即你所测物体内部的绝对压力与大气压的差是正是负。
正用1,负用2。
ps.《工程热力学(第六版)》书8页的系统,边界,外界有详细定义。
1、各种热力学物理量P:压强[单位Pa]v:比容(单位m^3/kg)R:气体常数(单位J/(kg*K))书25页T:温度(单位K)m:质量(单位kg)V:体积(单位m^3)M:物质的摩尔质量(单位mol)R:8.314kJ/(kmol*K),气体普实常数2、理想气体方程:Pv=RTPV=m*R。
*T/MQv=Cv*dTQp=Cp*dTCp-Cv=R另外求比热可以用直线差值法!1、闭口系统:Q=W+△U微元:δq=δw+du (注:这个δ是过程量的微元符号)2、闭口绝热δw+du=03、闭口可逆δq=Pdv+du4、闭口等温δq=δw5、闭口可逆定容δq=du6、理想气体的热力学能公式dU=Cv*dT一切过程都适用。
为什么呢?因为U是个状态量,只与始末状态有关、与过程无关。
U是与T相关的单值函数,实际气体只有定容才可以用6、开口系统ps.公式在书46页(3-12)7、推动功Wf=P2V2-P1V1(算是一个分子流动所需要的微观的能量)a、推动功不是一个过程量,而是一个仅取决于进出口状态的状态量。
b、推动功不能够被我们所利用,其存在的唯一价值是使气体流动成为开系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一部分(第一章~第五章)一、概念(一)基本概念、基本术语1、工程热力学:工程热力学是从工程的观点出发,研究物质的热力性质、能量转换以及热能的直接利用等问题。
2、热力系统:通常根据所研究问题的需要,人为地划定一个或多个任意几何面所围成的空间作为热力学研究对象。
这种空间的物质的总和称为热力系统,简称系统。
3、闭口系统:没有物质穿过边界的系统称为闭口系统。
系统包含的物质质量为一不变的常量,所以有时又称为控制质量系统。
4、开口系统:有物质流穿过边界的系统称为开口系统。
开口系统总是一种相对固定的空间,故又称开口系统为控制体积系统,简称控制体。
5、绝热系统:系统与外界之间没有热量传递的系统,称为绝热系统。
6、孤立系统:系统与外界之间不发生任何能量传递和物质交换的系统,称为孤立系统。
7、热力状态:我们把系统中某瞬间表现的工质热力性质的总状况,称为工质的热力状态,简称为状态。
8、状态参数:我们把描述工质状态特性的各种物理量称为工质的状态参数。
9、强度性状态参数:在给定的状态下,凡系统中单元体的参数值与整个系统的参数值相同,与质量多少无关,没有可加性的状态参数称为强度性参数。
10、广延性状态参数:在给定的状态下,凡与系统所含物质的数量有关的状态参数称为广延性参数。
11、平衡状态:在不受外界影响(重力场除外)的条件下,如果系统的状态参数不随时间变化,则该系统所处的状态称为平衡状态。
12、热力过程:把工质从某一状态过渡到另一状态所经历的全部状态变化称为热力过程。
13、准静态过程:理论研究可以设想一种过程,这种过程进行得非常缓慢,使过程中系统部被破坏了的平衡有足够的时间恢复到新的平衡态,从而使过程的每一瞬间系统部的状态都非常接近平衡状态,于是整个过程就可看作是由一系列非常接近平衡态的状态所组成,并称之为准静态过程。
14、可逆过程:当系统进行正、反两个过程后,系统与外界均能完全回复到初始状态,而不留下任何痕迹,这样的过程称为可逆过程。
15、热力循环:把工质从某一初态开始,经历一系列状态变化,最后又回复到初始状态的全部过程称为热力循环,简称循环。
16、循环热效率:正循环中热转换功的经济性指标用循环热效率表示,循环热效率等于循环中转换为功的热量除以工质从热源吸收的总热量。
17、卡诺循环:由两个可逆定温过程与两个可逆绝热过程组成的,我们称之为卡诺循环。
18、卡诺定理:卡诺定理可表达为:①所有工作于同温热源与同温冷源之间的一切热机,以可逆热机的热效率为最高。
②在同温热源与同温冷源之间的一切可逆热机,其热效率均相等。
19、孤立系统熵增原理:孤立系统的熵只能增大(不可逆过程)或不变(可逆过程),决不可能减小,此为孤立系统熵增原理,简称熵增原理。
(二)与工质性质有关的概念1、温度:把这种可以确定一个系统是否与其它系统处于热平衡的物理量定义为温度。
2、压力:流体单位面积上所受作用力的法向分量称为压力(又称压强)。
3、比容:单位质量工质所占有的容积称为工质的比容。
4、理想气体:理想气体是一种经过科学抽象的假想气体模型,它被假设为:气体分子是一些弹性的、不占有体积的质点,分子相互之间没有作用力(引力和斥力)。
5、比热:单位物量的物体,温度升高或降低1K 所吸收或放出的热量,称为该物体的比热,即dTqc δ=。
6、定容比热:在定容情况下,单位物量的气体,温度变化K 1所吸收或放出的热量,称为该气体的定容比热,即dTq c vv δ=。
7、定压比热:气体加热在压力不变的情况下进行,加入的热量部分用于增加气体的能,使其温度升高,部分用于推动活塞升高而对外作膨胀功。
即:dTq c pp δ=。
(三)与能量有关的概念1、功:在热力学里,我们这样来定义功:“功是物系间相互作用而传递的能量。
当系统完成功时,其对外界的作用可用在外界举起重物的单一效果来代替。
”2、膨胀功:由于系统容积发生变化(增大或缩小)而通过界面向外界传递的机械功称为膨胀功,也称容积功。
3、轴功:系统通过机械轴与外界传递的机械功称为轴功。
4、流动功:开口系统因工质流动而传递的功。
5、技术功:技术上可资利用的功,它是稳定流动系统动能、位能的增量与轴功三项之和。
6、热量:热量学的热量定义是,在温差作用下系统与外界传递的能量称为热量。
7、系统储存能:系统储存的能量称为储存能,它有部储存能和外部储存能之分。
8、部储存能:储存于系统部的能量,它与系统工质的分子结构及微观运动形式有关,称为能(或储存能)。
9、外部储存能:与系统整体运动以及外界重力场有关的能量,称为外储存能。
10、焓:焓的定义式为h u pv =+。
对于流动工质,焓具有能量意义,它表示流动工质向流动前方传递的总能量(共四项)中取决于热力状态的那部分能量。
对于不流动工质,因pv 不是流动功,焓只是一个复合状态参数,没有明确的物理意义。
11、熵:熵是一种广延性的状态参数。
熵的定义式re Q ds Tδ=,即熵的变化等于可逆过程中系统与外界交换的热量与热力学温度的比值。
1-5章 公式(一)基本定律、基本方程 1、理想气体状态方程①RT pv = (1kg 物量表示的状态方程式) ②mRT PV = (mkg 物量表示的状态方程式)③T R pV M 0= (kmol 1物量表示的状态方程式)④T nR pV 0= (nkmol 物量表示的状态方程式)2、热力学第一定律(1)闭口系统能量方程①w u q +∆= (任何工质,任何过程)②w du q δδ+= (任何工质,任何过程)③pdv du q +=δ (可逆过程) ④⎰+∆=21pdv u q (可逆过程)(2)开口系统能量方程22222211111122net cv Q h c gz m h c gz m W dE δδδδ⎛⎫⎛⎫=++-++-+ ⎪ ⎪⎝⎭⎝⎭(3)开口系统稳态稳流能量方程①t w h q +∆= (任何工质,任何过程)②t w dh q δδ+= (任何工质,任何过程)③q dh vdp δ=- (可逆过程) ④21q h vdp =∆-⎰(可逆过程)3、热力学第二定律①0QTδ≤⎰(循环过程)②rQS T δ∆≥⎰(闭口系统)③f g S S S ∆=+ (闭口系统)④0iso S ∆≥ (孤立系统或闭口绝热系统)(二)基本公式 1、温度273.15t T =-2、循环效率①12121101q q q q q q w -=-==η ②212021q q q w q -==ε ③211012q q q w q -==ε 3、理想气体比热①dT q c δ= ②04.22'ρc Mcc == ③MMc c =④R c c v p =- (梅耶公式) ⑤vp vpvp Mc Mc c c c c ===''κ ⑥1-=κR c v ⑦1-=κκR c p ⑧02R iMc v = ⑨022R i Mc p +=4、系统总储存能 gz c u e e u e p k ++=++=2215、理想气体能变化①dT c du v = (理想气体,任何过程) ②⎰=∆21dT c u v (理想气体,任何过程)6、理想气体焓变计算①dT c dh p = (理想气体,任何过程) ②⎰=∆21dT c h p (同)7、理想气体熵变计算①1212ln lnv v R T T c s v +=∆ ②1212ln ln p pR T T c s p -=∆ ③1212ln ln p pc v v c s v p +=∆ 8.膨胀功 ①w pdv δ= ②21w pdv =⎰(仅适用于可逆过9、流动功①f w pv = ②1122v p v p w f -= (移动kg 1工质进、出控制体净流动功) 10、技术功①s t w z g c w +∆+∆=221 (任何工质,任何过程) ②s t w gdz dc w δδ++=221(任何工质,任何过程)③vdp w t -=δ (可逆过程) ④⎰-=21vdp w t (可逆过程)11、热量①q Tds δ= ②⎰=21Tds q 12、多变指数 )/ln()/ln(2112v v p p n =13、多变比热 v n c n n c 1--=κ14、活塞式压气机余隙百分比313100%V c V V =⨯- 15、多级压气机每级升压比β=16、卡诺循环热效率①12,1T T c t -=η ②212,1T T T c -=ε ③21121101,2T T T q q q w q c -=-==ε 17、作功能力损失 ①g S T L 0= ②iso iso S T L ∆=0 18、熵方程①sys f g S S S ∆=+ (闭口系统) ②f g s s s s --=12 (稳态稳流的开口系统)(三)导出公式1、多变过程的过程方程式n p v Const ⋅=2、多变过程初、终状态参数间的关系①nv v p p ⎪⎪⎭⎫ ⎝⎛=2112 (定值=npv )②12112-⎪⎪⎭⎫ ⎝⎛=n v v T T (定值=-1n Tv)③nn p p T T 11212-⎪⎪⎭⎫ ⎝⎛=(定值=-nn pT 1)3、膨胀功2111221212111()11()1111n n w pdvp v p v n R T T n p RT n p -==--=--⎡⎤⎛⎫⎢⎥=- ⎪⎢⎥-⎝⎭⎢⎥⎣⎦⎰ 4、技术功 t w n w =⋅ 5.热量2112212121211()()()()11()()1n v v v v n R q c T T T T c T T c T T n n n c T T c T T n κκ-=-+-=------=-=--第二部分 水蒸气一、概念1、汽化:物质由液相转变为气相的过程,称为汽化。
气化有蒸发和沸腾两种形式。
蒸发是指液体表面的汽化过程,通常在任何温度下都可以发生,沸腾是指液体部的汽化过程,它只能在达到沸点温度时才会发生。
2、凝结:物质由气相转变为液相的过程,称为凝结。
3、水蒸气的饱和状态:液体汽化和气体凝结的动态平衡状况称为水蒸气的饱和状态。
4、汽化潜热:将1kg 饱和液体转变成同温度的干饱和蒸汽所需要的热量。
5、干度:单位质量湿蒸汽中所含干饱和蒸汽的质量叫作湿饱和蒸汽的干度。
6、临界点:当温度超过一定值c t 时,液相不可能存在,而只可能是气相。
c t 称为临界温度,与临界温度相对应的饱和压力c p 称为临界压力。
所以,临界温度和压力是液相与气相能够共存时的最高值。
当压力高于临界压力时,液-汽两相的转变不经历两相平衡共存的饱和状态,在定压下液-汽两个相区不存在明显的、确定的界线。
临界参数是物质的固有常数。
公式1.干度vf vm x m m =+ 2、湿饱和蒸汽的参数值 ①''(1)''("')y xy x y y x y y =+-=+-②'"'y y x y y -=- 3、汽化潜热 '"'")(h h s s T r s -=-=一、概念 第三部分 湿空气1、未饱和空气:由干空气与过热水蒸气(状态点a )所组成的湿空气称为未饱和空气。
