原电池与电解池的阴阳极
谈谈原电池与电解池的判别

谈谈原电池与电解池的判别作者:叶树潭来源:《新一代》2019年第24期摘要:原电池和电解池是氧化还原反应的重要表现形式,正确判定原电池正负极。
电解池的阴极接外电源的负极,阳极接外电源的正极,电解池的阴极发生还原反应,而阳极发生氧化反应。
关键字:原电池;正负极;电解池;阴阳极;电解质溶液;氧化反应;还原反应一、在电解过程中正负极的判定判定原电池正负极的方法通常有以下几种方法。
1、观察原电池的两极的电极材料,通常情况下,两极的电极材料由两种不同金属插在电解质溶液中,这样构成的原电池时,我们选择较活泼的金属,该金属电极就为负极。
不过也有例外,如:镁-铝原电池,电解质溶液为氢氧化钠溶液时,却是相对不活泼的Al作负极,而是相对活泼的Mg作正极。
因此更准确的判断,应为发生电极反应的那一极为负极。
由于镁-铝原电池,电解质溶液为氢氧化钠溶液时,发生电极反应的是Al电极,所以Al电极应为负极。
2、如果我们能判断出原电池中的电流方向(电子流动方向),我们也可以据此判断,这是因为电子流动方向是由原电池的负极流向正极,而电流方向是由原电池的正极流向负极的,所以电流流入(电子流出)的一极是负极。
3、如果我们能判断出原电池的电解质溶液中阴阳离子移动方向,也可据此判断。
这是因为在原电池的电解质溶液中,阳离子总是移向原电池的正极的,阴离子总是流向原电池的负极的。
因此,阳离子移向哪一极的,那么这一极就为正极,阴离子移向哪一极的,那么这一极就为阴极。
4、如果我们能判断出原电池的电极上发生的反应,我们也可据此判断。
这是因为,原电池的正极是发生还原反应的,负极是发生氧化反应的。
如:Zn与石墨为原电池的两极,CuSO4溶液位电解质溶液,构成的原电池,一段时间后,石墨电极上有紫红色的固体析出,这就说明石墨电极为原电池的正极,(Cu2+→Cu,是发生还原反应的)。
二、电解池阴阳极的判定电解池的阴极接外电源的负极,阳极接外电源的正极,电解池的阴极发生还原反应,而阳极发生氧化反应。
电解池阴极阳极

阴极
阳极
负极
正极
(与电源负极 (与电源正极 (电子流出的 (电子流入的
相连)
相连)
电极)
电极)
电极反应类型 还原反应
氧化反应
氧化反应
还原反应
能量转化
电能转变为化学能
化学能转变为电能
反应进行 是否自发
不是自发进行
自发进行
电极所带电荷
负电荷
正电荷
正电荷
负电荷
哪 些 离 子 移 动 阳离子
阴离子
阴离子
阳离子
通电后阴离子、阳离子移 阴极 Na+ H+
动方向
阳极 Cl- OH-
电极电反应式 总反应式
阴极 2H+ + 2e- = H2 ↑
阳极 2Cl- - 2e-aOH+H2 ↑+Cl2 ↑
【活动4】完成教材82页思考与交流
原电池与电解池的区别
电解池
原电池
电极名称
关于电极材料与离子放电顺序
1、电极材料
惰性电极(铂、金、石墨):不参与反应 活性电极(除铂、金外的金属):作为阳极时要参与反应
2、离子放电顺序: 阴极:Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+
阳极(1)惰性电极时: S2->I->Br->Cl->OH->SO42-(等含氧酸根离子)>F(OH-放电的电极反应式为:4OH— - 4e- = 2H2O + O2 ↑)
原电池与电解池比较

原电池与电解池比较(1)原电池与电解池的区别(2)可逆原电池的充电过程:可逆原电池的充电过程就是电解。
(3)电极名称:不管是原电池还是电解池,只要发生氧化反应的电极就是阳极,只要发生还原反应的就是阴极。
①原电池:A.根据组成原电池两极的材料来判断电极。
两极材料为活泼性不同的金属时, 则活泼性相对较强的一极为负极,另一极为正极。
由一种金属和另一种非金属(除氢外)作电极时,金属为负极,非金属为正极。
B.根据原电池内两极上发生的反应类型或现象来判定电极。
原电池的负极一般为金属,并且负极总是发生氧化反应:,故负极表现为渐渐溶解,质量减小。
由此可判定,凡在原电池工作过程中发生氧化反应或质量减少的一极为负极;凡发生还原反应或有物质析出的一极为正极。
注意:原电池的电极有两套称谓:负极又可称为阳极,正极又可称为阴极(不要把负极称为阴极;正极称为阳极)。
其中正负极一套称谓是对外电路而言,在物理中常用,阴阳极一套称谓是对内电路而言。
原电池也是作为电源向用电器提供电能的,所以一般都用外电路的电极名称,称为正负极而不称为阴阳极。
②电解池:A. 电解池是在外电源作用下工作的装置。
电解池中与电源负极相连的一极为阴极,阳离子在该极接受电子被还原;与电源正极相连的一极为阳极,阴离子或电极本身(对电镀而言)在该极失去电子被氧化。
B. 电解池(或电镀池)中,根据反应现象可推断出电极名称。
凡发生氧化的一极必为阳极,凡发生还原的一极必为阴极。
例如用碳棒做两极电解溶液,析出Cu的一极必为阴极;X匸「府.放出,的一极必为阳极- -4&胡円门。
注意:电解池中,与外电源正极相连的为阳极,与负极相连的为阴极,这一点与原电池的负对阳,正对阴恰恰相反。
•电解池的电极常称阴阳极,不称正负极。
•电镀池是一种特殊的电解池,电极名称的判定同电解池。
4 •电解过程中水溶液的pH变化用铂或石墨等惰性电极电解某些物质的水溶液时,溶液的pH往往发生变化,其原因主要有两个方面。
原电池和电解池的基本原理

原电池和电解池的基本原理原电池和电解池都是电化学装置,利用化学反应将化学能转化为电能或者将电能转化为化学能。
它们的基本原理有所不同。
首先来讨论原电池。
原电池是通过化学反应产生电能的装置。
它由两种不同金属通过电解质桥或者盐桥相连而构成。
其中一种金属被称为负极或阳极,另一种金属被称为正极或阴极。
电解质桥或者盐桥的作用是保持负极和正极之间的电中性。
在原电池中,两种金属的电势差会引起在电解质桥或者盐桥上移动的离子流。
这个流动的离子携带着电荷,产生电流。
原电池的工作原理基于两种不同金属之间的电化学电位差。
每种金属都有一个固有的电势差,被称为标准电极电势。
当这两种金属在电解质溶液中相互接触时,电解质中的离子会在两种金属之间移动,以平衡电势差。
这种移动产生的电流就是原电池的输出电流。
具体来说,当两种金属以及电解液结合在一起时,会发生氧化还原反应。
在这种反应中,一种金属会氧化成离子形式,而另一种金属则从离子形式还原回到金属形态。
这个氧化还原反应释放的能量会被转化为电能。
例如,经典的原电池就是锌-铜电池。
在这种电池中,锌金属(负极)会氧化成锌离子,铜金属(正极)则从铜离子还原回到铜金属。
这个氧化还原反应产生的电子将通过外部电路流动,从而产生电流。
电解池是另一种电化学装置,它将电能转化为化学能。
电解池由两个电极(阴极和阳极)和浸泡在电解质溶液中的物质组成。
当电流通过电解质溶液时,氧化反应(在阳极处)和还原反应(在阴极处)会同时进行。
这种反应可能是非自发的,即需要外部施加的电势才能进行。
阴极是电解池中的负极,在阴极上进行还原反应。
在还原反应中,金属离子从溶液中还原回到金属形态,同时从溶液中吸收电子。
阳极是电解池中的正极,在阳极上进行氧化反应。
在氧化反应中,金属原子氧化为离子,同时释放出电子。
电解质溶液中的离子扮演着重要的角色。
这些离子通过移动来维持电荷平衡,并在电解池中形成离子流。
需要注意的是,阴极和阳极中的离子流方向是相反的。
原电池与电解池的阴阳极

原电池与电解池的阴阳极
撰写人:张立
【案例描述】
学生在学习原电池之后,知道原电池分为正负极,学习电解池之后,知道电解池中分阴阳极,但在学习本章的最后一节内容:金属的防护的时候,出现了一种电化学保护方法,即:牺牲阳极的阴极保护法,此种保护方法,不是电解池,而是原电池,学生看到此处,头脑发晕,电解池和原电池的两极极易混淆。
【诊断分析】
1.学生具有思维定势;
2.学生对阴阳极的标准判断不清楚;
【策略步骤】
将原电池和电解池的经典模型进行对比比较,而后对电极进行判断,指出各电极所发生的反应类型,进而进一步深化阴阳极的判断标准。
即:标准1:发生氧化反应的一极为阳极,发生还原反应的一极为阴极。
标准2:规定:电解池中与电源正极相连一极为阳极,与电源负极相连一极为阴极。
【效果检测】
1、铜锌原电池中,Zn为,发生反应,也叫。
2、以石墨棒为两极,电解饱和食盐水,其中有黄绿色气体逸出一极为,向饱和食盐水中滴加酚酞,变红色的一极为。
答案:1、负极,氧化,阳极 2、阳极阴极
【感悟思考】
从某种意义上讲,电解池与原电池在电极判断上,因为所发生反应的类型相似性,可以规定两种池子的阴阳极,摆脱混淆问题的根本在于,阴阳极的定义。
通过习题强化,定义强化,可以使学生在短时间内,解决混淆问题。
如何区分原电池和电解池

原电池和电解池如何区分:
原电池是一种化学能转化为电能的装置,它作为电源,通常我们称其为负极和正极。
电解池中,连着负极的一极是电解池的阴极,连着正极的一极是电解池的阳极
1、电子的流向、发生的反应
原电池:负极失电子发生氧化反应
正极得电子发生还原反应
电解池:失去电子的极即氧化极,也就是阳极;
得到电子的极即还原极,也就是阴极。
2混合连接时
、原电池、电解池、电镀池的判断规律
(1)若无外接电源,又具备组成原电池的三个条件。
①有活泼性不同的两个电极;②两极用导线互相连接成直接插入连通的电解质溶液里;③较活泼金属与电解质溶液能发生氧化还原反应(有时是与水电离产生的H+作用),只要同时具备这三个条件即为原电池。
(2)若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池;当阴极为金属,阳极亦为金属且与电解质溶液中的金属离子属同种元素时,则为电镀池。
(3)若多个单池相互串联,又有外接电源时,则与电源相连接的装
置为电解池成电镀池。
若无外接电源时,先选较活泼金属电极为原电池的负极(电子输出极),有关装置为原电池,其余为电镀池或电解池。
原电池和电解池全面总结(热点)8篇

原电池和电解池全面总结(热点)8篇第1篇示例:原电池和电解池是当今社会中非常重要的能源存储和转换设备,广泛应用于电动车、手机、笔记本电脑等各种现代电子设备中。
在这篇文章中,我们将对原电池和电解池进行全面总结,包括其原理、结构、性能特点以及当前的热点问题。
一、原电池的原理和结构原电池是通过化学反应将化学能转化为电能的装置。
它由阳极、阴极和电解质组成。
当外部电路连接时,化学反应在阳极和阴极之间发生,产生电流。
常见的原电池有干电池和蓄电池两种类型。
干电池是一次性使用的电池,蓄电池则可以反复充放电使用。
二、原电池和电解池的性能特点1. 能量密度高:原电池和电解池在相同体积和重量下可以存储更多的能量,适合应用于现代电子设备中。
2. 长寿命:部分原电池和电解池可以进行多次充放电循环,使用寿命较长。
3. 环保:与传统的化石能源相比,原电池和电解池使用过程中不会产生二氧化碳等有害气体,对环境友好。
4. 快速充放电:随着技术的进步,原电池和电解池的充放电速度越来越快,用户体验更佳。
1. 安全问题:在过去的几年里,因为原电池和电解池自身的特性,如短路、过充、过放等问题导致的安全事故时有发生,如三星Note7手机爆炸事件、特斯拉电动车发生火灾等。
原电池和电解池的安全性一直备受关注。
2. 资源利用与环保:现有的原电池和电解池在制造和回收过程中对资源的消耗比较大,回收利用率较低,对环境造成了一定的压力。
如何提高原电池和电解池的资源利用率,保护环境成为了热点问题。
3. 高性能需求:随着电子设备的不断更新,用户对于原电池和电解池的性能要求也在不断提高,如快速充电、长使用时间、安全稳定等,如何满足用户需求也是当前的热点问题。
以上就是对原电池和电解池的全面总结,这些设备在当今社会中发挥着越来越重要的作用,我们期待未来能够有更多的创新,解决当前存在的问题,使得原电池和电解池能更好地适应现代社会的需求。
第2篇示例:原电池和电解池是当前热点话题之一,随着新能源技术的发展,原电池和电解池成为各行各业关注的焦点。
电化学知识点总结

1电化学知识点总结一【知识梳理】原电池正负极和电解池阴阳极的判断方法无论是原电池还是电解池,其本质都是在两个电极表面发生氧化还原反应。
在确定电极时用好对立统一规律,能起到事半功倍的效果。
如在原电池中,一个电极为正极,则另一电极为负极;在电解池中,一个电极为阳极,则另一电极为阴极。
(1)原电池正、负极的确定负极—⎪⎪⎪⎪⎪ —较活泼的金属 注意:特殊的电解质溶液可能会影响电极—电极的质量减小 适用于金属电极 —电子流出的电极—阴离子移向的电极—发生氧化反应的电极自己整理正极判断的一般方法。
(2)电解池阴、阳极的确定阴极—⎪⎪⎪⎪⎪—与电源负极相连的电极—电子流入的电极—阳离子移向的电极—质量增加的电极 适用于金属阳离子放电的电解过程—发生还原反应的电极自己整理阳极判断的一般方法。
【知识要点】化学电池的分类1一次电池 ①定义:一次电池,又称“原电池”,即电池放电后不能用充电方法使它复原的一类电池。
②举例:锌锰干电池、锌汞电池、碱锰电池、镉汞电池、锂亚硫酰氯电池。
2 二次电池 ①定义:二次电池又称“蓄电池”。
即电池放电后,可用充电方法使活性物质复原以后能 再放电,且充放电能反复多次循环使用的一类电池。
这类电池实际上是一个电化学能量储存装置,用直流电把电池充足,这时电能以化学能的形式贮存在电池中,放电时,化学能再转换成电能。
②举例:铅酸电池、Zn-Ni 电池、Cd-Ni 电池、Zn-Ag 电池、Fe-Ni 电池、MH/Ni 电池。
3 贮备电池 ①定义:贮备电池又称“激活电池”。
即正、负极活性物质和电解质在贮存期不直接接触, 使用前临时注入电解液或用其它方法使电池激活的一类电池。
②举例:镁银电池、钙热电池。
4 燃料电池 ①定义:燃料电池又称“连续电池”。
即只要活性物质连续地注入电池,就能长期不断地 进行放电的一类电池。
它的特点是电池自身只是个载体,可以把燃料电池看成一种需要电能时将反应物从外部送入电池的一次电池。
常见原电池、电解池的电极反应及电池反应的小结

常见原电池、电解池的电极反应及电池反应的小结一、一次电池1、伏打电池:(负极—Zn,正极—Cu,电解液—H2SO4)负极:正极:总反应离子方程式Zn + 2H+ == H2↑+ Zn2+2、铁碳电池(析氢腐蚀):(负极—Fe,正极—C,电解液——酸性)负极:正极:总反应离子方程式Fe+2H+==H2↑+Fe2+3、铁碳电池(吸氧腐蚀):(负极—Fe,正极—C,电解液——中性或碱性)负极:正极:总反应化学方程式:2Fe+O2+2H2O==2Fe(OH)2;(铁锈的生成过程) 4.铝镍电池:(负极—Al,正极—Ni,电解液——NaCl溶液)负极:正极:总反应化学方程式:4Al+3O2+6H2O==4Al(OH)3 (海洋灯标电池)5、普通锌锰干电池:(负极——Zn,正极——碳棒,电解液——NH4Cl糊状物)负极:正极:总反应化学方程式:Zn+2NH4Cl+2MnO2=ZnCl2+Mn2O3+2NH3+H2O6、碱性锌锰干电池:(负极——Zn,正极——碳棒,电解液KOH糊状物)负极:正极:总反应化学方程式:Zn +2MnO2 +2H2O == Zn(OH)2 + MnO(OH)7、银锌电池:(负极——Zn,正极--Ag2O,电解液NaOH )负极:正极:总反应化学方程式:Zn + Ag2O == ZnO + 2Ag8、镁铝电池:(负极--Al,正极--Mg,电解液KOH)负极(Al):正极(Mg):总反应化学方程式:2Al + 2OH-+ 6H2O =2【Al(OH)4】-+ 3H2↑9、高铁电池(负极--Zn,正极--碳,电解液KOH和K2FeO4)正极:负极:总反应化学方程式:3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH放电充电10、镁/H2O2酸性燃料电池正极:负极:总反应化学方程式:Mg+ H2SO4+H2O2=MgSO4+2H2O二、充电电池1、铅蓄电池:(负极—Pb 正极—PbO2 电解液—稀硫酸)负极:正极:总化学方程式Pb+PbO2 + 2H2SO4==2PbSO4+2H2O2、镍镉电池(负极--Cd、正极—NiOOH、电解液: KOH溶液)放电时负极:正极:总化学方程式Cd + 2NiOOH + 2H2O===Cd(OH)2 + 2Ni(OH)2三、燃料电池1、氢氧燃料电池:总反应方程式: 2H2 + O2 === 2H2O(1)电解质是KOH溶液(碱性电解质)负极:正极:(2)电解质是H2SO4溶液(酸性电解质)负极:正极:(3)电解质是NaCl溶液(中性电解质)负极:正极:2、甲醇燃料电池(注:乙醇燃料电池与甲醇相似)(1)碱性电解质(铂为两极、电解液KOH溶液)正极:负极:总反应化学方程式:2CH3OH + 3O2 + 4KOH=== 2K2CO3 + 6H2O(2)酸性电解质(铂为两极、电解液H2SO4溶液)正极:负极:总反应式2CH3OH + 3O2 === 2CO2 + 4H2O3、CO燃料电池(铂为两极、电解液H2SO4溶液)总反应方程式为:2CO +O2 =2CO2正极:负极:4、甲烷燃料电池(1)碱性电解质(铂为两极、电解液KOH溶液)正极:负极:总反应方程式:CH4 + 2KOH+ 2O2 === K2CO3 + 3H2O(2)酸性电解质(铂为两极、电解液H2SO4溶液)总反应方程式:CH4 + 2O2 === CO2 + 2H2O 正极:负极:5、肼(N2H4)燃料电池(电解质溶液是20%~30%的KOH溶液)总反应方程式:N2H4+ O2 === N2 +2H2O正极:负极:6、H2、Cl2电池(铂为两极,一极为H2,另一极为Cl2,电解质溶液是20%~30%的KOH溶液)正极:负极:总反应方程式:7、A g、Cl2电池(负极—Ag 、正极—铂,通入Cl2,电解液: 1 mol·L-1盐酸)正极:负极:总反应方程式:2Ag+ Cl2==2 Ag Cl8、H2、N2电池(铂为两极,一极为H2,另一极为N2,电解质溶液是盐酸、氯化铵溶液)正极:负极:总反应方程式:3H2 + N2 +2HCl==2 NH4Cl四、非水电池1、氢氧电池:一极为H2,另一极为空气与CO2的混合气,电解质为熔融K2CO3(盐)负极:正极:总反应方程式2H2 + O2 === 2H2O2、固体酸燃料电池(一极通入空气,另一极通入H2;电解质是CsHSO4固体传递H+)负极:正极:总反应方程式2H2 + O2 === 2H2O3、新型燃料电池(一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体)正极:负极:总反应方程式:2C4H10+13O2=8CO2+10H2O4、CO电池(一极为CO,另一极为空气与CO2的混合气,Li2CO3和Na2CO3的熔融盐作电解质)正极:负极:总反应方程式O2 +2CO==4CO25、Li-Al/FeS电池(一级是Li-Al合金,一极是粘有FeS的石墨,电解质是Li2CO3熔融盐)正极:负极:总反应方程式:2Li+FeS=Li2S+Fe五、电解池1、写出下列电解池的电极反应式和总反应式(1)用惰性电极电解硫酸钠溶液:若要恢复到原溶液浓度,加入一定量____________ 阳极: 。
原电池与电解池对比,金属的电化学腐蚀与防护
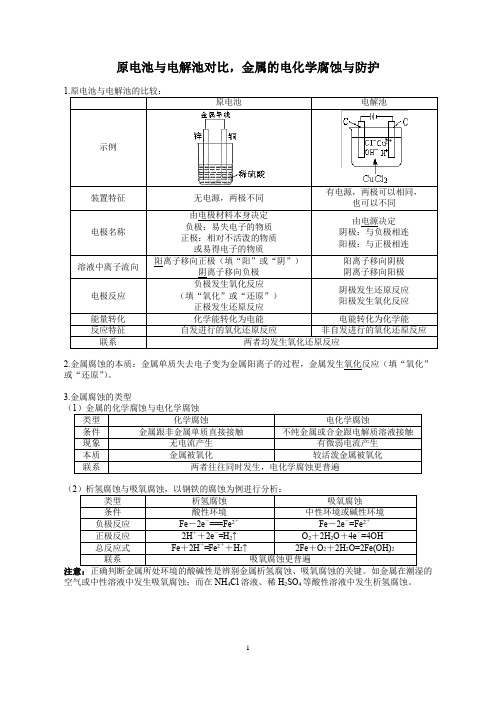
原电池与电解池对比,金属的电化学腐蚀与防护原电池电解池有电源,两极可以相同,2.金属腐蚀的本质:金属单质失去电子变为金属阳离子的过程,金属发生氧化反应(填“氧化”或“还原”)。
3.金属腐蚀的类型(2空气或中性溶液中发生吸氧腐蚀;而在NH 4Cl 溶液、稀H 2SO 4等酸性溶液中发生析氢腐蚀。
4.金属的防护(1)电化学防护利用如图装置,可以模拟铁的电化学防护。
为减缓铁的腐蚀a.若开关K置于M处,则X应为比铁活泼的金属Zn等,该电化学防护法称为牺牲负极的正极保护法。
或牺牲阳极的阴极保护法。
b.若开关K置于N处,则铁作阴极,铁很难被腐蚀,该电化学防护法为外加电流的阴极保护法。
总结:如果想利用原电池原理保护某金属,就应该让该金属作______极,找一个比它更活泼的金属材料作_________极。
如果想利用电池池原理保护某金属,就应该让该金属作______极。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
5.判断金属腐蚀快慢的规律(1)如果金属腐蚀加快,则腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀。
活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
(2)如果金属有防护措施,则防护效果:电解原理引起的防护>原电池原理引起的防护>有物理防护措施。
例1.(2014上海)如下图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是(B )A.K1闭合,铁棒上发生的反应为2H++2e→H2↑B.K1闭合,石墨棒周围溶液pH逐渐升高C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法D.K2闭合,电路中通过0.002N A个电子时,两极共产生0.001mol气体例2.如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序为(C)A.②①③④⑤⑥B.⑤④③①②⑥C.⑤④②①③⑥D.⑤③②④①⑥变式训练:1.关于金属的腐蚀与防护,下列叙述正确的是(B)A.金属腐蚀就是金属失去电子被还原的过程B.将需防腐的金属与外加直流电源的负极相连,正极与废铁相连C.镀锌铁皮发生腐蚀时,正极的电极反应式为:Fe-2e→ Fe2+D.铁钉在潮湿空气中生锈,是因为直接发生反应:4Fe+3O2→2Fe2O32.为保护地下钢管不受腐蚀,可使它与(C)①直流电源负极相连,②铜板相连,③锌板相连,④直流电源正极相连。
高中化学之原电池知识点

高中化学之原电池知识点电化学知识是以电解质溶液为载体,以氧化还原反应为核心,原电池的负极和电解池的阳极是氧化极,原电池的正极和电解池的阴极是还原极。
第一类原电池,如铜锌原电池,其组成条件有三条:(1)两个活泼性不同的电极(金属与金属、金属与石墨碳棒、金属与难溶金属氧化物);(2)电解质溶液,至少要能与一个电极发生有电子转移的氧化还原反应,一般是置换反应;(3)两电极插入电解质溶液中且用导线连接。
这种原电池中,较活泼的金属作负极,负极发生氧化反应,负极材料失去电子被氧化,形成阳离子进入溶液;较不活泼的金属作正极,正极上发生还原反应,溶液中原有的阳离子在正极上得到电子被还原,析出金属或氢气,正极材料不参与反应。
电子总是从负极沿着导线流入正极。
因此,原电池现象是“负极下,正极上,电子就在中间转”。
其特点是金属电极与电解质溶液之间存在自发的氧化还原反应。
例1.某原电池的总反应是Zn+Cu2+=Zn2++Cu,该原电池的正确组成是()A. B. C. D.正极Zn Cu Zn Cu负极Cu Zn Cu Zn电解质溶液CuCl2CuCl2ZnCl2ZnCl2解析:从总反应可知,Zn失去电子,且Zn比Cu活泼,Zn应为负极。
这是正规原电池,负极要能与电解质溶液发生置换反应,只能用CuCl2,故应选B。
第二类原电池的构成条件是:(1)两个活动性不同的电极;(2)任何电解质溶液(酸、碱、盐皆可);(3)形成回路。
这类原电池的特点是电极与电解质溶液不发生置换反应,电解质溶液只起导电作用。
其正极反应一般是吸氧腐蚀的电极反应式:O2+2H2O+4e=4OH-。
电化学腐蚀依然是原电池原理,分为析氢腐蚀(发生在酸性较强的溶液里,正极上H+还原)和吸氧腐蚀(发生在中性、碱性或极弱酸性溶液里,正极上是氧气被还原:O2+2H2O+4e=4OH-)。
例2.把铁钉和碳棒用铜线联接后,浸入0.01 mol/L的食盐溶液中,可能发生的现象是()A. 碳棒上放出氯气B. 碳棒近旁产生OH-C. 碳棒上放出氧气D. 铁钉上放出氢气E. 铁钉被氧化解析:由于Fe不与食盐溶液反应,属第二类原电池,溶液为中性,故发生吸氧腐蚀的反应。
原电池和电解池知识点总结

原电池和电解池1.原电池和电解池的比较: 2原电池正负极的判断:⑴根据电极材料判断:活泼性较强的金属为负极,活泼性较弱的或者非金属为正极。
⑵根据电子或者电流的流动方向:电子流向:负极→正极。
电流方向:正极→负极。
⑶根据电极变化判断:氧化反应→负极;还原反应→正极。
⑷根据现象判断:电极溶解→负极;电极重量增加或者有气泡生成→正极。
⑸根据电解液内离子移动的方向判断:阴离子→移向负极;氧离子→移向正极。
3电极反应式的书写:负极:⑴负极材料本身被氧化:n+2+①如果负极金属生成的阳离子与电解液成分不反应,则为最简单的:M-n e-=M 如:Zn-2 e-=Zn ②如果阳离子与电解液成分反应,则参与反应的部分要写入电极反应式中:如铅蓄电池,Pb+SO42--2e-=PbSO4⑵负极材料本身不反应:要将失电子的部分和电解液都写入电极反应式,如燃料电池CH4-O2(C作电极)电解液为KOH:负极:CH4+10OH-8 e-=C032-+7H2O 正极:⑴当负极材料能自发的与电解液反应时,正极则是电解质溶液中的微粒的反应,+H2SO4电解质,如2H+2e=H2 CuSO4电解质: Cu2++2e= Cu⑵当负极材料不与电解质溶液自发反应时,正极则是电解质中的O2反正还原反应-① 当电解液为中性或者碱性时,H2O比参加反应,且产物必为OH,如氢氧燃料电池(KOH电解质)O2+2H2O+4e=4OH+②当电解液为酸性时,H比参加反应,产物为H2OO2+4O2+4e=2H2O4.化学腐蚀和电化腐蚀的区别-6.金属的防护⑴改变金属的内部组织结构。
合金钢中含有合金元素,使组织结构发生变化,耐腐蚀。
如:不锈钢。
⑵在金属表面覆盖保护层。
常见方式有:涂油脂、油漆或覆盖搪瓷、塑料等;使表面生成致密氧化膜;在表面镀一层有自我保护作用的另一种金属。
⑶电化学保护法①外加电源的`阴极保护法:接上外加直流电源构成电解池,被保护的金属作阴极。
原电池和电解池的电极反应式写法

原电池和电解池的电极反应式写法1.原电池这种电池往往是以我们学过的一些基础的氧化还原反应为基础。
一般情况下,负极往往是活泼金属,如Mg、Al、Fe等,则负极反应一般由负极金属失去电子变成金属阳离子。
如Mg-2e-=Mg2+,Cu-2e-=Cu2+,Fe-2e-=Fe2+,注意不能写成Fe-3e-=Fe3+。
Al失电子后变为Al3+,但碱性介质中,Al3+将继续和OH-反应,电极反应式中要注意写上该反应。
如Mg-Al-NaOH溶液构成的电池,负极反应式应写成Al-3e-+4OH-=AlO2—+2H2O。
大概的分工就是,原电池本质是一个自发的氧化还原反应,在组成构形图时,每个部分都有分工,负责反应的一般是负极材料和溶液中的离子,导线负责传递负极流出来的电子,引导电子流向正极表面,然后正极表面的电子吸引溶液中离子(一般是溶液中的阳离子),使其在正极表面得到电子,形成一个完整的闭合回路。
正极反应有以下几种情况:(1)电解质溶液是不活泼金属的盐溶液,此时正极反应一般为溶液中的不活泼金属阳离子(如Ag+、Cu2+、Hg2+)得到电子生成相应的金属单质。
(2)电解质溶液中含强氧化性金属阳离子如Fe3+,此时正极反应一般是Fe3++e-=Fe2+,不能写为Fe3++3e-=Fe。
(3)电解质是非氧化性酸如稀盐酸、稀硫酸,此时正极反应为2H++2e-=H2↑。
(4)电解质是活泼金属的盐溶液,如NaCl、K2SO4、NaNO3等,此时应由溶液中的O2得电子,而不是水中的H+得电子。
在原电池中,水中的H+很少得电子。
(5)电解质是氧化性酸如浓、稀硝酸。
此时,若是稀硝酸,正极反应为NO3—+3e-+4H+=NO ↑+2H2O;若是浓硝酸,正极反应为NO3—+e-+2H+=NO2↑+H2O。
(书写时,得电子数目=化合价降低的值×原子个数;抓住O守恒,多余的O结合H+变成水)2. 燃料电池燃料电池本质依然是个原电池,负极是燃料,正极一般是氧气或者空气。
电解池阴阳极的放电顺序

电解池阴阳极的放电顺序
电解池阴阳极的放电顺序为:电解池阴极为阳离子放电,得电子能力强先放电;电解池阳极为阴离子放电或电极放电,失电子能力强先放电。
若阳极是活泼金属(金属活动顺序表Ag以前),溶液中的阴离子一律不放电,而是电极材料失电子。
若为惰性电极,则两极按照下列顺序放电:
-电解水型;
-电解电解质型:电解质电离出的阴、阳离子分别在两极放电;
-放氢气生碱型:阴极:水放氢气生碱;阳极:电解质阴离子放电;
-放氧气生酸型:阴极:电解质阳离子放电;阳极:水放氧气生酸。
若想了解更详细的内容,可参考相关专业书籍或网站。
(完整版)原电池和电解池知识点归纳

原电池和电解池知识点一.原电池和电解池的比较:二.原电池正负极的判断:⑴根据电极材料判断:活泼性较强的金属为负极,活泼性较弱的或者非金属为正极。
⑵根据电子或者电流的流动方向:电子流向:负极→正极。
电流方向:正极→负极。
⑶根据电极变化判断:氧化反应→负极;还原反应→正极。
⑷根据现象判断:电极溶解→负极;电极重量增加或者有气泡生成→正极。
⑸根据电解液内离子移动的方向判断:阴离子→移向负极;氧离子→移向正极。
三.电极反应式的书写:*注意点:1.弱电解质、气体、难溶物不拆分,其余以离子符号表示;2.注意电解质溶液对正负极的影响;3.遵守电荷守恒、原子守恒,通过添加H+ 、OH- 、H2O 来配平1.负极:⑴负极材料本身被氧化:①如果负极金属生成的阳离子与电解液成分不反应,则为最简单的:M-n e-=M n+如:Zn-2 e-=Zn2+②如果阳离子与电解液成分反应,则参与反应的部分要写入电极反应式中:如铅蓄电池,Pb+SO42--2e-=PbSO4⑵负极材料本身不反应:要将失电子的部分和电解液都写入电极反应式,如燃料电池CH4-O2(C作电极)电解液为KOH:负极:CH4+10OH-8 e-=C032-+7H2O2.正极:⑴当负极材料能自发的与电解液反应时,正极则是电解质溶液中的微粒的反应,H2SO4电解质,如2H++2e=H2 CuSO4电解质: Cu2++2e= Cu⑵当负极材料不与电解质溶液自发反应时,正极则是电解质中的O2反正还原反应①当电解液为中性或者碱性时,H2O参加反应,且产物必为OH-,如氢氧燃料电池(KOH电解质)O2+2H2O+4e=4OH-②当电解液为酸性时,H+参加反应,产物为H2O如氢氧燃料电池(KOH电解质) O2+4O2+4e=2H2O四.常见的原电池1.银锌电池:(负极—Zn、正极--Ag2O、电解液NaOH )负极:Zn+2OH––2e-== Zn(OH)2 (氧化反应)正极:Ag2O + H2O + 2e-== 2Ag + 2 OH-(还原反应)化学方程式Zn + Ag2O + H2O== Zn(OH)2 + 2Ag2.铝–空气–海水(负极--铝、正极--石墨、铂网等能导电的惰性材料、电解液--海水)负极:4Al-12e-==4Al3+ (氧化反应)正极:3O2+6H2O+12e-==12OH-(还原反应)总反应式为:4Al+3O2+6H2O===4Al(OH)3(铂网增大与氧气的接触面)——海洋灯标电池装置原电池电解池实例原理使氧化还原反应中电子作定向移动,从而形成电流。
电解池原电池正负极阴阳极

电解池原电池正负极阴阳极电解池和原电池,这听起来有点高大上的感觉,但其实它们和我们的日常生活息息相关,简直就像老朋友一样,随时在你身边。
想想看,我们的手机、电脑、甚至那些闪闪发光的遥控器,都离不开电池的支持。
这时候,你可能会问,电解池和原电池到底是什么呢?别急,我这就给你讲讲。
先来聊聊原电池,原电池就像是个能量的宝藏,能把化学能转化为电能,听起来是不是很神奇?就像你早上吃的那一碗热腾腾的粥,给你充电一样。
原电池通常由两个不同的金属构成,比如锌和铜,这两位“老兄弟”在电解液的陪伴下,互相较劲,产生电流。
你可以想象它们就像一对搭档,默契得很,锌是负极,铜是正极,它们一起出发,为我们的生活提供源源不断的电力。
电解池也很有意思。
电解池其实就是利用电能来促使化学反应。
这里面可有趣了,电流通过电解液的时候,就像是给化学反应加了一把火,推动它向前发展。
就好比你平时在炒菜,火候掌握得当,菜肴香气四溢;可要是火候过了,那可就惨了。
电解池的正负极分别叫阳极和阴极,阳极就是那个“出风头”的家伙,发生氧化反应;而阴极则是“低调”的一方,进行还原反应。
它们就像是一场化学盛宴,各显神通,热闹非凡。
现在,我们再深入一点,看看它们在生活中的应用。
原电池在我们的日常生活中真的是无处不在,比如你家里的遥控器,电动玩具,还有那种一次性电池。
你可能没注意,其实它们的工作原理就是利用原电池的能量转化原理。
生活中的这些小玩意儿,有时候真是让人觉得惊奇,没电的时候就像人没了精神,充上电后又活过来了,仿佛瞬间焕发了新生。
而电解池的应用就更广泛了。
比如,铝的生产过程就是通过电解池来实现的,铝这种金属无处不在,从铝箔到飞机制造,它的身影几乎无处不在。
电解池在电镀行业中也是大显身手,让各种金属表面变得光亮如新。
这就好比给金属穿上了华丽的外衣,既美观又耐用。
提到电解池和原电池,我们不能不提到一些小知识,比如它们的效率。
电池的容量和使用时间就像人一天的精力一样,得合理安排。
原电池正负极和电解池阴阳极的关系

原电池正负极和电解池阴阳极的关系下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!原电池正负极和电解池阴阳极的关系在研究电化学反应和电池工作原理时,理解原电池正负极与电解池阴阳极的关系至关重要。
原电池电解池离子放电顺序

原电池电解池离子放电顺序
电解池放电顺序为:电解池阴极为阳离子放电,得电子能力强先放电;电解池阳极为
阴离子放电或电极放电,失电子能力强先放电。
阳极是活泼金属(金属活动顺序表ag以前),溶液中的阴离子一律不放电,而是电极材料失电子。
电解池
电解池的主要应用领域用作工业制纯度低的金属,就是将电能转变为化学能的一个装置。
电解池由另加电源、电解质溶液和阴阳电极形成。
并使电流通过电解质溶液或熔融电
解质而在阴,阳两极引发还原成水解反应的过程。
电解池相关概念
1、并使电流通过电解质溶液或熔融的电解质而在阴、阳两极上引发还原成水解反应
的过程叫作电解。
2、把电能转变为化学能的装置叫做电解池或电解槽。
3、当离子抵达电极时,丧失或赢得电子,出现水解还原成反应的过程叫做电解原理。
阴极:与电源负极相连的电极,得电子发生还原反应。
阳极:与电源负极相连的电极,失电子出现水解反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
.
'. 原电池与电解池的阴阳极
撰写人:张立
【案例描述】
学生在学习原电池之后,知道原电池分为正负极,学习电解池之后,知道电解池中分阴阳极,但在学习本章的最后一节内容:金属的防护的时候,出现了一种电化学保护方法,即:牺牲阳极的阴极保护法,此种保护方法,不是电解池,而是原电池,学生看到此处,头脑发晕,电解池和原电池的两极极易混淆。
【诊断分析】
1.学生具有思维定势;
2.学生对阴阳极的标准判断不清楚;
【策略步骤】
将原电池和电解池的经典模型进行对比比较,而后对电极进行判断,指出各电极所发生的反应类型,进而进一步深化阴阳极的判断标准。
即:标准1:发生氧化反应的一极为阳极,发生还原反应的一极为阴极。
标准2:规定:电解池中与电源正极相连一极为阳极,与电源负极相连一极为阴极。
【效果检测】
1、铜锌原电池中,Zn为,发生反应,也叫。
2、以石墨棒为两极,电解饱和食盐水,其中有黄绿色气体逸出一极为,向饱和食盐水中滴加酚酞,变红色的一极为。
答案:1、负极,氧化,阳极 2、阳极阴极
【感悟思考】
从某种意义上讲,电解池与原电池在电极判断上,因为所发生反应的类型相似性,可以规定两种池子的阴阳极,摆脱混淆问题的根本在于,阴阳极的定义。
通过习题强化,定义强化,可以使学生在短时间内,解决混淆问题。
