原子吸收光谱法课件
合集下载
原子吸收光谱法

但是石墨炉原子化法的分析速度较慢,分析成本高 ,精密度差,基体干扰比较大。
低温原子化法:低温原子化法也称为化学原子化法 ,包括冷原子化法和氢化物发生法。
一般冷原子化法与氢化物发生法可以使用同一装置 。
冷原子化法:直接测量Hg 氢化物发生法:氢化物发生器生成金属或类金属元
素氢化物,进入原子化器。
第四节 干扰及其消除方法
物理干扰:由于溶液的物理性质(如粘度、表面张力、密度和蒸 气压等)的变化引起的试液抽吸过程、雾化过程和蒸发过程的比 例不同。消除物理干扰的主要方法是配制与被测试样相似组成的 标准溶液,或采用标准加入法。
电离干扰:在高温下,原子电离成离子,而使基态原子数目减少 ,导致测定结果偏低,此种干扰称电离干扰。消除办法是向试液 中加入过量比待测元素电离电位低的其他元素(通常为碱金属元 素)。例如,测钙时可加入过量的KCl溶液消除电离干扰。钙的 电离电位为6.1eV,钾的电离电位为4.3eV。由于K电离使钙离子 得到电子而生成原子。
{ C2H2:空气
> ¼ 富燃火焰 ≈¼ 中性火焰 化学计量火焰
< ¼ 贫燃火焰
根据燃气和助燃气的种类不同常用的有以下火焰:
乙炔-空气火焰; 氢-空气火焰; 乙炔-氧化亚氮火焰。
① Al,Ti,Ta,Zr等易形成难解离氧化物,不宜使用
② As 193.64,197.20nm;Se 196.09nm 不易使用 乙炔—空气火焰 是原子吸收测定中最常用的火焰,该火焰 燃烧稳定,重现性好,温度较高,可达23000C ,对大多数元
化学干扰:被测元素与共存组分发生化学反应,生成更稳定的 化合物,影响被测元素的原子化。由于PO43-的存在,钙与其形 成了磷酸钙、焦磷酸钙等化合物,这些化合物其键能很高,在 火焰中不易分解产生钙原子,结果偏低。消除方法:加入干扰 抑制剂的方法,如加入锶盐后Sr与PO43-反应生成比磷酸钙更加 稳定的化合物,从而释放出钙原子,消除了磷酸根离子对钙的 干扰。
低温原子化法:低温原子化法也称为化学原子化法 ,包括冷原子化法和氢化物发生法。
一般冷原子化法与氢化物发生法可以使用同一装置 。
冷原子化法:直接测量Hg 氢化物发生法:氢化物发生器生成金属或类金属元
素氢化物,进入原子化器。
第四节 干扰及其消除方法
物理干扰:由于溶液的物理性质(如粘度、表面张力、密度和蒸 气压等)的变化引起的试液抽吸过程、雾化过程和蒸发过程的比 例不同。消除物理干扰的主要方法是配制与被测试样相似组成的 标准溶液,或采用标准加入法。
电离干扰:在高温下,原子电离成离子,而使基态原子数目减少 ,导致测定结果偏低,此种干扰称电离干扰。消除办法是向试液 中加入过量比待测元素电离电位低的其他元素(通常为碱金属元 素)。例如,测钙时可加入过量的KCl溶液消除电离干扰。钙的 电离电位为6.1eV,钾的电离电位为4.3eV。由于K电离使钙离子 得到电子而生成原子。
{ C2H2:空气
> ¼ 富燃火焰 ≈¼ 中性火焰 化学计量火焰
< ¼ 贫燃火焰
根据燃气和助燃气的种类不同常用的有以下火焰:
乙炔-空气火焰; 氢-空气火焰; 乙炔-氧化亚氮火焰。
① Al,Ti,Ta,Zr等易形成难解离氧化物,不宜使用
② As 193.64,197.20nm;Se 196.09nm 不易使用 乙炔—空气火焰 是原子吸收测定中最常用的火焰,该火焰 燃烧稳定,重现性好,温度较高,可达23000C ,对大多数元
化学干扰:被测元素与共存组分发生化学反应,生成更稳定的 化合物,影响被测元素的原子化。由于PO43-的存在,钙与其形 成了磷酸钙、焦磷酸钙等化合物,这些化合物其键能很高,在 火焰中不易分解产生钙原子,结果偏低。消除方法:加入干扰 抑制剂的方法,如加入锶盐后Sr与PO43-反应生成比磷酸钙更加 稳定的化合物,从而释放出钙原子,消除了磷酸根离子对钙的 干扰。
原子吸收光谱法(AAS)

局限性:测不同的元素需不同的元 素灯,不能同时测多元素,难熔元 素、非金属元素测定困难。
原子吸收光谱法基本原理
1.原子的能级与跃迁
基态第一激发态,吸收一定频率的辐射能量。 产生共振吸收线(简称共振线) 吸收光谱 激发态基态,发射出一定频率的辐射。 产生共振吸收线(也简称共振线) 发射光谱
原子吸收光谱法基本原理
A kc
原子吸收分光度计
原子吸收分光度计
原子吸收分光度计
光源
原子化器
单色器
检测系统
思考:光学系统(单色器)为什么在原子化器和检 测系统之间?
光 源
提供待测元素的特征光谱。获得较高的 灵敏度和准确度。 光源应满足如下要求; (1)能发射待测元素的共振线; (2)能发射锐线; (3)辐射光强度大,稳定性好。
2.元素的特征谱线
(1)各种元素的原子结构和外层电子排布不同 基态第一激发态:
跃迁吸收能量不同——具有特征性。
(2)各种元素的基态第一激发态
最易发生,吸收最强,最灵敏线。特征谱线。
(3)利用原子蒸气对特征谱线的吸收可以进行定量分析
原子吸收光谱法基本原理
从光源发射出具有待测元素特征 谱线的光,通过试样蒸气时,被蒸气 中待测元素的基态原子所吸收,吸收 的程度与被测元素的含量成正比。故 可根据测得的吸光度,求得试样中被 测元素的含量。
将待测试样在专门的氢化物生成器中产生氢
化物,送入原子化器中检测。
单色器
•作用:将待测元素的吸收线与邻近线分开
•组件:色散元件 ( 棱镜、光栅 ) ,凹凸镜、 狭缝等
检测系统
•作用: 将待测元素光信号转换为电信号, 经放大数据处理显示结果。 •组件: 检测器、放大器、对数变换器、显 示记录装置。
原子吸收光谱法
无火焰法 特征量 65 种元素 5. 不能进行多元素同时测定
第二节 原子吸收光谱法的原理 A KbC 一、吸收定律
1. 入射光是单色光; 2. 入射线与吸收线中心频率重合 二、原子吸收线 1. 吸收线的轮廓
(△K小)
0 中心 吸收频率
λ0 中心 吸收波长
1
2
半宽度
△λ1/2
I
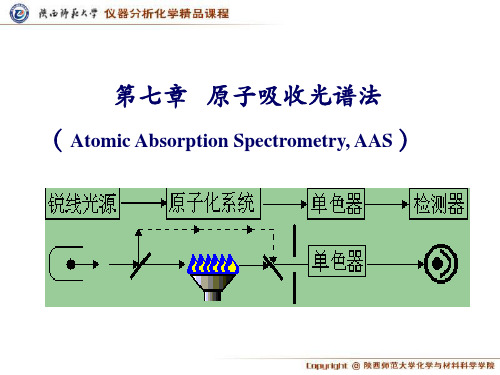
第七章 原子吸收光谱法 ( Atomic Absorption Spectrometry, AAS )
第一节
概
述
一、原子吸收光谱法(AAS) 根据物质的基态原子蒸气对其特征辐射的吸收作用来进行
元素定量分析的方法。
二、原子吸收光谱法简史 1.1802年 Wollaston发现:太阳连续光谱中几条位置固定的暗 线, 如 589.0 nm; 589.6nm 2. 1955年,Walsh发表了著名论文《原子吸收光谱法在 分析化学中的应用》, 提出了AAS技术 ①空心阴极灯; 3.1961年 ②火焰原子化器
2)火焰的类型
火焰的类型 富燃火焰 化学计量火焰 贫燃火焰 燃助比 约 1: 3 约 1: 4 约 1: 6 火焰的性质 还原性 中性 氧化性 火焰状态 层次模糊 呈亮黄色 应用范围 易氧化而形成难解离氧 化物的元素 大多数元素皆适用 不易氧化的元素
层次清楚 蓝色透明
火焰发暗 高度缩小
** 气流量
灵敏度
лЪвов 提出无火焰AAS
三、特点
1. 精密度高 RSD<1%
Ei kT
Ni gi e N0 g0
N0≈N , N0 对温度变化迟钝 相对误差 1~5%
2. 选择性好 准确度高 一种元素一个灯 3. 灵敏度高 火焰法
分析化学 第5章 原子吸收光谱法

24
原子化器(一)
• 作用:原子化器的功能在于将
试ห้องสมุดไป่ตู้转化为所需的基态原子 • 要求:
原子化效率高记忆效应小 背景影响和噪音低
装置简单耐用,易清洗
25
26
原子化器(二)
• 种类
• 火焰原子化器 • 非火焰原子化器
全消耗型 预混合型 电热原子化(石墨炉) 低温原子化
27
28
29
单色器
原子吸收光谱法
药物分析教研室
1
• 第 1节 • 第 2节 • 第 3节 • 第 4节
基本原理 仪器 实验技术 应用示例
2
• 要求
• 了解AAS的基本原理。 • 熟悉一般原子吸收分光光度计的 组成部分。 • 掌握原子吸收分光光度法定量分 析方法。 • 了解原子吸收测定的干扰情况。
3
概 述
定 义 特 点
12
• 塞曼效应(Zeemann effect)
• 电子在外加磁场作用下,发生 光谱项再分裂,分裂为子能级 数目可能为每个光谱支项所包 含的g=2J+1个 状态的现象。
13
原子在各能级的分布
• 物质激发态与基态原子数之比 服从Boltzmann分布律。
• 基态原子数≈原子总数
14
原子吸收线的形状及谱线变宽
缺 点
4
•定 义
• 基于蒸气相中被测元素的基 态原子对其原子共振辐射的 吸收来测定样品中该元素的 一种方法 。
5
UV与AAS比较
6
•特 点
• 检出限低,灵敏度高--- 10-9 g/ml
• 选择性好,准确度高---窄带吸收, 不同元素各自光源 • 分析速度快,测定范围广---可测元 素70多种
原子化器(一)
• 作用:原子化器的功能在于将
试ห้องสมุดไป่ตู้转化为所需的基态原子 • 要求:
原子化效率高记忆效应小 背景影响和噪音低
装置简单耐用,易清洗
25
26
原子化器(二)
• 种类
• 火焰原子化器 • 非火焰原子化器
全消耗型 预混合型 电热原子化(石墨炉) 低温原子化
27
28
29
单色器
原子吸收光谱法
药物分析教研室
1
• 第 1节 • 第 2节 • 第 3节 • 第 4节
基本原理 仪器 实验技术 应用示例
2
• 要求
• 了解AAS的基本原理。 • 熟悉一般原子吸收分光光度计的 组成部分。 • 掌握原子吸收分光光度法定量分 析方法。 • 了解原子吸收测定的干扰情况。
3
概 述
定 义 特 点
12
• 塞曼效应(Zeemann effect)
• 电子在外加磁场作用下,发生 光谱项再分裂,分裂为子能级 数目可能为每个光谱支项所包 含的g=2J+1个 状态的现象。
13
原子在各能级的分布
• 物质激发态与基态原子数之比 服从Boltzmann分布律。
• 基态原子数≈原子总数
14
原子吸收线的形状及谱线变宽
缺 点
4
•定 义
• 基于蒸气相中被测元素的基 态原子对其原子共振辐射的 吸收来测定样品中该元素的 一种方法 。
5
UV与AAS比较
6
•特 点
• 检出限低,灵敏度高--- 10-9 g/ml
• 选择性好,准确度高---窄带吸收, 不同元素各自光源 • 分析速度快,测定范围广---可测元 素70多种
原子吸收光谱法(共73张课件)

比尔定律:
▪ 分析中,待测元素的浓度与其吸收辐射的原子总数成正 比。在一定浓度范围和一定火焰宽度L下:
▪ 可以通过测吸光度可求得待测元素的含量。
▪ 原子吸收分光光度A分析k'的c定量基础。待测元素浓度
2024/8/30
27
§4-3 原子吸收分光光度计
一、基本构造
光源
原子化系统
分光系统
检测系统 显示装置
表
处吸收轮廓上两点间的距离
征
(即两点间的频率差)。
▪ 数量级为10-3 -10-2 nm (发射线10-4 -10-3 nm )。
图4.2 原子吸收光谱轮廓图
2024/8/30
12
谱线变宽: 自然宽度 :N
▪ 无外界影响下,谱线仍有一定宽度—自然宽度。
▪ 与原子发生能级间跃迁时激发态原子的平均寿命有关。
2024/8/30
图4.3 峰值吸收测量示意图
21
应用原理: ▪ 光源:
2024/8/30
A lg I0 I
I0
e
0
I0d
I
e
0
Id
I I0eKL
I e 0
I0eKLd
Alg
e
0
I0 d
I e d e
K L
0 0
则:
在满足瓦尔西方法的测量条件时,在积分界限
内 吸可 收以 系认 数为。为常数,并合K理 地使之等于峰值
5%,测定灵敏度极差。
噪音低;
用该元素的锐线光源发射出特征辐射。 特点: 原子吸收分析的主要特点是测定灵敏度高,特效
发射的谱线稳定性好、强度高且宽度窄。
共振线在外光路损失小。
试样在原子化器中被蒸发,解离为气态基态原子。 共Ok振! L线et(’s特Ha征ve谱a线B)re是ak元. 素所有谱线中最容易发生、最灵敏的线,又具有元素的特征,所以分析中用该谱线作为分析线。
原子吸收光谱法PPT课件

消除电离干扰的方法
加入消电离剂 利用富燃火焰也可抑制电离干扰 利用温度较低的火焰 提高溶液的吸喷速率 标准加入法
化学干扰
是指试样溶液转化为自由基态原子的过程中,待 测元素和其他组分之间发生化学作用而引起的干 扰效应.它主要影响待测元素化合物的熔融,蒸发 和解离过程.这种效应可以是正效应,增强原子吸 收信号;也可以是负效应,降低原子吸收信号.化学 干扰是一种选择性干扰,它不仅取决于待测元素与 共存元素的性质,还与火焰类型,火焰温度,火焰状 态,观察部位等因素有关.化学干扰是火焰原子吸 收分析中干扰的主要来源,其产生的原因是多方面 的.
物理干扰
吸喷速率
喷雾量和雾化效率
毛细管形状
物理干扰一般都是负干扰,最终影响火焰分 析体积中原子的密度.
消除物理干扰的方法
配制与待测试液基体相一致的标准溶液; 当前者困难时,可采用标准加入法; 当被测元素在试液中浓度较高时,可以稀释溶液来降低
或消除物理干扰; 在试液中加入有机溶剂,改变试液的粘度和表面张力,
A.
A lg
I0 I
KC
原子吸收光谱仪的构成
光源:提供特征锐线光谱 原子化器:产生原子蒸汽,使被测元素
原子化 分光系统:将被测分析线与光源其他谱
线分开,并阻止其他谱线进入检测器 检测系统:光电倍增管 数据处理系统器
测量条件的选择
吸收线的选择 灯电流的选择 火焰种类的选择 燃烧气和助燃气的流量 火焰高度 石墨炉原子化条件的选择
内标法:分别在标准试样和被测试样中加入已知量的第
三种元素作为内标元素,测定分析线和内标线的吸光度比
D (工D作,曲D线x .)然并后以在D对标应准标曲准线溶上液根中据被测元计素算含出量试或样浓中度待绘测制
大连理工分析化学课件-第7章 原子吸收光谱法

火焰原子化法:
3
cDL A
石墨炉原子化法:
V 3
mDL
A
第六节
原子吸收光谱法的应用
元素的原子吸收法测定
碱金属
碱土金属
有色金属
贵金属
如:人发中钴的测定。浓硝酸消解,萃取分离。 灯电流为6 mA,光谱通带为0.2 nm。测定Co 240.7 nm的吸光度。检出限为0.02 mg/L, RSD<6%,回收率 94.0% ~ 102.0%。
化学干扰的抑制(了解)
通过在标准溶液和试液中加入某种光谱化学缓 冲剂来抑制或减少化学干扰:
释放剂:与干扰元素生成更稳定化合物使待测 元素释放出来。
例:锶和镧可有效消除磷酸根对钙的干扰,因 为锶和镧与磷酸根形成更稳定的化合物。
保护剂:与待测元素形成稳定的络合物,防止 干扰物质与其作用。
例:测定钙时,加入EDTA生成EDTA-Ca2+,避 免磷酸根与钙作用。
洛伦兹变宽(碰撞变宽):由于原子相互 碰撞使能量发生稍微变化。
定量基础
钨丝灯光源和氘灯,经分光后,光谱通带0.2 nm 。而原子吸收线的半宽度:10-3 nm。
若用一般光源照射时,吸收光的强度变化仅为 0.5%,灵敏度极差。
若将原子蒸气吸收的全部
能量,即谱线下所围面积
测量出(积分吸收),则
是一种绝对测量方法,现
在的分光装置无法实现。
定量基础(续)
峰值吸收:峰值吸收系数K0与火焰中待测元素的 基态原子数N0成正比。
前提是:采用温度不太高的稳定的火焰原子化器 和使用锐线光源辐射。
(1)光源的发射线与吸收线的v0一致。 (2)发射线的Δv<吸收线的 Δv。 空心阴极灯可发射锐线光源。
第十章 原子吸收光谱法

20
二、原子化系统
作用是将试样中待测元素转变成原子蒸气。 1.火焰原子化法 (1)雾化器:作用是将试样溶液雾化。当助
燃气高速通过时,在毛细管外壁与喷嘴口构 成的环形间隙中,形成负压区,将试样溶液 吸入,并被高速气流分散成气溶胶,在出口 与撞击球碰撞,进一步分散成微米级的细雾。 (2)混合室:作用是将未被细微化的较大雾 滴在混合室内凝结为液珠,沿室壁流入泄漏 管排走;并让气溶胶在室内与燃气充分混匀。
第十章 原子吸收光谱法
§10-1 §10-2 §10-3 §10-4 §10-5 §10-6
试题
概述 原子吸收法的基本原理 原子吸收分光光度计 定量分析方法 干扰及其抑制方法 灵敏度与检出限
1
§10-1 概述
一、 原子吸收光谱法
原子吸收光谱是利用待测元素的原子蒸 气中基态原子对特征电磁辐射(共振线)的吸 收来测定的。
式中ν0为谱线中心频率;M 为吸光原子的相对 原子质量;T 为绝对温度。 ΔνD约10-3数量
级,是谱线变宽的主要原因。 3.碰撞变宽(压力变宽) 由于原子相互碰撞使能量发生轻微变化。
劳伦兹变宽ΔνL :待测原子和其他原子碰撞引
起的谱线变宽。
ΔνL约10-3数量级,是碰撞变宽的主要因素。
10
赫鲁兹马克变宽ΔνH :同种原子碰撞引起的
29
二、标准加入法
取若干份体积相同的试液(cX),依次按比 例加入不同量的待测物的标准溶液(cO), 定容后浓度依次为:cX、cX+cO、cX+2cO、 cX+3cO、cX+4cO,分别测得吸光度为:A0、 A1、A2、A3、A4。以A对浓度c做图得一直 线,图中cX点即待测溶液浓度。
30
注意: 1.本法只能消除基体效应带来的干扰,不能消
二、原子化系统
作用是将试样中待测元素转变成原子蒸气。 1.火焰原子化法 (1)雾化器:作用是将试样溶液雾化。当助
燃气高速通过时,在毛细管外壁与喷嘴口构 成的环形间隙中,形成负压区,将试样溶液 吸入,并被高速气流分散成气溶胶,在出口 与撞击球碰撞,进一步分散成微米级的细雾。 (2)混合室:作用是将未被细微化的较大雾 滴在混合室内凝结为液珠,沿室壁流入泄漏 管排走;并让气溶胶在室内与燃气充分混匀。
第十章 原子吸收光谱法
§10-1 §10-2 §10-3 §10-4 §10-5 §10-6
试题
概述 原子吸收法的基本原理 原子吸收分光光度计 定量分析方法 干扰及其抑制方法 灵敏度与检出限
1
§10-1 概述
一、 原子吸收光谱法
原子吸收光谱是利用待测元素的原子蒸 气中基态原子对特征电磁辐射(共振线)的吸 收来测定的。
式中ν0为谱线中心频率;M 为吸光原子的相对 原子质量;T 为绝对温度。 ΔνD约10-3数量
级,是谱线变宽的主要原因。 3.碰撞变宽(压力变宽) 由于原子相互碰撞使能量发生轻微变化。
劳伦兹变宽ΔνL :待测原子和其他原子碰撞引
起的谱线变宽。
ΔνL约10-3数量级,是碰撞变宽的主要因素。
10
赫鲁兹马克变宽ΔνH :同种原子碰撞引起的
29
二、标准加入法
取若干份体积相同的试液(cX),依次按比 例加入不同量的待测物的标准溶液(cO), 定容后浓度依次为:cX、cX+cO、cX+2cO、 cX+3cO、cX+4cO,分别测得吸光度为:A0、 A1、A2、A3、A4。以A对浓度c做图得一直 线,图中cX点即待测溶液浓度。
30
注意: 1.本法只能消除基体效应带来的干扰,不能消
第5章原子吸收光谱法

解: 设配制的100ml铁样溶液铁的浓度为Cx mg/L
Ax kcX
02:47
Ax s
k
C xVx Vx
CsVs Vs
Ax Cx (Vx Vs ) Axs CxVx CsVs
0.28 Cx (30.00 20.00) 0.61 30.00Cx 20.00 3.12
Cx=0.7905 mg/L
峰值吸收的基本条件是: (1)采用锐线光源,且要求∆ν发<<∆ν吸 (2)光源辐射的中心频率ν0发
与吸收线中心频率ν0吸 重合。
即ν0发=ν0吸
02:47
在这两个基本条件之下,可以证明: A=KN0L
A为吸光度;N0为基态原子数,L为火焰厚度,K 为吸收系数,为一常数值。 由于
N0=N总C 燃烧器长度一定时,L为常数,上式可写作下式
10
100% 0.0019%
0.2687
便用标准加入法时应注意下列几点:
(1)标准曲线是一条过原点的直线。 (2)被测元索的浓度应在标准曲线线性范围内。 (3)最少应采用四个点来制作外推曲线。 (4)加入标准的量不能过高或过低。
否则直线斜率过大或过小均引起较大误差。这可通过试喷试样溶液和标准 溶液,比较两者的吸光度来判断。
T=2500K时, T=3000K时,
N 2e 1.14 10 j
1.3861.6026231205304035.8091.008109
P0
4
N0
N 2e 5.80 10 j
1.3861.6026231300304035.8091.008109
4
N0
从以上计算可以看出,与基态原子数相比,激发态原子数可忽 略不计。
则:
Nj
原子吸收光谱分析ppt课件

原子吸收分光光度法 Atomic Absorption Spectrophotometry,
(AAS)
1.简述 2.方法原理 3.仪器设备 4.火焰原子化法测试的任务参数选择 5.石墨炉原子化法测试的任务参数选择 6.干扰及消除
第一节.简述
1.原子吸收的发现
1802年,伍朗斯顿(W. H. Wollaston)在进展太 阳察看时,发现太阳光谱中存在一些暗线。 夫郎霍费(J. Fraunhofer)在1814~1817年,布鲁 斯特(D. Brewster) 在1820年相继对这些暗线 进展仔细的察看,以为是由于太阳外围较 冷 的气体吸收了太阳光所引起的。
1964年,黄本立等将蔡司Ⅲ型滤光片式 火焰光度计改装为一台简易原子吸收光谱安装, 测定了溶液中的钠,发表了最早的原子吸收光谱 分析的研讨论文。
1965年吴庭照等利用自制的同心型气动 玻璃雾化器、预混合金属层流熄灭器、镁空心阴 极灯,英国Hilger的H-700火焰分光光度计的单色 器、10 cm长不锈钢平头水冷熄灭器的预混合型火 焰原子化器组装了原子吸收光谱仪器。完成了鋰 中微量镁的测定。
4.原子吸收光谱分析的特点
优点: ⑴ 检出限低 火焰原子吸收法的检出限可到达 ng/mL量级,石墨炉原子吸收光谱法的检出限可到 达10-13~10-14g。 ⑵ 选择性好 由于原子吸收是线状吸收,又采用 待测元素特征谱线作为光源,即使在溶液中有多 个元素共存,只需它们不与待测元素产生难原子 化的化合物,就不会产生较大的谱线干扰。加上 吸收谱线比发射谱线少的多,各元素谱线的重叠
鉴于沃尔什在建立和开展原子吸收光谱分析方 面的历史功勋,1991年在挪威卑尔根召开的第27 届国际光谱学大会(CSI)上授予他第一届CSI奖。
Alan Walsh(1916-1998)和他的原子吸收光谱仪
(AAS)
1.简述 2.方法原理 3.仪器设备 4.火焰原子化法测试的任务参数选择 5.石墨炉原子化法测试的任务参数选择 6.干扰及消除
第一节.简述
1.原子吸收的发现
1802年,伍朗斯顿(W. H. Wollaston)在进展太 阳察看时,发现太阳光谱中存在一些暗线。 夫郎霍费(J. Fraunhofer)在1814~1817年,布鲁 斯特(D. Brewster) 在1820年相继对这些暗线 进展仔细的察看,以为是由于太阳外围较 冷 的气体吸收了太阳光所引起的。
1964年,黄本立等将蔡司Ⅲ型滤光片式 火焰光度计改装为一台简易原子吸收光谱安装, 测定了溶液中的钠,发表了最早的原子吸收光谱 分析的研讨论文。
1965年吴庭照等利用自制的同心型气动 玻璃雾化器、预混合金属层流熄灭器、镁空心阴 极灯,英国Hilger的H-700火焰分光光度计的单色 器、10 cm长不锈钢平头水冷熄灭器的预混合型火 焰原子化器组装了原子吸收光谱仪器。完成了鋰 中微量镁的测定。
4.原子吸收光谱分析的特点
优点: ⑴ 检出限低 火焰原子吸收法的检出限可到达 ng/mL量级,石墨炉原子吸收光谱法的检出限可到 达10-13~10-14g。 ⑵ 选择性好 由于原子吸收是线状吸收,又采用 待测元素特征谱线作为光源,即使在溶液中有多 个元素共存,只需它们不与待测元素产生难原子 化的化合物,就不会产生较大的谱线干扰。加上 吸收谱线比发射谱线少的多,各元素谱线的重叠
鉴于沃尔什在建立和开展原子吸收光谱分析方 面的历史功勋,1991年在挪威卑尔根召开的第27 届国际光谱学大会(CSI)上授予他第一届CSI奖。
Alan Walsh(1916-1998)和他的原子吸收光谱仪
第5讲 原子吸收光谱法

00:49:45
三、定量分析方法
1.标准曲线法
配制一系列不同浓度的标准试样,由低到高依次分析, 将获得的吸光度A数据对应于浓度作标准曲线,在相同条件下 测定试样的吸光度A数据,在标准曲线上查出对应的浓度值; 或由标准试样数据获得线性方程, 将测定试样的吸光度A数据带入计算。 注意在高浓度时,标准曲线易发生 弯曲,压力变宽影响所致;
cDL=3SB/Sc
(2)石墨炉法
(单位:μgml-1 )
mDL=3SB/Sm (单位:ng或pg )
SB:标准偏差 Sc(Sm):待测元素的灵敏度,即工作曲线的斜率。
00:49:45
二、测定条件的选择
1.分析线
一般选待测元素的共振线作为分析线,测量高浓度时,
也可选次灵敏线。 2.光谱通带(可调节狭缝宽度改变) 无邻近干扰线(如测碱及碱土金属)时,选较大的通带, 反之(如测过渡及稀土金属),宜选较小通带。
(△λ =10-3,若λ 取600nm,单色器分辨率R =λ /△λ = 6×105 )
解决办法:
00:49:45
提供锐线光源,测定峰值吸收!
2.锐线光源
在原子吸收分析中需要使用锐线 光源,测量谱线的峰值吸收,锐线 光源需要满足的条件: (1)光源的发射线与吸收线的ν0
一致。
(2)发射线的Δν 1/2 小于吸收线 的 Δν1/2。 提供锐线光源的方法:空心阴极灯
(c)火焰温度取决于燃气与助燃气类型,常用空气—乙
炔,最高温度2600K,能测30多种元素。
00:49:45
火焰类型:
化学计量火焰: 温度高,干扰少,稳定,背景低,常用。 富燃火焰: 还原性火焰,燃烧不完全,测定 较易形成难熔氧化物的元素Mo、Cr 稀土等。
原子吸收光谱法atom

Insulator Anode
检测系统
Photocathode
Light Energy
eee---ee--e-eeБайду номын сангаас-ee-e- ee-
Dynode (9-13)
Quartz Window
*100 Million Amplification of Signal
Photomultiplier Tube Operation
一束频率 、强度为I0的平行光通过 厚度为L的原子蒸气,一局部光被吸收,透 过光的强度I 服从吸收定律
I = I0 exp(-k Lc)
式中k 是基态原子对频率为 的光的吸 收系数。不同元素原子吸收不同频率的光
I 与
I
的
关
系
0
二、原子吸收光谱仪
原子吸收光谱仪包括4局部: 光源 原子化器 波长选择 检测系统
原子吸收光谱法atom
本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢!
一、原子吸收原理
在通常的原子吸收测定条件下,原子 蒸气中基态原子数近似等于总原子数。
常用的火焰体系
乙炔-空气 火焰 是原子吸收测定中最常用 的火焰,该火焰燃烧稳定,重现性好,噪 声低,温度高,对大多数元素有足够高的 灵敏度
氢-空气火焰 燃烧速度较乙炔-空气 火焰高, 但温度较低,优点是背景发射较弱,透射 性能好。
乙炔-一氧化二氮火焰 的优点是火焰温度 高,而燃烧速度并不快,适用于难原子化 元素的测定,用它可测定70多种元素。
四、定量分析方法
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
石墨炉原子化装置
外气路中Ar气体沿石墨管外壁流动, 冷却保护石墨管;内气路中Ar气体由管两 端流向管中心,从中心孔流出,用来保护 原子不被氧化,同时排除干燥和灰化过程 中产生的蒸汽。
石墨炉原子化装置
原子化过程分为干燥、灰化(去除基体)、 原子化、净化(去除残渣)四个阶段,待测元 素在高温下生成基态原子。
A B C D cx+ 4cs cx cx+ cs cx+ 2cs
测得相应的吸光度
Ax
A1
A2
A4
标准加入法
以A为纵坐标,标准溶液浓度cs为横坐标, 绘制工作曲线,如下图:
延长工作曲线与横坐标 轴相交,交点至原点的距 离所相应的浓度cx ,即为 所求被测元素的浓度。
标准加入法
浓度直读法:
在标准曲线线性范围内,用几个标准溶 液喷雾,并用仪表指示调节到它们相应的 浓度值。然后在相同的实验条件下吸喷试 液,仪表上的读数就是该试液的浓度。
标准曲线法
注意:在高浓度时,标准曲线易发生弯曲。
标准加入法
计算法:
设容量瓶A,待测元素浓度Cx,吸光度Ax; 容量瓶B,待测元素浓度为(Cx+Cs),吸光 度为Ax+s,可求得被测试液元素的浓度为:
Ax cx cs Ax+s Ax
标准加入法
作图法:
设同体积容量瓶编号 试液+标准溶液浓度
A kc
原子吸收分光度计
原子吸收分光度计
光源
原子化器
单色器
检测系统
思考:光学系统(单色器)为什么在原子化器和检 测系统之间?
光 源
提供待测元素的特征光谱。获得较高的 灵敏度和准确度。 光源应满足如下要求; (1)能发射待测元素的共振线; (2)能发射锐线; (3)辐射光强度大,稳定性好。
光 源
——空心阴极灯的原理
用不同待测元素作阴极材料,可制成相应空 心阴极灯; 空心阴极灯的辐射强度与灯的工作电流有关。
优缺点: (1)辐射光强度大,稳定,谱线窄,灯容易更换。 (2)每测一种元素需更换相应的灯。
原子化器
将试液中的待测元素转变成基态原子蒸气
M 1(激发态原子)
MX(试液)
蒸发
MX(气态)
局限性:测不同的元素需不同的元 素灯,不能同时测多元素,难熔元 素、非金属元素测定困难。
原子吸收光谱法基本原理
从光源发射出具有待测元素特征 谱线的光,通过试样蒸气时,被蒸气 中待测元素的基态原子所吸收,吸收 的程度与被测元素的含量成正比。故 可根据测得的吸光度,求得试样中被 测元素的含量。
原子吸收光谱法基本原理
石墨炉原子化装置
优点:原子化程度高,试样用量少(1100μL),可测固体及粘稠试样,灵敏度 高,检测极限10-12 g/L。 缺点:精密度差,测定速度慢,操作 不够简便,装置复杂。
单色器
•作用:将待测元素的吸收线与邻近线分开
•组件:色散元件 ( 棱镜、光栅 ) ,凹凸镜、 狭缝等
检测系统
•作用: 将待测元素光信号转换为电信号, 经放大数据处理显示结果。 •组件: 检测器、放大器、对数变换器、显 示记录装置。
定量分析的依据
基态原子对共振线的吸收程度与 蒸气中基态原子的数目和原子蒸气厚 度的关系,在一定的条件下,服从朗 伯-比耳定律::
I0 A lg KN 0 L I
定量分析的依据
由于原子化过程中激发态原子数目和离子数很 少,因此蒸气中的基态原子数目实际上接近于被 测元素的总原子数目,而总原子数目与溶液中被 测元素的浓度c成正比。在L一定条件下:
概述
原子吸收光谱(atomic absorption spectrometry AAS ):是基于从光源发出的被测元素特征 辐射通过元素的原子蒸气时被其基态原子吸 收,由辐射的减弱程度测定元素含量的一种 现代仪器分析方法。
概述
特点:
(1) 检出限低,10-10~选择性高,一般情况下共存元素不干扰; (4) 分析速度快,应用广,可测定70多个元素。
原子吸收光谱法
概述
原子吸收光谱法基本原理
原子吸收分光度计 定量分析结果的计算
概述
原子吸收光谱法(也称原子吸收分光光 法)与可见、紫外分光光度法基本原理 相同,都是基于物质对光选择吸收而 建立起来的光学分析法。
概述
区别:在可见、紫外分光光度法中,吸光
物质是溶液中被测物质的分子或离子对光 的选择吸收,原子吸收光谱法吸光物质是 待测元素的基态原子对光的选择吸收,这 种光是由待测元素制成的空心阴极灯(称元 素灯)作光源。
Thank you for your cooperation!
光 源
——空心阴极灯
由一个钨丝作阳极,空心阴极由待测元素的高纯金 属或合金制成。接通电源发射出待测元素的特征谱线。
光 源
——空心阴极灯的原理
施加适当电压时,电子将从空心阴极内壁流向 阳极; 与充入的惰性气体碰撞而使之电离,产生正电 荷,其在电场作用下,向阴极内壁猛烈轰击; 使阴极表面的金属原子溅射出来,溅射出来的 金属原子再与电子、惰性气体原子及离子发生撞 碰而被激发,于是阴极内辉光中便出现了阴极物 质和内充惰性气体的光谱;
定量分析结果的计算
标准曲线法
计算法
标准加入法
作图法 浓度直读法
内标标准曲线法
内标法
内标计算法
标准曲线法
配制一组合适的标准溶液,由低浓度到高浓 度依次喷入火焰,将获得的吸光度 A 数据对应 于浓度c作标准曲线,在相同条件下测定试样的 吸光度 A ,在标准曲线上求出对应的浓度值。 或由标准试样数据获得线性方程,将试样的吸 光度A数据代入计算。
热解
激发
M 0(基态原子)+X(气态)
激发
Mn+(离子)+ne-(电子)
原子化器
分 火焰原子化器 无火焰原子化器(石墨炉原子化器)
火焰原子化装置
——雾化器和燃烧器
主要缺点:雾化效率低
火焰原子化装置
——雾化器和燃烧器
火焰:试样雾滴在火焰中,经蒸发,干
燥,离解(还原)等过程产生大量基态原子。
空气-乙炔火焰:最常用,可测定30多种元素; N2O-乙炔火焰:火焰温度高,可测定的增加到 70多种。
