2019年高考理科综合(全国I卷)化学试题标准答案与阅卷评分细则
2019年高考理综化学真题试卷(全国Ⅰ卷)(含答案及过程详解)

绝密★启用前2019年普通高等学校招生全国统一考试(全国卷Ⅰ)理科综合能力测试(化学)注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16 mg24 s32 fe56 u64一、选择题(共7题;共42分)1.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是()A. “雨过天晴云破处”所描述的瓷器青色,来自氧化铁B. 闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C. 陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D. 陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点2.关于化合物2−苯基丙烯(),下列说法正确的是()A. 不能使稀高锰酸钾溶液褪色B. 可以发生加成聚合反应C. 分子中所有原子共平面D. 易溶于水及甲苯3.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是()A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开KB. 实验中装置b中的液体逐渐变为浅红色C. 装置c中的碳酸钠溶液的作用是吸收溴化氢D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯4.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是()A. 冰表面第一层中,HCl以分子形式存在B. 冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)C. 冰表面第三层中,冰的氢键网格结构保持不变D. 冰表面各层之间,均存在可逆反应HCl ⇌H++Cl−5.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的K a1=1.1×10−3 ,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
2019年全国高考I卷理科综合试卷及答案

2019最新全国高考理科综合能力测试本试卷共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
1.细胞膜的选择透过性保证了细胞内相对稳定的微环境。
下列物质中,以(自由)扩散方式通过细胞膜的是A.Na+B.二氧化碳C.RNAD.胰岛素2.哺乳动物肝细胞的代谢活动十分旺盛,下列细胞结构与对应功能表述有误..的是A.细胞核:遗传物质储存与基因转录B.线粒体:丙酮酸氧化与ATP合成C.高尔基体:分泌蛋白的合成与加工D.溶酶体:降解失去功能的细胞组分3.光反应在叶绿体类囊体上进行。
在适宜条件下,向类囊体悬液中加入氧化还原指示剂DCIP,照光后DCIP由蓝色逐渐变为无色。
该反应过程中A.需要ATP提供能量B.DCIP被氧化C.不需要光合色素参与D.会产生氧气4.以下高中生物学实验中,操作不正确...的是A.在制作果酒的实验中,将葡萄汁液装满整个发酵装置B.鉴定DNA时,将粗提产物与二苯胺混合后进行沸水浴C .用苏丹Ⅲ染液染色,观察花生子叶细胞中的脂肪滴(颗粒)D .用龙胆紫染液染色,观察洋葱根尖分生区细胞中的染色体5.用Xho I 和Sal I 两种限制性核酸内切酶分别处理同一DNA 片段,酶切位点及酶切产物分离结果如图。
以下叙述不正确...的是A .图1中两种酶识别的核苷酸序列不同B .图2中酶切产物可用于构建重组DNAC .泳道①中是用Sal I 处理得到的酶切产物D .图中被酶切的DNA 片段是单链DNA6.下列我国科技成果所涉及物质的应用中,发生的不是..化学变化的是A .甲醇低温所制氢气用于新能源汽车B .氘、氚用作“人造太阳”核聚变燃料C .偏二甲肼用作发射“天宫二号”的火箭燃料D .开采可燃冰,将其作为能源使用7.我国科研人员提出了由CO 2和CH 4转化为高附加值产品CH 3COOH 的催化反应历程。
2019年高考化学试题及答案(全国卷ⅠⅡⅢ)

2019年高考全国卷化学试题全国卷Ⅰ全国卷Ⅱ全国卷Ⅲ2019年高考全国卷Ⅰ化学试题7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2−苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图。
下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10−3mol·L−1(设冰的密度为0.9g·cm−3)C.冰表面第三层中,冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HClH++Cl−11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的K a1=1.1×10−3,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
(完整版)2019年高考化学试题及答案

2019年普通高等学校招生全国统一考试理科综合能力测试化学2019-6-9H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2−苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)C.冰表面第三层中,冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl−11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的K a1=1.1×10−3 ,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b 点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
2019年全国卷Ⅰ高考理综真题-化学部分解读

2019年全国I卷高考理综真题-化学部分分析2019年6月8日一年一度的高考落下帷幕,每年这个时候都是几家欢乐几家愁。
现就高考真题做一下分析。
从2020年起,参加本科院校招生录取的考生的总成绩由语文、数学、外语3门统一高考成绩和考生选考的3门普通高中学业水平考试等级性考试科目成绩构成,其中选考科目每门满分100分,即高校招生录取总分满分值为750分。
一、试卷总体评价2019年全国卷I卷化学试卷结构与往年变化不大,与2018年基本保持一致略有改变,试卷整体重基础,抓创新,以文献为基础命制试题,呈现我国科学家发表的世界领先的科技成果,注重试题情境素材选取,考查考生对常见物质性质的掌握,凸显化学学科核心素养。
全卷内容设计合理、知识覆盖面广、整体难度适中,试题梯度合宜,全方位考查学生接受、整合化学信息能力以探究能力。
二、试卷考点分析7.常识类,以陶瓷性质为载体,考查硅酸盐的物理化学性质,一方面考查考生对中华优秀传统文化中化学知识的了解,另一方面考查考生对常见化合物性质的掌握情况,难度不大8.有机物的结构,考查有机化合物的基本性质,难度不大9.有机化学实验,侧重有机物的制备及试剂的用途,母本为教材基本实验,难度适中10.电解质的电离平衡,此题为情景题,需要学生结合图片及所学知识进行分析,考查学生的综合分析能力,难度较大11.酸碱中和图像分析,强碱滴定弱酸,从导电能力分析酸碱反应进行程度,难度适中12.原电池中的生物燃料电池,根据反应原理和化合价变化可以解决此题,难度不大13.元素周期表和周期律,以《Science》杂志报道的新化合物——双(三氯甲基)磷阴离子为素材背景,考查新型反应中间体中的元素及化合物的结构和性质,考查学生图像观察,信息提取和综合分析能力,难度较大。
26.工艺流程图,与之前的考试类型一致,但题目顺序有所改变。
根据流程书写方程式,成分分析,离子检验及基本处理方法,考查范围较广,注重基础知识点的考查,试题难度适中27.工艺流程题,但考查内容为基础实验操作,涉及内容有去油污,加热,除杂,调pH,离子水解及化学式的书写,多维度考查学生的实验基础掌握,试题难度较为基础,难度不大28.化学反应原理,考查内容不变但形式改变,涉及反应焓变,活化能的计算,反应速率的计算,考查学生的图像分析能力和信息提取能力,难度较大35.物质结构与性质,以我国科学家在顶级刊物《Nature》发表的“双相纳米高强度镁合金的方法”为情境,给出拉维斯相的晶体结构,考查原子核外电子排布和能级、化合物中成键原子的轨道杂化形式、分子构型、晶体结构及其性质等内容,有一定难度。
2019年高考重庆市化学卷真题及答案

B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点 溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
7.分子式为C4H8BrCl的有机物共有(不含立体异构)
B.澄清的石灰水久置后出现白色固体Ca(OH)2+CO2 CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2 2Na2O+O2↑
D.向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3 2Fe(OH)3+3MgCl2
6.绚丽多彩的无机颜料的应用曾创造了古代绘Байду номын сангаас和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
C.增加环戊烯浓度D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L−1
9.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: (g)= (g)+H2(g)ΔH1=100.3 kJ·mol−1①
H2(g)+ I2(g)=2HI(g)ΔH2=﹣11.0 kJ·mol−1②
2019高考山东卷化学试题解析(1)

2019年全国高考山东卷化学试题解析可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Mn 55一、选择题:本题共有6小题,每小题2分,共12分。
在每小题给出的4个选项中,只有1项符合题目要求的。
1.某试剂瓶标签上安全标志如右图,该试剂是A.氨水B.乙酸C.氢氧化钠D.硝酸 【答案】D 【解析】安全标志为腐蚀性和氧化性,硝酸符合,D 项正确。
2.我国古代典籍中有“石胆……浅碧色,烧之变白色真”的记载,其中石胆是指 A.CuSO 4 ·5H 2O B. FeSO 4 ·7H 2O C. ZnSO 4 ·7H 2O D. KAl(SO 4)2 ·12H 2O 【答案】A 【解析】CuSO 4 ·5H 2O 为蓝色晶体,CuSO 4为白色粉末,加热发生反应: CuSO 4 ·5H 2O =====△ CuSO 4 (白)+5H 2O ,A 项正确。
3. 反应C 2H 6(g) = C 2H 4(g) +H 2(g) H>0 在一定条件下于密闭容器中达到平衡,下列各项措施中,不能提高乙烷的平衡转化率的是A.增大容器容积B.升高反应温度C.分离出部分氢气D.等容下通入惰性气体 【答案】D 【解析】增大容器容积相当于减少压强,平衡向正向移动,乙烷的平衡转化率增大,A 项不符合题意;该反应为吸热反应,升高温度,平衡向正向移动,乙烷的平衡转化率增大,B 项不符合题意;分离出部分氢气,衡向正向移动,乙烷的平衡转化率增大,C 项不符合题意;等容下通入惰性气体,原平衡体系各物质的浓度不变,平衡不移动,乙烷的平衡转化率不变,D符合题意。
4. 下列各组化合物中不互为同分异构体的是A. B.C. D.【答案】B 【解析】同分异构体的概念为分子式相同,结构不同的物质互为同分异构体。
A 中分子式均为C 6H 6 结构不同,二者关系为同分异构体,不符合题意;B 中分子式分别为C 14H 24 、C 14H 22关系不属于同分异构体符合题意;C 中分子式均为C 3H 6O 2结构不同,二者关系为同分异构体,不符合题意;D 中分子式均为C 6H 6O 3结构不同,二者关系为同分异构体,不符合题意。
2019全国一卷化学解析

2019全国一卷化学解析一、试卷整体评价2019年全国一卷化学试卷在保持稳定的基础上有所创新,题目难度适中,既注重了对基础知识与技能的考查,又强调了对能力和学科素养的考察。
试卷整体风格与往年大致相同,题型包括选择题、填空题和实验题,内容覆盖了无机化学、有机化学、物理化学、结构化学等多个领域。
二、各个题型分析1. 选择题:共12小题,每题3分,共36分。
题目涉及化学反应原理、元素化学、有机化学、结构化学等多个方面,注重基础知识的考察,同时也有一定的灵活性和深度。
解题的关键是要准确理解题意,找出解题的关键点,并灵活运用基础知识进行解答。
2. 填空题:共7个小题,每空1-2分,共33分。
题目涉及无机化学、有机化学、物理化学等多个领域,要求考生综合运用基础知识进行解答。
解题时要注意把握题目的整体性和连贯性,认真分析题目中所给出的信息,找出解题的关键点,并按照题目要求进行回答。
3. 实验题:共3个小题,每题10分,共30分。
题目涉及化学实验基本技能、实验设计、实验分析等多个方面,既注重了对基础知识与技能的考查,又强调了对实验能力和学科素养的考察。
解题的关键是要掌握实验基本技能,理解实验目的和原理,分析实验数据和现象,并按照题目要求进行回答。
三、考点分析1. 重视基础知识与技能:试卷中多个题目都涉及到了化学基础知识与技能,如化学反应原理、元素化学、有机化学、结构化学等,这些知识是化学学科的核心内容,也是考生必须掌握的基本技能。
计算等多个方面。
这些题目不仅要求考生能够准确理解和运用基础知识,还要求考生能够灵活运用所学知识解决实际问题。
四、备考建议1. 注重基础知识与技能的复习:考生在备考过程中,要加强对化学基础知识和基本技能的复习,掌握化学学科的核心概念和基本原理,了解化学学科的基本研究方法。
2. 加强实验能力的训练:考生在备考过程中,要加强对实验基本技能的训练,熟悉实验操作的方法和步骤,掌握实验数据的分析和处理方法。
2019年高考理科综合能力测试化学卷(全国课标Ⅰ卷)分析报告 pdf
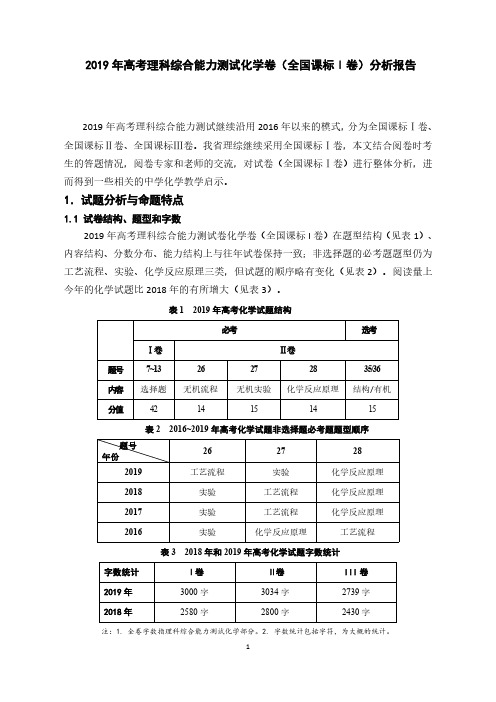
1.1 试卷结构、题型和字数 2019 年高考理科综合能力测试卷化学卷(全国课标 I 卷)在题型结构(见表 1)、
内容结构、分数分布、能力结构上与往年试卷保持一致;非选择题的必考题题型仍为 工艺流程、实验、化学反应原理三类,但试题的顺序略有变化(见表 2)。阅读量上 今年的化学试题比 2018 年的有所增大(见表 3)。
查学生对冰和 HCl 微观结构的探析。第 13 题通过新化合物
的结构,
考查学生基于原子结构和价健知识认识物质世界的能力:从结构图中“W+”推出 W 是
Li 或 Na,X 可能是 C 或 Si(形成四个共价键),Z 可能是 H 或 F 或 Cl(能形成一个
共价键),结合题干信息“Z 核外最外层电子数是 X 核外电子数的一半”得出 X 是 Si、
C
B
A
35)
杂化轨道理论、配合物
4
晶体类型及结构微粒间作用力;金
B
35(3)(4)
刚石晶胞及相关计算
3+6
有机物的结构和 命名 研究有机化合物 选 的一般方法 修 烃和卤代烃 5
烃的含氧衍生物
C
8C,36(1)(2)(3) 共面共线;官能团的名称;手性碳; 6*+1+2+
同分异构体
3
A
A
36(5)(7)
烃的溴代反应条件和反应类型
1+1*
含氧官能团的名称,醛基的性质,
C 36(1)(3)(4)(6) 酯化反应所需条件与试剂,酯的水 1*+3*+2
解反应
+2
3
续表 4:
考纲要求
2019 年考查知识及赋分
高考全国新课标Ⅰ卷化学试题评价与解析(共57张PPT)资料精选课件

新课标Ⅰ高考化学试卷评析
选做题部分 选做题中,选修三的37题,物质结构与性质 比去年难度有所降低。选修五的38题有机化学基 础,与去年类似,属于给出信息进行推断的题目 在试题设计中除了每年必考的反应类型、结 构简式、化学方程式的书写以及同分异构外,还 对反应条件进行了重点考查。
下面我把整套试题具体分析如下:
题目形式新颖,但实际上难度在降低, 再次体现回归基础。
高考试题分析之必做题
28.乙醇是重要的有机化工原料,可由乙烯气相直接水
合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢
乙酯 (C2H5OSO3H),再水解生成乙醇。写出相应反应的
【解析】 浓硫酸可使蔗糖碳化,并放出大量的热,
体现浓硫酸的脱水性,生成的碳继续与浓硫酸反应生成 SO2,使③中的溴水褪色,通过蔗糖变黑、溴水褪色可 以得出浓硫酸具有脱水性、氧化性, B正确,
高考试题分析之选择
点评:第13题以基础实验为切入点, 考查了元素化合物部分的知识。
四个选项中所涉及的知识均在历年高 考试题中出现过。
C.草木灰的有效成分K2CO3 水解显碱性, 而NH4Cl水解显酸性,二者混合使用会使水 解相互促进,产生氨气逸出而降低肥效
高考试题分析之选择
点评:第8题考查生活中的化学知识, 意在考查考生利用所学知识解决实际问题 的能力。知识来源于盐类的水解和氧化还 原反应部分。纯碱去油污,漂白粉变质、 铵态氮肥和草木灰不能混合使用,氯化铁 和铜线路板反应等等,这些知识都来源于 教材,难度小。
高考试题分析之必做题
(3)(H3PO2)的工业制法是:将白磷(P4)与Ba(OH)2溶 液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应。写出白磷与Ba(OH)2溶液反应的化学方程式 。
2019年全国高考I卷理综(化学)试题及答案

(5)⑤的反应类型是__________。
(6)写出F到G的反应方程式__________。
(7)设计由甲苯和乙酰乙酸乙酯(CH3COCH2COOC2H5)制备 的合成路线__________(无机试剂任选)。
化学部分解析
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127
D项、2-苯基丙烯为烃类,分子中不含羟基、羧基等亲水基团,,难溶于水,易溶于有机溶剂,则2-苯基丙烯难溶于水,易溶于有机溶剂甲苯,故D错误。
故选B。
【点睛】本题考查有机物的结构与性质,侧重分析与应用能力的考查,注意把握有机物的结构,掌握各类反应的特点,并会根据物质分子结构特点进行判断是解答关键。
3.实验室制备溴苯的反应装置如下图所示,关于实验操作或பைடு நூலகம்述错误的是
回答下列问题:
(1)在95℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
故选A。
【点睛】本题考查物质 性质,侧重分析与应用能力的考查,注意化学与生活的联系,把握物质性质、反应与用途为解答的关键。
2.关于化合物2−苯基丙烯( ),下列说法正确的是
2019高考全国Ⅰ卷化学试题解析版

2019年普通高等学校招生全国统一考试(全国卷I)化学试题一、选择题:本题共7个小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系,下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由粘土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀,抗氧化等优点【答案】A【解析】A 项氧化铁即三氧化二铁,红棕色。
瓷器青色一般不来自氧化铁。
故A错。
8.关于化合物2-苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯【答案】B【解析】分子中存在双键,可以使高锰酸钾溶液褪色,A错;可以发生加成聚合反应,B正确;分子中存在甲基,所有原子不可能共平面,C错;分子中碳原子数较多,且不存在亲水基团所以不易溶于水,D错。
9.实验室制溴苯的装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中Na2CO3的作用是吸收HBrD.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯。
【答案】D。
【解析】溴苯常温下为液体,反应后的混合液经稀碱溶液洗涤、分液,得到无色的溴苯。
10.固体界面上强酸的吸附和离解是多向化学在环境、催化、材料科学等领域研究的重要课题。
下图为为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图,下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10-3mol·L-1(设冰的密度为0.9g·cm-3)C.冰表面第三层中冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl-【答案】D。
2019年高考全国I卷理综化学化工流程图试题说题及解题模型

节日PPT模板:/jieri/ PPT素材下载:/sucai/
PPT背景图片:/beijing/ PPT图表下载:/tubiao/
优秀PPT下载:/xiazai/ PPT教程: /powerpoint/
一种以硼镁矿(含 Mg2B2O5 H2O 、 SiO2 及少量 Fe问2O3题、3A:l2O为3 )什为么原温料度生控产制硼在酸9及5℃轻质?
氧化镁的工艺流程如下:
问题4:如何书写该反应的离子方程式?
硫酸铵与硼镁矿的反应在微沸条件下进行问,题一5:方该面反可应加的快平反衡应常速数度是,多另少一? 方面可将反应过程中逸出的氨回收,H2形CO成3 氨4.2水×。1反0-7应(K温1)度过5.6高×,10虽-11能(K2) 加速反应,但反应体系中水分蒸发过NH快3•,H2导O致反1.7应8×后1期0-反5 应物料增稠,反 应速度降低,反应不完全; 反应温度过低,会导致反应速度减缓,延长反
硼酸( H3BO3 )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。
一种以硼镁矿(含 Mg2B2O5 H2O 、 SiO2 及少量 Fe2O3 、 Al2O3 )为原料生产硼酸及轻质
氧化镁的工艺流问程如题下11::碱式碳酸镁过滤后的母液主要成分为硫酸铵以及部分 碳化氨水,工业上常加入生石灰处理,请分析该操作的目的。
回答下列问题:
问题9:从结构角度解释硼酸奇怪的电离方式? 类似的电离方式还有哪些物质?
(3)根据 H3BO3 的解离反应: H3BO3 H2O H+ B(OH)4 , Ka 5.811010 ,可
判断
H BO 20:48 33
是
酸;在“过滤 2”前,将溶液 pH 调节至 3.5,目的是
。
26.(14 分) 问题10:根据碳化氨水的成分写出正确的沉镁反应离子方程式
2019北京高考化学试卷(含答案和解析)

2019北京高考化学试卷学校:___________姓名:___________班级:___________考号:___________一、单选题1.下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是A.A B.B C.C D.D2.下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)电解CuCl2溶液CH3COOH在水中电离NaCl溶于水H2与Cl2反应能量变化H2(g)+Cl2(g) 2HCl(g) NaCl Na++Cl−CuCl2Cu2++2Cl−ΔH=−183kJ·mol−13.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。
中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
铟与铷(37Rb)同周期。
下列说法不正确的是A.In是第五周期第ⅢA族元素B.11549In的中子数与电子数的差值为17C.原子半径:In>AlD.碱性:In(OH)3>RbOH4.交联聚合物P的结构片段如图所示。
下列说法不正确的是(图中表示链延长)A.聚合物P中有酯基,能水解B.聚合物P的合成反应为缩聚反应C.聚合物P的原料之一丙三醇可由油脂水解获得D.邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构5.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是A.A B.B C.C D.D6.探究草酸(H2C2O4)性质,进行如下实验。
(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)由上述实验所得草酸性质所对应的方程式不正确的是A.H2C2O4有酸性,Ca(OH)2+ H2C2O4CaC2O4↓+2H2OB.酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4NaHC2O4+CO2↑+H2OC.H2C2O4具有还原性,24MnO-+5224C O-+16H+2Mn2++10CO2↑+ 8H2OD.H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OHV垐垐?噲垐?浓硫酸C2H5OOCCOOC2H5+2H2O7.实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。
2019全国I卷 高考理科综合化学试题(含解析)

2019年普通高等学校招生全国统一考试(全国I)理科综合化学可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 1277.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是()A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2−苯基丙烯(),下列说法正确的是()A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是()A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是()A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)C.冰表面第三层中,冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl−11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的K a1=1.1×10−3 ,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是()A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
2019年高考理综化学试题、解析、答案及湖北省评分细则

19年高考理综化学试题、解析、答案及湖北省评分细则 (19全国理综I ,T6)下列各组离子,在溶液中能大量共存、加入NaOH 溶液后加热既有气体放出又有沉淀生成的一组是 A .Ba 2+、NO 3-、NH 4+、Cl - B .Ca 2+、HCO 3-、NH 4+、AlO 2-C .K +、Ba 2+、Cl -、HSO 3-D .Mg 2+、NH 4+、SO 42-、K +【解析】D A 项,加入N a O H 会与N 产生N H 3,但没有沉淀;B 项H C(19全国理综I ,T7)将15 mL 2 mol·L -1 Na 2CO 3溶液逐滴加入到41 mL 1.5 mol·L -1 MCl n 盐溶液中,恰好将溶液中的M n+离子完全沉淀为碳酸盐,则MCl n 中n 值是A .4B .3C .2D .1【解析】B M 的化合价为+n ,Na 2CO 3与MCln 反应对应的关系式为:2M n+ ~ nCO 32 - 2 n15×11-3×2 41×11-3×1.5 可得n=3,故选B 。
(19全国理综I ,T8)下列表示溶液中发生反应的化学方程式错误..的是 A .2Al +2NaOH +2H 2O =2NaAlO 2+3H 2↑B .KMnO 4+HCOOK +KOH =2K 2MnO 4+CO 2↑+H 2OC .MnO 2+4HCl(浓)MnCl 2+Cl 2↑+2H 2O D .K 2Cr 2O 7+6FeSO 4+7H 2SO 4=Cr 2(SO 4)3+3Fe 2(SO 4)3+K 2SO 4+7H 2O【解析】B 在碱性条件下,不可能产生CO 2气体,而应是CO 32 -,故B 项错。
(19全国理综I ,T9)现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a ,则碳的质量分数是A .7)1(a — B .43a C .76(1-a ) D .1312(1-a ) 【解析】C 乙酸的化学式为C 2H 4O 2,而单烯烃的通式为C n H 2n ,从化学式可以发现两者中,C 与H 之间的数目比为1:2,质量比为6:1,碳氢的质量分数一共为1-a,其中碳占76(1-a)。
2019年高考理综全国卷1-答案

2019年普通高等学校招生全国统一考试·全国I卷理综答案解析第Ⅰ卷一、选择题1.【答案】B【解析】胎儿手发育的过程中,手指间隙的细胞会发生细胞凋亡,A错误;小肠上皮细胞中衰老的细胞将会发生细胞凋亡,不断完成细胞的自然更新,B正确;被病原体感染的细胞属于靶细胞,机体通过细胞免疫将靶细胞裂解死亡,释放抗原,属于细胞凋亡,C错误;细胞凋亡是由基因所决定的细胞自动结束生命的过程,细胞坏死是在种种不利因素的影响下导致的细胞非正常死亡,D错误。
故选B。
【考点】细胞凋亡和细胞坏死的概念和实例【考查能力】理解能力2.【答案】C【解析】翻译的原料是氨基酸,要想让多肽链带上放射性标记,应该用同位素标记的氨基酸(苯丙氨酸)作为原料,而不是同位素标记的tRNA,①错误、③正确;合成蛋白质需要模板,由题知苯丙氨酸的密码子是UUU,因此可以用人工合成的多聚尿嘧啶核苷酸作模板,同时要除去细胞中原有核酸的干扰,④、⑤正确;除去了DNA和mRNA的细胞裂解液模拟了细胞中的真实环境,其中含有核糖体、催化多肽链合成的酶等,因此不需要再加入蛋白质合成所需的酶,故②错误。
综上所述,ABD不符合题意,C符合题意。
故选C。
【考点】翻译所需的条件【考查能力】理解能力3.【答案】A【解析】黄瓜幼苗可以吸收水,增加鲜重;也可以从土壤中吸收矿质元素,合成相关的化合物。
也可以利用大气中二氧化碳进行光合作用制造有机物增加细胞干重。
植物光合作用将光能转化成了有机物中的化学能,并没有增加黄瓜幼苗的质量,故黄瓜幼苗在光照下增加的质量来自于水、矿质元素、空气。
综上所述,BCD不符合题意,A符合题意。
故选A。
【考点】植物生长过程中的物质变化【考查能力】理解能力4.【答案】D【解析】兴奋在神经纤维上以电信号的形式传导,在突触部位以电信号-化学信号-电信号的形式传递,A 正确;惊吓刺激可以通过图像、声音、接触等刺激作用于视觉、听觉或触觉感受器,B正确;由题中信息:兴奋经过反射弧中的传出神经作用于肾上腺髓质,使其分泌肾上腺素,从而加快心跳,说明神经系统可通过内分泌活动间接调节心脏活动。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2019年高考理科综合(全国I卷)化学试题标准答案与阅卷评分细则硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。
一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如图所示:(1)在“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为。
标准答案:NH4HCO3+NH3===(NH4)2CO3 或(2分)NH 4HCO 3+2NH 3+H 2O===(NH 4)2CO 3+NH 3·H 2O评分细则: b.(1)平均分0.77a. 写成两步反应也可以, 但只写其中一步不给分;(2)“滤渣1”的主要成分有。
为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是。
标准答案:SiO2,Fe2O3,Al2O3 (3分)KSCN (1分)评分细则:a.写SiO2或SiO2、Fe2O3或SiO2、Al2O3均给2分;(2)平均分1.99Fe2O3,Al2O3给1分;只写这俩其中一个不给分; 只要有错的就不给分。
b.KSCN 或硫氰酸钾、硫氰化钾、亚铁氰酸钾、K4[Fe(CN)6]、K4Fe(CN)6、苯酚、NaOH、KOH均可凡错别字不给分(3)根据的解离反应:,可判断H3BO3是酸;在“过滤2”前,将溶液调节至3.5,目的是。
标准答案:一元弱(2分)转化为H3BO3,促进析出(2分)评分细则:a.只答“一元”或“弱”或“非氧化性弱”得1分。
b.答:促进H3BO3生成或者促进转化为H3BO3,或者抑制H3BO3解离,也得2分。
以下不给分:富集H3BO3;使H3BO3沉淀完全;有利于H3BO3的分离;得到纯净的H3BO3;(3)平均分1.56(4)在"沉镁"中生成沉淀的离子方程式为,母液经加热后可返回工序循环使用。
由碱式碳酸镁制备轻质氧化镁的方法是。
标准答案:2Mg2+ + 3CO32- + 2H2O === Mg(OH)2·MgCO3↓+2HCO3(2分)2Mg2+ + 2CO32- + H2O === Mg(OH)2·MgCO3 + CO2↑ 评分细则:a.写成2Mg2+ + 2CO32- + 2H2O===Mg(OH)2·MgCO3↓+H2CO3也给分;但这样不给分:2Mg2+ + 2CO32- + 2H2O===Mg(OH)2·MgCO3↓+H2O+CO2b.“==”“可逆号”“→”不扣分;“↓”“↑”不扣分;反应物产物错误,不配平0分。
标准答案:溶浸(1分)高温焙烧(1分)评分 c.错别字不给分;细则d.以下情况也得分::灼烧、煅烧、焙烧、高温加热、加热分解、蒸干灼烧/加热、热分解法、加热沉淀、写方程式在CO2/NH3/N2/O2空气中加热(在无影响的气体氛围加热给分)以下情况不得分:在碱浸/酸浸泡/HCl气流中加热、熔融加热、烘焙、灼热、高温氧化、溶解灼烧、热失重法、分解法、蒸馏、干馏(4)平均分1.667硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。
为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:(1)步骤①的目的是去除废铁屑表面的油污,方法是。
标准答案:碱煮水洗(2分)评分细则:得分:出现碱性物质即可得分。
比如Na2CO3、NaHCO3、NaOH等都可,肥皂水也可以。
不得分:出现洗洁精、洗衣液等,碱是固体如碱石灰体现不出水洗。
(1)平均分1.36(2)步骤②需要加热的目的是,温度保持80~95 ℃ ,采用的合适加热方式是。
铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为(填标号)。
标准答案:加快反应/提高反应速率(1分)评分细则:得分:体现反应速率加快即可不得分:有利于反应进行标准答案:热水浴/水浴加热(1分)评分细则:得分:有水浴就得分不得分:水浴关键字错误,沸水浴标准答案:C (2分)评分细则:答案唯一(2)平均分3.12 (3)步骤③中选用足量的H2O2,理由是。
分批加入H2O2,同时为了,溶液要保持pH小于0.5。
标准答案:将Fe2+氧化成Fe3+(1分),不引入杂质(1分)评分细则:得分:体现是将Fe2+氧化成Fe3+得1分,例如将Fe2+/铁元素氧化生成Fe3+,使溶液变为Fe2(SO4)3溶液。
体现不引入杂质的得1分。
如:对本实验无影响H2O2易除去,产物无污染不得分:表述错误:将Fe2+还原成Fe3+,将铁单质/Fe 氧化,将Fe3+氧化成Fe2+;H2O2绿色无污染,不污染环境,H2O2易分解(3)步骤③中选用足量的H2O2,理由是。
分批加入H2O2,同时为了,溶液要保持pH小于0.5。
标准答案:防止Fe3+/铁离子水解/防止Fe(OH)3沉淀生成(2分)评分细则:得分:防止Fe3+沉淀,防止Fe2(SO4)3水解沉淀不得分:没有防止及类似词(抑制/减少/减弱)没有明确出Fe3+(写Fe2+/铁元素等)(3)平均分1.57(4)步骤⑤的具体实验操作有,经干燥得到硫酸铁铵晶体样品。
标准答案:加热浓缩/蒸发浓缩冷却(降温)结晶/过滤(洗涤)(3分)评分细则:得分:第一步写成浓缩蒸发也可,每对一空得1分不得分:错别字不得分(4)平均分1.98 (5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。
硫酸铁铵晶体的化学式为。
标准答案:NH4Fe(SO4)2·12H2O (2分)评分细则:得分:整个式子加中括号,(NH4),中间·没有不得分:NH4Fe(SO4)2下标错误或在其他地方点点(5)平均分0.22分水煤气变换是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中,回答下列问题:(1)Shibata曾做过下列实验:①使纯缓慢地通过处于下的过量氧化钴,氧化钴部分被还原为金属钴,平衡后气体中的物质的量分数为0.0250。
②在同一温度下用还原,平衡后气体中的物质的量分数为0.0192。
(1)根据上述实验结果判断,还原为的倾向是(填“大于” 或“小于”)。
标准答案:大于(2分)评分细则:必须写汉字“大于”,写成“>”不给分(2)时,在密闭容器中将等物质的量的和混合,采用适当的催化剂进行反应,则平衡时体系中的物质的量分数为(填标号)。
A. <0.25B. 0.25C. 0.25-0.50D.0.50E. >0.50标准答案:C (2分)(1)(2)平均分2.57分评分细则:选C,答案唯一(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
可知水煤气变换的0(填“大于”“等于”或“小于”)。
该历程中最大能垒(活化能),写出该步骤的化学方程式。
标准答案:小于(1分) 2.02 (2分)评分细则:a.写汉字“小于”,写成“<”不给分;b.答案唯一标准答案:(2分)评分细则:相对看得松,除了答案上的两种,还可以*号不写、或部分写给分;写成-COOH •COOH 这种形式的也分(3)平均给分;连接符号不管;或者是方程式部分约给分,比1.62分如:COOH+H2O===COOH+H +OH H+H2O=2H+OH;写了两个不同形式对的方程式给分。
以下情况不给分:物质后注明状态的;没配平的;写了两个方程式,其中一个对,一个错;往上加物质的;物质上带上正负电荷的等(4)Shoichi研究了467℃、489℃时水煤气变换中和分压随时间变化关系(如图所示),催化剂为氧化铁,实验初始时体系中的p H2O和p CO相等、p CO2和p H2相等。
和p C O 随时间变化关系的曲线分别是、。
489℃时p H2和p C O随时间变化关系的曲线分别是、。
计算曲线a的反应在30-90min内的平均速率。
467℃时p H2标准答案:每空1分,共5分评分细则:a.速率数值看得松,得分:0.0047、0.004667、0.28/60、15/1400、30/2800 、0.014/3、4.7×10-3 、0.47×10-2 、4.667×10-3、0.0046上面写点表示循环、带上单位给分不得分:0.0046、0.00476、0.047、0.000467,分数比值不对等b.后面四个字母,答案唯一,除c,其他写成大写不给分,因为答题纸上不显示横线,必须写对位置并答对才给分。
(4)平均分1.4分化合物G是一种药物合成中间体,其合成路线如下:(1)A中的官能团名称是。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。
写出B的结构简式,用星号(*)标出B中的手性碳。
标准答案:羟基(1分)(2分)评分细则:(1)正确得1分,错答/多答不给分,写成-OH不给分。
(2)a.结构简式错误直接0分;b.写成结构式或结构简式皆对 c.只标一个手性碳且正确得1分 d.只要有标错的,0分。
(3)写出具有六元环结构、并能发生银镜反应的B的同分异构体的结构简式。
(不考虑立体异构,只需写出3个)标准答案:(3分)评分细则:a.每对一个得1分,超过3个,以前三个为准b.写成结构式或结构简式皆对(4)反应所需的试剂和条件是。
标准答案:C2H5OH/浓H2SO4,加热(2分)评分细则:a.试剂及条件各1分b.试剂不全或多答不得分,试剂写成中文或分子式都可以,加热可以用“△”表示。
(3)(4)平均分1.47分(5)反应⑤的反应类型是。
标准答案:取代反应(1分)评分细则:a.正确得1分,错答/多答不给分不写“反应”二字不扣(6)写出F到G的反应方程式。
标准答案:(2分)评分细则:a.每个方程式1分,反应物/生成物漏写或写错不得分b.两个方程式合并写并写对的,得2分,错的0分。
(5)(6)平均分0.72分(7)设计由甲苯和乙酰乙酸乙酯(4分)的合成路线标准答案:评分细则:两步路线,a.第一步2分;第二步2分b.第一步条件可以写Cl或Br;(7)平均分1.48分c.第一步条件1分,反应物和生成物1分d.第二步每个先水解再取代0分。
在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。
回答下列问题:(1)下列状态的镁中,电离最外层一个电子所需能量最大的是(填标号)。
标准答案:A (2分)评分细则:正确得2分,错答或多选不得分。
(2)乙二胺()是一种有机化合物,分子中氮、碳的杂化类型分别是、。
乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是,其中与乙二胺形成的化合物稳定性相对较高的是(填“Mg2+”或“Cu2+”)。
