热学试题(2)
北京工业大学传热学II真题及答案

将②式代入①式有: A[
解得:
d (t ) dt d 2t . (t ) 2 0 即为其微分方程。 dx dx dx
共 5 页第 2 页
易水制作,版权所有,盗版必究
6
权威北京工业大学传热学II、 工程热力学考研真题资料, 订购热线 QQ:1084688581
科目代码: 851 其导热微分方程为: 1 解得: t C1Inr C2 又由其边界条件有:
二.计算题(每题 10 分,共 70 分) 1.试推导有均匀分布内热源(强度为Ф,单位为 w/m ),变导数系 数的无限大平壁稳态导热的导热微分方程。 2.圆管壁外半径 r0,内半径 ri,外表面与内表面的温度分别是 t0 和 ti(t0 大于 ti) ,λ为常数,试导出其温度分布的表达式。
3
共 2 页第 1 页
共 2 页第 2 页
易水制作,版权所有,盗版必究
4
权威北京工业大学传热学II、 工程热力学考研真题资料, 订购热线 QQ:108468入学考试试题参考答案
科目代码: 851 科目名称: 传热学 II 一.简答题 1.解:设圆管的长度为 L,圆管的内径为 d1,外径为 d0,管内流体温度 为 t1,管外流体温度为 t2,管内外对流系数分别为 h1 和 h2。 则散热量 t1 t 2 L (t1 t 2 )
Adx 内热源生产热量:
dt d x dx ,导出热量: x dx x dx dx
Adx xdx 即 由能量守恒有: x
d x Adx dx dx
① ②
d 其中 x dx
d [ (t ) A
dt ] 2 dx A[ d (t ) . dt (t ) d t ] dx dx dx dx 2 d (t ) dt d 2t Adx . (t ) 2 ] dx dx dx
传热学试题库含参考答案(2)

传热学试题库含参考答案(2)《传热学》试题库第⼀章概论⼀、名词解释1.热流量:单位时间内所传递的热量2.热流密度:单位传热⾯上的热流量3.导热:当物体内有温度差或两个不同温度的物体接触时,在物体各部分之间不发⽣相对位移的情况下,物质微粒(分⼦、原⼦或⾃由电⼦)的热运动传递了热量,这种现象被称为热传导,简称导热。
4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合⽤的热量传递过程,称为表⾯对流传热,简称对流传热。
5.辐射传热:物体不断向周围空间发出热辐射能,并被周围物体吸收。
同时,物体也不断接收周围物体辐射给它的热能。
这样,物体发出和接收过程的综合结果产⽣了物体间通过热辐射⽽进⾏的热量传递,称为表⾯辐射传热,简称辐射传热。
6.总传热过程:热量从温度较⾼的流体经过固体壁传递给另⼀侧温度较低流体的过程,称为总传热过程,简称传热过程。
7.对流传热系数:单位时间内单位传热⾯当流体温度与壁⾯温度差为1K是的对流传热量,单位为W/(m2·K)。
对流传热系数表⽰对流传热能⼒的⼤⼩。
8.辐射传热系数:单位时间内单位传热⾯当流体温度与壁⾯温度差为1K是的辐射传热量,单位为W/(m2·K)。
辐射传热系数表⽰辐射传热能⼒的⼤⼩。
9.复合传热系数:单位时间内单位传热⾯当流体温度与壁⾯温度差为1K是的复合传热量,单位为W/(m2·K)。
复合传热系数表⽰复合传热能⼒的⼤⼩。
10.总传热系数:总传热过程中热量传递能⼒的⼤⼩。
数值上表⽰传热温差为1K时,单位传热⾯积在单位时间内的传热量。
四、简答题1.试述三种热量传递基本⽅式的差别,并各举1~2个实际例⼦说明。
(提⽰:从三种热量传递基本⽅式的定义及特点来区分这三种热传递⽅式)2.请说明在传热设备中,⽔垢、灰垢的存在对传热过程会产⽣什么影响?如何防⽌?(提⽰:从传热过程各个环节的热阻的⾓度,分析⽔垢、灰垢对换热设备传热能⼒与壁⾯的影响情况)3. 试⽐较导热系数、对流传热系数和总传热系数的差别,它们各⾃的单位是什么?(提⽰:写出三个系数的定义并⽐较,单位分别为W/(m·K),W/(m2·K),W/(m2·K))4.在分析传热过程时引⼊热阻的概念有何好处?引⼊热路欧姆定律有何意义?(提⽰:分析热阻与温压的关系,热路图在传热过程分析中的作⽤。
热力学试题二

… (3)
ΔrH m (3) = 247.7 kJ·mol-1 根据上述数据可获得 H—O 键的平均键能 εH—O 约为: ( )
(A) 925.5 kJ·mol-1 (B) 462.8 kJ·mol-1 (C) 120.9 kJ·mol-1 (D) 241.8 kJ·mol-1 2 分 (9013) 有一绝热不良的热源(温度为 Tb),缓慢地把热量散失给环境(温度为 Ta),经过相当长时间 后,热源损失了热量Q,而环境得到的热量为Q,计算过程的总熵变。 8. 2 分 (0146) 理想气体从相同始态分别经绝热可逆膨胀和绝热不可逆膨胀到达相同的压力, 则其终态 的温度、体积和体系的焓变必定是: ( ) (A) T 可逆 > T 不可逆,V 可逆 > V 不可逆,ΔH 可逆 > ΔH 不可逆 (B) T 可逆 < T 不可逆,V 可逆 < V 不可逆,ΔH 可逆 < ΔH 不可逆 (C) T 可逆 < T 不可逆,V 可逆 > V 不可逆,ΔH 可逆 < ΔH 不可逆 (D) T 可逆 < T 不可逆,V 可逆 < V 不可逆,ΔH 可逆 > ΔH 不可逆 9. ( 2 分 (0939) 在 300℃时,2 mol 某理想气体的吉布斯自由能 G 与赫姆霍兹自由能 F 的差值为: ) (A) G-F=1.247 kJ (B) G-F=2.494 kJ (C) G-F=4.988 kJ (D) G-F=9.977 kJ 7.
热力学二
试卷
( )
一、选择题 ( 共 15 题 30 分 ) 1. 2 分 (9032) 在标准压力 p和 268.15 K 下,冰变为水,体系的熵变ΔS 体应: (A) 大于零 (B) 小于零 (C) 等于零 (D) 无法确定 2. 2 分 (0486) ( ) Cl2(g)的燃烧热为何值? (A) HCl(g)的生成热 (B) HClO3 的生成热 (C) HClO4 的生成热 (D) Cl2(g)生成盐酸水溶液的热效应
化学热力学试题及答案

化学热力学试题及答案一、选择题(每题2分,共20分)1. 下列哪种物质在标准状态下不是气体?A. 水B. 氧气C. 氮气D. 氢气答案:A2. 化学热力学中,系统与环境之间能量交换的主要方式是:A. 热能B. 电能C. 光能D. 机械能答案:A3. 根据热力学第一定律,下列哪种情况描述正确?A. 能量守恒B. 能量可以创造C. 能量可以消失D. 能量可以转化为质量答案:A4. 熵是热力学中描述系统无序程度的物理量,下列哪种情况下系统的熵会增加?A. 液体凝固成固体B. 气体压缩成液体C. 固体溶解于液体D. 气体扩散到真空答案:D5. 吉布斯自由能(G)是描述化学反应自发性的一个物理量,其表达式为:A. G = H - TΔSB. G = H - TSC. G = ΔH - TΔSD. G = ΔH + TΔS答案:C二、填空题(每题2分,共20分)1. 热力学第二定律指出,不可能从单一热源_______热能并使之完全转化为_______而产生其他影响。
答案:吸取;机械功2. 绝对零度是温度的下限,其值为_______开尔文。
答案:03. 一个化学反应在恒温恒压下进行,如果反应的吉布斯自由能变化(ΔG)小于零,则该反应是_______的。
答案:自发4. 理想气体状态方程为PV=nRT,其中P代表_______,V代表_______,n代表_______,R代表_______,T代表_______。
答案:压强;体积;摩尔数;气体常数;温度5. 根据热力学第三定律,当温度趋近于绝对零度时,系统的熵趋近于_______。
答案:零三、简答题(每题10分,共30分)1. 简述热力学第一定律的内容及其物理意义。
答案:热力学第一定律,也称为能量守恒定律,表明能量既不能被创造也不能被消灭,只能从一种形式转化为另一种形式。
在任何封闭系统中,能量的总和在任何物理或化学过程中都是恒定的。
其物理意义在于,它为能量转换和守恒提供了一个基本的科学原则。
大学物理热学试题题库及答案

大学物理热学试题题库及答案一、选择题:(每题3分)1、在一密闭容器中,储有A、B、C三种理想气体,处于平衡状态.A种气体的分子数密度为n1,它产生的压强为p1,B种气体的分子数密度为2n1,C种气体的分子数密度为3n1,则混合气体的压强p为(A) 3 p1.(B) 4 p1.(C) 5 p1.(D) 6 p1.[]2、若理想气体的体积为V,压强为p,温度为T,一个分子的质量为m,k为玻尔兹曼常量,R为普适气体常量,则该理想气体的分子数为:(A) pV / m.(B) pV / (kT).(C) pV / (RT).(D) pV / (mT).[]3、有一截面均匀的封闭圆筒,中间被一光滑的活塞分隔成两边,如果其中的一边装有0.1 kg 某一温度的氢气,为了使活塞停留在圆筒的正中央,则另一边应装入同一温度的氧气的质量为:(A) (1/16) kg.(B) 0.8 kg.(C) 1.6 kg.(D) 3.2 kg.[]4、在标准状态下,任何理想气体在1 m3中含有的分子数都等于(A) 6.02×1023.(B)6.02×1021.(C) 2.69×1025(D)2.69×1023.(玻尔兹曼常量k=1.38×10-23 J·K-1 ) []5、一定量某理想气体按pV2=恒量的规律膨胀,则膨胀后理想气体的温度(A) 将升高.(B) 将降低.(C) 不变.(D)升高还是降低,不能确定.[]6、一个容器内贮有1摩尔氢气和1摩尔氦气,若两种气体各自对器壁产生的压强分别为p1和p2,则两者的大小关系是:(A) p1> p2.(B) p1< p2.(C) p1=p2.(D)不确定的.[]7、已知氢气与氧气的温度相同,请判断下列说法哪个正确?(A) 氧分子的质量比氢分子大,所以氧气的压强一定大于氢气的压强.(B) 氧分子的质量比氢分子大,所以氧气的密度一定大于氢气的密度.(C) 氧分子的质量比氢分子大,所以氢分子的速率一定比氧分子的速率大.(D) 氧分子的质量比氢分子大,所以氢分子的方均根速率一定比氧分子的方均根速率大.[]8、已知氢气与氧气的温度相同,请判断下列说法哪个正确?(A) 氧分子的质量比氢分子大,所以氧气的压强一定大于氢气的压强.(B) 氧分子的质量比氢分子大,所以氧气的密度一定大于氢气的密度.(C) 氧分子的质量比氢分子大,所以氢分子的速率一定比氧分子的速率大.(D) 氧分子的质量比氢分子大,所以氢分子的方均根速率一定比氧分子的方均根速率大. [ ]9、温度、压强相同的氦气和氧气,它们分子的平均动能ε和平均平动动能w 有如下关系:(A) ε和w 都相等. (B) ε相等,而w 不相等.(C) w 相等,而ε不相等. (D) ε和w 都不相等. [ ]10、1 mol 刚性双原子分子理想气体,当温度为T 时,其内能为(A) RT 23. (B)kT 23. (C)RT 25. (D)kT 25. [ ] (式中R 为普适气体常量,k 为玻尔兹曼常量)11、两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内的气体质量ρ,分别有如下关系:(A) n 不同,(E K /V )不同,ρ 不同.(B) n 不同,(E K /V )不同,ρ 相同.(C) n 相同,(E K /V )相同,ρ 不同.(D) n 相同,(E K /V )相同,ρ 相同. [ ]12、有容积不同的A 、B 两个容器,A 中装有单原子分子理想气体,B 中装有双原子分子理想气体,若两种气体的压强相同,那么,这两种气体的单位体积的内能(E / V )A 和(E / V )B 的关系(A) 为(E / V )A <(E / V )B .(B) 为(E / V )A >(E / V )B .(C) 为(E / V )A =(E / V )B .(D) 不能确定. [ ]13、两个相同的容器,一个盛氢气,一个盛氦气(均视为刚性分子理想气体),开始时它们的压强和温度都相等,现将6 J 热量传给氦气,使之升高到一定温度.若使氢气也升高同样温度,则应向氢气传递热量(A) 12 J . (B) 10 J(C) 6 J . (D) 5 J . [ ]14、压强为p 、体积为V 的氢气(视为刚性分子理想气体)的内能为: (A)25pV . (B) 23pV . (C) pV . (D) 21pV . [ ]15、下列各式中哪一式表示气体分子的平均平动动能?(式中M 为气体的质量,m 为气体分子质量,N 为气体分子总数目,n 为气体分子数密度,N A 为阿伏加得罗常量)(A) pV Mm 23. (B) pV M M mol 23. (C)npV 23. (D)pV N M M A 23mol . [ ]16、两容器内分别盛有氢气和氦气,若它们的温度和质量分别相等,则:(A) 两种气体分子的平均平动动能相等.(B) 两种气体分子的平均动能相等.(C) 两种气体分子的平均速率相等.(D) 两种气体的内能相等. [ ]17、一容器内装有N 1个单原子理想气体分子和N 2个刚性双原子理想气体分子,当该系统处在温度为T 的平衡态时,其内能为(A) (N 1+N 2) (23kT +25kT ). (B) 21(N 1+N 2) (23kT +25kT ). (C) N 123kT +N 225kT . (D) N 125kT + N 223kT . [ ]18、设声波通过理想气体的速率正比于气体分子的热运动平均速率,则声波通过具有相同温度的氧气和氢气的速率之比22H O /v v 为(A) 1 . (B) 1/2 .(C) 1/3 . (D) 1/4 . [ ]19、设v 代表气体分子运动的平均速率,p v 代表气体分子运动的最概然速率,2/12)(v 代表气体分子运动的方均根速率.处于平衡状态下理想气体,三种速率关系为(A) p v v v ==2/12)( (B) 2/12)(v v v <=p (C) 2/12)(v v v <<p (D)2/12)(v v v >>p [ ]20、已知一定量的某种理想气体,在温度为T 1与T 2时的分子最概然速率分别为v p 1和v p 2,分子速率分布函数的最大值分别为f (v p 1)和f (v p 2).若T 1>T 2,则(A) v p 1 > v p 2, f (v p 1)> f (v p 2).(B) v p 1 > v p 2, f (v p 1)< f (v p 2).(C) v p 1 < v p 2, f (v p 1)> f (v p 2).(D) v p 1 < v p 2, f (v p 1)< f (v p 2). [ ]21、 两种不同的理想气体,若它们的最概然速率相等,则它们的(A) 平均速率相等,方均根速率相等.(B) 平均速率相等,方均根速率不相等.(C) 平均速率不相等,方均根速率相等.(D) 平均速率不相等,方均根速率不相等. [ ]22、假定氧气的热力学温度提高一倍,氧分子全部离解为氧原子,则这些氧原子的平均速率是原来氧分子平均速率的(A) 4倍. (B) 2倍.(C) 2倍. (D) 21倍. [ ]23、 麦克斯韦速率分布曲线如图所示,图中A 、B 两部分面积相等,则该图表示(A) 0v 为最概然速率. (B) 0v 为平均速率. (C) 0v 为方均根速率. (D) 速率大于和小于0v 的分子数各占一半. [ ]24、速率分布函数f (v )的物理意义为:(A) 具有速率v 的分子占总分子数的百分比.(B) 速率分布在v 附近的单位速率间隔中的分子数占总分子数的百分比.(C) 具有速率v 的分子数.(D) 速率分布在v 附近的单位速率间隔中的分子数. [ ]25、若N 表示分子总数,T 表示气体温度,m 表示气体分子的质量,那么当分子速率v 确定后,决定麦克斯韦速率分布函数f (v )的数值的因素是(A) m ,T . (B) N .(C) N ,m . (D) N ,T .(E) N ,m ,T . [ ]26、气缸内盛有一定量的氢气(可视作理想气体),当温度不变而压强增大一倍时,氢气分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 和λ都增大一倍.(B) Z 和λ都减为原来的一半.(C) Z 增大一倍而λ减为原来的一半.(D) Z 减为原来的一半而λ增大一倍. [ ]27、一定量的理想气体,在温度不变的条件下,当体积增大时,分子的平均碰撞频率Z和平均自由程λ的变化情况是:(A) Z 减小而λ不变. (B)Z 减小而λ增大.f (v )0(C) Z 增大而λ减小. (D)Z 不变而λ增大. [ ]28、一定量的理想气体,在温度不变的条件下,当压强降低时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 和λ都增大. (B) Z 和λ都减小.(C) Z 增大而λ减小. (D) Z 减小而λ增大. [ ]29、一定量的理想气体,在体积不变的条件下,当温度降低时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 减小,但λ不变. (B) Z 不变,但λ减小.(C) Z 和λ都减小. (D) Z 和λ都不变. [ ]30、 一定量的理想气体,在体积不变的条件下,当温度升高时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 增大,λ不变. (B) Z 不变,λ增大.(C) Z 和λ都增大. (D) Z 和λ都不变. [ ]31、 在一个体积不变的容器中,储有一定量的理想气体,温度为T 0时,气体分子的平均速率为0v ,分子平均碰撞次数为0Z ,平均自由程为0λ.当气体温度升高为4T 0时,气体分子的平均速率v ,平均碰撞频率Z 和平均自由程λ分别为:(A) v =40v ,Z =40Z ,λ=40λ.(B) v =20v ,Z =20Z ,λ=0λ.(C) v =20v ,Z =20Z ,λ=40λ.(D) v =40v ,Z =20Z ,λ=0λ. [ ]32、在一封闭容器中盛有1 mol 氦气(视作理想气体),这时分子无规则运动的平均自由程仅决定于(A) 压强p . (B) 体积V .(C) 温度T . (D) 平均碰撞频率Z . [ ]33、一定量的某种理想气体若体积保持不变,则其平均自由程λ和平均碰撞频率Z 与温度的关系是:(A) 温度升高,λ减少而Z 增大.(B) 温度升高,λ增大而Z 减少.(C) 温度升高,λ和Z 均增大.(D) 温度升高,λ保持不变而Z 增大. [ ]34、一容器贮有某种理想气体,其分子平均自由程为0λ,若气体的热力学温度降到原来的一半,但体积不变,分子作用球半径不变,则此时平均自由程为 (A)02λ. (B) 0λ. (C)2/0λ. (D) 0λ/ 2. [ ]35、图(a)、(b)、(c)各表示联接在一起的两个循环过程,其中(c)图是两个半径相等的圆构成的两个循环过程,图(a)和(b)则为半径不等的两个圆.那么:(A) 图(a)总净功为负.图(b)总净功为正.图(c)总净功为零.(B) 图(a)总净功为负.图(b)总净功为负.图(c)总净功为正.(C) 图(a)总净功为负.图(b)总净功为负.图(c)总净功为零.(D) 图(a)总净功为正.图(b)总净功为正.图(c)总净功为负.36、 关于可逆过程和不可逆过程的判断:(1) 可逆热力学过程一定是准静态过程.(2) 准静态过程一定是可逆过程.(3) 不可逆过程就是不能向相反方向进行的过程.(4) 凡有摩擦的过程,一定是不可逆过程.以上四种判断,其中正确的是(A) (1)、(2)、(3).(B) (1)、(2)、(4).(C) (2)、(4).(D) (1)、(4). [ ]37、如图所示,当气缸中的活塞迅速向外移动从而使气体膨胀时,气体所经历的过程(A) 是平衡过程,它能用p ─V 图上的一条曲线表示. (B) 不是平衡过程,但它能用p ─V 图上的一条曲线表示.(C) 不是平衡过程,它不能用p ─V 图上的一条曲线表示.(D) 是平衡过程,但它不能用p ─V 图上的一条曲线表示. [ ]38、在下列各种说法 V 图(a) V 图(b) V 图(c)(1) 平衡过程就是无摩擦力作用的过程.(2) 平衡过程一定是可逆过程.(3) 平衡过程是无限多个连续变化的平衡态的连接.(4) 平衡过程在p-V图上可用一连续曲线表示.中,哪些是正确的?(A) (1)、(2).(B) (3)、(4).(C) (2)、(3)、(4).(D) (1)、(2)、(3)、(4).[]39、设有下列过程:(1) 用活塞缓慢地压缩绝热容器中的理想气体.(设活塞与器壁无摩擦)(2) 用缓慢地旋转的叶片使绝热容器中的水温上升.(3) 一滴墨水在水杯中缓慢弥散开.(4) 一个不受空气阻力及其它摩擦力作用的单摆的摆动.其中是可逆过程的为(A) (1)、(2)、(4).(B) (1)、(2)、(3).(C) (1)、(3)、(4).(D) (1)、(4).[]40、在下列说法(1) 可逆过程一定是平衡过程.(2) 平衡过程一定是可逆的.(3) 不可逆过程一定是非平衡过程.(4) 非平衡过程一定是不可逆的.中,哪些是正确的?(A) (1)、(4).(B) (2)、(3).(C) (1)、(2)、(3)、(4).(D) (1)、(3).[]41、置于容器内的气体,如果气体内各处压强相等,或气体内各处温度相同,则这两种情况下气体的状态(A) 一定都是平衡态.(B) 不一定都是平衡态.(C) 前者一定是平衡态,后者一定不是平衡态.(D) 后者一定是平衡态,前者一定不是平衡态.[]42、气体在状态变化过程中,可以保持体积不变或保持压强不变,这两种过程(A) 一定都是平衡过程.(B) 不一定是平衡过程.(C) 前者是平衡过程,后者不是平衡过程.(D) 后者是平衡过程,前者不是平衡过程.[]43、如图所示,一定量理想气体从体积V 1,膨胀到体积V 2分别经历的过程是:A →B 等压过程,A →C 等温过程;A→D 绝热过程,其中吸热量最多的过程(A) 是A →B.(B)是A →C. (C)是A →D.(D)既是A →B 也是A →C , 两过程吸热一样多。
热力学基础测试题

热力学基础测试题(一)的标准摩尔生成焓的反应是………(1) 表示CO2(2)下列情况中属于封闭体系的是………………………(A) 用水壶烧开水(B)氯气在盛有氯气的密闭绝热容器中燃烧(C) 氢氧化钠与盐酸在烧杯里反(D)反应在密闭容器中进行应(3)下列叙述中正确的是………………………(A) 恒压下ΔH=Q p及ΔH=H2-H1。
因为H2和H1均为状态函数,故Qp也为状态函数。
(B) 反应放出的热量不一定是该反应的焓变(C) 某一物质的燃烧焓愈大,其生成焓就愈小(D) 在任何情况下,化学反应的热效应只与化学反应的始态和终态有关,而与反应的途径无关(4) 按通常规定,标准生成焓为零的物质有…………………(A) C(石墨)(B) Br2(g) (C) N2(g)(D) 红磷(p)(5)下列叙述中正确的是………………(A) 由于反应焓变的常用单位是KJ/mol,故下列两个反应的焓变相等:(B) 由于CaCO3的分解是吸热的,故它的生成焓为负值(C) 反应的热效应就是该反应的焓变(D) 石墨的焓不为零(6)CO2(g)的生成焓等于…………………(A) CO2(g)燃烧焓的负值(B) CO(g)的燃烧焓(C) 金刚石的燃烧焓(D) 石墨的燃烧焓(7)由下列数据确定键N-F的键能为…………………………(A) 833.4KJ/mol(B) 277.8 KJ/mol(C) 103.2 KJ/mol(D) 261.9 KJ/mol(8)由下列数据确定水分子中键O-H的键能应为………………………(A) 121KJ/mol(B) 231.3 KJ/mol(C) 464 KJ/mol (D) 589 KJ/mol(9)由下列数据确定 CH4(g)的为…………(A) 211 KJ /mol(B) -74.8KJ/mol(C) 890.3KJ/mol(D) 缺条件,无法算。
(10)已知结晶态硅和无定形硅(Si)的燃烧热各为-850.6KJ/mol 和-867.3KJ/mol 则由无定形硅转化为结晶态硅的热效应为…………(A) 吸热(B) 放热(C) 16.7KJ/mol(D) 不能判断正确答案:1:(D)、2:(D)、3:(B)、4:(A)、5:(D)6:(D)、7:(B)、8:(C)、9:(B)、10:(B)热力学基础测试题(二)(1) 由下列数据确定 NH4Cl(s)溶解成NH4Cl(aq)的热效应应为(A) -6.1KJ/mol (B) +6.1 KJ/mol(C) -108.8 KJ/mol(D) +108.8 KJ/mol(2) 下列叙述中肯定正确的是………………………(A) 由于熵是体系内部微粒混乱程度的量度,所以盐从饱和溶液中结晶析出的过程总是个熵减过程。
大学热学试题题库及答案

大学热学试题题库及答案一、选择题1. 热力学第一定律表明,能量守恒,即能量不能被创造或消灭,只能从一种形式转换为另一种形式。
以下哪项描述正确?A. 能量可以被创造B. 能量可以被消灭C. 能量可以在不同形式间转换D. 能量只能以一种形式存在答案:C2. 在绝热过程中,系统与外界没有热量交换。
以下哪项描述正确?A. 绝热过程中系统的温度不变B. 绝热过程中系统的压力不变C. 绝热过程中系统的温度和压力都不变D. 绝热过程中系统的温度和压力都可能变化答案:D二、填空题1. 理想气体状态方程为__________,其中P表示压强,V表示体积,n 表示摩尔数,R表示气体常数,T表示温度。
答案:PV = nRT2. 根据热力学第二定律,不可能从单一热源吸热使之完全转化为功而不产生其他效果。
该定律的表述是__________。
答案:不可能从单一热源吸热使之完全转化为功而不产生其他效果。
三、简答题1. 简述热力学第二定律的开尔文表述及其意义。
答案:热力学第二定律的开尔文表述是:不可能从单一热源吸热使之完全转化为功而不产生其他效果。
其意义在于指出了自然界中能量转换的方向性和不可逆性,即能量在转换过程中总是伴随着熵增,表明了热机效率的极限。
2. 描述热力学第三定律,并解释其对低温物理研究的意义。
答案:热力学第三定律指出,当温度趋近于绝对零度时,所有纯物质的完美晶体的熵都趋向于一个共同的值。
这一定律对低温物理研究的意义在于,它为低温下物质的熵和热力学性质的研究提供了理论基础,使得科学家能够更准确地预测和控制低温条件下物质的行为。
四、计算题1. 一个理想气体在等压过程中从状态A(P=100kPa, V=0.5m³)变化到状态B(V=1.0m³)。
已知气体常数R=8.314J/(mol·K),摩尔质量M=28g/mol,求气体在该过程中的温度变化。
答案:首先计算气体的摩尔数n,n = PV/RT =(100×10³×0.5)/(8.314×T)。
热学试题及答案
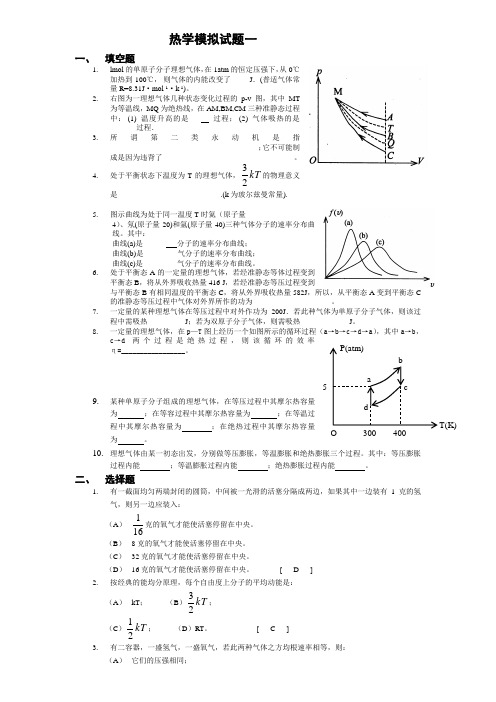
热学模拟试题一一、 填空题1.lmol 的单原子分子理想气体,在1atm 的恒定压强下,从0℃加热到100℃, 则气体的内能改变了_____J .(普适气体常量R=8.31J ·mol -1·k -1)。
2.右图为一理想气体几种状态变化过程的p-v 图,其中MT 为等温线,MQ 为绝热线,在AM,BM,CM 三种准静态过程中: (1) 温度升高的是___ 过程; (2) 气体吸热的是______ 过程. 3.所谓第二类永动机是指 _______________________________________ ;它不可能制成是因为违背了___________________________________。
4.处于平衡状态下温度为T 的理想气体,kT 23的物理意义是 ___________________________.(k 为玻尔兹曼常量).5.图示曲线为处于同一温度T 时氦(原子量 4)、氖(原子量20)和氩(原子量40)三种气体分子的速率分布曲线。
其中:曲线(a)是______ 分子的速率分布曲线; 曲线(b)是_________气分子的速率分布曲线; 曲线(c)是_________气分子的速率分布曲线。
6.处于平衡态A 的一定量的理想气体,若经准静态等体过程变到平衡态B ,将从外界吸收热量416 J ,若经准静态等压过程变到与平衡态B 有相同温度的平衡态C ,将从外界吸收热量582J ,所以,从平衡态A 变到平衡态C 的准静态等压过程中气体对外界所作的功为_____________________。
7. 一定量的某种理想气体在等压过程中对外作功为200J .若此种气体为单原子分子气体,则该过程中需吸热__________J ;若为双原子分子气体,则需吸热_____________J 。
8.一定量的理想气体,在p —T 图上经历一个如图所示的循环过程(a→b→c→d→a),其中a→b,c→d 两个过程是绝热过程,则该循环的效率η=_________________。
热力学基础试题及答案

热力学基础试题及答案一、选择题(每题2分,共20分)1. 热力学第一定律指出能量守恒,下列哪项描述是正确的?A. 能量可以被创造或消灭B. 能量可以从一个物体转移到另一个物体C. 能量可以在封闭系统中增加或减少D. 能量总是从高温物体流向低温物体答案:B2. 熵是热力学中描述系统无序度的物理量,下列哪项描述是正确的?A. 熵是一个状态函数B. 熵是一个过程函数C. 熵只与系统的温度有关D. 熵只与系统的压力有关答案:A3. 理想气体状态方程为PV=nRT,其中P代表压力,V代表体积,n代表摩尔数,R代表气体常数,T代表温度。
下列哪项描述是错误的?A. 理想气体状态方程适用于所有气体B. 在恒定温度下,气体的体积与压力成反比C. 在恒定压力下,气体的体积与温度成正比D. 在恒定体积下,气体的压力与温度成正比答案:A4. 热力学第二定律指出热量不能自发地从低温物体传递到高温物体,下列哪项描述是正确的?A. 热量总是从高温物体流向低温物体B. 热量可以在没有外界影响的情况下从低温物体流向高温物体C. 热量可以在外界做功的情况下从低温物体流向高温物体D. 热量可以在没有外界做功的情况下从低温物体流向高温物体答案:C5. 卡诺循环是理想化的热机循环,其效率只与热源和冷源的温度有关。
下列哪项描述是错误的?A. 卡诺循环的效率与工作介质无关B. 卡诺循环的效率与热源和冷源的温度差有关C. 卡诺循环的效率与热源和冷源的温度成正比D. 卡诺循环的效率在所有循环中是最高的答案:C6. 根据热力学第三定律,下列哪项描述是正确的?A. 绝对零度是可以达到的B. 绝对零度是不可能达到的C. 绝对零度下所有物质的熵为零D. 绝对零度下所有物质的熵为负值答案:B7. 热力学中的吉布斯自由能(G)是用来描述在恒温恒压条件下系统自发进行变化的能力。
下列哪项描述是错误的?A. 吉布斯自由能的变化(ΔG)是负值时,反应自发进行B. 吉布斯自由能的变化(ΔG)是正值时,反应非自发进行C. 吉布斯自由能的变化(ΔG)是零时,系统处于平衡状态D. 吉布斯自由能的变化(ΔG)与系统的温度和压力无关答案:D8. 相变是指物质在不同相态之间的转变,下列哪项描述是错误的?A. 相变过程中物质的化学性质不变B. 相变过程中物质的物理性质会发生变化C. 相变过程中物质的熵值不变D. 相变过程中物质的体积可能会发生变化答案:C9. 热力学中的临界点是指物质的气液两相在该点的物理性质完全相同。
工程热力学试题2

工程热力学试卷(01)一、问答题(每题5分,共25分)1. 在p-v 图及T-s 图上画出空气的n =1.2的膨胀过程1-2和n =1.6的压缩过程1-3,并确定过程1-2和1-3中功和热量的正负号及初终态热力学能的大小。
2. 若分别以某种服从p (v -b)=R g T 的气体(其中b 为物性常数)和理想气体为工质在两个恒温热源和之间进行卡诺循环,试比较哪个循环的热效率大一些,为什么?3. 下面的说法是否正确,为什么? “若从某一初态经不可逆与可逆两条途径到达同一终态,则不可逆途径的ΔS'必大于可逆途径ΔS ”4. 空气在气缸内经历不可逆过程,内能减少12kJ,对外作功10kJ,试分析空气的熵变有哪几种可能性?为什么?5. 提高活塞式内燃机循环热效率的热力学措施有哪些?其热力学依据是什么?二、计算题(共75分)1. 人体热量的消耗率通常为356kJ/h,在作激烈运动时则达628kJ/h 。
在热天皮肤经由汗的蒸发来散热,若汗的蒸发在定压且与皮肤相同温度(27℃)下进行,问运动时多余热量需每小时蒸发多少汗才能排出?(10分)已知:t =26℃: h'=108.95 kJ/kg 、h "=2548.6 kJ/kg ; t =28℃:h'=117.31 kJ/kg 、h "=2552.3 kJ/kg2. 容积V =0.5m 3的空气初压=0.3MPa,初温=150℃,经膨胀过程到终态=0.08MPa,=20℃,求过程中热力学能,焓及熵的变化量。
空气作为理想气体,其比热容可取定值, 气体常数=287J/(kg·K);=1005 J/(kg·K)。
(10分)3. 刚性容器内有2kg,35℃,2MPa 的氮气,向容器内注入适量的氧气,使容器内压力达3MPa,若过程中温度维持不变,求加入氧气的质量。
氧气比热容取定值, 气体常数=260J/(kg·K)、=917J/(kg·K);氮气比热容取定值, 气体常数=297J/(kg·K) ;=1038J/(kg·K)。
热学考试试题

热学考试试题一、选择题(每题2分,共20分)1. 热力学第一定律的数学表达式是:A. ΔU = Q + WB. ΔH = Q + WC. ΔS = Q/TD. ΔG = Q - W2. 在理想气体的等压过程中,气体的内能变化与哪些因素有关?A. 气体的质量B. 气体的温度C. 气体的体积D. 气体的压强3. 下列哪项不是热力学系统的宏观特性?A. 体积B. 温度C. 分子的质量D. 压强4. 根据热力学第二定律,下列哪种说法是正确的?A. 热量可以从低温物体自发地传递到高温物体B. 热量不能从低温物体自发地传递到高温物体C. 所有自发过程都会增加系统的熵D. 系统的熵永远不会减少5. 理想气体的内能只与什么有关?A. 气体的体积B. 气体的温度C. 气体的压强D. 气体的质量6. 在绝热过程中,理想气体的温度和压强之间的关系是:A. T/P = 常数B. T/V = 常数C. T/V^γ = 常数D. T·V^γ = 常数7. 根据热力学第三定律,绝对零度时,所有纯物质的熵:A. 都是零B. 都是无穷大C. 都等于零或一个正值D. 都是负值8. 什么是热力学温标?A. 摄氏温标B. 华氏温标C. 开尔文温标D. 兰氏温标9. 热传导的主要方式包括:A. 导热B. 对流C. 辐射D. 所有以上10. 热机的效率定义为:A. 热机输出的功与输入的热量之比B. 热机输入的热量与输出的功之比C. 热机输出的功与燃料的质量之比D. 热机输入的热量与燃料的质量之比二、填空题(每空1分,共10分)11. 热力学系统的熵是一个______的量,它与系统的______和______有关。
12. 理想气体状态方程为:______。
13. 热力学第二定律表明,不可能从单一热源吸热并把它全部用来做功而不引起其他变化,这是______的一个重要表述。
14. 在一个封闭系统中,如果发生不可逆过程,那么系统的______将______。
高考物理力学知识点之热力学定律基础测试题含答案解析(2)

高考物理力学知识点之热力学定律基础测试题含答案解析(2)一、选择题1.下列说法正确的是()A.物体放出热量,其内能一定减小B.物体对外做功,其内能一定减小C.物体吸收热量,同时对外做功,其内能可能增加D.物体放出热量,同时对外做功,其内能可能不变2.如图所示,一导热性能良好的金属气缸内封闭一定质量的理想气体。
现缓慢地向活塞上倒一定质量的沙土,忽略环境温度的变化,在此过程中()A.气缸内大量分子的平均动能增大B.气体的内能增大C.单位时间内撞击气缸壁单位面积上的分子数增多D.气缸内大量分子撞击气缸壁的平均作用力增大3.下列有关热学的叙述中,正确的是()A.同一温度下,无论是氢气还是氮气,它们分子速率都呈现出“中间多,两头少”的分布规律,且分子平均速率相同B.在绝热条件下压缩理想气体,则其内能不一定增加C.布朗运动是指悬浮在液体中的花粉分子的无规则热运动D.液体表面层分子间距离大于液体内部分子间距离,故液体表面存在张力4.一定质量的理想气体由状态A变化到状态B,气体的压强随热力学温度变化如图所示,则此过程()A.气体的密度减小B.外界对气体做功C.气体从外界吸收了热量D.气体分子的平均动能增大5.下列说法正确的是()A.布朗运动就是液体分子的热运动B.在实验室中可以得到-273.15℃的低温C.一定质量的气体被压缩时,气体压强不一定增大D.热量一定是从内能大的物体传递到内能小的物体6.一定质量理想气体的状态经历了如图所示的ab、bc、cd、da四个过程,其中ab与竖直轴平行,bc的延长线通过原点,cd与水平轴平行,da与bc平行,则 ( )A.ab过程中气体温度不变,气体不吸热也不放热B.bc过程中气体体积保持不变,气体放出热量C.cd过程中气体体积不断增加,气体吸收热量D.da过程中气体体积保持不变,气体放出热量7.一定质量的理想气体的状态变化过程如图所示,MN为一条直线,则气体从状态M到状态N的过程中A.温度保持不变B.温度先升高,后又减小到初始温度C.整个过程中气体对外不做功,气体要吸热D.气体的密度在不断增大8.重庆出租车常以天然气作为燃料,加气站储气罐中天然气的温度随气温升高的过程中,若储气罐内气体体积及质量均不变,则罐内气体(可视为理想气体)( )A.压强增大,内能减小B.吸收热量,内能增大C.压强减小,分子平均动能增大D.对外做功,分子平均动能减小9.如图所示,一定质量的理想气体密封在绝热(即与外界不发生热交换)容器中,容器内装有一可以活动的绝热活塞.今对活塞施以一竖直向下的压力F,使活塞缓慢向下移动一段距离后,气体的体积减小.若忽略活塞与容器壁间的摩擦力,则被密封的气体( )图13-2-4A.温度升高,压强增大,内能减少B.温度降低,压强增大,内能减少C.温度升高,压强增大,内能增加D.温度降低,压强减小,内能增加10.用相同材料制成质量相等的圆环A 和圆盘B,厚度相同,且起始温度也相同,把它们都竖立在水平地面上,如图所示.现给它们相同的热量,假设它们不与任何其他物体进行热交换,则升温后,圆环A的温度t A与圆盘B的温度t B的大小关系是A.t A>t B B.t A=t B C.t A<t B D.无法确定11.下列说法正确的是A.机械能全部变成内能是不可能的B.第二类永动机不可能制造成功的原因是因为能量既不会凭空产生,也不会凭空消失,只能从一个物体转移到另一个物体,或从一种形式转化成另一种形式C.根据热力学第二定律可知,热量不可能从低温物体传到高温物体D.从单一热源吸收的热量全部变成功是可能的12.下列过程中可能发生的是()A.将两瓶不同液体混合,然后它们又自发地各自分开B.利用其他手段,使低温物体温度更低,高温物体的温度更高C.打开一高压密闭容器,其内气体自发溢出后又自发溢进去,恢复原状D.某种物质从高温热源吸收20kJ的热量,全部转化为机械能,而没有产生其他任何影响13.如图所示,在大口的玻璃瓶内装一些水,水的上方有水蒸气。
热学试题1---4及答案

热学模拟试题一一、 填空题1.lmol 的单原子分子理想气体,在1atm 的恒定压强下,从0℃加热到100℃, 则气体的内能改变了_____J .(普适气体常量R=8.31J ·mol -1·k -1)。
2.右图为一理想气体几种状态变化过程的p-v 图,其中MT 为等温线,MQ 为绝热线,在AM,BM,CM 三种准静态过程中: (1) 温度升高的是___ 过程; (2) 气体吸热的是______ 过程. 3.所谓第二类永动机是指 _______________________________________ ;它不可能制成是因为违背了___________________________________。
4.处于平衡状态下温度为T 的理想气体,kT 23的物理意义是 ___________________________.(k 为玻尔兹曼常量).5.图示曲线为处于同一温度T 时氦(原子量 4)、氖(原子量20)和氩(原子量40)三种气体分子的速率分布曲线。
其中:曲线(a)是______ 分子的速率分布曲线; 曲线(b)是_________气分子的速率分布曲线; 曲线(c)是_________气分子的速率分布曲线。
6.处于平衡态A 的一定量的理想气体,若经准静态等体过程变到平衡态B ,将从外界吸收热量416 J ,若经准静态等压过程变到与平衡态B 有相同温度的平衡态C ,将从外界吸收热量582J ,所以,从平衡态A 变到平衡态C 的准静态等压过程中气体对外界所作的功为_____________________。
7. 一定量的某种理想气体在等压过程中对外作功为200J .若此种气体为单原子分子气体,则该过程中需吸热__________J ;若为双原子分子气体,则需吸热_____________J 。
8.一定量的理想气体,在p —T 图上经历一个如图所示的循环过程(a→b→c→d→a),其中a→b,c→d 两个过程是绝热过程,则该循环的效率η=_________________。
热学试题

②f(υ )dυ : _____________________________________________。(4 分)
B、当理想气体状态改变时,内能一定改变
C、mol 数相同的各种理想气体,只要温度相同,其内能都一样
D、理想气体内能的改变总是等于 M Cv μ
(T1
T 2
)
E、某给定理想气体,处在一定状态,就具有一定内能
3、如果只用绝热方法使系统初态变到终态,则( )
A、对于联结这两态的不同绝热过程,所作的功不同 B、对于联结这两态的所有绝热过程,所作的功都相同
三、计算题(48%) 1、 证明两绝热线不能相交。(6 分)
2、在半径 r = 0.3mm 的毛细管中注水,一部分在管的下端形成水滴,其形状 可以视作半径 R = 3mm 球的一部分,如图所示,已知水的表面张力系数 α =7.3×10-2N/m,上端液体与毛细管的接触角为 0 度,试求管中水柱的高度 h 。(10 分)
1
4、 一隔板把容器分成相等的两部分,一边盛有质量为 m1,摩尔质量为μ 1 的理想气体,另一边为真空。当抽掉隔板后, 则气体就自由膨胀而充满整个容器,试求系统的熵变。(8 分)
5、燃气涡轮机内工质进行如图所示的循环过程,其中 1—2,3—4 为
绝热过程:2—3,4—1 为等压过程。试证明这循环的效率η 为
值,该过程是( )
A、等容升温过程
B、等温膨胀过程
C、等压膨胀过程
D、绝热膨胀过程
二、填空题(28%) 1、 理想气体温标的定义:①_______________________(V 不变);②_______________________(P 不变)。(4 分) 2、麦克斯韦速率分布函数为________________________________。(2 分)
热学试题

热学[填空题]1 在什么温度下,下列一对温标给出相同的读数:(1)华氏温标和摄氏温标;(2)华氏温标和热力学温标;(3)摄氏温标和热力学温标?参考答案:[填空题]2 定容气体温度计的测温泡浸在水的三相点槽内时,其中气体的压强为50mmHg。
(1)用温度计测量300K的温度时,气体的压强是多少?(2)当气体的压强为68mmHg时,待测温度是多少?参考答案:[填空题]3用定容气体温度计测得冰点的理想气体温度为273.15K,试求温度计内的气体在冰点时的压强与水的三相点时压强之比的极限值。
参考答案:[填空题]4 用定容气体温度计测量某种物质的沸点。
原来测温泡在水的三相点时,其中气体的压强当测温泡浸入待测物质中时,测得的压强值为当从测温泡中抽出一些气体,使减为200mmHg时,重新测得当再抽出一些气体使减为100mmHg时,测得试确定待测沸点的理想气体温度。
参考答案:[填空题]5铂电阻温度计的测量泡浸在水的三相点槽内时,铂电阻的阻值为90.35欧姆。
当温度计的测温泡与待测物体接触时,铂电阻的阻值为90.28欧姆。
试求待测物体的温度,假设温度与铂电阻的阻值成正比,并规定水的三相点为273.16K。
参考答案:[填空题]6 在历史上,对摄氏温标是这样规定的:假设测温属性X随温度t做线性变化即,并规定冰点为设分别表示在冰点和汽化点时X的值,试求上式中的常数a和b。
参考答案:[填空题]7 水银温度计浸在冰水中时,水银柱的长度为4.0cm;温度计浸在沸水中时,水银柱的长度为24.0cm。
(1)在室温22.0℃时,水银柱的长度为多少?(2)温度计浸在某种沸腾的化学溶液中时,水银柱的长度为25.4cm,试求溶液的温度。
参考答案:[填空题]8 设一定容气体温度计是按摄氏温标刻度的,它在冰点和汽化点时,其中气体的压强分别为0.400atm和0.546atm (1)当气体的压强为0.100atm时,待测温度是多少?(2)当温度计在沸腾的硫中时(硫的沸点为444.60℃),气体的压强是多少?参考答案:[填空题]9 用L表示液体温度计中液柱的长度。
物理热学试题及答案

物理热学试题及答案一、选择题(每题3分,共30分)1. 热力学第一定律的表达式是()。
A. △U = Q - WB. △U = Q + WC. △U = W - QD. △U = Q + W2. 绝对零度是()。
A. -273.15℃B. 0℃C. -273.15KD. 0K3. 热传导的三种方式是()。
A. 传导、对流、辐射B. 传导、对流、蒸发C. 传导、蒸发、辐射D. 对流、蒸发、辐射4. 理想气体状态方程是()。
A. PV = nRTB. PV = mRTC. PV = (n/M)RTD. PV = (m/M)RT5. 热机效率的计算公式是()。
A. η = W/QB. η = Q/WC. η = W/Q_inD. η = Q_out/Q_in6. 根据热力学第二定律,下列说法正确的是()。
A. 热量可以从低温物体自发地传递到高温物体B. 热量不能从低温物体自发地传递到高温物体C. 所有自然过程都会使熵增加D. 熵是热力学系统的一个状态函数7. 热膨胀系数的定义是()。
A. 单位温度变化下物体体积的变化量B. 单位温度变化下物体长度的变化量C. 单位温度变化下物体质量的变化量D. 单位温度变化下物体密度的变化量8. 热力学第三定律的含义是()。
A. 绝对零度是不可能达到的B. 绝对零度是可能达到的C. 绝对零度是热力学温度的起点D. 绝对零度是热力学温度的终点9. 热力学系统的熵变可以通过()来计算。
A. △S = Q/TB. △S = Q/T - WC. △S = Q/T + WD. △S = Q/T + W/T10. 绝热过程中,系统与外界()。
A. 有热交换B. 没有热交换C. 有功交换D. 没有功交换二、填空题(每题2分,共20分)1. 热力学第一定律表明,能量在转换过程中______。
2. 绝对零度是温度的______,其数值为______K。
3. 热传导的三种方式中,______是不需要介质的。
热学试题精选及答案

热学试题精选及答案1.某体育馆内有一恒温游泳池,水温等于室温,现有一个气泡从水池底部缓缓上升,那么在上升过程中,泡内气体(可视为理想气体)(D )①分子间的平均距离增大②分子平均动能减小③不断吸热④压强不断减小A .①②B .②③C .②④D .①③④2.关于热学现象和热学规律,下列说法中正确的是(D )A .布朗运动就是液体分子的热运动B .用活塞压缩气缸里的空气,对空气做功2.0×105J ,同时空气的内能增加1.5×105J ,则空气从外界吸热0.5×105JC .第二类永动机不可能制成是因为它违反了能量守恒定律D .一定质量的理想气体,压强不变时,温度越高,单位体积内分子个数越少3.如图所示,甲分子固定在坐标原点O ,乙分子位于x 轴上,甲分子对乙分子的作用力与两分子间距离的关系如图中的曲线所示,F >0为斥力,F <0为引力.a 、b 、c 、d 为x 轴上四个特定的位置.现把乙分子从a 处由静止释放,则(C )A .乙分子从a 到b 做加速运动,由b 到c 做减速运动B .乙分子从a 到c 做匀加速运动,到达c 时速度最大C .乙分子从a 到b 的过程中,两分子间的分子势能一直减小D .乙分子到达c 时,两分子间的分子势能最小为零4.以下关于分子力的说法,正确的是(A)A .分子间既有引力作用又有斥力作用B .温度和质量都相同的水和水蒸气具有相同的分子势能C .当两分子间的距离大于平衡位置的间距r 0时,分子间的距离越大,分子势能越小D .气体分子的平均动能越大,其压强一定越大5.下列说法正确的是(BC )A .一个盛有一定质量气体的密闭容器,当容器做自由落体运动处于完全失重状态时,气体对容器底部的压力为零B .对于一定种类的大量气体分子,在一定温度时,处于一定速率范围内的分子数所占的百分比是确定的C .能量的耗散是从能量的转化角度反映出自然界中的宏观过程具有方向性D .只要有足够高的技术条件,绝对零度是可以达到的6.一定质量的气体的温度由T 1升高到T 2,在此过程中(D )A .如果气体体积膨胀,则分子的平均动能可能减小B .如果气体体积保持不变,则分子的平均动能可能不变C .当外界对气体做了功时,分子的平均动能才会增大D .不管气体体积怎样变化,分子的平均动能一定增大7.如图所示,甲分子固定在坐标原点O ,乙分子位于r 轴上距原点r 3的位置.虚线分别表示分子间斥力f 斥和引力f 引的变化情况,实线表示分子间的斥力与引力的合力f 的变化情况。
热力学第二定律试题

热力学第二定律试题(一)填空题(每题2分)1.气体经绝热不可逆膨胀,?S 0;气体经绝热不可逆压缩,?S 0。
(填>、<、=,下同)2. 1mol单原子理想气体从P1、V1、T1等容冷却到P2、V1、T2,则该过程的?U 0,?S 0,W 0。
3.理想气体的等温可逆膨胀过程中,?S 0,?G 0,??U 0,?H 0。
(填>、<、=)4.1mol液态水在373K、P0下汽化为水蒸气,则?S 0,?G 0,?U 0,?H 0。
(填>、<、=)5.热力学第二定律告诉我们只有过程的热温商才与体系的熵变相等,而不可逆过程的热温商体系的熵变。
6.在等温等压,不作其它功的条件下,自发过程总是超着吉布斯自由能的方向进行,直到自由能改变量为零就达到了态。
(二)单项选择题(每题1分)7.根据热力学第二定律的表述,下列说法错误的是()(A) 第二类永动机服从能量守恒原理 (B) 热不能全部转化为功而不引起其他变化(C) 热不能全部转化为功 (D) 从第一定律的角度看,第二类永动机允许存在8.关于自发过程方向性的说法错误的是()(A) 功可以自发的全部转变成热,但热却不能全部转化为功而不留下其它变化(B) 一切自发过程都是不可逆过程 (C) 一切不可逆过程都是自发过程(D) 功转变成热和其它过程一样具有方向性9.工作在393K和293K的两个大热源的卡诺热机,其效率为()(A) 83% (B) 25% (C) 100% (D) 20%10.在可逆循环过程中,体系热温商之和是()(A) 大于零 (B) 小于零 (C) 等于零 (D) 不能确定11.理想气体等温可逆膨胀过程,()(A) 内能增加 (B) 熵不变 (C) 熵增加 (D) 内能减少12.某体系在始态A和终态B之间有两条途径:可逆Ⅰ和不可逆Ⅱ,此时有()(A) SA =SB(B) QⅠ/T = QⅡ/T (C) ?SⅠ=?SⅡ(D) ?SⅠ=⎰T Q IIδ13.下列说法错误的是()(A) 孤立体系发生的任意过程总是向熵增大的方向进行(B) 体系在可逆过程中的热温商等于体系熵变 (C) 不可逆循环过程的热温商小于熵变(D) 体系发生某一变化时的熵变等于该过程的热温商14.热力学第二定律的表达式为dS≥?Q/T环,则()(A) 始、终态相同时,不可逆过程的熵变小于可逆过程的熵变(B) 如果发生某一过程,体系的熵变与热温商相等,则该过程为不可逆过程(C) 对于孤立体系,dS≥0 (D) 在某些情况,可能有dS≤?Q/T环15.300K时,1mol理想气体由A态等温膨胀到B态,吸热1.00KJ,所作的功为A到B等温可逆膨胀功的1/3,则体系的?S为()(A) 3.33J·K-1(B) 10.0 J·K-1(C) 1.11J·K-1 (D) -3.33 J·K-116.2mol单原子理想气体,等压由300K升温至600K,其?S为()(A) 3.47 J·K-1 (B) -14.4 J·K-1(C) 12.5 J·K-1 (D) 28.8 J·K-117.在标准压力时,苯的沸点为353.15K,1molC6H6(l)完全汽化为同温同压下的苯蒸气。
热力学考试试题

热力学考试试题一、选择题(每题 5 分,共 30 分)1、下列关于热力学第一定律的表述中,正确的是()A 系统从外界吸收的热量等于系统内能的增加量与系统对外做功之和B 系统内能的增加量等于系统从外界吸收的热量减去系统对外做功C 系统对外做功等于系统从外界吸收的热量减去系统内能的增加量D 以上表述都不正确2、一定质量的理想气体,在绝热膨胀过程中()A 气体的内能增大,温度升高B 气体的内能减小,温度降低C 气体的内能不变,温度不变D 气体的内能不变,温度升高3、对于热机,下列说法中正确的是()A 热机效率越高,做的有用功越多B 热机效率越高,消耗的燃料越少C 热机效率越高,燃料燃烧释放的内能转化为机械能的比例越大D 热机效率可以达到 100%4、下列过程中,可能发生的是()A 某一物体从外界吸收热量,内能增加,但温度降低B 某一物体从外界吸收热量,内能增加,温度升高C 某一物体对外做功,内能减少,但温度升高D 以上过程都不可能发生5、一定质量的理想气体,在等容变化过程中,温度升高,则()A 气体压强增大B 气体压强减小C 气体压强不变D 无法确定气体压强的变化6、关于热力学第二定律,下列说法正确的是()A 不可能使热量从低温物体传向高温物体B 不可能从单一热源吸收热量并把它全部用来做功,而不引起其他变化C 第二类永动机不可能制成,是因为它违反了能量守恒定律D 热力学第二定律说明一切宏观热现象都具有方向性二、填空题(每题 5 分,共 20 分)1、热力学温度与摄氏温度的关系为_____,当热力学温度为 273K 时,摄氏温度为_____℃。
2、一定质量的理想气体,在等温变化过程中,压强与体积成_____比。
3、卡诺循环包括_____个等温过程和_____个绝热过程。
4、熵增加原理表明,在任何自然过程中,一个孤立系统的熵总是_____。
三、计算题(每题 15 分,共 30 分)1、一定质量的理想气体,初始状态为压强 p₁= 10×10⁵ Pa,体积 V₁= 10×10⁻³ m³,温度 T₁= 300 K。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学物理竞赛训练题 热学(2)一、选择题1. 一定量的理想气体分别由初态a 经①过程ab 和由初态a ′经②过程a′cb 到达相同的终态b ,如p -T 图所示,则两个过程中气体从外界吸收的热量 Q 1,Q 2的关系为:(A) Q 1<0,Q 1>Q 2. (B) Q 1>0,Q 1> Q 2. (C) Q 1<0,Q 1< Q 2. (D) Q 1>0,Q 1< Q 2. [ ]2. 有两个相同的容器,容积固定不变,一个盛有氨气,另一个盛有氢气(看成刚性分子的理想气体),它们的压强和温度都相等,现将5J 的热量传给氢气,使氢气温度升高,如果使氨气也升高同样的温度,则应向氨气传递热量是:[ ](A) 6 J. (B) 5 J. (C) 3 J. (D) 2 J. 3. 某理想气体状态变化时,内能随体积的变化关系如图中AB 直线所示.A →B 表示的过程是 [ ](A) 等压过程. (B) 等体过程.(C) 等温过程. (D) 绝热过程.4.在所给出的四个图象中,哪个图象能够描述一定质量的理想气体,在可逆绝热过程中,密度随压强的变化?[ ]5. 气缸中有一定量的氦气(视为理想气体),经过绝热压缩,体积变为原来的一半,则气体分子的平均速率变为原来的 [ ] (A) 24/5倍. (B) 22/3倍. (C) 22/5倍. (D) 21/3倍.6. 对于室温下的双原子分子理想气体,在等压膨胀的情况下,系统对外所作的功与从外界吸收的热量之比W / Q 等于 [ ](A) 2/3. (B) 1/2. (C) 2/5. (D) 2/7. 7. 理想气体卡诺循环过程的两条绝热线下的面积大小(图中阴影部分)分别为S 1和S 2,则二者的大小关系是: (A) S 1 > S 2. (B) S 1 = S 2. (C) S 1 < S 2. (D) 无法确定.[ ]pρp(A) ρ p(C)ρp(B)ρp (D)8.如图所示,一绝热密闭的容器,用隔板分成相等的两部分,左边盛有一定量的理想气体,压强为p 0,右边为真空.今将隔板抽去,气体自由膨胀,当气体达到平衡时,气体的压强是(A) p 0. (B)p 0 / 2.(C) 2γp 0. (D) p 0 / 2γ. [ ](=γC p /C V )9. 一定量的理想气体,开始时处于压强,体积,温度分别为p 1,V 1,T 1的平衡态,后来变到压强,体积,温度分别为p 2,V 2,T 2的终态.若已知V 2 >V 1,且T 2 =T 1,则以下各种说法中正确的是:(A) 不论经历的是什么过程,气体对外净作的功一定为正值. (B) 不论经历的是什么过程,气体从外界净吸的热一定为正值. (C) 若气体从始态变到终态经历的是等温过程,则气体吸收的热量最少.(D) 如果不给定气体所经历的是什么过程,则气体在过程中对外净作功和从外界净吸热的正负皆无法判断. [ ] 10. 如图所示,一定量的理想气体,沿着图中直线从状态a ( 压强p 1 = 4 atm ,体积V 1 =2 L )变到状态b ( 压强p 2 =2 atm ,体积V 2 =4 L ).则在此过程中: (A) 气体对外作正功,向外界放出热量. (B) 气体对外作正功,从外界吸热. (C) 气体对外作负功,向外界放出热量. (D) 气体对外作正功,内能减少.[ ] 11. 一定量的理想气体,从a 态出发经过①或②过程到达b 态,acb 为等温线(如图),则①、②两过程中外界对系统传递的热量Q 1、Q 2是(A) Q 1>0,Q 2>0. (B) Q 1<0,Q 2<0.(C) Q 1>0,Q 2<0. (D) Q 1<0,Q 2>0.[ ]12. 一定量的理想气体经历acb 过程时吸热500 J .则经历acbda 过程时,吸热为(A) –1200 J . (B) –700 J .(C) –400 J . (D) 700 J .[ ]p 0V (L)12341234 a bOabc① ②p (×105 Pa)V (×10-3 m 3)abcde O11413. 如图所示,设某热力学系统经历一个由c →d →e 的过程,其中,ab 是一条绝热曲线,e 、c 在该曲线上.由热力学定律可知,该系统在过程中(A) 不断向外界放出热量. (B) 不断从外界吸收热量.(C) 有的阶段吸热,有的阶段放热,整个过程中吸的热量等于放出的热量.(D) 有的阶段吸热,有的阶段放热,整个过程中吸的热量大于放出的热量.(E) 有的阶段吸热,有的阶段放热,整个过程中吸的热量小于放出的热量. [ ]14. 理想气体经历如图中实线所示的循环过程,两条等体线分别和该循环过程曲线相切于a 、c 点,两条等温线分别和该循环过程曲线相切于b 、d 点a 、b 、c 、d 将该循环过程分成了ab 、bc 、cd 、da 四个阶段,则该四个阶段中从图上可肯定为放热的阶段为(A) ab . (B) bc . (C) cd . (D) da . [ ]15. 某理想气体分别进行了如图所示的两个卡诺循环:Ⅰ(abcda )和Ⅱ(a'b'c'd'a'),且两个循环曲线所围面积相等.设循环I的效率为η,每次循环在高温热源处吸的热量为Q ,循环Ⅱ的效率为η′,每次循环在高温热源处吸的热量为Q ′,则 (A) η<η′, Q < Q ′. (B) η<η′, Q > Q ′. (C) η>η′, Q < Q ′. (D) η>η′, Q > Q ′. [ ]16. 关于可逆过程和不可逆过程有以下几种说法: (1) 可逆过程一定是平衡过程. (2) 平衡过程一定是可逆过程.(3) 不可逆过程发生后一定找不到另一过程使系统和外界同时复原. (4) 非平衡过程一定是不可逆过程. 以上说法,正确的是: (A) (1)、(2)、(3). (B) (2)、(3)、(4).(C) (1)、(3)、(4). (D) (1)、(2)、(3) 、(4). [ ]abc deVp OVp Oabcda' b'c' d'17. 所列四图分别表示理想气体的四个设想的循环过程.请选出其中一个在物理上可能实现的循环过程的图的标号.[ ]18. 如图所示:一定质量的理想气体,从同一状态A 出发,分别经AB (等压)、AC (等温)、AD (绝热)三种过程膨胀,使体积从V 1增加到V 2.问哪个过程中气体的熵增加最多?哪个过程中熵增加为零?正确的答案是:(A) 过程AB 熵增加最多,过程AC 熵增加为零.(B) 过程AB 熵增加最多,过程AD 熵增加为零. (C) 过程AC 熵增加最多,过程AD 熵增加为零.(D)过程AD 熵增加最多,过程AB 熵增加为零.[ ]19. 设1 mol 理想气体,从同一初始平衡态出发,进行可逆的等压过程或等体过程.在温熵图(T ~S )中,对于相同的温度(A) 等压过程曲线的斜率大于等体过程曲线的斜率. (B) 等压过程曲线的斜率小于等体过程曲线的斜率. (C) 两种过程曲线的斜率相等. (D) 两种过程曲线的斜率孰大孰小取决于温度的值. [ ]二、填空题1. (5分)一定量理想气体,从同一状态开始把其体积由0V 压缩到021V ,分别经历以下三种过程:(1) 等压过程;(2) 等温过程;(3) 绝热过程.其中:__________过程外界对气体作功最多;__________过程气体内能减小最多;__________过程气体放热最多. 2. (3分) 水的定压比热为 K J/g 2.4⋅.有1 kg 的水放在有电热丝的开口桶内,如图所示.已知在通电使水从30℃升高到80 ℃的过程中,电流作功为 4.2×105 J ,那么过程中系统从外界吸收的热量Q =______________.3. (3分) 3 mol 的理想气体开始时处在压强p 1 =6 atm 、温度T 1 =500 K 的平衡态.经过一个等温过程,压强变为p 2=3atm .该气体在此等温过程中吸收的热量为Q =_____________J . (普适气体常量11K m ol J 31.8--⋅⋅=R )绝热等温等体绝热等温等体绝热绝热等压绝热等温绝热pV O (A)pV O(B)pVO(C)pVO(D)V12I4. (3分) 右图为一理想气体几种状态变化过程的p -V 图,其中MT 为等温线,MQ 为绝热线,在AM 、BM 、CM 三种准静态过程中:(1) 温度升高的是__________过程;(2) 气体吸热的是__________过程.5. (3分)一定量的理想气体,在p —T 图上经历一个如图所示的循环过程(a→b →c →d →a),其中a →b ,c →d 两个过程是绝热过程,则该循环的效率η =______________.6. (5分) 设在某一过程中,系统由状态A 变为状态B ,如果_________________________________________________,则该过程称为可逆过程; 如果__________________________________________则该过程称为不可逆过程. 7. (4分)所谓第二类永动机是指____________________________________________, 它不可能制成是因为违背了____________________________________________. 8. (3分)由绝热材料包围的容器被隔板隔为两半,左边是理想气体,右边真空.如果 把隔板撤去,气体将进行自由膨胀过程,达到平衡后气体的温度__________(升高、降低或不变),气体的熵__________(增加、减小或不变).9. (3分)已知某理想气体的比热容比为γ ,若该气体分别经历等压过程和等体过程,温度由T 1升到T 2,则前者的熵增加量为后者的______________倍.10. (4分) 1 mol 理想气体在气缸中进行无限缓慢的膨胀,其体积由V 1变到V 2. (1) 当气缸处于绝热情况下时,理想气体熵的增量∆S = _________________. (2) 当气缸处于等温情况下时,理想气体熵的增量∆S = _________________. 11. (5分)三个附图所示分别是一定量理想气体经历的可逆过程曲线.试判断各图上a ,b 两点中处于哪一点的状态时理想气体的熵大,在熵大的那一点上画上“√”,若在两点时的熵一样大,则在两点上都画上“√”.12. (4分)一个能透热的容器,盛有各为1 mol 的A 、B 两种理想气体,C 为具有分子筛作用的活塞,能让A 种气体自由通过,不让B 种气体通过,如图所示.活塞从容器的右端移到容器的一半处,设过程中温度保持不变,则(1) A 种气体熵的增量∆S A =_____________________, (2) B 种气体熵的增量∆S B = ______________________.三、计算题1. (5分)气缸内盛有单原子分子的理想气体,若绝热压缩使其体积减半,问气体分子的方均根速率变为原来的几倍?2. (5分) ν摩尔的某种理想气体,状态按p a V /=的规律变化(式中a 为正常量),当气体体积从V 1膨胀到V 2时,试求气体所作的功W 及气体温度的变化T 1-T 2各为多少. 3. (8分) 温度为25℃、压强为1 atm 的1 mol 刚性双原子分子理想气体,经等温过程体积膨胀至原来的3倍. (普适气体常量R =8.31 1--⋅⋅K mol J 1,ln 3=1.0986) (1) 计算这个过程中气体对外所作的功.(2) 假若气体经绝热过程体积膨胀为原来的3倍,那么气体对外作的功又是多少? 4. (10分) 一个可以自由滑动的绝热活塞(不漏气)把体积为2V 0的绝热容器分成相等的两部分Ⅰ和Ⅱ.I、Ⅱ中各盛有摩尔数为ν的刚性分子理想气体(分子的自由度为i ),温度均为T 0.今用一外力作用于活塞杆上,缓慢地将Ⅰ中气体的体积压缩为原体积的一半.忽略摩擦以及活塞和杆的体积,求外力作的功.5. (5分) 如图所示,AB 、DC 是绝热过程,CEA 是等温过程,BED 是任意过程,组成一个循环。
