原创-有机物分子共线共面完整问题
有机物分子中原子的共面共线问题

有机物分子中原子的共面共线问题有机分子中原子的共面共线是中学有机化学教学的一个难点。
此类题目的解题思维方法如下:原子共面共线问题思维的基础:甲烷的正四面体结构;乙烯、苯的平面结构;乙炔的直线结构。
1、甲烷的正四面体结构在甲烷分子中,一个碳原子和任意个氢原子可确定一个平面。
当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
丙烷其结构式可写成如图2所示,丙烷分子中最多原子可能共面。
2、乙烯的平面结构乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
CH3CH=CH2 原子一定共面,最多原子可能共面。
3.苯的平面结构苯分子所有原子在同一平面内,键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯如右下图所示,甲苯分子中最多有可能是个原子共面。
4.乙炔的直线结构乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线。
丙炔如图所示,丙炔分子中有个原子共线。
巩固练习:1、描述CH3-CH=CH-C≡C-CF3分子结构下列叙述中,正确的是A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子有可能都在一个平面上D.6个碳原子不可能都在一个平面上2、甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是()A.分子式为C25H20B.分子中所有原子有可能处于同一平面C.该化合物分子中所有原子不可能处于同一平面D.分子中所有原子一定处于同一平面3、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是()A.盆烯是苯的一种同分异构体B.盆烯分子中所有的碳原子不可能在同一平面上C.盆烯是乙烯的一种同系物D.盆烯在一定条件下可以发生加成反应4、某烃的结构简式为CH3―CH2―CH=C(C2H5)―C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为()A.4、3、5 B.4、3、6 C.2、5、4 D.4、6、45、观察以下有机物结构:CH3 CH2CH3(1) C = CH H (2) H—C≡C—CH2CH3 (3) —C≡C—CH=CF2思考:最多有几个碳原子共面、、最多有几个碳原子共线、、有几个不饱和碳原子、、不饱和度及其应用不饱和度又称为“缺氢指数”,用希腊字母Ω来表示,顾名思义,它是反映有机物分子不饱和程度的量化标志。
有机物分子中原子共线共面问题

二、乙烯的空间构型----平面型
乙烯分子中的所有原子都在同一平面内,键角120°
当乙烯分子中某氢原子被其他原子或原子团取代时, 则代替该氢原子的原子一定在乙烯的平面内。
例2:判断丙烯中最多有几个原子 共面,最少有几个原子共面?
其结构式可写成如图4所示。三个氢原子(①②③)和 三个碳原子(④⑤⑥)六原子一定共面。根据三角形 规则[⑤C,⑥C,⑦H构成三角形]。⑦H也可能在这个 平面上。至少6个原子(3个碳原子,3个氢原子),至 多7个原子[3个碳原子和4个氢原子]共面。
同理可分析萘
分子中10个碳原子,8个
氢原子18原子共面和蒽
分子中14个碳
原子,10个氢原子,共24个原子共面的问题。
四.乙炔的直线结构
乙炔分子中的2个碳原子和2个氢原子 一定在一条直 线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代 时,代替该氢原子的原子一定和乙炔分子的其他原子 共线。
以甲烷母体模型衍变为-------一氯甲烷、乙烷
C-C单键可以自由转动,同样这些原子不能 共面。可见凡是碳原子以单键形式存在其 所连四个碳原子不能共面
延伸:甲烷分子中的4个氢原子全部被苯基取代,可 得如图所示的分子,对该分子的描述不正确的是
A.分子式为C25H20 B.分子中所有原子有可能处于同一平面 C.该化合物分子中所有原子不可能处于同一平面 D.分子中所有原子一定处于同一平面
例6:
中一定有几个原子共面?
11个碳原子,萘环上的6个氢原子共17个原子共面。 亚甲基上的两个氢原子分别位于平面的两侧(①C ② C ③C构成三角形)。
1.请分析苯乙炔(
课堂练习
C CH)分子中有多少个原子共平面?
有机物共面、共线问题总结(含习题答案)

二、比较重要的是需要记住——共线必共面以下几个基本规律:单键是可旋转的,是造成有机物原子不在同一平面上最主要的原因1. 结构中每出现一个饱和碳原子,则整个分子不再共面。
2. 结构中每出现一个碳碳双键,至少有 6个原子共面;3. 结构中每出现一个碳碳三键,至少有 4个原子共线;4. 结构中每出现一个苯环,至少有12个原子共面三、结构不同的基团连接后原子共面分析H _O—H1.直线与平面连接:直线结构中如果有 2个原子(或者一个共价键)与一个平面结构共用,则直f “一 H线在这个平面上。
如 CH=CHdCH 其空间结构为,中间两个碳原子既在乙烯平 面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2. 平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重H/合,但可能重合。
如苯乙烯分子中共平面原子至少12个,最多16个。
JH有机物分子中原子共线、共面问题代表物空间构 型结构球棍模型 结构特点CH正四面 体C -任意3点(原子)共面 C —C 键可以旋转平面结 构C lx123° =C/ ~\巴j6点共面 C=C 建不能旋转GH2直线型180° 血4点共线(面) C ^C 键不能旋转C6H平面正 六边形II H-'Hisffq12点共面HCHO平面O IIX.4点共面.熟记五类分子空间构型上述几种分子的空间构型,以其为母体并将其从结构上衍变至复杂有机物中判断原子是否共线共面。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原4 .直线、平面与立体连接:如图所示的大分子中共平面原子至少12个,最多19个。
分析时要注的碳原子数为b, —定在同一平面内的碳原子数为c,则a, b, c分别为(意两点:①观察大分子的结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可;②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上。
原创_有机物分子共线共面完整问题

有机物分子共线、共面问题分子原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型1.常见分子的空间构型:①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C—H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型5个原子中最多有3个原子共平面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线。
更共面乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H 键之间的夹角为180°。
2.单键的转动思想有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
二、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分子中共平面原子至少12个,最多16个。
同理可分析萘分子中10个碳原子,8个氢原子18原子共面和蒽分子中14个碳原子,10个氢原子,共24个原子共面问题。
有机物分子中原子共线共面问题

有机物分子中原子的共面共线问题衡南二中胡必爱有机分子中原子的共面共线是中学有机化学教学的一个难点。
此类题目的解题思维方法如下:原子共面共线问题思维的基础:甲烷的正四面体结构;乙烯、苯、萘、蒽的平面结构;乙炔的直线结构。
1.甲烷的正四面体结构在甲烷分子中,一个碳原子和任意两个氢原子可确定一个平面,其余两个氢原子分别位于平面的两侧,即甲烷分子中有且只有三原子共面(称为三角形规则)。
当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
其结构式可写成如图2所示。
左侧甲基和②C构成“甲烷分子。
此分子中⑤H,①C,②C构成三角形。
中间亚甲基和①C,③C构成“甲烷”分子。
此分子中①C,②C,③C构成三角形,同理②C,③C,④H构成三角形,即丙烷分子中最多两个碳原子(①C,②C,③C)三个氢原子(④H,⑤H)五原子可能共面。
2.乙稀的平面结构乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
其结构式可写成如图4所示。
三个氢原子(①②③)和三个碳原子(④⑤⑥)六原子一定共面。
根据三角形规则[⑤C,⑥C,⑦H构成三角形]。
⑦H也可能在这个平面上。
至少6个原子(6个碳原子),至多10个原子[6个碳原子和4个氢原子(每个甲基可提供一个氢原子)]共面。
3.苯的平面结构苯分子所有原子在同一平面内,键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子一定共面。
此外甲基上1个氢原子(①H,②C,③C构成三角形)也可以转到这个平面上,其余两个氢原子分布在平面两侧。
故甲苯分子中最多有可能是13个原子共面。
同理可分析萘分子中10个碳原子,8个氢原子18原子共面和蒽分子中14个碳原子,10个氢原子,共24个原子共面问题。
有机物分子中原子共线、共面问题(带答案)
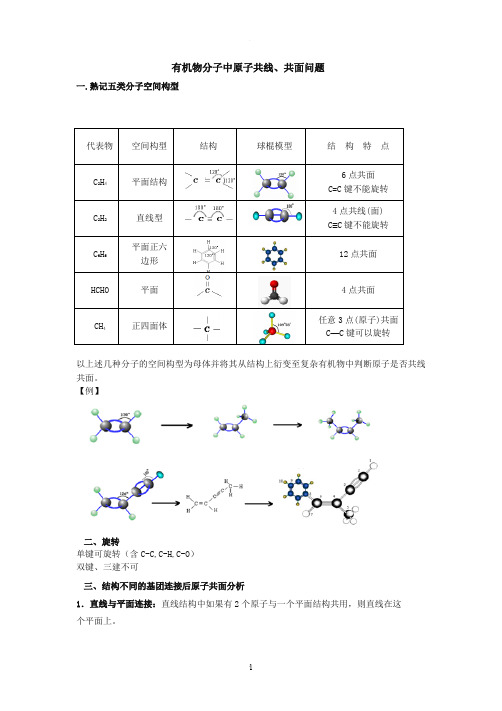
有机物分子中原子共线、共面问题一.熟记五类分子空间构型以上述几种分子的空间构型为母体并将其从结构上衍变至复杂有机物中判断原子是否共线共面。
【例】二、旋转单键可旋转(含C-C,C-H,C-O ) 双键、三建不可三、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子与一个平面结构共用,则直线在这个平面上。
代表物 空间构型 结构 球棍模型 结 构 特 点 C 2H 4 平面结构6点共面 C=C 键不能旋转 C 2H 2 直线型4点共线(面) C ≡C 键不能旋转 C 6H 6平面正六边形12点共面HCHO平面4点共面CH 4 正四面体任意3点(原子)共面C —C 键可以旋转如CH 2=CH-C ≡CH ,其空间结构为 ,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分子中共平面原子至少12个,最多16个。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如丙烯分子中,共面原子至少6个,最多7个。
4.直线、平面与立体连接:如图所示的大分子中共平面原子至少12个, 最多19个。
分析时要注意两点:①观察大 分子的结构,先找出甲烷、乙烯、乙炔和 苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可;②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上。
强化练习:1.描述CH 3-CH =CH -C ≡C -CF 3分子结构的叙述中,正确的是( BC ) A .6个碳原子有可能都在一条直线上 B .6个碳原子不可能都在一条直线上 C .6个碳原子有可能都在同一平面上 D .6个碳原子不可能都在同一平面上 2.下列有机化合物分子中的所有碳原子不可能...处于同一平面的是( D )A .B .C .D .3.在 分子中,处于同一平面上的原子数最多 可能是( D )A .12个B .14个C .18个D .20个 4.在分子中,处于同一平面上碳原子数最少是( A )A .10个B .8个C .14个D .12个HC —CH 3 —CH 3 CH 3 —CH — CH 3 CH 3CH 2 C CH 3 —CH 35.甲烷分子中的4个氢原子全部被苯基取代,得如图所示分子,对该分 子描述不正确的是 ( D ) A .分子式为C 25H 20 C .此物质属于芳香烃类物质 D .分子中所有碳原子有可能处于同一平面6.某烃的结构简式为。
有机物共面、共线问题总结(含习题答案)

二、比较重要的是需要记住——共线必共面以下几个基本规律:单键是可旋转的,是造成有机物原子不在同一平面上最主要的原因1. 结构中每出现一个饱和碳原子,则整个分子不再共面。
2. 结构中每出现一个碳碳双键,至少有 6个原子共面;3. 结构中每出现一个碳碳三键,至少有 4个原子共线;4. 结构中每出现一个苯环,至少有12个原子共面三、结构不同的基团连接后原子共面分析H _O—H1.直线与平面连接:直线结构中如果有 2个原子(或者一个共价键)与一个平面结构共用,则直f “一 H线在这个平面上。
如 CH=CHdCH 其空间结构为,中间两个碳原子既在乙烯平 面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2. 平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重H/合,但可能重合。
如苯乙烯分子中共平面原子至少12个,最多16个。
JH有机物分子中原子共线、共面问题代表物空间构 型结构球棍模型 结构特点CH正四面 体C -任意3点(原子)共面 C —C 键可以旋转平面结 构C lx123° =C/ ~\巴j6点共面 C=C 建不能旋转GH2直线型180° 血4点共线(面) C ^C 键不能旋转C6H平面正 六边形II H-'Hisffq12点共面HCHO平面O IIX.4点共面.熟记五类分子空间构型上述几种分子的空间构型,以其为母体并将其从结构上衍变至复杂有机物中判断原子是否共线共面。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原4 .直线、平面与立体连接:如图所示的大分子中共平面原子至少12个,最多19个。
分析时要注的碳原子数为b, —定在同一平面内的碳原子数为c,则a, b, c分别为(意两点:①观察大分子的结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可;②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上。
高中必读 有机物分子共线 共面问题大全

有机物分子共线、共面问题分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型1.常见分子的空间构型:①CH分子为正四面体结构,其分子最多有3个原子共处同一平面。
4个共价键时,空间结构都是4 凡是碳原子与4个原子形成—甲烷型:正四面体结构,4个CH 健不在同一平面上个原子共平面。
5个原子中最多有3正四面体结构以及烷烃的空间构型四乙烯基甲烷最多多少原子共面个碳共原子与这5C个原子共面,且使得6个HC-C最多有11个原子共面。
见图,单键旋转后,能使得中间的5 个原子共面。
面,共有11②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线更共面。
8/ 1凡是位于乙炔结构上的四个原子共直线。
乙炔型:直线型结构。
四个原子在同一条直线上④苯分子中所有原子共平面。
12凡是位于苯环上的个原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面CHO分子中所有原子共平面。
⑤H—1)熟记四类空间构型(中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
)理解三键三角(2 键不能旋转。
键、C≡C—三键:CC键可以旋转,而C=C键HC—120°C键之间的夹角为109°28′,乙烯和苯环中的—H键之间的夹角为,乙炔中的HC三角:甲烷中的—180°。
之间的夹角为单键的转动思想2.有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
二、结构不同的基团连接后原子共面分析8/ 21.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面,中间两个碳原子既在乙烯平面上,又在乙炔直线上,=CH-C≡CH,其空间结构为上。
如CH2共平面。
所以直线在平面上,所有原子2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重中共平面原子至少12个,最多合。
有机物分子共线共面问题大全 (2)
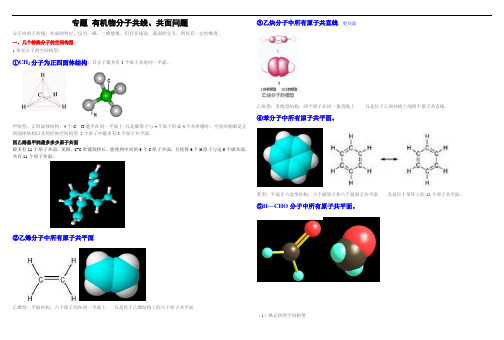
专题有机物分子共线、共面问题分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型1.常见分子的空间构型:①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C—H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型 5个原子中最多有3个原子共平面。
四乙烯基甲烷最多多少原子共面最多有11个原子共面。
见图,C-C 单键旋转后,能使得中间的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线。
更共面乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型.中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C —H键之间的夹角为120°,乙炔中的C—H键之间的夹角为180°。
2.单键的转动思想有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
二、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH 2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
有机物分子共线共面问题大全
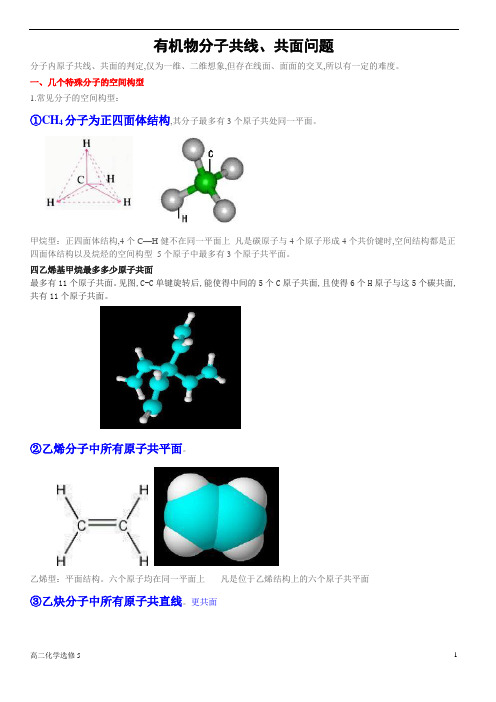
有机物分子共线、共面问题分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型1.常见分子的空间构型:①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C—H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型 5个原子中最多有3个原子共平面。
四乙烯基甲烷最多多少原子共面最多有11个原子共面。
见图,C-C单键旋转后,能使得中间的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线。
更共面乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H键之间的夹角为180°。
2.单键的转动思想有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
二、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
(完整版)有机物共线共面问题专题突破
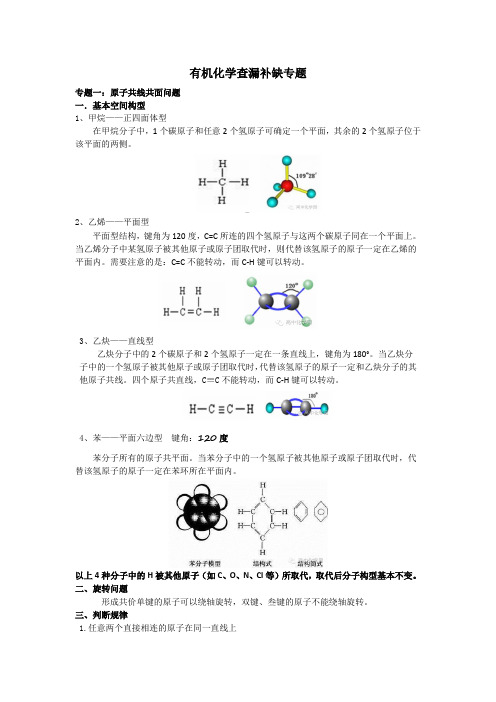
有机化学查漏补缺专题专题一:原子共线共面问题一.基本空间构型1、甲烷——正四面体型在甲烷分子中,1个碳原子和任意2个氢原子可确定一个平面,其余的2个氢原子位于该平面的两侧。
2、乙烯——平面型平面型结构,键角为120度,C=C 所连的四个氢原子与这两个碳原子同在一个平面上。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
需要注意的是:C=C不能转动,而C-H键可以转动。
3、乙炔——直线型乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线。
四个原子共直线,C≡C不能转动,而C-H键可以转动。
4、苯——平面六边型键角:120度苯分子所有的原子共平面。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯环所在平面内。
以上4种分子中的H被其他原子(如C、O、N、Cl等)所取代,取代后分子构型基本不变。
二、旋转问题形成共价单键的原子可以绕轴旋转,双键、叁键的原子不能绕轴旋转。
三、判断规律1.任意两个直接相连的原子在同一直线上2.任何满足炔烃结构的分子,若只含一个碳碳三键,与其三键相连的所有原子均在同一直线上。
3.中学学的有机物中,全部原子能够共面的有乙烯、乙炔、苯、苯乙烯、1,3-丁二烯、苯乙炔等。
四、分割法(例题1)1.一点定面:分子中有一个碳形成4个单键,则该分子中所有原子不可能共面。
2.分割组合:若有机物中碳原子的共线、共面问题,要进行单元分割,必要时兼顾分子对称性。
分割后结合键的旋转性确定共线或共面的原子个数,注意题目要求。
五.注意关键字审题时注意“碳原子”“所有原子”“可能”“一定”“最少”“最多”“共线”“共面”。
【例题】1、下列关于CH3—CH=CH—C≡C—CF3分子结构的叙述中正确的是()。
A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子一定都在同一平面上D.6个碳原子不可能都在同一平面上【答案】B、C【解析】根据(1)乙烯分子中的6个原子共平面。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机物分子共线、共面问题
分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型
1.常见分子的空间构型:
①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C—H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型 5个原子中最多有3个原子共平面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面
③乙炔分子中所有原子共直线。
更共面
乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型
中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角
三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H 键之间的夹角为180°。
2.单键的转动思想
有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
二、结构不同的基团连接后原子共面分析
1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面
上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重
合。
如苯乙烯分子中共平面原子至少12个,最多16个。
同理可分析萘分子中10个碳原子,8个氢原子18原子共面
和蒽分子中14个碳原子,10个氢原子,共24个原子共面问题。
再如:其结构简式可写成最少6个碳原子(因双键与双键之间的碳碳单键可以转动)6个原子,最多10个碳原子共面。
16个原子
再如:中11个碳原子,萘环上的6个氢原子共17个原子共面。
亚甲基上的两个氢原子分别位于平面的两侧(甲烷型①C ②C ③C构成三角形)。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如丙烯分子中,共面原子至少6个,最多7个。
甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子一定共面。
此外甲基上1个氢原子(①H,②C,③C构成三角形)也可以转到这个平面上,其余两个氢原子分布在平面两侧。
故甲苯分子中最少12个,最多有可能是13个原子共面。
4.直线、平面与立体连接:如图所示的大分子中共平面原子至少12个,最多19个。
分析时要注意两点:①观察大分子的结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可;②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上。
不要忽视8号碳原子对位上的9号碳原子,
三、比较重要的是需要记住-------共线必共面
以下几个基本规律:单键是可旋转的,是造成有机物原子不在同一平面上最主要的原因 1. 结构中每出现一个饱和碳原子,则整个分子不再共面。
2. 结构中每出现一个碳碳双键,至少有6个原子共面; 3. 结构中每出现一个碳碳三键,至少有4个原子共线; 4. 结构中每出现一个苯环,至少有12个原子共面
5. 正四面体结构:甲烷
平面结构:乙烯、苯、萘( )、蒽 、甲醛( ) 直线结构:乙炔
与饱和碳(CH 4型)直接相连的原子既不共线也不共面。
与 或 或 或 直接相连的原子共面。
与—C≡C—直接相连的原子共线。
碳碳单键可任意旋转,而双键或三键均不能旋转。
例题:
1、丙烷中最多有 3 个碳原子共面,最多有 5 个原子共面。
2、① 丙烯中有 3 个C 原子共面和 3 个H 原子一定共面。
丙烯中至少有 3 个C 原子共面和 3 个H 原子共面。
丙烯中最多有 3 个C 原子共面和 4 个H 原子共面。
丙烯中可能有 3 个C 原子共面和 4 个H 原子共面。
O H —C —H
╲ ╱ ╱ ╲ C=C
②2,3—二甲基—2—
丁烯至少有 6 个原子共面,最多有10 个原子共面。
③右上图的二烯烃至少有 6 个C原子共面,最多有10 个C原子共面。
至少有 6 个原子共面,最多有16 个原子共面。
3、甲苯有12 个原子一定共面,最多有13 个原子共面。
4、丙炔有4 个原子一定共线,最多有 5 个原子共面。
5、①下图该有机物有4 个原子一定在一条直线上,至少有8 个原子共面,最多有9 个原子共面。
CH3-CH2—CH=C(C2H5)-C≡CH中含四面体结构的碳原子数为4 ,
在同一直线上的碳原子数最多为 3 ,一定在同一平面内的碳原子数为6 ,
最少共面的原子数为8 ,最多共面的原子数为12 。
③CH3-CH=CH-C≡C-CH3分子中,处于同一平面上的原子数最多可能是20 个。
C=C
CH3
╲
CH3
╱
H3C
╱
╲
H3C
C=C
╲
CH3
╱
╱
H3C
C=C
CH3
╲
CH3
╱
H3C
╱
H3C
╲
【练习】
1、下列有机分子中,所有的原子不可能处于同一平面的是(D )
A.CH2=CH-CN B.CH2=CH-CH=CH2
C. -CH=CH2
D.CH2=C-CH=CH2
CH3
2、描述CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是(B)
A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上
C.6个碳原子一定都在同一平面上D.6个碳原子不可能都在同一平面上
该分子结构中至少可以有8 个原子在同一个平面?最多可以有10 个原子在同一个平面
3、甲烷分子中四个氢原子都可以被取代。
若甲烷分子中的四个氢被苯基取代,则可得到的分子如下图,对该分子的描述,不正确的是( B )
A.分子式为C25H20
B.所有碳原子都在同一平面上(中心碳原子甲烷型)
C.此物质属于芳香烃
D.此分子最多有13个碳原子在一个平面上
(提示:有可能两个苯和一个中心碳原子,共一个平面。
)
4、六苯乙烷为白色固体,其结构表示如图:
下列有关说法中不正确的是( C )
A.它是一种芳香烃,易溶于乙醚中
B.它的分子式为C38H30,是非极性分子
C.它的一氯代物只有一种
D.在同一平面上的原子最多有14个。
