第6章 烷烃
有机化学第6章卤代烃12.概要

CH3CH2CH2CH2MgBr
Br + Mg THF THF MgBr 苯基溴化镁
四氢呋喃
Grignard Reagent在有机合成中应用非常广泛,是最
重要的有机金属化合物(金属原子直接与C原子连接的有 机物)之一。
R
R
O R Mg X O R R
以无水乙醚作溶剂,因为它可与格氏试剂形成路易 斯酸和路易斯碱的络合物而使格氏试剂稳定。
一般过渡态能量最高一步的反应的活化能最高反应的速率最小这一多步反应的整个反应的速率就取决于这最慢的一步即决定整个反应速率的一步叫作速率决定步骤ratedeterminingstep简rds在一个多步反应中每一步的反应速率是不同的有快bimolecularnucleophlicsubstitutionunimolecularnucleophilicsubstitution631双分子亲核取代反应s2p138bimolecularnucleophlicsubstitutionchhochbroh二级反应反应速率与溴甲烷及碱的浓度成正比
而把有Grignard试剂参与的反应,称为Grignard反应。
重点掌握
卤代烷与金属镁反应的活性顺序是:
> RF RI > RBr > RCl >
CH3CH2Br
+
RX > ArX
Mg
无水乙醚
CH3CH2MgBr 乙基溴化镁
Mg 无水乙醚
CH3CH2CH2CH2OH
HBr
CH3CH2CH2CH2Br
*卤代烷水解制醇较少应用。
2)醇解反应----被烷氧基取代 (-OR)
卤代烷与醇钠(或酚钠)作用, X 被 -OR取代, 生成醚。
R—X + NaOR’——> R—O—R’+ NaX
有机化学-第六章

按与烯烃加成的试剂不同,可把加成反应分成若 干类型进行研究。
一、催化加氢反应
烯烃与氢作用生成烷烃的反应称为加氢反应,又 称氢化反应。
加氢反应的活化能很大,即使在加热条件下也难 发生,而在催化剂的作用下反应能顺利进行,故 称催化加氢。
4.应用 用硼氢化、碱性氧化水解制备醇的另一优点是烯烃的碳 架不发生重排,这在有机合成中很有意义:
5.反应的特点 气体的硼烷和高挥发性的低碳烷基硼对空气极敏感,在 空气中自燃,硼氢化反应需在惰性气体保护下进行。 烯烃硼氢化反应是间接水合生成反马氏产物,是高区域 选择性、高立体选择性、不发生碳架重排的反应。烷基硼 对氧很敏感,遇氧燃烧,但对水很稳定,可以用水洗的方 法纯化烷基硼。
3.质子酸酸性的影响
酸性越强加成反应越快,卤化氢与烯烃加成反应 的活性: HI > HBr > HCl
酸是弱酸如H2O和ROH,则需要强酸做催化剂,如
四、加次卤酸反应
烯烃与卤素的水溶液反应生成β-卤代醇。例:
丙烯与氯的水溶液反应,生成1-氯代-2-丙醇, 又称β-氯醇。后者脱HCl,是工业上制备环氧丙 烷的方法。
写成通式:
三、烯烃与质子酸反应的立体化学——碳原子 的构型
在前面讨论了烯烃与溴的加成反应中,讨论了C原 子的构型,在烯烃与质子酸加成反应中,C原反应得到的活泼中间体及产物的 构型。
烯烃的硼氢化反应
一、硼氢化反应
烯烃与硼烷加成反应生成烷基硼的反应称为烯烃的硼氢 化反应。 这个反应是美国化学家布朗发现的,因此布朗获1979年 Noble化学奖。最简单的硼烷应是甲硼烷(BH3),但硼和 铝一样是缺电子的,甲硼烷很不稳定,两个甲硼烷结合生 成乙硼烷:
有机化学 第06章 卤代烃

乙烯型卤代烃,由于 P-π共轭,C-X键间的电子 密度比卤代烷中的有所增 加,也就是氯与碳的结合 比在卤代烷中牢固,所以 卤原子的活性比卤代烷中 的卤原子差。
亲核取代反应的立体化学
1. SN2的立体化学
亲核试剂Nu-并不是简单地替代离去团(L-),而是在它原位置 背面进攻中心碳原子,并造成C* 的构型反转,就象大风吹翻一把雨 伞。这种反转关系称为构型翻转式叫瓦尔登(Walden)转化。
不同卤代烃对亲核取代反应的活性比较:
H2C CH CH2 X CH2X H2C CH
( CH2 )n X
H2C
CH
X X
(
)>
n≥ 2 (RX)
>(
乙烯型卤代烃
)
烯丙型卤代烃
卤代烷及X与=远隔型卤代烃
这三类卤代 烃对于取代 反应的活性 差异是由分 子中的电子 效应决定的:
烯丙型卤代烃,由于取代 反应中形成的中间离子(烯丙 基正离子CH2=CH2—CH2+)的 碳正离子上的空P轨道与C=C上 的P轨道共轭,使其上的正电 荷得以分散,因而烯丙基正离 子格外稳定。
本章主要内容
卤代烃的分类、命名 卤代烃的性质 亲核取代反应历程 重要的卤代烃
卤代烃的分类、命名
一、分类
卤代烷 如:R-X 伯卤代烷 :RCH2-X 仲卤代烷 :R2CH-X 叔卤代烷 :R3C-X
一卤代烃
卤代烯
如: R-CH = CH X
分 类
多卤代烃
卤代芳香烃 如: 如: CHCl3
x
二、命名
1. 饱和卤代烃
2 3 4 5 以烃为母体命名,按照烃的命名法编号 5 4 3 2 1
CH3CH2CHCH2CH2CH3
高等有机第六章-构象

OH OH
OH
OH OH
OH
O H HO
H O O
H
OH OH
.
1,2-ae
1,2-ee
均为优势构象
1,3-aa
由于桥连或氢键使下列化合物的船式构象能稳定存在。
H
O
O HO
樟脑
顺-1,4-环己二醇
CH3
HO
N
Me
Me Me Me
O
Ph
4-羟基-1,2,2,6,6-五甲基-4-苯基哌啶
顺1,2-二叔丁基环己烷由于一个叔丁基必须处于a键,使椅式构象 张力很大,低温NMR表明其以椅式和扭船式的平衡混合物存在。
CH3
CH3
H
H
H
H
Ⅴ
室温下, Ⅰ占约70%,Ⅲ和Ⅴ各占约15%
.
CH3
H
H
H
HⅠ
CH3
s
取代基在同侧用s表示(syn)
a
取代基在异侧用a表示(anti)
p cc
p
叠位:p (perplarr) 错位:c (clinar)
sp sc sc ac ac
ap
CH3
H
H
H
3
C H
CH3
H
CH3
H 3 CC H 3
S-trans 73%
H
唯一可测出构象
当甲基被其它体积更大的烷基取代时,S-顺所占比例会随取代基 体积增大而增加。因为大的R基团与C=C重叠不利。
C H 3
O C H 3
R
HR
R=Me 70%
R=Et 55%
R=i-Pr 30%
R=t-Bu 0
.
第6章习题及参考答案
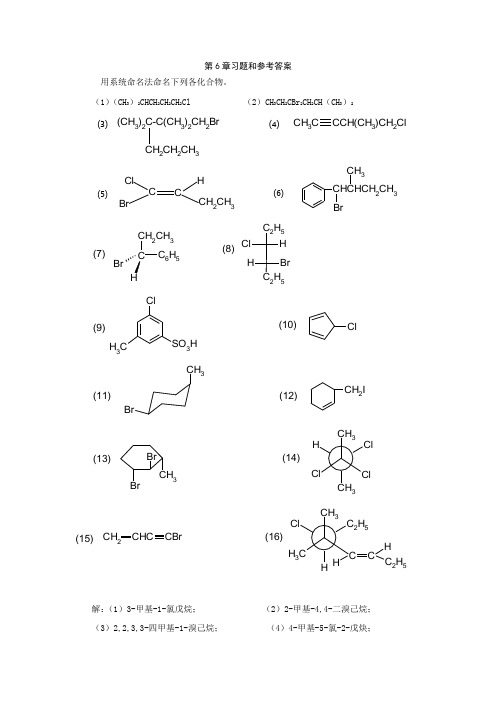
第6章习题和参考答案用系统命名法命名下列各化合物。
(1)(CH 3)2CHCH 2CH 2CH 2Cl (2)CH 3CH 2CBr 2CH 2CH (CH 3)2(CH 3)2C-C(CH 3)2CH 2Br2CH 2CH 3CH 3C CCH(CH 3)CH 2Cl⑶⑷CH Cl BrCH 2CH 3CHCHCH 2CH 3BrCH 3⑸⑹C 2H 52H 5H ClBr HCCH 2CH 3C 6H 5Br(7)(8)ClClCH 3SO 3H (9)(10)CH 3BrCH 2I(11)(12)CH 3ClClCl CH 3HBrCH 3Br (13)(14)CH 3CH 3C 2H 5H ClHH C 2H 5CCH 2CHCCBr(15)(16)解:(1)3-甲基-1-氯戊烷; (2)2-甲基-4,4-二溴己烷; (3)2,2,3,3-四甲基-1-溴己烷; (4)4-甲基-5-氯-2-戊炔;(5)(Z )-1-氯-1-溴-1-丁烯; (6)2-甲基-1-苯基-1-溴丁烷; (7) (R )-1-苯基-1-溴丙烷; (8)(3R ,4R )-3-氯-4-溴己烷; (9) 3-甲基-5-氯苯磺酸; (10)5-氯-1,3-环己二烯; (11) 顺-1-甲基-4-溴环己烷; (12) 3-碘甲基环己烯(13) (1S ,2R ,3R )-1-甲基-2,3-二溴环己烷; (14) (S )-2,2,3-三氯丁烷 (15) 4-溴-1-丁烯-3-炔; (16) (3E ),(6R )-5,5-二甲基-6-溴-3-辛烯写出下列化合物的结构式。
(1) 异丙基氯; (2) 烯丙基溴; (3) β-苯基乙基溴; (4) 对氯苄基溴; (5) 新戊基碘; (6) 叔丁基氯(7) (S)-2-碘辛烷 (8) 6,7-二甲基-5-氯二环[辛烷(9) 反-1-苯基-2-氯环己烷 (10) 1,2,3-三氯环己烷所有异构体的稳定构象 解:CH 3CH 2CH 2CHCH 3ClBrCH 2CH CH 2(1)(2)CH 2CH 2Br CH 2BrCl(3)(4)C CH 2CH 3CH 3CH 3I C Cl CH 33CH 3(5)(6)C 6H 133I HCH 3C H 3ClClPh(9)(8)(7)ClClClClClClClClCl(10)写出1-溴丁烷与下列试剂反应的主要产物。
第六章 烃基化反应

用于治疗痤疮和银屑病的药物阿达帕林中间体6-5的合成, 是由硫酸二甲酯与酚在碳酸钾存在下发生甲基化反应完成的。
4. 芳磺酸酯是应用十分广泛的一类用作烃基化剂的酯,其中对甲苯磺酸 酯和苯磺酸酯是最常见的。磺酸负离子为优良的离去基团,因此芳磺酸 酯作为烃基化剂的反应活性很好,在药物合成中需要引入分子量较大的 烃基时显示出其优势。用于治疗慢性乙肝炎的药物阿德福韦酯中间体6-6的合成中,一条优势
4. 环氧乙烷类烃基化剂在烃基化反应中活性高,反应条件温和,且反应 速率快,在药物合成中应用广泛。眼科用药曲伏前列素中间体6-8的合成,通过
选择环氧氯丙烷为烃基化剂,完成酚羟基氧原子上烃基化反应。
第二节 N原子上的烃基化反应
N原子上的烃基化反应,是指向氨或胺的氮原子上引入烃 基的反应。这是制备各种脂肪族和芳香族伯、仲、叔胺的 主要方法。此类反应也属于亲核取代反应。由于氨和胺氮原
• 鉴于胺或氨与卤代烃的直接烃基化反应产物的难控性,因此在药物 合成中的应用受到了极大的限制。选择性地实现N原子上的烷基化在 药物合成中具有重要的应用价值,常见的方法包括下述几种。
1. Delépline反应:利用卤代烃为原料,通过N-烃基化反应制备伯胺的一 种重要方法。首先,六亚甲基四胺与卤代烃反应形成季铵盐,然后利用 六亚甲基四胺易水解的性质,在醇中进行酸性水解即可得到伯醇。由于 环六亚甲基四胺中的氮原子均为叔胺氮,能保证不发生多烃基化反应。 Delépline反应具有反应选择性高、原料便宜、操作简便等优点,但由于 六亚甲基四胺上氮原子的亲核性较弱,只能与具有较高反应活性的卤代 烃(如苄基卤、烯丙基卤等)反应形成季铵盐,因此也限制了其应用范围。
2. 影响反应的主要因素 1) 羟基化合物结构的影响 a) 醇羟基氧含有的孤对电子可作为亲核试剂发生相应的亲核取代反应, 但反应通常是在碱性条件下完成的。弱酸性的醇在碱性条件下,能可逆 地生成相应的烷氧基负离子,通常其显现出比羟基更强的亲核性。 b) 不同结构的醇,羟基的酸性不同。在同种碱存在下,亲核能力也不同。 即使二苯甲醇,在醇钠等碱存在下,也能与氯代烃发生O-烃基化反应。 对空间位阻大的醇羟基氧的羟基化,通常在类似条件下是不能完成的, 特别是当烃基化剂是甲基以外的其他烃基化剂时,这种现象更加突出。
有机化学 第六章 卤代烃

第六章卤代烃卤代烃是一种简单的烃的衍生物,它是烃分子中的一个或多个氢原子被卤原子(F, CL, Br,I)取代而生成的化合物。
一般可以用R-X表示,X代表卤原子。
由于卤代烃的化学性质主要有卤原子决定,因而X是卤代烃的官能团。
根据卤代烃分子中烃基的不同,可以将卤代烃分为卤代烷烃、卤代烯烃、卤代炔烃和卤代芳烃等。
第一节卤代烷烃一.卤代烷烃的分类和命名(一)卤代烷烃的分类1.根据卤代烷烃分子中所含卤原子的种类,卤代烷烃分为:氟代烷:如CH3-F氯代烷:如:CH3-CL溴代烷:如:CH3-Br碘代烷:如:CH3-I2.根据卤代烷烃分子中所好卤原子的数目的多少,卤代烷烃分为:一卤代烷:如:CH3CL, CH3-CH2-Br二卤代烷:如:CH2CL2,多卤代烷:CHCL33. 根据卤代烷烃分子中与卤原子直接相连的碳原子的类型的不同,卤代烷烃可以分为: 伯卤代烷(一级卤代烷) R-CH 2-Br 仲卤代烷(二级卤代烷)CHXR 1R 2叔卤代烷(三级卤代烷)CXR 1R 2R 3(二) 卤代烷烃的命名 1. 普通命名使用范围:结构比较简单的卤代烷常采用普通命名法 命名:原则:根据卤原子的种类和与卤原子直接相连的烷基 命名为“某烷”,或按照烷烃的取代物命名为“卤某烷”。
如:CH 3CL CH 3CH 2Br CH 3CH 2CH 2CH 2I CH CH 3H 3CCH 2CLCHBrH 3CCH 2CH 3CCH 3H 3CCH 3CL甲基氯(氯甲烷)乙基溴(溴乙烷)正丁基碘(正碘丁烷)异丁基氯(异氯丁烷)仲丁基溴(仲溴丁烷)叔丁基氯(叔氯丁烷)2. 系统命名法范围:复杂的卤代烷烃一般采用系统命名法。
原则:将卤原子作为取代基,按照烷烃的命名原则来进行命名。
方法: 1)选择连有卤原子的最长碳链为主链,并根据主链所含碳原子的数目命名为“某烷”作为母体; 2) 将支链和卤原子均作为取代基;3)对于主链不带支链的卤代烷烃,主链编号从距离卤原子最近的一端开始; 4)对于主链带支链的卤代烷烃,主链的编号应遵循“最低系列规则”; 5)把取代基和卤原子的名称按“次序规则”依次写在“某烷”之前(次序按先后顺序写),即得该卤代烷烃的名称。
有机化学 06第六章 卤代烃2

离去基团的影响:
R-Cl
R-Br
R-I
反应速度增大
6.3.2 消除反应 E (Elimination reaction)
βα
醇
R CH CH 2 + NaOH △
HX
RCH=CH 2 + NaX + H 2O
从分子中脱去一个简单小分子,如HX、H2O等,同时 产生不饱和键的反应称为消除反应。
反应中除α碳脱去X外,在β碳上脱去H,故称为β-消 除反应。
C2H5O- + CH3
CH3 C CH3
Br
[C2H5O-
进攻-H
] H
CH3
CH2 C CH3
Br
CH 3 CH3 C =CH2 + C2H5OH + Br-
SN2反应机理
HO- + CH3Br
[ ] H H HO C Br
进攻-C H
CH3OH + Br-
试剂碱性强,升高温度有利于E2反应。
四、亲核取代反应与消除反应的关系
醇溶液
胺RNH2 + HX
RONO2 + Ag X
硝酸酯
亲核取代反应通式:
RCδ+H2 Xδ- + Nu -
RCH2Nu + X -
反应底物
亲核试剂
产物
离去基团
卤代烷
HO- 、CN- 、 OR-、NH3 ONO-2等
醇、腈、 醚、胺 硝酸酯等
卤素离子
由试剂的负离子部分或未共用电子对去进攻而引
发反应,进攻试剂都有较大的电子云密度,能提供一
写出下列反应的主要产物
CH3
Br NaOH ,C2H5OH
烷烃

第二章 烷烃一 . 基本内容1. 定义及命名法只含碳和氢两种元素且分子中只存在单键的饱和烃称为烷烃。
除简单的烷烃可以用普通命名法外,主要是掌握系统命名法,系统命名法的原则如下:(1)选取主链:选择最长的碳链作为母体,称为某烷。
当有一种以上的碳链可供选择时,应选择碳链上支链(支链可视为取代基)最多的碳链作母体。
(2)主链编号:编号的原则是从最靠近取代基的一端开始依次用阿拉伯数字编号,位次和取代基之间要用半字线“-”连接。
当首先出现的取代基所连碳原子的编号相同时,则尽可能使连有较多取代基的碳原子的编号最小,如CH 3CH 2CH(CH 2CH 3)C- (CH 3)2CH 2CH 3应命名为3,3-二甲基-4-乙基己烷。
主链上碳原子的编号有几种可能时,则采取“最低系列”的编号方法,即逐个比较两种编号中取代基位次的数字,最先遇到位次较低者,定为“最低系列”,如CH 3CH(CH 3)CH 2CH(CH 3)CH(CH 3)CH 3命名为2,3,5-三甲基己烷。
(3)取代基的名称写在母体名称之前,取代基的排列次序按“优先次序规则”排列,将较优的基团后列出。
2. 反应烷烃在常温下与强酸(如浓硫酸、浓硝酸),强碱(如熔化的氢氧化钠),强氧化剂(如重铬酸钾、高锰酸钾),强还原剂(如锌加盐酸、钠加乙醇)等都不起反应或反应速度很慢。
但在适当的温度、压力和催化剂的作用下可以起反应。
(1) 烷烃的燃烧:烷烃完全燃烧生成二氧化碳和水,同时放出大量的热。
反应的通式为:(2)烷烃的热解:烷烃热解时,碳-碳或碳-氢键断裂,生成含有未配对电子的烷基自由基,烷基自由基的反应活性很高,寿命很短,可发生如下反应: CH 3· + ·CH 2CH 3 → CH 3CH 2CH 3 ·CH 2CH 3 + ·CH 2CH 3 → CH 3CH 3 + CH 2=CH 2(3) 烷烃的卤化C H 2n +2+O 2n CO 2+n+1H 2On 3n +12烷烃的卤化产物通常是混合物。
第6章 烃类裂解及裂解气分离

Ⅲ、芳烃→无侧链芳烃基本上不易裂解为烯烃有侧链的芳 烃主要是侧链逐步断裂及脱氢,芳环则倾向于脱氢缩合生 成稠环芳烃,直至结焦
Ⅳ、烯烃→大分子的烯烃能裂解为乙烯、丙烯等低级烯 烃,烯烃脱氢生成二烯烃能进一步反应生成芳烃以及焦 裂解易难顺序为: 异构烷烃>正构烷烃>环烷烃(C6>C5)>芳烃
2.烃类裂解二次反应
CH2CH2CH2CH=CH2 + C5H12 C长侧链先在侧链中央断裂, 有侧链的环烷烃比无侧链的环烷烃裂解能得到较多的烯烃
Ⅱ、环烷烃脱氢生成芳烃比开环生成烯烃容易 Ⅲ、五碳环比六碳环较难裂解 Ⅳ、环烷烃比链烷烃更易生成焦油、产生焦炭
⑶芳香烃裂解
裂解气
再生载气
去深冷
加热炉
5.脱炔
• 乙炔、甲基乙炔、丙二烯 • 危害:炔烃影响乙烯和丙烯衍生物生产过程 影响催化剂寿命 恶化产品质量 形成不安全因素 产生不希望的副产品 • 要求:乙炔<5×10-5 丙二烯<5×10-5 • 脱炔方法:溶剂吸收、催化加氢
溶剂吸收法
• 吸收裂解气中的乙炔 • 同时回收一定量的乙炔 • 常用溶剂 二甲基甲酰胺(DMF)(图3-25) N-甲基吡咯烷酮(NMP) 丙酮 主要根据沸点和熔点及溶解量选择溶剂
3
2.操作条件的影响
⑴常用裂解指标 ⑵操作条件影响 Ⅰ、裂解温度(一次反应产物分布及对二次反应的竞争)
Ⅱ、停留时间(减少二次反应的发生,增加乙烯收率)
Ⅲ、压力(有利于提高一次反应平衡转化率,抑制二次反应)
Ⅳ、稀释剂、烃分压(高温不宜真空操作)
稀释剂降压(惰性气、水蒸汽)
优点 一般采用水蒸汽: ①水蒸汽热容大,稳定炉温 ②水蒸汽易于分离、价廉易得,抑制原料中硫对炉的腐蚀 ③对炉管壁的铁、镍氧化形成氧化膜,抑制生炭反应 ④高温下能与裂解管中积炭、焦反应,有一定的清焦作用 适宜的稀释比
有机化学烷烃

有机化学烷烃有机化学烷烃是一类简单而又重要的有机化合物,其分子结构中只包含碳和氢原子,通过碳碳单键连接构成链状结构。
烷烃可以分为直链烷烃和支链烷烃两大类,它们在化学性质和应用领域上有着各自的特点。
直链烷烃是指碳原子按直线排列连接而成的烷烃分子,最简单的直链烷烃就是甲烷,其分子中只含有一个碳原子和四个氢原子。
直链烷烃的命名遵循一定的规则,以正己烷为例,其中“正”表示直链结构,“己”表示碳原子数为六,“烷”表示为烷烃。
直链烷烃在燃料领域有着重要的应用,如天然气中的甲烷就是一种常见的直链烷烃。
支链烷烃是指碳原子通过支链连接而成的烷烃分子,最简单的支链烷烃为异丙烷,其分子中含有一个主链和一个支链。
支链烷烃的命名也有一定的规则,以异丙烷为例,其中“异”表示支链结构,“丙”表示碳原子数为三,“烷”表示为烷烃。
支链烷烃在化工工业中有着广泛的应用,如异丙醇可以被用作有机合成中的重要原料。
烷烃的物理性质主要取决于其碳原子数和分子结构,一般来说,碳原子数越多,分子越大,沸点和熔点也越高。
此外,直链烷烃的分子间作用力比支链烷烃要强,因此直链烷烃的沸点和熔点通常也比支链烷烃要高。
在有机合成中,烷烃可以作为重要的中间体参与到各种反应中,如裂解反应、氧化反应、还原反应等。
通过烷烃的反应可以制备出各种重要的有机物,如醇、醛、酮等。
此外,烷烃还可以用作燃料,如汽油、柴油等,为人类生活和工业生产提供能源支持。
总的来说,有机化学烷烃是一类简单而又重要的有机化合物,其在化学性质和应用领域上有着广泛的应用。
通过深入研究烷烃的结构和性质,可以更好地理解有机化学的基础知识,并为有机合成和能源开发提供重要的理论基础。
希望未来能有更多的研究能够深入探讨烷烃的新领域,为人类社会的发展做出更大的贡献。
第六章卤代烃

CH3CCH3
NaI
CH3CHCH2CN
I
NaBr
丙酮的存在使生成的NaCl、NaBr不溶,使平 衡向右移动。
(5)与硝酸银-乙醇溶液作用 反应是典型SN1历程,生成沉淀的速度是: R3CX >R2CHX> RCH2X
可用于鉴别不同结构的卤烷。
RX
C2H5OH
AgNO3
RONO2
AgX
用化学方法鉴别: 1—溴丁烯 3—溴丁烯 4—溴丁烯 2—溴丁烷
(c)烯丙基型和苄基型卤代烃对SN反应的影响
++
CH2 CH CH2
++
CH2
由于这些碳正离子相当稳定,所以相应卤代烃 SN1反应活性很高。(比叔卤烷活性高)
SN2反应活性也很高(比伯卤烷活性高),因为 共轭而使过渡态活化能降低。
X δH
CCC H
Nu δ-
(d)乙烯型卤化物对SN反应活性的影响
支链增多对消除有利。 2、试剂碱性和亲核性 碱性强对消除有利,对E2更有利;(KOH/醇、
RONa/醇、RONa/DMSO)。 亲核性强对取代有利,SN2更有利,试剂体积
增大对消除有利。
3、反应温度
提高反应温度对取代、消除都有利,对消除更 有利。
六、有机氟化物
1、有机氟化物的命名
(1)含有一个或少数氟原子的化合物可采用系统 命名法命名。
C2H5OH/H2O
回流
CH3CH2CH2OH
NaBr
采用乙醇/水溶液作为溶剂,主要是增加卤烷在
反应体系中的溶解度。
此法常用于高级醇的制备。
(2)被氰基取代得到腈 伯卤烷与氰化钠在乙醇-水溶液中反应,可以得
第6章 高分子化学— 开环聚合(全)

起始剂浓度
环氧化合物开环聚合过程中,由于起始剂的酸性、引发 环氧化合物开环聚合过程中,由于起始剂的酸性、 剂的活性不同,引发、增长、交换反应的相对速率不同; 剂的活性不同,引发、增长、交换反应的相对速率不同;使 聚合物的分子量、分子量分布各不相同,情况十分复杂。 聚合物的分子量、分子量分布各不相同,情况十分复杂。
14
(3)向单体链转移 )
环氧丙烷阴离子聚合,存在着向单体链转移, 环氧丙烷阴离子聚合,存在着向单体链转移,结果使聚合物分子 量降低。 量降低。
转移反应首先 夺取与环相连 的甲基上的H, 的甲基上的 , 生成单阴离子: 生成单阴离子:
单阴离子
单阴离子迅速 开环, 开环,生成烯 丙基醚阴离子: 丙基醚阴离子:
9
1——自由基聚合 2——阴离子聚合 3——逐步聚合
聚合物分子量和转化率之间的关系 是区别链式和逐步聚合的主要标志。 。
开环聚合反应的聚合上限温度较低,聚合过 程中常有 聚合-解聚 平衡,使过程复杂化。 以工业上几种重要的开环聚合为例进行说明
[ 环氧乙烷、环氧丙烷、三聚甲醛、3,3‘-二(氯亚甲基)环丁醚、已内酰胺 ] 环醚、内酰胺、 环醚、内酰胺、环缩醛
2
如:直链烷烃中CH2的燃烧热=659.0 kJ/mol。 环丙烷中CH2的燃烧热=697.6 kJ/mol。 则:环丙烷中每一个亚甲基的张力=697.6-659.0=38.6 kJ/mol。 所以,环丙烷的张力能=38.6×3=115.8 kJ/mol 。
第6章 卤代烃消除反应(2)
分子内脱去 1分子HCl生 成烯烃。
这种在分子内脱去一个简单分子如 H2O、 HX等形成不饱和结构的反应称为消除反应 (Elimination)。
R-CH-CH-CH-CH-R HXXH
KOH- 醇 R-CH=CH-CH=CH-R + 2NaX + 2H2O
Hβ X + 2NaOH X
Hβ '
乙醇
+ 2NaX + 2H2O
5
+
苄基正碳离子中,
存在着p-共轭,电子云
离域,使正电荷分散至
苯环而稳定。
苄基卤中的卤素原子也非常活泼,能在室温 下与硝酸银醇溶液反应生成卤化银沉淀。
可见:对于烯丙基型卤代烯烃来说,卤原 子反应活性最高,所以无论发生SN1还是SN2,活 性都大。
3.孤立式卤代烃 RCH=CH(CH2)2-X
(n≥2)
CH3CH2CH=CHCH3 + CH3CH2CH2CH=CH2
Br
69%
31%
2-溴戊烷
2-戊烯
1-戊烯
仲卤代烷烃
主要产物
主要产物是由卤代烃分子中的卤原子X和含氢较少 的β-C上的H原子脱去HX。
查依采夫规律Saytzeff Rule: 消除反应主要产物是双键C原子上连有最多烃基的烯烃 (即较为稳定的烯烃)。
轭,π电子离域的结果使正电
荷不再集中于一个C上,使正电
荷得以分散,正碳离子趋向稳
定而易生成
烯 丙 基 氯 (CH2 = CH-CH2-Cl) , 容 易 离 解 成烯丙基C+和Cl-,因而表现出按SN1反应的活 泼性;有利于亲核取代反应的进行。
烯丙基型卤代烃在室温下就能与硝酸银醇 溶液发生反应,生成卤化银沉淀。
第六章 烃方《医用化学基础》

数目和名称写在烯烃名称之前(这一点与烷烃的命 名原则相同)。例如:
C H 2 = C H - C H 2 - C H 2 - C H 3
1-戊烯
4-甲基-1-已烯
2,4-二甲基-2-戊烯
3-甲基-2-乙基-1-丁烯
2-甲基丙烯
炔烃的系统命名方法与烯烃极为相似, 只需将烯烃母体名称中的 “烯”字换为 “炔”即可。例如:
第6章 烃
皖北卫生职业学院 方迎春 威海市卫生学校 张宗霞
制作
学习要点:
1.烷烃的同分异构现象和命名 2.烯烃和炔烃的结构、命名、化学性质 3.脂环烃的结构和命名 4.苯的结构、化学性质,苯的同系物的命名
只含有碳和氢两种元素的化合物,
称为碳氢化合物,简称为烃。烃可以 看作是有机化合物的母体。
饱和链烃(烷烃)
有机化合物分子中的氢原子被卤素原子 取代的反应称为卤代反应。
讨论与思考:
2011年2月15日,苹果公司公布《2010年供应商责 任报告》,首度公开承认它的中国供应商员工有137 名工人因污染导致健康遭受到不利影响;这些工人所 在的车间使用的清洁剂是正己烷。查找资料讨论一下 这些工人“生病”的原因。
第二节 烯烃和炔烃
(二)乙炔及炔烃的结构
炔烃中最简单、最重要的是乙炔,分 子式为C2H2,其结构式为 CH CH 乙炔的分子结构如图
二、烯烃和炔烃的命名
烯烃的命名步骤如下: 1.选主链:选择含有碳碳双键的最长碳链作
为主链,称为“某烯”。
2.编 号:从靠近双键的一端将主链碳原子
依次编号,双键的位次,以双键上编号较小的数字 表示,写在烯烃名称之前。
4.名称表示:把取代基的位号、数目和
有机化学第六章 卤代烃-09.04.15
己二酸
6. 硝酸银作为亲核试剂
R X + AgNO3
卤代烷反应活性:
C2H5OH
R O NO2 + AgX↓
RI > RBr > RCl
由于生成Ag X 沉淀,因此该反应可用来鉴别卤代烃。 不同结构的卤代烃与AgNO3 反应的速度有明显差异。 可以鉴别活性不同的卤代烃。
CH2-Cl
R—X + R O Na
/
R-O-R + Na X
/
R-X: 一般为伯卤代烷
CH3(CH2)2ONa + CH3CH2 I
CH3(CH2)2 OH △ , 70%
CH3CH2CH3OCH2CH3
叔卤代烷及大多数仲卤代烷与醇钠反应时,常发生卤代烷 的消除反应,主要产物为烯烃。
3.氨作为亲核试剂
R-CH2X + 2NH3 R-CH2X + R/ NH2 RCH2-NH2 + NH4X
υ=k [(CH3)3CBr] ------表示为SN1
机理: 第一步 :叔丁基溴解离成叔丁基正离子
(CH3)3C Br
慢
(CH3)3C Br 过渡态T1
(CH3)3C + Br
第二步: 叔丁基正离子与亲核试剂 OH-作用
(CH3)3C + OH
+ 快
(CH3)3C OH
过渡态T2
2-甲基-3-氯 丁烷
2
3
4
5
5
4
3
2
1
CH3CH2CHCH2CH2CH3
1 CH2Br
CH3CHCH2CHCH3 Cl CH3 2-甲基-4-氯戊烷 Cl H3C Cl CH3CH-C-CH2CHCH3 2 3 4 5 6 1 Cl 2-甲基-3, 3, 5-三氯己烷
烷烃
(2)带有支链的烷烃
•选择主链 ——把构造式中连续的最长碳链--作为母
体称为某烷.若最长碳链不止一条,选择其中含较多支 链的为主链. 例1:
最长连续碳链有八个碳原子,该化合物母体的名称为辛烷
例2:
六个碳的主链上有四个取代基
六个碳的主链上有两个取代基
带有支链的烷烃编号:
按最接近取带基的一端开始将主链碳原子用阿拉伯 数字1,2,3...编号. (使取代基的位次最小)
CH3CH3CH2CH3CH2CH2(CH3)2CHCH3CH2CH2CH2CH3CH2CHCH3
Me Et n-Pro i-Pro n-Bu sec-Bu
CH3CH2CH2CH3 sec-Butyl
iso-Butane—— iso-Butyl
(CH3)2CHCH3 tert-Butyl
(CH3)2CHCH2(CH3)3C-
条件:催化剂KMnO4,MnO2或脂肪酸锰.120℃,1.5~3MPa
其中C10~C20的脂肪酸可代替天然油脂制取肥皂. CH3 2.6.2 异构化反应 AlBr3+HBr,27℃ •CH3CH2CH2CH3 CH3-CH-CH3 20% 80%
2.6.3 裂化反应
•裂化——在高温下使烷烃分子发生裂解的过程。
丁烷
C4H10
戊烷
C5H12
CH3(CH2)3CH3
Name Methane(甲烷) Ethane(乙烷)
Condensed Structure 甲基: -Methyl CH4 CH3CH3
Propane(丙烷)
Butane(丁烷) Pentane Hexane Heptane Octane Nonane Decane Undecane Dodecane
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第六章烷烃Alkanes第一节烷烃Alkanes学习目标Learning objectives■什么是烷烃?■如何给烷烃命名?■烷烃有何特性?大纲参考:3.1.6烷烃是饱和的碳氢化合物;这些化合物仅含有碳-碳和碳-氢单键。
这些化合物是化学性质最不活泼的有机化合物。
它们可被用作燃料和润滑剂,同时也可用作其他多种化合物的起始合成原料。
这意味着它们对于工业很重要。
烷烃的主要来源是原油。
■通式(The general formula)所有链式烷烃的通式是C n H2n+2。
碳氢化合物可能是无分支的链式烷烃、有分支的链式烷烃或环状烷烃。
无分支的链式烷烃(Unbranched chians)例如,戊烷——C5H12:(结构式)(结构简式)通常将无分支的链式烷烃称为“直链”烷烃,但其C-C-C角度为109.50(见3.9小节)。
这意味着碳链实际上并不是直的。
在某种无分支的烷烃中,每个碳原子带有两个氢原子,但末端碳原子除外,其上还有一个多余的氢原子。
有分支的链式烷烃(Branched chains)例如,甲基丁烷——C5H12,这是戊烷的一个异构体:(结构式)(结构简式)环式烷烃(Ring alkanes)环式烷烃的通用分子式为C n H2n,因为在环状烷烃中不需要“末端”氢原子。
■如何给烷烃命名(How to name alkanes)直链烷烃(Straight chain)烷烃名称来自词根,可告诉我们碳原子的数量,同时后缀-ane表示是一种烷烃,见表1。
支链烷烃(branched chain)当你命名一种带有直链的碳氢化合物时,你必须首先找出最长的无分支链——有时还需要一点智慧,见下面的实例。
这里给出了词根名,然后按将前缀:methyl-、ethyl-、propyl-等来命名分支或侧链。
最后,添加编号,以表明侧链与哪个碳原子相连。
例如下面两种碳氢化合物相同,尽管乍一看它们似乎是不同的。
在以上两个结构图中,最长的未分支链(红色)为五个碳原子,因此其词根为pentane。
仅有一个碳原子构成的侧链,因此其应命名为methyl-。
该侧链与3号碳原子相连,因此其名称应为3-甲基戊烷(3-methylpentane)。
■结构(Structure)异构现象(Isomerism)甲烷、乙烷和丙烷没有异构体,但其后面的烷烃,随着分子中碳原子的数量增加,其可能出现的异构体数量也会增加。
例如,丁烷有四个碳原子,就有两种异构体,而戊烷则有三种异构体。
戊烷甲基丁烷2,2-双甲基丙烷异构体的数量随碳链长度增加而快速增加。
葵烷(C10H22)有75种异构体,而C30H62的异构体则超过4百万种。
表1前六种烷烃的名称■物理特性(Physical properties)极性(polarity)大多数烷烃均是非极性的,因为碳原子的电负性(2.5)和氢原子的电负性(2.1)相似,见3.3小节。
因此,这些分子之间仅有的分子间作用力是很弱的范德华力;分子越大,范德华力越强。
沸点(Boiling point)这种逐渐增加的分子间作用力就是烷烃的沸点随碳链长度增加而增高的原因。
在室温下,较短的链式烷烃为气体。
有五个碳原子的戊烷,是一种液体,其沸点很低,为309K(36℃)。
然后当烷烃的碳链达到18个碳原子的长度时,烷烃在室温下为固体,看起来与蜡相似。
与相同碳原子数的直链烷烃相比,支链烷烃的熔点较低。
这是因为直链烷烃不能像支链烷烃那样能够紧密包裹在一起,因此范德华力的作用不再有效。
溶解性(Solubility)烷烃不溶于水。
这是因为,水分子通过氢键保持在一起,而氢键的强度远大于在烷烃分子间起作用的范德华力。
但是,烷烃却能与其他相对无极性的液体混合在一起。
■烷烃如何反应(How alkanes react)烷烃的化学性质相对不活泼。
他们具有很强的碳-碳键和碳-氢键。
他们不与酸、碱、氧化剂和还原剂反应。
但是,它们却能燃烧,在合适条件下,能与卤素反应。
在充分供氧的情况下,它们能燃烧并形成二氧化碳和水(或在供氧不足的情况下,形成一氧化碳和水)。
图1 液化气是丙烷和丁烷和混合物。
极地探险使用丙烷含量较高的特殊混合气体,因为丁烷在低于272K温度下为液体。
图2 碳链长度增加对烷烃物理特性的影响问题小结Summary questions1 给烷烃CH3CH2CH(CH3)CH3命名并画出其结构式。
2 画出2-甲基己烷的结构式和结构简式。
3 给2-甲基己烷的一个异构体命名,该异构体为直链。
4 在问题3中,两种异构体中哪个的熔点更高?并解释之。
第二节原油的分馏Fractional distillation of crude oil学习目标Learning objectives■原油的来源是什么?■在工业规模上,如何将原油分离为有用的组分?大纲参考3.1.6目前,原油是全世界有机化合物的主要来源。
我们将原油称为化石燃料,因为它是千百万年前深埋在地下的植物和动物尸骨在高温高压下发生降解而形成的。
由于原油形成非常缓慢,这种资源无法有效再生。
多数情况下,原油是烷烃的混合物,包括未分支的和分支的烷烃。
来源不同的原油,其组分也不一样。
表1中给出了典型北海石油的组分。
原油还含有少量其他组分,溶解在其中。
这些组分来自形成石油的远古植物和动物的其他元素,例如,某些原油含有硫元素。
当这些原油燃烧时,可产生二氧化硫(SO2)。
这是造成酸雨的原因之一;二氧化硫可与大气中含量很高的氧发生反应,生成三氧化硫。
三氧化硫在与大气中的水反应,就形成了硫酸。
表1典型北海石油的组分产品气体石油石脑油煤油汽油燃油和蜡近似沸点/K 310 310-450 400-490 430-523 590-620 超过620碳链长度1-5 5-10 8-12 11-16 16-24 25+百分比 2 8 10 14 21 45提示Hint现在正在产生原油,但是沉积物的累积是一个十分漫长的过程。
原油的分馏(Fractional distillation of crude oil)为了将原油转化为有用的产品,我们必须将混合物分开。
我们通过加热原油,并收集在不同温度范围内蒸发出来的组分来实现这一目的。
每种组分都是具有相似碳链长度的碳氢化合物组成的混合物,因此,这些组分具有相似的特性,见图1。
这个过程就称为分馏(fractional distillation),这一过程是在分馏塔(fractionating tower)中完成的。
■首先在加热炉中将原油加热。
■将液体和气体混合物通入一个分离塔,塔顶部(而不是底部)装有冷却器。
■蒸汽通过一系列含有泡罩的收集盘通向塔顶,直至达到一个充分冷却(收集盘的温度低于其沸点)的收集盘。
然后这些气体就被冷凝为液体。
■冷凝在每个收集盘上的液体混合物通过管道被移除。
■碳链较短的碳氢化合物被冷凝在越靠近塔顶部的收集盘中,这个地方的温度更低,因为混合物的沸点更低。
■在塔底部收集到的厚重残留物称为柏油或沥青。
这些材料可用于铺路,由于其供应常常超过了需求,因此往往对这个组分进行深加工,以产生更有价值的产品。
学习建议Study tip学生无需记住各种组分及其沸点,但你应当明白分馏的基本原理。
Gasoline tray:汽油收集盘Rising vapours:上升的蒸汽Gasoline:汽油Kerosene tray:煤油收集盘Kerosene:煤油Descending liquid:下降的液体gases:气体fuel on site:原地点燃gasoline/petrol(naphtha)cars:汽油/汽油(石脑油)小汽车用kerosene/paraffin:煤油/石蜡jet fuel, lighting飞机燃料,照明Diesel oil:柴油Lorries and taxis:卡车和出租车用Vaporized crude oil in:原油在塔中蒸发Lubricating oil and waxes:重油和蜡Candles and engine oil:蜡烛和引擎油Fuel oil:燃油Ships,power stations:船舶和电站Tar/bitumen柏油/沥青Roads and roofing:铺路和屋顶防水图1 原油的分馏高度为40米)中通过分馏作用被分离为各种组分。
石化厂的规模各不相同,但典型石化厂每年能处理三百五十万吨原油。
提示Hint分馏是一个物理过程,因此分子内没有共价键断裂。
在蒸发过程中,只有分子间的范德华力被破坏,而在冷凝时又会重新形成。
问题小结Summary questions1、画出己烷的分子式和结构式。
2、在表1中,在所命名的原油组分中,哪一种最可能是己烷?3、什么是分馏,它与蒸馏有何区别?第三节工业裂解Industrial cracking学习目标Learning objectives■ 什么是裂解?■ 热裂解的条件和产物是什么?■ 催化裂解的条件和产物是什么?■进行热裂解的经济原因是什么?大纲参考:3.1.6原油通过分馏作用得到的石脑油组分,在石油和化学工业方面有巨大需求。
碳链较长的组分作用不大,因此其经济价值较低。
大多数原油中的长链组分比想要的短链组分多,而石脑油组分往往不够多。
与碳链较长的物质相比,碳链较短的产品在经济上更有价值。
为满足对碳链较短的碳氢化合物的需求,需要将较长碳链的组分裂解为碳链较短(裂化的)的产品。
这可得到两种有用的结果:1、可产生更有用的碳链较短的产品,尤其是石油。
2、某些产物为烯烃,这种产物的反应性较烷烃强。
需要注意的是,石油主要是烷烃的混合物,含有四至十二个碳原子。
烯烃可用作化工原料(这意味着它可以为工业提供起始合成物料,可用于生产不同的物质)并可转化为多种别的化合物,包括多聚物和从油漆至药物等多种产品。
乙烯很可能是最重要的烯烃,这是合成聚乙烯的起始物料。
烷烃的反应性很差,需要很苛刻的条件才能使其降解。
有很多方式可使其发生裂解。
■热裂解(Thermal cracking)这种反应是将烷烃加热到700-1200K的温度,在高压下(高达7000kPa)。
碳-碳键断裂,其断裂方式为两个碳原子夺得共价键电子对中的一个电子。
因此,最初就产生了两条较短的碳链,每条碳链的一个末端碳原子带有一个未配对的电子。
这些片段被称为自由基。
自由基是反应性很高的中间产物,能以各种方式反应,形成多种较短的碳链分子。
由于没有足够的氢原子来产生两种烷烃,因此新的碳链必须含有一个碳碳双键,于是就形成了一种烯烃:自由基-黑点表示未配对的电子图2热裂解学习建议Study tip学生应明白裂解的经济意义。
图1从原油中获得的各种产品任何数量的碳-碳键均可断裂,而碳链不一定是从中间断开。
也可产生氢原子。
热裂解倾向于产生高比例的烯烃。
