IFS第六版内审检查表
内审检查表(新准则)

检查纠正措施程序中是否规定产生 原因的责任部门。实验室用什么方法分析潜在不符合的可能性?
纠正措施的制定过程,并检查纠正措施的跟踪审核记录。
4.9
21记录
实验室应建立和维持适合自身情况并符合现行质量体系的记录制度。实验室质量记录的编制、填写、更改、识别、收集、索引、存取、存档、存放、维护和清理等应按照适当程序规范进行。
重点要检查提供检定校准的服务方的资格、项目、评价及记录
4.6
18合同评审
实验室应建立和维持评审客户要求、标书和合同的程序。
明确客户的要求。
18检查《检验合同书》,客户要求应合理、明确,文件齐全。要求应便于理解,评审的目的是确保实验室能很好理解客户的要求,明确他们的最终要求。
对合同的不同意见,一定在检测开始前得到解决,双方必须认同合同条款。
16 若有分包,检查分包合同、项目及其相关记录。
4.5
17服务和供应品的采购
实验室应有以选择和购买对检测质量有影响的服务和供应品的政策和程序。
还应有及检测有关的试剂和消耗材料的购买、验收和存储的程序,以确保其质量。
17检查服务和材料、设备采购程序、采购计划申请表、材料验收单。检查采购文件及其内容是否符合要求,采购文件上有无技术管理层的审批签字。
23是否制定了管理评审程序,能否以最高管理职责的力度为管理体系的运行提供支持及保障?
管理评审是否由最高管理者主持,是否每12个月至少组织一次?
评审会议是否讨论了较为广泛的输入信息,还是只是内审的总结?
管理评审会议有否记录并形成结论,对提出的问题是否有纠正措施?
内审通用检查检查表(全套表格-适合各部门)
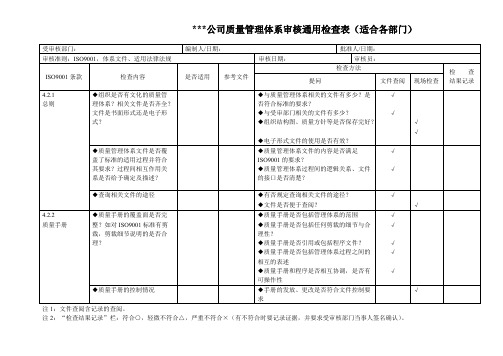
编制人/日期:
审核日期:
是否适用 参考文件
提问
批准人/日期: 审核员:
检查方法
文件查阅 现场检查
◆与质量管理体系相关的文件有多少?是
√
否符合标准的要求?
◆与受审部门相关的文件有多少?
√
◆组织结构图、质量方针等是否保存完好?
√
√
◆电子形式文件的使用是否有效?
◆质量管理体系文件的内容是否满足
√
ISO9001 的要求?
√
◆程序中是否包含对记录的质量要求?
√
◆是否有保存期限的规定?
√
◆记录管理的实况
◆是否对记录进行了清理,并列出了清单? √
√
√
◆对记录的标识、贮存、检索、保护是否
与书面程序的要求相一致?
√
◆记录是否填写正确、字迹清楚?
√
◆贮存是否便于存取和检索?
√
◆贮存环境如温度、湿度是否适宜,防尘、
防蛀等保护措施是否得当?
现场检 查
√ √
√
√
√ √
√ √ √
续表
检查 结果记录
受审核部门: 审核准则:ISO9001,体系文件、适用法律法规
ISO9001 条款
检查内容
5.4.1 质量目标
◆有无目标实现的证据 ◆目标是否定期评审、修订
5.4.1 质量目标
◆策划是否满足质量目标及 质量管理体系总要求?质量 管理体系策划的输出是否形 成文件?
专项技能、技术和财务资源?提供资源的
途径是否明确?
◆承担管理职责的人员,如何表明其对持
√
续改进的承诺?
◆管理者如何参与和支持质量活动?
√
√
◆有关职责、权限如何传达
IFS国际食品标准第6.1版内部审核检查表

–企业方针应传达给所有员工。
1.1.2企业方针应在相关部门分解成具体的目标。各部门应明确其完成目标的职
责和时限。
1.1.3根据企业的方针,企业的质量和食品安全目标应传达给各个相关部门的员
工,并应得到切实执行。
1.1.4最高管理者应确保定期评审所有目标的完成情况,至少每年一次。
1.1.5企业应确保所有与食品安全和质量有关的信息能有效并及时地向有关人员
1.2.9企业应确保相关员工了解所有程序(文件化的和非文件化的)并且持续应 1.2.10企业应建立相应的体系,以确保及时掌握与食品安全和质量有关的法规、 科学和技术的发展,以及行业规范方面的信息。 1.2.11企业应尽快通知其顾客与产品规格有关的任何问题,特别是由主管当局指 出的可能发生的,已经发生的或者曾经发生的与产品安全性和/或合法性有关的 所有不符合,这些问题包括但不限于警示问题。 1.3以客户为关注焦点 1.3.1应建立文件化的程序,以识别顾客的基本需求和期望。 1.3.2应对识别的结果进行评估,并以此来确定质量和食品安全目标。 1.4管理评审 1.4.1最高管理者应确保定期评审质量和食品安全管理体系,至少每年一次,当 体系有变化时应增加评审的频率。此评审须至少包括: 审核的结果,顾客反 馈,过程符合性和产品符合性,预防和纠正措施的状态,上次管理评审的整改情 况,可能影响食品安全和质量管理体系的变化和对于持续改进的建议。 1.4.2管理评审应包括评估质量和食品安全管理体系的控制措施,以及持续改进 的过程。 1.4.3企业应识别并定期评审(例如通过内部审核或现场检查)满足符合产品要 求所需的基础设施。至少应包括以下内容: –建筑物 –供应系统 –机器及设备 –运输。 评审的结果应为投资规划提供参考,并充分考虑到风险。 1.4.4企业应识别并定期评审(例如通过内部审核或现场检查)满足符合产品要 求所需的工作环境。至少应包括以下内容: –员工设施 –环境条件 –卫生条件 –工作场所设计
内审检查表

内审检查表
QR-管-02 内审检查表
深圳市凯胜威电子有限公司
内审检查表
审核部门:管理层
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:业务课
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:物控课采购
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:物控课仓库
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:品质工程
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:生产课
深圳市凯胜威电子有限公司
内审检查表
审核部门:生产课
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核部门:品管课
深圳市凯胜威电子有限公司
内审检查表
审核部门:品管课
深圳市凯胜威电子有限公司
内审检查表
审核/日期:检查/日期:编制/日期:QR-管-02
深圳市凯胜威电子有限公司
内审检查表
审核/日期:检查/日期:编制/日期:QR-管-02深圳市凯胜威电子有限公司
内审检查表
审核/日期:检查/日期:编制/日期:QR-管-02。
内审检查表(全部)
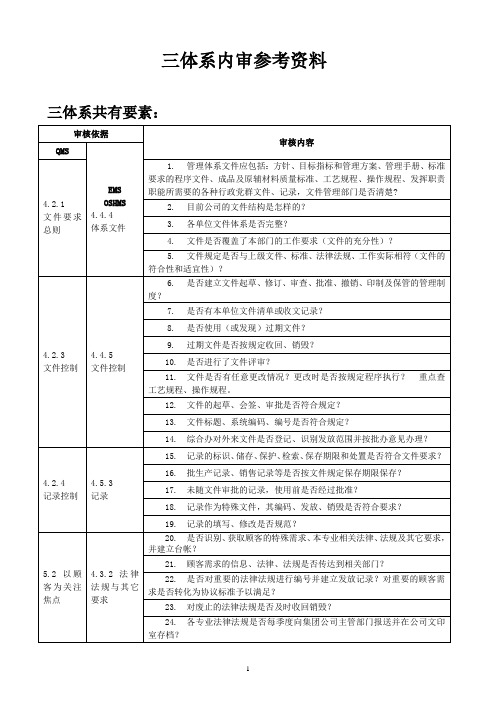
14.事故和紧急情况发生后是否按响应和处理流程进行处理,并将发生的原因、经过、处理方法、程序等上报生产管理处?
5.3质量方针
4.2环境方针、职业安全健康方针
25.是否理解方针的主要内容及其特点、含义?
26.实际工作中如何体现了对满足顾客需求、法律法规及其它要求的承诺;对管理体系持续改进的承诺?
27.怎样传达到员工并作为制订和评审各项工作目标的框架?
5.4.1
质量目标
EMS4.3.3目标指标和管理方案
OSHMS
8.是否使用(或发现)过期文件?
9.过期文件是否按规定收回、销毁?
10.是否进行了文件评审?
11.文件是否有任意更改情况?更改时是否按规定程序执行?重点查工艺规程、操作规程。
12.文件的起草、会签、审批是否符合规定?
13.文件标题、系统编码、编号是否符合规定?
14.综合办对外来文件是否登记、识别发放范围并按批办意见办理?
4.3.3
目标指标
28.目标是否体现了与工作方针的一致性?是否体现了持续改进、可测量性?
29.是否制定工作目标并在相关的职能和层次上进行分解?
30.目标是否可测量?
31.是否对目标进行定期诊断并建立记录?
5.4.2
质量体系策划
EMS4.3.3目标指标和管理方案OSHMS
4.3.4
管理方案
32.是否为各项管理方案的实施提供了必要的资源?
8.产品稳定性、生产设备适用性、包材及储存适用性、内控质量标准的确定。
9.项目实施阶段的对过程和结果的评审,以及对出现的问题提出的改进措施。
10.对产品和工艺改进实施验证。
{财务管理内部审计}第六版内审检查表

为关键控制点建立关键限值-食品法典第八步,原理3
2.9.1
为了清楚地识别工艺是否处于控制之中,就应规定每个关键控制点的关键限值。关键限值应当是:
●无论如何,关键限值应当可测量的(例如时间,温度,PH值)
●基于主观测量的关键限值,应当有清楚的指导书或者样品的支持(如照片)
2.9.2
食品安全小组应当确认每一个关键控制点。书面的证据能够证明选择的控制措施和确定的关键限值能够持续控制危害到规定的可接受的水平。
保持HACCP文件和记录-食品法典第十二步,原理7
2.13.1
保持的文件和记录应是充分的,以使得公司可验证:HACCP控制措施(包括前提方案)是适当的和持续的。
2.14
HACCP计划的评审
2.14.1
食品安全小组应当对HACCP计划和前提方案进行评审,至少每年进行一次。任何对产品的安全性产生影响的改变,也需要对以上内容进行评审。作为指导,评审应当考虑但不限于以下几点:
3.1
食品安全和质量手册
对于满足本标准要求的流程和程序,应形成文件,以便能始终如一的贯彻执行,同时方便培训,并支持安全产品的生产。
3.1.1
公司有书面程序,作业方法和操作规范应整理到印刷的或者电子版的质量手册中。
3.1.2
3.1.2食品安全和质量手册应被全面实施,质量手册或相关的部分能被主要员工获取并阅读。
●顾客要求
2.4
识别预期用途—食品法典第3步
2.4.1
应清楚地描述顾客对产品的预期用途,规定消费对象,包括产品对易受伤害的消费人群(例如婴儿,老年人,过敏症患者等)的适宜性。
2.5
绘制流程图-食品法典第四步
2.5.1
应绘制覆盖每种产品,产品类别和过程的流程图。从原材料的接收到产品的加工,存储和分销,流程图应阐明了HACCP范围内食品加工操作的各个方面。作为指导,这应当包括但不局限于以下信息:
IFS国际食品标准第6.1版内审检查表【IFS内部审核】

管理评审应包括评估质量和食品安全管理体系的控制措施,以及持续改进的过程。
1.4.3
企业应识别并定期评审(例如通过内部审核或现场检
查)满足符合产品要求所需的基础设施。至少应包括以下内容:
– 建筑物
– 供应系统
– 机器及设备
– 运输。
评审的结果应为投资规划提供参考,并充分考虑到风险。
1.4.4
2.2.3.2
识别预期用途(步骤3 )
产品预期用途须考虑到使用该产品的最终消费者,包括敏感消费群体的利益。
2.2.3.3
制定工艺流程图(步骤4 )
每种产品或产品类别都应有生产流程图,并包括所有的过程和子过程的变化(包括返工和重新加工)。流程图应标注日期,注明所有的CCP及编号。有任何变化时,流程图应更新。
1.1.4
最高管理者应确保定期评审所有目标的完成情况,至少每年一次。
1.1.5
企业应确保所有与食品安全和质量有关的信息能有效并及时地向有关人员通报。
1.2
组织结构
1.2.1
企业应建立组织结构图,表明其组织结构。
1.2.2
应明确规定职责和权限,包括职责代理。
1.2.3
应明确描述从事影响产品要求工作的员工的工作职责。
1.2.8
负责质量和食品安全管理的部门应直接向最高管理者进行报告。
1.2.9
企业应确保相关员工了解所有程序(文件化的和非文件化的)并且持续应用。
1.2.10
企业应建立相应的体系,以确保及时掌握与食品安全和质量有关的法规、科学和技术的发展,以及行业规范方面的信息。
1.2.11
企业应尽快通知其顾客与产品规格有关的任何问题,特别是由主管当局指出的可能发生的或者曾经发生的
IFS内审检查表

过敏原和生产的特定条件
5.1
内部审核
5.2
现场检查
5.3
过程控制
5.4
测量和监控装置的校准和检查
5.5
计量检查(计量控制/装填数量)
5.6
产品分析
5.7
产品隔离和产品放行
5.8
权威机构和顾客投诉的处理
5.9
危机管理-产品撤回和产品召回
5.10
不合格品管理
5.11
纠正措施
检查人:
检查时间:
IFS内审检查表
序号
检查项目
检查结果
1.1
企业方针/企业原则
1.2
企业组织结构
1.3
以客户为关注焦点
1.4
管理评审
2.1
HACCP(基于法典委员HACCP原理)
2.2
文件要求
2.3
记录保持
3.1
人力资源管理
3.2
人力资源
3.3
培训
3.4
个人卫生设施、设备和员工设施
4.1
合同评审
4.2
产品规范
4.3
产品开发
4.4
采购
4.5
产品包装
4.6
工厂环境标准
4.7
现场管理和卫生
4.8
废弃物/废弃物处理
4.9
金属、碎玻璃和木制品等异物污染风险
4.10
虫害监控/虫害控制
4.11
物料的接收和存储
4.12
运输
4.13
维护和维修
4.14
设备
4.15
工艺认
4.16
可追溯性(包括GMO和过敏原)
4.17
转基因生物(GMOs)
内审检查表

xx年内部审核检查表Xxxx单位要素条款条款内容检查内容检查方法检查记录结果评价4 评审要求4.1 机构4.1.1 检验检测机构应是依法成立并能够承担相应法律责任的法人或者其他组织。
1)检验检测机构的法人登记、注册证书(营业执照)文件是否由相关行政主管部门核发;2)是否处于有效期内;3)资质认定证书所用名称、地址是否与法人登记、注册文件一致;4)登记、注册文件中的经营范围是否包含检验、检测、检验检测或者相关表述;5)是否有影响其检验检测活动公正性的经营项目(诸如生产、销售等)。
管理体系文件□相关记录□工作现场□抽查报告□提问或核查设备□其他:符合□基本符合□不符合□不适用□检验检测机构或者其所在的组织应有明确的法律地位,对其出具的检验检测数据、结果负责,并承担相应法律责任。
体系文件中是否有规定:1)对其出具的检验检测数据、结果负责,并承担相应法律责任。
2)因检验检测机构自身原因导致检验检测数据、结果出现错误、不准确或者其他后果的,应当承担相应解释、召回报告或证书的后果,并承担赔偿责任。
3)涉及违反相关法律法规规定的,需承担相应的法律责任。
管理体系文件□相关记录□工作现场□抽查报告□提问或核查设备□其他:符合□基本符合□不符合□不适用□不具备独立法人资格的检验检测机构应经所在法人单位授权。
/ / / /内审员签名:年月日被审核部门负责人签名:年月日共51页,第1页要素条款涉及要素检查内容检查方法检查记录结果评价4.1.2 检验检测机构应明确其组织结构及管理、技术运作和支持服务之间的关系。
1)查看组织结构图,是否清晰表明了其管理体系的职责和相互关系;2)非独立法人的检验检测机构是否通过组织结构图表明了与其他部门的关系,说明其独立运作;3)检验检测机构是否设置质量管理、技术管理和行政管理部门或岗位;4)查看管理体系职能分配表,是否清楚表达了三者间的关系。
管理体系文件□相关记录□工作现场□抽查报告□提问或核查设备□其他:符合□基本符合□不符合□不适用□检验检测机构应配备检验检测活动所需的人员、设施、设备、系统及支持服务。
内部审计检查表Internal audit checklist form
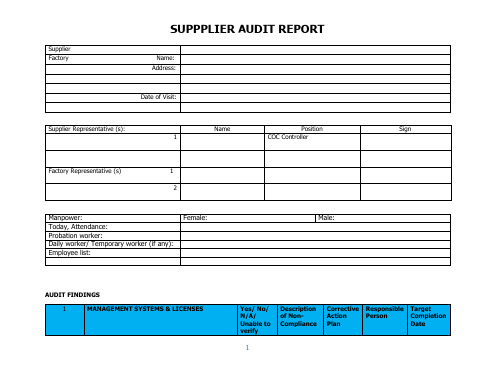
Factory Name:
Address:
Date of Visit:
Supplier Representative (s):
Name
Position
Sign
1
COC Controller
Factory Representative (s) 1
2
Manpower:
Female:
Male:
6
Discrimination
Yes/ No/ N/A/
Unable to verify
Description of Non-Compliance
Corrective Action Plan
Responsible Person
Target Completion Date
6.1
Does employment record show any evidence of discrimination?(e.g., discrimination in hiring, access to training, promotion, compensation, benefits etc., based on race, religion, tribe, cast, gender, sexual or political orientation, national/ethnic/social origin, union membership etc.).
Building Inspection Report 3
Building Inspection Report 4
1.16
Fire Safety Inspection Report 1
Fire Safety Inspection Report 2
IFS第六版内审检查表

2.2.2.
2
负责建立和维护HACC体系的人员应有一个内部的HACC组长,并应接受足够的关于HACC原理的应用方 面的培训。
222.
3
HACC小组应获得高层管理的有力支持,应在整个组 织内部得到组建和充分传达。
编号
IFS FOOD标准要求
关键不 符合项/严不符 合项/不 适用项
A
B
C
D
备注/注释
1
高级管理层职责
1.1
企业方针/企业原则
1.1.1
企业高级管理层应制定和实施企业的方针。应至少包
括:
-以客户为中心
-保护环境的责任
-可持续
-道德和员工职责
-产品要求(包括:产品的安全性、质量、合法性、 过程和规格书)
1.2.10
企业应建立相应的体系,以确保及时掌握与食品安全 和质量有关的法规、科学和技术的发展,以及行业规
范方面的信息。
1.2.11
企业应尽快通知其顾客与产品规格有关的任何问题, 特别是由主管当局指岀的可能发生的或者曾经发生 的
与产品安全性和/或合法性有关的所有不符合,这些 问题包括但不限于警示问题。
-员工设施
-环境条件
-卫生条件
-工作场所设计
-外部影响(如噪音,振动)。
评审的结果应为投资规划提供参考,并充分考虑到风
险。
2
质量和食品安全管理体系
2.1
质量管理
2.1.1
文件要求
2.1.1.
1
食品安全和质量管理体系应形成文件并得到执行,体
系文件应保存在适当的地方(体系文件指纸质的或电
06内审检查表

内审检查表序号准则要求审核内容和方法审核意见符合基本符合不符合缺此项评论与说明4.1 依法成立并能够承担相应法律责任的法人或者其他组织。
4.1.1 检验检测机构或者其所在的组织应有明确的法律地位,对其出具的检验检测数据、结果负责,并承担相应法律责任。
不具备独立法人资格的检验检测机构应经所在法人单位授权。
查:工商营业执照,工商营业执照营业范围应有相关检验检测或技术服务内容。
4.1.2 检验检测机构应明确其组织结构及质量管理、技术管理和行政管理之间的关系。
查:有无组织机构框图、质量职能分配表、质量保证框图。
(组织机构框图表述是否正确;质量职能分配表是否合理;质量保证框图是否明确,技术运作和支持服务之间的关系是否明确)4.1.3 检验检测机构及其人员从事检验检测活动,应遵守国家相关法律法规的规定,遵循客观独立、公平公正、诚实信用原则,恪守职业道德,承担社会责任。
查:是否有客观、公正、诚信的声明或承诺及相关的程序或制度,有无违规现象。
4.1.4 检验检测机构应建立和保持维护其公正和诚信的程序。
检验检测机构及其人员应不受来自内外部的、不正当的商业、财务和其他方面的压力和影响,确保检验检测数据、结果的真实、客观、准确和可追溯。
查:是否制定了保证公正性和诚信的程序文件;能否有效防止任何有损独立性和诚信度的活动;能否有措施防止任何形式的商业贿赂。
若检验检测机构所在的单位还从事检验检测以外的活动,应识别并采取措施避免潜在的利益冲突。
查:检测活动和检测以外的活动是否存在利益、从属、财务等关系,影响检测活动的独立性和公正性。
检验检测机构不得使用同时在两个及以上检验检测机构从业的人员。
查:机构人员一览表,上岗证和检验检测人员承诺书,是否对使用人员有管理规定和措施。
序号准则要求审核内容和方法审核意见符合基本符合不符合缺此项评论与说明是否有被使用人员的自身诚信性承诺。
人员是否有在两个及以上检验检测机构从业的情况。
4.1.5 检验检测机构应建立和保持保护客户秘密和所有权的程序,该程序应包括保护电子存储和传输结果信息的要求。
内部审核检查表
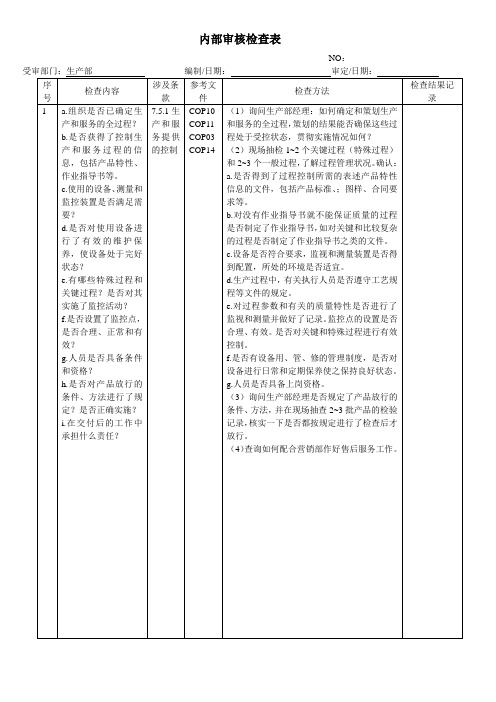
NO:
受审部门:生产部编制/日期:审定/日期:
序号
检查内容
涉及条款
参考文件
检查方法
检查结果记录
1
a.组织是否已确定生产和服务的全过程?
b.是否获得了控制生产和服务过程的信息,包括产品特性、作业指导书等。
c.使用的设备、测量和监控装置是否满足需要?
d.是否对使用设备进行了有效的维护保养,使设备处于完好状态?
询问生产技术部经理参加产品要求(合同)评审的情况以及如何配合营销部做好售后服务工作。
16
设计和开发
7.3
COP04
(1)询问生产技术部经理是否参加设计评审、设计确认。
(2)询问生产技术部经理是如何负责产品的工艺设计的,是如何根据其他部门的意见修改工艺文件的。
17
生产和服务提供的控制
7.5.1
COP11
(1)查看生产部资源是否充足。
6
以顾客为关注焦点
5.2
质量手册
COP24
询问2~3名员工,如何看待以顾客为关注焦点,如何将顾客的要求转化为相关工作要求并确实实施。
7
质量方针
5.3
质量手册
COP24
向生产部经理2~3名员工询问公司的质量方针是什么?如何为实现质量方针作出贡献?
8
质量目标
5.4
质量手册
COP24
内部审核检查表
NO:
受审部门:生产技术部编制/日期:审定/日期:
序号
检查内容
涉及条款
参考文件
检查方法
检查结果记录
1
a.组织内有哪些特殊过程?
b.是否对特殊过程进行了确认?确认时考虑了哪些因素?是否对确认的程序和方法进行了规定?
内审检查表全套(企业各部门通用)
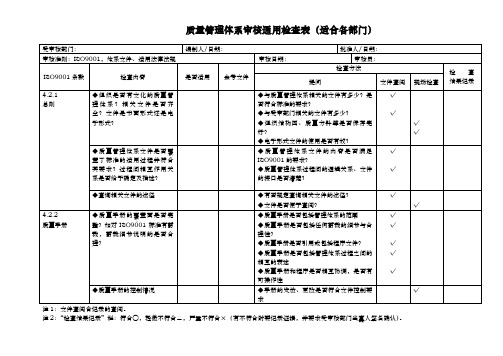
质量管理体系审核通用检查表(适合各部门)注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
IFS国际食品标准第6.1版内审检查记录表【IFS内部审核检查表】

审核日期:2020.07.07 审核员: 审核组长:
审核条款及审核内容
审核记录
审核结果
1高级管理层职责
1.1企业方针/企业原则
1.1.1企业高级管理层应制定和实施企业的方针。应至少包括:
□符合□不符合
–以客户为中心
–保护环境的责任
–可持续
–外部影响(如噪音,振动)。
□符合□不符合
评审的结果应为投资规划提供参考,并充分考虑到风险。
□符合□不符合
2质量和食品安全管理体系
2.1质量管理
2.1.1文件要求
2.1.1.1食品安全和质量管理体系应形成文件并得到执行,体系文件应保存在适当的地方(体系文件指纸质的或电子版的食品安全和质量手册)。
□符合□不符合
□符合□不符合
1.4.2管理评审应包括评估质量和食品安全管理体系的控制措施,以及持续改进的过程。
□符合□不符合
1.4.3企业应识别并定期评审(例如通过内部审核或现场检查)满足符合产品要求所需的基础设施。至少应包括以下内容:
□符合□不符合
–建筑物
□符合□不符合
–供应系统
□符合□不符合
–机器及设备
□符合□不符合
□符合□不符合
2.1.2记录保存
2.1.2.1所有与产品要求相关的记录都应完整,详尽,得到妥善的保管, 并应在需要时予以提供。
□符合□不符合
2.1.2.2记录应清楚、真实,应得到妥善保管,禁止事后修改记录。
□符合□不符合
2.1.2.3所有记录的保存期限应符合法规的要求,并至少保存至货架期结束后一年。对于没有货架期的产品,记录保存时间应有合理的理由,并且理由应形成文件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
IFS FOOD 标准要求
关键不符合项/严不符合项/不适用项
A
B
C
D
备注/注释
1
高级管理层职责
1.1
企业方针/企业原则
1.1.1
企业高级管理层应制定和实施企业的方针。应至少包
括:
–以客户为中心
–保护环境的责任
–可持续
–道德和员工职责
–产品要求(包括:产品的安全性、质量、合法性、
过程和规格书)
–企业方针应传达给所有员工。
–员工设施
–环境条件
–卫生条件
–工作场所设计
–外部影响(如噪音,振动)。
评审的结果应为投资规划提供参考,并充分考虑到风险。
2
质量和食品安全管理体系
2.1
质量管理
2.1.1
文件要求
2.1.1.1
食品安全和质量管理体系应形成文件并得到执行,体系文件应保存在适当的地方(体系文件指纸质的或电子版的食品安全和质量手册)。
2.2.1.3
企业应确保HACCP体系的建立参考了与产品生产和程序有关的科学文献或技术资料,并应随着新技术的发展及时更新。
2.2.1.4
应评审HACCP体系,且当产品、加工过程或任何步骤有任何变更时,HACCP体系应有必要的修订。
2.2.2
HACCP小组
2.2.2.1
组建HACCP小组(步骤1)
HACCP小组应是多学科的,并且包括操作人员。HACCP小组成员应具有ACCP体系的专门知识,了解产品工艺知识及相关的危害。当公司内人员能力不充分时,应获得外部专家的建议。
–成分
–物理、感官、化学和微生物参数
–产品的食品安全法规要求
–处理方法
–包装
–保质期(货架期)
–储存条件,运输和配送方法。
2.2.3.2
识别预期用途(步骤3)
产品预期用途须考虑到使用该产品的最终消费者,包括敏感消费群体的利益。
2.2.3.3
制定工艺流程图(步骤4)
每种产品或产品类别都应有生产流程图,并包括所有的过程和子过程的变化(包括返工和重新加工)。流程图应标注日期,注明所有的CCP及编号。有任何变化时,流程图应更新。
1.2.5
对产品要求有影响的员工,应意识到自己的职责,并应能够证明他们了解自己的职责。
1.2.6
企业应有最高管理者任命的一位IFS代表。
1.2.7
最高管理者应提供充足的资源,以满足产品的要求。
1.2.8
负责质量和食品安全管理的部门应直接向最高管理者进行报告。
1.2.9
企业应确保相关员工了解所有程序(文件化的和非文件化的)并且持续应用。
以客户为关注焦点
1.3.1
应建立文件化的程序,以识别顾客的基本需求和期望。
1.3.2
应对识别的结果进行评估,并以此来确定质量和食品安全目标。
1.4
管理评审
1.4.1
最高管理者应确保定期评审质量和食品安全管理体系,至少每年一次,当体系有变化时应增加评审的频率。此评审须至少包括:审核的结果,顾客反馈,过程符合性和产品符合性,预防和纠正措施的状态,上次管理评审的整改情况,可能影响食品安全和质量管理体系的变化和对于持续改进的建议。
2.2.2.2
负责建立和维护HACCP体系的人员应有一个内部的HACCP组长,并应接受足够的关于HACCP原理的应用方面的培训。
2.2.2.3
HACCP小组应获得高层管理的有力支持,应在整个组织内部得到组建和充分传达。
2.2.3
HACCP分析
2.2.3.1
产品描述(步骤2)
全面描述与产品安全有关的信息,例如:
1.4.2
管理评审应包括评估质量和食品安全管理体系的控制措施,以及持续改进的过程。
1.4.3
企业应识别并定期评审(例如通过内部审核或现场检
查)满足符合产品要求所需的基础设施。至少应包括以下内容:
–建筑物
–供应系统
–机器及设备
–运输。评审的结果应为投资 Nhomakorabea划提供参考,并充分考虑到风险。
1.4.4
企业应识别并定期评审(例如通过内部审核或现场检查)满足符合产品要求所需的工作环境。至少应包括以下内容:
2.1.2.2
记录应清楚、真实,应得到妥善保管,禁止事后修改记录。
2.1.2.3
所有记录的保存期限应符合法规的要求,并至少保存至货架期结束后一年。对于没有货架期的产品,记录保存时间应有合理的理由,并且理由应形成文件。
2.1.2.4
任何记录修改只能由经过授权的人员实施。
2.1.2.5
记录应安全保存,并容易获得。
1.2
组织结构
1.2.1
企业应建立组织结构图,表明其组织结构。
1.2.2
应明确规定职责和权限,包括职责代理。
1.2.3
应明确描述从事影响产品要求工作的员工的工作职责。
1.2.4
KO
第一个KO项:
最高管理者应确保员工都了解其与食品安全和质量有关的职责,并且建立机制,以监控其操作的有效性。此机制须明确并形成文件。
1.1.2
企业方针应在相关部门分解成具体的目标。各部门应明确其完成目标的职责和时限。
1.1.3
根据企业的方针,企业的质量和食品安全目标应传达给各个相关部门的员工,并应得到切实执行。
1.1.4
最高管理者应确保定期评审所有目标的完成情况,至少每年一次。
1.1.5
企业应确保所有与食品安全和质量有关的信息能有效并及时地向有关人员通报。
1.2.10
企业应建立相应的体系,以确保及时掌握与食品安全和质量有关的法规、科学和技术的发展,以及行业规范方面的信息。
1.2.11
企业应尽快通知其顾客与产品规格有关的任何问题,特别是由主管当局指出的可能发生的或者曾经发生的
与产品安全性和/或合法性有关的所有不符合,这些问题包括但不限于警示问题。
1.3
2.2
食品安全管理
2.2.1
HACCP体系
2.2.1.1
企业的食品安全控制体系应基于食品法典委员会的原则,应是系统的、综合的、全面实施的HACCP体系。应考虑到以上原则之外的生产国和目的国的法规要
求,HACCP体系应在每个生产场所予以实施。
2.2.1.2
HACCP体系应涵盖所有原材料,产品或产品系列,以及从产品到发货的所有过程,包括产品开发和产品包装。
2.2.3.4
现场确认流程图(步骤5)
2.1.1.2
应建立文件化的文件及其修改控制程序。
2.1.1.3
所有文件应清晰易读,意思明确、完整,并能随时供相关人员使用。
2.1.1.4
为符合产品要求所需的所有文件应是最新版本。
2.1.1.5
应记录任何修改文件的原因,特别是修改与产品要求相关的文件的原因。
2.1.2
记录保存
2.1.2.1
所有与产品要求相关的记录都应完整,详尽,得到妥善的保管,并应在需要时予以提供。
