高中化学竞赛试题顺反构象异构体
全国高中化学竞赛习题汇总

C生成3-甲基环戊酮并放出气泡;而D却只能得到3-甲基
-5-羰基已酸。
请给出下列物质的结构简式:A
B
C
D
。
A CH3
CH2 Cl
B CH3
CH3
Cl
C CH3
CH2
D CH3
CH3
3′ 分子式均为 C7H13Cl 的卤代烃A、B能发生下列反应:
A NaOH
ROH
C KMnO4 H+
O
+ 气泡
O
NaOH
B ROH
D KMnO4 H+
请写出A、B、C、D的结构简式。
COOH
A
Cl B
Cl C
D
4. 某有机物分子群分子式均为C8H12,经高锰酸钾酸性溶 液处理后,A得到丙二酸和乙基丙二酸各1 mol;B得到3乙酰基戊二酸并放出气泡;C得到丁二酸并见到大量气泡 放出。请给出A、B、C的结构简式并命名。
(2)
[Ag(NH3)2]+
Ag
NH4+ NH3
(3)
10.请画出六、六、六的所有异构体的结构简式。
Cl
Cl
Cl Cl
Cl Cl
体 dl
Cl Cl
Cl
Cl
Cl Cl
ε体
Cl Cl Cl
Cl Cl Cl
β体
Cl
Cl
Cl Cl
Cl Cl
η体
Cl
Cl Cl Cl
Cl Cl
γ体
Cl
Cl Cl
Cl
Cl Cl
A
B
9. 化合物 A 分子式为 C7H10 有弱酸性。经酸性高锰酸钾溶液处
理后得到 丙酸和 2-羰基丙酸各1mol,并有气泡放出。请给出A的 结构简式和A的系统命名;请写出它和多伦试剂(银氨溶液)反应 的方程式;请写出A的有弱酸性的含共轭结构的链式异构体的结构 简式:
2020年全国奥林匹克浙江省高中学生化学竞赛试题含详细答案及点拨

在化竞的学习过程中,掌握国初核心知识点、明确一条合理的学习路径至关重要。
化竞知识庞杂,不少学化竞的同学对于自己应该学什么,或先学什么后学什么摸不清头脑,甚至有些同学临近考前了,还在问这个知识点国初考不考,要不要学。
因为对国初核心知识点不够了解,并且没有一条清晰合理的学习路径,走了不少冤枉路。
温馨提醒:在开始学习国初知识之前,同学们需先研读全国高中学生化学(奥林匹克)竞赛基本要求(2008年4月版大纲),了解国初考试对知识点的要求。
以下为分模块需掌握的知识点:化学基本原理1.现代化学入门:宏观手段对物质的分类,原子的发现,测量,有效数字,化学计量,化学反应的质量关系2.原子结构:原子结构模型,原子轨道,电子排布,元素周期表,元素周期律3.成键&离子键:化学键,电负性,键的极性,离子,离子晶体结构4.共价键理论&分子结构:共价键,键能,Lewis结构,八隅体规则,价键理论,VSEPR理论,杂化轨道,分子轨道理论5.气体:气体的温度和压强,理想气体定律,Dalton分压定律,Henry定律6.液体和固体:分子间作用力,液态,金属和金属键,晶体结构初步7.溶液的性质:溶液的组成,溶解度,相似相溶,蒸气压,熔沸点,胶体8.化学热力学:焓,Hess定律,标准生成热,键能,熵,热力学第二定律,自发过程,自由能,自由能和平衡,Gibbs-Helmholtz方程及应用9.化学平衡:平衡条件,平衡常数,化学平衡的移动10.溶液中的平衡:酸碱平衡,沉淀溶解平衡,氧化还原平衡&电化学,配位平衡&配位结构初步11.化学动力学初步&核化学:反应速率,速率方程,反应机理,催化剂,放射性衰变,放射性的应用与防护,同位素,核裂变和核聚变有机化学1.有机结构基础:基本概念,成键和结构,有机酸碱理论2.烷烃、环烷烃、构象:烷烃、环烷烃、构象3.立体化学:对映异构、非对映异构、顺反异构、构象异构4.烷烃、自由基取代反应:自由基、自由基反应、烷烃的自由基反应5.卤代烃、亲核取代反应:卤代烃、碳正离子,SN1,SN26.消除反应:E1, E2, Substitution Vs Elimination7.醇、醚:醇、硫醇、醚、环氧8.烯、炔的加成反应:构对比;亲电、自由基、亲核加成9.烯、炔:氧化、还原、聚合反应10.醛、酮:羰基、亲核加成、α,β-不饱和醛酮的加成、氧化、还原、wittig反应11.羧酸、羧酸衍生物、胺:羧酸、羧酸衍生物、胺、卡宾12.缩合反应:烯醇、烷基化反应、与羰基反应13.共轭、芳香性:共轭体系、分子轨道理论、芳香性14.共振、芳环的取代反应:共振论、芳环亲电取代、芳环亲核取代15.周环反应:前线轨道、经典周环反应机理举例16.重排反应:经典重排反应机理举例17.有机波谱分析:IR、MS、NMR在有机产物和中间体结构表征中的综合应用。
立体异构

COOH HO H H OH COOH 2S, 3S HO HO
COOH H H COOH 2S, 3R
COOH OH H H OH COOH
由于内消旋体的存在使对映体数目< 2n
内消旋体 ---- 分子中虽有手性碳原子,但因有对称因素而使旋 光性在内部抵消,成为不旋光的物质(纯净物) 外消旋体----等量的左右旋体构成的混合物
正丁烷分子中,有三个C—C σ 键可以旋转,若选择C2—C3 单键旋转,可产生四个极限构象:
四种极限构象的稳定性次序为:全交叉式 > 斜交叉式 > 部 分重叠式 > 全重叠式
但它们之间的位能相差不大,常温时可以相互转变,达到动 态平衡。
环已烷也存在椅式和船式两种构象
He Ha
椅式 0 kJ/mol
Cl CH3 H H
.
H H Cl CH3
H H CH3 Cl
镜子
.
Cl CH3 H
Cl CH3 H
.
H H Cl CH3
转换为
H
H
实物分子
镜像分子
能够重合
分子中存在对称中心,该分子的镜像可以与实物重合
具有对称面的分子,不具有手性 ; 具有对称中心的分子和它的镜像能够叠合,不具有手性 。 对称中心的影响大于对称面(i>)
CH3 H Cl Cl H C2H5
CH3 H Cl Cl H C2H5
CH3 Cl H Cl H C2H5
【典型例题】
例1、指出下列化合物哪些具有旋光性。
分析:分子的手性 特征是其具有旋光性的 充分和必要条件。此题 主要是判断分子是否具 有手性。(1)含有一个 C*。含有一个C*的化合 物一定具有旋光性。 (5)、(6)中两个双 键(或两个环)所在平 面相互垂直,整个分子 没有对称面和对称中心, 因此是手性分子,具有 旋光性。
高中化学竞赛题--多手性旋光异构

中学化学竞赛试题资源库——多手性旋光异构A组1.材料一:在有机物中,有一类化合物的化学式相同,原子的连接方式和次序也相同(即结构式相同),但原子在空间排列的方式上不同,因而具有实物与镜像一样的结构,虽然这两种结构非常相似,但不能重叠,这种异构现象叫对映异构,这一对映异构之间的关系就旬人的左手和右手一样,故这类化合物的分子叫手性分子。
材料二:在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子就叫做手性碳原子或不对称碳原子,含有手性碳原子的分子一般是手性分子,手性分子就可能存在对映异构。
试回答下列问题:(1)3-氯-2-丁氨酸的结构简式为:一个3-氯-2-丁氨酸分子中含有个手性碳原子。
其中一对对映异构体用简单的投影式表示为(右图):则另一对对映异构体的简单投影式为:和()(2)化学式为的分子属于手性分子,一定条件下发生下列反应后,生成有机物仍然是手性分子的是:A 与乙酸发生酯化反应B 与氢氧化钠溶液共热C 在催化剂存在下与氢气作用D 与银氨溶液作用2.有机化学中常用各种投影式表示分子中各原子关系。
下面是D和L一甘油醛的投影式(图中A和B式),它们表示,如果以2—位碳原子为中心放在纸平面上,则该碳原子分别向纸后方向连接了—CHO和—CH2OH,向纸前方向连接了—H和—OH(横线表示向前,竖线表示向后),A式和B式非常相似互为镜像,但不能叠合(恰如左右手的关系),所以它们互为对应异构体。
本题中2—位碳原子属于手性碳原子(碳原子连接的四个基团各不相同)。
(1)请指出下面(1)~(6)哪几个跟A式完全相同(多一个或少一个各扣两分)(1) (2) (3) (4) (5) (6)(2)某化合物C 分子式为C 6H 10,催化氢化后得化合物D ,分子式C 6H 12,C 有手性,D 没有。
请写出C 的所有可能结构,用*表示其手性碳原子。
(3)右图是一种刚合成的有机化合物,用*表示出手性碳原子,并计算该化合物理论上的异构体数目3.下列各式为描述化合物立体结构的构型式,请判断各对构型式是否代表同一种化合物(用“是”或“不是”表示)。
顺反构象异构体

顺反构象异构体A组F2)分子中的四个原子都在一个平面上,i.二氟二氯(N由于几何形状的不同,它有两种同分异构体,如右图所示。
这种原子排布次序相同,几何形状不同的异构体被称为几何异构体,在下列化合物中存在着几何异构体的是A CHCl=CHClB CH2=CCl2C CH2=CHCH2CH3D CH3C≡CHii.NH2有两种同分异构体,是哪两种?为什么C2H2无同分异构体?2iii.因有机物分子中碳碳双键()不能旋转而产生的同分异构体叫顺反异构体。
某些顺反异构体在光的照射下可以相互转化,例如顺式丁烯二酸反式丁烯二酸人和高等动物眼睛里的光敏细胞中含有镶嵌在视蛋白中的单顺式视黄醛,在光的作用下可转化为全反式视黄醛:单顺式视黄醛全反式视黄醛由于全反式视黄醛分子的侧链是“直”的,导致其脱离视蛋白,并由此引起人和动物的视觉。
(1)视黄醛分子的顺反异构体共有A 4种B 8种C 16种D 32种(2)1mol视黄醛分子与H2充分发生加成反应时要消耗mol H2。
(3)将视黄醛链端的-CHO还原为-CH2OH即得维生素A。
以下关于维生素A的叙述中正确的是A 人体缺乏维生素A时易患夜盲症B 维生素A是易溶于水的醇B 侧链上的碳原子都在同一平面上D 所有碳原子都在同一平面上B组iv.下列化合物中,有顺、反异构体的是A C6H5CH=CH2B C6H5-NH-OHC C6H5CH=N-OHD C6H5-NH-NH2v.1,2,3,4,5,6-环己六醇的所有异构体(包括顺反、旋光)共有A 7个B 8个C 9个D 10个vi.下列化合物中哪一个,其偶极短显然不等于零。
A B CD Evii.分子式为CH10的烃的同分异构体中,属于顺反异构的结构式是,具有对5映异构的结构式是。
viii.如果不考虑环形化合物,下列分子的构造异构体和几何异构体是多少?(1)C3H5Cl,(2)C3H4Cl2,(3)C4H7Cl,(4)C5H10?ix.写出CH8的所有构造异构体和几何异构体?4x.下面化学式分别能画出几种构造异构体:(1)CH12,(2)C3H7Cl,(3)C3H6Cl2,(4)5C4H8Cl2,(5)C5H ll Cl,(6)C6H14,(7)C7H16xi.用纽曼投影式面出乙烷的重叠式构象和交叉式构象,并回答下列问题:(1)乙烷的重叠式构象和交叉式构象是乙烷仅有的两种构象吗?(2)室温下乙烷的优势构象是哪一种?为什么?(3)温度升高时构象会发生什么变化?xii.用纽曼投影式画出下列化合物的交叉式构象,并比较其稳定性:(1)CH3CH2-CH2CH3(2)(CH3)2CH-CH2CH3xiii.将下列透视式改写成相应的纽曼投影式:xiv.下列化合物是否有顺反异构体?若有,试写出它们的顺反异构体。
中学化学竞赛试题资源库——顺反构象异构体
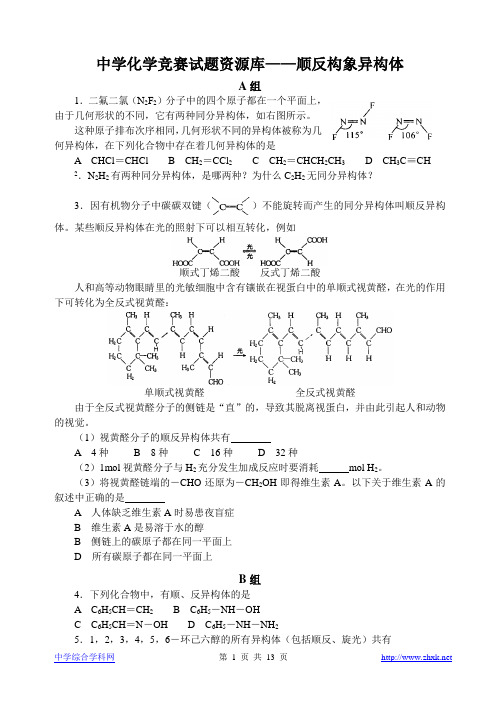
中学化学竞赛试题资源库——顺反构象异构体A组1.二氟二氯(N2F2)分子中的四个原子都在一个平面上,由于几何形状的不同,它有两种同分异构体,如右图所示。
这种原子排布次序相同,几何形状不同的异构体被称为几何异构体,在下列化合物中存在着几何异构体的是A CHCl=CHClB CH2=CCl2C CH2=CHCH2CH3D CH3C≡CH2.NH2有两种同分异构体,是哪两种?为什么C2H2无同分异构体?23.因有机物分子中碳碳双键()不能旋转而产生的同分异构体叫顺反异构体。
某些顺反异构体在光的照射下可以相互转化,例如顺式丁烯二酸反式丁烯二酸人和高等动物眼睛里的光敏细胞中含有镶嵌在视蛋白中的单顺式视黄醛,在光的作用下可转化为全反式视黄醛:单顺式视黄醛全反式视黄醛由于全反式视黄醛分子的侧链是“直”的,导致其脱离视蛋白,并由此引起人和动物的视觉。
(1)视黄醛分子的顺反异构体共有A4种 B 8种 C 16种 D 32种(2)1mol视黄醛分子与H2充分发生加成反应时要消耗mol H2。
(3)将视黄醛链端的-CHO还原为-CH2OH即得维生素A。
以下关于维生素A的叙述中正确的是A人体缺乏维生素A时易患夜盲症B 维生素A是易溶于水的醇B 侧链上的碳原子都在同一平面上D 所有碳原子都在同一平面上B组4.下列化合物中,有顺、反异构体的是A C6H5CH=CH2B C6H5-NH-OHC C6H5CH=N-OHD C6H5-NH-NH25.1,2,3,4,5,6-环己六醇的所有异构体(包括顺反、旋光)共有A7个 B 8个 C 9个 D 10个6.下列化合物中哪一个,其偶极短显然不等于零。
A B CD E7.分子式为C5H10的烃的同分异构体中,属于顺反异构的结构式是,具有对映异构的结构式是。
8.如果不考虑环形化合物,下列分子的构造异构体和几何异构体是多少?(1)C3H5Cl,(2)C3H4Cl2,(3)C4H7Cl,(4)C5H10?9.写出C4H8的所有构造异构体和几何异构体?10.下面化学式分别能画出几种构造异构体:(1)C5H12,(2)C3H7Cl,(3)C3H6Cl2,(4)C4H8Cl2,(5)C5H ll Cl,(6)C6H14,(7)C7H1611.用纽曼投影式面出乙烷的重叠式构象和交叉式构象,并回答下列问题:(1)乙烷的重叠式构象和交叉式构象是乙烷仅有的两种构象吗?(2)室温下乙烷的优势构象是哪一种?为什么?(3)温度升高时构象会发生什么变化?12.用纽曼投影式画出下列化合物的交叉式构象,并比较其稳定性:(1)CH3CH2-CH2CH3(2)(CH3)2CH-CH2CH313.将下列透视式改写成相应的纽曼投影式:14.下列化合物是否有顺反异构体?若有,试写出它们的顺反异构体。
高中化学竞赛试题配位结构和异构

中学化学竞赛试题资源库——配位结构和异构A 组1.已知[Co(NH 3)6]3+呈正八面体结构:各NH 3分子间距相等,Co 3+位于正八面的中心。
若其中二个NH 3分子被Cl -取代,所形成的[Co(NH 3)4Cl 2]+的同分异构体的种数有A 2种B 3种C 4种D 5种2.Co(NH 3)63+离子是正八面体而非三棱柱或平面六边形构型的理由是A 其一氯取代物不存在同分异构体B 它是非极性分子C 它的键长与键角都相等D 其二氯取代物只存在两种同分异构体3.我国科学工作者合成了许多结构复杂的天然有机化合物,如叶绿素、血红素、维生素B 12等。
叶绿素的结构如图。
下列有关说法中正确的是 A 叶绿素属于高分子化合物 B 叶绿素分子中含有三种类型的双键 C 叶绿素不属于芳香烃 D 在一定条件下,叶绿素能发生加成、水解、酯化等反应 4.本题涉及4种组成不同的配合物,它们都是平面正方形结构。
(1)PtCl 2·2KCl 的水溶液与二乙硫醚(Et 2S )反应(摩尔比1︰2)得到两种结构不同的黄色配合物,该反应的化学方程式和配合物的立体结构是:(2)PtCl 2·2KCl 的水溶液与足量Et 2S 反应获得的配合物为淡红色晶体,它与AgNO 3反应(摩尔比1︰2)得到两种组成不同的配合物,写出上述两个反应的化学方程式。
5.本题涉及3种组成不同的铂配合物,它们都是八面体的单核配合物,配体为OH -和/或Cl -。
(1)PtCl 4·5H 2O 的水溶液与等摩尔NH 3反应,生成两种铂配合物,反应式为: (2)BaCl 2·PtCl 4和Ba(OH)2反应(摩尔比2︰5),生成两种产物,其中一种为配合物,该反应的化学方程式为: 6.铍及锌分别为ⅡA 及ⅡB 族元素,在很多性质上相类似。
例如,它们的氧化物及其水合物表现为两性,卤化物有显著的共价性,易于形成配位数为4的配合物。
化学竞赛题库化学键与分子几何构型答案

B
. . . . C C N. . . . . .
(2) BC2N 分子是直线型的,所以(BC2N)n 理应属于一维晶体。 (3) 既然(BC2N)n 可以制成单壁纳米管材料,这说明(BC2N)n 首先应聚合成二维平面, 然后受外力而卷曲成单壁纳管材料,所以每个原子都应象石墨中的 C 原子那样, 采取 sp2 杂化,然后聚合成下面的单层结构:
船式
八、1.K︰C =
0.289 0.711 ︰ =7.39 ´ 10-3︰0.05925 = 1︰8 该化合物的分子式为 KC8。 39.10 12.00
2.2KC8 + 2C2H5OH KC8 + C2H5OH
2C2H5OK + H2 + 16C(graphite) C2H5OK + C8H
3.存在离子键。金属 K 失去价电子(4s1) ,成为 K+离子层,插入石墨层之间,石墨层获
23 ´ 14.01 = 0.9124 23 ´ 14.01 + M X
解得 MX = 30.9
0.9124MX = 28.227
-
∴该元素为 P,故(D)的离子式为[N5+][P(N3)6 ] 4[N5+][P(N3)6 ] + 5O2
-
P4O10 + 46N2
二、1.类硼为 Sc,类铝为 Ga,类硅为 Ge。要预言元素,只能预言一周期中的中间元素, 通过前、后两元素的性质比较,才能确定是否存在有中间元素。但稀有气体是一周期中
Cl P N Cl
Cl N P Cl
Cl P N Cl
Cl N
2. N
Cl
这两种结构式都有 N2PCl2 四面体最小重复单元。
高中化学竞赛总训练4化学键理论与分子几何构型

中学化学竞赛总训练四、化学键理论与分子几何构型1.NO的生物活性已引起科学家高度重视,它与O2-反应,生成A。
在生理pH条件下,A的t1/2= 1~2秒。
⑴写出A的可能的Lewis结构式,标出形式电荷。
推断它们的稳定性。
⑵A与水中的CO2快速一对一地结合,试写出此物种可能的路易斯结构式,表示出形式电荷,推断其稳定性。
⑶含Cu+的酶可把NO2-转化为NO,写出此反应方程式。
⑷在固定器皿中,把NO压缩到100atm,发觉气体压强快速降至略小于原压强的2/3,写出反应方程式,并说明为什么最终的气体总压略小于原压的2/3。
2.试画出N5+离子的Lewis全部可能结构式,标出形式电荷,探讨各自稳定性,写出各氮原子之间的键级。
你认为N5+的性质如何?它应在什么溶剂中制得。
3.在地球的电离层中,可能存在下列离子:ArCl+、OF+、NO+、PS+、SCl+。
请你预料哪一种离子最稳定?哪一种离子最不稳定?说明理由。
4.硼与氮形成类似苯的化合物,俗称无机苯。
它是无色液体,具有芳香性。
⑴写出其分子式,画出其结构式并标出形式电荷。
⑵写出无机苯与HCl发生加成反应的方程式⑶无机苯的三甲基取代物遇水会发生水解反应,试推断各种取代物的水解方程式,并以此推断取代物可能的结构式。
⑷硼氮化合物可形成二元固体聚合物,指出这种聚合物的可能结构,并说明是否具有导电性。
⑸画出Ca2(B5O9)Cl·2H2O中聚硼阴离子单元的结构示意图,指明阴离子单元的电荷与硼的哪种结构式有关。
5.用VSEPR理论推断下列物种的中心原子实行何种杂化类型,指出可能的几何构型。
(1)IF3(2)ClO3-(3)AsCl3(CF3)2(4)SnCl2(5)TeCl4(6)GaF63-170℃ 6.试从结构及化学键角度回答下列问题:一氧化碳、二氧化碳、甲醛、甲酸等分子(1)画出各分子的立体构型,并标明各原子间成键状况(σ、π、Πmn ) (2)估计分子中碳—氧键的键长改变规律7.近期报导了用二聚三甲基铝[Al(CH 3)3]2 (A)和2, 6 —二异丙基苯胺(B)为原料,通过两步反应,得到一种环铝氮烷的衍生物(D): 第一步:A + 2B === C + 2CH 4其次步:□C □D + □CH 4 (□中填入适当系数)请回答下列问题:(1)分别写出两步反应配平的化学方程式(A 、B 、C 、D 要用结构简式表示 (2)写出D 的结构式(3)设在第一步反应中,A 与过量B 完全反应,产物中的甲烷又全部挥发,对反应后的混合物进行元素分析,得到其质量分数如下:C (碳):73.71%,N (氮):6.34% 试求混合物中B 和C 的质量分数(%)(已知相对原子量:Al :26.98、C :12.01、N :14.01、H :1.01)8.四氨合铜(II)离子在微酸性条件下,与二氧化硫反应生成一种沉淀物(A),该沉淀物中Cu:N:S (原子个数比)=1:1:1,结构分析证明:存在一种正四面体和一种三角锥型的分子或离子,呈逆磁性。
第07讲——顺反异构和构象异构

4、取代环己烷的构象
(1)一取代环己烷,连e键比连a键稳定
H H
R
R
基团越大,e键取代构象越多。
基团 e式占比例
—CH3 95%
—CH(CH3)2 —C(CH3)3
环丙烷 ——平面结构,完全重叠式,扭转张 力、角张力均较大,不稳定。
环丁烷 ——3平1高,不完全重叠式 构象,扭转张力有所减小、角张力 增大,总体不稳定。
环戊烷 ——4平1高,基本交叉式构象,扭 转张力、角张均较小,稳定。
分类 小环 普通环 中环 大环
环数 3-4
5-7 8-12 >12
07-9 环癸烷
反-1,2-二甲
基环丙烷
基环丙烷 CH3
(3)若多于两个基团,选择位次最小者作为标准(r)
?
Cl
反-1, 顺- 2-二氯- r- 环戊烷甲酸
1 Cl 2
3 Cl r- 1,反- 2, 顺-3-三氯环戊烷
COOH Cl 1
2Cl H
3基①CH团按I>3第大B2一小r>原如CO子何1lH>的排F原序>子—O>—序反N“数次>-,5序-C氯由>规-大rH则-1到,”4顺小–C-3排C3l->O环列O–己CH2烷(CC二HO3甲O)3H酸
优势构象? 07-5 环己烷椅式船式比较
椅式构象(99.9%) 船式构象
4
6 2
5 3
1
无张力环
4 5
6 键角均 4 5 6 1
3
2
为109.50 1
3
2
纽曼投影式
4
高中化学竞赛试题(有机化学)

高中化学竞赛试卷(有机化学)高二化学(实验班)第Ⅰ卷(60分)一、选择题(每题只有1个选项,每题2分) 1.下列化合物存在顺反异构体的是A .1-丁烯B .2-丁烯C .1,1-二氯-1-丙烯D .2-甲基-1-丙烯2.(CH 3)2CHCH 2Cl 与(CH 3)3CCl 是什么异构体 (A)碳架异构 (B) 位置异构 (C) 官能团异构 (D) 互变异构 3.异戊二烯经臭氧化,在锌存在下水解,可得到哪一种产物? (A) HCHO + OHCCH 2CHO (B) HCHO + HOOCCH 2COOH(C) HCHO + CH 3COCHO(D) CH 3COCHO + CO 2 + H 2O4.在NaOH 水溶液中,(CH 3)3CX(I),(CH 3)2CHX(II),CH 3CH 2CH 2X(III),CH 2=CHX(IV)各卤代烃的反应活性次序为: (A )I>II>III>IV (B) I>II>IV>III (C) IV>I>II>III (D) III>II>I>IV 5.下列四种离子,碱性最强的是: (A)HO - (B)CH 3O - (C)C 6H 5O - (D)CH 3COO - 6.下列化合物哪个没有芳香性+A. B. C. D.7.沸点升高的顺序是:(A) I,II,III,IV (B) IV,III,II,I(C) I,II,IV ,III (D) I II,IV,II,I8.用Grignard 试剂合成 , 不能使用的方法是什么?(A) C 6H 5COCH 3CH 3CH 2MgBr(B) CH 3CH 2CCH 3OC 6H 5MgBr(C) C 6H 5CCH 2CH 3CH 3MgI(D) C 6H 5MgBr CH 3CHO++++C 6H 5CCH 3OHCH 2CH 39.上述构型的正确命名是: (A )(1)R (2)R (3)S (B )(1)R (2)S (3)S (C )(1)S (2)S (3)S (D )(1)R (2)R (3)R 10.下列构象的稳定性顺序为:11.薄荷醇 理论上所具有的立体异构体数目应为:(A) 8种 (B) 16种 (C) 2种 (D) 4种 12.下列化合物与AgNO 3/醇溶液反应,活性最大为A .氯苄B .对甲基氯苄C .对硝基氯苄D .氯苯13.在稀碱作用下,下列哪组反应不能进行羟醛缩合反应? (A) HCHO + CH 3CHO (B) CH 3CH 2CHO + ArCHO (C) HCHO + (CH 3)3CCHO (D) ArCH 2CHO + (CH 3)3CCHO14.下列四个试剂,不跟CH 3CH 2COCH 2CH 3反应的是: (A) RMgX (B) NaHSO 3饱和水溶液 (C) PCl 5 (D) LiAlH 415.下面的氧化反应,用何种氧化剂较好(A) K 2Cr 2O 7/H + (B) CrO 3·吡啶 (C) Ag(NH 3)2+ (D) 稀、冷KMnO 416.C 6H 5OCH 3(I),C 6H 5COCH 3(II),C 6H 6(III),C 6H 5Cl(IV)四种化合物硝化反应速率次序为: (A) I>III>II>IV (B) I >III>IV>II(C) IV>I>II>III (D) I>IV>II>III17.傅-克反应烷基易发生重排,为了得到正烷基苯,最可靠的方法是: (A) 使用AlCl 3作催化剂 (B) 使反应在较高温度下进行H NH 2CH 3Ph Br CH 2OHCH 3H Cl CH 2NH 2CH 2NHCH 3Br (1)(2)(3)CH O CO 2H OH(C) 通过酰基化反应,再还原 (D) 使用硝基苯作溶剂 18.下列化合物进行E2反应,哪个活性最大?C H 3Cl (CH 3)3C Cl(CH 3)3C ClA. B. C.19.由苯合成对氯间硝基苯磺酸可由三步反应完成,你看三步反应以哪个顺序较好?(A) (1)磺化 (2)硝化 (3)氯化 (B) (1)氯化 (2)磺化 (3)硝化 (C) (1)硝化 (2)磺化 (3)氯化 (D) (1)氯化 (2)硝化 (3)磺化 20.确定有机反应属于哪种类型:(A) 亲电反应 (B) 亲核反应 (C) 自由基反应 (D) 周环反应21.在下列化合物中,能被2,4-二硝基苯肼鉴别出的是: (A) 丁酮 (B) 丁醇 (C) 丁胺 (D) 丁腈 22.下述反应不能用来制备α,β-不饱和酮的是:(A) 丙酮在酸性条件下发生羟醛缩合反应 (B) 苯甲醛和丙酮在碱性条件下加热发生羟醛缩合 (C) 甲醛与苯甲醛在浓碱条件下反应(D) 环己烯臭氧化水解, 然后在碱性条件下加热反应 23.下列各酯水解速率最快的是: (A) CH 3CH 2CO 2CH 3 (B) CH 3CO 2CH 3 (C) (CH 3)2CHCO 2CH 3 (D) HCO 2CH 3 24.下列各化合物中,碱性最弱的一个是:25.为合成 应采用乙酰乙酸乙酯和下列哪种试剂反应?(A) 碘甲烷及溴丙烷 (B) 2-氯戊烷 (C) 溴;乙烷及溴丙烷 (D) 乙酰溴26.合成 应采用丙二酸二乙酯二钠盐与下列哪种化合物作用?(A) (B) B rCH 2CH 2Br(C) BrCH 2COOH (D) 2molCH 3I27.下列化合物的亚甲基哪个活性(或相对酸性)最强?HCN(CH 3)2C CH 2COCH 3CN(CH 3)2C CHCOCH (A) CH 3CNHCH 3 (B) PhNH 2 (C) CH 3CNH 2 (D) O ONH O O CH 3CCHCH 2CH 2CH 3O CH 3COOHBr (D)(C)(B)(A)CH 3CCH 2CCH 3O O CH 3CCH 2COC 2H 5O O CH 3C O H 5C 2OCCH 2COC 2H 5O O CH 2NO 228.可以进行分子内酯缩合的二酯是: (A) 丙二酸二乙酯 (B) 丁二酸二乙酯 (C) 对苯二甲酸二乙酯 (D) 己二酸二乙酯29.下列哪化合物不能发生碘仿反应C 2H 5OHO OHOH CH 3A. B. C. D.30.心酮胺是治疗冠心病的药物。
高中化学奥林匹克竞赛(有机化学)高二检测题(附答案)
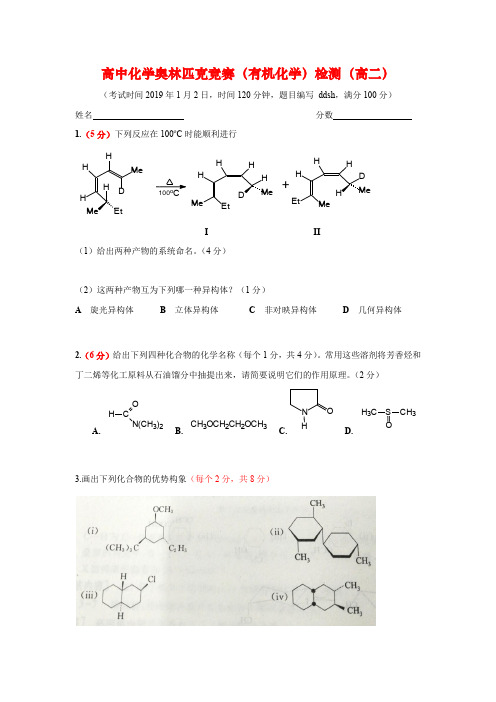
高中化学奥林匹克竞赛(有机化学)检测(高二)(考试时间2019年1月2日,时间120分钟,题目编写 ddsh ,满分100分) 姓名 分数 1.(5分)下列反应在100o C 时能顺利进行I II(1)给出两种产物的系统命名。
(4分)(2)这两种产物互为下列哪一种异构体?(1分)A 旋光异构体B 立体异构体C 非对映异构体D 几何异构体2.(6分)给出下列四种化合物的化学名称(每个1分,共4分)。
常用这些溶剂将芳香烃和丁二烯等化工原料从石油馏分中抽提出来,请简要说明它们的作用原理。
(2分)A. B.C.D.3.画出下列化合物的优势构象(每个2分,共8分)+H CO N(CH 3)2CH 3OCH 2CH 2OCH 3N OHH 3C S OCH 34.判断下列分子是否具有光学活性(共10分)5.下列各组化合物都能够发生分子内的SN2反应。
对各组反应的难易程度进行排序(6分)6.(每式1分,每个命名1分,共9分)2004年是俄国化学家马科尼可夫(V . V . Markovnikov ,1838-1904)逝世100周年。
马科尼可夫因提出C =C 双键的加成规则(Markovnikov Rule )而著称于世。
本题就涉及该规则。
给出下列有机反应序列中的A 、B 、C 、D 、E 、F 和G 的结构式,并给出D 和G 的系统命名。
7.(13分)写出下列反应的每步反应的主产物(A 、B 、C )的结构式;若涉及立体化学,请用Z 、E 、R 、S 等符号具体标明。
(B 是两种几何异构体的混合物)8.(13分)以氯苯为起始原料,用最佳方法合成1-溴-3-氯苯(限用具有高产率的各反应,标明合成的各个步骤)。
CH 2COOH CH 2COOHACH CHO(等摩尔)BHBrC9.(10分)用苯、不超过四个碳的有机化合物和合适的无机试剂为原料合成以下产物:10.(20分)写出下列转化的反应流程高中化学奥林匹克竞赛(有机化学)检测(高二)(答案和评分)(满分100分,时间120分钟)考试时间2019年1月2日 试题编制 dds姓名 分数 1. (5分) 下列反应在100o C 时能顺利进行:I II(1)给出两种产物的系统命名。
2023年化学竞赛有机化学专项训练
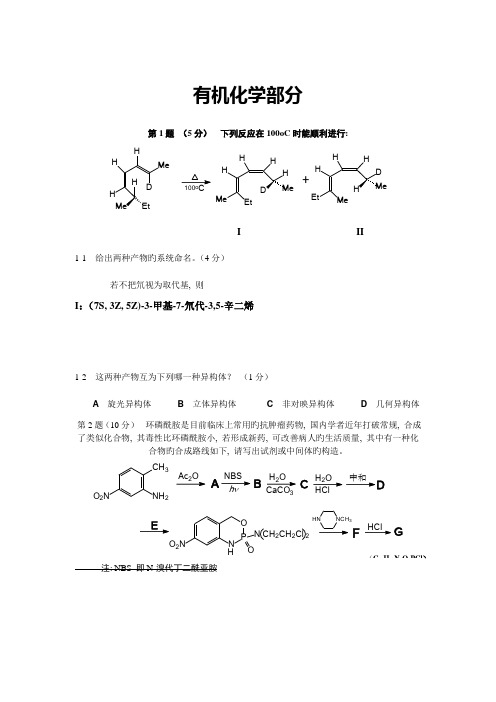
有机化学部分第1题(5分)下列反应在100oC时能顺利进行:+I II1-1 给出两种产物旳系统命名。
(4分)若不把氘视为取代基, 则I:(7S, 3Z, 5Z)-3-甲基-7-氘代-3,5-辛二烯1-2 这两种产物互为下列哪一种异构体?(1分)A旋光异构体B立体异构体C非对映异构体D几何异构体第2题(10分)环磷酰胺是目前临床上常用旳抗肿瘤药物, 国内学者近年打破常规, 合成了类似化合物, 其毒性比环磷酰胺小, 若形成新药, 可改善病人旳生活质量, 其中有一种化合物旳合成路线如下, 请写出试剂或中间体旳构造。
CH3O2N NH22AhB H2O3C H2OHClEO2N NPOON CH2CH2ClHNCH3HNHCl G 注: NBS 即N-溴代丁二酰亚胺第3题 (10分) 以氯苯为起始原料, 用最佳措施合成1-溴-3-氯苯(限用品有高产率旳各反应, 标明合成旳各个环节)。
第4题 (11 分)4-1画出下列转换中A.B.C 和D 旳构造简式(不规定标出手性)。
A (C 14H 26O 4) B (C 12H 22O 2)12H 24O )D (C 12H 22Br 1. Mg/苯1. LiAlH 4 无水醚22. H 2O4-2 画出下列两个转换中产物1.2和3旳构造简式, 并简述在相似条件下反应, 对羟基苯甲醛只好到一种产物, 而间羟基苯甲醛却得到两种产物旳原因。
CHOOHCH 3(CH 2)11Br, K 2CO 3丙酮,回流1CH 3(CH 2)11Br, K 2CO 3丙酮,回流2CHOOH3+原因:第5题 ( 7 分) 灰黄霉素是一种抗真菌药, 可由A 和B 在三级丁醇钾/三级丁醇体系中合成, 反应式如下:(CH 3)3COK/ (CH 3)3COHOOOCH 3H 3COClOO OCH 3H 3COClO HCH 3OH 3COCCCCH +AB灰黄霉素OCHCH 3CH35-1在下面灰黄霉素构造式中标出不对称碳原子旳构型。
高级中学化学同分异构体的练习题和答案.doc

高中化学同分异构体的练习题和答案高中化学同分异构体的练习题同分异构体立体异构2顺反异构:双键的不可旋转,使双键碳原子连有两个不同基团时,会产生顺反异构。
必须条件:和,实例:对映异构:在有机物分子中,若某碳原子连接着四个不同的原子或原子团,这种碳原子称为手性碳原子,有1个手性碳原子,存在两种对映异构体。
必须条件:实例:1.1,2,3一三苯基环丙烷的3个苯基可以分布在环丙烷环平面的上下,因此有如下2个异构体。
[ 是苯基,环用键线表示。
C、H原子都未画出]据此,可判断1,2,3,4,5一五氯环戊烷(假定五个碳原子也处于同一平面上)的异构体数是( )A.4 B.5 C6 D72.已知化合物C6H6(苯)与B3N3H6(硼氮苯)的分子结构相似,如图所示,则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为()A.2B.3C.4D.63.已知与互为同分异构体(顺反异构),则化学式为C3H5Cl的链状的同分异构体有( )A.3种B.4种C.5种D.6种4.烯烃分子中双键两侧的基团在空间的位置不同,也可引起同分异构顺反异构。
例如:与是同分异构体。
请回答组成为C5H10的有机物,其所有同分异构体中属于烯烃的共有()A.4种B.5种C.6种D.7种5.在有机物分子中,当一个碳原子连有4个不同的原子或原子团时,这种碳原子被称为手性碳原子,凡具有一个手性碳原子的化合物一定具有光学活性,常在某些物理性质、化学变化或生化反应中表现出奇特的现象。
例如:其中带*号的碳原子即是手性碳原子,现欲使该物质因不含手性碳原子而失去光学活性,下列反应中不可能实现的是()A、加成反应B、消去反应C、水解反应D、氧化反应6.手性分子是早就为化学工作者熟知的,但美国和日本的三位科学家却因为他们在手性分子可用来加速并控制化学反应方面的创造性工作,分享了2001年诺贝尔奖。
在有机物分子中,若某碳原子连接着四个不同的原子或原子团,这种碳原子称为手性碳原子,凡只有一个手性碳原子的物质一定具有光化学活性。
(完整word版)高中化学竞赛配位化合物练习

配合物选择题:1、(NH4)3[CrCl2(SCN)4]的名称是()A.二氯四硫氰酸根合铬(Ⅲ)酸铵B.四硫氰酸根二氯合铬(Ⅲ)酸铵C.四异硫氰酸根二氯合铬(Ⅲ)酸铵D. 二氯四异硫氰酸根合铬(Ⅲ)酸铵2、Ni(CO)4,Ni(CN)42-,Ni(NH3)62+的空间构型分别为()A.正四面体,正四面体,正八面体B.平面正方形,平面正方形,正八面体C.正四面体,平面正方形,正八面体D.平面正方形,变形八面体,正八面体3、某金属离子在八面体弱场中的磁矩为4.90B.M,而在八面体强场中的磁矩为0,该离子是( )A.Cr3+B. Mn2+C. Fe2+D. Co2+E. Ni2+F. Fe3+4、在配位数为4的Co2+四面体配合物与平面方形配合物(低自旋)中,未成对电子数分别为()A.2与0B.2与1C.3与0D.3与15、根据有效原子序数规则(EAN),下列配合物化学式正确的是()A.Fe(CO)3B. Fe(CO)4C. Fe(CO)5D. Fe(CO)66、在H x Co(CO)4中,x值应为()A.1B.2C.3D.47、已知M为配合物的中心原子,A、B、C为配体,在具有下列化学式的配合物中,哪一个有两种异构体()A.MA5CB.MA6C.MA2B2C2D.MA2BC(平面方形)8.根据十八电子规则,[(CO)3Ni-Co(CO)3]Z中Z值为A +B 3+C 3-D 09、在下列配离子中,存在几何异构体的是()A.[Cr(NH4)5Cl]2+B.[Pt(py)BrClNH3]C.[Cr(en)Cl4]-D.Cr(en)33+10、下列配离子中,属于反磁性的是()A.Co(CN)63—B.Cu(NH3)42+C.Fe(CN)63—D.Mn(CN)64—11、下列配合物中,除存在几何异构体外,还存在旋光异构体的是()A.[Pt(NH3)2Cl2]B.[Co(NH3)4Cl2]ClC.[Co(en)2Cl2]ClD.[PtNH3ClBr(py)]12、按照18电子规则,下列各配合物中应当以双聚体存在的是()A.Mn(CO)4NOB.Fe(CO)5C.Cr(CO)6D.Co(CO)413、两种配合物[PtBr(NH3)3]NO2和[PtNO2(NH3)3] Br互为( )A.键合异构B.配位异构C.电离异构D.聚合异构14.已知[Fe(C2O4)3]3-的磁矩大于5.75B.M;其空间构型及中心离子的杂化轨道类型是()。
高中化学异构体试题及答案

高中化学异构体试题及答案一、选择题1. 下列化合物中,属于碳链异构的是:A. 甲烷和乙烷B. 乙烷和乙烯C. 甲烷和甲醛D. 甲烷和乙醇2. 同分异构体是指具有相同分子式但:A. 不同结构的化合物B. 不同化学性质的化合物C. 不同物理性质的化合物D. 不同元素组成的化合物3. 以下哪种异构体是位置异构体?A. 正丁烷和异丁烷B. 1-丁烯和2-丁烯C. 乙醇和甲醚D. 环己烷和甲基环戊烷4. 官能团异构体是指:A. 具有不同官能团的化合物B. 具有相同官能团但不同位置的化合物C. 具有相同分子式但不同官能团的化合物D. 具有不同分子式但相同官能团的化合物5. 以下化合物中,哪些是同分异构体?A. 乙醇和甲醚B. 甲酸和甲酸甲酯C. 丙酮和乙酸D. 乙酸和乙酸乙酯二、填空题6. 写出分子式为C4H10O的两种醇的同分异构体名称。
7. 异构体分为几种类型,请列举并简述每种类型的特点。
三、简答题8. 解释什么是碳链异构,并给出一个具体的例子。
9. 请简述官能团异构体和位置异构体的区别。
四、计算题10. 某化合物分子式为C5H12O,已知其为醇类化合物,请写出所有可能的同分异构体,并说明它们属于哪种异构类型。
答案一、选择题1. A2. A3. A4. C5. A二、填空题6. 正丁醇和异丁醇。
7. 异构体分为碳链异构、位置异构、官能团异构和立体异构四种类型。
碳链异构是指碳原子骨架不同;位置异构是指官能团在碳链上的位置不同;官能团异构是指具有相同分子式但官能团不同的化合物;立体异构是指分子中的原子在空间排列方式不同。
三、简答题8. 碳链异构是指具有相同分子式,但碳原子骨架不同的化合物。
例如,正丁烷和异丁烷都是C4H10,但它们的碳链结构不同。
9. 官能团异构体是具有相同分子式但官能团不同的化合物,如乙醇和甲醚;位置异构体是具有相同分子式和官能团,但官能团在碳链上的位置不同,如1-丁烯和2-丁烯。
四、计算题10. C5H12O的可能同分异构体包括:- 正戊醇(1-戊醇)- 异戊醇(2-戊醇)- 新戊醇(3-戊醇)- 叔戊醇(2-甲基-1-丁醇)- 异戊醇(3-甲基-1-丁醇)- 叔戊醇(2-甲基-2-丁醇)这些醇的异构类型主要是碳链异构和位置异构。
2019年全国奥林匹克北京市高中化学竞赛(选拔赛)试题含详细答案及指导

在化竞的学习过程中,掌握国初核心知识点、明确一条合理的学习路径至关重要。
化竞知识庞杂,不少学化竞的同学对于自己应该学什么,或先学什么后学什么摸不清头脑,甚至有些同学临近考前了,还在问这个知识点国初考不考,要不要学。
因为对国初核心知识点不够了解,并且没有一条清晰合理的学习路径,走了不少冤枉路。
温馨提醒:在开始学习国初知识之前,同学们需先研读全国高中学生化学(奥林匹克)竞赛基本要求(2008年4月版大纲),了解国初考试对知识点的要求。
以下为分模块需掌握的知识点:化学基本原理1.现代化学入门:宏观手段对物质的分类,原子的发现,测量,有效数字,化学计量,化学反应的质量关系2.原子结构:原子结构模型,原子轨道,电子排布,元素周期表,元素周期律3.成键&离子键:化学键,电负性,键的极性,离子,离子晶体结构4.共价键理论&分子结构:共价键,键能,Lewis结构,八隅体规则,价键理论,VSEPR理论,杂化轨道,分子轨道理论5.气体:气体的温度和压强,理想气体定律,Dalton分压定律,Henry定律6.液体和固体:分子间作用力,液态,金属和金属键,晶体结构初步7.溶液的性质:溶液的组成,溶解度,相似相溶,蒸气压,熔沸点,胶体8.化学热力学:焓,Hess定律,标准生成热,键能,熵,热力学第二定律,自发过程,自由能,自由能和平衡,Gibbs-Helmholtz方程及应用9.化学平衡:平衡条件,平衡常数,化学平衡的移动10.溶液中的平衡:酸碱平衡,沉淀溶解平衡,氧化还原平衡&电化学,配位平衡&配位结构初步11.化学动力学初步&核化学:反应速率,速率方程,反应机理,催化剂,放射性衰变,放射性的应用与防护,同位素,核裂变和核聚变有机化学1.有机结构基础:基本概念,成键和结构,有机酸碱理论2.烷烃、环烷烃、构象:烷烃、环烷烃、构象3.立体化学:对映异构、非对映异构、顺反异构、构象异构4.烷烃、自由基取代反应:自由基、自由基反应、烷烃的自由基反应5.卤代烃、亲核取代反应:卤代烃、碳正离子,SN1,SN26.消除反应:E1, E2, Substitution Vs Elimination7.醇、醚:醇、硫醇、醚、环氧8.烯、炔的加成反应:构对比;亲电、自由基、亲核加成9.烯、炔:氧化、还原、聚合反应10.醛、酮:羰基、亲核加成、α,β-不饱和醛酮的加成、氧化、还原、wittig反应11.羧酸、羧酸衍生物、胺:羧酸、羧酸衍生物、胺、卡宾12.缩合反应:烯醇、烷基化反应、与羰基反应13.共轭、芳香性:共轭体系、分子轨道理论、芳香性14.共振、芳环的取代反应:共振论、芳环亲电取代、芳环亲核取代15.周环反应:前线轨道、经典周环反应机理举例16.重排反应:经典重排反应机理举例17.有机波谱分析:IR、MS、NMR在有机产物和中间体结构表征中的综合应用。
高中化学奥林匹克竞赛 专题十六 立体化学基础练习
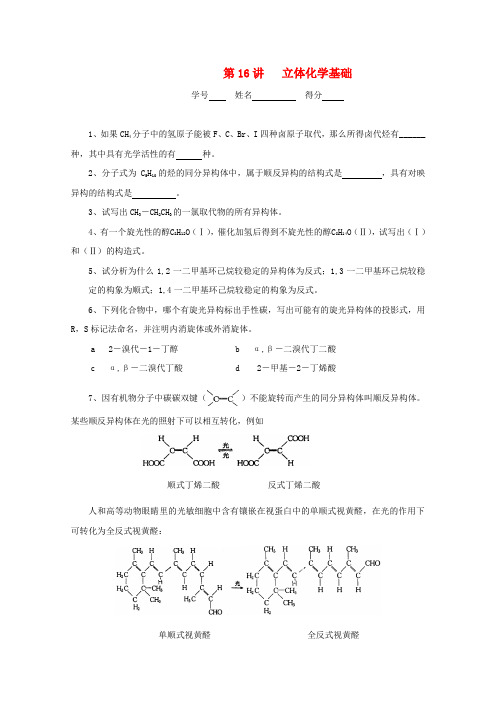
第16讲立体化学基础学号姓名得分1、如果CH4分子中的氢原子能被F、C、Br、I四种卤原子取代,那么所得卤代烃有______种,其中具有光学活性的有种。
2、分子式为C5H10的烃的同分异构体中,属于顺反异构的结构式是,具有对映异构的结构式是。
3、试写出CH3-CH2CH3的一氯取代物的所有异构体。
4、有一个旋光性的醇C8H12O(Ⅰ),催化加氢后得到不旋光性的醇C8H14O(Ⅱ),试写出(Ⅰ)和(Ⅱ)的构造式。
5、试分析为什么1,2一二甲基环己烷较稳定的异构体为反式;1,3一二甲基环己烷较稳定的构象为顺式;1,4一二甲基环己烷较稳定的构象为反式。
6、下列化合物中,哪个有旋光异构标出手性碳,写出可能有的旋光异构体的投影式,用R,S标记法命名,并注明内消旋体或外消旋体。
a 2-溴代-1-丁醇b α,β-二溴代丁二酸c α,β-二溴代丁酸d 2-甲基-2-丁烯酸7、因有机物分子中碳碳双键()不能旋转而产生的同分异构体叫顺反异构体。
某些顺反异构体在光的照射下可以相互转化,例如顺式丁烯二酸反式丁烯二酸人和高等动物眼睛里的光敏细胞中含有镶嵌在视蛋白中的单顺式视黄醛,在光的作用下可转化为全反式视黄醛:单顺式视黄醛全反式视黄醛由于全反式视黄醛分子的侧链是“直”的,导致其脱离视蛋白,并由此引起人和动物的视觉。
(1)视黄醛分子的顺反异构体共有A.4种 B.8种 C.16种 D.32种(2)1mo视黄醛分子与H2充分发生加成反应时要消耗 mo H2。
(3)将视黄醛链端的-CHO还原为-CH2OH即得维生素A。
以下关于维生素A的叙述中正确的是A.人体缺乏维生素A时易患夜盲症B.维生素A是易溶于水的醇C.侧链上的碳原子都在同一平面上D.所有碳原子都在同一平面上8、2022年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了某些手性分子可用作某些化学反应的催化剂,为合成对人类有用的重要化合物开辟了一个全新的研究领域。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中学化学竞赛试题资源库——顺反构象异构体A组1.二氟二氯(N2F2)分子中的四个原子都在一个平面上,由于几何形状的不同,它有两种同分异构体,如右图所示。
这种原子排布次序相同,几何形状不同的异构体被称为几何异构体,在下列化合物中存在着几何异构体的是A CHCl=CHClB CH2=CCl2C CH2=CHCH2CH3D CH3C≡CH2.NH2有两种同分异构体,是哪两种?为什么C2H2无同分异构体?23.因有机物分子中碳碳双键()不能旋转而产生的同分异构体叫顺反异构体。
某些顺反异构体在光的照射下可以相互转化,例如顺式丁烯二酸反式丁烯二酸人和高等动物眼睛里的光敏细胞中含有镶嵌在视蛋白中的单顺式视黄醛,在光的作用下可转化为全反式视黄醛:单顺式视黄醛全反式视黄醛由于全反式视黄醛分子的侧链是“直”的,导致其脱离视蛋白,并由此引起人和动物的视觉。
(1)视黄醛分子的顺反异构体共有A 4种B 8种C 16种D 32种(2)1mol视黄醛分子与H2充分发生加成反应时要消耗mol H2。
(3)将视黄醛链端的-CHO还原为-CH2OH即得维生素A。
以下关于维生素A的叙述中正确的是A 人体缺乏维生素A时易患夜盲症B 维生素A是易溶于水的醇B 侧链上的碳原子都在同一平面上D 所有碳原子都在同一平面上B组4.下列化合物中,有顺、反异构体的是A C6H5CH=CH2B C6H5-NH-OHC C6H5CH=N-OHD C6H5-NH-NH25.1,2,3,4,5,6-环己六醇的所有异构体(包括顺反、旋光)共有A 7个B 8个C 9个D 10个6.下列化合物中哪一个,其偶极短显然不等于零。
A B CD E7.分子式为C5H10的烃的同分异构体中,属于顺反异构的结构式是,具有对映异构的结构式是。
8.如果不考虑环形化合物,下列分子的构造异构体和几何异构体是多少?(1)C3H5Cl,(2)C3H4Cl2,(3)C4H7Cl,(4)C5H10?9.写出C4H8的所有构造异构体和几何异构体?10.下面化学式分别能画出几种构造异构体:(1)C5H12,(2)C3H7Cl,(3)C3H6Cl2,(4)C4H8Cl2,(5)C5H ll Cl,(6)C6H14,(7)C7H1611.用纽曼投影式面出乙烷的重叠式构象和交叉式构象,并回答下列问题:(1)乙烷的重叠式构象和交叉式构象是乙烷仅有的两种构象吗?(2)室温下乙烷的优势构象是哪一种?为什么?(3)温度升高时构象会发生什么变化?12.用纽曼投影式画出下列化合物的交叉式构象,并比较其稳定性:(1)CH3CH2-CH2CH3(2)(CH3)2CH-CH2CH313.将下列透视式改写成相应的纽曼投影式:14.下列化合物是否有顺反异构体?若有,试写出它们的顺反异构体。
①②③④15.下列各对化合物中,哪一对互为异构体?A 和B 和C 和D 和E 和16.试写出分子式为C4H7Cl的所有异构体的结构简式。
17.有机化合物的最简式是C2H3Br,A有两种异构体A1和A2;它们被O3氧化后,在Zn/H+作用下最终得到相同的有机产物B;A1在金属钠作用下可以得到C,而A2不能;C可以被酸性KMnO4溶液作用,得到D;D在干燥剂作用下得到碳氧化合物E;E中碳、氧两元素的质量分数分别为0.50;经光谱分析知,E分子是平面分子,且分别有两种不能类型的碳原子和氧原子。
(1)A的化学式是。
(2)A1和A2的结构简式是。
(3)写出A除A1、A2以外的全部链状同分异构体的结构简式(有立体异构体的只要指出即可)。
(4)写出B~E的结构简式。
18.醛、酮最主要的化学性质发生在碳氧双键上。
由于碳基原子带部分正电荷,易受亲核试剂的进攻而发生亲核加成反应。
如NH2OH(羟氨)与醛、酮反应就能得到一种叫做肟的化合物。
请回答:(1)为什么NH2OH和对称的酮R2C=O反应得到单一的肟,而和醛或不对称酮(RR’C =O)反应时可得到两种不同的肟?(2)酮肟在酸性催化剂(如PCl5)存在下可重排为酰胺(Beckmann重排),反应是经过向缺电子的氮进行1,2-迁移而完成的。
请问:从环己酮的肟经重排后得到什么化合物?19.化学式为C5H4的烃,理论上同分异构体的数目可能有30多种。
如:①CH2=C=C=C=CH2②CH≡C-CH=C=CH2③④-C≡CH ⑤-CH=CH2……请不要顾忌这些结构能否稳定存在,完成下面各小题:(1)异构体①、②是链状分子,请再写出2种链状分子的结构简式:(2)若核磁共振表明氢原子的化学环境没有区别,则满足条件的异构体除①、③外还有(只需答出一例)(3)有人认为异构体①中四个氢原子是共平面的,也有人认为不共平面,请分别写出这两种观点中碳原子的杂化类型和碳原子间π键成键情况;(4)异构体②和③中四个碳原子是否共平面,方便说明理由;(5)比较异构体④和⑤,何者相对更稳定些,为什么?(6)除题干和以上小题涉及到的异构体外,请至少再写出5种异构体,要求每种异构体都有对称性(存在一条对称轴)。
20.顺式-4-叔丁基环己醇的优势构象是A B C D21.下面几个邻-2-二甲基环己烷的Newman投影式中,最稳定的构象是A BC DC组22.用Newman投影式表示2,3一二甲基丁烷的各种构象异构体(交叉式和重叠式),并比较其相应能量高低。
23.试分析为什么1,2一二甲基环己烷较稳定的异构体为反式;1,3一二甲基环己烷较稳定的构象为顺式;1,4一二甲基环己烷较稳定的构象为反式。
24.在环己烷的椅式构象中,薄荷醇的羟基和邻位的-CH(CH3)2是反式构型,而新薄荷醇的羟基和邻位的-CH(CH3)2是顺式构型,它们互为构型异构体。
但它们分别与对硝基苯甲酰氯作用生成酯时,其反应速度前者是后者的16.5倍。
请解释为什么薄荷醇的酯化速度比新薄荷醇的酯化速度快?25.卤代烃用NaOH/C2H5OH处理时可以得到醇。
顺-1-异丙基-4-氯环己烷和它的反式异构体分别用NaOH/C2H5OH处理时,请用构象分析说明哪一个的反应速度快?26.根据原子或原子团之间的相互排斥作用,将丁烷的各种构象依次画出,可得四种极限构象:(1)按名称画出相应的纽曼投影式a反交叉式;b部分重叠式;c顺交叉式;d全重叠式(2)上述几种构象中,稳定性大小依次排列为:。
(3)依次画出2,3一二甲基丁烷的三种交叉式构象,并比较其能量高低。
27.试指出下列化合物哪些是顺式?哪些是反式?并指出构象的类型。
(1)(2)(3)(4)28.A的双键位上的亚甲基的氢被氘选择性地取代,然后溴化,再消除溴化氢,便得到产物B和无氘产物C:A:B:C:(1)一氘化的A有什么构型?解此题需要写出反应并简短地解释为什么只生成B和C。
(2)给出由无氟化合物A起始,立体选择性地生成一氘化物的步骤。
29.羧酸是一类重要的有机物。
(1)试写出丁烯二酸的结构式。
(2)丁烯二酸存在两种异构体A和B,试写出A和B的立体结构式,标出其构型和俗名。
(3)A和B是顺反异构体还是对映异构体?说明理由。
(4)在室温、无光照下,A和B跟溴反应得到什么化合物?写出反应的化学方程式,指出产物的构型和系统命名的名称。
(提示:在上述条件下,溴在烯双键上的加成为异面加成)30.某羧酸A的分子式为C5H8O2,有两种几何异构体:cis–A’和trans–A’’。
用Pt/H2氢化上述A的两种异构体,都得到相同的外消旋的羧酸B,B可拆分成光学异构体(+)-B和(-)-B,在293K及黑暗条件下,A’和A’’都能快速地与1mol Br2的四氯化碳溶液反应。
(1)试写出A和B的结构式。
(2)试写出A’和A’’的立体结构式和B的光学异构体的Fischer投影式[不考虑符号(+)或(-)]。
(3)用溴处理A’和A’’,将能同时生成C的几种立体异构体?(4)简明地叙述(3)的答案的理由。
(5)写出C的所有立体异构体的Fischer投影式和Newman投影式(构象式)。
指明对映异构体与非对映异构体。
31.含碳85.7%的烃有两种异构体A和B。
(1)写出它们的化学通式;烃A和B具有如下的性质:它们与臭氧反应后生成的物质在酸的存在下用锌粉处理后得到一种单一有机物C。
产物C经氧化得到一种单一的羧酸D。
根据光谱数据,除羧基上氢以外,该酸中的氢原子都在甲基上。
在标准状况下D的蒸气密度为9.1g/L。
在同冷的中性高锰酸钾反应时,化合物A比B更为活泼。
从A得到单一化合物F,从B得到异构体G1和G2所构成的1︰1的混合物。
(2)分别画出化合物D在水溶液中和在气相中的结构式。
(3)写出C的分子式。
(4)画出异构体A和B的结构式。
(5)①写出由A或B转化为C和D的反应式。
②写出由A和B转化为F,G1和G2的反应式。
(6)在酸存在下,G1和G2都易于和丙酮反应,生成化合物H1和H2,画出H1和H2的结构式。
(7)化合物A和B与溴水反应,这些反应产物之一是非极性的(该分子的偶极矩事实上为零),并无光学活性,画出该产物的立体化学结构;写出生成该产物的反应式。
确定该分子中手性原子的绝对构型,并用R或S来表示。
烯烃与过氧酸反应,将氧加到双键上,而生成含氧的三元环。
这种环氧化反应具有高的立体选择性,而保持与氧原子相连接的键上的各构成部分相对位置不变。
A跟过氧酸反应产生单一化合物K。
在同样条件下,B产生异构体L1和L2的混合物(1︰1)。
(8)说明化合物K是否具有光学活性。
画出K的立体结构式。
说明单一的化合物L1和L2是否具有光学活性,画出L1和L2的结构。
参考答案(F9)1 A2 N2H2分子中N=N为双键,不能自由旋转(因双键中π轨道叠加有方向性),故有顺式和反式两种异构体,它们的结构式如下:两种异构体中N原子都用sp2杂化轨道成键,分子呈平面形。
顺-N2H2分子属C2v。
点群,反-N2H2分子属C2h点群。
两者皆无旋光性。
C2H2分子的C原子采用sp杂化轨道成键,分子呈直线形,属D∞h点群,因而它无同分异构体。
C2H2分子的结构如下图。
3 (1)32 (2)6mol (3)A、C4 C5 C6 A7 和8 (1)4 (2)7 (3)11 (4)6910 (1)3 (2)2 (3)4 (4)9 (5)8 (6)5 (7)911 乙烷的重叠式构象;交叉式构象(1)乙烷的重叠式构象和交叉式构象不是乙烷仅有的两种构象,它们仅是乙烷的两个极端构象,介于它们二者之间还有无数个中间状态的构象。
(2)室温下乙烷的优势构象是交叉式构象。
在C-C键旋转的过程中,相邻碳原子上C-H键的电子云互相排斥,交叉式中两个碳原子上的C-H键相距最远,排斥力最小。
因此,该构象体系的能量最低,稳定性增加,为乙烷的优势构象。
(3)分子在不停地运动,温度越高,C -C 键旋转的速度越快,重叠式等能量较高的构象出现的概率增加。
