高考化学原子结构题
高考化学原子结构与元素周期表(大题培优)含答案

高考化学原子结构与元素周期表(大题培优)含答案一、原子结构与元素周期表练习题(含详细答案解析)1.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E 同处另一周期。
C、B可按原子个数比2∶1和1∶1分别形成两种离子化合物甲和乙。
D、A按原子个数比3∶2形成离子化合物丙。
E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:(1)B元素在周期表中的位置是__________,乙物质化学式是__________。
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是__________(用元素符号填写)。
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是____________________________________。
【答案】第二周期VIA族 Na2O2 O<N<Al<Mg<Na 2Al+2OH-+2H2O=2AlO2-+3H2↑【解析】【分析】C、B可按原子个数比2∶1和1∶1分别形成两种离子化合物甲和乙,可知C为Na元素,B为O元素,甲为Na2O,乙为Na2O2;E是地壳中含量最高的金属元素,则E为Al元素;A、B、C、D、E都是短周期元素,原子均小于Al的原子序数,D、A按原子个数比3∶2形成离子化合物丙,可知A为N元素,D为Mg元素,丙为Mg3N2。
【详解】(1)B为O元素,在周期表中第二周期VIA族,乙物质为过氧化钠,化学式是Na2O2,故答案为:第二周期VIA族;Na2O2;(2)Na、Mg、A l在第三周期,O、N在第二周期,同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,则O<N<P<Al<Mg<Na,即O<N<Al<Mg<Na,故答案为:O<N<Al<Mg<Na;(3)铝能跟氢氧化钠溶液发生反应生成偏铝酸盐和氢气,其反应的离子反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑。
高考化学原子结构与元素周期表综合题附详细答案

【分析】
根据元素周期表可知①为H元素、②为B元素、③为C元素、④为N元素、⑤为O元素、⑥为F元素、⑦为Fe元素、⑧为Cu元素、⑨为Zn元素。
【详解】
(1)元素⑦为Fe元素,位于周期表的d区,故答案为:d;
(2)元素③为C元素、元素⑤为O元素,其形成的稳定化合物为二氧化碳,结构式为:O=C=O,故答案为:O=C=O;
c.Na与水反应比Al剧烈,说明金属性:Na>Al,可以比较,故c正确;
d.元素的金属性越强,最高价氧化物对应水化物的碱性越强,可以比较,故d正确;
答案选cd;
(4)①A为分液漏斗,A中发生氯气与NaBr的氧化还原反应,离子方程式为2Br-+Cl2=Br2+2Cl-;
②NaOH溶液用于吸收氯气,离子方程为Cl2+2OH-=H2O+Cl-+ClO-;
4.下表是元素周期表的一部分,回答下列问题:
(1)B在周期表中的位置是__;写出A、B的单质之间发生反应的化学方程式:__。
(2)写出表中位于长周期的卤族元素的名称:__;属于短周期的碱金属元素的元素符号为__。
【答案】第3周期ⅥA族2K+S K2S溴Li、Na
【解析】
【分析】
根据元素周期表的结构及物质性质分析解答。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式______。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为______(用离子符号表示)。
【答案】 HClO4>HNO3>H3PO4Be(OH)2+2NaOH=Na2BeO2+2H2OCl->F->Na+
高考化学 原子结构与元素周期表 综合题及答案解析

高考化学 原子结构与元素周期表 综合题及答案解析一、原子结构与元素周期表练习题(含详细答案解析)1.磷化铝(AlP )和磷化氢(PH 3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:________________。
AlP 遇水蒸气会发生反应放出PH 3气体,该反应的另一种产物的化学式为________。
(2)PH 3具有强还原性,能与CuSO 4溶液反应,配平该反应的化学方程式:________CuSO 4+_____PH 3+_____H 2O =_____Cu 3P ↓+_____H 3PO 4+_____H 2SO 4(3)工业制备PH 3的流程如图所示。
①次磷酸属于________元酸。
②白磷和烧碱溶液反应的化学方程式为:____________________________________。
③若起始时有1 mol P 4参加反应,则整个工业流程中共生成________mol PH 3。
(不考虑产物的损失)【答案】第3周期第VA 族 Al (OH )3 24 11 12 8 3 24 1 P 4 + 3NaOH + 3H 2O =PH 3↑+ 3NaH 2PO 2 2.5【解析】【分析】(1)原子结构中电子层数等于周期数,最外层电子数等于族序数,AlP 遇水蒸气会发生反应放出PH 3气体,根据元素守恒确定该反应的另一种产物的化学式;(2)配平化学方程式,就是通过在各物质的化学式前面添加系数,使反应中每种原子个数在反应前后相等的过程,但对于复杂的化学反应通常通过观察,找出变化的特点或规律,常使用化合价来配平,保证化合价升高与降低的数相等即可;(3)①根据物质电离出的氢离子数目确定酸的元数;②根据图示信息:白磷和烧碱溶液反应生成PH 3、NaH 2PO 2,据此书写方程式; ③根据发生反应的过程寻找关系式,进行计算即可。
【详解】(1)P 处于第3周期ⅤA 族,AlP 遇水蒸气会发生反应放出PH 3气体,根据元素守恒,确定该反应的另一种产物是Al (OH )3,故答案为:第3周期第VA 族;Al (OH )3;(2)该方程式中Cu 价态由+2下降为+1,P 价态由-3升高为+5,为保证化合价升降数相等,Cu 3P 与H 3PO 4计量数分别为8、3,CuSO 4的系数是24,H 2SO 4系数是24,根据元素守恒,得到:4323342424CuSO +11PH +12H O=8Cu P +3H PO +24H SO ↓,故答案为:24,11,12,8,3,24;(3)①根据氢氧化钠过量时只能生成NaH 2PO 2可知次磷酸只能电离出1个氢离子,因此次磷酸属于一元酸,故答案为:1;②根据图示信息:白磷和烧碱溶液反应生成PH 3、NaH 2PO 2,方程式为:42322P + 3NaOH + 3H O = PH + 3NaH PO ↑;故答案为:42322P + 3NaOH + 3H O = PH + 3NaH PO ;③P 4+3NaOH +3H 2O =PH 3↑+3NaH 2PO 2;2H 3PO 2=PH 3↑+H 3PO 4,即P 4~2.5PH 3,若起始时有1molP 4参加反应,则整个工业流程中共生成2.5molPH 3;故答案为:2.5。
高考化学考点规范练25 原子结构(含答案)

考点规范练原子结构一、选择题1.(2021河北卷)用中子轰击 Z N X 原子产生α粒子(即氦核 24He)的核反应为Z N X+01n →P 7Y +24He 。
已知元素Y 在化合物中显+1价。
下列说法正确的是( )。
A.H 3XO 3可用于中和溅在皮肤上的NaOH 溶液B.Y 单质在空气中燃烧的产物是Y 2O 2C.X 和氢元素形成离子化合物D.6Y 和7Y 互为同素异形体2.下列叙述中,不正确的是( )。
A.在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析B.p 轨道电子云形状是哑铃形C.电子的运动状态可从能层、能级、轨道、自旋方向4个方面进行描述D.3p 能级上只有一个空轨道的原子和3p 能级上有两个未成对电子的原子,对应为同一元素3.某元素基态原子4s 轨道上有1个电子,则该基态原子价层电子排布不可能是( )。
A.3p 64s 1B.4s 1C.3d 54s 1D.3d 104s 14.下列说法中正确的是( )。
A.同一原子中3s 、3p 、3d 、4s 能量依次升高B.某原子核外电子由1s 22s 22p 63s 23p 1→1s 22s 22p 63s 13p 2,原子放出能量C.p 能级的原子轨道呈哑铃形,随着能层数的增加,p 能级原子轨道数也在增多D.按照泡利原理,在同一个原子中不可能存在两个运动状态完全相同的电子5.下列说法中正确的是( )。
A.37Cl 原子核内的中子数为17B.1H 和2H 的化学性质几乎完全相同C.H 216O 与H 218O 互为同素异形体D.Na 和Na +属于同种元素,且性质相同6.(2021湖北武汉高三月考)具有下列电子层结构的原子,其对应元素一定属于同一周期的是( )。
A.两种原子的电子层上全部都是s 电子B.3p 能级上只有一个空轨道的原子和3p 能级上只有一个未成对电子的原子C.最外层电子排布式为2s22p6的原子和最外层电子排布式为2s22p6的离子D.原子核外M层上的s能级和p能级都填满了电子,而d能级上尚未有电子的两种原子7.下列电子排布式或轨道表示式正确的是()。
高考化学原子结构一轮复习小题训练(原卷版)

原子结构1.人类认识原子的历史是漫长的。
下列与原子结构模型的演变无关的科学家是( ) A.玻尔B.道尔顿C.卢瑟福D.爱因斯坦2.首次将量子化概念运用到原子结构,并解释了原子稳定性的科学家是()A.玻尔B.爱因斯坦C.门捷列夫D.鲍林3.下列各电子层中不包含d能级的是()A.N电子层B.M电子层C.L电子层D.O电子层4.下列原子轨道中,可容纳电子数最多的是()A.5d B.6p C.4f D.7s5.原子结构模型的演变如图所示,下列符合历史演变顺序的一组排列是( )A.(1)(3)(2)(4)(5) B.(1)(2)(3)(4)(5) C.(1)(5)(3)(2)(4) D.(1)(3)(5)(4)(2)6.以下现象与核外电子跃迁有关的是( )①棱镜分光②石油蒸馏③凸透镜聚光④日光灯通电发光⑤冷却结晶A.①②B.③④C.①⑤D.④7.当电子层、能级和原子轨道确定后,仍不能确定该原子轨道的()A.数目B.空间伸展方向C.能量高低D.电子数8.在多电子原子中,决定轨道能量的是()A.电子层B.电子层和能级C.电子层、能级和原子轨道空间分布D.原子轨道空间分布和电子自旋方向9.下列符号表述合理的是()A.5s1B.2p10C.2d6D.3f1410.N原子核外能量最高的电子具有不同的()A.电子亚层B.电子云伸展方向C.电子云形状D.自旋方向11.有关氮原子核外p亚层中的电子的说法错误的是()A.能量相同B.电子云形状相同C.电子云伸展方向相同D.自旋方向相同12.3p x所代表的含义是()A.p x轨道上有3个电子B.第三电子层p x轨道有3个伸展方向C.p x电子云有3个伸展方向D.第三电子层沿x轴方向伸展的p轨道13.关于氢原子电子云图的说法正确的是()A.黑点密度大,电子数目大B.黑点密度大,单位体积内电子出现的机会小C.电子云图是对电子运动无规律的描述D.电子云图描述了电子运动的客观规律1.在实验室中用下列装置可以得到氢原子光谱,实验证明该光谱为线状光谱,该光谱的发现在原子结构的认识过程中,有极为重要的意义,根据它产生了()A.卢瑟福核式原子模型B.汤姆逊“葡萄干布丁”模型C.玻尔核外电子分层排布模型D.原子结构的量子力学模型2.下列说法正确的是()A.氢原子光谱是元素的所有光谱中最简单的光谱之一B.“量子化”就是不连续的意思,微观粒子运动均有此特点C.玻尔理论不但成功地解释了氢原子光谱,而且还能推广到其他原子光谱D.原子中的电子在具有确定半径的圆周轨道上像火车一样高速运转着3.对充有氖气的霓虹灯管通电,灯管发出红色光。
高考化学原子结构与元素周期表(大题培优易错试卷)及答案
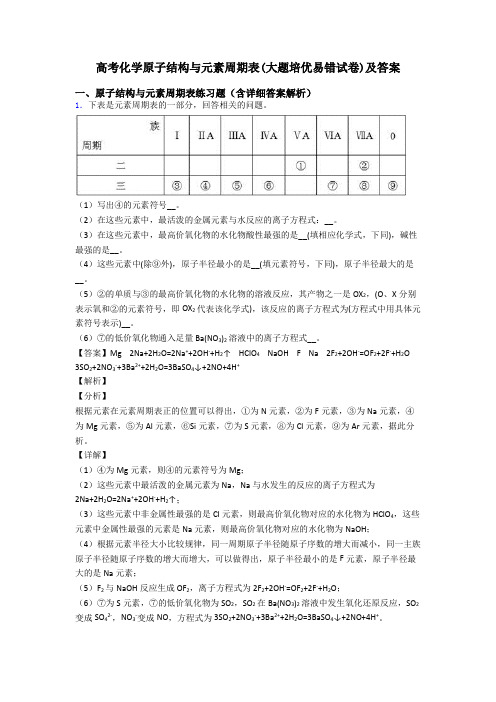
高考化学原子结构与元素周期表(大题培优易错试卷)及答案一、原子结构与元素周期表练习题(含详细答案解析)1.下表是元素周期表的一部分,回答相关的问题。
(1)写出④的元素符号__。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:__。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是__(填相应化学式,下同),碱性最强的是__。
(4)这些元素中(除⑨外),原子半径最小的是__(填元素符号,下同),原子半径最大的是__。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为(方程式中用具体元素符号表示)__。
(6)⑦的低价氧化物通入足量Ba(NO3)2溶液中的离子方程式__。
【答案】Mg 2Na+2H2O=2Na++2OH-+H2↑ HClO4 NaOH F Na 2F2+2OH-=OF2+2F-+H2O 3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+【解析】【分析】根据元素在元素周期表正的位置可以得出,①为N元素,②为F元素,③为Na元素,④为Mg元素,⑤为Al元素,⑥Si元素,⑦为S元素,⑧为Cl元素,⑨为Ar元素,据此分析。
【详解】(1)④为Mg元素,则④的元素符号为Mg;(2)这些元素中最活泼的金属元素为Na,Na与水发生的反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑;(3)这些元素中非金属性最强的是Cl元素,则最高价氧化物对应的水化物为HClO4,这些元素中金属性最强的元素是Na元素,则最高价氧化物对应的水化物为NaOH;(4)根据元素半径大小比较规律,同一周期原子半径随原子序数的增大而减小,同一主族原子半径随原子序数的增大而增大,可以做得出,原子半径最小的是F元素,原子半径最大的是Na元素;(5)F2与NaOH反应生成OF2,离子方程式为2F2+2OH-=OF2+2F-+H2O;(6)⑦为S元素,⑦的低价氧化物为SO2,SO2在Ba(NO3)2溶液中发生氧化还原反应,SO2变成SO42-,NO3-变成NO,方程式为3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+。
高中化学的原子结构检测试题及答案

高中化学的原子构造检测试题及答案1.(20XX年福州质检)11H、12H、13H、H+、也是()A.氢的五种同位素B.五种氢元素C.氢的五种核素D.氢元素的五种不同粒子2.以下有关钋(21084Po)的说法正确的选项是()A.钋原子的核外电子数是126B.钋原子核内中子数与质子数之差是42C.钋是金属元素,最外层电子数小于4D.钋元素的相对原子质量是2103.四种主族元素的离子aXm+、bYn+、cZn一和dRm—(a、b、c、d为元素的原子序数),它们具有相同的电子层构造,假设m〉n,那么对以下表达的判断正确的选项是()①a—b=n—m②元素的原子序数a〉b〉c〉d③元素非金属性Z〉R④最高价氧化物对应水化物碱性X〉YA.②③B.③C.①②③④D.①②③4.1〜18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层构造,以下关系正确的选项是()A.质子数c>dB.离子的复原性Y2—>Z—C.气态氢化物的稳定性H2Y〉HZD.原子半径X5.假设R元素无同位素,元素R原子的质量数为A,Rm—的核外电子数为x,那么WgRm—离子所含中子的物质的量为()A.(A—x+m)molB.(A—x—m)molC.WA(A—x+m)molD.WA(A—x—m)mol6.短周期元素X、Y的原子序数相差7,以下有关判断错误的选项是()A.X和Y可能处于同一周期B.X和Y可能处于相邻周期C.X和Y可能处于同一主族D.X和Y可能处于相邻主族7.以下元素周期表的表达,不正确的选项是()A.共有7个周期,16个族B.形成化合物种类最多的元素在第二周期C.第IIA族的右边是第IIIB族,第IIIA族的左边是第IIB族D.某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m—nR或RH2m—n8.(xx嘉兴模拟)以下有关物质性质的比拟中,正确的选项是()①热稳定性:CH4〉NH3〉H2O②复原性:I—〉Br—〉Cl—③酸性:H3P04〉H2S04〉HCl04④原子半径:Na〉Mg〉OA.①③B.②④C.①④D.②③9.(xx年广东高考)下表是元素周期表的一局部,有关说法正确的选项是()族周期IAIIAIIIAWAVAPA训A2cd3abefA.e的氢化物比d的氢化物稳定B.a、b、e三种元素的原子半径:e〉b〉aC.六种元素中,e元素单质的化学性质最活泼D.c、e、f的最高价氧化物对应的水化物的酸性依次增强10.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,根据碱金属元素性质的递变规律预测其性质,其中不正确的选项是()A.在碱金属元素中它具有最大的原子半径B.钫在空气中燃烧时,只生成化学式为Fr20的氧化物C.它的氢氧化物化学式为FrOH,这是一种极强的碱D.它能跟水反响生成相应的碱和氢气,由于反响剧烈而发生爆炸11.居里夫人发现的镭是元素周期表中第七周期的IIA族元素,以下关于镭的性质的描述中不正确的选项是。
高考化学原子结构与元素周期表综合经典题含答案

高考化学原子结构与元素周期表综合经典题含答案一、原子结构与元素周期表练习题(含详细答案解析)1.磷化铝(AIP )和磷化氢(Pf )都是粮食储备常用的高效熏蒸杀虫剂。
(1) ____________________________________________ 磷元素在元素周期表中的位置: 。
AIP遇水蒸气会发生反应放出 _____________________________________ PH 3气体,该反应的另一种产物的化学式为 ___________________ 。
(2) PH 3具有强还原性,能与 CuSQ 溶液反应,配平该反应的化学方程式:_______ CuSO 4 + ___ PH 3+ ______ H 2O = ___ Cu 3P J + ______ H 3PO 4 + (3) 工业制备PH 3的流程如图所示。
PH次磷敲钠孟勰分解(NaH IXX) IIDI L ―① ____________________ 次磷酸属于元酸。
② 白磷和烧碱溶液反应的化学方程式为: ________________________③ 若起始时有1 mol P 4参加反应,则整个工业流程中共生成 产物的损失) 【答案】第 3 周期第 VA 族 Al( OH) 324 11 12 8 3 24 1 P+ 3NaOH + 3H 2O =PH 3 f + 3NaH 2PO 22. 5【解析】 【分析】(1)原子结构中电子层数等于周期数,最外层电子数等于族序数,AIP 遇水蒸气会发生反应放出PH 3气体,根据元素守恒确定该反应的另一种产物的化学式;(2 )配平化学方程式,就是通过在各物质的化学式前面添加系数,使反应中每种原子个数 在反应前后相等的过程,但对于复杂的化学反应通常通过观察,找出变化的特点或规律, 常使用化合价来配平,保证化合价升高与降低的数相等即可; (3) ①根据物质电离出的氢离子数目确定酸的元数; ② 根据图示信息:白磷和烧碱溶液反应生成PH 3、NaH 2PQ ,据此书写方程式;③ 根据发生反应的过程寻找关系式,进行计算即可。
2024全国高考真题化学汇编:原子结构与元素性质章节综合

2024全国高考真题化学汇编原子结构与元素性质章节综合一、单选题1.(2024上海高考真题)下列关于氟元素的性质说法正确的是A .原子半径最小B .原子第一电离能最大C .元素的电负性最强D .最高正化合价为+72.(2024甘肃高考真题)X 、Y 、Z 、W 、Q 为短周期元素,原子序数依次增大,最外层电子数之和为18。
Y 原子核外有两个单电子,Z 和Q 同族,Z 的原子序数是Q 的一半,W 元素的焰色试验呈黄色。
下列说法错误的是A .X 、Y 组成的化合物有可燃性B .X 、Q 组成的化合物有还原性C .Z 、W 组成的化合物能与水反应D .W 、Q 组成的化合物溶于水呈酸性3.(2024全国高考真题)W 、X 、Y 、Z 为原子序数依次增大的短周期元素。
W 和X 原子序数之和等于-Y 的核外电子数,化合物 -+6W ZY 可用作化学电源的电解质。
下列叙述正确的是A .X 和Z 属于同一主族B .非属性:X>Y>ZC .气态氢化物的稳定性:Z YD .原子半径:Y>X>W4.(2024湖北高考真题)主族元素W 、X 、Y 、Z 原子序数依次增大,X 、Y 的价电子数相等,Z 的价电子所在能层有16个轨道,4种元素形成的化合物如图。
下列说法正确的是A .电负性:W>YB .酸性:2324W YX >W YX C .基态原子的未成对电子数:W>XD .氧化物溶于水所得溶液的pH Z>Y:二、解答题5.(2024河北高考真题)25V O 是制造钒铁合金、金属钒的原料,也是重要的催化剂。
以苛化泥为焙烧添加剂从石煤中提取25V O 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。
工艺流程如下。
已知:i 石煤是一种含23V O 的矿物,杂质为大量23Al O 和少量CaO 等;苛化泥的主要成分为323CaCO NaOH Na CO 、、等。
ⅱ高温下,苛化泥的主要成分可与23Al O 反应生成偏铝酸盐;室温下,偏钒酸钙 32Ca VO 和偏铝酸钙均难溶于水。
高考化学原子结构与元素周期表(大题培优)及详细答案

a.配位键b.极性键c.非极性键d.离子键e.金属键f氢键g.范德华力h.π键i.σ键
(3)表中列出了核电荷数为21~25的元素的最高正化合价:
【点睛】
本题考查了原子结构与物质性质及元素在周期表位置关系应用,根据原子结构关系或物质性质推断元素是解题关键,理解影响微粒半径大小的因素,注意识记常见10电子、18电子微粒,理解酸式盐可以与碱反应产生正盐,结合物质的溶解性及电解质的强弱和物质的拆分原则书写反应的离子方程式。
5.原子序数依次增大的A、B、C、D、E、F都是元素周期表中前20号元素,B、C、D、E同周期,A、D同主族,且A的原子结构中最外层电子数是电子层数的3倍。F和其他元素既不在同周期也不在同主族,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。根据以上信息,回答下列问题:
(2)①H2C2O4的结构式为 ,含碳氧双键,则碳原子的杂化轨道类型为sp2杂化,分子中含有7个σ键、2个π键,所以σ键和π键数目之比为:7:2,故答案为:sp2杂化;7:2;
②H2O中O原子的价层电子对数 ,且含有两个2个孤对电子,所以H2O的VSPER模型为四面体形,分子空间构型为V形,等电子体是原子数相同,电子数也相同的物质,因此,与H2O互为等电子体的阴离子可以是NH2-,故答案为:四面体形;NH2-;
【详解】
(1)由分析可知AB2为CaCl2,X为Ca(OH)2,Y为Ca(ClO)2,Z为HClO。,故答案为:CaCl2;Ca(OH)2;Ca(ClO)2;HClO;
(2)AB2的形成过程用电子式表示为 ,故答案为: ;
高考化学原子结构与元素周期表(大题培优)

高考化学原子结构与元素周期表(大题培优)一、原子结构与元素周期表练习题(含详细答案解析)1.电气石是一种具有保健作用的天然石材,其中含有的主要元素为B、Si、Al、Mg、Na、O等元素。
(1)上述元素中,原子半径最小的是_________(用元素符号表示),在元素周期表中处于金属和非金属分界线附近的元素是_____________(用元素符号表示);(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式,从中选择最详尽描述核外电子运动状态的方式,来表示氧元素原子核外电子的运动状态______________;(3)B与最活泼的非金属元素F形成化合物BF3,检测发现BF3分子中三根B—F键的键长相等,三根键的键角相等,能否仅仅依据此数据此判断BF3分子的极性____________;(4)SiO2晶体的熔点比BF3晶体________(选填“高”、“低”)。
【答案】O B、Si、Al 非极性高【解析】【分析】(1)同周期自左而右原子半径减小,电子层越多原子半径越大;在元素周期表中处于金属和非金属分界线附近的元素是B、Si、Al;(2)最详尽描述核外电子运动状态的方式为核外电子轨道排布式,根据核外电子排布规律画出;处于不同能级的电子,能量不同,处于同一能级不同轨道的电子能量相同;(3)BF3分子中三根B﹣F键的键长相等且键角也相等,为平面正三角形结构,正负电荷重心重合;根据晶体类型判断熔点高低,一般熔点:原子晶体>离子晶体>分子晶体;(4)BF3是分子晶体,SiO2是原子晶体。
【详解】(1)同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Mg>Al>Si >B>O,在元素周期表中处于金属和非金属分界线附近的元素是B、Si、Al;(2)最详尽描述核外电子运动状态的方式为核外电子轨道排布式,氧元素原子核外电子轨道排布式为:;(3)BF3分子中三根B﹣F键的键长相等且键角也相等,为平面正三角形结构,正负电荷重心重合,为非极性分子;(4)BF3是分子晶体,SiO2是原子晶体,故SiO2晶体的熔点比BF3晶体高。
高考化学压轴题之原子结构与元素周期表(高考题型整理,突破提升)附详细答案

高考化学压轴题之原子结构与元素周期表(高考题型整理,突破提升)附详细答案一、原子结构与元素周期表练习题(含详细答案解析)1.南京理工教授制出了一种新的全氮阴离子盐—AgN5,目前已经合成出钠、锰、铁、钴、镍、镁等几种金属的全氮阴离子盐。
(1)基态Mn2+的价电子排布式为____;银与铜位于同一族,银元素位于元素周期表的___区。
(2)[Mg(H2O)6]2+[(N5)2(H2O)4]2-的晶体的部分结构如图1所示:N、O、Mg元素的前3级电离能如下表所示:元素I1/kJ∙mol-1I2/kJ∙mol-1I3/kJ∙mol-1X737.71450.77732.7Y1313.93388.35300.5Z1402.32856.04578.1①X、Y、Z中为N元素的是____,判断理由是__________。
②从作用力类型看,Mg2+与H2O之间是________、N5与H2O之间是________。
③N5-为平面正五边形,N原子的杂化类型是_______。
科学家预测将来还会制出含N4-、N6-表示,其中m代表等平面环状结构离子的盐,这一类离子中都存在大π键,可用符号πnm参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则N4-中的大π键应表示为_________。
(3)AgN5的立方晶胞结构如图2所示,Ag+周围距离最近的Ag+有_______个。
若晶体中紧邻的N5-与Ag+的平均距离为a nm,N A表示阿伏加德罗常数的值,则AgN5的密度可表示为_____g∙cm-3(用含a、N A的代数式表示)。
【答案】3d5 ds Z X最外层为2个电子,X为镁;N的2p轨道处于半充满的稳定状态,其失去第一个电子较难,I1较大,则Z为氮元素配位键氢键 sp254π 12223A8.910 N a⨯⨯【解析】【分析】(1)根据构造原理书写出25号Mn元素的原子核外电子排布式,Mn原子失去最外层2个电子得到Mn2+;根据原子结构与元素在周期表的位置确定Ag在周期表所属区域;(2)①根据元素的电离能大小结合原子结构确定X、Y、Z三种元素,然后判断哪种元素是N 元素;②根据图示,判断晶体中阳离子、阴离子中含有的作用力类型;③结合N5-为平面正五边形结构,结合原子杂化类型与微粒构型关系分析判断,结合微粒的原子结构分析大π键的形成;(3)根据晶胞中离子的相对位置判断Ag+的配位数,利用均摊方法计算1个晶胞中含有的AgN5的个数,结合ρ=mV计算密度大小。
高考化学试题含解析——原子结构

跟踪检测(十六)原子结构1.元素周期表中铊元素的数据如图,下列说法正确的是()A.铊元素的质量数是204.4B.铊原子的中子数为81C.铊对应的氢氧化物有两性D.铊元素位于第ⅢA族解析:选D铊元素的相对原子质量是204.4,故A错误;铊原子的质子数为81,故B 错误;铊不位于金属与非金属的分界线处,对应的氢氧化物没有两性,故C错误;铊元素最外层有3个电子,位于第ⅢA族,故D正确。
2.(2018·重庆十八中月考)我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫铝铍测年法。
关于26Al和10Be的说法不正确的是()A.10Be和9Be是中子数不同质子数相同的不同原子B.10Be的原子核内中子数比质子数多C.5.2 g 26Al3+中所含的电子数约为1.2×1023D.26Al和26Mg的质子数、中子数和核外电子数都不相同解析:选C10Be和9Be互为同位素,中子数不同质子数相同,A项正确;10Be的原子核内,质子数为4,中子数为10-4=6,中子数比质子数多,B项正确;5.2 g 26Al3+中所含的电子数约为5.2 g26 g·mol-1×(13-3)×N A mol-1≈1.2×1024,C项错误;26Al和26Mg的质子数分别为13、12,中子数分别为13、14,核外电子数等于质子数,故两者所含质子数、中子数和核外电子数都不相同,D项正确。
3.(2018·泰安一检)下列有关化学用语表达正确的是()A.35Cl-和37Cl-的结构示意图均可以表示为B.HClO的结构式:H—Cl—OD.质子数为92、中子数为146的U原子:14692U解析:选A35Cl-和37Cl-的核电荷数均为17,核外电子总数均为18,其结构示意图均可表示为,A项正确;次氯酸分子中O原子分别与H、Cl原子之间形成1个共用电子对,故HClO的结构式为H—O—Cl,B项错误;HF属于共价化合物,电子式为,C 项错误;质子数为92、中子数为146的U 原子的质量数为238,该原子可表示为238 92 U ,D 项错误。
高考化学一轮复习专题练习:原子结构与性质

第十一单元物质结构与性质(选考)第1节原子结构与性质一、选择题1.下列说法正确的是()。
A.原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相像B.Zn2+的最外层电子排布式为3s23p63d10C.基态铜原子的最外层电子排布图:D.基态碳原子的最外层电子排布图:2.下列轨道表示式中,能正确表示该元素原子的最低能量状态的是()。
A.B.C.D.3.Cr原子处于基态时,价电子排布可用电子排布图表示成,而不是。
下列说法中,正确的是()。
A.这两种排布方式都符合能量最低原理B.这两种排布方式都符合泡利原理C.这两种排布方式都符合洪特规则D.这个实例说明洪特规则有时候和能量最低原理是冲突的4.下列各组元素的性质正确的是()。
A.第一电离能:B>Al>GaB.电负性:F>N>OC.最高正价:F>S>SiD.原子半径:P>N>C5.(2019年湖北黄冈期末)人们常将在同一原子轨道上运动的、自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”。
以下有关主族元素原子的“电子对”和“未成对电子”的说法,错误..的是()。
A.核外电子数为奇数的基态原子,其原子轨道中肯定含有“未成对电子”B.核外电子数为偶数的基态原子,其原子轨道中肯定不含“未成对电子”C.核外电子数为偶数的基态原子,其原子轨道中肯定含有“电子对”D.核外电子数为奇数的基态原子,其原子轨道中可能含有“电子对”6.(2019届河北定州中学期中)第三周期元素的基态原子中,不行能出现d电子,主要依据是()。
A.能量守恒原理B.泡利不相容原理C.洪特规则D.近似能级图中的依次3d轨道能量比4s轨道高7.(2019届安徽安庆六校联考)以下有关结构与性质的说法不正确...的是()。
A.下列基态原子中:①1s22s22p63s23p2;②1s22s22p3;③1s22s22p2,电负性最大的是②B.下列基态原子中:①[Ne]3s23p2;②[Ne]3s23p3;③[Ne]3s23p4,第一电离能最大的是③C.某主族元素的逐级电离能分别为738、1451、7733、10 540、13 630……,当它与氯气反应时生成的阳离子是X2+D.物质的熔点凹凸:金刚石>晶体硅>钠>干冰二、非选择题8.(1)(2019年安徽卷)C、N、O、Al、Si、Cu是常见的六种元素。
高考化学原子结构与元素周期表综合经典题含详细答案

高考化学原子结构与元素周期表综合经典题含详细答案一、原子结构与元素周期表练习题(含详细答案解析)1.下表为元素周期表的粗表,①~⑧分别表示元素周期表中对应位置的元素①⑧③⑤②④⑥⑦(1)用电子式表示①与②形成化合物A 的过程:________(2)已知⑥原子的最外层有2个电子,请画出⑥原子的结构示意图:______________(3)含有④元素的某种18 电子的离子与H+及OH-均可发生反应,请写出该离子的电子式______(4)元素③④⑤的简单气态氢化物的稳定性由强到弱的顺序是_________(用化学式表示),其沸点由高到低的顺序是_______ (用化学式表示)(5)已知⑦的稳定化合态为+2 价,且⑦与③可按3:4 形成某化合物,该化合物具有较强氧化性,可以与浓盐酸反应并释放出一种黄绿色的气体,请写出该化学方程式:_________________(6)①与③,①与④能形成18个电子的化合物,此两种化合物在溶液中发生反应的化学方程式为_________。
(7)⑧的一种氧化物为无色气体,在空气中能迅速变成红棕色。
在一定条件下,2L的该无色气体与0.5 L 的氧气混合,该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则所生成的一种含氧酸盐的化学式是_________。
(8)两种均含①与②③④四种元素的化合物相互反应放出气体的离子方程式为_________。
【答案】 HF>H2O>H2SH2O>HF>H2S Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O H2S+H2O2=S+H2O NaNO2 HSO3-+H+=【解析】【分析】根据题干图表分析可知,①元素位于元素周期表的第一周期第ⅠA族,为H元素,②元素位于元素周期表的第三周期第ⅠA族,为Na元素,③元素位于元素周期表的第二周期第ⅥA族,为O元素,④元素位于元素周期表的第三周期第ⅥA族,为S元素,⑤元素位于元素周期表的第二周期第ⅦA族,为F元素,⑥元素位于元素周期表第四周期第Ⅷ族,为26号元素Fe,⑦元素位于元素周期表的第六周期第ⅣA族,为Pb元素,⑧元素位于元素周期表的第二周期第ⅤA族,为N元素,据此分析解答问题。
高考化学《原子结构与性质》练习题(含答案)

高考化学《原子结构与性质》练习题(含答案)一、选择题(共10题)1.某元素原子外围电子构型为3d54s2,其应在( )A.第四周期ⅡA族B.第四周期ⅡB族C.第四周期ⅦA族D.第四周期ⅦB族2.下列对电负性的理解不正确的是( )A.电负性是人为规定的一个相对数值,不是绝对标准B.元素电负性的大小反映了元素对键合电子吸引力的大小C.元素的电负性越大,则元素的非金属性越强D.元素的电负性是元素固有的性质,与原子结构无关3.下列各组原子中,化学性质一定相似的是( )A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子D.最外层都只有一个电子的X、Y原子4.下列说法中正确的是( )A.第三周期所有元素中钠的第一电离能最小B.钠的第一电离能比镁的第一电离能大C.在所有元素中,氟的第一电离能最大D.钾的第一电离能比镁的第一电离能大5.下列化学用语的表述错误的是( )A.18O2-离子的结构示意图:B.甲烷分子的比例模型:C.二氧化碳分子的电子式:D.氮原子核外电子排布的轨道表示式:6.下列说法中正确的是( )A.所有金属元素都分布在d区和ds区B.最外层电子数为2的元素都分布在s区C.元素周期表中ⅢB族到ⅡB族10个纵列的元素都是金属元素D.s区均为金属元素7.已知X 、Y 是主族元素,I 为电离能,单位是kJ·mol -1。
请根据下表数据判断,下列选项错误的是( ) 元素I 1 I 2 I 3 I 4 X500 4 600 6 900 9 500 Y 580 1 800 2 700 11 600 A.元素X 的常见化合价是+1价B .元素Y 是第ⅢA 族元素C .元素X 与氯形成化合物时,化学式可能是XClD .若元素Y 处于第三周期,它可与冷水剧烈反应8.下列说法正确的是( )A .原子核外电子排布式为1s 2的原子与原子核外电子排布式为1s 22s 2的原子化学性质相似B .Zn 2+的最外层电子排布式为3s 23p 63d 10C .基态铜原子的外围电子排布图:D .基态碳原子的最外层电子排布图: 9.已知X 、Y 元素同周期,且电负性X >Y ,下列说法不正确的是( )A .X 与Y 形成化合物时,X 显负价,Y 显正价B .第一电离能Y 可能小于X ,也可能大于XC .含氧酸的酸性:X>YD .气态氢化物的稳定性:H m Y 小于H n X10.下列各组表述中,两个原子不属于同种元素原子的是( )A .3p 能级有一个空轨道的基态原子和核外电子的排布式为1s 22s 22p 63s 23p 6的原子B .2p 能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布式为2s 22p 6的原子C .M 层全充满而N 层为4s 2的原子和核外电子排布式为1s 22s 22p 63s 23p 64s 2的原子D .最外层电子数是核外电子总数15的原子和最外层电子排布式为4s 24p 6的原子 二、非选择题(共5题)11.(1)下面是s 能级与p 能级的原子轨道图:请回答下列问题:s电子的原子轨道呈________形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道。
高考化学考点复习《原子结构》真题练习含答案

高考化学考点复习《原子结构》真题练习含答案1.(2023年湖北省普通高中学业水平合格性考试)核素146C具有放射性,考古时可用于测定某些文物的年代,该核素的质量数为A.6B.8C.14D.20【答案】C【解析】核素AZ X中,Z表示质子数,A表示质量数,则核素146C的质量数为14,C正确;故选C。
2.(2023年上海市普通高中学业水平合格性考试)氢元素有1H、2H和3H三种核素,它们含有相同的A.中子数B.质量数C.质子数D.核外电子数【答案】C【解析】氢元素的核素具有相同的质子数,不同的中子数,故答案选C。
3.(2023年云南省普通高中学业水平考试)利用放射性同位素释放的射线可以育种、给金属探伤、诊断和治疗疾病等。
关于放射性核素146C的说法正确的是A.与126C互为同位素B.中子数为6C.与石墨烯互为同素异形体D.质子数为8【答案】A【解析】A.14C、12C质子数均为6,中子数分别为8、6,因此它们互为同位素,故A正确;B.14C的中子数为14-6=8,故B错误;C.14C为核素,石墨烯为单质,两者不互为同素异形体,故C错误;D.14C的质子数为6,中子数为8,故D错误;答案为A。
4.(2023年四川省高中学业水平合格性考试)铼可用于制造航空发动机的核心部件。
铼元素在周期表中的信息如图所示。
下列有关该元素说法错误的是A.属于金属元素B.元素符号为ReC.质子数为75D.相对原子质量为186.2g【答案】D【解析】A.Re属于金属元素,故A正确;B.Re为元素符号,故B正确;C.75为元素的质子数,故C正确;D.Re的相对原子质量为186.2,故D错误;故选D。
Se的质子数为5.(2023年湖南省普通高中学业水平考试)硒(Se)是人体必需的微量元素,8034A.34B.46C.80D.114【答案】ASe可看出Se的质子数是34,质量数为80,中子数为46,故选A。
【解析】由80346.(2023年云南省普通高中学业水平考试)某元素的原子结构示意图为。
高考化学原子结构与元素周期表综合练习题及答案

高考化学原子结构与元素周期表综合练习题及答案一、原子结构与元素周期表练习题(含详细答案解析)1.锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)Zn 原子核外电子排布式为__________洪特规则内容_____________泡利不相容原理内容______________________(2)黄铜是人类最早使用的合金之一,主要由Zn 和Cu 组成。
第一电离能I 1(Zn)__________I 1(Cu)(填“大于”或“小于”)。
原因是__________(3)ZnF 2具有较高的熔点(872℃ ),其化学键类型是__________;ZnF 2不溶于有机溶剂而ZnCl 2、ZnBr 2、ZnI 2能够溶于乙醇、乙醚等有机溶剂,原因是__________(4)金属Zn 晶体中的原子堆积方式如图所示,这种堆积方式称为__________,配位数为____六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A ,Zn 的密度为__________g·cm -3(列出计算式)。
【答案】1s 22s 22p 63s 23p 63d 104s 2或[Ar ]3d 104s 2 原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低 每个原子轨道上最多只能容纳两个自旋状态不同的电子 大于 Zn 核外电子排布为全满稳定结构,较难失电子 离子键 ZnF 2为离子化合物,ZnCl 2、ZnBr 2、ZnI 2的化学键以共价键为主、极性较小 六方最密堆积(A 3型2A 3N 6a c ⨯⨯⨯ 【解析】【分析】【详解】(1)Zn 原子核外有30个电子,分别分布在1s 、2s 、2p 、3s 、3p 、3d 、4s 能级上,其核外电子排布式为1s 22s 22p 63s 23p 63d 104s 2或[Ar]3d 104s 2,洪特规则是指原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低,而泡利原理是指每个原子轨道上最多只能容纳两个自旋状态不同的电子,故答案为:1s 22s 22p 63s 23p 63d 104s 2或[Ar]3d 104s 2;原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低;每个原子轨道上最多只能容纳两个自旋状态不同的电子;(2)轨道中电子处于全满、全空、半满时较稳定,失去电子需要的能量较大,Zn 原子轨道中电子处于全满状态,Cu 失去一个电子内层电子达到全充满稳定状态,所以Cu 较Zn 易失电子,则第一电离能Cu <Zn ,故答案为:大于;Zn 核外电子排布为全满稳定结构,较难失电子;(3)离子晶体熔沸点较高,熔沸点较高ZnF 2,为离子晶体,离子晶体中含有离子键;根据相似相溶原理知,极性分子的溶质易溶于极性分子的溶剂,ZnF 2属于离子化合物而ZnCl 2、ZnBr 2、ZnI 2为共价化合物,ZnCl 2、ZnBr 2、ZnI 2分子极性较小,乙醇、乙醚等有机溶剂属于分子晶体极性较小,所以互溶,故答案为:离子键;ZnF 2为离子化合物,ZnCl 2、ZnBr 2、ZnI 2的化学键以共价键为主,极性较小;(4)金属锌的这种堆积方式称为六方最密堆积,Zn 原子的配位数为12,该晶胞中Zn 原子个数=12×16+2×12+3=6,六棱柱底边边长为acm ,高为ccm ,六棱柱体积=[(6×23a )×3×c]cm 3,晶胞密度=2A m V 3N 6a c =⨯⨯⨯,故答案为:六方最密堆积(A 3型);12;2A 3N 6a c ⨯⨯⨯。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学原子结构题
一、背景引入(100字)
原子结构是化学基础知识的重要组成部分,也经常出现在高考题目中。
了解原子结构能够帮助我们更好地理解和预测元素的性质和反应
行为。
本文将围绕高考化学原子结构题展开,探讨相关知识点,帮助
考生更好地准备高考。
二、原子结构基础知识概述(400字)
原子是物质的基本组成单位,由电子、质子和中子组成。
质子和中
子位于原子的核心,其中质子具有正电荷,中子没有电荷。
电子绕着
核心的轨道上运动,具有负电荷。
原子的电子数量决定了其化学性质。
电子的能级分布遵循科学家尼尔斯·玻尔提出的规则,即层、壳、亚壳
和轨道。
三、电子结构的表示方法(300字)
为了方便描述和理解电子结构,化学家采用了一系列符号和规则。
原子序数Z代表元素的质子数,也是元素唯一的标识。
元素的电荷数
等于其质子数,而中子数则等于质量数A减去质子数。
电子结构常用
元素符号和以下格式表示:1s²2s²2p⁶等。
其中数字代表能级壳和亚壳,字母代表轨道类型,指数代表轨道上电子的数量。
这种表示方法可用
于解释元素的化学活性和周期特征。
四、原子结构中的相关概念(500字)
在了解基本的电子结构表示方法后,我们需要掌握一些相关概念,
如原子核的电荷数、元素周期表和键结构等。
原子核电荷数等于质子数,决定了原子的正电荷。
元素周期表按照原子序数升序排列,周期
表的每一行都代表一个能级,每一列都代表一个元素组。
元素周期表
的布局很大程度上反映了原子结构的周期性特征。
键结构描述了原子
之间通过原子共享轨道形成的化学键的结构。
五、高考化学原子结构题解析(800字)
高考中原子结构题目常涉及如原子序数、元素电子结构、周期表元
素位置、共价键等。
在解题过程中,我们先确定所给元素的原子序数,并根据元素的周期表位置了解其主要电子结构。
其次,根据轨道和能
级规则,推算出对应能级和轨道的电子数。
最后,根据共价键结构、
电子的填充规则等确定键的类型和数量。
六、巩固练习与解析(300字)
为了巩固所学知识,我们可以进行一些高考化学原子结构题的练习。
例如,找出原子序数在5-10范围内的元素,写出其电子结构;根据所
给元素的周期表位置,推算其主要电子结构和键结构。
通过大量的练
习和解析,我们可以更好地掌握原子结构的相关知识,并在高考中取
得好成绩。
七、总结(100字)
高考化学原子结构题是考查学生对原子结构及其相关知识的掌握程
度的题目。
通过了解原子结构的基础知识,掌握电子结构的表示方法
以及相关概念,我们能够更好地应对这类题目。
通过大量的练习和巩固,我们可以达到理解和预测元素性质和反应行为的目标。
加油,相信你一定能在高考中取得成功!。
