实验七
实验七:精馏塔板效率测定实验

实验七精馏塔塔板效率测定实验一、实验目的1、熟悉精馏单元操作过程的设备与流程;2、了解板式塔结构与流体力学性能;3、掌握精馏塔的操作方法与原理;4、学习精馏塔效率的测定方法。
二、实验原理蒸馏原理是利用混合物中组分间挥发度的不同来分离组分,经多次平衡分离的蒸馏过程称为精馏。
常见的精馏单元过程由精馏塔、冷凝器、再沸器、加料系统、回流系统、产品贮槽、料液贮槽及测量仪表等组成。
精馏塔本身又分为板式精馏塔和填料精馏塔,本产品为板式精馏塔。
可进行连续或间歇精馏操作,回流比可任意调节,也可以进行全回流操作。
在板式精馏塔中,混合液的蒸气逐板上升,在塔顶冷凝后回流液逐板下降。
气液两相在塔板上接触实现热质传递,从而达到分离的目的。
如果在每层塔板上,下降液体与上升蒸气处于平衡状态,则该塔板称为理论板。
然而在实际操作的精馏塔中,由于气液两相在塔板上接触的时间有限,气液两相不可能完全达到平衡,亦即实际塔板的分离效果达不到理论板的作用,因此精馏塔所需要的实际板数总是比理论板数要多。
对于二元物系,如已知其气液平衡数据,则根据精馏塔的原料液组成、进料热状况、操作回流比及塔顶馏出液组成、塔底釜液组成,即可以求出该塔的理论板数N t。
1、精馏塔的正常与稳定操作精馏塔从开车到正常稳定操作是一个从不稳定到稳定、不正常到正常的渐进过程。
因为刚开车时,塔板上均没有液体,蒸汽可直接穿过干板到达冷凝器,被冷凝成液体后再返回塔内第一块塔板,并与上升的蒸汽接触;而后,逐板溢流至塔釜。
首先返回塔釜的液体经过的塔板数最多,达到的气液平衡次数也最多,所以其轻组分的含量必然最高;而第一块塔板上的液体轻组分含量反而会比它下面的塔板上的液体轻组分含量低一些,这就是“逆行分馏”现象。
从“逆行分馏”到正常精馏,需要较长的转换时间。
对实验室的精馏装臵,这一转换时间至少需30分钟以上。
而对于实际生产装臵,转换时间有可能超过2小时。
所以精馏塔从开车到稳定、正常操作的时间也必须保证在30 分钟以上。
实验七 铬、锰

重 铬 酸 钾 与 浓 盐 酸 反 应 演 示
(5)铬酸根和重铬酸根在溶液中的平衡
Cr2O72- 与CrO4- 在不同酸度时的转化
(6)微溶性铬酸盐的生成
铬 酸 钾 与 金 属 离 子 反 应
(6)微溶性铬酸盐的生成
重 铬 酸 钾 与 金 属 离 子 反 应
实验七 铬、锰
一、实验目的
★ 掌握铬、锰化合物的氧化还原性及介质对产 物的影响。 ★掌握铬、锰价态相互转化的规律及转化条件。 ★学会离子的鉴定方法。 ★熟练掌握沉淀的分离、洗涤等操作。
二、内容提要(一)
表 1 铬、锰常见氧化态 稳定氧化态
Cr
+3,+6
Mn
+2,+4,+6,+7
不稳定氧化态 +2
+3,+5
二、内容提要(二)
铬的各种主要价态化合物的重要性质,各种价态的转化条件
CrO5 蓝色 H+(O2)Cr3+(兰紫色)适量 OH- Cr(OH)3 灰蓝色过量 OH- CrO2-绿色 H+
H2O2+HNO3 H++SO32-
乙醚
OHCr2O72-(橙红色)
H+
CrO42-(黄色)
H2O2+OH-
Pb2+ Ag+ Ba2+
使用什么酸做酸性介质?
(2)Mn(Ⅳ)的生成和氧化性
①MnO2 的制取及其氧化性 ②MnO2与浓盐酸反应
二氧化 锰与浓 盐酸反 应及生 成物鉴 定
(3)Mn(VI)的生成和氧化还原稳定性 注意使用40%浓NaOH,水浴加热
实验七-实验报告

实验七:超声化学法制备纳米多孔氧化物及其电化学性能研究专业:材料物理姓名:许航学号:141190093一、实验内容与目的1、学习超声化学反应的基本原理,熟悉反应装置的构成;2、通过与其他方法比较,了解超声化学法在多孔纳米材料制备方面的优缺点;3、学习超声化学法制备多孔金属氧化物的实验步骤,了解多孔纳米材料的表征方法;4、学习电化学工作原理,掌握电容测试方法,熟悉超级电容器常用的金属氧化物材料。
二、实验原理超声化学主要源于声空化导致液体中微小气泡形成、振荡、生长收缩与崩裂及其引起的物理、化学效应。
液体声空化是集中声场能量并迅速释放的过程,空化泡崩裂时,在极短时间和空化极小空间内,产生5000K以上的高温和约5.05×108Pa的高压,速度变化率高达1010K/s,并伴有强烈的冲击波和时速高达400km的微射流生成,使碰撞密度高达1.5kg/s;空化气泡的寿命约0.1μs,它在爆炸时释放出巨大的能量,冷却速率可达109K/s。
这为一般条件下难以或不能实现的化学反应提供了一种特殊的环境。
这些极端条件足以使有机物、无机物在空化气泡内发生化学键断裂、水相燃烧和热分解条件,促进非均相界面之间搅动和相界面的更新,极大提高非均相反应的速率,实现非均相反应物间的均匀混合,加速反应物和产物的扩散,促进固体新相的生成,并控制颗粒的尺寸和分布。
通过将超声探头浸入反应溶液中就可将超声波引入到一个有良好控温范围的反应系统。
利用超声来使反应体系中的物质得到充分的反应,从而制备出颗粒分布、大小尺寸均匀的纳米多孔氧化物。
三、实验数据及处理1.循环伏安曲线在恒定扫描速率下,伏安特性曲线为闭合曲线,且扫描速率越快,围成的图形面积越大。
2.恒流充放电电压-时间曲线曲线包括充电和放电两个过程,设定电压从0V充到0.6V,再放电到0V。
随着充电电流的增加,充放电总时间增长,曲线的峰点向时间增加的方向移动。
3.电容与充放电电流的关系通过公式C=I×∆t/∆v计算样品的电容值,做出电容-充放电电流曲线图,发现随着充放电电流的增加,测定的电容值减小,电容与电流几乎呈线性关系四、思考与讨论1、超声化学法来制备多孔金属氧化物纳米材料的过程中,超声波起了什么作用?答:超声在纳米材料的制备中的作用源自空化效应。
实验7(挥发酚的测定)

4-AAP分光光度法测苯酚
1、条件: pH9.8~10.2 2、原理:在铁氰化钾存在的条件下,酚类 化合物与4-AAP反应生成橙红色染料。
λmax=510nm
λmax=510nm
pH9.8~10.2
比色管 (5Biblioteka mL)0.1 mL 氯化铵 缩合 反应
0.1 mL 4-AAP 0.2 mL 铁氰化钾
橙红色 λmax=510nm
3.实验仪器与试剂
仪器: 分光光度计 比色管 刻度吸管 移液管
试剂: 苯酚标准液 溴酸钾--溴化钾 pH=10缓冲液 4-氨基安替比林 铁氰化钾 淀粉 碘化钾 硫代硫酸钠
4.操作步骤
用硫代硫酸钠标定苯酚,制作标准色列 管 分光光度计的校正 水样显色、比色 标准曲线绘制 计算
备注
注意事项: 每加完一种试剂,须摇匀,使反应完全; 分光光度计的校正; 矫零和测定用同一个比色皿; 注意测定过程中不要碰到波长旋钮; 掌控好标准液的加入体积,末梢一滴不吹; 需带:坐标纸、铅笔、橡皮擦、直尺。 课时:4
作业
1、完成实验报告。
环境质量监测技术
本次课内容
实验七:挥发酚的测定
1.实验目的
掌握4-氨基安替比林( 4-AAP )分光 光度法测挥发酚的原理和方法。 练习标准系列的比色法; 巩固标准曲线的制作方法。
2.原理
预处理:蒸馏法
原理: 4-氨基安替比林与酚类化合物在PH=10 溶液中,在氧化剂铁氰化钾作用下,生 成橙红色的吲哚酚安替比林染料,于 510nm波长下测吸光度,由标准曲线上 查出含量。
实验7 局部阻力系数实验

实验七 局部阻力系数实验1实验目的和要求1.掌握测量局部阻力系数的方法;2.测量管道突然扩大、突然缩小时的局部阻力系数;3.了解影响局部阻力系数的因素2局部阻力系数实验的原理水流在流动过程中,由于水流边界条件或过水断面的改变,引起水流内部各质点的流速、压强也都发生变化,并且产生旋涡。
在这一过程中,水流质点间相对运动加强,水流内部摩擦阻力所作的功增加,水流在流动调整过程中消耗能量所损失的水头称为局部水头损失。
局部水头损失的一般表达式为gvh j 22ζ= (1)式中,j h 为局部水头损失;ζ为局部水头损失系数,即局部阻力系数,它是流动形态与边界形状的函数,即)(e R f 边界形状,=ζ,一般水流的雷诺数e R 足够大时,可以认为ζ系数不再随e R 而变化,可视作为一常数;v 为断面平均流速,一般用发生局部水头损失以后的断面平均流速,也有用损失断面前的平均流速,所以在计算或查表时要注意区分。
局部水头损失可以通过能量方程进行分析。
图1为一水流突然扩大的实验管段,在发v 1图1 局部水头损失分析简图j h =gv v p z p z 2)()(2222112211ααγγ-++-+(2)式中,)()(2211γγp z p z +-+为断面1-1和2-2的测压管水头差;v 1、v 2 分别为1-1断面和2-2断面的平均流速。
管道局部水头损失目前仅有断面突然扩大(图1)可利用动量方程,能量方程和连续方程进行理论分析,并可得出足够精确的结果,其它情况尚需通过实验方法测定局部阻力系数。
对于管道突然扩大,理论公式为gv v h j 2221)(-= (3)由连续方程A 1v 1=A 2v 2,解出v 1或v 2代入上式可分别得 g v A A h j 2122212)(-= , 21211)(扩大-=A A ζ (4)或 gv A A h j 2121221)(-=, 22121)(扩大A A -=ζ (5)式中,A1、A2分别为断面1-1和2-2的过水断面面积;1扩大ζ、2扩大ζ叫做突然放大的局部阻力系数。
实验七ABO血型鉴定

实验七、ABO血型鉴定一、实验原理血型是指红细胞膜上特异的抗原(凝集原)类型,常用血型系统有ABO系统、Rh系统。
血清中存在能与红细胞膜上相应抗原发生反应的抗体,称为凝集素。
ABO血型鉴定原理是血清中抗体(或凝集素)与红细胞的相应抗原起反应,产生凝集反应,而后发生血溶现象。
各种血型抗原与抗体分布:血型红细胞抗原(凝集原)血浆中抗体(凝集素)A A 抗BB B 抗AAB AB 无O 无抗A、抗B二、实验步骤1、双凹载玻片加两种血清:黄色抗B;蓝色抗A;2、消毒、采血(灭菌牙签);3、静置10分钟,观察。
三、实验结果ABO血型系统根据红细胞表面有无特异性抗原(凝集原)A和B来划分的血液类型系统。
根据凝集原A、B的分布把血液分为A、B、AB、0四型。
红细胞上只有凝集原A的为A 型血,其血清中有抗B凝集素;红细胞上只有凝集原B的为B型血,其血清中有抗A的凝集素;红细胞上A、B两种凝集原都有的为AB型血,其血清中无抗A、抗B凝集素;红细胞上A、B两种凝集原皆无者为O型,其血清中抗A、抗B凝集素皆有。
具有凝集原A的红细胞可被抗A凝集素凝集;抗B凝集素可使含凝集原B的红细胞发生凝集。
如上表所示,当与抗A试剂反应为阳性,与抗B反应为阴性时,血型为A;当与抗A试剂反应为阴性,与抗B试剂反应为阳性时,血型为B;当与抗A、抗B试剂反应均为阳性时,血型为AB;而当与抗A、抗B试剂反应均为阴性时,血型则为O。
输血时若血型不合会使输入的红细胞发生凝集,引起血管阻塞和血管内大量溶血,造成严重后果。
所以在输血前必须作血型鉴定。
正常情况下只有ABO血型相同者可以相互输血。
在缺乏同型血源的紧急情况下,因O 型红细胞无凝集原,不会被凝集,可输给任何其他血型的人。
AB型的人,血清中无凝集素,可接受任何型的红细胞。
但是异型输血输入量大时,输入血中的凝集素未能被高度稀释,有可能使受血者的红细胞凝集。
所以大量输血时仍应采用同型血。
实验7:甲基橙的制备(6h)
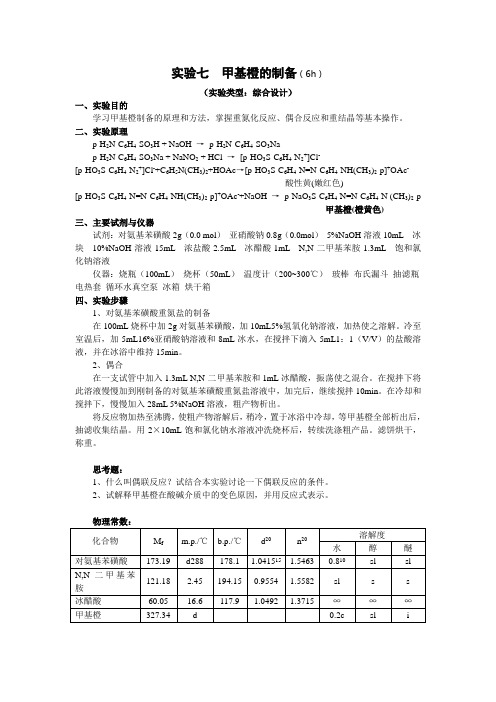
实验七甲基橙的制备(6h)(实验类型:综合设计)一、实验目的学习甲基橙制备的原理和方法,掌握重氮化反应、偶合反应和重结晶等基本操作。
二、实验原理p-H2N-C6H4-SO3H + NaOH →p-H2N-C6H4-SO3Nap-H2N-C6H4-SO3Na + NaNO2 + HCl →[p-HO3S-C6H4-N2+]Cl-[p-HO3S-C6H4-N2+]Cl-+C6H5N(CH3)2+HOAc→[p-HO3S-C6H4-N=N-C6H4-NH(CH3)2-p]+OAc-酸性黄(嫩红色)[p-HO3S-C6H4-N=N-C6H4-NH(CH3)2-p]+OAc-+NaOH →p-NaO3S-C6H4-N=N-C6H4-N (CH3)2-p甲基橙(橙黄色)三、主要试剂与仪器试剂:对氨基苯磺酸2g(0.0 mol)亚硝酸钠0.8g(0.0mol)5%NaOH溶液10mL 冰块10%NaOH溶液15mL 浓盐酸2.5mL 冰醋酸1mL N,N-二甲基苯胺1.3mL 饱和氯化钠溶液仪器:烧瓶(100mL)烧杯(50mL)温度计(200~300℃)玻棒布氏漏斗抽滤瓶电热套循环水真空泵冰箱烘干箱四、实验步骤1、对氨基苯磺酸重氮盐的制备在100mL烧杯中加2g对氨基苯磺酸,加10mL5%氢氧化钠溶液,加热使之溶解。
冷至室温后,加5mL16%亚硝酸钠溶液和8mL冰水,在搅拌下滴入5mL1:1(V/V)的盐酸溶液,并在冰浴中维持15min。
2、偶合在一支试管中加入1.3mL N,N-二甲基苯胺和1mL冰醋酸,振荡使之混合。
在搅拌下将此溶液慢慢加到刚制备的对氨基苯磺酸重氮盐溶液中,加完后,继续搅拌10min。
在冷却和搅拌下,慢慢加入28mL 5%NaOH溶液,粗产物析出。
将反应物加热至沸腾,使粗产物溶解后,稍冷,置于冰浴中冷却,等甲基橙全部析出后,抽滤收集结晶。
用2×10mL饱和氯化钠水溶液冲洗烧杯后,转续洗涤粗产品。
实验七----电导法测定醋酸的电离度和电离常数

一. 实验目的1、掌握醋酸解离度和解离常数测定方法,加深对电离度,电离常数和溶液浓度与电导关系的理解。
2、学习电导法测电离度的原理和在井穴板中进行电导率测量的操作;理解酸度计的使用。
3、进一步掌握溶液的配制、滴定操作。
二. 实验原理1、醋酸(CH3COOH或HAc)是弱电解质,在水溶液中存在下列解离平衡:起始浓度(mol/L) c 0 0平衡浓度(mol/L) c- cαcαcα若c为醋酸的起始浓度,α为醋酸的解离度,[H+]、[Ac-]、[HAc]分别为H+、Ac-、HAc的平衡浓度,Kα为醋酸的解离常数,则[H+]=[Ac-]= cα [HAc]= c(1-α)解离度:α=[H+]/c×100%解离常数:Kα=[H+][Ac-]/[HAc]= cα2/(1-α)=[H+]2 /(c-[H+])已知pH=-lg[H+],所以测定了已知浓度的醋酸溶液的pH值,就可以求出它的解离度和解离常数。
2、PHS-3C酸度计直接电位法测定pH值的原理PHS-3C型精密级酸度计是一3(1/2)位数字显示的酸度计,适用于研究室、医药、学校、化工、环保等化验室的取样测定水溶液的酸度(pH值)和测量电极电位(mV值)。
如配上适当的离子选择电极,则可以作为电位滴定。
其工作原理是利用复合电极对被测水溶液中不同的酸度产生直流电位,通过前置阻抗转换器把高内阻的直流电位转变成低内阻的直流电位,输入到A/D转换器,以达到pH值数字显示。
同样,配上适当的离子选择电极作电位滴定分析时,以达到终点电位显示。
以pH玻璃电极作指示电极,甘汞电极作参比电极,插入溶液中即组成测定pH值的原电池。
在一定条件下,电池电动势E是试液中pH值的线性函数。
测量E时,若参比电极(甘汞电极)为正极,则E=K+0.059pH(25℃)当pH玻璃-甘汞电极对分别插入pHS标准缓冲溶液和pH x未知溶液中,电动势E S和Ex 分别为E S=K+0.059pH S(25℃)Ex=K+0.059pH x(25℃)两式相减,得(25℃)三. 仪器设备及试剂仪器:容量瓶(50mL),吸量管(10mI),移液管(25mL),烧杯(50mL),锥形瓶(250mL),碱式滴定管(50mL),pHs-3C型酸度计。
(实验七)求最大值和最小值实验报告

实验七求最大值和最小值一、实验目的1、学习子程序的定义和调用方法。
2、掌握子程序设计、调试。
二、实验内容对内存中给定的几个无符号字节数,求其最大值和最小值并在数码管上显示。
三、实验程序框图四、实验步骤脱机模式:(1)在P.态下,按SCAL键,然后在内存4000H~4007H中写入任意八个字节的数,按下MON键,返回P状态。
(2)在P.态下,输入2E70,按EXEC键。
(3)数码管显示为:“XX——XX”,最左两位为最大值,最右两位为最小值。
(4)按“系统复位”键,退出运行状态,数码管返回“P。
”状态。
联机模式:(1)在内存4000H~4007H中写入任意八个字节的数,按下MON键,返回P状态。
(2)在PC机和实验系统联机状态下,运行该实验程序,可用鼠标左键单击菜单栏“文件”或工具栏“打开图标”,弹出“打开文件”的对话框,然后打开8kAsm文件夹,点击S7.ASM 文件,单击“确定”即可装入源文件,再单击工具栏中编译,即可完成源文件自动编译、装载目标代码功能,再单击“调试”中“连续运行”或工具图标运行,即开始运行程序。
(3)数码管显示为:“XX——XX”,最左两位为最大值,最右两位为最小值。
(4)按“系统复位”键,退出运行状态,数码管返回“P。
”状态。
五、实验程序清单X:\DICE-8086K3微机原理与接口实验箱CDROM\CODE\86kasm\S7.ASMCODE SEGMENT ;S7.ASM,LOOK FOR MAX & MINASSUME CS:CODEORG 2E70H ;INPUT DATA 4000H--4007HSTART: JMP START0PA EQU 0FF21H ;字位口PB EQU 0FF22H ;字形口PC EQU 0FF23H ;键入口BUF DB ?,?,?,?,?,?data1:db0c0h,0f9h,0a4h,0b0h,99h,92h,82h,0f8h,80h,90h,88h,83h,0c6h,0a1hdb 86h,8eh,0ffh,0ch,89h,0deh,0c7h,8ch,0f3h,0bfh,8FH START0: MOV SI,4000H ;数据首址MOV CX,0008H ;长度CALL MAXMIN ;调用比较大小子程序CALL BUF1 ;最大最小值送显示缓冲区CON1: CALL DISP ;循环调用显示子程序JMP CON1MAXMIN: JCXZ EXIT ;比较结束子程序返回PUSH SI ;压栈PUSH CXPUSH BXMOV BH,[SI] ;取第一个数MOV BL,BH ;保存数据到BLCON2: LODSB ; 取数CMP AL,BH ;比较两数JNA X1 ;小于等于转MOV BH,AL ;BH存大的数JMP X2 ;转X2X1: CMP AL,BL ;比较两数JNB X2 ;大于等于转MOV BL,AL ;BL存小的数X2: LOOP CON2 ;未完继续MOV AX,BX ;POP BX ;出栈POP CXPOP SIEXIT: RET ;返回DISP: MOV AL,0FFH ;显示子程序5msMOV DX,PAOUT DX,ALMOV CL,0DFH ;注释略,见实验六显示程序MOV BX,OFFSET BUFDIS1: MOV AL,[BX]MOV AH,00HPUSH BXMOV BX,OFFSET DATA1ADD BX,AXMOV AL,[BX]POP BXMOV DX,PBOUT DX,ALMOV AL,CLMOV DX,PAOUT DX,ALPUSH CXDIS2: MOV CX,00A0HLOOP $POP CXCMP CL,0FEH ;01HJZ LX1MOV AL,0FFH ;00HMOV DX,PAOUT DX,ALINC BXROR CL,1 ;SHR CL,1JMP DIS1LX1: MOV AL,0FFHMOV DX,PBOUT DX,ALRETBUF1: MOV BH,AHCALL ZHMOV BUF+5,ALMOV BUF+4,AHMOV AL,BHCALL ZHMOV BUF,AHMOV BUF+1,ALMOV BUF+2,17HMOV BUF+3,17HRET;-------------------------------------------------------- ZH: MOV BL,AL ;数据拆送MOV CL,4ROL AL,CLAND AL,0FHMOV AH,ALMOV AL,BLAND AL,0FHRET;------------------------------------------------------- CODE ENDSEND START。
实验七 乙酰苯胺的制备

实验七 乙酰苯胺的制备一、实验目的:1、掌握苯胺乙酰化反应的原理和实验操作。
2、了解重结晶原理,初步学会用重结晶方法提纯固体有机化合物。
3、掌握热过滤和抽滤操作。
二、实验原理:反应原理NH 2COCCH 3CH 3OO NH 2C OCCH 3CH 3O O N HCCH 3O CH 3COOH+δ+δ-+++三、主要试剂及物理常数:名称 分子量 熔点℃ 沸点℃ 密度 苯胺 93 -6.2 184.4 1.0216 冰醋酸 60 16.7 118 1.049 乙酰苯胺135114.33051.2105四、实验步骤:1、用100 mL 园底烧瓶搭成回流装置。
2、向反应瓶中加入10 mL 新蒸的苯胺、15 mL 冰醋酸和15ml 醋酐(注:加入酸酐时体系会剧烈放热)、0.1g 锌粉,摇匀。
接好回流冷凝管,然后加热到微沸,保持15分钟。
3、渐升温,反应物维持在100-110℃约1小时。
4、反应结束后用流水稍冷反应瓶后倒入盛有50ml 水和40~50g 冰的烧杯中,既有白色固体析出,充分搅拌冷却后抽滤,收集固体。
5、粗产物以水重结晶。
注1:乙酰苯胺的溶解度:5.55%(100℃) 3.45%(100℃)0.84%(50℃)0.45%(20℃)五、注意事项:1、反应所用玻璃仪器必须干燥。
2、久置的苯胺因为氧化而颜色较深,最好使用新蒸馏过的苯胺。
3、冰乙酸在室温较低时凝结成冰状固体(凝固点16.6 C ),可将试剂瓶置于热水浴中加热熔化后量取。
4、锌粉的作用是防止苯胺氧化,只要少量即可。
加得过多,会出现不溶于水的氢氧化锌。
5、反应时间至少30min。
否则反应可能不完全而影响产率。
6、反应时分馏温度不能太高,以免大量乙酸蒸出而降低产率。
7、重结晶时,热过滤是关键一步。
布氏漏斗和吸滤瓶一定要预热。
滤纸大小要合适,抽滤过程要快,避免产品在布氏漏斗中结晶。
8、重结晶过程中,晶体可能不析出,可用玻棒摩烧杯壁或加入晶种使晶体析出。
实验七、流体压强及其测量演示实验

流体压强及其测量演示实验一、实验目的1、掌握绝对压强、表压强和真空度之间的区别和联系。
2、掌握流体液柱高度、压头与压强之间的区别和联系。
3、掌握用U 形管测流体压强、压差的方法。
二、基本原理1、 压力定义及表征静止流体所受的外力有质量力和压应力两种,其中在单位面积上所收的压应力称为压强,习惯上又称为静压力。
因为静止流体中任一点不同方向的静压力数值相等,所以静压力只要说明其大小即可,通常用符号p 表示。
在国际单位制(SI )中,压力的单位是2/N m ,称为帕斯卡Pa ,帕斯卡与其他压力单位之间的换算关系为51.013101(()Pa atm at ⨯=标准大气压)=1.033工程大气压276010.33m m H g m H O== 当使用压力的实际数值来表示压力大小时,称为绝对压力,简称绝压。
另外,因为整个地球都处在大气层的压力下,故压力还可以当地大气压为基准来计量,通常用压力表或真空表测出,称为表压或真空度。
表压或真空度与绝压的关系为表压=绝压-当地大气压真空度=当地大气压-绝压在同一地理位置,表压越大,绝压也越大;真空度越大,绝压越小,真空度就高。
而大气压即大气层压力的大小,与经纬度、海拔高度等因素有关,当地大气压可用气压计测得。
2、 测压原理及仪器对于连续、均质且不可压缩流体,流体密度ρ为常数,在静止状态下,有2112()p p g z z ρ=+- 式中1p 、2p 为静止流体任意两点处压强,1z 、2z 为该两点的竖直高度,g 为重力加速度。
将上式两边同除以g ρ,得2112()p p z z g gρρ=+- 式中,1p g ρ、2p gρ有高度单位,称为静压头;相应地,1z 、2z 称为位头。
工程实际中应用静力学原理测量流体压力和压力差相当广泛,液柱压差计就是利用流体静力学原理测量静压力的仪器,主要形式介绍如下。
(1) 单管压力计如图1所示,将一单管与被测压力容器A 相连通,单管另一端通大气,这就构成了单管压力计。
实验七过氧化物酶的显示

【观察与成果】
骨髓细胞内能够见到蓝色或者棕色旳颗粒, 即过氧化物酶所在旳部位。
【试验环节】
用颈椎脱臼法处死小鼠,剪开大腿上旳皮肤和肌肉, 取出股骨;
剪断或者折断股骨,用牙签挑取骨髓,放置于载玻片 上制成涂片,晾干;
将涂片上滴加几滴0.5% CuSO4,固定1分钟; 倾去CuSO4溶液,滴加0.1%联苯胺混合液,染色6分
钟; 用自来水或蒸馏水冲洗,滴加1%番红染液(染色细胞
试验7 细胞内过氧化物酶旳显示
联苯胺反应
【试验目旳】
掌握联苯胺反应法显示细胞内过氧化物酶旳原 理和措施。
过氧化物酶 - 定义
利用过氧化氢作为电子受体来催化底物氧化作 用旳酶。
【试验原理】
细胞内旳过氧化物酶能够催化过氧化氢氧化联 苯胺成蓝色或者棕色产物,蓝色为中间产物联 苯胺蓝,很不稳定,可自然转变为棕色旳联苯 胺腙,经过产物颜色间接显示出细胞内过氧化 物酶旳分布。
【试验仪器、材料和试剂】
光学显微镜;小白鼠、剪刀、镊子、载玻片、 牙签、吸管。
0.5% CuSO4(0.5克CuSO4溶于100ml蒸馏 水中)、联苯胺混合液(0.1克联苯胺在研钵 中加少许蒸馏水研成细浆,加入100ml蒸馏水, 过滤后加入2滴3%双氧水,放棕色瓶中备用)、 1%番红[1克番红O(Safranine O)染料溶于 100ml蒸馏水中]。
实验七:室内及皮肤表面微生物分布测定技术

实验七 室内及皮肤表面微生 物分布测定技术
一、实验目的
1. 验证空气中微生物的存在 2. 掌握室内环境中微生物的检测方法 3. 验证人体的皮肤表面正常菌群的存在 4. 掌握人体正常菌群的检测技术
二、实验原理
悬浮在空气中的微生物落在适宜于它们生长的固 体培养基表面,在适宜温度下培养一段时间后, 每个分散的菌体就会形成一个个肉眼可见的细胞
100cm2培养基上平均菌落数 每立方米空气中活菌数 = × 1000 20 实验证明:在空气中暴露10min后,每100cm2培养 基表面生长的菌落数相当于20L空气中所含的微生物数。
(二)皮肤表面微生物分布测定 1. 熔化培养基: 100℃水浴加热使培养基完全熔化。 2. 倒平板:将已熔化的培养基冷却至60℃左右, 倒3块营养琼脂培养基平板,待凝固后分别如下记 号:1、洗手前,2、洗手后,3、酒精消毒。 3. 洗手前用右手食指在1号培养基的表面画“+”字。 4. 用洗手液洗手,以流水冲洗3min以上,用镊子 取无菌棉球擦干右手食指,然后在2号培养基的表 面画“+”字。 5.用酒精棉球消毒右手食指后,在3号培养基的表 面画“+”字。 6.将上述平板倒置于37℃培养箱培养48小时。 7.观察结果并计数。
皿盖以作对照。
每立方米空气中活菌数
4. 培养:将平板置于37℃培养箱倒置培养48
小时。
5. 观察平板菌落生长情况,计数平板菌落数 目,记录结果。
6. 根据下列公式计算出100cm2培养基的菌落 数及每立方米空气中的活菌数。
计算公式 100cm2培养基的菌落数
=
r为平板半径
每个平皿菌落数 × 100 2 ∏r
高中物理实验7测动摩擦因数和重力加速度等

实验七 测重力加速度、摩擦因数和反应时间江苏省特级教师 戴儒京一、实验原理、装置、步骤和数据处理用光电门测重力加速度 实验原理:在加速度为a 的运动过程中,如果0t =时,速度为1V ,位移0x =,那么在0t >的任意时刻,位移都可以表示成2112x at V t =+,如果在t T =时刻的位移为d ,速度为2V ,那么经过简单的代换,21V V T a-=,就可以得到加速度的表达式22212V V a d -=。
把前面的方程运用到自由落体过程中,重力加速度可以表达为22212V V g d-=,实验中让一个矩形挡光片依次穿过相距为d 的两个光电门,因为两个光电门可以先后测量速度1V ,2V ,能够测量重力加速度的大小。
前面的推导也可由机械能守恒简单得到,物体在自由落体过程中假设1t 时刻的速度1V ,下一个时刻2t 的速度为2V ,中间通过的位移为d ,当然,这里有12V V <,那么,22211122mgd mV mV =-,重力加速度可以表达为22212V V g d -=。
实验目的:理解光电门的工作方式,用这种方式测重力加速度。
实验装置:计算机,数据采集器,两个光电门,铁架台,直尺,单摆,矩形挡光片实验步骤:1.按实验装置图搭建实验平台,把上面的光电门称为光电门1,把它连接到数据采集器的1通道,把下面的光电门称为光电门2,把它连接到数据采集器的2通道。
注意,两个光电门的位置不能接反了。
2.调节两个光电门的位置,使挡光片在下落过程中能顺利穿过光电门,用直尺测量矩形挡光片的宽度,和两个光电门间的距离,并记录下来。
3.将数据采集器与计算机连接,开启采集器电源,进入实验专用界面,在专用界面右下脚的参数窗口输入光电门间的距离,挡光片宽度选项分别输入记录的值。
4.在采集数量窗口输入合适的数值,点击开始按钮,手持矩形挡光片,悬于两个光电门的上方,释放后,挡光片依次通过光电门,多次反复操作。
实验七--食品中金黄色葡萄球菌的检验

实验七食品中金黄色葡萄球菌的检验一、实验目的要求1、了解食品的质量与金黄色葡萄球菌检验的意义.2、掌握金黄色葡萄球菌的生物学特性.3、掌握金黄色葡萄球菌检验的生化试验的操作方法和结果的判断。
4、掌握食品中金黄色葡萄球菌检验的方法和技术。
二、原理葡萄球菌在自然界分布极广,空气、土壤、水、饲料、食品(剩饭、糕点、牛奶、肉品等)以及人和动物的体表粘膜等处均有存在,大部分是不致病,也有一些致病的球菌.金黄色葡萄球菌是葡萄球菌属一个种。
可引起皮肤组织炎症,还能产生肠毒素。
如果在食品中大量生长繁殖,产生毒素,人误食了含有毒素的食品,就会发生食物中毒,故食品中存在金黄色葡萄球菌对人的健康是一种潜在危险,检查食品中金黄色葡萄球菌及数量具有实际意义。
金黄色葡萄球菌能产生凝固酶,使血浆凝固,多数致病菌株能产生溶血毒素,使血琼脂平板菌落周围出现溶血环,在试管中出现溶血反应.这些是鉴定致病性金黄色葡萄球菌的重要指标。
三、试剂和仪器(一)最先准备的器材规格名称数量用途1、500ml广口瓶1个稀释样品2、500ml三角瓶1个制生理盐水3、250ml三角瓶3个制培养基等4、10×100mm试管6支血浆凝固酶试验5、1ml移液管2支6、10ml移液管 2 支7、直径为90 mm平皿12套制血平板B—P平板8、250ml量筒1支(二)应灭菌的其它器材剪刀1把不锈钢汤匙1把称量纸适量(三)应制备的培养基培养基总量所用容器1.无菌水50ml/瓶1瓶250ml三角瓶(全班共用)2.0。
85%生理盐水70ml/瓶1瓶250ml三角瓶(全班共用)3.0.85%生理盐225ml/瓶1瓶500ml三角瓶4.7。
5%NaCl肉汤50ml/瓶1瓶250ml三角瓶5.普通营养琼脂100ml/瓶1瓶250ml三角瓶6.B—P培养基95ml/瓶1瓶250ml三角瓶7.兔血液5ml四、实验内容(一)、增菌培养法样品处理→→选择性增菌→→选择性平板分离→→血浆凝固酶试验鉴别→→结果报告第一天样品处理和增菌培养(一)、样品处理固体或半固体食品:以无菌操作称取25g样品,放入装有225mL灭菌生理盐水的灭菌均质杯内,于8000r/min均质1~2min,制成1:10样品匀液。
实验七 坐姿压力测试实验

实验七座椅表面压力测试实验一、实验目的(1)通过实验使学生掌握表面压力测量方法,能对TEKSCAN软件和硬件熟练使用,获取坐姿作业过程中的人体的压力参数并进行分析处理。
(2)找出影响座椅表面压力的关键因素,并对其进行评价。
二、实验说明在各种作业形式下,人体与接触面的压力分布会对作业者自身的舒适感受产生影响。
因此,压力测试实验在人因工程学中应用广泛,是一项非常重要的实验。
而随着现代化办公方式的不断发展,坐姿成为大部分人的主要作业形式,座椅的舒适性会影响作业者疲劳状态,因此,获得人体在座椅上的压力分布数据,可以改善座椅的设计。
三、实验仪器Tekscan 人体压力量测系统(BPMS)Tekscan公司生产的人体压力量测系统广泛用于量测人体在汽车座椅和办公椅上的压力分布情况,获取的信息可以用来改进座椅的设计,提高舒适性。
Tekscan压力分布测试及分析系统该系统使用独特的柔性薄膜网格压力传感器,能够对任何接触面之间的压力分布进行动态测量,并以直观、形象的二维、三维彩色图形显示压力分布轮廓和数值,进而做出评估。
Tekscan 人体压力量测系统这套系统包括了USB数据撷取器、操作软件和薄膜压力感测片(感测垫)。
此套系统所搭配的感测片,其空间分辨率最高可达每平方公分分布一个感测点,每片感测片可包括高达2,016个感测点。
并且,系统可扩充及支持多组感测片同时操作,最多可扩充到同时处理16,128个感测点。
而感测片细薄的厚度,能够被便捷地安装在测体上,却不破坏原始接触表面的性质。
这些特色使得该设备能够精准地测量局部压力的峰值,以及整体压力的分布状态。
体压分布就是当人坐在座椅上,座椅对人体各部分压力的大小及其分布状态。
一般而言,常用体压分布的各项数据是座椅舒适度评价的依据之一。
常用的体压分布的指标有最大压力、平均压力、最大压力梯度、平均压力梯度、不对称系数、纵向压力分布曲线和纵向力矩分布曲线等。
四、实验内容1、设计合理的作业任务:本次实验任务为模拟办公室文员的坐姿作业;2、被试选择:坐姿压力测量任务需要选择20余名健康的被试,本次实验仅以一人为例;3、数据获取:运用Tekscan压力分布测试系统获取坐姿作业过程中的人体的压力参数;4、数据分析:对获取的数据进行分析并加以评价。
实验七_正溴丁烷的制备

正溴丁烷的制备【实验目的】1.了解以正丁醇、溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法。
2.掌握带有害气体吸收装置的加热回流操作。
3.进一步熟悉巩固洗涤、干燥和蒸馏操作。
【实验原理】n-C 4H 9OH + NaBr + H 2SO 4n-C 4H 9Br + NaHSO 4 + H 2O副反应:CH 3CH 2CH 2CH 2OHCH 3CH 2CH=CH 2 + H 2O CH 3CH 2CH 2CH 2OH 浓H SO (CH 3CH 2CH 2CH 2)2O + H 2O HBr + H2SO 422Br 2 + SO 2 + 2H 2O【实验的准备】仪 器:圆底烧瓶(50 ml 、100 ml 各1个);冷凝管(直形、球形各1支);温度计套管(1个);短径漏斗(1个);烧杯(800 ml 1个);蒸馏头(1个);接引管(1个);水银温度计(150℃ 1支);锥形瓶(2个);分液漏斗(1个)。
药 品: 正丁醇 5 g 6.2 ml (0.068 mol);溴化钠(无水) 8.3 g (0.08 mol);浓硫酸(d =1.84) 10 ml (0.18 mol);10 % 碳酸钠溶液、 无水氯化钙。
【物理常数】【仪器安装要点】1.按教材p28图1.15-(3)安装仪器。
2.有害气体吸收装置的漏斗要靠近水面,但不能浸入水中,以免水倒吸。
纯化过程:【操作要点】1.加料:(1)溴化钠不要粘附在液面以上的烧瓶壁上。
(2)从冷凝管上口加入已充分稀释、冷却的硫酸时,每加一次都要充分振荡,混合均匀。
否则,因放出大量的热而使反应物氧化,颜色变深。
2.加热回流:开始加热不要过猛,否则回流时反应液的颜色很快变成橙色或橙红色。
应小火加热至沸,并始终保持微沸状态。
反应时间约30 min 左右,反应时间太短,反应液中残留的正丁醇较多(即反应不完全);但反应时间过长,也不会因时间增长而增加产率。
本实验在操作正常的情况下,反应液中油层呈淡黄色,冷凝管顶端亦无溴化氢逸出。
实验七--水中硝酸盐氮、硫酸盐及氨氮的测定

实验七水中硝酸盐氮、硫酸盐与氨氮的测定(一)水中硝酸盐氮的测定1.1 麝香草酚分光光度法1.1.1 范围本标准规定了用麝香草酚分光光度法测定生活饮用水与其水源水中的硝酸盐氮。
本法适用于生活饮用水与其水源水中硝酸盐氮的测定。
本法最低检测质量为0.5μg硝酸盐氮,若取1.00 mL水样测定,则最低检测质量浓度为0.5 mg/L。
亚硝酸盐对本标准呈正干扰,可用氨基磺酸铵除去;氯化物对本标准呈负干扰,可用硫酸银消除。
1.1.2原理硝酸盐和麝香草酚在浓硫酸溶液中形成硝基酚化合物,在碱性溶液中发生分子重排,生成黄色化合物,比色测定。
415nm1.1.3试剂1.1.3.1 氨水(ρ=0. 88 g/ mL)。
1.1.3.2 乙酸溶液(1+4)。
1.1.3.3 氨基磺酸铵溶液(20 g/L):称取2.0 g氨基磺酸铵(NH4S03NH2),用乙酸溶液(1+4)溶解,并稀释为100 mL。
1.1.3.4 麝香草酚乙醇溶液(5 g/L):称取0.5 g麝香草酚[(CH3)(C3H7)C6H3OH,Thymol,又名百里酚],溶于无水乙醇中,并稀释至100mL。
1.1.3.5 硫酸银硫酸溶液(10g/L):称取1.0g硫酸银(Ag2SO4),溶于100mL硫酸(ρ=1.84 g/mL)中。
1硝酸盐氮标准储备溶液[ρ(NO3--N)=1 mg/mL]:称取7.2180g经105℃~110℃干燥lh的硝酸钾(KNO3),溶于纯水中,并定容至1000mL。
加2mL三氯甲烷为保存剂。
1硝酸盐氮标准使用溶液[ρ(NO3--N)=10ug/mL]:吸取 5.00mL硝酸盐氮标准储备溶液(1.1.3.6)定容至500mL。
1.1.4仪器1.1.4.1 具塞比色管:50mL。
1分光光度计。
1.1.5分析步骤1.1.5.1 取1. 00mL 水样于干燥的50mL 比色管中。
1.1.5.2 另取50 mL 比色管6支,分别加入硝酸盐氮标准使用溶液(1.1.3.7)0mL ,0.05mL ,0.10mL ,0.30mL ,0.50mL ,0.70mL 和1.00mL ,用纯水稀释至1.00mL 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
河南工业大学实验报告
课程数据库技术基础实验名称实验7
院系中英国际学院专业班级软件1602
姓名姜棚学号201630910220
指导老师:程凤娟日期2017-11-21
1、目的与要求
(1)掌握存储过程的使用方法;
(2)掌握触发器的使用方法;
2、实验准备
(1)了解存储过程的使用方法;
(2)了解触发器的使用方法
(3)了解inserted逻辑表和deleted逻辑表的使用;
(4)了解如何编写CRL存储过程与触发器。
3、实验内容
1)存储过程
(1)创建存储过程,使用Employees表中的员工人数来初始化一个局部变量,并调用这个存储过程。
执行该存储过程,并查看结果;
(2)创建存储过程,比较两个员工的实际收入,若前者比后者高就输出0,否则输出1。
执行该存储过程,并查看结果:
(3)创建添加职员记录的存储过程EmployeeAdd。
执行该存储过程:
(4)创建一个带有OUTPUT游标参数的存储过程,在Employees表中声明并打开一个游标。
声明一个局部游标变量,执行上述存储过程,并将游标赋值给局部游标变量,然后通过该游标变量读取记录:
(5)创建存储过程,使用游标确定一个员工的实际收入是否排在前三名。
结果为1表示是,结果为0表示否。
执行该存储过程,并查看结果:
思考与练习:
●创建存储过程,要求当一个员工的工作年份大于6年时将其转到经理办公室
工作。
●创建存储过程,根据每个员工的学历将收入提高500元。
●创建存储过程,使用游标计算本科及以上学历的员工在总员工人数所占的比
例。
●使用命令方式修改存储过程的定义。
2)触发器
对于YGGL数据库,表Employees的DepartmentID列与表Departments的DepartmentID列应满足参照完整性规则,即:
●向Employees表添加记录时,该记录的“DepartmentID”字段值在
Departments表中应存在。
●修改Departments表的DepartmentID字段值时,该字段在Employees表中
的对应值也应修改。
删除Departments表中的记录时,该记录的DepartmentID字段值在Employees表中对应的记录也删除。
对于上述参照完整性规则,在此通过触发器实现。
在“查询分析器”中输入各触发器的代码并执行。
(1)向Employees表插入或修改一个记录时,通过触发器检查记录的DepartmentID值在Departments表中是否存在,如不存在,则取消插入或修改操作。
(2)修改Departments表“DepartmentID”字段值时,该字段在Employees 表中的对应值也做相应修改。
(3)删除Departments表中记录的同时删除该记录“DepartmentID”字段值在Employees表中对应的记录。
(4)创建INSTEAD OF触发器,当向Salary表中插入记录时,先检查EmployeeID 列上的值在Employees是否存在,如果存在则执行插入操作,如果不存在则提示“员工号不存在”。
(5)创建DDL触发器,当删除YGGL数据库的一个表时,提示“不能删除表”,并回滚删除表的操作。
思考与练习
●对与YGGL数据库,表Employees的Employees的EmployeeID列与表
Salary的EmployeeID列应满足参照完整性规则,请用触发器实现两个表间的参照完整性。
●当修改表Employees时,若将Employee表中员工的工作时间增加一
年,则将收入增加500,若增加2年则增加1000,依次增加。
若工作时间减少则无变化。
创建UPDATE触发器,当Salary表中Income值增加500时,OutCome 值则增加50。
●创建INSTEAD OF 触发器,实现向不可更新视图插入数据。
●创建DDL触发器,当删除数据库时,提示“无法删除”并回滚删除操
作。
