有机化学课后答案第十章醇和醚
有机化学 第十章 醇和醚2

H R C H O H
醇的化学反应主要发生在下列几个部位: 醇的化学反应主要发生在下列几个部位:
H+ δ C C H
O ..
δ..
H
δ+
α-H 氧化反应 弱酸性 弱碱性、 弱碱性、亲核性 亲核取代反应 β-H 消除反应
与活泼金属反应 10.4.1 与活泼金属反应
H2 O Na NaOH H2
作 碱性 试剂 或 亲核 试剂 作消 除反 应试剂
CH2OH CHOH + 3HONO2 CH2OH
CH2ONO2 CHONO2 + 3H2O CH2ONO2
甘油三硝酸酯
(硝化甘油) 硝化甘油)
硝酸酯是极不稳定的物质, 硝酸酯是极不稳定的物质,受热后会发生快速分解 甚至引起爆炸。多元醇的硝酸酯是烈性炸药。 甚至引起爆炸。多元醇的硝酸酯是烈性炸药。
决定于醇的结构和反应条件 1)醇的结构 醇脱水成烯的反应速率:3o醇 > 2o醇 > 1o醇 醇脱水成烯的反应速率:
α-C上支链越多,越有利于消除反应。 上支链越多,越有利于消除反应。
2)反应条件 2)反应条件
试剂碱性强,溶剂极性小,反应温度高, 试剂碱性强,溶剂极性小,反应温度高, 有利于消除反应。 有利于消除反应。
O ROH + HOPOH OH
-H2O
O ROPOH OH
磷酸二氢酯 ROH -H2O
O ROPOH OR
磷 酸一氢酯
O
3 ROH
POCl3
ROPOR OR
磷酸三酯
磷酸三酯常用作增塑剂、 磷酸三酯常用作增塑剂、萃取剂和杀虫剂 等。
10.4.4 脱水反应
脱水方式有两种:1.分子间脱水 2.分子内脱水 脱水方式有两种:1.分子间脱水 2.分子内脱水 脱水方式与醇的结构和反应条件有关。 脱水方式与醇的结构和反应条件有关。
有机化学 高鸿宾 第四版 答案 第十章_醚和环氧
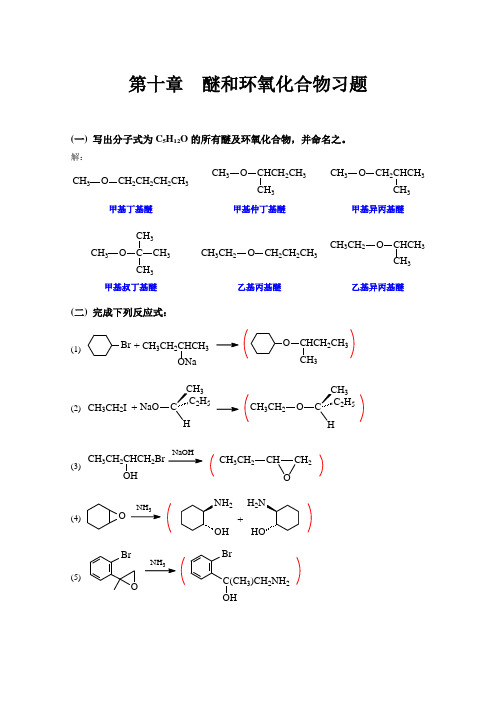
第十章醚和环氧化合物习题(一) 写出分子式为C5H12O的所有醚及环氧化合物,并命名之。
解:CH3O CH2CH2CH2CH3CH3O CHCH2CH33CH3O CH2CHCH3CH3甲基丁基醚甲基仲丁基醚甲基异丙基醚CH3O C CH3CH33CH3CH2O CH2CH2CH3CH3CH2O CHCH3CH3甲基叔丁基醚乙基丙基醚乙基异丙基醚(二) 完成下列反应式:(1) Br+ CH3CH2CHCH3O CHCH2CH33(2) CH3CH2I +CNaO2H53COH2H53CH3CH2(3) CH3CH2CHCH2BrOHCH2CHOCH3CH2(4)ONH2H2+(5)BrO3BrC(CH3)CH2NH2(6)CH 2CH OHCl 3CH 2OHCH Cl+CH 2CHO(三) 在3,5-二氧杂环己醇OOOH的稳定椅型构象中,羟基处在a 键的位置,试解释之。
解:羟基处于a 键时,有利于形成具有五元环状结构的分子内氢键:或O OOH(四) 完成下列转变:(1)C OCH 3OCH 2OCH 3解:C OCH 3OCH 2OCH 33NaOHNa + C H OHCH 2OH(2)BrOH O Ph及解:K Cr O 24OHOMgBr2+MgTHFOHBrC H CO HO(TM)(3)Br 及CH 2CHCH 3OHCH 3CHCH 3解:CH 3CHCH 3OHCH CH 2OCH 324CH 2=CHCH 3CF 3CO 3HCH 2CHCH 3MgBr2+MgTHFBr CH CH 2OCH 3(4)CH 2OH CH 3CH 2OHCH 2CH 2CH 2OCH 2CH 3及解:CH 3CH 2Br24o33CH 3CH 2OH CH =CH CH 2CH 2OCH 22+CH 2OH CH 2MgClMg dry etherO2CH 2CH 2CH 2OC 2H 5CH 2CH 2CH 2OH25(5)及CH 3CH 2OH解:24oCH 3CH 2OHCH 2=CH 2CH 2=CH 2+CF 3CO 3H(五) 推测下列化合物A~F 的结构,并注明化合物E 及F 的立体构型。
有机化学第二版-徐寿昌-课后答案

徐寿昌编《有机化学》第二版习题参考答案第二章烷烃1、用系统命名法命名下列化合物(1)2,3,3,4-四甲基戊烷(2)3-甲基-4-异丙基庚烷(3)3,3,-二甲基戊烷(4)2,6-二甲基-3,6-二乙基辛烷(5)2,5-二甲基庚烷(6)2-甲基-3-乙基己烷(7)2,2,4-三甲基戊烷(8)2-甲基-3-乙基庚烷2、试写出下列化合物的结构式(1) (CH3)3CC(CH2)2CH2CH3(2) (CH3)2CHCH(CH3)CH2CH2CH2CH3(3) (CH3)3CCH2CH(CH3)2(4) (CH3)2CHCH2C(CH3)(C2H5)CH2CH2CH3(5)(CH3)2CHCH(C2H5)CH2CH2CH3(6)CH3CH2CH(C2H5)2(7) (CH3)2CHCH(CH3)CH2CH3(8)CH3CH(CH3)CH2CH(C2H5)C(CH3)33、略4、下列各化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
均有错,正确命名如下:(1)3-甲基戊烷(2)2,4-二甲基己烷(3)3-甲基十一烷(4)4-异丙基辛烷(5)4,4-二甲基辛烷(6)2,2,4-三甲基己烷5、(3)>(2)>(5)>(1) >(4)6、略7、用纽曼投影式写出1,2-二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称。
交叉式最稳定重叠式最不稳定8、构象异构(1),(3)构造异构(4),(5)等同)2),(6)9、分子量为72的烷烃是戊烷及其异构体(1) C(CH3)4(2) CH3CH2CH2CH2CH3 (3) CH3CH(CH3)CH2CH3(4) 同(1)10、分子量为86的烷烃是己烷及其异构体(1)(CH3)2CHCH(CH3)CH3(2) CH3CH2CH2CH2CH2CH3 , (CH3)3CCH2CH3(3)CH3CH2CH(CH3)CH2CH3(4)CH3CH2CH2CH(CH3)214、(4)>(2)>(3)>(1)第三章烯烃1、略2、(1)CH 2=CH — (2)CH 3CH=CH — (3)CH 2=CHCH 2— CH 2CH CH 3MeH H i-PrEt Men-PrMe Me Et i-Prn-Pr (4)(5)(6)(7)3、(1)2-乙基-1-戊烯 (2) 反-3,4-二甲基-3-庚烯 (或(E)-3,4-二甲基-3-庚烯 (3) (E)-2,4-二甲基-3-氯-3-己烯 (4) (Z)-1-氟-2-氯-2-溴-1-碘乙烯(5) 反-5-甲基-2-庚烯 或 (E)-5-甲基-2-庚烯 (6) 反-3,4-二甲基-5-乙基-3-庚烯 (7) (E) -3-甲基-4-异丙基-3-庚烯 (8) 反-3,4-二甲基-3-辛烯 4、略 5、略 6、CH 3CH 2CHCH 2CH 3CH 3CH 2CCHCH 3CH 3OH BrCH 3CH 2CCHCH 3CH 3Cl ClCH 3CH 2C CHCH 3CH 3OH OHCH 3CH 2CH CHCH 3CH 3OHCH 3CH 2COCH 3CH 3CHOCH 3CH 2CH CHCH 3CH 3Br(1)(2)(3)(4)(5)(6)(7)7、活性中间体分别为:CH 3CH 2+ CH 3CH +CH 3 (CH 3)3C + 稳定性: CH 3CH 2+ > CH 3CH +CH 3 > (CH 3)3C + 反应速度: 异丁烯 > 丙烯 > 乙烯8、略9、(1)CH 3CH 2CH=CH 2 (2)CH 3CH 2C(CH 3)=CHCH 3 (有顺、反两种) (3)CH 3CH=CHCH 2CH=C(CH 3)2 (有、反两种)用KMnO 4氧化的产物: (1) CH 3CH 2COOH+CO 2+H 2O (2)CH 3CH 2COCH 3+CH 3COOH (3) CH 3COOH+HOOCCH 2COOH+CH 3COCH 310、(1)HBr ,无过氧化物 (2)HBr ,有过氧化物 (3)①H 2SO 4 ,②H 2O (4)B 2H 6/NaOH-H 2O 2 (5)① Cl 2,500℃ ② Cl 2,AlCl 3(6)① NH 3,O 2 ② 聚合,引发剂 (7)① Cl 2,500℃,② Cl 2,H 2O ③ NaOH 11、烯烃的结构式为:(CH 3)2C=CHCH 3 。
有机化学第10章 醇、酚、醚

①醇可依分子中所含羟基数目分为一元醇、二元醇及三元醇等,二
元及二元以上的醇称为多元醇。例如:
CH3CH2OH CH2CH2 OH OH
乙醇(一元醇) 乙二醇(二元醇)
CH2CH CH2 OH OH OH
丙三醇(三元醇)
3
②醇也可依分子中烃基的不同而分为脂肪醇(包括饱和醇及不饱和 醇)、脂环醇和芳香醇。 例如:
C(CH3)2或 C(CH3)3
23
在醇的核磁共振谱图中,羟基质子(O—H)由于受
分子间氢键的影响,其化学位移(δ)出现在1~5.5范围 内,在核磁共振谱中产生一个单峰。由于氧的电负性 较大,羟基所连碳原子上的质子的化学位移一般在 3.4~4.0。
24
10.1.4 醇的化学性质
羟基是醇的官能团,作为反应中心羟基决定了醇的化学性质。
2,3-二甲基-3-戊醇
12
不饱和醇的命名,除应选择同时连有羟基和不饱和键的最长碳 链作为主链外,其它原则与饱和醇相同。
CH3CH2CH2CHCH2CH2CH2OH CH CH2
5 6
4
3
2
1
4-丙基-5-己烯-1-醇
CH CHCH3 CH3CH2CHCHCH2CHCH3 CH3 OH
4-甲基-5-乙基-6-辛烯-2-醇
32
醇和氢卤酸反应的速率与醇的结构的关系: 醇的活性顺序是:烯丙型醇、苄基型醇>叔醇>仲醇>伯醇。 例如:
33
利用不同醇与盐酸反应速率的不同,可以区分伯、仲、叔醇。无
水氯化锌与浓盐酸配制的溶液,叫做Lucas试剂。因为水溶性较好的
醇与Lucas试剂反应后,生成与水不互溶的氯代烃,形成乳状的混浊 溶液或分层,所以可利用Lucas试剂鉴别低碳(C6以下)一元伯、仲、叔 醇(C6以上的一元醇水溶性较差,难于用Lucas试剂鉴别)。例如:
第10章醇、酚、醚练习与实践参考答案

[练习与实践]一、选择题1.乙醇在浓硫酸在170℃时脱水反应的产物是( B )A 、乙烷B 、乙烯C 、 丁醚D 、乙醚2.下列物质不能与溴水发生反应的是( A )A 、苯B 、乙烯C 乙炔D 、苯酚3.下列化合物属于叔醇的是( A ),能氧化并生成酮的是( C )。
A 、 B 、 C 、 D 、4.下列化合物互为同分异构体的是( D )A 、乙醚和丁醇B 、邻甲酚和苯甲醇C 、戊烯和环戊烷D 、以上都是5.下列化合物一般不容易被氧化的是( D )A 、丁醇B 、2,2-二甲基丁醇C 、3,3-二甲基-2-丁醇D 、2 -甲基-2-丁醇二、写出下列化合物的名称或结构式2,3-二甲基-2-丁醇 2,4-己二醇CH 3CH 2C CH 3OHCH 3CH 3CH CH CH 3OH 3CH 3CH CH 2CH 3OH CH 3C CH 2OH CH 3CH 3CH C OH3CH 33CH 3(1)CH 3O H (3)CH 2CH CH 3(4)CH CH 3CH 2CH 2CH CH 3(2)间甲基苯酚(3-甲基苯酚) 1-苯基-2-丙醇间苯二酚(1,2-苯二酚) 苯甲醚(7) 2,3-二甲基-2-戊醇 (8)甘油(9)苯甲醇 (10)亚硝酸异戊酯三、完成下列化学反应 1)(2)(3)CH 3CH OH CH 32H 24o CH 3C H CH 2CH 3OH[O]OH +Br 2四、用化学方法鉴别下列各组化合物(1)苯甲醇、苯酚和苯乙烯(2)乙醇、甘油五、推导结构式某有机化合物的分子式为C 5H 12O ,能发生下列反应:(1)与金属钠作用放出氢气(2)被酸性高锰酸钾溶液氧化生成酮(3)与浓硫酸共热只生成1种烯烃,若将生成的烯烃催化氢化得2-甲基丙烷。
写出该化合物的结构式和名称,并写出有关的反应方程式。
OH OH (5)OCH 3(6)CH 3CH CH 3OH [O](2)CH 3CH 2OH 2(1)浓硫酸 140℃。
大学有机化学第十章醇酚醚

② 与金属离子的络合
MgCl2•6ROH CaCl2•4ROH
结晶醇 (溶于水\不溶于有机溶剂)
因此:
不能用无水CaCl2干燥ROH
2. 醇与活泼金属的反应 ——弱酸性
+ CH3CH2OH Na
+ CH3CH2ONa H2
+ (CH3)3COH K
+ (CH3)3COK H2
醇金属: 强碱性试剂和强亲核性试剂
OH
R'
OH
R
30 叔醇( R' C OH ): (CH3)3COH R''
② 按羟基所连的烃基分:
饱和醇:
OH
CH3CH2OH (CH3)3COH
不饱和醇:
OH
CH2=CHCH2OH CH3C≡ CCH2OH
芳香醇:
CH OH 2
CH OH 2
③ 按羟基的数目分类:
一元醇: CH3CH2CH2OH
② RX的制备:10 醇,可采用 HX作卤化剂;
不是10 醇,不采用 HX作卤化剂,否则易得到重排产物。 可采用SOCl2 , PX3 , PX5作卤化剂
i) 与SOCl2反应
ROH SOCl2 RC+l SO2 + HCl
优点:1) 不重排,且产物构型保持
2) 副产物均为气体,易于除去 3) 产率高,产物容易分离
i. 伯醇氧化成醛和羧酸
[O]
[O]
RCH2OH
RCHO
RCOOH
[O]:KMnO4/H+、HNO3、 CrO3/ H2SO4、 K2Cr2O7/H2SO4、Na2Cr2O7/H2SO4 等
e.g.
CrO3 / H2SO4
有机化学(第五版)第十章 醇、酚、醚

2) 根据分子中烃基的类别分为:脂肪醇、脂环醇、 和芳香醇(芳环侧链有羟基的化合物,羟基直接连在 芳环上的不是醇而是酚)。
3) 根据分子中所含羟基的数目分为:一元醇、二元 醇和多元醇。 两个羟基连在同一碳上的化合物不稳定,这种结 构会自发失水,故同碳二醇不存在。另外,烯醇是不 稳定的,容易互变成为比较稳定的醛和酮。 井冈山大学化学化工学院
井冈山大学化学化工学院
关于频哪醇重排需要注意的问题
3.某些环状结构的频哪醇,重排后可得环扩大产物
井冈山大学化学化工学院
五、Preparation of Alcohols
1.由烯烃制备 1) 烯烃的水合 2) 硼氢化-氧化反应
硼氢化反应操作简单,产率高,是制备伯醇的好办法。
井冈山大学化学化工学院
3)羟汞化-脱汞反应
井冈山大学化学化工学院
乙醇液膜
乙醇(CCl4)
四、Chemical Properties of Alcohols
醇的化学性质主要由羟基官能团所决定,同时也受到烃 基的一定影响,从化学键来看,反应的部位有 C—OH、 O—H、和C—H。
分子中的C—O键和O—H键都是极性键,因而醇分子中有 两个反应中心。 又由于受C—O键极性的影响,使得α—H具 有一定的活性,所以醇的反应都发生在这三个部位上。 井冈山大学化学化工学院
(2)双分子消除反应(E2)
一步反应:
E2反应的特点: 1)一步反应,与SN2的不同在于B:进攻β-H。 E2与SN2是互相竟争的反应。 2)反应要在浓的强碱条件下进行。 3)通过过渡态形成产物,无重排产物。 井冈山大学化学化工学院
2. 消除反应的取向
A. Saytzeff规则:优先生成具有较多烷基取代的(也是较稳定的)烯烃。
第十章醇和醚(一)醇醇是脂肪烃分子中的氢原子被羟基(—OH)

CH3CH2OHOH CH2CH2OH 第十章醇和醚一醇醇是脂肪烃分子中的氢原子被羟基—OH取代的衍生物也可看作是水中的氢原子被脂肪烃基取代的产物。
10.1 醇的分类和命名1醇的分类根据羟基所连烃基的结构可把醇分为脂肪醇、脂环醇、芳香醇羟基连在芳烃侧链上的醇等。
例如脂肪醇脂环醇芳香醇根据羟基所连烃基的饱和程度可把醇分为饱和醇和不饱和醇。
例如CH3CH2CH2OH CH2CH—CH2OH 饱和醇不饱和醇根据分子中羟基的数目可把醇分为一元醇、二元醇和多元醇。
饱和一元醇的通式为CnH2n2O。
在二元醇中两个羟基连在相邻碳原子上的称为邻二醇两个羟基连在同一碳原子上的称为胞二醇不稳定。
例如一元醇二元醇二元醇邻二醇根据羟基所连碳原子的类型可把醇分为伯醇一级醇、仲醇二级醇和叔醇三级醇。
例如伯醇一级醇仲醇二级醇叔醇三级醇2醇的命名结构简单的醇可用普通命名法命名即在“醇”字前加上烃基的名称“基”字一般可以省去。
例如异丁醇仲丁醇烯丙醇苄醇结构复杂的醇则采用系统命名法命名。
首先选择连有羟基的最长碳链为主链从距CH3CHCH3OHCH2CH2OHOHCH2CH2CH2OHOHCH3CHCH2OHCH2CHCH2OHC H3CH3CH2CHCH3OHRCH2OHRCH2CHROHRCROHR123。
CH2OHCH3CH2OHCHCH2CHCH2CHCH2CH2OHOHOHCH3CCH3CH2CCH3CHCH3 OH羟基最近的一端给主链编号按主链所含碳原子的数目称为“某醇”取代基的位次、数目、名称以及羟基的位次分别注于母体名称前。
例如CH3CH3CH3CCH2OHCH3CH3CC2H5OHCH3CHCHCH3 3—甲基—2—戊醇244—三甲基—2—戊醇命名不饱和醇时主链应包含羟基和不饱和键从距羟基最近的一端给主链编号按主链所含碳原子的数目称为“某烯醇”或“某炔醇” 羟基的位次注于“醇”字前。
例如2—甲基—3—丁烯—1—醇Z—34—二甲基—3—己烯—2—醇命名芳香醇时将芳环看作取代基。
李景宁《有机化学》第5版课后习题(醇酚醚)【圣才出品】
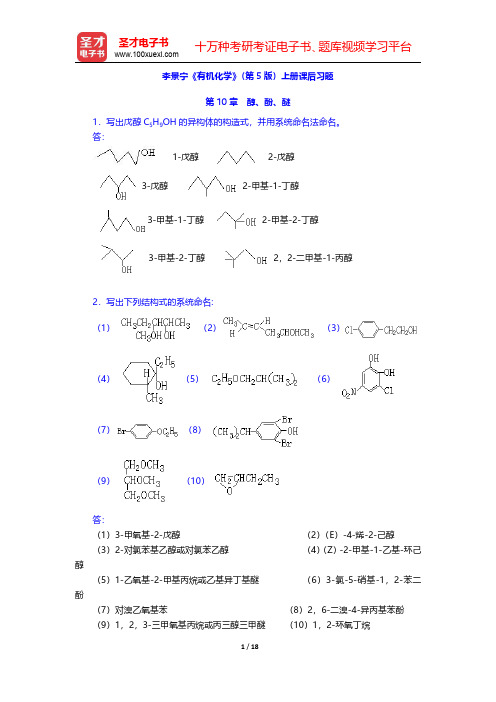
李景宁《有机化学》(第5版)上册课后习题第10章醇、酚、醚1.写出戊醇C5H9OH的异构体的构造式,并用系统命名法命名。
答:1-戊醇2-戊醇3-戊醇2-甲基-1-丁醇3-甲基-1-丁醇2-甲基-2-丁醇3-甲基-2-丁醇2,2-二甲基-1-丙醇2.写出下列结构式的系统命名:(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)答:(1)3-甲氧基-2-戊醇(2)(E)-4-烯-2-己醇(3)2-对氯苯基乙醇或对氯苯乙醇(4)(Z)-2-甲基-1-乙基-环己醇(5)1-乙氧基-2-甲基丙烷或乙基异丁基醚(6)3-氯-5-硝基-1,2-苯二酚(7)对溴乙氧基苯(8)2,6-二溴-4-异丙基苯酚(9)1,2,3-三甲氧基丙烷或丙三醇三甲醚(10)1,2-环氧丁烷3.写出下列化合物的构造式:(1)(E)-2-丁烯十醇(2)烯丙基正丁醚(3)对硝基苄基苯甲醚(4)邻甲基苯甲醚(5)2,3-二甲氧基丁烷(6)α,β-二苯基乙醇(7)新戊醇(8)苦味酸(9)2,3-坏氧戊烷(10)15-冠-5答:4.写出下列化合物的构造式。
(1)2,4-dimethyl-1-hexanol(2)4-penten-2-ol(3)3-bromo-4-methylphenol(4)5-nitro-2-naphthol(5)tert-butyl phenyl ether(6)1,2-dimethoxyethanel答:(1)(2)(3)(4)(5)(6)5.写出异丙醇与下列试剂作用的反应式:(1)Na(2)Al(3)冷浓H2SO4(4)H2SO4>1600C(5)H2SO4〈1400C(6)NaBr+H2SO4(7)红磷+碘(8)SOCl2(9)CH3C6H4SO2Cl(10)(1)的产物+C2H5Br(11)(1)的产物+叔丁基氯(12)(5)的产物+HI(过量)答:(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)(11)(1)的产物+叔丁基氯(12)(5)的产物+HI(过量)6.在叔丁醇中加入金属钠,当Na被消耗后,在反应混合物中加入溴乙烷,这时可得到C6H14O;如在乙醇与Na反应的混合物中加入2-溴-二甲基丙烷,则有气体产生,在留下的混合物中仅有乙醇一种有机物,试写出所有的反应,并解释这两个实验为什么不同?答:第一个实验是亲核反应,第二个实验以消除反应为主,生成烯烃气体放出,过量的乙醇没参加反应而留下。
常州大学江苏工业学院有机化学复习考试题及答案第十章醇和醚幻灯片

CH3CH2OH
(100 %)
例2:
CH3
CH3
CH3—C—COOH
+ LiAlH4
(1) 乙醚 (2) H2O
CH3—C—CH2OH
CH3
CH3
新戊醇(92%)
• 酯要更高温、高压才能催化加 还原,O 一般不能用NaBH4还原:
氢。
可用
LiAlH4
R—C—OC2H5
Na C2H5OH
RCH2OH + C2H5OH
正丙醇
例3:
异丁醇
(BH3)2
CH 3
H2O2 HO-
OH H 8 5 % 顺式
H CH3
10.2.3 从醛、酮、羧酸及其酯还原
(1)催化加氢(催化剂为镍、铂或钯)
(2)用还原剂(LiAlH4或NaBH4)还原生成醇。
O • 醛 R—C—H
[H] 还原剂
R—CH2OH
• 伯醇
O • 酮 R—C—R’
• 官能团位置异构:
CH3CH2CH2OH
正丙醇
CH3—CH—CH3
OH
异丙醇
命名:
(1) 习惯命名法: 烃基的习惯名称后加一“醇”字来命 名.
(2) 衍生物命名法: 其它醇看作是甲醇的烷基衍生物来
命名. (3) 系统命名法:
1、选择主链; 2、编号(靠近羟基的一端开始) 3、按照主链中所含碳原子数目而称为某醇;支链的位次、 名称及羟基的位次写在名称的前面。
1,2-丙二醇 ( -二醇)
1,3-丙二醇 ( -二醇)
例2:
1,2,3-丙三醇 简称:丙三醇 ( 俗称: 甘油 )
2,2-双(羟甲基)-1,3-丙二醇 (俗名: 季戊四醇)
有机化学Chapter10(醇和醚)

碱性 碱性:ROH + H
ROH 2 钅 离子 羊
低级醇能与氯化钙形成络合物—结晶醇(CaCl2·4C2H5OH) 不能用氯化钙干燥醇 可用氯化钙去除少量杂质醇
2、与无机酸的作用
醇与酸失水生成酯。
O C2H5OH + CH3COH
H
O CH3COC 2H5 + H2O
HIO4 HIO4
RCHO + R'CHO + HIO 3 RCHO + R'CO2H + HIO 3 RCHO + R'CHO + HCO2H + HIO 3
RCH CH CHR' HIO4 OH OH OH
可用于多羟基化合物结构分析; 反应是定量地进行的,可用来定量测定1,2-二醇的含量。
(四) 重要代表物
1、甲醇 (CH3OH) 又名木醇,木酒精
毒性:工业酒精中大约含有 4%的甲醇,被人饮用后, 就会产生甲醇中毒。甲醇 的致命剂量大约是70毫升。
甲醇的中毒机理是,甲醇经人 体代谢产生甲醛和甲酸(俗称 蚁酸),然后对人体产生伤害。
甲醇是一种无色、透明、易燃、 易挥发的有毒液体,略有酒精 气味。相对密度0.792(20/4℃), 沸点64.5℃
第十章
一、醇
(一)命名
醇 和 醚
(二)物理性质 (三)化学性质
1、似水性 2、与无机酸的作用 3、脱水反应 4、氧化或脱氢 5、邻二醇与高碘酸的作用
(四)重要代表物
二、醚
(一)命名 (二)物理性质 (三)化学性质
1、醚键的断裂 3、形成过氧化物 羊 2、形成钅 盐与络合物
(四)环醚
有机化学课后习题答案10第十章 醇和醚 答案

C (CH3)2 ;
(C) (CH3)2 C C (CH3)2 HO OH
2. A: (CH3)2CHCH2OH ; B: (CH3)2CHCHO; C: (CH3)2C=CH2 ; D:(CH3)2C(OH)-CH2OH E:HCHO ; F: CH3COCH3 3.
(A) ; (B) OH Br
二.写出下列化合物的结构式 1.
CH3 H3CC CCCH2OH CH3
2.
H3C CH3 C C H CHCH2Cl OH
Br H H OH
3.
HO H3C
Cl
4.
5. 7.
H2C CHCH2OCH2C6H5
O CH2CHCCCH3 CH3 CH3
6. 8.
CH3CH2OCH2CH2OH
H3COH2C H
CH3
18.
CH(CH3)2
19.
CHO CHO
20.
Br
21.
CHCH2OH OCH3
22.
OO
104
23.
CH3CH2CHCH2CH3 + OH
CH3Br
24. 25. 26.
CHO
O
OCH2CH3 H3CH2CHC CH2 OH 四.选择题
1. A 2. D 3. B 4. B 5. C 6. A 7. D 8. A 9. B 10.C 11.C 12.C 13.B 14.D 15.A 16.C 17.D 五.鉴别与分离 1.用简单的化学方法区别下列各组化合物: (1)
Br2 hv
Br2 hv
Br2 hv
(CH3) 3CBr
(CH3)3 CBr KOH / C2H5OH CH3 CH2 CCH3
邢其毅《基础有机化学》(第3版)(上册)课后习题-醇和醚(圣才出品)

第10章醇和醚习题10-1低级醇的熔点和沸点比碳原子数相同的烷烃的熔点和沸点高得多,请加以解释。
解:因为醇分子间有氢键的缔合作用。
习题10-2(i)比较正丙醇、正丁醇和正戊醇的沸点高低,并对实验数据加以解释。
(ii)比较正戊醇、异戊醇、环戊醇和新戊醇的沸点高低。
并对实验数据加以解释。
(iii)比较正戊烷、正丙基氯、正丁醇和1,3-丙二醇的沸点高低,并对实验数据加以解释。
(iv)结合(i)(ii)(iii)归纳影响沸点的因素有哪些?解:(i)沸点:正戊醇(138.0℃)>正丁醇(117.8℃)>正丙醇(97.2℃)解释:对于支链一元醇,分子质量越大,范德华引力越大,沸点越高。
(ii)沸点:环戊醇(140℃)>正戊醇(138.0℃)>异戊醇(131.5℃)>新戊醇(113.4℃)解释:环戊醇分子间排列紧密,分子间作用力比碳原子数相同链状醇的作用力大,故沸点高;含支链的醇的沸点比碳原子数相同的支链醇的沸点低。
(iii)沸点:1,3-丙二醇(215℃)>正丁醇(117.8°C)>正丙基氯(47℃)>正戊烷(38℃)解释:正丙基氯极性比正戊烷大,相对分子质量也比正戊烷大,故沸点比正戊烷高;正丁醇分子间有氢键,沸点高于分子间无氢键的正丙基氯;1,3-丙二醇分子有两个羟基,分子间氢键比正丁醇还多,故沸点也比正丁醇高。
(iv)影响沸点的因素主要有氢键,偶极—偶极间的相互作用,以及范德华引力。
其中,氢键的影响最大,范德华引力和分子质量有关,相对分子质量越大,范德华引力也就越大;分子间有氢键的物质的沸点高于分子间无氢键的物质的沸点;对于结构相似的物质,相对分子质量越大,沸点也越高。
习题10-3请分别用伞形式、锯架式、纽曼式画出(S,S)-2,3-丁二醇的各稳定构象式.判断其中哪个构象为优势构象(以C(2)-C(3)键为旋转轴),并阐明确定优势构象的理由。
解:(ii)为优势构象,因为其两个甲基处于对位,两个羟基处于邻交叉位,又可形成分子内氢键,故分子的能量最低,最稳定。
有机化学C第10章 醇酚醚问题参考答案
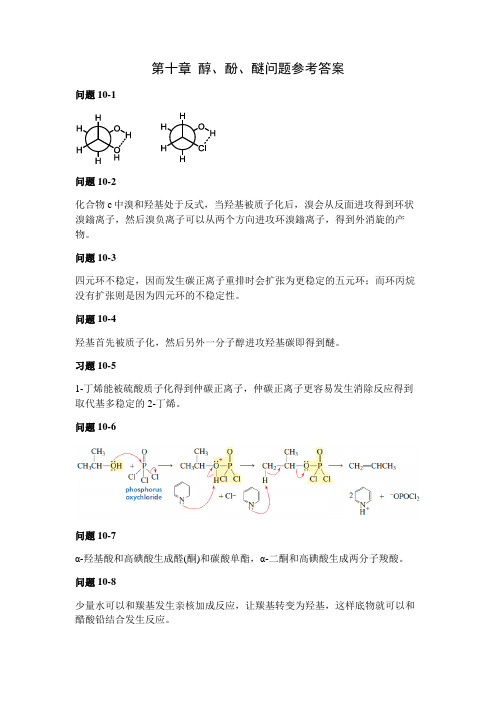
第十章醇、酚、醚问题参考答案问题10-1问题 10-2化合物c中溴和羟基处于反式,当羟基被质子化后,溴会从反面进攻得到环状溴鎓离子,然后溴负离子可以从两个方向进攻环溴鎓离子,得到外消旋的产物。
问题10-3四元环不稳定,因而发生碳正离子重排时会扩张为更稳定的五元环;而环丙烷没有扩张则是因为四元环的不稳定性。
问题10-4羟基首先被质子化,然后另外一分子醇进攻羟基碳即得到醚。
习题10-51-丁烯能被硫酸质子化得到仲碳正离子,仲碳正离子更容易发生消除反应得到取代基多稳定的2-丁烯。
问题10-6问题10-7α-羟基酸和高碘酸生成醛(酮)和碳酸单酯,α-二酮和高碘酸生成两分子羧酸。
问题10-8少量水可以和羰基发生亲核加成反应,让羰基转变为羟基,这样底物就可以和醋酸铅结合发生反应。
问题10-9乙醇中氧的电负性强,分子间形成氢键的作用比较强;而硫的电负性比氧弱,因而分子间氢键没有乙醇强,所以沸点比乙醇低。
问题10-10问题10-11二价镁具有Lewis酸性,能和羰基氧络合,然后碳负离子进攻羰基碳。
问题10-12邻硝基苯酚酸性最强,间硝基苯酚酸性最弱。
邻对位硝基苯酚由于共轭效应具有比间硝基苯酚强的酸性;而且邻硝基苯酚的诱导效应比对硝基苯酚强,同时还可以形成分子内氢键。
问题10-13邻位产物会形成分子内氢键,具有较低的沸点,因而可以将邻位产物的对位产物分开。
问题10-14硝基越多芳环的亲电性越强,反应条件越温和。
问题10-15苯酚与NaOH反应生成盐后具有更强的亲核性,可以与醛发生亲核加成反应。
问题10-16四氢呋喃为环状结构,氧更加裸露,因而更容易与水形成氢键相互作用,因而可以与水互溶。
问题10-17因为在该反应中没有进攻手性中心,所以手性构型不发生变化。
问题10-18问题10-19伯醇为S N2反应,羟基先被质子化,然后另外一分子醇进攻羰基碳得到醚。
仲醇可能会发生S N2反应和S N1反应。
问题10-20。
有机化学第十章醇醚习题解答

解答: 本题由快到慢:
(2)>(3)>(1)
卢卡斯试剂—将浓盐酸与无水ZnCl2所配制的溶液。 与醇反应生成水和氯烷,氯烷不溶于水而呈浑浊或分 层。根据观察现象出现的快慢判断醇的类型。
4. 区别下列各组化合物 解答:方法1
方法2 * 三种样品中分别加入卢卡斯试剂,出现浑浊(或分 层 ) 快 的 为 CH2=CHCH2OH , 加 热 下 出 现 浑 浊 的 为 CH3CH2CH2OH,无此现象的为CH3CH2CH2Cl。
解答: * 三种样品中分别加入卢卡斯试剂,立即出现浑浊 (或分层)的为叔丁醇,几分钟后出现浑浊的为仲丁 醇,加热后才反应出现浑浊的为正丁醇。
解答: 2种样品中分别加入卢卡斯试剂,立即出现浑浊
(或分层)的为-苯乙醇,慢的为-苯乙醇。P215
5. 顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反 应后,生成何种产物? 解答:
(P225例题)
解答:
注意:用HCl(重排),另外,对应的卤代烃水解制 该醇不行,易消除生成烯烃。
解ቤተ መጻሕፍቲ ባይዱ:
13. 用指定原料合成下列化合物(其他试剂任用)。 解答:
干 醚
•也可用傅克酰基化反应,再还原。
16:
解答:
反应式:略
21. 完成下列各组化合物的反应式: 解答:
比较3、4。4以 消除为主P236
(2)扩环后生成的2级 碳正离子比扩环前的伯 碳正离子稳定。
10. 用适当的格利雅试剂和有关醛酮合成下列醇(各 写出2种不同组合) 解答:
注意反应条 件(干醚)
解答:
注意反应条 件(干醚)
11. 合成题 解答:
《有机化学》徐寿昌 第二版 第10章 醇和醚

顺-1,2-环戊二醇 环戊二醇
10.2 醇的制法
10.2.1 烯烃水合 (1)烯烃直接水合: )烯烃直接水合: 用于一些简单的醇制备,符合马氏规律。 用于一些简单的醇制备,符合马氏规律。
H3PO4-硅藻土 硅藻土 CH2=CH2 + HOH CH3CH2-OH 280~300℃,8MPa ℃
CH3-CH=CH2 + HOH
Na/C2H5OH
R—CH2OH OH R—CH—R’ R—CH2OH
伯醇
仲醇
O 羧酸 R—C—OH O 羧酸酯R—C—OR’
伯醇
R—CH2OH + R’OH 伯醇
例如: 例如:
(CH3)3CCOOH O R—C—OC2H5
1. LiAlH4 2.乙醚,H2O 乙醚, 乙醚
(CH3)3CCH2OH
烯丙基氯(易从丙烯高温氯化得到) 烯丙基氯(易从丙烯高温氯化得到)
烯丙醇
苄氯(甲苯高温氯化) 苄氯(甲苯高温氯化)
苄醇
10.3 醇的物理性质
◆低级醇为无色透明液体;C12以上的直链醇为固体 低级醇为无色透明液体; 以上的直链醇为固体. 沸点:直链饱和一元醇的沸点比相应烷烃的沸点高. ◆沸点:直链饱和一元醇的沸点比相应烷烃的沸点高
10.2.3 从醛、酮、羧酸及其酯还原*** 从醛、 催化加氢( ◆催化加氢(Ni/H2;Pd/H2;Pt/H2) 用还原剂还原( ◆用还原剂还原(NaBH4、LiAlH4、Na/C2H5OH) ) 、 O 醛 R—C—H O 酮 R—C—R’
[H] NaBH4 [H] NaBH4 [H] LiAlH4 [H]
① 按-OH数 数 目分类: 目分类:
二元醇: 二元醇:
CH2—CH2 OH OH CH2—CH—CH2 OH OH OH
基础有机化学王兴明主编十章醇酚醚答案

第十章醇酚醚习题答案习题1请参照教材中醇的命名部分习题2有两个红外吸收的应为顺式异构体,除了羟基的伸缩振动,另一个吸收是形成分子内氢键后的吸收。
只有一个吸收的应为反式异构体,它只有羟基的伸缩振动。
分子内的氢键不会随浓度变化。
习题 3(a) 正己醇 > 正戊醇 > 2-戊醇 > 2,2-二甲基丙醇 > 正戊烷(b) 乙酸 >乙醇 > 乙醚习题 4习题 5习题 6三溴化磷先和醇发生S N2反应,得到构型翻转的溴化物;然后甲氧基负离子再次与溴化物发生S N2反应,构型再次翻转,最终得到构型不变的产物。
对甲苯磺酰氯先和醇反应得到对甲苯磺酸酯,构型不变;然后然后甲氧基负离子与中间体发生S N2反应,得到构型翻转的产物。
习题 7习题 8习题 9硅胶上吸附的氧化剂重铬酸盐,遇到司机酒精含量过高,将被还原为绿色的三价铬。
习题 10习题 11d右边用乙醇-乙酸-腈乙酸的方式构建,酰化后保护,碱水解CN部分,LiAlH4还原,PPh3处理,连上苯甲醛,水解右边,格式试剂习题12顺式1,2-二醇更容易和高碘酸形成环状中间体。
习题 13习题 14b最快, a为顺式,反应没有反式快;b中正好羟基和溴处于直立键,反应比c 快。
习题 15习题16请参照教材中环氧丙烷的化学性质,注意酸性条件下和碱性条件下反应的区域选择性。
习题17底物a被质子化后会开环得到b’和c’,其中b’能形成烯丙基碳正离子,没有破坏另外一个环的芳香性,而c’则需要破坏苯环的芳香性来稳定碳正离子;因而b’比c’具有更高的稳定性,从而导致b是主要产物。
习题 18习题 19请参照教材中醇的化学性质习题20习题 21习题22加水溶解环己醇,然后用NaHCO3与苯甲酸反应,接着用Na2CO3与苯酚反应,最后用分液漏斗分离环己烷。
习题 23弗里斯重排是一个分子间反应,既可以与含有13C的化合物也可以同没有标记的化合物反应。
习题 24习题25请参照教材中苯酚的化学性质部分习题26习题 27二氧六环中的氧含有孤电子,也可以进攻底物形成磺酸根离去的中间体,水进攻该中间体会得到构型保持的产物;而水直接进攻底物得到构型翻转的产物;因而二氧六环的引入会降低产物的光学纯度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十章 醇和醚
一. 将下列化合物按伯仲叔醇分类,并用系统命名法命名。
仲醇,异丙醇 仲醇,1-苯基乙醇 仲醇,2-壬烯-5-醇
二. 预测下列化合物与卢卡斯试剂反应速度的顺序。
1.正丙醇 2.2-甲基-2-戊醇 3.二乙基甲醇 解:与卢卡斯试剂反应速度顺序如下:
2-甲基-2-戊醇>二乙基甲醇>正丙醇 三. 比较下列化合物在水中的溶解度,并说明理由。
四. 区别下列化合物。
仲醇,2-戊醇
叔醇,叔丁醇
叔醇,3,5-二甲基-3-己醇
仲醇,4-甲基-2-己醇 伯醇1-丁醇 伯醇 1,3-丙二醇
3.α-苯乙醇β-苯乙醇
解:与卢卡斯试剂反应,α-苯乙醇立即变浑,β-苯乙醇加热才变浑。
五、顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反应
后,生成何种产物?
解:
六、写出下列化合物的脱水产物。
七、比较下列各组醇和溴化氢反应的相对速度。
1.苄醇,对甲基苄醇,对硝基苄醇
解:反应速度顺序:
八、1、 3-丁烯-2-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:
2、 2-丁烯-1-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:
九、反应历程解释下列反应事实。
解:反应历程如下:
十、用适当的格利雅试剂和有关醛酮合成下列醇(各写出两种不同的组合)。
1.2-戊醇
4.2-苯基-2-丙醇
十一、合成题
1.甲醇,2-丁醇合成2-甲基丁醇
解:
2.正丙醇,异丙醇
2- 甲基-2-戊醇
2.2-甲基-2-丁醇
3.1-苯基-1-丙醇
3.甲醇,乙醇正丙醇,异丙醇
解:
4.2-甲基-丙醇,异丙醇 2,4-二甲基-2-戊烯解:
5.丙烯甘油三硝酸甘油酯
6.苯,乙烯,丙烯
3-甲基-
1-苯基-2-丁烯十二、完成下面转变。
1.乙基异丙基甲醇 2-甲基-2-氯戊烷
解:。
解:
2.3-甲基-2-丁醇 叔戊醇
解:
3.异戊醇 2-甲基-2-丁烯
解:
解: (2)
十四、某醇C5H12O氧化后生成酮,脱水则生成一种不饱和烃,将此烃氧化可生成酮和羧酸两种产物的混合物,推测该化合物的结构。
十五、从某醇依次和溴化氢,氢氧化钾醇溶液,硫酸和水,K2Cr2o7+H2SO4作用,可得到2-丁酮,试推测原化合物的可能结构,并写出各步反应式。
解:化合物结构式为:CH3CH2CH2CH2OH
十六、有一化合物(A)的分子式为C5H11Br,和氢氧化钠水溶液共热后生成C5H12OB),(B)具有旋光性,能与钠作用放出氢气,和硫酸共热生成C5H10(C),(C)经臭氧化和还原剂存在下水解则生成丙酮和乙醛,是推测(A),(B),(C)的结构,并写出各步反应式。
解:
4.五个碳以下的有机物
解:
十七、新戊醇在浓硫酸存在下加热可得到不饱和烃,将这个不饱和烃臭氧化后,在锌纷存在下水解就可以得一个醛和酮,试写出这个反应历程及各步反应产物的结构式。
十八、由化合物(A)C 6H 13Br 所制得格利雅试剂与丙酮作用可生成2,4-二甲基-3-乙基-2-戊醇。
(A )可发生消除反应生成两种异构体(B ),(C),将(B )臭氧化后再在还原剂存在下水解,则得到相同碳原子数的醛(D )酮(E),试写出各步反应式以及(A )-(E)的结构式。
解:各步反应式结(A )-(B)的结构式如下:
十九、写出下列醚的同分异构体,并按习惯命名法和系统命名法命名。
甲基正丙基醚,1-甲氧基丙烷
甲基异丙基醚,2-甲氧基丙烷
乙醚,乙氧基乙烷
甲基正丁基醚,1-甲氧基丁烷
甲基仲丁基醚,2-甲氧基丁烷
甲基异丁基醚,2-甲基-1-甲氧基丙烷
甲基叔丁基醚,2-甲基-2-甲氧基丙烷
乙基正丙基醚,1-乙氧基丙烷
乙基异丙基醚,2-乙氧基丙烷
二十、分离下列各组化合物。
1.1,乙醚中混有少量乙醇:解:加入金属钠,然后蒸出乙醚。
2,戊烷 1-戊炔 1-甲氧基-3-戊醇
炔与硝酸银反应生成炔银分出,加硝酸生成炔。
液相用浓硫酸处理,戊烷不溶于浓硫酸分出,醇溶于硫酸,用水稀释分出醇(醚)。
二十一、完成下列各组化合物的反应式。
1.乙烯,甲醇乙二醇二甲醚,三甘醇二甲醚2.乙烯二乙醇胺
3.甲烷二甲醚
4.丙烯异丙醚
5.苯,甲醇 2,4-硝基苯甲醚
6.乙烯正丁醚
二十三、乙二醇及其甲醚的沸点随相对分子量的增加而降低,试解释之。
沸点1970C 沸点1250C 沸点840C
解:乙二醇分子内有两个羟基,通过分子间氢键缔合成大分子,而单甲醚只有一个羟基,氢键作用减少。
对于二甲醚,分子中已没有羟基,不能形成分子间氢键。
所以乙二醇沸点最高,乙二醇二甲醚沸点最低。
二十四、下列各醚和过量的浓氢碘酸加热,可生成何种产物?
C6H14O,常温下不与钠作用,和过量的浓氢碘酸共热生成碘烷,此碘烷与氢氧化银作用则生成丙醇,试推测此化合物的结构,并写出反应式。
二十六、有一化合物分子式为C7H16O,并知道:
1.1,在常温下不和金属钠作用
2.2,过量浓氢碘酸共热生成两种物质为C2H5I和C5H11I,后者用
AgOH处理后所生成的化合物沸点为1380C。
试根据表10-2,推测其结构,并写出各步反应式。
解:沸点为1380C的物质为正戊醇。
此化合物为乙基正戊基醚。
二十七、有一化合物分子式为C20H21O4N,,与热的浓氢碘酸作用可生成碘代甲烷,表明有甲氧基存在。
当此化合物4 .24mg用HI处理,并将所生成的碘代甲烷通入硝酸银的醇溶液,得到11.62mgAgI,问此化合物含有几个甲氧基?
解: 碘化银分子量为234.8,11,62mgAgI为0.05mmole,
根据分子式指导此化合物分子量为339,4.24mg 为0.0125mmole,可见此化合物有四个甲氧基。
二十八、写出环氧乙烷与下列试剂反应的方程式:
1.有少量硫酸存在下的甲醇
2.有少量甲醇钠存在下的甲醇。
注意,这里有重排
问题解:
环氧乙烷在酸催化及碱催化产物是相同的,但是,1,2-环氧丙烷产物是不同的。
酸催化:
碱催化:。
