几种茶叶中咖啡因含量的测定
几种茶叶中咖啡因含量的测定

几种茶叶中咖啡因含量的测定茶叶作为一种广受喜爱的饮品,其种类繁多,包括绿茶、红茶、乌龙茶、黑茶等。
而咖啡因作为茶叶中的一种重要成分,其含量的多少不仅影响着茶叶的口感和风味,还与人体对茶叶的生理反应密切相关。
因此,测定不同种类茶叶中咖啡因的含量具有重要的意义。
咖啡因,化学名称为1,3,7-三甲基黄嘌呤,是一种中枢神经兴奋剂。
适量摄入咖啡因可以提神醒脑、增强注意力,但过量摄入可能会导致失眠、焦虑等不良反应。
茶叶中咖啡因的含量会受到多种因素的影响,如茶叶的品种、产地、加工工艺等。
在测定茶叶中咖啡因含量的方法中,常见的有高效液相色谱法(HPLC)、气相色谱法(GC)、紫外分光光度法等。
下面以高效液相色谱法为例,介绍其测定原理和步骤。
高效液相色谱法是利用样品中各组分在固定相和流动相之间的分配系数不同,从而实现分离和定量分析的一种方法。
在测定茶叶中咖啡因含量时,首先需要对茶叶样品进行前处理。
将茶叶样品研磨成粉末,准确称取一定量的粉末放入容器中,加入适量的有机溶剂(如甲醇或乙醇)进行萃取。
萃取过程通常在超声条件下进行,以提高萃取效率。
萃取完成后,将提取液过滤、浓缩,然后用流动相稀释至适当的浓度。
接下来,将处理好的样品溶液注入高效液相色谱仪中。
色谱柱内填充有特定的固定相,流动相在高压作用下携带样品溶液通过色谱柱。
由于咖啡因与其他成分在固定相和流动相之间的分配系数不同,它们在色谱柱中的保留时间也不同,从而实现分离。
通过检测器对分离出的咖啡因进行检测,常用的检测器有紫外检测器和二极管阵列检测器。
检测器将咖啡因的浓度信号转化为电信号,传输给数据处理系统,得到咖啡因的色谱峰面积或峰高。
根据事先建立的咖啡因标准曲线,可以计算出样品中咖啡因的含量。
为了保证测定结果的准确性和可靠性,实验过程中需要注意以下几点:一是样品的采集和处理要规范,确保样品具有代表性;二是实验仪器要经过校准和验证,保证性能稳定;三是实验操作要严格按照标准方法进行,控制好实验条件,减少误差。
茶叶中咖啡因的含量测定方法探索

茶叶中咖啡因的含量测定方法探索作者:武开业来源:《科技视界》 2014年第28期武开业(榆林市环境监测总站,陕西榆林 719000)【摘要】本文建立了用反相高效液相色谱法(HPLC)测定茶叶中咖啡因的方法。
茶叶经预处理后,通过Diomonsil C18(2)5u色谱柱分离,以甲醇+水混合溶液为流动相进行洗脱,于286 nm 波长下紫外检测,一次进样分析仅需4 m in, 咖啡因在10~150 ug/mL 范围内的线性关系良好, 在加标水平为20、30、50 ug /mL时,被测物的回收率为97.9%~103.8%。
【关键词】高效液相色谱;茶叶; 咖啡因咖啡因(C8H10N4O2)是从茶叶、咖啡果中提炼出来的一种甲基黄嘌呤的生物碱,化学名是1,3,7-三甲基黄嘌呤或3,7-二氢-1,3,7三甲基-1H-嘌呤-2,6-二酮,纯的咖啡因是白色的,具有强烈苦味的粉状物,熔点238°, 升华温度178°,易溶于水、乙醇、丙酮及氯仿等有机溶剂。
适度地使用咖啡因有祛除疲劳、兴奋神经的作用,临床上用于治疗神经衰弱和昏迷复苏。
但是,大剂量或长期使用也会对人体造成损害,特别是它也有成瘾性,一旦停用会出现精神萎顿、浑身困乏疲软等各种戒断症状,甚至导致吸食者下一代智能低下,肢体畸形,因此也被列入受国家管制的精神药品范围。
茶叶是常见的饮品,不同品种的茶叶含有的咖啡因含量也不同,反应在口感上也不同,所以对茶叶中含有的咖啡因进行测定是非常必要的。
图1 咖啡因的结构式1 实验部分1.1 仪器与试剂Waters 1525双泵高效液相色谱仪(美国沃特斯公司);0.45um滤膜过滤装置(上海摩速有限责任公司);万分之一电子分析天平(梅特勒-托利多公司);25uL微量注射器(Australia);KQ-50B超声仪(昆山市超声仪器有限公司);咖啡因标准品:纯度99%以上(广佛精细化工公司);CH3OH(色谱纯);三氯甲烷(分析纯);无水硫酸钠(分析纯);氯化钠(分析纯);试剂用水为18.2MΩ二次去离子水。
多种茶叶不同泡法茶水中咖啡因浓度的测定

多种茶叶不同泡法茶水中咖啡因浓度的测定作者:胡孟宇张云艳席红霞张婧来源:《化学教学》2022年第03期摘要:通过模拟生活中泡茶工艺,泡制白茶、铁观音、普洱茶、碧螺春、正山小种、高山云雾、西湖龙井及云南红茶多种茶叶水。
在高效液相色谱仪上开发适用于分析茶水中咖啡因浓度的色谱方法,并用以检测上述各种茶水中咖啡因的浓度。
结果表明,模拟泡茶a,经1小时浸泡白茶茶水中咖啡因含量较高,接近200mg·L-1,碧螺春其次,而正山小种的含量最低。
模拟泡茶b,高山云雾、西湖龙井及云南红茶茶水中咖啡因浓度从一泡到六泡均呈下降趋势,且从一泡到二泡,下降趋势明显。
模拟泡茶c,从一泡到六泡,普洱茶茶水中咖啡因的浓度总体上处于下降的趋势。
关键词:茶水; 咖啡因; 模拟泡茶; 高效液相色谱; 实验探究文章编号: 1005-6629(2022)03-0076-04中图分类号: G633.8文献标识码: B中国是“茶之国”,喝茶已有四千多年的历史。
茶叶中化学成分的研究始于1827年,人们在茶中发现嘌呤碱化合物,茶叶中的生物碱又以咖啡因为主,含量一般为2%~4%。
咖啡因具有提神醒脑、兴奋中枢神经的作用[1],摄入咖啡因的量非常关键,被分为不同等级[2]。
鲁科版高中化学选修6《实验化学》教材中设置了“从茶叶中提取咖啡因”的探究实验,希望通过该实验帮助学生理解从茶叶中提取咖啡因的基本原理和方法,了解咖啡因的一般性质,并进一步熟悉萃取、蒸馏、升华等实验基本操作。
但教材实验提取茶叶中咖啡因时用到的是有机溶剂,有一定毒性,且需要对提取液进行升华来测试茶叶的咖啡因含量,过程较繁琐[3];有文献采取水提法或者溶剂浸提法[4]。
水提法既无法提取茶叶中全部咖啡因,又不能表示茶水中咖啡因含量,且对茶叶种类局限性很大,而溶剂浸提法则具有一定毒性[5]。
可见用这些方法提取及分析茶叶中的咖啡因含量,不适宜作为中学生的实验活动。
为了克服上述提取方式的缺点,本实验使用高效液相色谱仪作为提取和分析茶叶中咖啡因含量的手段,可以方便准确地获知各种茶水的咖啡因含量。
茶叶中咖啡因的HPLC分析

茶叶中咖啡因的高效液相色谱分析一、实验目的:⑴ 了解反相色谱的原理和应用⑵ 掌握标准曲线定量法二、实验原理:咖啡因又称咖啡碱,属黄嘌呤衍生物,化学名称1,3,7-三甲基黄嘌呤,可由茶叶或咖啡中提取而得的一种生物碱。
它能兴奋大脑皮层,使人精神兴奋。
咖啡中含咖啡因1.2%-1.8%,茶叶约含2.0%-4.7%。
其分子式为C 8H 10O 2N 4,结构式:N NN N CH 3CH 3CH 3OO样品在碱性条件下,用氯仿定量提取,采用反相液相色谱柱进行分离,以紫外检测器进行检测,以咖啡因标准系列溶液的色谱峰面积对其浓度作工作曲线,再根据样品中的咖啡因面积,由工作曲线算出浓度。
三、 实验仪器与药品⑴仪器Waters2695型高效液相色谱仪操作软件色谱柱(EconosphereC18)自动进样器⑵药品①甲醇(色谱纯)双蒸水氯仿(A.R)1mol/LNaOH;NaCl(A.R.) Na2SO4(A.R.)咖啡因(A.R.)茶叶②1000mg/L咖啡因储备液将咖啡因在110℃下烘干1小时,准确称取0.1000g咖啡因,用氯仿溶解,转移至100mL容量瓶中,定容至刻度。
四、实验步骤:⑴色谱条件:柱温:室温流动相:甲醇/水=60:40流量:1.0mL/min检测波长:275nm⑵咖啡因标准系列溶液配制:分别用吸量管吸取0.40、0.60、0.80、1.00、1.20、1.40mL咖啡因储备液于六只容量瓶中,用氯仿定容至刻度,浓度分别为40、60、80、100、120、140mg/L⑶样品处理:①准确称取茶叶0.3g,加蒸馏水30mL煮沸10min,冷却后将清液转移至100mL容量瓶,并按此操作重复两次,定容至刻度。
将3份样品溶液分别进行干过滤,弃去前过滤液,取后面的过滤液。
②分别取上述三份样品溶液25.0mL于125mL分液漏斗中,加饱和氯化钠溶液,溶液,然后用氯仿分三次萃取。
将氯仿提取液分离后经装有无水硫酸钠小漏斗,过滤至容量瓶中,最后用少量氯仿多次洗涤小漏斗,定容至刻度。
绿茶中咖啡因含量的测定

摘要本文对一系列绿茶的化学成分及其抗氧化性进行了研究。
利用紫外分光光度法测定其茶黄酮类化合物、茶多糖的含量;绿茶样品多糖含量为57.19-357.8m g/g。
同时提取12种绿茶样品中的咖啡因和茶多酚,分别用氯仿和乙酸乙酯进行萃取,经H P L C分别测定其含量。
绿茶样品的咖啡因含量为 4.637-12.99m g/g,其中福建绿螺含量最高。
茶多酚含量为48.904-110.86m g/g,其中浙江龙井含量最高。
利用气相色谱-质谱联用技术,通过水蒸气蒸馏提取法对两种工艺相同的绿茶样品的挥发性成分进行分离和结构鉴定。
运用气相色谱面积归一化法确定各个成分的相对百分含量。
结果表明人工培育的鞍山金壶中二苯胺含量最高。
以邻苯三酚—碳酸盐缓冲溶液—鲁米诺发光体系的发光强度为空白发光峰值,流动注射化学发光法测定12种绿茶样品的抗氧化性,其I C50值为0.182-0.840m g/m L。
关键词:绿茶;化学成分;高效液相色谱法;抗氧化性;流动注射化学发光法目录摘要 (I)Abstract (II)1绪论 (4)1.1茶的起源 (4)1.2茶文化 (5)1.3饮茶 (6)1.4茶叶的分类 (7)1.5绿茶 (7)1.5.1绿茶简介 (7)1.5.2绿茶的分类 (8)1.5.3绿茶的主要化学成分 (9)2绿茶中咖啡因含量的测定 (12)2.1 引言 (12)2.2 实验部分 (13)2.2.1目前的测定方法 (19)2.2.2测定 (19)2.3 结论 (21)3咖啡因的应用与展望 (21)参考文献 (23)1 绪论我国是茶树原产国,也是世界上最早发现和利用茶叶的国家[1]。
茶属双子叶植物,约30属,500种,分布于热带和亚热带地区,我国有14属,397种,主产长江以南各地。
绿茶是我国六大茶类之一,属于不发酵茶。
绿茶做为中国的主要茶类,全国年产10万吨茶叶,产量位居六大初制茶之首。
中国生产绿茶的范围极为广泛,浙江、河南、安徽、江西、江苏、四川、湖南、湖北、广西、福建、贵州为我国的绿茶主产省份。
茶叶提取物中咖啡因含量的测定

茶叶提取物中咖啡因含量的测定一、试验原理当前茶饮料因其具有一定的保健功能而十分流行,其中主要的有效成分是茶叶提取物,茶叶(Tea)提取物中含有咖啡因(Caffeine)。
是一种生物碱化合物,有提神醒脑的作用,是一种中枢神经高兴剂。
同样含有咖啡因成分的咖啡、可乐等软饮料及能量饮料在市场上亦非常畅销,但长久、大量饮用有成瘾的趋势。
此外,咖啡因也是世界上最普遍用法的精神药品之一,我国将咖啡因列为“精神药品”加以管制。
咖啡因的测定办法以高效液相色谱法为主,通过色谱柱将咖啡因与样品基体组分分别,用紫外检测器测定其含量。
在高效液相色谱法中应用最为广泛的是反相色谱,即流淌相的极性大于固定相。
本试验以非极性的C18键合相色谱柱、极性的/水流淌相分别样品中咖啡因,用法紫外检测器,以色谱峰面积为定量分析指标,计算饮料中咖啡因的含量。
二、主要仪器和药品高效液相色谱仪(C18反相键合相色谱柱4.6 mm x15 cm,微量注射器)、紫外检测器(波长254 nm)。
流淌相::水=60:40,流速0.5 ml·min-1. (分析纯)、储备液(配制成咖啡因1000 mg·ml-1的甲醇溶液)、(色谱纯)、试验用水用法纯水机制取。
三、试验步骤 1.标准溶液配制将咖啡因储备液用甲醇稀释成浓度分离为20、40、80、120、160 mg·L-1的标准系列,备用。
2.样品处理依据样品状态不同,实行相应的处理办法。
常用的样品处理办法如下:①取100 ml液态饮料(特殊是可乐等碳酸饮料)于250 ml 干燥烧杯中,经超声脱气5 min,驱除其中C02等气体,依其含量适当稀释。
②精确称取固态咖啡0.25 g(精确至0.0001g),水溶解,定容100.0 ml,摇匀备用。
③精确称取茶叶0.3 g(精确至0.0001g) ,30 ml水煮沸10 min,冷却后将上清液转移至100 ml容量瓶中,重复上述过程两次,定容并摇匀备用。
拉曼光谱测茶叶中咖啡因的含量

1 7
������/L的纯咖数据绘制在 一张图中,结果如下:
图二
2 号茶水
图五不同浓度的咖啡因拉曼光谱扫描 图中横坐标为扫描波长,纵坐标为峰强。图中 B-H 曲线依次代表浓度的降低。 咖啡因溶液的浓度和峰强列表如下: 图 三 3 号茶水
表一不同浓度的咖啡因样品对应的峰强 对浓度和峰强进行线性拟合,所得图形如 下: 图四 4 号茶水 上面四幅图从左到右、 从上到下分别为 1、 2、 3、 4 四种茶叶的 750-770nm 的拉曼光谱扫描, 从图中可以清晰的看出,四种茶叶在 797.7nm 处出现了明显的咖啡因的拉曼光谱特征峰, 从 而清晰的证明了茶水中存在咖啡因, 且咖啡因 的拉曼光谱特征峰十分明显。 从图中还可以看出, 不同茶叶的咖啡因的 拉曼光谱特征峰的峰强不同, 从而表明四种茶 叶的茶水中咖啡因的浓度也不同。 2.3.2 茶水中咖啡因含量的定量测量 取咖啡因固体粉末, 用超纯水各自配置浓 度为1������/L、 ������/L、 ������/L、 ������/L、 ������/L、 ������/L、
2 3 4 5 6 1 1 1 1 1
图六咖啡因浓度和峰强的拟合直线 图中横坐标为浓度( g/L ) , 纵坐标为峰强。
因此, 本次测量中咖啡因拉曼光谱峰强与浓度 的线性关系可表示如下: I=7092.663*C+1012.057 因此,可得 C=(I-1012.057)/7092.663 (3) 四种茶水中咖啡因浓度如下: (2)
其中,I 为光学系统表面所收集到的样品表面 拉曼信号强度;K 为分子的拉曼散射截面积; Φ 为样品表面的激光入射功率; 和 分 别是入射光和散射光的吸收系数 ;Z 为入射光 和散射光通过的距离 ; 输函数;b 为样品池的厚度。 由上式可以看出,在一定条件下,拉曼光 谱的强度与样品溶液的浓度 C 成正比,因此, 在实验中,注意控制其他条件不变,用不同浓 度的纯咖啡因样品进行扫描, 便可以定出峰强 与浓度的关系。 2.2 实验仪器及试剂 本实验采用天津港东 LRS- Ⅲ型激光拉曼 光谱仪,光源波长为 532.0nm,采用光电倍增 管作为拉曼光谱的单通道接受器件, 并应用计 图一 1 号茶水 为光学系统的传
高效液相色谱法测定六安茶叶中的咖啡因

高效液相色谱法测定六安茶叶中的咖啡因摘要:用高效液相色谱仪分别测定金寨、霍山、舒城、独山等产地茶叶中咖啡因的含量,比较咖啡因含量与地区及与茶叶采摘期的关系。
方法采用ods-c18柱,以ch3oh-h2o(35:65)溶液做流动相,紫外检测波长为275nm。
可在5min内将咖啡因与基体分离,咖啡因含量与峰面积在30μg/ml -180μg/ml范围内成线性关系,回归方程为:y=21470x+1962620,相关系数r=0.9992。
方法线性良好,平行样测定rsd≤1.1℅,加标回收率为97.5℅~106℅。
结果表明,六安地区同一种茶采摘期不同咖啡因的含量不同,不同产地的茶中其咖啡因的含量也不同。
关键词:咖啡因; hplc;茶叶中图分类号:x830.2 文献标识码:a 文章编号:1007-0370 (2012) 01-0145-03igh performance liquid chromatographic method for the determination of caffeine in tea of lu’anyu min1, feng xinzhang2, zhang li-li 2(1.lu’an jin an district environmental protection bureau,anhui 237002;2. lu’an environmental monitoring center,anhui 237001)abstract:were determined by high performance liquid chromatography jinzhai、huoshan、shucheng、dushan and other origin tea caffeine content, caffeine content compared with the region’s relationship and the relationship with the tea picking period.the methods ods-c18,pillar, ch3oh-h2o (35:65) solution is mobile phase, uv detection wavelength of 275nm. in 5min and the substrate within the isolated caffeine, caffeine content and the peak area of 30μg/ml -180μg/ml linear range, regression equation: y = 21470x +1962620, r = 0.9992. the linear sound and rsd≤1.1℅.spiked recoveries between 97.5℅ and 106℅.the results show that tea picking period lu’an different regions the same caffeine content is different in different areas of its caffeine content of tea is different.key words:caffeine; hplc; tea茶叶中含有一定量的咖啡因,对其中咖啡因进行有效分离与准确测定,将有助于对产品质量进行准确监控,常用来测定咖啡因的方法有薄层层析法[1]、气相色谱-质谱法[1]等。
紫外分光光度法测定安徽罗汉尖老茶中咖啡因含量

水 定 容 至 刻 度 , 成 t 0 0“ / 的 咖 啡 因 供 试 品 制 0 . g ml
叶中富含 咖 啡 因 、 多 酚 、 茶 儿茶 素 、 多 糖 等 药理 成 茶
茶 中 的 咖 啡 因含 量 。 1 仪 器 与 试 药
溶 液 。取 2ml 试 品溶液 加入 1 容量 瓶 中 , 供 0ml 加
蒸 馏水 定容 至刻度 。
2 2 2 茶树 老 叶和粗 老茶供 试 品溶液 制备 : 别取 .. 分 茶 树老 叶和 粗老茶 的粉 末 ( 4 过 0目筛 ) . , 4 0 3 0g 加 5
2 2 2 4n 处 测 定 咖 啡 因的 吸 收 度 。 结 果 以 浓 度 ( ) 吸 光 度 ( 的 回 归 方 程 为 A —O 0 8c 0 0 8 7 ~ 7 m c对 A) .4 + . 2 , r 0 9 8 线 性 范 围 为 1 ~ 3 g ml平 均 回 收 率 为 9 . 。 结 论 这 种 紫 外 分 光 光 度 法 简 便 , 敏 度 高 , 一 .9, 0 0t / ,  ̄ 77 灵 可 用 于 茶 树 老 叶 和 粗 老 茶 中咖 啡 因 的含 量 测 定 。
分[ 。为 了达到对粗 老茶 和茶树老 叶 的科 学利用 , 1 ] 进
一
步发掘茶树 的潜 在资源 , 需要对粗 老茶提 取物 中咖
啡因的含量进行准 确测定 。咖啡 因含有 嘌呤环 , 有 具
共轭 双键体 系 , 在紫 外分光光度法测 定时具 有特征 性 的吸收光谱l ] 2 。本实验 旨在测定 提取 出的精制 咖啡 因的纯度 , 以及茶树 老叶中 、0 8年老茶 和 2 0 年 老 20 09
高效液相色谱法测定五种茶叶中咖啡因含量

高效 液相 色谱 法 测 定 五 种 茶 叶 中咖 啡 因含 量
贾 巧 李 龙 孙晓琴 徐 晓兰 杨 驰 边清泉
( 纬阳师范学院化学与化学工程学院 四川绵 阳 6 10 ) 2 0 0
摘要 : 目的: 采用 高效液相色谱 法测定了 5种茶叶中咖啡因的含量。方法 : 采用 P eomex ( . m× 5 m, hnn nCs 4 6m 2 0m 5 m) 反相色谱柱 , 流动相 C 3 H : 0= . 4 5 H O H2 5 5: . ,流速 I0( . mL-a ) 检测波长为 2 2n , 温为 3 rn i , 7 l 柱 n 5℃ , 在 所 选条 件下 , 品中待测组分与其它组分分离 良好 ( >1 5 , 样 R . ) 通过重 复性实 验和 加标 回收实验 , 验证 了方法 的稳 定 性和可靠性。在本实验范围内各 组分的峰面积和浓度之间具有 良好的线性关 系 ,2= .9 5种茶叶的咖啡因 r 099 9, 回收率 9 .8 ~17 7 % , S = . % ~3O 。 7 4 % 0 .3 R D 2 6 .%
m tao a r5 5: . ) tevlc yo o a . e n l t ( . 4 5 , } e i f w w s 0mL・mi ~,teu e c o ae n t w s h w e l ot f l 1 n h V dt t nw vl g a ei e h
a d s mp e r c v r x e me tv rf e sa ii n eibi t ft eme o 。Th e u t ho t a e n a l e o e y e p r n eiy t tb lt a d r la l y o t d i h y i h h e r s l s w tt s h h
高效液相色谱法测定绿茶中咖啡因含量

本科毕业论文( 2013 届 )题目:高效液相色谱法测定绿茶中咖啡因含量学院:化学化工学院专业:学生姓名:指导合作导师:职称(学位):完成时间:成绩:目录摘要 (3)引言 (4)1提取实验 (6)1.1提取实验原理 (6)1.2仪器 (7)1.3试剂 (7)1.4主要装置图 (7)1.5咖啡因对照品的提取及提纯 (7)2检测实验 (8)2.1仪器 (8)2.2试剂 (8)2.3色谱条件 (9)2.4溶液配制 (9)2.4.1咖啡因标准储备液 (9)2.4.2标准系列配制 (9)2.4.3样品制备 (9)2.4.4 流动相(20mmol/L乙酸铵溶液)的配制 (10)2.5色谱进样标准曲线的绘制 (9)2.6样品测定 (13)2.7回收率试验测定 (13)2.8注意事项 (15)3结论 (16)参考文献 (17)致谢 (18)高效液相色谱法测定绿茶中咖啡因含量摘要:本文主要是以茶叶为原料在索式提取器中用95%乙醇提取茶叶中的咖啡因作为标准样品,并配制标准系列溶液,实验简便、易操作,采用高效液相色谱法测定系列溶液及处理后的待测样品溶液,绘制出咖啡因标准曲线,并求出样品中咖啡因含量。
高效液相色谱Aglient TC-C18(4.6×150)以20mmol/L乙酸铵溶液—甲醇(75:25)为流动相,在检测波长254nm的条件下测定。
关键词:咖啡因;高效液相色谱;含量HPLC Method for the Determination ofCaffeine in DrinksCollege of chemistry and chemical engineering Applied chemistryMeng Xiaoting(20907032037)Direcyor:Guan Tingting (Lecturer)Abstract:This article is based on tea as the raw material and used the method that extract the caffeine as the control products by adding tea in the Soxhlet extractor using 95% ethanol extraction. Then compound of the standard series solution. The experiment is very simplicity, easy controlling. And then used the HPLC method for the determination of the standard series solution and the sample solution afer treatment. Drawing the standard curve of caffeine, and found out caffeine content in the sample solution. The Aglient TC-C18 column (150 mm ×4. 6 mm) was used with 20mmol/L ammonium acetate solution –methanol (75:25) as the mobile phrase. Caffeine content of drinks was determined at 254 nm.Key Words:caffeine; HPLC; contents引言咖啡因是存在于茶叶、咖啡、可可以及某些植物中的生物碱之一,属黄嘌呤衍生物,它的化学名称是1,3,7-三甲基黄嘌呤,分子式:810242C H O N H O 。
高效液相色谱法测定茶叶中咖啡因

-
1 2 3
4
高效液相色谱法测定茶叶中咖啡因
实验目的
实验目的
本实验旨在通过高效液相色 谱法(HPLC)测定茶叶中咖啡 因的含量,了解茶叶品质与 咖啡因含量的关系,为茶叶 的品质控制和评价提供科学
依据
PART 2
实验原理
实验原理
高效液相色谱法是一种常用的分离分析方法,具有高 分离效能、高灵敏度、高速度等优点。其原理是基于 不同物质在固定相和流动相之间的分配系数差异,实 现多组分的分离。在HPLC实验中,待测物质在色谱柱 上的吸附与解吸附过程不断进行,最终实现分离
本实验采用C18色谱柱,以甲醇-水溶液为流动相,在 紫外检测器下对茶叶提取液进行检测。咖啡因在紫外 光下有较强吸收,通过测定其峰面积,可计算出咖啡 因的含量
PART 3
实验步骤
实验步骤
样品处理:称取适量茶叶 样品,用研钵研磨成细粉 末。准确称取一定量茶叶 粉末于离心管中,加入适 量甲醇,超声提取一定时 间。离心后取上清液,进
量
PART 4结果分析结果分析Fra bibliotek3,658
通过本实验,可以得出不同茶叶 样品中咖啡因的含量,进而分析 茶叶品质与咖啡因含量的关系
咖啡因含量可作为评价茶叶品质 的重要指标之一
74%
30000
此外,本实验可为茶叶生产、加 工和品质控制提供参考依据
-
感谢观看
汇报人:XXXX
指导老师:XXX
行下一步分析
色谱条件:色谱柱为C18 柱,流动相为甲醇-水溶 液(体积比为7:3),流速 为1.0 mL/min,检测波长
为274 nm
测定:将处理后的样品注 入高效液相色谱仪,记录 咖啡因的色谱峰。通过对 比标准品色谱峰,确定咖 啡因的保留时间。根据峰
普洱茶中咖啡因含量的红外光谱法快速判别

普洱茶中咖啡因含量的红外光谱法快速判别张雪娟;李亮星;胡栋宝;高雪春;伍贤学【摘要】利用红外光谱和紫外分光光度法对四种市售普洱茶中咖啡因的相对含量进行判别分析和测定.从610 cm-1处红外光特征吸收峰的相对强弱可以判断,四种茶中咖啡含量从高到低的顺序为..Tea4(0.000 70 A)>Tea2(0.000 62 A)>Tea1(0.000 55 A)>Tea3(0.000 40 A),而紫外分光光度法分析结果为:Tea4(4.31%)>Tea2(4.13%)>Tea1(3.75%)>Tea3(3.22%).说明两种分析方法对茶中咖啡因含量高低顺序的判别结果一致,同时说明通过进一步研究可望建立一种基于红外光谱技术的不同茶叶中咖啡因含量高低的原位、快速判别方法.【期刊名称】《玉溪师范学院学报》【年(卷),期】2016(032)012【总页数】5页(P27-31)【关键词】普洱茶;咖啡因;相对含量;红外光谱【作者】张雪娟;李亮星;胡栋宝;高雪春;伍贤学【作者单位】玉溪师范学院资源环境学院,云南玉溪653100;玉溪师范学院资源环境学院,云南玉溪653100;玉溪师范学院资源环境学院,云南玉溪653100;玉溪师范学院资源环境学院,云南玉溪653100;玉溪师范学院资源环境学院,云南玉溪653100【正文语种】中文【中图分类】O657.33咖啡因是一种黄嘌呤生物碱类化合物,具有兴奋神经、强心、利尿等生理作用.咖啡因在茶叶、咖啡豆、可可等经济作物中广泛存在,茶叶中的咖啡因普遍含量为2%~5%,有的可高达7%,是天然咖啡因的最重要来源.茶叶因其抗氧化等广泛的保健功能而广受大众欢迎,但对于咖啡因的敏感人群而言,咖啡因的摄入可能导致失眠及进一步的健康问题.因此,茶叶中咖啡因含量的高低是大家普遍关心的问题. 目前,检测茶叶中咖啡因的国标方法有高效液相色谱法和紫外分光光度法[1].文献[2~5]报道分别报道了利用红外光谱法、近红外、高效液相色谱法等测定茶叶中咖啡因含量的方法,这些分析方法为准确测定茶叶中咖啡因的含量起到了非常重要的作用.但是,这些检测方法操作繁琐、耗时费力,因此亟需一种绿色环保、简便快捷的判别方法.本研究前期的研究工作表明,基于红外光谱技术可能实现上述目标. 红外光谱法是经典的有机结构分析方法之一,主要通过化合物红外光谱分析进行有机官能团的鉴定.近年来,大量的红外光谱研究对象由化合物转为复杂混合物样品.孙素琴等在中药、食品等复杂体系的红外光谱研究方面做了大量卓有成效的研究工作,表明基于现代红外光谱技术很可能建立一种简便易行、快速有效的混合物整体分析方法[6~8].本研究以普洱茶为例,基于红外光谱分析判断茶叶中咖啡因含量的相对高低,并与紫外分光光度法测定结果进行比较,初步探究一种基于红外光谱技术的不同茶叶中咖啡因相对含量的快速判别方法.1.1 样品来源与预处理四种普洱熟茶均为云南大叶茶种制品,采购于当地茶叶市场,分别为Tea1(普洱熟茶)、Tea2(陈年熟普)、Tea3(普洱熟沱)及Tea4(三级熟普).各取10 g茶叶样品60 ℃烘干24 h后,取5 g留作紫外分光光度法测定咖啡因含量,剩余茶样用万能中药粉碎机粉碎至200目以上,收集茶粉于聚乙烯自封袋并置于干燥器中保存备用. 1.2 仪器及试剂红外光谱的测定:Frontier型傅立叶变换红外光谱仪(Perkin-Elmer,USA);DTGS 检测器;扫描范围:4 000~400 cm-1;分辨率,4 cm-1;累计扫描32次;扫描时自动扣除H2O和CO2的干扰.原始红光谱由Spectrum 10.0红外光谱软件(Perkin-Elmer,USA)处理,二阶导数红外光谱经Savitzky-Golay拟合得到(13点平滑).溴化钾为天津天光化学试剂公司产品.1.3 实验方法咖啡因的含量测定:本实验采用紫外分光光度法(GB/T 8312-2013)对茶样中的咖啡因含量进行定量分析,分析结果为红外光谱分析结果提供参考.所用的紫外分光光度计型号为岛津UV-160A型.分别取0、1、2、5、6、8、10、12 mL咖啡因标准液(100 μg/L)配成一系列50 mL的标准溶液,于波长274 nm处进行测定系列标准溶液的吸光度.同样依据国标方法制备了四种茶样的咖啡因试液并进行吸光度测定.红外光谱采集方法:分别取茶样粉末约2 mg与约100 mg溴化钾(天津天光)混合研磨均匀后放入压片模具,8吨压力下保持2 min,然后进行红外测试得茶样的红外光谱.采用同样的方法测定咖啡因的红外光谱供对比分析用.2.1 红外光谱分析及二阶导数红外光谱分析从图1可以看出,咖啡因的主要红外光谱特征吸收峰有1 702、1 658、1 549、1 485、1 238、745、611、482 cm-1等,但它们中的绝大多数吸收峰与茶叶中其他组分的红外光谱吸收峰重叠严重,导致难以直接对茶样中咖啡因的存在及相对含量状况进行分析.二阶导数红外光谱可以增强光谱的表观分辨率,故对上述红外光谱进行了二阶导数处理.红外光谱的吸收规律和其他分光光度法一样,在一定范围内都遵守朗伯-比尔定律.通过与对照品的红外光谱对比分析,不仅可直接获得对照品在混合物样品中是否存在(定性),还可根据特定的特征峰相对强弱比较同类混合物样品中该对照品的相对含量(定量).图2(左)是四种茶叶及咖啡因的二阶导数红外光谱重叠图.通过对茶叶与咖啡因的二阶导数红外光谱对比分析发现,绝大多数咖啡因的特征峰仍然被茶叶其他组分的吸收峰掩盖,但610和487 cm-1处例外.从图2(左)可知,咖啡因对照品在482 cm-1处的特征峰在茶样光谱中向高波数方向移动了约5个波数到了487 cm-1处.这可能是因为茶叶中呈碱性咖啡因与呈酸性的茶多酚等茶叶成分发生了一定程度的相互作用所致,值得进一步深入研究.对于透射红外光谱而言,越往低波数方向红外光能量就越弱,噪音会相应增强,进而影响谱图的解析.基于上述分析,选择610 cm-1处特征峰作为茶叶中咖啡因相对含量判别分析的特征峰.为了便于观察,对610 cm-1处的局部谱图进行了放大处理,如图2(右)所示.从图2(右)可以看出,四种普洱茶的二阶导数红外光谱在610 cm-1处的吸收峰强度彼此存在一定差异.图2(右)下方给出了四种茶的二阶导数红外光谱在610.43cm-1处的吸光度值.根据肉眼观察结果或根据610 cm-1处的吸光度值大小判断四种茶中咖啡因含量的高低顺序为:Tea4(0.000 70 A)>Tea2(0.000 62A)>Tea1(0.000 55 A)>Tea3(0.000 40 A),即三级熟普(Tea4)中咖啡因含量最高,而普洱熟沱(Tea3)中的含量最低.为了验证红外光谱分析结果是否可靠,采用测定咖啡因国标方法之一的紫外分光光度法对四种茶样中的咖啡因进行了定量测定.2.2 四种普洱熟茶中咖啡因的紫外分光光度法分析结果根据测定结果制作出标准工作曲线(图3),将所测吸光度值代入回归方程,计算茶汤中咖啡因的浓度并及算出茶叶中咖啡因的质量百分含量(见附表).从附表中的紫外分光光度法测定结果可知,四种普洱茶中咖啡因含量高低顺序为:Tea4(4.31%)>Tea2(4.13%)>Tea1(3.75%)>Tea3(3.22%).红外光谱法对本研究中四种茶叶的咖啡因含量高低顺序判别结果与紫外分光光度法的判断结果一致,即四种茶中咖啡含量高低顺序为:Tea4>Tea2>Tea1>Tea3,三级熟普(Tea4)中咖啡因含量最高,而普洱熟沱(Tea3)中的含量最低.红外光谱法具有低碳环保、简便易行、既可定性又可定量等诸多特点,在复杂混合物分析中具有独特的优势.本文的研究以咖啡因为对照品,通过红外光谱及二阶导数红外光谱分析,确定了610 cm-1是咖啡因在茶样红外光谱中基本不受茶叶中其他组分干扰的特征吸收峰,根据四种茶叶二阶导数红外光谱在610 cm-1处吸收峰的相对强弱得出,四种茶叶中咖啡因含量高低顺序为Tea4>Tea2>Tea1>Tea3,通过紫外分光光度法(GB/T 8312-2013)测定结果证明了红外光谱法的判别结果的有效性,红外光谱判别结果与紫外光谱法判定结果一致.本文的初步研究结果说明,通过进一步系统研究有望建立起一种基于红外光谱技术的茶叶中咖啡因含量的快速分析方法,而这是具有重要的市场价值的.【相关文献】[1]GB/T 8312-2013,茶咖啡碱测定[S].北京:中国标准出版社,2014.[2]Manish MP,Joseph I. Rapid determination of caffeine content in soft drinks using FTIR-ATR spectroscopy[J].Food Chem,2002 (78):261-266.[3]Sinija VR,Mishra. HN.FT-NIR spectroscopy for caffeine estimation in instant green tea powder and granules[J].LWT-Food Sci Technol,2009(42):998-1002.[4]Hideki H,Atsushi N,Tomomi U,et al.Rapid determination of caffeine in tea leaves[J].J Chromatogr A,2002 (942):271-273.[5]Rostagno M,Manchon N,Arrigo MD,et al.Fast and simultaneous determination of phenolic compounds and caffeine in teas, mate, instant coffee, soft drink and energetic drink by high-performance liquid chromatography using a fused-core column[J].Anal Chim Acta,2011 (685):204-211.[6]Sun SQ,Chen JB,Zhou Q.Application of mid-infrared spectroscopy in the quality control of traditional Chinese medicines[J].Planta Med,2010(76):1987-1996.[7]Sun SQ,Zhou Q,Chen JB.Infrared spectroscopy for complexmixtures[M].Beijing:Chemical Industry Press,2011.[8]Xu,CH Wang Y,Chen JB.Infrared macro-fingerprint analysis-through-separation for holographic chemical characterization of herbal medicine[J].J Pharm Biomed Anal,2013(74):298-307.。
茶叶中咖啡因含量的测定与分析

茶叶中咖啡因含量的测定与分析茶叶是一种被广泛消费的饮料,而其中的咖啡因含量则成为人们关注的焦点之一。
本文将介绍茶叶中咖啡因含量的测定方法,并分析其意义和影响因素。
一、测定方法咖啡因是一种生物活性成分,可以通过多种方法进行测定。
其中,最常用的方法是高效液相色谱法(HPLC)。
该方法的步骤包括样品制备、样品进样、色谱分离和检测咖啡因峰。
1. 样品制备将茶叶样品研磨成细粉,并通过适当的方法提取咖啡因。
常用的提取方法包括水浸提、乙酸乙酯提取等。
2. 样品进样将提取得到的茶叶样品溶液通过进样器进入液相色谱仪,并设置合适的进样量。
3. 色谱分离使用高效液相色谱仪进行色谱分离,常用的色谱柱为反相色谱柱。
通过调节流动相的组成和流速,实现峰的分离。
4. 检测咖啡因峰使用紫外检测器检测咖啡因的吸收峰。
根据峰的面积和高度,可以定量分析茶叶样品中的咖啡因含量。
二、意义与影响因素对茶叶中咖啡因含量进行测定和分析具有一定的意义和影响因素。
以下将详细介绍。
1. 了解茶叶咖啡因含量测定茶叶中咖啡因含量可以帮助人们了解茶叶的咖啡因含量水平。
不同种类的茶叶中咖啡因含量不同,这也是人们选择饮用不同茶叶的一个重要参考指标。
2. 社会健康关注咖啡因是一种中枢神经兴奋剂,摄入过多可能对人体健康产生不良影响。
通过测定茶叶中咖啡因含量,有助于人们合理控制咖啡因的摄入量,关注社会健康。
3. 其他影响因素除了茶叶的种类和制备方法外,其生长环境、采摘季节等因素也可能会对茶叶中咖啡因含量产生影响。
对这些影响因素的研究和分析,有助于进一步了解和优化茶叶的生产和质量控制。
总结:通过高效液相色谱法测定茶叶中咖啡因含量,可以从科学的角度对茶叶进行分析和研究。
这对于了解茶叶的质量、选择适合自己的茶叶品种和控制咖啡因的摄入量都有一定的意义。
同时,还需要深入研究和探讨茶叶中咖啡因含量的影响因素,以进一步提高茶叶的品质。
注:本文所述测定方法仅作参考,具体操作请参考相应文献或专业指导。
高效液相法测定红茶中的咖啡因含量

高效液相色谱法测定红茶中的咖啡因含量高效液相色谱法测定红茶中的咖啡因含量茶叶中咖啡因的含量是衡量茶叶质量的重要指标之一,也具有多种药理活性[1]。
咖啡因(C8H10N4O2)又名咖啡碱,属甲基黄嘌呤化合物,具有提神醒脑等刺激中枢神经的作用,可溶于水、醇、氯仿、二氯甲烷等溶剂。
红茶中的咖啡因含量与绿茶接近;氨基酸及肽、有机酸和游离糖略高于绿茶;维生素类远低于绿茶。
红茶中的主要化学成分和特性与绿茶差异很大,从中医的角度上说,红茶性温,绿茶性凉。
因此,红茶品质特征和保健作用也有其独特性。
红茶性温,擅温中驱寒,温胃驱寒,能化痰、消食、开胃。
可见,红茶宜脾胃虚弱者饮用。
因此,在日常生活中,脾胃不好的消费者宜选用红茶进行品饮,喝红茶对健康有明显助益。
对于茶叶中咖啡因含量测定的常用方法有:紫外分光光谱法[2],高效液相色谱法[3]等。
文献中用高效液相色谱法分析咖啡因时主要采用C18色谱柱[3],运用反相键合相色谱法原理进行测定。
咖啡因结构式高效液相反相键合相色谱法基本原理:反相键合相色谱法采用非极性键合相为固定相,如十八烷基硅烷(C18)、辛烷基(C8)等化学键合相,有时也用弱极性和中等极性的键合相为固定相。
流动相以水作为基础溶剂再加入一定量与水混溶的极性调整剂,常用甲醇-水、乙腈-水等。
总之,固定相的极性比流动相得极性弱。
用于分离非极性或弱极性物质。
高效液相色谱仪主要包括五大系统:输液系统、进样系统、色谱柱系统、检测系统和数据记录处理系统。
1 实验仪器与试剂1.1 仪器高效液相色谱仪(Waters2690,美国)、紫外检测器(Waters2487,美国)、水相过滤用膜(0.22μm,直径50mm,上海半岛实业有限公司净化器材厂,批号 2008年10月6日)、电子天平(AB135-S,梅特勒-托利多仪器(上海)有限公司METTLER TOLEDO)、微孔滤膜(0.45μm,上海兴亚净化材料厂,批号2007年5月8日)1.2 试剂 超纯水、咖啡因储备液(660μg/ml ,实验室提供)、咖啡因对照品(中国药品生物制品检定所,200808)、绿茶(市售)、绿茶样品溶液(实验室提供)2 方法与结果2.1 系统适用性实验 使用咖啡因对照品图谱验证系统适用性,由图1所得理论塔板数为2501.6(大于2000),理论塔板高度为0.099mm ,分离度为6.25(大于1.5),均符合药典规定。
不同茶叶中茶多酚和咖啡因成分的对比分析

2 0 1 3 , 4 l ( 1 ) : l 0 ~l 5
Gu i z t l O L l F e a
不 同茶 叶 中 茶 多酚 和 咖 啡 因成 分 的对 比分 析
罗 婧 ,顾 颖 颖 ,刘 易 成 ,郭 梁。
( 1 . 上 海 理 工 大 学 环 境 与 建 筑 学 院 ,上 海 2 0 0 0 9 3 ;2 . 上海 理 工 大 学 理 学 院 , 上海 2 0 0 0 9 3 )
Ab s t r a c t :Pol y ph e n ol s a n d c a f f e i ne we r e e xt r a c t e d f r o m d i f f e r e nt t e a s wi t h h o t wa t e r a n d a l c o h o1.Th e c o nt e nt s o f c a f f e i n e a r e d e t e r mi ne d by U V s p e c t r o ph ot ome t r y, wh i l e t he c o nt e nt s of p o l y p he no l s a r e de t e r mi ne d by f e r r ou s t a r t r a t e me t ho d. Re s ul t s s h owe d t ha t t he t he o r de r of po l yp he no l s c on t e nt s i n di f f e r e nt t e a s i S gr e e n t e a> o ol o ng t e a> b l a c k t e a> d a r k t e a, wh i l e t he c h a n ge o r d e r of c a f f e i n e i S a s f o l l owi ng:bl a c k t e a> o o l on g t e a, g r e e n t e a i s t he l owe s t .I nv e s t i ga t i o ns i nt o t h e s i mu l a t i o n o f d a i l y dr i n ki n g t e a r e ve a l e d t ha t t he t e a p ou r 2 t O 3 t i me s we r e t he be s t ,t he a c t i v e i ngr e d i e nt s c a n be f u l l y ob t a i n e d i n wa t e r a t t he mo me nt . Ke y wo r ds : Te a Po l y ph e no I ;Ca f f e i ne ; Te a
红茶中咖啡因含量的测定
䊱ผᬢ䬠喋NJO喌
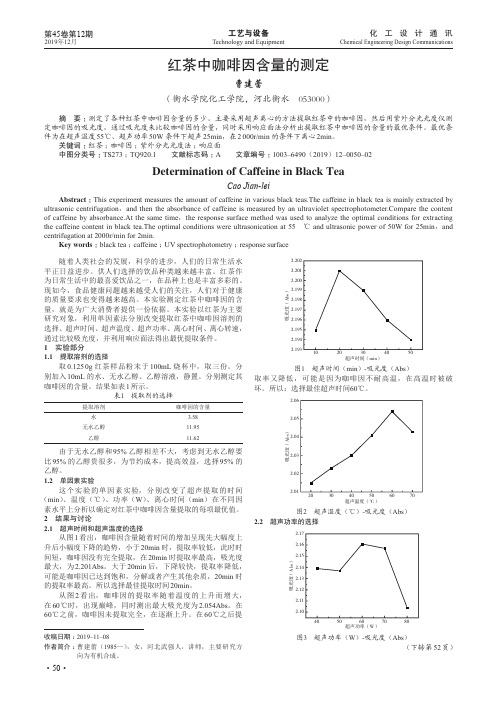
图1 超声时间(min)-吸光度(Abs) 取率又降低,可能是因为咖啡因不耐高温,在高温时被破 坏。所"CT喌
由于无水乙醇和 95% 乙醇相差不大,考虑到无水乙醇要
化工设计通讯
Chemical Engineering Design Communications
度的特点,可以将其引入催化燃烧室通过充分燃烧使其分解 为 CO2 与 H2O,以达到净化的目的。
因此,为了保证有机废气处理过程,通常使用双活性炭 箱的方式,即一使用一备用,保证循环。使用活性炭箱处于 吸附状态,负责处理有机废气,备用活性炭箱处于脱附状态, 将之前吸附的有机废气送入催化燃烧室燃烧处理。但是还需 要考虑脱附过程中的操作要求,由于有机气体的浓度与温度 较高,燃烧过程中氧气混入不当极易产生爆炸现象。而且由 于是燃烧处理,如果有机气体中含有氯、硫等元素,会与导 致脱附催化剂产生反应而破坏催化效果。
।ٵᏒ喋"CT喌
最大,为 2.201Abs。大于 20min 后,下降较快,提取率降低,
可能是咖啡因已达到饱和,分解或者产生其他杂质,20min 时
的提取率最高。所以选择最佳提取时间 20min。 从图 2 看出,咖啡因的提取率随着温度的上升而增大,
在 60℃时,出现巅峰,同时测出最大吸光度为 2.054Abs。在 60℃之前,咖啡因未提取完全,在逐渐上升。在 60℃之后提
素水平上分析以确定对红茶中咖啡因含量提取的每项最优值。
2 结果与讨论 2.1 超声时间和超声温度的选择
从图 1 看出,咖啡因含量随着时间的增加呈现先大幅度上 升后小幅度下降的趋势,小于 20min 时,提取率较低,此时时 间短,咖啡因没有完全提取,在 20min 时提取率最高,吸光度
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
..
ABSTRACT
Abstract: Application of soxhlet extraction method to extract caffeine from different tea, the same time under the different tea extract to the caffeine content is different. Tea contains a variety of alkaloids, its main composition is caffeine. A small amount of caffeine can make body and mind is in a state of excitement, stimulates the central nervous system, inducing the adrenaline released into the blood, and increase the body's blood sugar level, concentration. Too much caffeine makes people mental fatigue, body tremble, difficult to fall asleep, stimulate the gastric mucosa. So the determination of caffeine in tea, can help us to have a better understanding of the tea. Key words: tea, soxhlet extractor, caffeine, extraction, determination of content
溶液回流入圆底烧瓶,因此可萃取出溶于乙醇的部分物质。就这样利
用溶剂回流和虹吸作用,使茶叶末中的可溶物富集到圆底烧瓶内。
咖啡因是从茶叶、咖啡果中提炼出来的一种生物碱,适度地使用
有祛除疲劳、兴奋神经的作用,临床上用于治疗神经衰弱和昏迷复苏。
但是,大剂量或长期使用也会对人体造成损害,特别是它也有成瘾性,
一旦停用会出现精神萎顿、浑身困乏疲软等各种戒断症状,虽然其成
瘾性较弱,戒断症状也不十分严重。
一、茶叶的背景及主要成分:
1.1 茶叶的背景
中国历史上有很长的饮茶纪录,已经无法确切地查明到底是在什
么年代了,但是大致的时代是有说法的。并且也可以找到证据显示,
确实在世界上的很多地方饮茶的习惯是从中国传过去的。所以,很多
人认为饮茶就是中国人首创的,世界上其它地方的饮茶习惯、种植茶
叶的习惯都是直接或间接地从中国传过去的。
茶叶中含咖啡因虽然较低,但因我国是产茶大国,并有悠久的历
史,所以资源丰富。中国是茶树的原产地,因而也是茶叶的故乡,是
发现和利用茶叶最早的国家。数千年前就在我国的云南、贵州、四川
等地发现了野生茶树。茶叶是人类最佳的天然保健饮料,茶叶中含多
Hale Waihona Puke 种有机化合物、无机矿物质及人体必需的营养成分和药用成分。
论文作者签名:
签字日期: 年 月 日
指导教师签名:
签字日期: 年 月 日
..
摘要
应用索氏提取法从不同茶叶中提取咖啡因,相同的时间下不同的 茶叶中所提取到的咖啡因含量是不同的。茶叶中含有多种生物碱,其 主要成分为咖啡因。少量的咖啡因可以使身心处于一种兴奋状态,刺 激机体的中枢神经系统,诱发肾上腺素释放入血,增高机体血糖水平, 注意力集中。过量的咖啡因使人精神疲倦、身体发颤、难以入睡、刺 激胃黏膜。因此测定茶叶中的咖啡因,有助于我们对茶叶有更好的认 识。
1.2.2 功效及口感
(1)金骏眉
提神消疲、生津清热、利尿、消炎杀菌、解毒、暖胃养胃。最适
饮用时间为秋冬季,其汤色浓郁,兼有果香和蜜香,滋味比较醇厚。
(2)铁观音 减肥瘦身、抗癌、抗衰老、防治心血管疾病,不适宜在睡前和空
腹饮用,胃功能较差的人不适宜多喝。最适饮用时间为秋天,其冲泡
毕业论文作者签名:
签字日期: 年 月 日
..
毕业论文版权使用授权书
本毕业论文作者完全了解青海民族大学有关保留、使用毕业论文 的规定。特授权青海民族大学可以将毕业论文的全部或部分内容编入 有关数据库进行检索,并采用影印、缩印或扫描等复制手段保存、汇 编以供查阅和借阅。同意学校向国家有关部门或机构送交论文的复印 件和磁盘。
1.2 茶叶的茶种、产地及功效和口感
1.2.1 茶叶种类、产地
茶叶名称
茶叶种类
产地
..
金骏眉 红茶 普洱 茯茶 铁观音 大红袍 碧螺春 龙井 信阳毛尖 云雾绿茶 黄山毛峰 茉莉花茶
红茶 发酵茶 黑茶 黑茶 乌龙茶 乌龙茶 绿茶 绿茶 绿茶 绿茶 绿茶 花茶
福建武夷山 福建安溪 云南 江苏苏州 福建武夷山 浙江 陕西 浙江 河南 湖南 福建武夷山 安徽黄山
吸管和连接管。索氏提取器是利用溶剂回流和虹吸原理,使固体物质
每一次都能为纯的溶剂所萃取,所以萃取效率较高。萃取前应先将茶
叶研磨细,以增加乙醇浸溶的面积。然后将茶叶末放在滤纸套内,放
置于提取器中。当乙醇加热沸腾后,蒸汽通过导气管上升,被冷凝为
液体滴入提取器中。当液面超过虹吸管最高处时,即发生虹吸现象,
..
..
引言
茶叶中含咖啡因虽然较低,但因我国是产茶大国,并有悠久的历
史,所以资源丰富。具有关资料报道,茶叶中咖啡因的质量分数约为
1%~4%。多年来,一直有人用不同方法从茶叶中提取天然咖啡因,主
要方法有溶剂萃取法和升华法两大类。
本文利用索氏提取法从不同种类的茶叶中提取咖啡因,索氏提取
器是由提取瓶、提取管、冷凝器三部分组成的。提取管两侧分别有虹
..
青海民族大学
毕业论文(设计)
论文题目:
几种茶叶中咖啡因含量的测定
学生姓名: 隆学庆
学号:0904040006
指导教师: 杨尚梅
职称:
院 系:
化学与生命科学学院化学系
专业班级:
10 化学师范
二○一四年四月二十二日
..
独创性声明
本人声明所呈交的毕业论文是本人在导师指导下进行的理论学 习、实习实践以及研究所取得的成果,除了文中特别加以标注和致谢 之处外,论文中不包含其他人已经发表或撰写过的研究成果,也不包 含获得青海民族大学或其他教育机构的学位或证书而使用过的材料。 与我一起探讨、工作的同学对本论文所做的任何贡献均已在论文中作 了明确的说明并表示了谢意。
..
目录
引言............................................................................................................................ 1 一、茶叶的背景及主要成分: .......................................................................... 1 1.1 茶叶的背景 ....................................................................................................... 1 1.2 茶叶的茶种、产地及功效和口感 ............................................................... 1 1.2.1 茶叶种类、产地 ........................................................................................... 1 1.2.2 功效及口感 .................................................................................................... 2 1.3 主要成分............................................................................................................ 4 二、茶叶中提取咖啡因的背景、历史 ............................................................. 4 2.1 背景、历史 ....................................................................................................... 4 2.2 咖啡因的用途................................................................................................... 5 四、实验内容.......................................................................................................... 6 4.1 实验原理............................................................................................................ 6 4.2 试剂、仪器 ....................................................................................................... 6 4.2.1 试剂.................................................................................................................. 6 4.2.2 仪器.................................................................................................................. 7 4.3 实验步骤............................................................................................................ 7 五、实验结果及讨论 ............................................................................................ 9 六、综述................................................................................................................... 9 七、结语 ................................................................................................................. 10 参考文献: ............................................................................................................10 致谢 .......................................................................................................................... 11
