食品添加剂对羟基
常用食品防腐剂

常用食品防腐剂集团标准化工作小组 #Q8QGGQT-GX8G08Q8-GNQGJ8-MHHGN#常用食品防腐剂1、苯甲酸和苯甲酸钠苯甲酸又名安息香酸,是各国允许使用而且历史比较悠久的食品防腐剂。
苯甲酸为白色鳞片状或针状结晶,难溶于水,易溶于乙醇。
苯甲酸钠易溶于水,生产上使用较为广泛。
苯甲酸和苯甲酸钠在酸性条件下,以未解离的分子起抑菌作用,其防腐效果视介质的PH而异,一般PH<5时抑菌效果较好,~时抑菌效果最好。
例如,当PH由7降至时,其防腐效力可提高5~10倍。
FAO(联合国粮农组织)和WHO(世界卫生组织)1994年规定,苯甲酸的ADI(每日允许摄入量)为0~5mg/kg。
根据我国食品添加剂使用卫生标准(GB2760-1996)规定,苯甲酸和苯甲酸钠的使用标准见表:苯甲酸与苯甲酸钠的使用标准使用苯甲酸时,先用少量乙醇溶解,再添加到食品中。
使用苯甲酸钠时,一般先配制成20%~30%的水溶液,再加入到食品中,搅拌均匀即可。
2、山梨酸和山梨酸钾山梨酸又名花楸酸,为无色针状或白色粉末状结晶,无臭或稍有刺臭,耐光耐热,但在空气中长期放置易被氧化变色,防腐效果也有所降低。
山梨酸难溶于水而易溶于乙醇等有机溶剂。
山梨酸钾极易溶于水,也易溶于高浓度蔗糖和食盐溶液,因而在生产上被广泛使用。
山梨酸是一种不饱和脂肪酸,能在人体内参与正常的代谢活动,最后被氧化成二氧化碳和水,故国际上公认其为无害的食品防腐剂。
山梨酸的ADI为0~kg(FAO/WHO,1994)。
山梨酸和山梨酸钾属于酸型防腐剂,以未解离的分子起抑菌作用,其防腐效果随PH降低而增强,但适宜的PH范围比苯甲酸广,以PH<6的介质中使用未宜。
根据我国食品添加剂使用卫生规定(GB2760-1996)规定,山梨酸与山梨酸钾的使用标准如下:使用山梨酸时,应先将其溶解在少量乙醇或碳酸氢钠、碳酸氢钾的溶液中,随后添加到食品中。
为了防止山梨酸受热挥发,最好在食品加热过程后期添加。
食品添加剂与安全2.

增味剂
能赋于食品鲜味、增强食品风味的食品添加 剂。除食盐外,是人类耗用最大的一类调味 料。其中谷氨酸钠是味精的主要成分,核苷 酸类具有特别强的增味作用。
主要有:谷氨酸钠、 5'-肌苷酸二钠, 5'-鸟 苷酸钠, 酵母抽提物
应用于方便 面调料包、 调味品等
面粉处理剂
能改善面粉及其制品组织质量的添加剂。
苯甲酸及其钠盐:苯甲酸又名安息香酸。由于其在水
中溶解度低,故多使用其钠盐。成本低廉。苯甲酸进
入机体后,大部分在9~15小时内与甘氨酸化合成马尿
酸而从尿中排出,剩余部分与葡萄糖醛酸结合而解毒。
山梨酸及其盐类:又名花楸酸。由于在水中的
溶解度有限,故常使用其钾盐。山梨酸是一种
不饱和脂肪酸,可参与机体的正常代谢过程,
应用于面包、 糕点、油条、 膨化食品等
护色剂
又称发色剂,能与食品中某些成分作用, 致食品有良好色泽的食品添加剂。
主要有硝酸钠 和亚硝酸钠
应用于肉 类腌制
作用机理 (1)协同作用:一种防腐剂抑菌效果是有限的,当二 种以上的防腐剂共同应用时 ,其抑菌效果会大大增 强。 (2)增效作用:食品中的一些成分本身无抑菌作用, 但它们却能增强或削弱防腐剂的抑菌能力,如柠檬酸 、葡萄糖酸、Vc等 。 (3)拮抗作用:降低防腐剂的抑菌能力如CaCl2。
⑵还原性漂白剂: 这是我国主要应用的品种,主要是亚硫酸盐类, 它们可以防止食品在空气中因氧化而产生颜色,尤其 是褐变的颜色。但由于属于还原性漂白,故此时间久 长又会因氧化而呈色。 亚硫酸盐在食品中有多种作用,主要有:
1.抗氧化作用:
亚硫酸盐具有还原性,可以同食品中的O2和H2O2反应 SO32-+O2→SO42- H2O2+SO32-→SO42- +H2O 它有效地防止食品中Vc氧化,故此有利于Vc的保留:
对羟基苯甲醛

对羟基苯甲醛的合成技术[摘要]本文介绍了对羟基苯甲醛的一些性质及应用,并讲述其应用发展。
叙述了对羟基苯甲醛的合成方法与技术,并对方法的优缺点作了简要对比。
其合成方法较多,以苯酚、对氨基苯甲醛、对硝基甲苯和对甲酚为原料均可合成对羟基苯甲醛。
本文对其合成方法进行了探讨,当反应时间为6h,碱用量140g,反应压力19.6~24.5Pa为最佳。
[关键词]对羟基苯甲醛;应用;发展;合成;Synthesis of p-hydroxybenzaldehydeAbstract:This paper introduces some properties of hydroxyl benzene formaldehyde and its application, and describes its application and development. Narrated on the synthesis methods and technology, and the advantages and disadvantages of the methods are compared briefly. The synthesis method is more, phenol, amino benzaldehyde, p-nitrotoluene and p-cresol as raw material can be the synthesis of p-hydroxybenzaldehyde. In this paper, the synthesis method is discussed, when the reaction time was 6h,140g alkali dosage, reaction pressure is 19.6 ~24.5Pa is the best.Key words:P-hydroxybenzaldehyde; application; development; synthesis一、绪论1.1 对羟基苯甲醛的主要性质对羟基苯甲醛又称对甲醛苯酚,4一羟基苯甲醛(简称PHBA),分子式CH6O2,为白色结晶性粉末,有芳香味。
调味品食品安全风险清单和措施清单

调味品食品安全风险清单和措施清单1. 酱油(1)风险隐患因素①真菌毒素:黄曲霉毒素B1限量超标;②质量指标:氨基酸态氮不合格;③微生物:菌落总数、大肠菌群限量超标;④食品添加剂:超限量使用苯甲酸、对羟基苯甲酸酯等防腐剂;同一功能的防腐剂混合使用时,各自用量占其最大使用量的比例之和超过1;⑤非法添加:无完整酿造工艺,以配制法代替酿造工艺,使用香精勾兑代替酿造酱油,非法添加植物水解蛋白、三氯丙醇等物质。
(2)原因分析①进货查验控制不严格,原料存储条件不符合要求;②生产过程中发酵条件不符合要求,原料中蛋白质转化率不足;③生产过程灭菌工序控制不严格;④配方管理、配料环节控制不严格;⑤食品安全管理人员培训不到位;⑥出厂检验落实不到位。
(3)防控措施①严格执行原料进货查验制度,结合企业原料特性开展快速检测;加强原料仓储条件控制,严格落实仓储管理要求;②严格控制发酵工序的发酵条件,确保氨基酸态氮的质量控制符合要求;③严格落实生产工艺,保证灭菌工序执行到位;④加强配方管理,严格落实配料工序质量控制;⑤加强食品生产企业法律法规及标准培训;⑥严格落实出厂检验制度,保证出厂产品质量。
2. 食醋(1)风险隐患因素①微生物:菌落总数、大肠菌群限量超标;②质量指标:总酸不合格;③食品添加剂:超限量使用苯甲酸、对羟基苯甲酸酯等防腐剂;同一功能的防腐剂混合使用时,各自用量占其最大使用量的比例之和超过1;超范围使用冰乙酸等酸度调节剂;④非法添加:无完整酿造工艺,以配制法代替酿造工艺,使用香精勾兑代替酿造食醋,非法添加工业用乙酸等物质。
(2)原因分析①生产过程灭菌工序控制不严格;②生产过程中发酵条件不符合要求;③贮运环节控制不严格;④配方管理、配料环节控制不严格;⑤食品安全管理人员培训不到位;⑥出厂检验落实不到位。
(3)防控措施①严格落实生产工艺,保证灭菌工序执行到位;②严格控制发酵工序的发酵条件,确保总酸的质量控制符合要求;③加强贮运管理制度的执行,严格落实贮运管理要求;④加强配方管理,严格落实配料工序质量控制;⑤加强食品生产企业法律法规及标准培训;⑥严格落实出厂检验制度,保证出厂产品质量。
常见的食品添加剂

其实,目前除了纯奶没有添加剂(过去也有,现 在国家规定不让加了),花色口味的牛奶(或奶 饮料)都要添加的。许多产品的特性决定了它必 须要添加剂才能做出来的。纯牛奶本身是相对稳 定的一个体系,在添加了其它辅料后,就有可能 破坏这种稳定,所以一定要添加剂来维持这个稳 定体系的。 举例来说,常见的种酸味奶饮料。牛奶遇酸,蛋 白就会沉淀的(PH=4.3~4.6),而想要它不沉 淀,只有加入一些胶体保护蛋白,才能重新形成 一个稳定体系。
文章指出,在美国,美国食品药物管理局公布的 食品添加剂就达3000多种。不过庆幸的是,大多 数食品添加剂都是健康的,只有少数有潜在的危 害。 文章称,这些添加剂都藏身于食物中,就算你不 信它们对人体有害,但至少承认,减少这种添加 成分更健康。
前五名上榜最恐怖添加剂
1、蔗糖聚酯
宝洁公司推出含有这种物质的“零脂肪”薯片的 时候,商标上必须要有警告信息,提示消费者可 能有拉肚子危险
副作用:木糖醇不会被胃里的酶分解,直接进入肠 道,吃多了对胃肠有一定刺激。由于木糖醇在肠 道内吸收率不到20%,易在肠壁积累,造成腹泻。 被膜剂(防腐剂) 可防止微生物入侵,抑制水分蒸发或吸收和调节 食物呼吸作用。
常见的食品添加剂
防腐剂:山梨酸、山梨酸钾、苯甲酸、苯甲酸 钠、二氧化硫、丙酸钙、丙酸钠、尼泊尔金乙 酯、尼泊尔金丙酯、对羟基苯、脱氢醋酸等抗 氧化剂:BHA、BHT、没食子酸、异抗坏血 酸等 发色剂:硝酸钠、亚硝酸钠 品质改良剂:磷 酸三钠、三聚磷酸钠、磷酸二氢钠、六偏磷酸 钠、焦磷酸钠等 乳化剂:蔗糖脂肪酸酯、SP60、田青胶等
氢化植物油:有导致心脏病的风险。
亚硫酸盐类:或致呼吸困难。
偶氮甲酰胺:用于发泡剂,改善面团的弹性、韧 性,或致哮喘。 角叉菜胶:动物实验显示,可能和癌、结肠癌和 溃疡相关。
(整理)尼泊金酯系列

尼泊金酯系列(对羟基苯甲酸酯系列)尼泊金酯,化学名称:对羟基苯甲酸酯。
尼泊金酯为无色或白色结晶状粉末。
在水中溶解度小,溶于乙醇和丙二醇。
对霉菌和酵母菌有特别强的抑制作用,对细菌特别是革兰氏阴性菌效果稍差。
本品抗微生物作用比苯甲酸、山梨酸强,抑菌作用随酯基中R碳链的增长而增大,但水溶性则减少。
丙酯的抑菌作用几乎为乙酯的4—5倍。
将乙酯和丙酯配合使用时,不仅可提高溶解度,且有增效防腐作用。
因尼泊金酯属酯类,中性防腐剂,不受酸碱性影响,化学性质相当稳定。
在PH=4–8范围内抑菌效果较好。
尼泊金酯的毒性较低,安全性好。
尼泊金酯系列是目前世界上应用领域最广、用量最大、使用频率最高的防腐剂系列。
广泛应用于医药、食品、啤酒、饮料、烟草、饲料、化妆品、清洁剂、纺织、造纸、涂料等工业领域。
在医药方面:主要用于琼酯乳剂、生物溶液、油膏、浸膏、激素、乳油、注射乳液、鱼肝油乳剂、防腐漱口液、栓剂、酊剂、洗剂、软膏、口腔用剂、擦剂、糖浆等。
用量为0.01%—0.5%。
在化妆品方面:主要用于洗面奶、膏剂、霜剂、洗发剂、凝胶剂、护肤乳剂、脂剂、唇膏、漱口药、保健粉、消毒粉、牙膏、除臭剂及各种护肤护发用品。
用量为0.01%—0.5%。
在食品方面:主要用作食品添加剂、降腐剂、用于冰淇淋、火腿肠、色拉、黄酱、果汁、蜜饯、水果及蔬菜汁、调味品、乳酪、啤酒、饮料等。
还用于烟草防腐。
按我国食品添加剂卫生标准,其最大允许用量为尼泊金乙酯0.1g/kg、丙酯0.012g/kg。
尼泊金酯还应用于饲料添加剂,起防腐保鲜的作用。
其无影响的添加量为2%。
尼泊金酯还用于热敏记录纸张中的显色剂;涂料、粘合剂的杀菌防腐剂,感光胶片的防腐剂;纺织、淀粉糊等水溶性制品的抑菌剂。
本公司尼泊金酯系列产品有甲、乙、丙酯、异丙酯等。
质量标准执行国标。
防腐剂(食品添加剂)编辑词条发表评论(0)防腐剂是指能抑制食品中微生物的繁殖,防止食品腐败变质,延长食品保存期的物质。
常用食品防腐剂
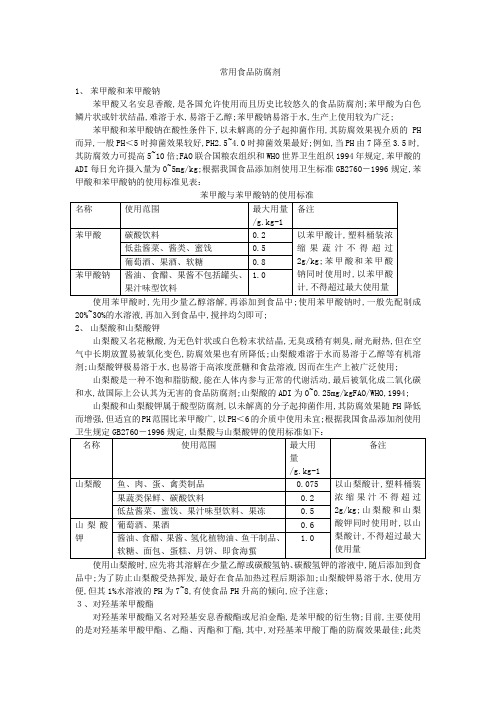
常用食品防腐剂1、苯甲酸和苯甲酸钠苯甲酸又名安息香酸,是各国允许使用而且历史比较悠久的食品防腐剂;苯甲酸为白色鳞片状或针状结晶,难溶于水,易溶于乙醇;苯甲酸钠易溶于水,生产上使用较为广泛;苯甲酸和苯甲酸钠在酸性条件下,以未解离的分子起抑菌作用,其防腐效果视介质的PH 而异,一般PH<5时抑菌效果较好,PH2.5~4.0时抑菌效果最好;例如,当PH由7降至3.5时,其防腐效力可提高5~10倍;FAO联合国粮农组织和WHO世界卫生组织1994年规定,苯甲酸的ADI每日允许摄入量为0~5mg/kg;根据我国食品添加剂使用卫生标准GB2760-1996规定,苯甲酸和苯甲酸钠的使用标准见表:苯甲酸与苯甲酸钠的使用标准20%~30%的水溶液,再加入到食品中,搅拌均匀即可;2、山梨酸和山梨酸钾山梨酸又名花楸酸,为无色针状或白色粉末状结晶,无臭或稍有刺臭,耐光耐热,但在空气中长期放置易被氧化变色,防腐效果也有所降低;山梨酸难溶于水而易溶于乙醇等有机溶剂;山梨酸钾极易溶于水,也易溶于高浓度蔗糖和食盐溶液,因而在生产上被广泛使用;山梨酸是一种不饱和脂肪酸,能在人体内参与正常的代谢活动,最后被氧化成二氧化碳和水,故国际上公认其为无害的食品防腐剂;山梨酸的ADI为0~0.25mg/kgFAO/WHO,1994;山梨酸和山梨酸钾属于酸型防腐剂,以未解离的分子起抑菌作用,其防腐效果随PH降低而增强,但适宜的PH范围比苯甲酸广,以PH<6的介质中使用未宜;根据我国食品添加剂使用品中;为了防止山梨酸受热挥发,最好在食品加热过程后期添加;山梨酸钾易溶于水,使用方便,但其1%水溶液的PH为7~8,有使食品PH升高的倾向,应予注意;3、对羟基苯甲酸酯对羟基苯甲酸酯又名对羟基安息香酸酯或尼泊金酯,是苯甲酸的衍生物;目前,主要使用的是对羟基苯甲酸甲酯、乙酯、丙酯和丁酯,其中,对羟基苯甲酸丁酯的防腐效果最佳;此类物质为无色小结晶或白色结晶性粉末,五臭,开始无味,随后稍有涩味,难溶于水而易溶于乙醇、丙酮等有机溶剂;对羟基苯甲酸酯也是由未解离分子发挥抑菌作用,其效力强于苯甲酸和山梨酸,而且使用范围更广,一般在PH为4~8范围内效果较好;对羟基苯甲酸酯在人体内的代谢途径与苯甲酸酯基本相同,且毒性比苯甲酸低;毒性与烷基链的长短有关,烷基链短者毒性大,故对羟基苯甲酸甲酯很少作为食品防腐剂使用;对羟基苯甲酸酯在世界各国普遍使用,通常用于碳酸饮料、果酱、食醋等,其ADI为0~10mg/kgFAO/WHO,1994;根据我国食品添加剂使用卫生标准GB2760-1996规定,对羟基苯甲酯类防腐剂使用标准如下对羟基苯甲酸酯类在水中溶解度小,通常都是将其配置成氢氧化钠溶液、乙醇溶液或醋酸溶液使用;4.丙酸盐作为食品防腐剂使用的丙酸盐通常是丙酸钠和丙酸钙,两者均为白色的结晶颗粒或结晶性粉末,无臭或有异臭,易溶于水;丙酸盐属酸性防腐剂,在PH较低的介质中抑菌作用强,例如,最低抑菌浓度在PH5.0时为0.01%,在PH6.5时为0.5%;丙酸盐对霉菌,需氧芽孢杆菌或革兰氏阴性杆菌有较强的抑菌作用,对引起食品发粘的菌类如枯草杆菌抑菌效果好,对防止黄曲霉毒素的产生有特效,但是对酵母菌几乎没效;根据这一特性,丙酸盐常用于面包和糕点的防霉;丙酸是食品中的正常成分,也是人体代谢的中间产物,丙酸盐不存在毒性问题,故ADI无需做特殊规定;丙酸已广泛用于面包、糕点、果冻、酱油、醋、豆制品等的防霉;在以上食品中;丙酸盐以丙酸计算的最大使用量为2.5g/kg;丙酸钠用于加工干酪,最大使用量为3g/kg;在面包和西式糕点制造中,丙酸钠的最大使用量低于2.5g/kg,面包发泡稍差些;5、脱氢醋酸和脱氢醋酸钠脱氢醋酸为无色到白色针状或片状结晶,无臭或有微臭,易溶于乙醇等有机溶剂而难溶于水,故多用其钠盐作防腐剂;脱氢醋酸钠为白色结晶性粉末,在水中的溶解度可达到33%;脱氢醋酸和脱氢醋酸钠是毒性很低、对热较稳定的防腐剂,适应的PH范围较宽,但以酸性介质中的抑菌效果更好;我国规定脱氢醋酸可用于腐乳、什锦菜、原汁橘浆,最大用量为0.30g/kg;国外各种食品的最大用量为:干酪、奶油、人造奶油2g/kg,清凉饮料0.05g/kg,乳酸和乳酸饮料0.2g/kg;脱氢醋酸钠为乳制品的主要防腐剂,常用于干酪、奶油和人造奶油,使用量为0.61g/kg 以下;使用时一般是将0.1%~0.2%的水溶液喷洒在制品表面或包装材料上,喷洒量为20~40ml/kg;6、天然防腐剂天然防腐剂一般是指从动植物体中直接分离出来的,或从它们的代谢物中分离的具体防腐作用的一类物质;这些物质阿安全性较好,能满足人们对食品越来越高的要求;开发这类防腐剂将成为今后食品添加剂开发研究的热点;1乳球菌肽乳酸链球菌素又称乳酸菌肽,是由乳酸链球菌产生的一种多肽物质,商品名称为乳酸链球菌制剂,由乙醇结晶制得;该产品对革兰氏阳性菌有抑菌作用,可用于乳制品和肉制品得抑菌防腐;对革兰氏阴性菌、霉菌和酵母菌一般无抑制作用;乳酸链球菌素的安全性高,ADI为33000IU/kgFAO/WHO,1994;用于罐装食品、植物蛋白食品防腐的最大用量为0.2g/kg,乳制品和肉制品的最大用量为0.5g/kg.2香辛料提取物许多食用香辛料含有杀菌、抑菌成分;因此,近年来有研究从香辛料中提取有效成分作为食品防腐剂;这些物质一般都既安全又有效;使用最多的是大蒜素;大蒜属百合科植物,具有很强的杀菌、抑菌能力;大蒜的食疗作用早已被人们所认识,它可以治疗肠胃病、肺病、感冒等病症;大蒜起杀菌、抑菌作用的主要成分是蒜辣素和蒜氨酸;蒜辣素具有不愉快的臭气,而蒜氨酸则无味;因此,蒜氨蒜适合作为食品防腐剂;在提取制备蒜氨酸时,应先加热杀死蒜酶,防止蒜氨酸转化为蒜辣素;此外,丁香中所含的丁香油、肉豆蔻中所含的肉豆蔻油及芥子油均具有杀菌、抑菌作用,但是由于多数具有辛辣味,没有被作为食品防腐剂大量使用;。
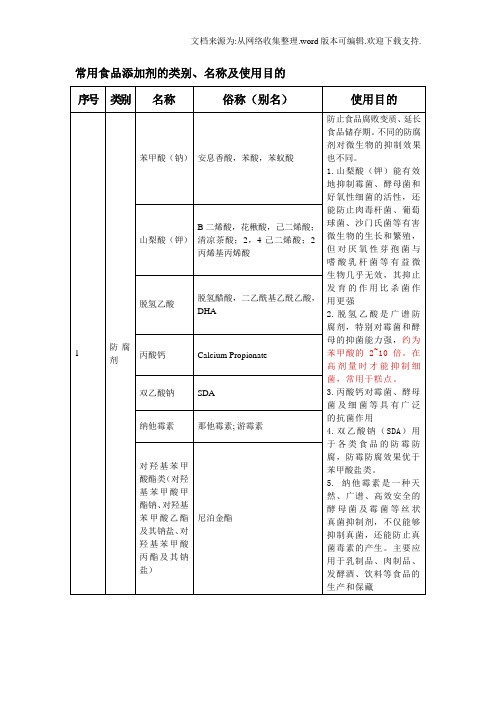
常用食品添加剂的类别、名称及使用目的
PG
6
护色剂
亚硝酸钠(钾)
亚硝酸盐,硝盐(民间俗称)
与肉制品中肌红蛋白、血红蛋白生成鲜艳、亮红色的亚硝基肌红蛋白或亚硝基血红蛋白而护色,并可使腌肉产生特殊的风味
硝酸钠(钾)
智利硝,智利硝石
7
膨松剂
硫酸铝钾
钾明矾,白矾
能使产品发起并形成致密多孔组织,从而使制品膨松、柔软或酥脆
硫酸铝铵
铵明矾,铵矾;铝铵矾
二氧化硫
SO2
焦亚硫酸钠
偏重亚硫酸钠;重硫氧;焦性亚硫酸钠;偏亚硫酸钠
焦亚硫酸钾
偏亚硫酸钾
亚硫酸钠
sodium sulfite
亚硫酸氢钠
酸式亚硫酸钠
硫磺
硫磺,S
4
着色剂
胭脂红
1-(4-磺酸-1-萘偶氮)-2-羟基-6,8-萘二磺酸三钠盐,胭脂,1-(4′-磺基-1′-偶氮苯)-2-萘酚-6,8-二磺酸三钠盐,C.I.食用色素红色7,C.I.酸性红18;丽春红4R;食用胭脂油;新胭脂虫红,胭脂虫,洋红酸,胭脂虫红铝,胭脂虫(洋)红,胭脂红
2.脱氢乙酸是广谱防腐剂,特别对霉菌和酵母的抑菌能力强,约为苯甲酸的2~10倍。在高剂量时才能抑制细菌,常用于糕点。
3.丙酸钙对霉菌、酵母菌及细菌等具有广泛的抗菌作用
4.双乙酸钠(SDA)用于各类食品的防霉防腐,防霉防腐效果优于苯甲酸盐类。
5.纳他霉素是一种天然、广谱、高效安全的酵母菌及霉菌等丝状真菌抑制剂,不仅能够抑制真菌,还能防止真菌毒素的产生。主要应用于乳制品、肉制品、发酵酒、饮料等食品的生产和保藏
山梨酸(பைடு நூலகம்)
B二烯酸,花楸酸,己二烯酸;清凉茶酸;2,4-己二烯酸;2-丙烯基丙烯酸
食品中常见的添加剂与有害物质

甜味剂
2.甜蜜素环己基氨基磺酸钠)
易溶于水,水溶液呈中性,几乎不溶于乙醇等有机溶剂,对酸、碱、光、 热稳定。甜味好,后苦味比糖精低。但甜度不高,约为蔗糖的40~50倍,因此用 量大,容易超标使用。甜蜜素自面世以来对人体是否有害一直存在争议,如加拿 大、东南亚、日本等国禁止作为食品添加剂使用,我国对甜蜜素的使用也有严格 的规定,凉果类、果丹(饼)类≤8.0g/kg,糕点、配制酒、饮料等≤0.65g/kg。
还原型漂白剂大多属于亚硫酸及其盐类化合物,主要包括亚硫酸钠(Na2SO3)、亚硫酸 氢钠(NaHSO3)、低亚硫酸钠又名保险粉(Na2S2O4)、焦亚硫酸钠(Na2S2O5)和硫 磺燃烧生成的二氧化硫。安全性问题表现在可诱发过敏性疾病和哮喘,破坏维生素B1.
漂白剂
2011年,卫生部、工业和信息化部、商务部、国家工商总局、国家质检总局、 国家粮食局、国家食品药品监管局联合发布《关于撤销食品添加剂过氧化苯甲酰 、过氧化钙的公告》。 《公告》指出,根据《食品安全法》关于食品添加剂应当在技术上确有必要且经 过风险评估证明安全可靠,方可列入允许使用范围的规定,经审查,食品添加剂 过氧化苯甲酰、过氧化钙已无技术上的必要性,现决定予以撤销。
漂白剂
漂白剂(bleaching agent)是指能够破坏或抑制食品的发色因素,使其转变为无色或使食 品免于褐变的一类物质。根据作用原理可以分为氧化型漂白剂和还原型漂白剂两大类。
氧化型漂白剂能使着色物质氧化分解而漂白的漂白剂。常用的有过氧化氢、过氧化钙、过
氧化苯甲酮、过氧化苯甲酰等。缺点:不但能使β-胡萝卜素褪色,同事破坏维生素A,E,B1.
防腐剂
酸型防腐剂:常用的有苯甲酸(钠)、山梨酸(钾)、丙酸(及其盐类)。抑菌效果主要 取决于他们未解离的酸分子,其效力随pH值而定,酸性越强效果越好,而在碱性中几乎无 效。
食品添加剂对羟基苯甲酸丙脂

010 — 每毫摩C 1 : 2 .8 1 2 的质量,9。 o 0 H 取其 值为报告结果,平行测定两个结果之差不得大于 .%. 算术平均 02
23 熔点的测定 . 按G 6 -7 熔点测定法》进行。 7 7《 B 1 24 酸度的测定 . 241 试剂和溶液 ..
凡 = m - 2、0 ....・・・・・… ( ) 一 l 1 ...・・・・・… 2 m 0 ...・・・・・ ...・・・ ・・
式中: l 干 称量瓶与样品总质量, m— 燥前 9, m — 干燥后称量瓶与样 2 品总质量, , 9 m— 一 3 干 燥前样品质量, 0 9 取算术平均 值作为报告结果。 2 灼烧残渣的测定 二
溶液 (... )振摇混合,取水层用乙醚洗两次,每次2m 261 2 01 ,然后加5 l m 硫酸溶液 (...)及 261 3 3 1 0 乙醚再振摇,取出乙醚层,将乙醚层加Im 水,轻轻振摇混合,除去水层,过滤。用少量的乙 m Ol 醚洗涤容器和滤纸。洗液和滤液合并, 置蒸发皿里,在水浴上 使乙醚蒸发,再在盛有硫酸的干 燥器中 于 燥至恒重,其残留物的质量应不 超过5 m g,把这些残留物溶于2m 51 水中,在约7℃加热过滤,取 0
民 口 口 / NN 7 J 9 4 r
GB 二 51 二 一
一 ’
对 轻 基 苯 甲酸丙 醋
Fo d d ii e o a d tv
2 滴甲基红指示液 (...),用氢氧化钠标准溶液 (...)滴至黄色,消耗氢氧化钠溶液不 2411 241 2
GB 6 一二 8 51
得超过02 , . 。 m
Y与 硫酸盐的侧定 . 251 试剂和溶液 .. 2511 盐酸 ( B 2 7 ... G 6 -7): 1+3 2 溶液,
高效液相色谱法测定食品中的对羟基苯甲酸酯类

l i q u i d c h r o ma t o g r a p h y ,wi t h TC - C1 8 c o l u mn ( 4 . 6× 2 5 0 mm , 5 m),b y Me OH/ Hz 0( 7 O:3 0 ) , f l o w r a t e o f 0 . 8 mL / mi n .W a v e l e n g t h o f 2 5 5 n m ,c o l u mn t e mp r e t u r e o f 3 0 ℃ wi t h Ph o t o d i o d e Ar r a y De —
关键 词 : 高效液相 色谱 法 ; 食 品 ;对羟基 苯 甲酸 酯
中图分 类 号 : TS 2 0 1 . 1
文 献标识 码 : A
d o i : 1 0 . 3 9 6 9 / j . i s s n . 1 0 0 O 一9 9 7 3 . 2 0 1 3 . 0 2 . 0 2 4
t e c t o r .Re c o v e r y o f p - h y d r o x y b e n z o i c a c i d e s t e r s i s 8 4 ~1 0 3 . Th e me t h o d i s s i mp l e a n d o f h i g h
文 章编 号 : 1 O 0 O 一9 9 7 3 ( 2 0 1 3 ) 0 2 -0 0 8 7 —0 2
Det er mi n a t i o n o f P — Hy dr O x y b en z Oi C Aci d Es t er s i n F o o d b y HPL C
1 . 1 仪器 设备
1 2 0 0液 相 色谱 仪 带 二 极 管 阵列 检 测 器 Ag i l e n t ;
关于对羟基苯甲酸的毕业设计

1 绪论1.1 概述对羟基苯甲酸(para-Hgdroxybenzoic acid)分子式C7H6O2,分子量为138.12,结构式HO COOH,它是一种白色针状晶体或粉末晶体,无味无臭,口尝时有麻舌感。
熔点为214~217℃,密度(20℃)为1.497g/cm3,燃烧热为3031kJ/mol。
本品易溶于热水和醇、醚、丙酮,微溶于冷水、苯和氯仿,不溶于二硫化碳。
本品在熔点以上温度分解为苯酚和二氧化碳[1]。
对羟基苯甲酸主要用于工业合成尼泊金酯类即对羟基苯甲酸酯类,作为食品、医药和化妆品的防腐剂,也是有机合成、染料和合成杀真菌剂的中间体。
具有广泛用途的新型耐高温聚合物对羟基苯甲酸类聚酯也以此为基础原料。
近年来,发展了一种线型对羟基苯甲酸聚合物,该聚合物在325℃以上温度暴露于空气中具有长久的稳定性[2]。
此外,该聚合物具有自身润滑特性,并且与其他聚合物相比具有较高的弹性模数、导热性、电绝缘性和耐溶剂性能。
1.2 国内外生产和发展状况1.2.1 国外情况世界上生产对羟基苯甲酸最大的厂家是日本的上野制药公司,年生产能力为8000吨,还有三井、东亚公司和吉富制药公司,合计生产能力为9500吨/年。
欧美生产对羟基苯甲酸的只有德拜耳公司一家,其能力不足1000吨/年。
英国的尼帕公司生产量为20~25吨/年。
在用途与需求方面,日本1976年对羟基苯甲酸的需求量为4000吨,主要用作防腐剂、杀菌消毒剂,广泛用于化妆品、食品添加剂、医药和某些工业部门[3]。
1.2.2 国内情况经过多年研发与生产,我国目前已经成为世界对羟基苯甲酸主要生产和供应国。
我国自20世纪80年代初开始研发与生产对羟基苯甲酸,近10年来年产能力快速增加,由1995年的5000吨增加到2002年的1.5万吨,生产厂家近20家[3]。
1978年,广东省番禺农药厂和浙江省宁波市鄞县农药厂建立了PHBA生产装置,主要用于生产杀螟腈农药。
但由于收率低和技术等问题,我国PHBA产品发展较慢,直到1987年以后,为了适应引进国外食品、医药和化妆品生产技术和设备的配套要求,沈阳化工研究院加速研究PHBA,并在国家科研管理部门立项,生产技术/工艺得到改进,并分别在浙江省、江苏省、吉林省和上海市等地建立了生产装置。
食品添加剂答案~~

"食品添加剂"复习题第一章绪言一、名词解释1、食品添加剂〔GB2760定义〕:为改善食品品质和色、香、味,以及为防腐、保鲜和加工工艺的需要而参加食品中中的化学合成或者天然物质。
2、最大无作用量〔MNL〕是指动物长期摄入该受试物而无任何中毒表现的每日最大摄入量3、每日允许摄入量〔ADI〕是指终人或动物每日摄入*种化学物质〔食品添加剂、农药等等〕,对安康无任何不良效应的剂量。
4、残留量是物质在成品材料或物品中的最大的允许残留数量,以在与食品接触的每 6平方分米的外表含 1毫克表示。
二、填空题1、一个食品添加剂的代码用5位数字表示。
前两位数字表示该食品添加剂所属的_类目标识__,后三位数字表示该食品添加剂的类目中的编码代号。
2、.毒理学试验通常分为急性毒性试验、遗传毒性试验、亚慢性毒性试验、慢性毒性试验四个阶段。
三、单项选择题1、每一个食品添加剂的代码用5位数字表示。
前两位数字表示〔 A 〕A 该食品添加剂所属的类; B该食品添加剂的;C该食品添加剂的最大使用量;3、食品用香料是按照香料名称的汉字笔画顺序编排的,用三位数字表示,数字前分别冠以英文字母,表示该香料的来源,则在香料的名称前冠以N表示该香料是〔 A〕A 天然香料; B天然等同香料; C人工合成香料;四、多项选择题1、食品添加剂的作用包括〔ABC〕A提高食品的保藏性、防止腐败变质; B改善食品的感观性状;C保持或提高食品的营养价值;D便于食品加工2、对食品添加剂的要求包括〔 ABC 〕A 不应对人体产生任何安康危害; B不应掩盖食品腐败变质;C 不应掩盖食品本身或加工过程中的质量缺陷或以掺杂、掺假、伪造为目的而使用食品添加剂;D食品工业用加工助剂一般应在制成最后成品之前除去,有规定食品中残留量的除外五、简答题1、按来源食品添加剂可分为哪两类"天然食品添加剂和人工化学合成品2、"食品添加剂使用标准"〔GB2760〕对食品添加剂作了那些主要规定。
新型高效低毒食品防腐剂—对羟基苯甲酸酯钠

① 作者简介 : 杨寿清 , 男 , 江南大学食品学院 , 工学硕士 , 高级工程师 。主要从事食品加工 、食品保鲜技术和食品防腐剂 、食品保 鲜剂以及新型食品资源的开发研究 。
② 该文为 “2003 中国国际饮料科技报告会”论文 。
© 1994-2006 China Academic Journal Electronic Publishing House. All rights reserved.
·18 ·
饮料工业 Beverage Indust
ry
200316
第Vo6l1卷6 第N6o1期6
量也远比苯甲酸钠和山梨酸钾低得多 。因此 , 实际 使用安全性对羟基苯甲酸酯钠最好 , 对羟基苯甲酸 酯钠 山梨酸钾 苯甲酸钠 。事实上 , 苯甲酸钠作 为食品添加剂在许多国家受到限制 , 我国也规定 A 级绿色食品中不允许使用苯甲酸钠[6 ] 。由于对羟
干基计 , 1g 对羟基苯甲酸甲酯钠 、对羟基苯甲酸 乙酯钠 、对羟基苯甲酸丙酯钠和对羟基苯甲酸丁酯 钠分别相当于 01873g 对羟基苯甲酸甲酯 、01883g 对羟基苯甲酸乙酯 、01891g 对羟基苯甲酸丙酯和 01898g 对羟基苯甲酸丁酯 。
微生物在食品体系中仅仅出现在水相中 , 一切 与生命活动相关的酶促生化反应也均在水相中进 行 , 进入酯相的防腐剂被认为是无效的[12 ,13 ] , 防 腐剂主要是通过抑制微生物的能量代谢 , 造成能量
·19 ·
物质 A TP 和还原力 NADH 的亏缺 , 代谢方向趋于 水解 , 最后导致细胞自溶而发挥抑菌作用[12 ] 。因 此 , 防腐剂分子必须具备亲水基团才能进入水相中 的菌体中 , 与合成代谢酶系统起作用 。
微生物的生物膜系统是微生物进行能量转化 、 物质代谢等生命活动的主要场所[2 ,12 ,15 ] , 其结构 的完整性保证了细胞能量代谢及对物质选择透过性 等生命活动的正常进行 。防腐剂分子中具有易溶于 生物膜相的疏水基团动态踞留于生物膜相后 , 一方 面破坏了细胞膜结构的完整性 , 扰乱了微生物的正 常生命活动 , 另一方面生物膜中的脂溶性成分代谢 速率较低 , 不易被微生物自身的酶系分解 , 延长了 防腐剂的抑菌时间 。因此 , 防腐剂分子必须同时具 备亲水基团和易溶于生物膜相的疏水基团 。防腐剂 透过细胞壁进入菌体的能力与水相中的溶解度直接 有关 , 抑菌性则取决于防腐剂在菌体细胞膜双磷脂 层中的溶解度[15 ,16 ,17 ] 。对羟基苯甲酸酯钠的抑菌 效果与烷基酯链的长度成正比 , 说明了防腐剂分子 中疏水基团的存在可以增强抑菌效果 。如表 2 所 示 , 随着对羟基苯甲酸酯钠中 R 烷基碳链的增大 , 对羟基苯甲酸酯钠的毒性降低 , 抗菌活性增 大[17 ,18 ] , 其中 R 为 C11 、C12 的具有最大的抗菌活 性[2 ] 。这是因为 R 烷基碳链越长 , 疏水性越强 , 菌体对对羟基苯甲酸酯的吸附量也越大 , 因而抗菌 活性也越大[16 ,17 ,18 ] 。
食品添加剂和防腐剂的区别.

食品添加剂和防腐剂的区别【转载】常见防腐剂有苯甲酸钠、山梨酸钾、脱氢乙酸钠、丙酸钙、双乙酸钠、乳酸钠、对羟基苯甲酸丙酯、乳酸链球菌素、过氧化氢等。
食品添加剂跟防腐剂的区别:我国《食品卫生法》规定,食品添加剂是为改善食品品质和色、香、味,以及为防腐和加工工艺的需要而加入食品中的化学合成或天然物质。
在我国,食品营养强化剂也属于食品添加剂的范畴,是指为增强营养成分而加入食品中的天然或人工合成的属于天然营养素范围的食品添加剂。
纳入使用标准,也会根据食品添加剂的最新评价结果,将那些曾纳入食品添加剂名单的不适宜继续作为食品添加剂的品种从名单中去除。
食品防腐剂是用于防止食品因微生物引起的变质,提高食品保存性能,延长食品保质期而使用的食品添加剂.防腐剂有苯甲酸钠、山梨酸钾、脱氢乙酸钠、丙酸钙、双乙酸钠、乳酸钠、对羟基苯甲酸丙酯、乳酸链球菌素、过氧化氢等防腐剂是用于保持食品原有品质和营养价值为目的食品添加剂,它能抑制微生物的生长繁殖,防止食品腐败变质而延长保质期。
防腐剂的防腐原理,大致有如下3种:一是干扰微生物的酶系,破坏其正常的新陈代谢,抑制酶的活性。
二是使微生物的蛋白质凝固和变性,干扰其生存和繁殖。
三是改变细胞浆膜的渗透性,抑制其体内的酶类和代谢产物产物的排除,导致其失活。
谈到防腐剂,人们往往认为有害,其实在安全使用范围内,对人体是无毒副作用的。
我国防腐剂使用有严格的规定,防腐剂应符合以下标准:1.合理使用对人体无害;2.不影响消化道菌群;3.在消化道内可降解为食物的正常成分;4.不影响药物抗菌素的使用;5.对食品热处理时不产生有害成分。
我国到目前为止已批准了32种使用的食物防腐剂,其中最常用的有苯甲酸钠、山梨酸钾等。
苯甲酸钠的毒性比山梨酸钾强,而且在相同的酸度值下抑菌效力仅为山梨酸的1/3,因此许多国家逐渐用山梨酸钾。
但因苯甲酸钠价格低廉,在我国仍普遍使用,主要用于碳酸饮料和果汁饮料。
山梨酸钾抗菌力强,毒性小,可参与人体的正常代谢,转化为CO2和水。
对羟基苯甲酸乙酯

对羟基苯甲酸乙酯班级:应化三班学号:姓名:韩毅简介对羟基苯甲酸乙酯又称尼泊金乙酯,对霉菌,酵母及细菌有广泛的抗菌作用。
本品无毒性,是食品,饮料,化妆品,日用品,医药等广泛使用的有效保鲜剂和杀菌防腐剂,也是医疗器械的清洗消毒剂,同时在食品行业,生物化工和生化试验中用作消毒剂。
由于本品无毒性,欧美发达国家采用本品作消毒剂的用量不断增大,我国也在推广用本品作消毒剂。
随着人民生活水平的不断提高,使用本品作消毒剂的量也将越来越大,而目前国内生产规模和生产总量相对较小,尚不能满足市场的需求,尤其是不能满足出口的需求,市场缺口很大。
本品也是重要的有机合成原料。
目录:基本信息……………………………………………………………………1.1 性状介绍……………………………………………………………………2.1 质量标准……………………………………………………………………3.1 药理作用……………………………………………………………………4.1 作用用途……………………………………………………………………5.1 应用测定实例………………………………………………………………6.1 相关品种……………………………………………………………………7.1 生产工艺流程………………………………………………………………8.1 摘选出处……………………………………………………………………9.1 工艺流程图…………………………………………………………………10.1基本信息:【外文名】Ethyl Hydroxybenzoate, Nipagin A,Ethylparaban 【药理作用】本品对真菌的抑菌效果较强,但对细菌的抑菌效果较弱。
用作抑菌防腐剂,广泛用于液体制剂及半固体制剂,也可用于食品及化妆品的防腐。
【规格】常用浓度0.03%~0.l5%。
另0.l%滴眼剂可用于治疗真菌性角膜溃疡。
0.2%为食物防腐,0.3%为制剂防腐。
【相对分子量】166.18【熔点(℃)】116~118【沸点(℃)】297~298(分解)性状介绍:本品为白色、晶状、几乎无臭的粉末。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
HO
COOCH2CH2CH3 + R'OH
有机合成的原则:
• • • • 原料丰富、价格低廉 条件合适、操作方便 原理正确、步骤简单 产物纯净、污染物少
酯化
• 酯化反应通常是指醇或酚和含氧酸类(包 括无机和有机酸)或其衍生物作用生成酯 的过程。 • 其实质是醇或酚分子中的羟基氢原子被酰 基取代而生成酯的反应,又叫做O-酰化反 应。
用羧酸的酯化(直接酯化反应)
H RCOOH + R'OH RCOOR' + H
2O
(1)反应特点:酯化反应是可逆反浓度(一般是加过量的低级醇) b 移走低沸点的酯或水
(2) 酯化反应的活性次序: 酸相同时 CH3OH > RCH2OH > R2CHOH > R3COOH 醇相同时 HCOOH < CH3COOH <RCH2COOH <R2CHCOOH < R3CCOOH
实验步骤
• 在100mL 圆底烧瓶中加入对羟基苯甲酸用量 6.9g(0.05mol),11.2ml(0.15mol)正丙醇,4.8g(用量 为反应物总质量的30%)大孔树脂,5ml环己烷(带水剂) 和沸石充分混匀,磁力搅拌,加热分水回流三个小时(分 水器中不再生成水)冷却烧瓶、静置,将反应液用倾析法 转移至蒸馏瓶,蒸馏分离未反应的正丙醇以及环己烷,固 体催化剂留于瓶底待重复利用。将蒸馏余液倾入蒸馏水中, 用10 %的碳酸钠溶液调pH至7-8,先搅拌后静置,待固体 产物全部析出,经抽滤,洗涤,烘干至恒重,得白色晶体 状固体产品,称重,计算出尼泊金丙酯的产率。比较两种 催化剂的效率,选择最佳催化剂。
O C O C
=
=
R OH + H
O C
18
O
R'
H
+
18
R
OR’
+
H 2O
叔醇与羧酸的酯化是按烷氧键断裂进行的。
O C
=
R O H +
=
18
HO
C R '3
H
+
18
R
OCR’
3
+
H 2O
H2O中无O18,说明反应为酰氧断裂。
酯化反应历程 1°、2°醇为酰氧断裂历程,
O R C OH H
+
OH R C OH
食品添加剂对羟基苯甲酸丙酯的 合成
(酯化反应)
学习目标与要求
知识目标:掌握酯化反应的定义、分类、特点及 反应影响因素。通过知识拓展具有有机合成中的 活性中间体与酸碱理论的知识储备,并加入少量 的红外光谱的知识。 能力目标:利用所学酯化反应的知识及常见的反 应仪器和设备、组装对羟基苯甲酸丙酯的合成装 置、完成产品的合成及提纯操作,具有从事酯化 反应产品研发的职业基础能力和一定的创新能力。
产品 中间产物Ⅰ 中间产物Ⅱ ‥ ‥ ‥ 原料
综合分析法:即采用顺逆向思维方法相结 合,从两端推中间或中间推向两端。
路线分析
• 逆向分析:
HO
COOCH2CH2CH3
HO
COOH
+ HOCH2CH2CH3
• 路线一:直接酯化法
逆向分析:
HO COOR' + HOCH 路线二:酯交换法 2CH2CH3
对羟基苯甲酸丙酯的概述
对羟基苯甲酸酯类防腐剂属 于,其商品名为尼伯金 酯类,是对羟基苯甲酸与 低碳醇生成的酯。其通式 为:
ROO C OH
与传统的苯甲酸、山梨酸等防腐剂相比,对羟基苯甲酸酯类 防腐剂具有高效、低毒、易配伍、使用的pH值范围宽等 特点,是国际上采用的安全有效的抑菌剂和防腐剂,广泛 应用于食品、医药及化妆品等行业。由于具有毒性低,几 乎无味、无刺激性以及在较宽的pH值范围内能保持较好 的抗菌效果等有点,使其成为在食品加工中应用较广的食 品防腐剂。对霉菌、酵母菌的作用较强,对革兰阴性杆菌 及乳酸菌作用较差。其抗菌力比苯甲酸、山梨酸强,使用 量约为苯甲酸钠的1/10,毒性低于苯甲酸,使用范围 pH=4~8。抗菌作用随着烷基(R-)链的增长而增强。它是 无色结晶或白色结晶粉末,无味,无臭、对光和热稳定, 吸湿性极小。缺点是水溶性较差,价格较高。
1
][ H 2 O ]
1
][ R OH ]
催化剂
• ①硫酸 • 最常用的催化剂之一。 • 优点:可溶于反应体系中,反应条件较温和、催化效果好、性质稳定、 吸水性强及价格低廉等。 • 缺点(1)反应温度超过160℃,易使反应物发生磺化、碳化、聚合、 脱水生成烯烃或醚以及异构化等副反应,不饱和酸、羟基酸、甲酸、草酸和丙酮酸、碳
• 分子式: C10H12O3 • 分子结构式
HO
COOCH2CH2CH3
合成路线设计思路:
• 顺合成分析法:即正向思维方法,从已知 原料入手,找出合成所需的中间产物,逐 步推向待合成的有机物。其思维程序是 :原料 中间产物Ⅰ 中间产物Ⅱ ‥ ‥ ‥ 产品
逆合成分析法:即采用逆向思维方法,从产品入手, 逆推出合成该物质的前一步反应的物质,若该物 质不是原料,再进一步逆推出此中间产物又是如 何从另一有机物经一步反应而制得,如此至推到 题目给定的原料。
+
* R 'O H R
OH C
+
OH
* HOR'
OH
+
OH OH2 -H 2 O R C
+
O -H
+
R
C
* OR'
R
C
* OR'
* R' O
3°醇(叔醇)为烷氧断裂历程
R 3 C-OH
O `R C OH
+
+
H
+
R 3C
+
+
H 2O
O
R 3C
+
`R C
O
O
+
H
CR 3
O `R C O
+
H
3
`R
C
O-CR
合成装置
• 铁架台、加热套、三口烧瓶、分水器、球 星冷凝管、电动搅拌器、温度计等
• 仪器与试剂仪器与试剂仪器与试剂 药品试剂: 尼泊金酸、正丙醇、饱和氯化钠溶液、95%乙醇、 10 %的碳酸钠、大孔树脂,环己烷、沸石、活性 炭。 仪器:显微熔点测定仪(含载片);真空抽 滤机;磁力搅拌电热套(包括磁粒);天平;分 水回流装置(包括三口烧瓶1个,分水器一个,球 形冷凝管一个,橡胶塞一个,带塞温度计一个, 橡胶管若干);蒸馏装置(包括100ml圆底烧瓶2 个,蒸馏头1个,带塞温度计1个,直形冷凝管1 个,接引管1个,橡胶管若干);减压抽滤装置 (布氏漏斗1个,吸滤瓶1个,滤纸若干,表面皿 1个,吸耳球1个);酸度计;100ml容量瓶1个, 烧杯2个,玻璃棒1根,蒸发皿1
产品分析:
• (1)重结晶:将粗产品按粗酯:95%乙醇:水:活性炭 为1:0.6:4.0:0.06的比例混合,加热至粗酯溶解,趁 热减压抽滤,将滤液冷却结晶,减压抽滤获得重结晶后晶 体。 (2)熔点测定:将电源线和传感器按要求连接好。 将两片载玻片洗净晒干后,取几颗重结晶后样品放在一载 玻片上,用另一载玻片盖上,轻轻压实,然后将其放置于 加热台上,盖上隔热玻璃。调节显微镜,使其焦点对准样 品。打开电源开关,测定待测样品的熔点,让升温由快→ 渐慢→平缓。观察待测样品的熔化过程。当晶体棱角开始 变圆并有液体产生时为初熔,完全液化为全熔,记录初熔 点和全熔点。如需重复测试,需使温度降至熔点值以下 40℃
3
+
H
+
CR
• • • • • •
(1)增加反应物的浓度 正丙醇的过量。 对羟基苯甲酸:正丙醇的摩尔比通 常要达到1:4~10左右。 (2)从体系中及时移走生成物 水与苯、甲苯、环己烷、三氯甲烷 等多种有机溶剂易形成共沸物。 带水剂与醇的摩尔比通常为1:1
Kc
[ ArCOOR [ ArCOOH
(3) 成酯方式
O R C O H + H O R' H R C O R' O + H 2O 酰氧断裂 O R C O H + H O R' H R C O R' O + H 2O
烷氧断裂
究竟按哪种方式脱水,与羧酸和醇的结构及反应条件有关。经同位素标记醇的办法 证实:
伯醇和仲醇与羧酸的酯化是按酰氧键断裂进行的。
对羟基苯甲酸丙酯性质及分子结构的分析
• 性质 外观:无色细小结晶或白色结晶性粉末,几乎无
臭,稍有涩味。 熔点:95~98℃ 沸点:295℃ 溶解性:微溶于水(0.05g/100ml,25℃),易溶于 乙醇(95g/100mI)、丙酮(105g/l00ml),可溶于花生油 (1.4g/100ml)。 密度:1.0630 折射率:1.5050(20℃) 毒性LD50(mg/kg):小鼠经口3700
合成工艺条件
• • • • • • • • • (1)物料配比 n(对羟基苯甲酸)∶n(正丙醇)≈0.1∶0.8 实训室合成:对羟基苯甲酸 .13.8g(4.14g) 0.1mol 正丙醇 60ml(18g) 0.8mol V(正丙醇):V(环己烷)=1:1 环己烷 60ml(18ml) (2)反应温度 反应液沸腾温度 (3)压力:常压
• ③氯化铁 • 易从酯化反应体系中回收分离。但由于传质的原因及本身 酸性较弱,催化效率较硫酸等低,反应所需的时间较长。 • 用量一般为3%左右。 • ④强酸性阳离子交换树脂 • 为固体强酸,由于能解离出H+,故可作为酯化反应的催化 剂。但由于传质的原因,催化效率较硫酸等稍低。 • 优点是:反应条件温和、选择性好;产物后处理简单,无 需中和及水洗;树脂可循环使用,并可进行连续化生产; 对设备无腐蚀以及减少废水排放量。由于上述优点,强酸 性阳离子交换树脂已广泛用于酯化反应,其中最常用的有 酚磺酸树脂及磺化苯乙烯树脂。离子交换树脂目前已商品 化,可由商品牌号查得该树脂的性质及组成。
