初三化学化学质量守恒定律的专项培优 易错 难题练习题及答案
初三化学人教版质量守恒定律练习题及答案

初三化学人教版质量守恒定律练习题及答案一、选择题1.下列各项:①原子的数目;②分子的数目;③元素的种类;④物质的种类;⑤物质的分子个数;⑥各种原子的总数。
在化学反应前后,肯定没有变化的是()A.①②③⑤B.①⑥C.②③⑤D.①③⑥2.在A+B→C+D的反应中,5克A和一定的B恰好完全反应,生成3克C和10克D,则B的质量是()A.18克 B.7克C.8克D.6克3.对质量守恒定律的解释正确的是()A.化学反应前后原子种类不变,原子数目改变。
B.化学反应前后原子种类改变,原子个数不变。
C.在一切化学反应里,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有改变。
D.在化学反应中反应物的分子数等于生成的分子数。
4.充分加热a克氯酸钾与b克二氧化锰的混合物,留下残余固体c克,则生成氧气的质量为()A.(a-b)克B.(a-b-c)克C.(a+b-c)克D.(a-b+c)克5.某化合物X燃烧时发生的反应为:2X+5O2=4CO2+2H2O,根据质量守恒定律,可判断X的化学式为()A.C2H4B.CH4C.C2H2D.C6H66.下列各组物质,在敞口容器里发生反应,容器内物质的总质量在反应前后不变的是()A.镁条放入盐酸中B.高锰酸钾固体受热分解C.硫酸铜溶液中加入氢氧化钠溶液D.在空气中加热铜粉7.根据质量守恒定律及2Mg+O2==2MgO的反应方程式,下列各组数据正确的是()A.镁的质量2克,氧气质量3克,氧化镁质量5克。
B.镁的质量3克,氧气质量2克,氧化镁质量5克。
C.镁的质量1克,氧气质量4克,氧化镁质量5克。
D.镁的质量4克,氧气质量1克,氧化镁质量5克。
8.已知反应3A+2B==2C+D,A、B两种物质完全反应时质量比为3:4,若生成C和D共140克,则该反应消耗B的质量为()A.60克B.80克C.90克D.120克9.下列说法中,正确的是()A.煤燃烧后剩余的煤渣比较轻,因此不符合质量守恒定律B.蜡烛燃烧后生成的气态物质的质量之和等于蜡烛减少的质量与消耗的氧气的质量之和C.一定量的水的质量与全部蒸发后所生成的水蒸气的质量相等,因此符合质量守恒定律D.只要做一个“白磷燃烧前后质量的测定”的实验就能得出质量守恒定律10.在A+B→C+D反应中,有52克的A与适量的B完全反应,生成了34克C和20.8克D,则反应用去的B的克数是()A.54.8克B.52克C.18克D.2.8克11.在化学反应A+2B=C中,1.5克A与足量的B充分反应后,生成9.5克C,参加反应的B的质量为()A.3克 B.9.5克C.8克D.4克12.有A、B两种物质,它们之间能发生化学反应,6克A与足量B反应生成8克C和3克D。
初三化学质量守恒定律习题(含复习资料)

质量守恒定律月考题60分钟 100分可能用到的相对原子质量:27, 16, 39, 35.5 -55 C12,一、我会选(每小题只有一个正确选项。
每小题2分,共20分)1.下列关于书写化学方程式的说法中,不正确的是( )A.以客观事实为基础B. 反应前后物质的总质量不变C.遵循质量守恒定律D.生成物中的气体一定要标注“↑”2.下列关于化学方程式2 =2的叙述中,不正确的是( )A.碳加氧气生成二氧化碳B.碳在氧气中充分燃烧生成二氧化碳C每.12份质量的碳和32份质量的氧气完全反应生成44份质量的二氧化碳D.在点燃的条件下,1个碳原子能与1个氧气分子反应生成1个二氧化碳分子3铝在氧气中燃烧这个反应中,铝,氧气,氧化铝质量比是( ) A27: 32: 102 B 108: 96 :204 C 27: 24 :43 D 4: 3 :2 4 某工地多次食物中毒,经化验误食工业食盐亚硝酸钠所致,亚硝酸钠化学式2 ,其中N的化合价( )A +2 3 C +4 D +55、在我们的日常生活中出现了加碘食盐、增铁酱油、高钙牛奶、富硒茶叶等。
这里的碘、铁、钙、硒应理解为()A、单质B、分子C、元素D、氧化物6 下列物质中,按单质、化合物、混合物顺序排列的是()A、二氧化碳、水、空气B、氢气、海水、可口可乐C、氧化镁、矿泉水、食盐D、汞、冰、生理盐水7、日常生活中发生的下列变化都属于化学变化的一组是()A、玻璃杯被摔碎、米饭变馊B、酒精挥发、湿衣服晾干C、蜡烛燃烧、乒乓球变瘪D、菜刀生锈、牛奶变酸8 化学反应前后肯定没有发生变化的是( )A 原子种类B 元素化合价C 分子个数D 物质种类9.某化合物[R]在空气中燃烧的化学方程式是:2[R]+3O2 =22+4H2O,则化合物[R]的化学式为( )4 2H4 3 2H510 现把10克的A和足量的B混合发生化学反应,完全反应后生成8克C 和4克D,则参加反应的和的质量比为( )A 1 :1B 2: 1C 4 : 1 D5 : 1二填空每空2分。
初三化学质量守恒定律易错(难)强化练习含答案
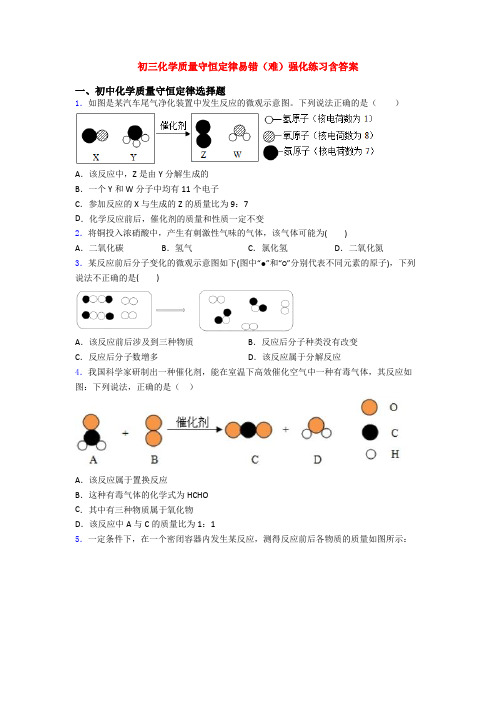
初三化学质量守恒定律易错(难)强化练习含答案一、初中化学质量守恒定律选择题1.如图是某汽车尾气净化装置中发生反应的微观示意图。
下列说法正确的是()A.该反应中,Z是由Y分解生成的B.一个Y和W分子中均有11个电子C.参加反应的X与生成的Z的质量比为9:7D.化学反应前后,催化剂的质量和性质一定不变2.将铜投入浓硝酸中,产生有刺激性气味的气体,该气体可能为()A.二氧化碳B.氢气C.氯化氢D.二氧化氮3.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应4.我国科学家研制出一种催化剂,能在室温下高效催化空气中一种有毒气体,其反应如图:下列说法,正确的是()A.该反应属于置换反应B.这种有毒气体的化学式为HCHOC.其中有三种物质属于氧化物D.该反应中A与C的质量比为1:15.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示:下列说法正确的是()A.x的值为36 B.该反应属于化合反应C.W由碳、氢两种元素组成D.W中碳、氢元素质量比为1︰36.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。
则关于此反应的认识正确的是()物质X Y Z W反应前的质量(g)211616反应后的质量(g)18m611A.该反应为分解反应B.该反应为化合反应C.m=1 D.反应后容器中Z与Y的质量比为1:6 7.如图是某化学反应的微观模型,“”、“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是()A.该反应属于分解反应B.反应中共有两种元素参加C.反应物和生成物中只有一种单质D.参加反应的两种物质分子个数之比为2:38.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的图像正确的是A.B.C .D .9.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。
初三化学化学质量守恒定律的专项培优 易错 难题练习题(含答案)及答案

初三化学化学质量守恒定律的专项培优 易错 难题练习题(含答案)及答案一、初中化学质量守恒定律1.在反应3X +4Y =2Z 中,已知X 的相对分子质量是32,Z 的相对分子质量是102,则Y 的相对分子质量为( ) A .172 B .108C .70D .27【答案】D 【解析】 【分析】 【详解】在反应3X+4Y=2Z 中,参加反应的X 的质量和Y 的质量之和等于生成物Z 的质量,Y 的相对分子质量为:(102×2-32×3)÷4=27。
故选D 。
2.在不同时刻,某反应中的甲、乙、丙、丁四种物质的质量如下表。
已知甲的相对分子质量为丁的 2 倍。
则下列说法不正确的是( )A .乙和丙为生成物B .a 等于 21C .b 等于 37D .该反应方程式中甲与丁的化学计量数之比为 1:2 【答案】D 【解析】 【详解】A 、b =64+10+1+16﹣54=37,根据题目提供信息可知,甲、丁是反应物,乙、丙是生成物,故A 正确;B 、设t 时刻生成乙的质量为x++64g 54g-10g 64g-48g x甲丁乙丙64g 64g-48g=54g-10g xx =11ga =10g+11g =21g ,故B 正确;C 、根据A 中计算结果可知b =37,故C 正确;D 、设丁的相对分子质量为m ,则甲的相对分子质量为2m ,该反应的化学方程式可表示为:a +bc +d 26416am bm g g甲丁乙丙 2am 64g=bm 16ga :b =2:1,故D 错误。
故选:D 。
3.据报道,中国科学技术大学研究人员利用钴及其氧化物成功研制一种新型催化剂,可将二氧化碳高效“清洁”地转化成液体,反应的微观示意图如图所示。
有关该反应的说法正确的是( )A .反应前后原子总数减少B .反应物和生成物中共有两种氧化物C .得到的液体燃料化学式是H 2C 2OD .可用于减少二氧化碳的排放 【答案】D 【解析】 【分析】据题目信息结合微观示意图,排除未反应的分子的干扰,可写出反应的方程式为:CO 2+H 2H 2CO 2。
初三化学质量守恒定律易错(难)单元测试题附答案(1)

初三化学质量守恒定律易错(难)单元测试题附答案一、初中化学质量守恒定律选择题1.一定条件下,甲、乙混合后发生化学反应,测得反应前后各物质的质量变化如下表所示。
下列说法中,不正确的是()物质甲乙丙丁反应前的质量/g50200反应后的质量/g23X243A.x的值等于2 B.甲一定是化合物C.该反应是化合反应D.反应时丙和丁的质量比为8:12.下列说法正确的是A.镁条的质量等于它燃烧后生成物的质量B.蜡烛燃烧时逐渐变短,不符合质量守恒定律C.高锰酸钾受热分解的总质量等于生成物的总质量D.12 g碳和16 g氧气反应,可生成28 g二氧化碳3.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应4.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A.该反应属于置换反应B.反应中乙、丙两物质质量比为2: 7 C.图示中x的数值为4 D.反应前后氢元素的化合价发生了改变5.浓盐酸跟二氧化锰混合加热会产生一种黄绿色的有毒气体,该气体可能是A.Cl2B.H2C.NH3D.HCl6.某个化学反应的微观示意图如图。
有关说法正确的是()A.该反应为分解反应B.该反应不遵守质量守恒定律C.该反应前后分子种类未发生变化D.该反应的化学方程式为H2+Cl22HCl7.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z8.在反应3X+4Y=2Z中,已知X的相对分子质量是32,Z的相对分子质量是102,则Y 的相对分子质量为()A.172 B.108 C.70 D.279.如图为某化学反应的微观模拟示意图,下列说法中,正确的是A.反应前后氢元素的化合价没有改变B.n=3C.反应过程中原子种类发生了变化D.该反应生成了两种单质10.下列化学用语及结构正确的是()A.3个铁离子:3Fe2+B.氦气:He2C.4个氢原子:4H D.氯离子的结构示意图:11.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法正确的是物质a b c d反应前的质量(g)7.4 4.2 5.0 3.8反应后的质量(g) 6.2x 5.2 3.8A.物质a是生成物B.x=5.2C.d一定是催化剂D.反应后原子数目减少了12.40%的甲醛(CH2O)溶液被称为福尔马林。
化学初三质量守恒练习题

化学初三质量守恒练习题1. 某实验室用1.0g的碳粉末和1.0g的硫粉末进行反应,若生成的化合物完全无机质残留,求生成物的质量是多少?解析:根据质量守恒定律,反应前后物质的质量是不变的。
因此,碳粉末和硫粉末的质量和生成物的质量之和应该等于 1.0g+1.0g=2.0 g。
2. 一个密封的容器中有氧气和氢气,当用火花引燃后,所有氧气和氢气完全反应,生成的水蒸气充满容器,问容器的质量是否发生变化?解析:根据质量守恒定律,反应前后物质的质量是不变的。
因此,即使氧气和氢气发生了完全反应生成水蒸气,容器的质量不会发生变化。
3. 某个反应的化学方程式为2H₂ + O₂ → 2H₂O,如果有2.0g的氢气和16.0g的氧气完全反应,求生成水的质量是多少?解析:根据化学方程式中的化学计量比,可以得出2mol的氢气反应需要1mol的氧气,而2mol的氢气和1mol的氧气反应会生成2mol的水。
根据摩尔质量的关系,2mol的氢气质量为2.0g,16.0g的氧气质量为1mol。
因此,由于化学计量比的限制,氧气以完全反应完,生成的水质量为2.0g。
4. 当丁醇完全燃烧生成二氧化碳和水时,实验得到了180g的二氧化碳和90g的水,问初始丁醇的质量是多少?解析:根据反应前后物质的质量不变,二氧化碳和水的质量之和应等于初始丁醇的质量。
所以,初始丁醇的质量为180g+90g=270g。
5. 某实验室用20.0g的氢气和40.0g的氧气进行反应,若完全反应,求生成水的质量是多少?解析:根据化学方程式2H₂ + O₂ → 2H₂O可以得知,2mol的氢气反应需要1mol的氧气,并会生成2mol的水。
通过摩尔质量的关系,可以计算出20.0g的氢气为1mol,40.0g的氧气为1mol。
因此,由于化学计量比的限制,氧气以完全反应完,生成的水质量为2mol,即36.0g。
总结:质量守恒定律是化学中的基本原理之一,它指出在任何化学反应中,反应物的总质量等于生成物的总质量。
初三化学质量守恒定律 知识点 习题及答案

初三化学质量守恒定律_知识点_习题及答案第五单元:质量守恒定律一、质量守恒定律:1总和。
说明:①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏。
2、微观解释:在化学反应前后,原子的种类、数目、质量均保持不变(原子的“三不变”)。
3、化学反应前后(1)一定不变宏观:反应物、生成物总质量不变;元素种类不变微观:原子的种类、数目、质量不变(2)一定改变宏观:物质的种类一定变微观:分子种类一定变(3)可能改变:分子总数可能变二、化学方程式1、遵循原则:①以客观事实为依据② 遵守质量守恒定律2、书写:(注意:一写、二配、三标、四等)3、含义:以为例①宏观意义:表明反应物、生成物、反应条件氢气和氧气在点燃的条件下生成水②微观意义:表示反应物和生成物之间分子个氢分子与1个氧分子化合生成2个个水分子(对气体而言,分子个数比等于体积之比)③各物质间质量比(系数×相对分子质量之比)每4份质量的氢气与32份质量的氧气完全化合生成36份质量的水 4、化学方程式提供的信息包括①哪些物质参加反应(反应物);②通过什么条件反应:③反应生成了哪些物质(生成物);④参加反应的各粒子的相对数量;⑤反应前后质量守恒等等。
5、利用化学方程式的计算三、化学反应类型 1、四种基本反应类型①化合反应:由两种或两种以上物质生成另一种物质的反应②分解反应:由一种反应物生成两种或两种以上其他物质的反应③置换反应:一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应④复分解反应:两种化合物相互交换成分,生成另外两种化合物的反应2、氧化还原反应氧化反应:物质得到氧的反应还原反应:物质失去氧的反应氧化剂:提供氧的物质还原剂:夺取氧的物质(常见还原剂:H2、C、CO) 3、中和反应:酸与碱作用生成盐和水的反应4:在3Fe+2O2Fe3O4的反应中,_____份质量的铁跟_____份质量的氧气反应,生成_____份质量的四氧化三铁。
2020-2021中考化学培优 易错 难题(含解析)之流程图附详细答案

一、中考初中化学流程图1.《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO 3)和煤炭饼装入炼锌罐(如下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
(已知:锌的熔点 为 419℃,沸点为 907℃)(1)反应区中,ZnCO 3 分解生成 ZnO 和另一种氧化物,反应的化学方程式为_________。
C 与 ZnO 发生置换反应得到 Zn ,反应中化合价升高的元素是_____。
(2)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是_____℃。
(3) “冷定”后方能“毁罐”取锌、从化学变化角度解释其原因:_____。
【答案】ZnCO 3加热ZnO +CO 2↑ C (或“碳”) 419~907 防止生成的锌在较高温度下又被氧化成氧化锌(或“2Zn +O 2加热2ZnO”)【解析】【分析】 碳酸锌高温生成氧化锌和二氧化碳,碳和氧化锌高温生成锌和二氧化碳,锌和氧气加热生成氧化锌。
【详解】(1)反应区中,ZnCO 3 分解生成 ZnO 和二氧化碳,反应的化学方程式为32ZnCO ZnO+CO 加热。
C 与 ZnO 发生置换反应得到Zn 和二氧化碳,故反应中化合价升高的元素是碳。
(2)锌的熔点为 419℃,沸点为 907℃,冷凝区中,锌由气态转化为液态,故该区应控制的温度范围是419~907℃。
(3)锌在较高温度被氧化成氧化锌,“冷定”后方能“毁罐”取锌,原因是防止生成的锌在较高温度下又被氧化成氧化锌。
2.盐化工是我国的一项重点产业,绿色应用是化工生产的发展方向!为了除去 NaCl 溶液中含有少量的 MgCl2、CaCl2和 Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
请回答下列问题:①实验Ⅱ中加入的试剂 B 是_______________溶液。
②实验Ⅰ中加入试剂 A 除去的杂质是_______________。
中考化学专项训练:质量守恒定律易错(难)检测题含答案

中考化学专项训练:质量守恒定律易错(难)检测题含答案一、初中化学质量守恒定律选择题1.某化学反应的微观示意图如图所示,则下列说法正确的是( )A.反应前后分子种类、数目均不变B.该反应属于置换反应C.该反应中,反应物的质量比是1:2D.该反应的生成物均为氧化物2.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示:下列说法正确的是()A.x的值为36 B.该反应属于化合反应C.W由碳、氢两种元素组成D.W中碳、氢元素质量比为1︰33.浓盐酸跟二氧化锰混合加热会产生一种黄绿色的有毒气体,该气体可能是A.Cl2B.H2C.NH3D.HCl4.某有机物在空气中完全燃烧,测得生成物中含有二氧化碳、水蒸气、二氧化硫,下列对该有机物的组成推断正确的是()A.一定含碳、氢、硫元素B.一定含有碳、氢、氧元素C.只含碳、氢元素D.一定含碳、氢、氧元素,可能含有硫元素5.在化学反应A+B2=2C中,已知20gA和足量B2充分反应后,生成30gC。
已知B的相对原子质量为16,则C的相对分子质量是()A.20B.32C.48D.966.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列说法错误的是( )A.x的值是7B.丙可能是该反应的催化剂C.该反应是化合反应D.参加反应的甲和乙质量比为2:77.将一定量xFeSO4•y(NH4)2SO4•6H2O晶体加入到过量NaOH溶液中,加热生成NH30.85g(假如生成NH3的全部逸出),过滤、洗涤、灼烧,得Fe2O3固体2.0g.则x,y 的关系正确的是()A.x:y=1:1 B.x:y=1:2 C.x:y=1:4 D.x:y=2:18.科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微观示意图如下图,有关该反应的说法正确的是()A.该反应属于化合反应B.反应前碳元素的化合价为+2 价C.生成物的化学式可用 C2H2O 表示D.参加反应的两物质的质量比为 1:19.用下列装置来验证质量守恒定律(托盘天平未画出),能达到目的是()A.B.C.D.10.在反应3X+4Y=2Z中,已知X的相对分子质量是32,Z的相对分子质量是102,则Y 的相对分子质量为()A.172 B.108 C.70 D.2711.如图所示:3个甲分子与1个乙分子反应生成两个丙分子.根据图示所得信息正确的是()A.物质甲的化学式为H6B.该反应为化合反应C.化学反应中,分子是最小的微粒D.该图示不符合质量守恒定律12.工业制钛反应为:TiF4+2H2SO4Δ4HF+2X+TiO2,X 的化学式为A.H2S B.P4C.SO2D.SO313.下列化学用语书写正确的是A.3个硝酸根离子:3NO3-B.2个铝原子:Al2C.五氧化二磷分子:O2P5D.标出氯化镁中氯元素的化合价:-22Mg Cl 14.下列化学方程式书写正确的是()A.H2+O2点燃H2OB.2Mg+O2点燃2MgOC.2KClO3催化剂2KCl+3O2D.4 Fe+3O2点燃2Fe2O315.质量守恒定律是帮助我们认识化学反应实质的重要理论.某物质与水和氧气反应的化学方程式为224242R+2H O+7O=2FeSO+2H SO:则R的化学式应为A.FeS B.Fe2S3C.FeO D.FeS216.甲、乙、丙、丁4种物质在密闭容器里反应,质量变化如下。
初三化学质量守恒定律单元复习测试题附答案

初三化学质量守恒定律单元复习测试题附答案一、初中化学质量守恒定律选择题1.“神舟七号“太空舱利用NiFe2O4将航天员呼出的CO2转化为O2,而NiFe2O4的质量和化学性质在化学反应前后都不发生变化。
该过程中NiFe2O4是()A.生成物B.反应物C.催化剂D.氧化剂2.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。
则关于此反应的认识正确的是()物质X Y Z W反应前的质量(g)211616反应后的质量(g)18m611A.该反应为分解反应B.该反应为化合反应C.m=1 D.反应后容器中Z与Y的质量比为1:6 3.某有机物在空气中完全燃烧,测得生成物中含有二氧化碳、水蒸气、二氧化硫,下列对该有机物的组成推断正确的是()A.一定含碳、氢、硫元素B.一定含有碳、氢、氧元素C.只含碳、氢元素D.一定含碳、氢、氧元素,可能含有硫元素4.如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是()A.苯分子由碳、氢两种元素组成B.苯中氢元素的质量分数小于10%C.六氯苯中碳氯两种元素的质量比为1:1D.六氯苯有6个碳原子和6个氯原子构成5.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z6.用下列装置来验证质量守恒定律(托盘天平未画出),能达到目的是()A.B.C.D.7.“绿色化学”的特点之一是“零排放”.在一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,该产物化学式是()A.CH4O B.CH2O2C.C2H6O D.C2H4O28.如图为某化学反应的微观模拟示意图,下列说法中,正确的是A.反应前后氢元素的化合价没有改变B.n=3C.反应过程中原子种类发生了变化D.该反应生成了两种单质9.元素观是化学的重要观念之一。
九年级化学化学质量守恒定律的专项培优 易错 难题练习题(含答案)含答案

学变化中元素的种类不发生改变,正确。故选 B。
11.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前 后各物质的质量变化见下表。下列说法错误的是( )
物质
甲
乙
丙
丁
反应前物质的质量(g) 8
32
5
4
反应后物质的质量(g) 16
X
5
24
A.该反应为分解反应 B.丙可能是该反应的催化剂 C.甲、丁两物质反应前后质量变化之比为 2:5 D.X 值为 28 【答案】D 【解析】 【分析】 根据质量守恒定律,在化学反应中,反应前参加反应的各物质的质量总和等于生成物的各 质量总和,反应后增加的是反应物,减少的是生成物。 【详解】
A、反应后甲增加了16g-8g=8g ,则甲是生成物,丁增加了 24g-4g=20g ,则丁是生成
物,丙反应前后质量没变,丙可能没参加反应或是催化剂,根据质量守恒定律,则有
8g+32g+5g+4g=16g+X+5g+24g ,则 X=4g ,则反应表达式是乙 甲+丙,属于分解
反应,故 A 正确; B、丙反应前后质量没变,可能是该反应的催化剂或者没参加反应,故 B 正确;
7.图反映了某个化学反应各物质质量与时间的关系。下列描述正确的是
A.该反应是化合反应 B.甲的相对分子质量大于乙 C.丙是反应物,甲和乙是生成物 D.t1 时,丙的质量一定等于甲、乙的质量之和 【答案】C 【解析】 【分析】 【详解】 A、由图知从 0 到 t1 时间内丙物质逐渐减少,甲乙两物质逐渐增加。所以,丙为反应物, 甲、乙为生成物,该反应分解反应,描述错误; B、甲的生成量比乙多,但分子个数不知,相对分子质量甲不一定比乙大,描述错误; C、 丙是反应物,甲和乙是生成物,描述正确; D、t1 时,参加反应的丙质量一定等于甲、乙的质量之和,描述错误。 故选 C。
2020-2021中考化学培优 易错 难题(含解析)之探究题附详细答案

一、中考初中化学科学探究题1.化学兴趣小组的同学按图示装置(K I , K 2开始处于关闭状态)及步骤探究碱的化学性质。
[实验步骤]实验I:沿分液漏斗将一定量NaOH 客液注入A 中,关闭漏斗活塞。
实验II :打开K I ,观察到B 中部分溶液倒吸入A 中,待停止倒吸。
实验III :打开K 2, 观察到C 中溶液分别倒吸入A 、B 中,轻轻振荡,直到液面稳定。
[思考与交流] (1) B 中滴有酚酞的Ca (OH)2溶液呈红色,说明Ca (OH)2的溶液的pH___7. (填“<”“>"或“=”)(2)实验I 中在A 装置的锥形瓶内观察到的现象有______________________________ 根据实验I 和II____ (填 “能”或“不能”)证明CO 2和NaOH 溶液发生了反应。
(3)实验III , B 中反应的化学方程式是_________________(4)实验III , C 中溶液倒吸入A 装置的锥形瓶内,充分反应后溶液星无色。
经分析,瓶中混合物一定含有水、 氯化钠和酚酞,可能含有碳酸钙。
为进步确定溶液中还可能含有哪些溶质,提出以下猜想: (已知:氯化钙溶液呈中性) 猜想一: CaCl 2:猜想二:___________________ ①请完成猜想二。
②请你帮助设计实验方案,验证猜想正确 (写出实验操作过程及实验现象)______________【答案】> B 装置中的液体倒吸进A 装置 不能 ()222C a OH +2HCl=CaCl +2H O 23CaCl CaCO 、 取少量溶液于试管中,滴加稀盐酸溶液,产生气泡,则说明含有碳酸钙【解析】 【分析】二氧化碳和氢氧化钠反应生成碳酸钠和水,稀盐酸和氢氧化钙生成氯化钙和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
【详解】[思考与交流] (1) B 中滴有酚酞的2Ca(OH)溶液呈红色,说明2Ca(OH)的溶液的pH>7。
人教版九年级化学上册全方位培优测评卷专项训练:质量守恒定律(详细全解析)

人教版九年级化学上册专项训练(一)——质量守恒定律的应用一、选择题1.氯碱工业电解食盐水得到的产物中,不可能包含下列哪种物质( ) A.碳酸钠B.氯气C.氢气D.氢氧化钠2.在化学变化中,下列说法正确的是( ) ①原子的种类、元素的种类、分子的种类均不变 ②原子的数目、分子的数目均不变 ③原子的质量、元素的质量、物质的总质量均不变 ④原子核的种类、数量、质量均不变 A.①②B.①③C.③④D.②④3.相同质量的下列物质完全分解制取氧气,制取氧气最多的是( ) A. KMnO 4B. KClO 3C. H 2OD. H 2O 24.下列四个反应的生成物都是C ,如果C 的化学式为A 2B 5,则该反应的化学方程式为( ) A.2AB 2+B 2=2CB.3AB 2+B 2=2CC.4AB 2+B 2=2CD. AB 2+4B 2=2C5.下列叙述完全符合质量守恒定律的是( ) A.水结成冰前后,质量保持不变B.50mL 水和50mL 乙醇混合后总体积小于100mLC.在100g 过氧化氢溶液中,含有30g 过氧化氢和70g 水D.1.2g 碳与3.2g 氧气恰好完全反应可生成4.4g 二氧化碳6.煤油中含有噻吩(用表示),噻吩具有令人不愉快的气味,其燃烧时发生反应的化学方程式表示为:X+6O 2=4CO 2+SO 2+2H 2O ,则噻吩的化学式为( ) A.C 4H 4SB.H 4H 6SC. CH 4D. C 4H 8S 7.实验室使用一定质量的高锰酸钾加热分解制氧气,各物理量随加热时间变化的图象正确的是( )8.氯气(Cl 2)和氧气(O 2)都是活泼的非金属单质,在一定条件下它们都能跟甲烷(CH 4)反应。
已知O 2和CH 4充分反应后的生成物是CO 2和H 2O ,由此推断Cl 2和CH 4充分反应后的生成物是( ) l 4和HCll 4和H 2C.CH 2Cl 2和H 2D.C 和HCl9.下列关于2CO+O 2=2CO 2的说法不正确的是( ) 点点燃A.表示一氧化碳与氧气在点燃条件下反应生成二氧化碳B.参加反应的一氧化碳与氧气的质量比为7:8C.反应前后碳原子、氧原子的个数均保持不变D.参加反应的一氧化碳与生成的二氧化碳的分子个数比为1:110.用如图所示装置验证质量守恒定律能达到实验目的的物质组合是( )A.锌和稀硫酸B.碳酸钠和稀盐酸C.铁和硫酸铜溶液D.硝酸钠和稀盐酸11.以下是某两种物质在一定条件下发生化学反应的微观示意图:(其中和●分别表示两种不同的原子):由图可知,下列说法中正确的是( )①该反应属于化合反应②一定是氢气和氧气反应生成水③反应遵守质量守恒定律④反应前后分子和原子种类都不变⑤分子在化学变化中可以再分,而原子不能再分A.①②③⑤B.①②④⑤C.①③⑤D.①②③④⑤12.已知:某密闭容器中,12gA加热完全分解产生B和C,其中B的质量为2g,同时C又能部分分解产生0.1gD和7.9gE,则最终该密闭容器中B和C的质量比为( )A.1:1B.1:2C.1:4D.1:513.某化学反应的反应物和生成物的微观示意图及反应前后的质量如下表所示。
2020-2021中考化学培优 易错 难题(含解析)之气体和固体分离和提纯及答案
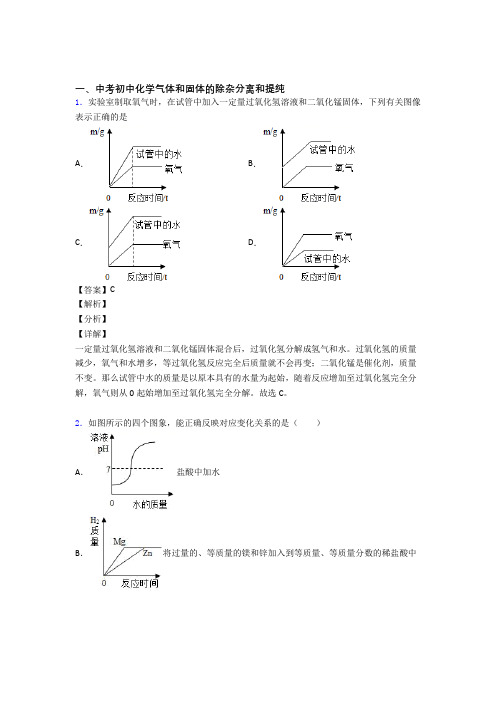
一、中考初中化学气体和固体的除杂分离和提纯1.实验室制取氧气时,在试管中加入一定量过氧化氢溶液和二氧化锰固体,下列有关图像表示正确的是A.B.C.D.【答案】C【解析】【分析】【详解】一定量过氧化氢溶液和二氧化锰固体混合后,过氧化氢分解成氢气和水。
过氧化氢的质量减少,氧气和水增多,等过氧化氢反应完全后质量就不会再变;二氧化锰是催化剂,质量不变。
那么试管中水的质量是以原本具有的水量为起始,随着反应增加至过氧化氢完全分解,氧气则从0起始增加至过氧化氢完全分解。
故选C。
2.如图所示的四个图象,能正确反映对应变化关系的是()A.盐酸中加水B.将过量的、等质量的镁和锌加入到等质量、等质量分数的稀盐酸中C.在一定温度下向接近饱和的硝酸钾溶液中加入硝酸钾固体,溶液中溶质质量分数的变化D.煅烧一定质量的石灰石【答案】B【解析】【分析】【详解】A. 盐酸中加水,酸性变弱,溶液的pH增大,但不会等于或大于7,选项错误;B. 金属与酸反应生成氢气的质量等于参加反应的的酸中氢元素的质量。
将过量的、等质量的镁和锌加入到等质量、等质量分数的稀盐酸中,此时酸完全反应,所以酸决定氢气的质量,质量、质量分数相同的同种酸,生成氢气质量相同,选项正确;C. 在一定温度下,向接近饱和的硝酸钾溶液中加入硝酸钾固体,溶液中溶质质量分数增大,但溶质的质量分数不会等于零,起点错误,选项错误;D. 煅烧一定质量的石灰石,反应为碳酸钙在高温条件下分解生成氧化钙和二氧化碳,固体的质量减少,反应时固体中钙元素质量分数就增大,完全反应,质量分数不变,选项错误。
故选B。
3.向一定量某固体中逐滴加入某溶液至过量,x轴表示加入溶液的质量.下列选项中y轴表示的含义与所给图象变化趋势一致的是( )选项固体溶液y轴含义A二氧化锰过氧化氢溶液溶液中氢元素的质量B铜粉和锌粉稀硫酸固体质量C氯化钠和碳酸氢钠的固体混合物稀盐酸溶液中氯化钠的质量分数D大理石(杂质不参加反应)稀盐酸固体中杂质的质量分数A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化氢中含有氢元素,随着反应的进行,溶液中氢元素的质量不断增加,继续加入过氧化氢溶液,溶液中氢元素的质量仍在增加,故选项y轴表示的含义与所给图象变化趋势不一致。
培优 易错 难题计算题辅导专题训练及详细答案

一、中考初中化学计算题1.将Na2CO3和NaCl固体混合物32.9g放入烧杯中,此时总质量为202.9g,加入326.9g盐酸,恰好完全反应,待没有气泡逸出后再次称量,总质量为521.0g.计算所得溶液中溶质的质量分数______(CO2的溶解忽略不计).【答案】10【解析】【分析】首先根据质量守恒定律:化学反应前后,物质的质量不变,可先求出产生的气体二氧化碳的质量=202.9g+326.9g-521.0g=8.8g,再根据化学反应方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑可知,反应后所得溶液中溶质是NaCl,但NaCl来自两部分,一是反应生成的,二是原固体混合物中含有的,生成的NaCl可通过化学方程式来求解,原固体混合物中含有的NaCl可通过混合物32.9g减去Na2CO3的质量【详解】解:根据质量守恒定律,反应生成的CO2质量=202.9g+326.9g-521.0g=8.8g设Na2CO3的质量为x,生成的NaCl的质量为y。
2322Na CO+2HCl=2NaCl+H O+CO10611744x y8.8g↑10611744==x y8.8g解得x=21.2g y=23.4g所得溶液中溶质的质量分数=23.4g+32.9g-21.2g100% 32.9g+326.9g-8.8g⨯ =10%答:所得溶液中溶质的质量分数为10%。
2.向一定质量的5%的氢氧化钠溶液中加入66.9g硫酸铜溶液,恰好完全反应,得到4.9g 蓝色沉淀。
请计算:(1)所用氢氧化钠溶液的质量________。
(2)反应后所得溶液的溶质质量分数__________。
【答案】80g5%【解析】设参加反应的氢氧化钠的质量为x,反应生成硫酸钠的质量为y;2NaOH + CuSO4 = Cu(OH)2↓+ N a2SO480 98 142x 4.9g y80/98=x/4.9g x= 4g142/98=y/4.9g y=7.1g氢氧化钠溶液的质量为:4g÷5%=80g反应后所得溶液中溶质的质量分数是:答:所用氢氧化钠溶液的质量80g;反应后所得溶液的溶质质量分数为5%。
初三化学质量守恒定律易错(难)复习提高测试题含答案

初三化学质量守恒定律易错(难)复习提高测试题含答案一、初中化学质量守恒定律选择题1.观察图片,结合已学知识,判断下列说法正确的是()A.反应前的物质都是化合物B.反应后的粒子一定是水分子C.反应前后原子数目一定发生变化D.反应前后分子种类一定发生变化2.某反应前后分子变化的微观示意图如下。
下列说法不正确...的是A.该反应中共有3种分子B.该反应中分子数减少C.甲和乙的相对分子质量之和与丙的相对分子质量相等D.该反应属于化合反应3.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A.该反应属于置换反应B.反应中乙、丙两物质质量比为2: 7C.图示中x的数值为4 D.反应前后氢元素的化合价发生了改变4.食盐不仅可以做调味品,还是一种重要的化工原料。
电解饱和食盐水,不可能得到的产物是()A.H2B.Cl2C.NaOH D.Na2CO35.浓盐酸跟二氧化锰混合加热会产生一种黄绿色的有毒气体,该气体可能是A.Cl2B.H2C.NH3D.HCl6.下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。
下列说法正确的是()A.该反应属于置换反应B.参加反应的两种分子个数比为1:1C.1个X分子中含有3个原子D.1个X分子中含有3种不同的原子7.氯气是一种有毒的气体,实验室制取氯气时,可以用氢氧化钠溶液来吸收尾气,其反应原理为Cl2 + 2NaOH = X + NaClO + H2O, 则X 的化学式为A.H2B.NaCl C.HCl D.HClO8.某仓库工作人员违章操作,在雨天转运“保险粉”引起爆炸。
“保险粉”化学名为连二亚硫酸钠(Na2S2O4),主要用于印染工业。
该化学品在潮湿空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4=Na2S2O3+Na2SO3+X。
下列有关说法错误的是A.X 的化学式为 SO2B.连二亚硫酸钠与水能剧烈反应,化学性质很活泼C.Na2SO3 是一种盐,其中硫元素的化合价为+3 价D.Na2S2O4 通常要在干燥阴凉处密闭贮存9.科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微观示意图如下图,有关该反应的说法正确的是()A.该反应属于化合反应B.反应前碳元素的化合价为+2 价C.生成物的化学式可用 C2H2O 表示D.参加反应的两物质的质量比为 1:1 10.如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是()A.苯分子由碳、氢两种元素组成B.苯中氢元素的质量分数小于10%C.六氯苯中碳氯两种元素的质量比为1:1D.六氯苯有6个碳原子和6个氯原子构成11.如图是某化学反应的微观模型,“”、“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是()A.该反应属于分解反应B.反应中共有两种元素参加C.反应物和生成物中只有一种单质D.参加反应的两种物质分子个数之比为2:312.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的图像正确的是A.B.C.D.13.在一密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如下表,对该反应,下列描述正确的是():物质甲乙丙丁反应前物质质量/g25m188反应后物质质量/g9待测384A.“待测”数值一定为2g B.该反应中甲和丁为反应物C.乙一定是该反应的催化剂D.反应中甲和丙的质量比为9:3814.甲烷在一定量的氧气中燃烧.测得反应前后各物质的质量如下:物质甲烷氧气水二氧化碳X反应前质量 3.211.2000/g反应后质量007.2 4.4待测/g下列判断不正确的是A.X不是该反应的催化剂B.反应后X的质量为2.8gC.X中两种元素的质量比为1:2D.反应中甲烷与氧气的化学计量数之比为4:715.40%的甲醛(CH2O)溶液被称为福尔马林。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物的分子中含 2 个 原子和 4 个 原子共 6 个原子,反应前后原子种类、数目都不变;故
C 不正确;
D、反应前的分子是 和 ,反应后的分子是
,所以反应前后分子种类一定发生
变化,故 D 正确。故选 D。
【点睛】
由同种元素组成的纯净物是单质,由不同元素组成纯净物是化合物。
3.过氧乙酸(C2H4O3)是常见的消毒剂。下列有关过氧乙酸的说法正确的是
C.由苯的化学式 C6H6 可知,其中碳元素和氢元素的质量比为:(12×6):(1×6)=12: 1,说法错误,故不符合题意; D.苯是由碳元素与氢元素组成的,由质量守恒定律可知,苯完全燃烧生成二氧化碳和 水,说法正确,故符合题意; 故选 D 【点睛】 考查了化学式的意义以及有关化学式的计算,特别注意质量比和个数比是否混淆。
15.下列是酒精被氧化,最终生成乙酸的过程。下列说法正确的是( )
A.甲、乙完全燃烧的产物不同
B.转化②中乙和氧气的分子个数之比为
2∶ 1 C.转化①和转化②都是化合反应
D.丙物质中碳元素的质量分数大于甲物质
【答案】B
【解析】
【详解】
A、甲乙均为有机物,完全燃烧的产物相同,故 A 错误;
B、由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为 1:2,故 B
Δ
6.金属单质 M 与非金属单质硫发生如下反应为 2M + S M2S。甲、乙二组学生在实验室
分别进行该实验,加入的 M 和硫的质量各不相同。充分反应后,实验数据记录如下表,则 M 的相对原子质量是
M 的质量/
S 的质量/ g
M2S 的质量/ g
甲
6.0
2.5
7.5
乙
7.0
1.5
7.5
A.64 【答案】A 【解析】
A.苯属于有机高分子化合物 B.苯由 6 个碳原子和 6 个氢原子构成 C.苯中碳氢两种元素的质量比为 1:1 D.苯完全燃烧产物有 CO2 和 H2O 【答案】D 【解析】 【详解】 A.有机高分子化合物的相对分子质量大到几万、甚至几十万,而苯的相对分子质量为: 12×6+1×6=78,不属于有机高分子化合物,说法错误,故不符合题意; B.苯是由苯分子构成的,而不是由原子直接构成的,说法错误,故不符合题意;
11.在反应 3X+4Y=2Z 中,已知 X 的相对分子质量是 32,Z 的相对分子质量是 102,则 Y
的相对分子质量为( )
A.172
B.108
C.70
D.27
【答案】D
【解析】
【分析】
【详解】
在反应 3X+4Y=2Z 中,参加反应的 X 的质量和 Y 的质量之和等于生成物 Z 的质量,Y 的相对
14.工业制钛反应为:TiF4+2H2SO4 Δ 4HF+2X+TiO2,X 的化学式为
A.H2S 【答案】D
B.P4
C.SO2
D.SO3
【解析】
【详解】
加热
由 TiF4+2H2SO4
4HF+2X+TiO2 可知,反应前后钛原子都是 1 个,氟原子都是 4 个,氢
原子都是 4 个,反应前硫原子是 2 个,反应后应该是 2 个,包含在 2X 中,反应前氧原子是 8 个,反应后应该是 8 个,其中 6 个包含在 2X 中,X 的化学式是 SO3。 故选:D。
A.过氧乙酸中含有 O3 分子
B.过氧乙酸中碳元素的质量分数为 31.6%
C.过氧乙酸的相对分子质量为 76g
D.过氧乙酸中碳、氢、氧元素质量比为
2:4:3
【答案】B
【解析】
【详解】
A、过氧乙酸(C2H4O3)是由分子构成的,分子是由原子构成的,过氧乙酸分子中含有氧 原子而不是 O3 分子,故选项错误;
【解析】 【详解】 由 2FeTiO3+6C+7Cl2═ 2X+2TiCl4+6CO 可知,反应前铁原子是 2 个,反应后应该是 2 个,包含 在 2X 中,反应前后钛原子都是 2 个,碳原子都是 6 个,氧原子都是 6 个,反应前氯原子 是 14 个,反应后应该是 14 个,其中 6 个包含在 2X 中,因此 X 的化学式是 FeCl3。故选 A。
物;而 表示由同种原子构成的分子,为单质分子,所以为单质;故 A 不正确;
B、虽然
中原子的个数比是 2:1,但反应物的分子是 和 ,即化合物和单质的
反应,类似于一氧化碳和氧气反应产生二氧化碳,因此反应后的微粒不一定是水分子,故
B 不正确;
C、反应前的三个分子中共含有 2 个 原子和 4 个 原子共 6 个原子,反应后的二个生成
5.在一个密闭容器内有
四种物质,在一定条件下充分反应,测得反应前后各
物质的质量如下,下列说法正确的是
物质
A
B
C
D
反应前质量
4
6
111
4
反应后质量
待测
15
0
84
A.该密闭容器中发生的化学变化属于化合反应 B.密闭容器中发生的化学变化属于分解反应 C.该反应中四种物质(参加反应或生成)的质量比为 D.反应后密闭容器中 的质量为 【答案】B
应时 B2 会剩余 2g,根据质量守恒定律可知生成的 AB 会是 12g。故选 A。
9.如图为某反应的微观示意图,下列说法正确的是( )
A.该反应属于分解反应
B.反应前后分子种类没有改变
C.反应前后原子数目发生改变D.参加反应的两种Fra bibliotek子个数比为 1:1
【答案】D
【解析】
A、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误;
初三化学化学质量守恒定律的专项培优 易错 难题练习题及答案
一、初中化学质量守恒定律
1.甲、乙、丙、丁 4 种物质在密闭容器里反应,质量变化如下。下列说法正确的是
()
物质
甲
乙
丙
丁
反应前质量
20
4
/g
20
20
反应后质量 2
/g
待测
32
26
A.乙一定是与该反应无关的杂质 B.甲是一种化合物 C.丙、丁在反应中的质量比是 16:13 D.该反应是化合反应 【答案】B 【解析】 【分析】 【详解】 由表中数据分析可知,反应前后甲的质量减少了 20g-2g=18g,所以是反应物,参加反应的 甲的质量为 18g;同理可以确定丙是生成物,生成的丙的质量为 32g-20g=12g;丁是生成 物,生成的丁的质量为 26g-20g=6g;由质量守恒定律,乙的质量不变,可能作该反应的催 化剂,也可能没有参加反应。 A、乙的质量不变,可能作该反应的催化剂,也可能没有参加反应,故 A 错误; B、该反应的反应物为甲,生成物是丙和丁,符合“一变多”的特征,属于分解反应,甲是 分解反应的反应物,甲是一种化合物,故 B 正确; C、丙、丁在反应中的质量比是 12g:6g=2:1,故 C 错误; D、该反应的反应物为甲,生成物是丙和丁,符合“一变多”的特征,属于分解反应,故 D 错误。 故选 B。
8.在化学反应 2A+B2=2AB 中,A 与 B2 反应的质量关系如图所示,现将 6g A 和 8g B2 充分反 应,则生成 AB 的质量是
A.12g
B.11g
C.9g
D.14g
【答案】A
【解析】
【详解】
由两者反应时的质量关系可知,两者反应的质量比是 1:1,则可判断 6g A 和 8g B2 充分反
1:12,故选项错误。故选 B。
4.DNA 承载着生命遗传密码,胞嘧啶是 DNA 水解的产物之一,其化学式为 C4H5N3O,下
列有关叙述不正确的是( )
A.胞嘧啶中含有的最小粒子是氢原子 B.胞嘧啶中碳、氢、氮、氧四种原子的个数比为 4:5:3:1 C.胞嘧啶分子中质子数等于电子数 D.胞嘧啶是由碳、氢、氧、氮四种元素组成的 【答案】A 【解析】 【详解】 A、胞嘧啶是由胞嘧啶分子构成的,胞嘧啶分子是由碳原子、氢原子、氮原子与氧原子构 成的,其中最小的微粒是电子,故错误; B、由化学式可知,胞嘧啶中碳、氢、氮、氧四种原子的个数比为 4:5:3:1,故正确; C、分子是由原子构成的,在原子中,质子数=核外电子数,所以胞嘧啶分子中质子数等于 电子数,故正确; D、由化学式可知,胞嘧啶是由碳、氢、氧、氮四种元素组成的,故正确。 故选:A。 【点睛】 质子数=核外电子数=核电荷数=原子序数
13.2018 年 10 月 28 日,我国首艘国产航母第三次试海成功。用到的金属钛主要通过下列
反应制得:
①2FeTiO3+6C+7Cl2═ 2X+2TiCl4+6CO,②TiCl4+2Mg═ Ti+2MgCl2.则 X 的化学式为( )
A.FeCl3
B.FeCl2
C.Fe2O3
D.FeO
【答案】A
分子质量为:(102×2-32×3)÷4=27。
故选 D。
12.关于分子和原子两种微粒的叙述正确的是 A.物质只能由分子构成 B.分子在不断运动,原子静止不动 C.相同原子可能构成不同的分子 D.化学变化中分子数目一定发生变化 【答案】C 【解析】A、物质可以由分子、原子、离子微观三粒子构成,故错误; B、分子和原子都在不断的做无规则的运动,故错误; C、相同原子可能构成不同的分子,比如碳原子和氧原子可以构成一氧化碳和二氧化碳, 故正确; D、化学变化的过程中,分子的数目可能改变,可能不变,但分子的种类一定改变,故错 误。故选 C。
正确;
C、根据反应图示可知,转化①不属于化合反应,故 C 错误;
D、根据甲和丙的化学式,丙物质中碳元素的质量分数小于甲物质,故 D 错误。
故选 B。
