GSP季度质量信息汇总分析表
GSP认证表格大全(内含31个)
药品购进验收记录库存药品质量养护检查记录编号:检查日期:备注:1.进库达一个季度以上的药品方列入养护之列。
2.如检查中无质量问题,在质量情况一栏中,填写“正常”即可。
3.数量栏填写库存实际数量。
不合格药品报销销毁记录药品购进记录年月日药品储存记录表药品出库复核、配送记录药品质量查询、投诉、抽查情况记录库房温湿度记录表(常温库□阴凉库□冷库□)药品购进退出记录药品销后退回验收记录计量器具检定记录表制表人:年月日质量事故报告书报告单位(人):质量管理制度执行情况检查考核记录处方药留存和处方药销售记录枣庄康维药业连锁有限公司销售凭证枣庄康维药业连锁有限公司销售凭证药品缺货记录表顾客意见簿员工健康检查档案员工培训档案编号:药品质量档案表药品养护档案质量问题,应填写质量问题状况。
处理措施栏:有质量问题应填写具体处理措施,无质量问题填写“——”。
供货方档案表设施和设备及定期检查、维修、保养档案计量器具管理档案供货企业资质审批表药品资质审批表注:本表附药品生产许可证、营业执照、批准文件、质量标准、出厂检验报告书、样品、价格批文、GMP证书以及临床总结报告等资料。
不合格药品报损审批表编号:报告时间:年月日药品质量信息汇总表药品质量问题查询追踪记录表近效期药品催销表药品不良反应 / 事件报告表新的□严重□一般□医疗卫生机构□生产企业经营企业□个人□编码□□□□□□□□□□□□□□□□□□□单位名称:部门:电话:报告日期:年月日。
季度药品质量信息汇总分析表
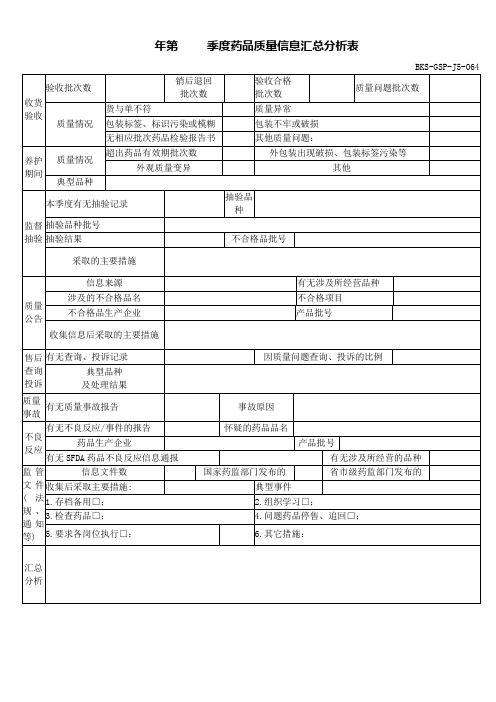
年第季度药品质量信息汇总分析表
BKS-GSP-J5-064
收货验收验收批次数
销后退回
批次数
验收合格
批次数
质量问题批次数质量情况
货与单不符质量异常
包装标签、标识污染或模糊包装不牢或破损
无相应批次药品检验报告书其他质量问题:
养护期间质量情况
超出药品有效期批次数外包装出现破损、包装标签污染等外观质量变异其他
典型品种
监督抽验本季度有无抽验记录
抽验品
种
抽验品种批号
抽验结果不合格品批号采取的主要措施
质量公告
信息来源有无涉及所经营品种涉及的不合格品名不合格项目
不合格品生产企业产品批号
收集信息后采取的主要措施
售后查询投诉有无查询、投诉记录因质量问题查询、投诉的比例典型品种
及处理结果
质量
事故
有无质量事故报告事故原因
不良反应有无不良反应/事件的报告怀疑的药品品名
药品生产企业产品批号
有无SFDA药品不良反应信息通报有无涉及所经营的品种
监管文件(法规、通知等)
信息文件数国家药监部门发布的省市级药监部门发布的收集后采取主要措施: 典型事件
1.存档备用□;
2.组织学习□;
3.检查药品□;
4.问题药品停售、追回□;
5.要求各岗位执行□;
6.其它措施:
汇总分析。
GSP-季度质量信息汇总分析表

购进
验收
验收总批次
拒收总批次
中药饮片验收总批次
中药饮片拒收总批次
中西成药验收总批次
中西成药拒收总批次
拒收
情况
中药饮片假伪品批次
中药饮片较多掺杂批
次
近效期批次
包装破损批次
来货超过冷藏温度批次
外观质量不合格批次
票、货不相符(含数量短 少)的批次
已来货未办理首营手 续的批次
无检验报告书批次(进口、 生物制品、自营品种)
典型查询、投诉事件:
监管
文件
信息文件数
质量事故
涉及品 规数
收集后采取主要措施:1.存档备用口;2.组织学习口;3.检查药品口;4•问题药品停售、追 回口;5.要求各岗位执行口;6.其它措施□:;
典型品种、事件:
汇总
分析
分析人:年 月日
改进
措施
建议人:年 月日
主管
领导
意见
签 字:年月日
来货非公司计划采购 品种的批次
养护
检查
检查品规总批次
质量问题品规总数
质里情况
循环检查批次
重点养护批次
近效期品规数
长时间储存品规数
典型品种:
监督
抽检
抽检品规总数
合格品规数
不合格品规数
未定品规数
不合格典型品种:
F=p曰. 质量
公告
公告不合格品规数
已经营品规数
收集信息后采取的主要措施:
查询
投诉
查询、投诉:
GSP质量记录表格精品资料

X X X药业有限公司质量记录X X X药业有限公司20年月—月质量体系内部审核记录�R E C112-V1�保存期限�年�200年月—200年月�归档/装订人�归档/装订日期�X X X药业有限公司质量记录质量记录清单编号�R E C100-V1序号记录名称编号保存期限责任部门1文件编制审批记录R E C101-V13年质管部门2文件发放回收记录R E C102-V13年质管部门3文件修订申请记录R E C103-V13年质管部门4文件废除销毁记录R E C104-V13年质管部门5文件状态档案R E C105-V13年质管部门6年度管理评审计划R E C106-V13年质管部门7质量管理制度执行情况检查考核记录R E C107-V13年质管部门8年度进货质量情况评审表R E C108-V13年质管部门9年度进货质量情况评审表(附表)R E C108A-V13年质管部门10纠正和预防措施处理单R E C109-V13年质管部门11质量方针目标实施情况检查表R E C110-V13年质管部门12质量体系内部审核计划R E C111-V13年质管部门13质量体系内部审核记录R E C112-V13年质管部门14质量信息台帐R E C113M-V13年质管部门15质量信息传递反馈表R E C113-V13年质管部门16药品分类目录R E C114M-V15年质管部门17药品质量档案R E C114-V15年质管部门18员工花名册R E C200M-V13年质管部门19员工登记表R E C200-V13年质管部门20员工体检情况登记表R E C201M-V13年质管部门21个人健康档案R E C201-V13年质管部门22年度质量教育培训计划R E C202M-V13年质管部门23培训签到记录表R E C202-V13年质管部门24会议签到记录表R E C203-V13年质管部门25培训考核统计评价记录R E C204-V13年质管部门26计划外培训申请表R E C205-V13年质管部门27员工培训登记表R E C206M-V13年质管部门28个人培训档案R E C206-V13年质管部门29卫生安全情况检查记录R E C207-V13年质管部门30仪器设备管理台帐R E C301M-V13年储运部门31仪器设备档案R E C301-V15年储运部门32仪器设备维修保养记录R E C302-V13年储运部门33仪器设备使用记录R E C303-V13年储运部门34合格供方一览表R E C401M-V15年业务部门35首营企业审批表R E C401-V15年业务部门36首营品种审批表R E C402-V15年业务部门37药品采购计划审批表R E C403-V13年业务部门38药品采购计划表�附表�R E C403A-V13年业务部门39药品到货通知单R E C404-V16年业务部门40药品直调申请审批表R E C405-V13年业务部门X X X药业有限公司质量记录序号记录名称编号保存期限责任部门41直调药品购进凭证R E C406-V16年业务部门42药品验收购进入库凭证R E C501-V16年质管部门43直调药品验收记录R E C502-V16年质管部门44药品外观质量检查记录R E C503-V16年质管部门45销后退回药品验收入库凭证R E C504-V16年质管部门46药品拒收单R E C505-V13年质管部门47药品货位卡R E C600-V13年储运部门48温湿度记录表R E C601-V13年储运部门49重点养护药品确定表R E C602-V13年储运部门50药品养护计划及检查记录R E C603-V13年储运部门51药品养护档案目录R E C604M-V15年储运部门52药品养护档案R E C604-V15年储运部门53药品养护情况季度报表R E C605-V13年储运部门54近效期药品催销表R E C606-V13年储运部门55药品出库/复核/销售凭证R E C701-V16年储运部门56购进退出药品出库复核凭证R E C702-V16年储运部门57合格顾客一览表R E C801M-V15年业务部门58顾客资信情况调查表R E C801-V15年业务部门59直调药品销售凭证R E C802-V16年业务部门60顾客投诉和处理情况记录表R E C803-V13年业务部门61顾客满意度调查表R E C804-V13年业务部门62销后退回药品台帐R E C805M-V13年储运部门63药品销后退回通知单R E C805-V13年业务部门64购进退出药品台帐R E C806M-V13年储运部门65药品购进退出通知单R E C806-V13年业务部门66药品质量复检通知单R E C807-V13年质管部门67药品停售通知单R E C808-V13年业务部门68药品恢复销售通知单R E C809-V13年质管部门69药品抽样单R E C810-V13年质管部门70药品回收通知单R E C811-V13年质管部门71不合格药品报告表R E C812-V13年质管部门72药品报损审批表R E C813-V13年质管部门73报损药品销毁单R E C814-V13年质管部门74不合格药品季度统计分析报表R E C815-V13年质管部门75药品质量查询登记表R E C816M-V13年质管部门76药品质量查询便函R E C816-V13年质管部门77质量事故报告记录表R E C817-V13年质管部门78质量事故分析报告书R E C818-V13年质管部门79药品不良反应监测调查表R E C819-V13年业务部门80药品不良反应报告表�S D A表格�3年业务部门编制人�编制日期�X X X药业有限公司质量记录文件编制审批记录编号�R E C101-V1序号�序号文件名称申请原因�申报部门负责人�日期�审核意见�审核人�日期�审批意见�批准人�日期�此表格在制订文件后使用。
药品储存养护信息汇总分析表

经汇总分析,现有养护措施能够保证在库药品质量要求。养护员:
质量管理部门意见
继续注意近效期药品及滞销药品的质量,建议业务部门慎重采购。
质量部经理:
药品储存养护信息汇总分析表
年第季度年月日
已经检查药品质量情况
本季度共养护在库药品品种**批次,未发现有质量异常。
重点养护品种质量情况
本季度重点养护品种药品品种**批次,经重点检查未发现有质量异常。
养护用设施、设备质量情况
仓库养护用设备、设备的质量情况:
对仓库的空调、温湿度检测系统、照明设施等检查,未发现有异常情况。
仓库温湿度情况
一月份:最高温度最高湿度
最低温度最低湿度
平均温度湿度
平均温度平均湿度
三月份:最高温度最高湿度
最低温度最低湿度
平均温度平均湿度
近效期药品及长时间储存药品情况
1、本季度在库近效期药品**品种,未发现有质量异常。
2、本季度长时间在库药品**品种,在养护过程中,未发现有质量异常。
仓储管理情况的检查
各库区管理较好、货位整齐、五距适当、色标明显,卫生状况较好。
汇总分析
通过对在库药品的养护(一般养护和重点养护),总体情况达到GSP条款要求,针对近效期的**品种,及长时间储存的**品种,共计**品种,加强养护管理,保证药品质量不受影响。建议公司领导通过对这个品种销售情况分析,结合仓库库存及库容,加强对进货计划的审核力度,以保证药品不积压,合理利用库容,对销量小或不稳定的采取少进货或不进货的方式,以减少品种挤占库容。
质量季度检查记录表

质量季度检查记录表
概述
本文档旨在记录质量季度检查的过程和结果,以便跟踪质量管
理的进展和改进。
本检查记录表适用于每个季度的质量检查,包括
以下内容:检查日期、检查对象、检查内容、检查结果、改进建议、执行负责人等。
检查日期: [填写日期]
质量季度检查的日期。
检查对象: [填写对象]
被检查的质量管理对象,如产品、服务、流程等。
检查内容: [填写内容]
质量季度检查的具体内容和范围。
可以包括但不限于以下方面:质量控制、问题解决、流程优化、员工培训等。
检查结果: [填写结果]
根据质量季度检查的内容和标准,填写检查结果。
可以采用评分、等级或简要描述的方式。
改进建议: [填写建议]
根据质量季度检查的结果,提出改进的建议和措施。
执行负责人: [填写负责人]
负责执行改进建议和措施的责任人。
总结
质量季度检查对于保证产品或服务质量至关重要。
通过记录和分析检查结果,可以持续改进和优化质量管理体系,提升整体质量水平。
(完整版)新版GSP表格大全

质量方针目标展开图质量方针:依法经营,质量第一,用户至上经理审批签字:年月日质量方针目标检查表质量方针:填表日期:年月日经理审批签字:年月日年度质量培训计划表编号:审批人:人力资源部:质量管理部:编号:培训主题:培训时间:编号:填表日期:主管领导:人力资源:质量管理部:填表人:员工培训效果调查表编号:填表日期:员工个人培训教育档案档案编号:年度企业员工健康检查汇总表编号:员工健康档案编号:建档时间:注:应将历次体检结果证明文件存入档案。
文件编码登记表页码:文件发放、回收记录编号:编号:编号:文件销毁审批记录编号:信息联系处理单编号:本单一式三份:信息发出部门、接收部门、质量管理部门各一份编号:建档时间:编号:药品购货计划表(年第季度)编号:制表日期:制表人:业务部门经理:质管部:财务部:总经理/副总经理:19首营企业审批表编号:填表日期:首营品种审批表编号:药品购进记录编号:22购进药品验收记录编号:23销后退回药品验收记录编号:24药品验收入库通知××××药品仓储保管组:以下购进/退回药品经质量检查验收合格,请予办理入库手续。
编号:验收员:保管员:入库日期:25编号:药品停售通知单年第号名有关部门:以下药品因质量问题决定停售,请按有关规定采取有效措施停止出售,等等处理。
药品通用名称规格产品批号有效期生产日期生产企业质量管理部年月日(一式四联:一联质管部留存,二联仓储部,三联业务部门,四联必要时送外联客户)解除停售通知单解除停售通知单年第号各有关部门:以下药品经质量复查结果合格,撤消年第号“药品停售通知单”,请恢复正常出库发货及销售,特此告知。
药品通用名称规格产品批号有效期生产日期生产企业质量管理部年月日(一式四联:一联质管部留存,二联仓储部,三联业务部门,四联必要时送外联客户)药品质量复查报告单编号:说明:本表一式三联,一联申请复查部门留存,二联质量管理部门复查后留存,三联复查后返回申请部门。
GSP监督检查情况汇总表
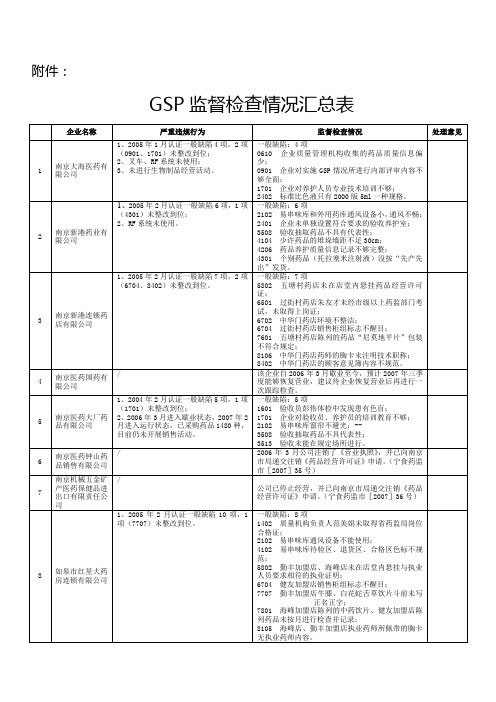
2402标准比色液只有2000版5ml一种规格。
2
南京新港药业有限公司
1、2005年2月认证一般缺陷6项,1项(4301)未整改到位;
2、RF系统未使用。
一般缺陷:6项
2102易串味库和外用药库通风设备小,通风不畅;
2401企业未单独设置符合要求的验收养护室;
2102易串味库通风设备不能使用;
4102易串味库待验区、退货区、合格区色标不规范;
5802勤丰加盟店、海峰店未在店堂内悬挂与执业人员要求相符的执业证明;
6704健友加盟店销售柜组标志不醒目;
7707勤丰加盟店牛膝、白花蛇舌草饮片斗前未写正名正字;
7801海峰加盟店陈列的中药饮片、健友加盟店陈列药品未按月进行检查并记录;
1502企业验收员、养护员未经市药监部门的培训;
1601企业验收、养护、保管员健康检查时未做视力、辩色力检查;
1702企业质量负责人未经省药监部门的培训;
1801库房内环境欠整洁;
2402标准比色液过期;
2501企业设施设备档案不够健全(电猫、电子灭蚊灯未建立档案);
3701 05-06年天平未检定;
35
涟水县松寿堂药业零售连锁有限公司
/
企业于2007年4月10日停业,GSP证书由省局收回。
36
涟水县医药公司
/
企业于2007年4月10日停业,GSP证书由省局收回。
37
盱眙都梁大药房连锁有限公司
1、2006年认证跟踪检查严重缺陷1项、一般缺陷4项,1项(0901)未整改到位。
一般缺陷:3项
0901企业07年GSP内部评审报告内容不全面;
7705一乾药店拆零记录不准确。拆零复方新诺明30板错写成50板。
药品质量信息汇总分析表部分

药品质量信息汇总分析表×××2013 年8 月□报刊杂志□上级来文来源□其他网上下载收集时间2013年23日8月收集人×××国家总局办公厅同意注销北京双鹤现代医药技术有限公司溴异丙)东莨菪碱气雾剂药品批准证明文件及批准文号(国药准字H11022168 质量信息分析在今后的经营活动中也要禁止该我公司未经营过该品种,经排查,品种的流入管理应用备注1 / 16×××药品质量信息汇总分析表2013 年8 月□报刊杂志□上级来文来源□其他网上下载收集时间201327日年8月收集人×××充分认识到了当前禁毒工作的严峻形势,严格按照《通知》和《关严的有关要求,于切实加强部分含特殊药品复方制剂销售管理的通知》杜绝现金交格审查供货方和销售方资质,加强特药的流通和票据管理,质量信息分析易,防止流入非法渠道附件的相关信息表已报送临沂市食品药品监督管理管理应用备注2 / 16药品质量信息汇总分析表×××2013 年8 月□报刊杂志□上级来文来源□其他网上下载收集时间2013年8月30日×××收集人的规定,(试行)》国家总局根据《处方药与非处方药分类管理办法种,中成药种药品(化学药品组织论证和审定,将肠炎宁胶囊等132种药品名单及其非处方药说明书范本(见1113种)转换为非处方药,不得继续使用原药品说明书月30日前,102013;附表)生产企业在年质量信息分析)。
双跨的品种除外(3 / 16药品质量信息汇总分析表×××9月2013 年□报刊杂志□上级来文来源□其他网上下载收集时间日月9 年20139收集人×××3264年上半年完成的市两级药品检验机构本质量公告为省、2013批次产品不符合标准规定,抽验批的基本药物抽验情况汇报,其中,6 99.82%合格率为,被抽验基本药物总体质量良好。
年 季度药品质量信息报表
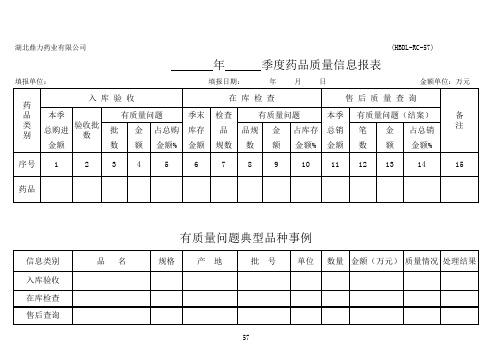
售 后 质 量 查 询 有质量问题(结案) 笔 数 12 金 额 13 占总销 金额% 14
有质量问题典型品种事例
信息类别 入库验收 在库检查 售后查询
57
品
名
规格
产 地
批 号
单位
数量 金额(万元) 质量情况
7)
额单位:万元
备 注Leabharlann 15处理结果湖北鼎力药业有限公司
(HBDL-RC-57)
年
填报单位: 填报日期:
季度药品质量信息报表
年 月 日 金额单位:万元
药 品 类 别 序号 药品
入 库 验 收 本季 总购进 金额 1 2 验收批 数 批 数 3 有质量问题 金 额 4 占总购 金额% 5 季末 库存 金额 6
在 库 检 查 检查 品 规数 7 品规 数 8 有质量问题 金 额 9 占库存 金额% 10 本季 总销 金额 11
质量信息分析表
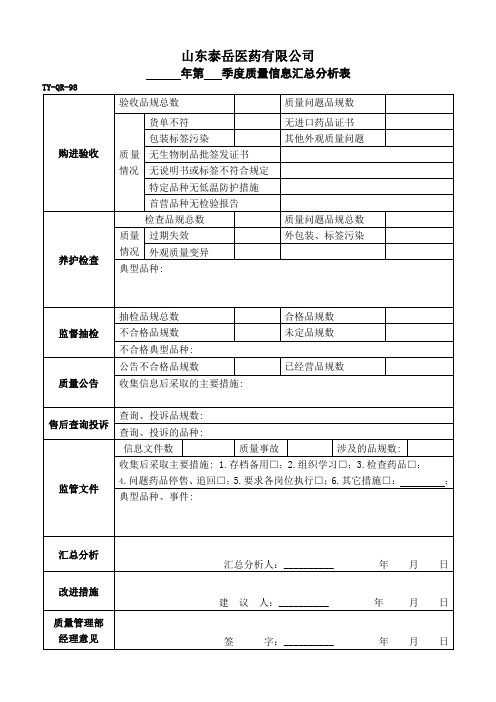
年第季度质量信息汇分析表
TY-QR-98
购进验收
验收品规总数
质量问题品规数
质量情况
货单不符
无进口药品证书
包装标签污染
其他外观质量问题
无生物制品批签发证书
无说明书或标签不符合规定
特定品种无低温防护措施
首营品种无检验报告
养护检查
检查品规总数
质量问题品规总数
质量情况
过期失效
外包装、标签污染
4.问题药品停售、追回□;5.要求各岗位执行□;6.其它措施□:;
典型品种、事件:
汇总分析
汇总分析人:__________年 月日
改进措施
建议人:__________年月日
质量管理部
经理意见
签字:__________年 月日
外观质量变异
典型品种:
监督抽检
抽检品规总数
合格品规数
不合格品规数
未定品规数
不合格典型品种:
质量公告
公告不合格品规数
已经营品规数
收集信息后采取的主要措施:
售后查询投诉
查询、投诉品规数:
查询、投诉的品种:
监管文件
信息文件数
质量事故
涉及的品规数:
收集后采取主要措施:1.存档备用□;2.组织学习□;3.检查药品□;
养护定期汇总和分析情况表

填报日期: 年 月 日
上报部门如:
2.储存温度是否符合规定要求?
□ 是 □否, 如:
3.五距是否符合规定要求?
□是 □否
4.药品有无倒置现象?
□有 □无
5.放置药品是否轻拿轻放
□是 □否
1.储存条件
□符合GSP规定 □不符合GSP规定
2.防护措施
□有
□无
3.库内卫生环境 □卫生 清洁 符合规定
□待打扫 □不符合规定
1.是否按时记录? □是
□否
1.库房温湿度数据的监测
2.超出范围时是否排查原因? □是
3.是否采取措施?
□是
□否 □否
4.温度超标报警次数:
应急措施处理次数:
1.是否有避光、防鼠、除湿等措施 □是
□否
2.设备设施是否正常运行
2.各类设备运行是否运行 □是
年 季度养护药品质量信息定期汇总和分析情况表
填表人( 养护员): 1.指导督促储存人员对药品进行合理储存与作业
2.检查并改善储存条件、防护措施、卫生环境
3.对库房温湿度进行有效监测、调控
4.重点养护品种养护情况 5.自动生成药品养护计划的药品养护情况 6.养护档案建立情况 7.养护过程中所发现的质量问题
□否
3.每天是否检查冷库 □是
□否
1.按制度规定已重点养护 □
2.未按制度规定重点养护 □
1.按制度规定已养护 □
2.未按制度规定养护 □
1.已建立□ 2.未建立□ 分建立□ 1.未发现 □
3.部
2.发现的质量问题(质量变异、包装破损、标签污染、超有效期等):
典型品种:
产生的原因:
比率:
改进措施:
(模板)GSP质量记录表格汇总之一【竖排】

文件会稿单文件借(查)阅登记表文件销毁申请单文件收回销毁记录ABYY-ZR008-00 文件名称: 文号或编码:《药品经营质量管理规范》内部评审和公司质量管理体系审核计划ABYY-ZR011-00按照国家《药品经营质量管理规范》的要求以及公司制度规定,公司应组织人员对每年度的质量管理体系进行审核以及对《药品经营质量管理规范》在我公司的实施情况进行内部评审。
公司《质量管理制度》中的“质量管理体系审核制度”的7.2条具体规定:公司的质量管理体系审核应“每年进行一次,按照公司质量管理制度规定进行。
”同时还明确了,在进行质量管理体系审核时“同时实施《药品经营质量管理规范》的内部评审”。
200 年度体系审核和“GSP”评审计划安排如下:一.检查时间:二.检查人员:三.检查内容:1.质量管理体系运行状况;2. 《药品经营质量管理规范》实施情况;四.评审时间:五.评审地点:六.评审内容:1.质量体系运行情况;2.本公司经营方式和经营范围; *04013.组织机构与管理职责; 0501-07024.质量管理制度执行情况; *0801- *08025.人员与培训教育情况; 1001-17026. 健康体检 1601-16027.经营和仓储设施、设备运行状态; 1801-25018.进货质量管理; 2701-34019.入库验收质量管理;*3501-351310. 不合格药品管理; 4001-400511.药品保管与储存; 3601、*4101-411112.药品在库养护 3701、4201-420913.药品出库管理 4301-450114. 药品运输管理 4601-490215.药品销售和售后服务工作; 5001--570216.存在问题的整改及预防措施。
七.评审方式:会议评审。
八.评审部门:公司质量领导小组。
九.评审结果:报告形式。
四川省XXX医药有限公司质量管理部年月日《药品经营质量管理规范》实施情况内部评审公司质量管理体系年度审核审批表ABYY-ZR012-00编制时间:年月日四川省XXX医药有限公司质量管理体系评审记录表ABYY-ZR013-00不合格项通知书ABYY-ZR014-00 通知部门:编号:通知发出部门:GSP内部评审小组整改检查:质量管理部年月日整改实施报告ABYY-ZR015-00 GSP内部评审小组:编号:报告部门:经办人:质量信息传递、反馈表ABYY-ZR017-00建档日期:存档编号:ABYY-ZR018-00质量管理工作随笔四川省XXX医药有限公司四川省XXX医药有限公司质量管理工作随笔日期:事件:处理与结果:日期:事件:处理与结果:日期:事件:处理与结果:日期:事件:处理与结果:制度执行情况监督检查记录ABYY-ZR019-00制度执行情况监督检查记录整改通知单药品不合格报告、确认单四川省XXX医药有限公司药品不合格报告、确认单药品拒收通知单ABYY-ZR024-00四川省XXX医药有限公司药品拒收通知单药品质量复检通知单ABYY-ZR025-00。
季度药品养护汇总分析表及模版
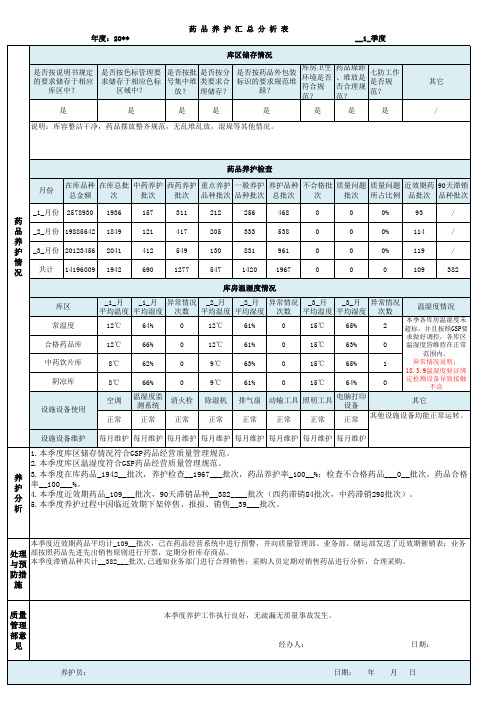
空调
温湿度监 测系统
消火栓
除湿机
排气扇
动输工具
照明工具
电脑打印 设备
其它
正常
正常
正常
正常
正常
正常
正常
正常 其他设施设备均能正常运转。
设施设备维护 每月维护 每月维护 每月维护 每月维护 每月维护 每月维护 每月维护 每月维护
1.本季度库区储存情况符合GSP药品经营质量管理规范。 2.本季度库区温湿度符合GSP药品经营质量管理规范。 养 3.本季度在库药品_1942__批次,养护检查__1967___批次,药品养护率_100__%;检查不合格药品___0__批次,药品合格 护 率__100___%。 分 4.本季度近效期药品_109___批次,90天滞销品种__382____批次(西药滞销84批次,中药滞销298批次)。 析 5.本季度养护过程中因临近效期下架停售、报损、销售__39___批次。
12℃
64%
0
12℃
61%
0
15℃
65%
本季各库房
12℃
66%
0
12℃
61%
0
15℃
63%
0
温湿度皆维持在正常
范围内。
8℃
62%
0
9℃
63%
0
15℃
65%
1
异常情况说明:
18.3.9温湿度验证绑
8℃
66%
0
9℃
61%
0
15℃
64%
0
定检测设备导致接触 不良
防措
施
质量 管理 部意
见
养护员:
本季度养护工作执行良好,无疏漏无质量事故发生。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
购进验收
验收品规总数
质量问题品规数
质量情况
货单不符
无进口药品证书
包装标签污染
其他外观质量问题
批号或有效期不符
无说明书或标签不符合规定
特定品种无低温防护措施
中药饮片无标签
陈列检查
检查品规总数
质量问题品规总数
质量情况
过期失效
外包装、标签污染
外观质量变异
典型品种:(可附明细)
监督抽检
抽检品规总数
合格品规数
不合格品规数
未定品规数
不合格典型品种:
质量公告
公告不合格品规数
已经营品规数
收集信息后采取的主要措施:
查询投诉
查询、投诉品规数:
查询、投诉的品种:(可附明细)
监管文件
信息文件数
质量事故
涉及的品规数:
收集后采取主要措施: 1.存档备用□;2.组织学习□;3.检查药品□;
4.问题药品撤柜□;5.要求各岗位执行□;6.其它措施□:;
典型品种、事件:(可附明细)
汇总分析及
改进措施
汇总分析人:__________年 月
