肺癌重磅新药在中国获批上市!
新型抗癌药能治25种癌症!

国内有望上市⼀半患者肿瘤缩⼩!国内有望上市新型抗癌药能治25种癌症!⼀半患者肿瘤缩⼩!去年,全球第三款不限癌种的抗癌药恩曲替尼重磅上市,再次引起了巨⼤的轰动!与⾸款上市的NTRK抑制剂拉罗替尼不同,恩曲替尼针对的靶点和癌症更多,不仅对NTRK1 / 2/3融合的患者有“特效”,同时对ROS1和ALK基因的融合和改变的癌症也能发挥巨⼤的抗癌功效,并且还有超强的⼊脑效果,这意味着,对⼤部分药物都束⼿⽆策的脑转移,这款药物也能完美应对。
此外,这款药物之前公布的数据显⽰,对于存在NTRK融合的⼉童患者,有效率能够⾼达100%,这是史⽆前例的。
可以说,这是⼀款药物是不分年龄,不分癌种,有效率超⾼的抗癌“神药”。
官⽅数据:有效率57%!长效缓解在官⽹公布的TRK融合癌患者的三项⼤型临床试验汇总数据显⽰,恩曲替尼的总缓解率ORR为57%,其中7.4%的患者完全缓解(肿瘤全部消退)。
并且对于特定的⼈群,恩曲替尼的有效率能达到100%,⽐如在研究中4例TPR-NTRK1融合的患者,肿瘤全部缩⼩。
续缓解时间从2.8个⽉~26个⽉不等。
研究证实:对多种癌症有效⽬前已发现NTRK融合存在于超过25类癌症中,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,成⼈和⼉童患者都可以使⽤。
◀肺癌▶关于ROS1阳性⾮⼩细胞肺癌的汇总分析包括来⾃Ⅱ期STARTRK-2,Ⅰ期STARTRK-1和Ⅰ期ALKA-372-001的数据,招募了15个国家/地区和150个临床试验地点的患者,这些患者都是局部晚期或转移性ROS1融合的⾮⼩细胞肺癌患者,在可评估的53名患者中,结果显⽰:有77%(41例)的患者在数据截⽌时达到了缓解(ORR),其中包括3名(6%)完全缓解(CR),38名(72%)部分缓解( PRs),以及1名(2%)病情稳定的患者。
中位⽆进展⽣存时间(PFS)为19.0个⽉。
%!其中20%的患者完全缓解!值得⼀提的是,这些患者包括23名未治疗和治疗的伴有脑转移患者,反应率为55%!治疗前治疗两个周期后◀消化道肿瘤▶在2020年最新举⾏的额ESMO⼤会上,专门采集了entrectinib 在ALKA-372-001和STARTRK-1,STARTRK-2研究中NTRK融合阳性的胃肠道恶性肿瘤患者数据。
科研界的最新突破:成功开发出能够治愈癌症的新药

1.引言癌症一直是全球范围内的重大健康问题,给患者和其家人带来了巨大的负担。
多年以来,科学家们一直在努力寻找治愈癌症的有效方法。
近期,科研界取得了一项令人振奋的突破:成功开发出能够治愈癌症的新药。
本文将介绍这一突破的背景、关键技术和前景展望。
2.背景癌症是由于异常细胞的不受控制增殖和扩散而引起的疾病。
传统的癌症治疗方法包括手术切除、放射疗法和化学治疗。
然而,这些方法存在着一些限制,例如手术切除可能无法完全清除癌细胞,放射疗法会对正常细胞造成损伤,而化学治疗则可能导致副作用。
为了克服这些限制,科研界开始探索新的治疗策略。
其中一种新方法是利用靶向治疗,即通过针对特定癌细胞上的分子靶点,抑制其生长和扩散。
这种方法被认为有望提高癌症治愈率,并降低对正常细胞的伤害。
3.关键技术新药的成功开发离不开关键技术的支持。
在这项突破性研究中,科学家们利用了基因编辑技术和人工智能算法,以及针对癌症细胞特异性靶向治疗的策略。
首先,科学家们使用基因编辑技术对癌症细胞进行基因改造,使其表达一种特定分子。
这种分子具有高度的亲和力,可以与新药中的活性成分结合,并抑制癌细胞的生长。
通过这种方式,新药能够更加精确地作用于癌细胞,减少对正常细胞的损害。
其次,科学家们利用人工智能算法对大量的癌症数据进行分析和模拟,找出与癌细胞增殖和扩散相关的关键信号通路。
然后,他们设计出一种新型的药物,能够干预这些信号通路,并阻止癌细胞的生长和扩散。
这种个性化的治疗策略可以根据患者的具体情况进行调整,提高治疗效果。
4.新药的临床试验在开发出新药之后,科学家们进行了一系列的临床试验,以评估其安全性和有效性。
这些试验包括药物的毒性实验、细胞培养实验、动物模型实验和临床前试验。
在动物模型实验中,科学家们将新药注射到癌症小鼠体内,并观察其对肿瘤的影响。
结果显示,新药可以显著抑制肿瘤的生长,并且没有引起明显的副作用。
在细胞培养实验中,科学家们使用癌细胞株进行了药物的体外评估,并发现新药能够选择性地抑制癌细胞的增殖和扩散。
2021.v5版非小细胞肺癌NCCN指南新鲜出炉!十大靶点治疗方案更新解读!

2021.v5版⾮⼩细胞肺癌NCCN指南新鲜出炉!⼗⼤靶点治疗⽅案更新解读!NCCN全称美国国⽴综合癌症⽹络(National Comprehensive Cancer Network ),每年都会发布各种恶性肿瘤临床实践指南,已成为全球临床医师遵循和认可的临床治疗标准和参考,意义重⼤。
2021年6⽉,NCCN官⽹将⾮⼩细胞肺癌(NSCLC)的临床实践指南更新⾄第五版,主要是两⼤重磅抗癌新药JNJ-6372和AMG510接连提前获批上市,实现了EGFR 20ins和KRAS两⼤靶点0靶向药的突破,对肿瘤患者意义重⼤,指南及时将这些抗癌“特药”纳⼊指南,给病友们带来新的选择和希望。
全球肿瘤医⽣⽹医学部为病友们整理了指南更新的最新治疗⽅案,希望给⼤家带来帮助。
NCCN指南:⾮⼩细胞肺癌需要检测的⼗⼤靶点⽬前,⾮⼩细胞肺癌NCCN指南推荐肺癌患者应检测的靶点为EGFR(19del和L858R)、EGFR 20ins、KRAS G12C、ALK、ROS1、BRAF、NTRK1/2/3、MET、RET、PD-L1⼗⼤靶点。
注:最新版指南推荐的检测中,将敏感的EGFR突变阳性,分为EGFR突变阳性(19del和L858R),以及EGFR 20外显⼦插⼊突变阳性,此靶点之前没有专门获批的靶向药物,4代EGFR药物Amivantamab-vmjw上市,使得其成为可⽤药靶点,这是EGFR外显⼦20插⼊突变肺癌患者的⾸款靶向疗法,是医学届对于这部分患者的⼀项重⼤进步,具有⾥程碑式的意义!最新版指南推荐的检测中,增加了KRAS G12C阳性突变,此靶点堪称史上“最难治”靶点,研发40年终于在今年迎来新药AMG510这款重磅药物上市。
肺癌NCCN指南⼗⼤靶点治疗⽅案更新解读EGFREGFR(epidermal growth factor receptor,ErbB-1或HER1)全称表⽪⽣长因⼦受体。
主要在肺腺癌、亚裔、⾮吸烟及⼥性患者中,⼤约有 15% 的⽩种⼈和 30-50% 的亚洲⼈中有 EGFR 基因突变。
典型新闻报道内容

典型新闻报道内容中国科学家成功研发出新型抗癌药物近日,中国科学家在抗癌领域取得了重大突破,成功研发出一种新型抗癌药物。
这一消息引起了广泛的关注和热议。
据悉,这种新型药物具有独特的作用机制,能够有效抑制癌细胞的生长和扩散,为癌症患者带来了新的希望。
该新型抗癌药物是由一支由中国科学院领导的科研团队共同研发的。
经过多年的努力和不懈探索,科学家们最终成功地合成了这种具有抗癌活性的化合物。
据介绍,这种药物通过靶向癌细胞的特定分子,干扰其正常的生物活动,从而达到抑制癌细胞生长的效果。
与传统的化疗药物相比,这种新型药物具有更高的选择性和更低的毒副作用,能够更好地保护患者的健康。
在临床试验中,这种新型抗癌药物显示出了良好的疗效。
研究人员对一批癌症患者进行了治疗,并观察了药物的疗效和安全性。
结果显示,该药物在抑制肿瘤生长和减轻患者症状方面表现出了显著的效果。
同时,患者在接受治疗期间的生活质量也得到了明显的改善。
这一研究成果的取得对于抗癌领域具有重要的意义。
癌症一直是全球范围内的重大健康问题,给患者和家庭带来了巨大的负担。
而这种新型抗癌药物的问世,为癌症患者提供了一种更有效、更安全的治疗选择,有望为他们带来更多的生存机会和康复希望。
然而,科学家们也表示,这种新型抗癌药物目前仍处于研发阶段,还需要进一步的临床试验和验证。
他们将继续努力,进一步完善药物的性能和疗效,争取尽早将其推向市场,造福更多的癌症患者。
中国科学家成功研发出新型抗癌药物的消息给人们带来了新的希望。
这一突破性的科研成果将为癌症患者提供一种更有效、更安全的治疗选择,有望为他们带来更多的生存机会和康复希望。
相信在科学家们的不懈努力下,抗癌事业将取得更大的进展,为人类健康事业作出更大的贡献。
最新抗癌药替拉扎明详细介绍

一类新药—替拉扎明项目简介一、概况据世界卫生组织(WHO)统计,全球平均每年死于恶性肿瘤者达690万人,新发病为870万例,且这一数字还在逐年增加。
全世界每年新确诊肿瘤疾病患者达到1000万人,预计到2020年,全世界每年将新发生2000万例肿瘤,其中1400万例在亚洲、非洲和拉丁美洲的发展中国家。
据我国卫生部统计,目前我国每年有106万左右的恶性肿瘤新生患者,同时有106.7万左右的良性肿瘤患者,两者合计约有212.7万,即肿瘤的全国发病率约在1.65‰左右。
每年,我国因肿瘤死亡人数约有154万人左右,癌症(肿瘤)成为继心脑血管疾病后的我国第二大疾病。
缺氧是诱导肿瘤血管生成的一个非常重要的因素,在目前国内外均有大量的实验和临床研究证实了这一点。
缺氧对促进肿瘤血管生成的调节主要是通过在分子水平上,缺氧对促进肿瘤血管生成的细胞因子转导的调节而实现的。
与缺氧有关的促进肿瘤血管生成的细胞因子有如下几种。
1、HIF-1(缺氧诱导因子-1),2、VEGF(血管内皮生长因子)以及血管内皮生长因子的两个受体(flt-1,KDR/flk-1),3、bFGF(碱性成纤维细胞生长因子),4、IGF(胰岛素样生长因子)及其主要受体IGF-IR,5、MMP(基质金属蛋白酶)。
目前,临床上对肿瘤的治疗仍以手术和放、化疗为主,但由于在实体瘤中存在着10%~50%的乏氧细胞,这些乏氧细胞对射线及化疗药物的耐受性比有氧细胞强2.5~3倍。
因而,在常规放(化)疗剂量治疗时,乏氧细胞不能被有效杀死,于是埋下了癌症复发祸根。
要想杀灭肿瘤乏氧细胞,只有加大放(化)疗剂量,然而,这又给患者带来难以承受的毒副反应和痛苦。
总之,乏氧细胞是肿瘤难治愈、易复发和转移的重要因素之一。
二、项目优势替拉扎明(tirapazamine,TPZ)化学名称:3-氨基-1,2,4苯并三唑-1,4-二氮-氧化物(3-Amino-1,2,4-benzotuiazine-1,4-dioxide)又名Win59075或SR4233,是一种新型的生物还原活性物。
恒瑞医药:艾瑞昔布获批上市意义重大
第25期晨会掘Industry ·责任编辑:蔡晓铭荫蔡晓铭47本周市场继续下行,尤其是上证指数周四大幅跳空低开并震荡走低,令市场情绪更感悲观。
周五开盘后略微下探就已跌破今年年初的阶段低点2661点。
策略方面,我们前期已提示尽管从估值来看市场处于历史低位,但新股的快速发行、解禁股的陆续涌向市场,在中期内增加了市场大量的证券供应,因此单纯从估值的角度出发制定操作策略仍显单薄。
面对这样一个具有一定特殊性的市场时期,投资者应采取偏于保守的策略。
国泰君安本周晨会推荐了恒瑞医药(600276),公司研制的国家一类新药“艾瑞昔布片及原料”获得国家食品药品监督管理局颁发的《新药证书》及《药品注册批件》。
艾瑞昔布是新一代非甾体抗炎类创新药,主要用于缓解骨关节炎的疼痛症状,这是恒瑞医药第一个获批上市的国家一类新药。
艾瑞昔布的生产上市,国泰君安指出这一事件对恒瑞医药而言具有标志意义,将掀开公司成长的新篇章。
如果说过去十年是恒瑞医药抢仿全球重磅品种的十年,那么下一个十年将是公司收获专利品种的十年。
凭借产品梯队,恒瑞医药有望完成从“抢仿”到“创新”的华丽转身。
具体的看,艾瑞昔布是新一代非甾体抗炎类创新药,属于COX-2酶抑制剂,主要用于缓解骨关节炎的疼痛症状。
恒瑞医药于1999年开启该品种的临床前研究,2002年进入临床一期,被科技部列入国家“863计划。
艾瑞昔布是公司第一个获批上市的国家一类新药,有望成为5~10亿销售规模的重磅品种。
从市场规模来看,我国类风湿性关节炎药物市场一直维持着快速增长的态势,年复合增长率22.3%,2009年的销售总额达到了38.56亿元,同比增长高达41.86%,甚至要高于近几年增长势头强劲的抗肿瘤和降压药市场。
国泰君安预计,此类药物未来能继续保持20%复合增速。
估计国内类风湿关节炎用药市场的理论规模就达到140亿元;若市场占有率达到10%,就能成为过10亿的重磅品种。
对于市场此前略有担忧的药品的安全性问题,国泰君安的观点是昔布类安全性问题可控。
中国十大癌症特效药

中国十大癌症特效药癌症,作为目前威胁人类生命和健康的头号杀手,正愈来愈收到社会各界的关注,人们对于癌症的检测和抗癌的进程也不断取得各种突破。
抗癌是一个漫长而艰辛的过程,而治疗癌症更需要根据体检的病理类型和分区来决定相应的治疗方法。
针对药物治疗,目前中国主要的十大抗癌特效药分别有以下几种:1、奥沙利铂(Oxaliplatin)由瑞士Debiopharm公司研究开发,法国Sanofi公司生产销售,1999年10月在法国率先上市,随后在欧洲、南美等地上市。
我国于1999年批准进口奥沙利铂注射剂。
此品对大肠癌、非小细胞肺癌、卵巢癌等多种动物和人类肿瘤细胞株均有显着的抑制作用。
2、紫杉醇(Paclitaxel)美国百时美-施贵宝公司开发的一个全新植物抗癌药,1993年10月首次在美国上市,国内首次上市的时间为1995年。
该产品主要以抑制肿瘤细胞重要的分裂方式(微管蛋白合成)使肿瘤体积逐渐缩小,而非直接杀死白细胞。
3、异长春花碱(Vinorebine)又名长春瑞滨、去甲长春碱,由法国PierreFabre公司开发,1989年法国上市,1992年在国内上市。
此品是一种半合成的第四代长春花属生物碱,上市剂型为静脉注射剂,规格为10毫克誜10毫升,是广谱抗肿瘤药。
4、多西他赛(Docetaxel)法国赛诺菲-安万特公司研制开发并生产的一种新型抗肿瘤药物,用于治疗晚期乳腺癌和非小细胞瘤。
1995年4月首次在墨西哥上市,随后在英、美、法、意、德、日等地上市,1996年进入我国,自2002年起先后有多家国内企业开始生产仿制品。
5、吉西他滨(Gemcitabine)由礼莱公司开发,1995年在瑞典、荷兰、芬兰和南非等地首次上市,1999年12月批准在国内应用。
此药是二氟核苷类抗代谢抗癌新药,为去氧胞苷的水溶性类似物,最初开发时用于抗病毒。
目前,该药已批准用于治疗胰腺癌和非小细胞肺癌,用于治疗乳腺癌、卵巢癌、膀胱癌、前列腺癌以及白血病和淋巴瘤的研究正在进行。
首个国产曲妥珠单抗获批!中国生物类似药百花齐放

⾸个国产曲妥珠单抗获批!中国⽣物类似药百花齐放8⽉14⽇,复宏汉霖曲妥珠单抗(HLX02)正式获得国家药品监督管理局批准上市,商品名为汉曲优®。
今年7⽉27⽇,欧盟委员会(EC)已正式批准HLX02在欧盟的上市销售申请,商品名为Zercepac®。
汉曲优®成为⾸个由中国企业开发、⽣产和上市的Herceptin®(曲妥珠单抗)⽣物类似药,也是⾸个成功登陆欧盟的“中国籍”单抗⽣物类似药,开辟了中国医药企业参与单抗⽣物类似药“世界杯”⽐赛的先河。
继去年2⽉国内⾸个⽣物类似药利妥昔单抗注射液汉利康®(HLX01)获批上市之后,复宏汉霖拥有了第2款进⼊商业化阶段的产品。
国内获批上市的⽣物类似药基于适应症外推,汉曲优®同时获批原研全部3个适应症根据我国现⾏的《⽣物类似药研发与评价技术指导原则》以及药品注册管理办法,⽣物类似药在临床开发时可以采⽤“适应症外推”的策略来缩减研发成本和周期,但是要求外推的适应症应当与开展⽐对试验的适应症具有相同的临床相关病理机制、作⽤机理以及靶点,并且外推的适应症应当是原研产品已经在国内批准上市的适应症。
汉曲优®此次获批了与原研产品Herceptin在中国完全相同的3个适应症,包括HER2阳性早期乳腺癌、HER2阳性转移性乳腺癌和HER2阳性转移性胃癌。
从管线产品的开发进度上看,复宏汉霖⽬前已经在⾎液肿瘤(⾮霍奇⾦淋巴瘤)和实体瘤(乳腺癌、胃癌)都有了商业化阶段的产品,这也将为复宏汉霖的其他肿瘤产品HLX04(贝伐珠单抗,III期完成)、HLX10(PD-1单抗,III期)、HLX07(EGFR单抗,II期)的商业化推⼴打下基础。
⾃动进⼊医保,降低患者⽀付负担乳腺癌在我国⼥性恶性肿瘤中的发病率和死亡率分别居第1位和第5位,2019年新增病例约为30.4万,占⼥性恶性肿瘤发病的17.10%,呈现上升的趋势。
HER2突变阳性率在乳腺癌中⼤约为20%。
替雷利珠单抗在肺癌治疗的研究进展

替雷利珠单抗在肺癌治疗的研究进展
刘自力
【期刊名称】《临床肺科杂志》
【年(卷),期】2024(29)4
【摘要】肺癌是发病率和死亡率很高的恶性肿瘤,严重威胁人类健康,给社会和患者家庭带来重大的经济负担。
免疫治疗在肺癌领域进展最快,已成为肺癌治疗重要选择之一,替雷利珠单抗是我国自主研发的程序性死亡受体1抑制剂创新药,具有独特的结构和作用机制,其联合化疗一线治疗晚期非小细胞肺癌以及单药二线或三线治疗晚期非小细胞肺癌,替雷利珠单抗均表现出良好的疗效和安全性。
【总页数】9页(P623-631)
【作者】刘自力
【作者单位】淮北矿工总医院呼吸与危重症医学科
【正文语种】中文
【中图分类】R73
【相关文献】
1.替雷利珠单抗联合安罗替尼治疗晚期非鳞状非小细胞肺癌的临床效果
2.替雷利珠单抗联合PC方案治疗晚期肺癌的疗效及对血清PI3K、Akt的影响
3.替雷利珠单抗联合铂类治疗中晚期非小细胞肺癌的近期疗效和安全性研究
4.白蛋白紫杉醇与卡铂联合替雷利珠单抗治疗晚期非小细胞肺癌的效果
5.替雷利珠单抗联合安罗替尼治疗晚期非小细胞肺癌的临床研究
因版权原因,仅展示原文概要,查看原文内容请购买。
癌症靶向药年终大盘点

随着医学科技的飞速发展,癌症治疗领域取得了举世瞩目的成就。
靶向药物作为一种新型的抗癌治疗手段,以其精准、高效、低毒等特点,受到了全球医学界的广泛关注。
2021年,我国癌症靶向药物研发取得了丰硕的成果,本文将对2021年癌症靶向药进行年终大盘点。
一、肺癌靶向药物1. EGFR抑制剂针对EGFR基因突变的非小细胞肺癌(NSCLC)患者,我国已有多个靶向药物获批上市,如吉非替尼、厄洛替尼、奥希替尼等。
2021年,我国新增一款EGFR抑制剂——奥赛替尼,其在EGFR T790M突变阳性患者中显示出优异的疗效。
2. ALK抑制剂针对ALK基因融合的NSCLC患者,我国已有克唑替尼、阿来替尼、塞瑞替尼等靶向药物。
2021年,我国新增一款ALK抑制剂——恩沙替尼,其在ALK阳性患者中表现出良好的疗效。
3. PD-1抑制剂PD-1抑制剂在肺癌治疗中取得了显著成果,如纳武单抗、帕博利珠单抗等。
2021年,我国新增一款PD-1抑制剂——替雷利珠单抗,其在晚期肺癌患者中显示出良好的疗效。
二、乳腺癌靶向药物1. HER2抑制剂针对HER2阳性的乳腺癌患者,我国已有曲妥珠单抗、帕妥珠单抗、拉帕替尼等靶向药物。
2021年,我国新增一款HER2抑制剂——阿贝替尼,其在HER2阳性乳腺癌患者中显示出良好的疗效。
2. CDK4/6抑制剂CDK4/6抑制剂在乳腺癌治疗中发挥着重要作用,如帕博西尼、瑞博西尼等。
2021年,我国新增一款CDK4/6抑制剂——阿比特西尼,其在乳腺癌患者中表现出良好的疗效。
3. PI3K抑制剂PI3K抑制剂在乳腺癌治疗中发挥着重要作用,如阿帕替尼、依维莫司等。
2021年,我国新增一款PI3K抑制剂——艾地替尼,其在乳腺癌患者中显示出良好的疗效。
三、结直肠癌靶向药物1. EGFR抑制剂针对RAS野生型结直肠癌患者,我国已有西妥昔单抗、帕尼单抗等靶向药物。
2021年,我国新增一款EGFR抑制剂——尼妥珠单抗,其在结直肠癌患者中显示出良好的疗效。
带你全面了解O药、K药、T药、I药、B药
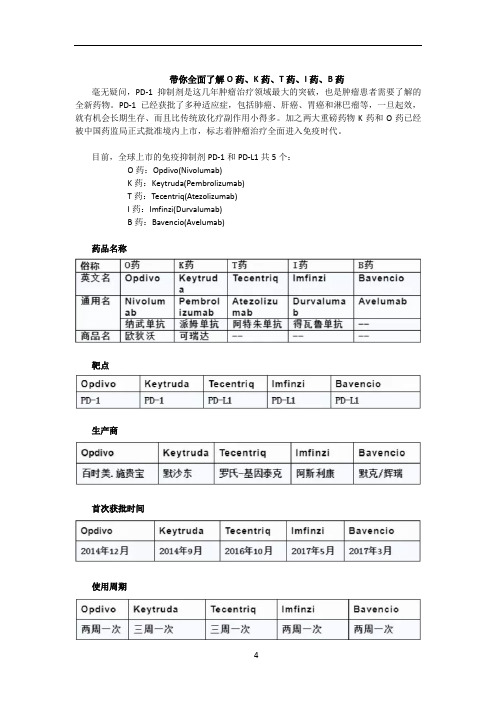
带你全面了解O药、K药、T药、I药、B药毫无疑问,PD-1抑制剂是这几年肿瘤治疗领域最大的突破,也是肿瘤患者需要了解的全新药物。
PD-1已经获批了多种适应症,包括肺癌、肝癌、胃癌和淋巴瘤等,一旦起效,就有机会长期生存、而且比传统放化疗副作用小得多。
加之两大重磅药物K药和O药已经被中国药监局正式批准境内上市,标志着肿瘤治疗全面进入免疫时代。
目前,全球上市的免疫抑制剂PD-1和PD-L1共5个:O药:Opdivo(Nivolumab)K药:Keytruda(Pembrolizumab)T药:Tecentriq(Atezolizumab)I药:Imfinzi(Durvalumab)B药:Bavencio(Avelumab)药品名称靶点生产商首次获批时间使用周期剂型规格使用剂量适应症国内上市情况价格关于PD-1的几大问题1.疗效如何?在绝大多数、未经挑选的实体瘤中,单独使用PD-1抑制剂的有效率只有10%-30%左右。
唯一的例外,是经典型霍奇金淋巴瘤,有效率突破60%以上。
究其受到追捧的原因是:PD-1抑制剂疗效的持久性。
由于免疫系统具有记忆功能,因此一旦PD-1抑制剂起效,其中部分病友实现临床治愈,也就是说五年、十年不复发、不进展、长期生存,尤其是较早的恶性黑色瘤、肾癌以及非小细胞肺癌。
2.如何预测疗效?1)PD-L1表达:PD-L1表达越高,有效率越高。
PD-L1表达,在肺腺癌、恶性黑色瘤等肿瘤中,格外有用。
PD-L1表达超过50%的晚期非小细胞肺癌,可以直接首选单独的PD-1抗体K药治疗,有效率在40%上下。
2)MSI检测:MSI-H的消化道肿瘤,有效率可以达到50%左右。
MSI检测特别适合消化道肿瘤、子宫内膜癌等患者。
3)肿瘤基因突变负荷(TMB)检测:一般认为,TMB大于20个突变/Mb,就是TMB 高。
TMB高的患者,接受PD-1抑制剂治疗的有效率高、生存期长。
4)肿瘤浸润淋巴细胞(TIL)检测:浸润的淋巴细胞越多,PD-1抑制剂的有效率越高。
速递丨一线治疗肝癌!双重免疫组合疗法降低死亡风险22%

速递⼁⼀线治疗肝癌!双重免疫组合疗法降低死亡风险22%领星资讯栏⽬“Breaking News”每周⾼频更新,内容包括国内外肿瘤新药获批情况、临床试验进展、⾏业动态等。
每天只要1分钟,轻松掌握⼀⼿新闻。
国内新药获批【肺癌】恒瑞医药阿得贝利单抗申报上市19⽇,CDE官⽹显⽰,恒瑞医药的PD-L1单抗阿得贝利单抗上市申请获受理。
这是国产第5款申报上市的PD-L1单抗。
2021年10⽉27⽇,恒瑞医药宣布阿得贝利单抗(研发代号:SHR-1316)联合化疗⼀线治疗⼴泛期⼩细胞肺癌的随机、双盲、安慰剂对照、多中⼼的III期临床研究主要研究终点结果达到⽅案预设的优效标准。
研究结果表明,SHR-1316联合化疗对⽐安慰剂联合化疗可以显著延长患者⽣存(OS)。
(insight数据库)国外新药获批【肺癌】⼀线治疗肺癌患者 PD-1抑制剂组合疗法离获批再近⼀步2022年1⽉19⽇,再⽣元公司(Regeneron)宣布,美国FDA已接受PD-1抑制剂Libtayo(cemiplimab)的补充⽣物制品许可申请(sBLA),⽤于联合含铂双重化疗,⼀线治疗晚期⾮⼩细胞肺癌(NSCLC)患者。
(药明康德)临床试验进展【头颈部鳞状细胞癌】Nektar Therapeutics IL-2免疫刺激疗法在中国获批临床18⽇,CDE公⽰显⽰,Nektar Therapeutics申报的bempegaldesleukin已获得临床试验默⽰许可,拟开发⽤于头颈部鳞状细胞癌。
(CDE)【实体瘤】复宏汉霖HLX208单药或联合治疗晚期实体瘤获批临床18⽇,复星医药发布公告称,其控股⼦公司复宏汉霖收到NMPA关于同意靶向⼈类BRAF蛋⽩V600E突变⼩分⼦抑制剂HLX208单药或联合治疗晚期实体瘤开展临床试验的批准。
(企业公告)【肝癌】⼀线治疗肝癌!双重免疫组合疗法降低死亡风险22%19⽇,阿斯利康宣布,重磅PD-L1抑制剂度伐利尤单抗与抗CTLA-4抗体tremelimumab联⽤,在⼀线治疗不可切除的肝细胞癌患者的3期临床试验中与活性对照相⽐,显著延长患者的总⽣存期。
中国军团逐年崛起!国内九大上市抗癌靶向药盘点!

研发药企:先声药业市场售价:1030元/⽀适应症:联合长春瑞滨和顺铂化疗⽅案(NP⽅案)⽤于治疗初治或复治的Ⅲ/Ⅳ期⾮⼩细胞肺癌(NSCLC)患者。
研发药企:贝达药业市场售价:1345元/盒适应症:治疗EGFR突变晚期NSCLC,也可⽤于治疗既往接受过⾄少⼀个化疗⽅案失败后的晚期NSCLC。
研发药企:⽯药集团市场售价:1800元/⽀适应症:⾮髓性恶性肿瘤患者在接受会发⽣有临床意义发热性中性粒细胞减少的抑制⾻髓的抗肿瘤药治疗时,使⽤本品可降低发热性中性粒细胞减少引起的感染发⽣率。
研发药企:深证微芯⽣物市场售价:9240元/盒适应症:既往⾄少接受过⼀次全⾝化疗的复发或难治的外周T细胞淋巴瘤(PTCL)患者。
研发药企:恒瑞医药市场售价:1360元/盒适应症:既往⾄少接受过 2 种系统化疗后进展或复发的晚期胃腺癌或胃-⾷管结合部腺癌患者。
研发药企:正⼤天晴市场售价:6200元/盒适应症:既往⾄少接受过2种系统化疗后进展的晚期NSCLC;三线及以上治疗⼴泛期SCLC(⼩细胞肺癌);⼆线治疗晚期软组织⾁瘤,⼀线治疗腺泡状软组织⾁瘤。
研发药企:和记黄埔市场售价:7320元/盒(5mg/粒)、6153元/盒(1mg/粒)适应症:三线及以后治疗晚期结直肠癌患者。
研发药企:恒瑞医药市场售价:9960元/盒适应症:联合卡培他滨治疗HER2阳性、既往未接受或接受过曲妥珠单抗的复发或转移性乳腺癌患者。
研发药企:复宏汉霖市场售价:1398元/瓶(100mg/10ml)适应症:复发或耐药的滤泡性中央型淋巴瘤(国际⼯作分类B、C 和D 亚型的B 细胞⾮霍奇⾦淋巴瘤)的治疗。
带你全面了解O药、K药、T药、I药、B药
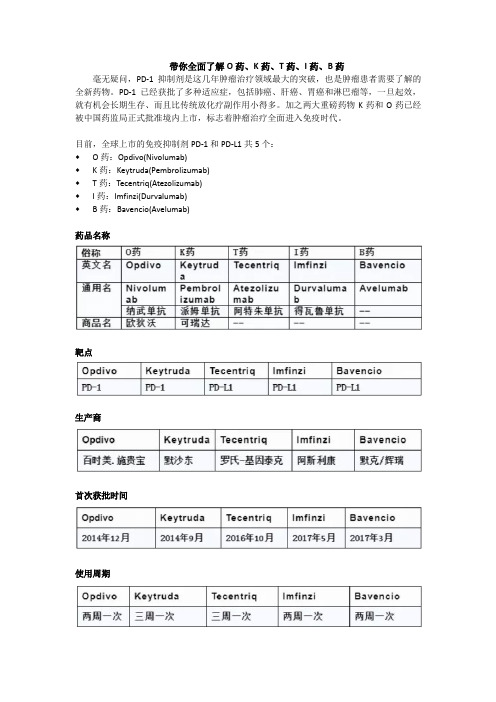
带你全面了解O药、K药、T药、I药、B药毫无疑问,PD-1抑制剂是这几年肿瘤治疗领域最大的突破,也是肿瘤患者需要了解的全新药物。
PD-1已经获批了多种适应症,包括肺癌、肝癌、胃癌和淋巴瘤等,一旦起效,就有机会长期生存、而且比传统放化疗副作用小得多。
加之两大重磅药物K药和O药已经被中国药监局正式批准境内上市,标志着肿瘤治疗全面进入免疫时代。
目前,全球上市的免疫抑制剂PD-1和PD-L1共5个:♦O药:Opdivo(Nivolumab)♦K药:Keytruda(Pembrolizumab)♦T药:Tecentriq(Atezolizumab)♦I药:Imfinzi(Durvalumab)♦B药:Bavencio(Avelumab)药品名称靶点生产商首次获批时间使用周期剂型规格使用剂量适应症国内上市情况价格关于PD-1的几大问题1.疗效如何?在绝大多数、未经挑选的实体瘤中,单独使用PD-1抑制剂的有效率只有10%-30%左右。
唯一的例外,是经典型霍奇金淋巴瘤,有效率突破60%以上。
究其受到追捧的原因是:PD-1抑制剂疗效的持久性。
由于免疫系统具有记忆功能,因此一旦PD-1抑制剂起效,其中部分病友实现临床治愈,也就是说五年、十年不复发、不进展、长期生存,尤其是较早的恶性黑色瘤、肾癌以及非小细胞肺癌。
2.如何预测疗效?1)PD-L1表达:PD-L1表达越高,有效率越高。
PD-L1表达,在肺腺癌、恶性黑色瘤等肿瘤中,格外有用。
PD-L1表达超过50%的晚期非小细胞肺癌,可以直接首选单独的PD-1抗体K 药治疗,有效率在40%上下。
2)MSI检测:MSI-H的消化道肿瘤,有效率可以达到50%左右。
MSI检测特别适合消化道肿瘤、子宫内膜癌等患者。
3)肿瘤基因突变负荷(TMB)检测:一般认为,TMB大于20个突变/Mb,就是TMB高。
TMB高的患者,接受PD-1抑制剂治疗的有效率高、生存期长。
4)肿瘤浸润淋巴细胞(TIL)检测:浸润的淋巴细胞越多,PD-1抑制剂的有效率越高。
国家药监局附条件批准纳鲁索拜单抗注射液上市

国家药监局附条件批准纳鲁索拜单抗注射液上市
佚名
【期刊名称】《中国处方药》
【年(卷),期】2024(22)1
【摘要】近日,国家药品监督管理局通过优先审评审批程序附条件批准上海津曼特生物科技有限公司申报的纳鲁索拜单抗注射液(商品名:津立生)上市。
该药品用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。
纳鲁索拜单抗注射液(JMT103)为重组全人源抗核因子-κB受体活化因子配体(RANKL)单克隆抗体,通过与细胞表面的RANKL特异性结合。
【总页数】1页(PI0001)
【正文语种】中文
【中图分类】R73
【相关文献】
1.国家药监局附条件批准卡度尼利单抗注射液上市
2.国家药监局批准佩索利单抗注射液上市
3.国家药监局附条件批准伊基奥仑赛注射液上市
4.国家药监局附条件批准纳基奥仑赛注射液上市
5.国家药监局批准仑卡奈单抗注射液上市
因版权原因,仅展示原文概要,查看原文内容请购买。
治疗非小细胞肺癌的新药_吉非替尼_黄莹

1.1 上市情况 吉非替尼是表皮生长因子受体酪氨酸激酶 (EG F R -T K )
的新型抑制剂 , 目前已进行完 Ⅰ 、 Ⅱ 、 Ⅲ期临床试验 , 先后在包 括日本 、美国 、澳大利亚在内的 36 个国家上市 , 其中于 2003 年 5 月初通过美国食品与药品管理局(F DA)审批在美国上市 , 作 为 二 线或 三 线 药 物 用 于 治 疗 晚 期 或 其 他 治 疗 方 案 无 效 的 N SCL C 患者 ;于 2005 年 2 月 25 日经国家食品药品监督管理 局批准正式在中国上市 。 1.2 化学成分
常增生和转移 , 抑制肿瘤细胞的发展 , 诱导其凋亡 , 起到抗肿瘤 作用 。 1.4 药效学
吉非 替 尼抗 细胞 增 殖作 用 表现 在可 选 择性 抑 制 H ER/
erbB 受体 ,包括 EG F R 。已有研究表明其还可广泛抑制异种移 植于裸鼠的人肿瘤细胞的生长 , 抑制其血管生成 , 在体外可增 加人肿 瘤细 胞衍生 系的凋 亡并 抑制血 管内 皮血管的形成 [3] 。在动物实验 或体外研究中已证实 , 吉非替尼可提高化 、放疗及激素治疗的
[ 4] F ukuoka M , Y ano S , G iaccone G , et al .M ulti -institutio nal ra ndo mized pha se Ⅱ tr ial of gefitinib for previously tre ated patients w ith adv ance d non -sm all cell lung ca nce r[ J] .J C lin O ncol , 2003 , 21(12):2 237.
吉非替尼 最常见不良反应为 腹泻和皮疹 ;此外还 可见恶 心 、呕吐 、皮肤干燥 、间质性肺炎等 。多数于停药后或经对症处 理即可缓解 , 间质性肺炎虽然罕见却可致命 , 值得临床高度重 视。
奥希替尼(泰瑞沙)终于在中国获批一线用药!

奥希替尼(泰瑞沙)终于在中国获批⼀线⽤药!(⼀)今天,中国药监局⽹站传出重磅消息,批准了靶向药奥希替尼(泰瑞沙)⽤于EGFR突变阳性晚期或转移性⾮⼩细胞肺癌(NSCLC)成⼈患者的⼀线治疗!中国EGFR突变晚期⾮⼩细胞肺癌患者的治疗,将迎来⾰命性的改变!截图来⾃国家药品监督管理局⽹站由于数据突出,奥希替尼⼀年多前在美国已经获批⼀线治疗。
我当时就预测它在中国获批只是时间问题。
好药不⼀定要留到最后使⽤ (详情阅读:新⼀代靶向药,早⽤早好,还是救命稻草?)。
泰瑞沙应该算是最近上市的进⼝抗癌药中,名⽓最⼤,对中国患者影响最⼤的药物之⼀。
主要因为它针对的EGFR突变晚期⾮⼩细胞肺癌患者,在中国特别的多,远远多于欧美!因此,很多⼈说,这是欧美制药企业为中国患者定制的新药。
奥希替尼不是第⼀次在中国上市,它2015年11⽉在美国被批准,2017年3⽉在中国获批,成为有史以来进⼊国内最快的进⼝抗癌新药。
既然不是新药,为啥今天这个新闻还能让专业⼈⼠兴奋呢?因为上次是批的⼆线治疗,这次是⼀线治疗。
从⼆线治疗上升到⼀线治疗,是个巨⼤的飞跃。
任何⼀个好的抗癌药,终极⽬标都是成为⼀线治疗!最主要的原因,是接受⼀线治疗的患者数量远⽐⼆线多。
据统计,在⼆线治疗情况下,5位携带EGFR敏感突变的患者中,只有1位最终⽤上了奥希替尼。
现在它成了⼀线治疗,那意味着5位患者或许都能⽤上这个药。
治疗的患者多,不仅意味着能帮助更多⼈,也代表给公司带来更⼤经济回报。
但成为⼀线治疗⾮常难,绝⼤多数抗癌药都没有机会。
为什么呢?因为成为⼀线治疗,需要专家认定它是⽬前这类癌症患者最好的选择之⼀。
要达到这⼀点,需要在临床试验中表现优异,战胜⽬前的标准疗法。
奥希替尼做到了。
(⼆)奥希替尼获批⼀线,最重要的试验,是代号为FLAURA的国际⼤型双盲临床研究。
500多名(60%以上是亚裔)有EGFR敏感突变的新诊断晚期⾮⼩细胞肺癌患者被随机分为两组,⼀组接受⽬前的标准治疗(1代EGFR靶向药),⼀组接受3代靶向药奥希替尼。
多纳非尼Donafenib靶向药

多纳⾮尼Donafenib靶向药甲苯磺酸多纳⾮尼⽚(Donafenib)是由中国⾃主研发的靶向药,是⼀种新型的多激酶抑制剂。
药理研究表明,多纳⾮尼可以同时抑制VEGFR、PDGFR等多种受体酪氨酸激酶的活性,也可直接抑制各种Raf激酶,并抑制下游的Raf/MEK/ERK信号传导通路,抑制肿瘤细胞增殖和肿瘤⾎管的形成,发挥双重抑制、多靶点阻断的抗肿瘤作⽤。
ZGDH3研究是中国⾸个完成的、⽤于评估多纳⾮尼⼀线治疗晚期肝细胞癌的II/III期的临床试验,从2016年3⽉⾄2018年4⽉共招募了668位患者,是迄今为⽌中国患者⼊组数最多的⼀线晚期肝癌临床试验。
在今年刚结束的56届美国肿瘤学会年会(ASCO2020)上,研究者通过⼝头报告向全世界公布了ZGDH3最新研究成果,证明了多纳⾮尼在肝癌靶向治疗⽅⾯取得突破性进展。
ZGDH3研究按1:1将患者随机分⾄Donafenib组(0.2g,每⽇两次⼝服)及索拉⾮尼组(0.4g,每⽇两次⼝服)。
研究结果表明:主要终点总⽣存期(OS)多纳⾮尼组优于对照(索拉⾮尼)组。
中位总⽣存期(mOS)在多纳⾮尼组达到了12.1个⽉,⽽索拉⾮尼组是10.3个⽉,相差了1.8个⽉。
多纳⾮尼组患者风险⽐索拉⾮尼组下降了17%。
安全性⽅⾯,两组患者的不良反应基本相似,多纳⾮尼组常见不良反应有⼿⾜⽪肤反应(50.5%)、腹泻(36.6%)、天冬氨酸转氨酶升⾼(40.5%)、⾎胆红素升⾼(39.0%)、⾎⼩板计数减少(37.8%)。
与索拉⾮尼组患者相⽐,多纳⾮尼在严重不良反应和导致减量或暂停⽤药的不良事件均显著低于索拉⾮尼组。
多纳⾮尼是12年来晚期肝癌治疗领域第⼀个在⼤型III期临床试验中⽣存期优于索拉⾮尼的分⼦靶向药物。
ZGDH3研究显⽰,与索拉⾮尼相⽐,多纳⾮尼可改善晚期肝癌患者的⽣存期,⽽且安全性及耐受性好。
⽬前泽璟制药已经向国家药品监督管理局(NMPA)新药审评中⼼提交新药上市申请。
国内批准上市11个替尼类药物

国内批准上市11个替尼类药物1、伊马替尼(Imatinib)2001年5月上市商品名“格列卫”2、吉非替尼(Gefitinib)2003年5月上市商品名“易瑞沙”3、厄洛替尼(Erlotinib)2004年11月上市商品名“特罗凯”4、舒尼替尼(Sunitinib) 2006年6月商品名“索坦”5、达沙替尼(dasatinib)2006年6月上市商品名“施达赛”6、拉帕替尼(Lapatinib)2007年3月上市商品名“泰立沙”7、尼洛替尼(Nilotinib)2007年10月上市商品名“达希纳”8、埃克替尼(Icotinib)2011年上市商品名“凯美纳”9、克唑替尼(Crizotinib)2013年1月上市商品名“赛可瑞”10、阿帕替尼(Apatinib)2014年上市商品名“艾坦”第一个国产11、阿昔替尼(Axitinib)2012年1月上市商品名“英立达”近10多年来,“替尼”类药物(酪氨酸激酶抑制剂,PTKs)一直是药物研发的热点,目前这类药物在肿瘤及非肿瘤领域(银屑病关节炎、哮喘等)均有着重要作用。
目前,全球约有20多个“替尼”类药物获批,而处于Ⅲ期临床阶段的此类药物也有20余个。
截至2015年6月底,国内获批上市的“替尼”类药物共有11个,分别介绍如下:1、伊马替尼(Imatinib)该药由诺华公司开发,是全球第一个上市的酪氨酸激酶抑制剂,主要抑制BCRABL。
2001年5月经优先审评通道获FDA批准上市,用于治疗费城染色体阳性(Ph+)的慢性粒细胞白血病(CML)患者;2002年4月在我国进口上市,商品名格列卫。
目前该药在美国共获批了10个适应证,是很多肿瘤疾病的一线用药,但靶点单一,易产生耐药性。
而正是因其适应证广且易耐药,才使得后续研发的大部分“替尼”类药物都要在伊马替尼耐药或不耐受的基础上才可以使用。
2、吉非替尼(Gefitinib)该药由阿斯利康公司开发,是一种表皮生长因子受体(EGFR)酪氨酸激酶抑制剂,同时也是第一个EGFR抑制剂,用于治疗既往接受过化疗(主要是铂类和多西他赛)的局部晚期或转移性非小细胞肺癌(NSCLC)患者。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肺癌重磅新药在中国获批上市!
勃林格殷格翰昨日宣布,第二代EGFR靶向药物阿法替尼已在国内获批,为中国的肺癌患者带来了新的希望。
勃林格殷格翰的TKI类药物阿法替尼是多靶点激酶抑制剂,其作用于HER2的同时,也不可逆转地抑制EGFR。
研究发现该药与易瑞沙等相比,可以显著提升非小细胞肺癌的治疗效果,因此该药获得了FDA突破性认定,在70多个国家上市。
我国肺癌人群众多,阿法替尼具有巨大的市场机会。
FDA批准适应症:EGFR突变的转移性非小细胞肺癌,NCCN推荐用于HER2突变的非小细胞肺癌。
用法:口服,40mg,一天
一次,进餐前一小时或者餐后2小时。
剂量:
30mg/40mg/50mg阿法替尼与一代EGFR-TKI的区别阿法
替尼是靶向EGFR的抑制剂,被称为二代EGFR-TKI,在NCCN指南中,与一代TKI(易瑞沙、特罗凯、凯美纳)共同被推荐为EGFR突变的晚期NSCLC患者的临床一线用药。
一代与二代的主要区别在于:1、阿法替尼作用的靶点不仅
只针对于EGFR,而且对HER2基因突变及ErbB4的信号
通路均有抑制作用,因此对于肺癌中检测到HER2突变的患者,可以考虑阿法替尼的靶向用药。
2、阿法替尼与与第一
代可逆的EGFR TKI不同的是,阿法替尼会不可逆地与EGFR结合,从而达到关闭癌细胞信号通路、抑制肿瘤生长
的目的,因此阿法替尼的作用强度更大。
3、在LUX2\3\6的汇总研究中发现,阿法替尼对部分EGFR的罕见突变(如Gly719Xaa, Leu861Gln, and Ser768Ile)有明显抑制活性。
意味着这类突变类型的患者一线选择阿法替尼疗效更好。
3、目前LUX-Lung8的临床试验表明,阿法替尼对于之前治疗失败的肺鳞癌患者具有临床优势,因而阿法替尼也比一代TKI增加了肺鳞癌(不论EGFR基因突变与否)的后线治疗的适应症。
UX-Lung 7:阿法替尼与吉非替尼头对头临床试验UX-Lung 7是全球首例头对头比较第二代和第一代EGFR 靶向治疗药物(分别为阿法替尼和吉非替尼)治疗EGFR突变阳性非小细胞肺癌患者(既往未接受过治疗)的试验。
IIb 期试验包括常见EGFR突变(del19或L858R)的319例晚期非小细胞肺癌患者。
试验的主要复合终点为独立审查的PFS、至治疗失败时间和OS;次要终点包括ORR、疾病控制率、肿瘤体积缩小、患者报告的结局与安全性。
临床结果阿法替尼显著降低肺癌进展风险和治疗失败风险27%,PFS 的改善随时间推移更加显著,治疗2年后,阿法替尼组存活且无进展的患者数量是吉非替尼组的2倍以上(18个月后:27% 与15%;24个月后:18% 与8%)。
与吉非替尼组相比,阿法替尼组发生客观缓解(ORR;肿瘤体积有临床意义减少)的患者显著更多。
这一阳性结果展示了阿法替尼相比一代TKI的临床优势。
UX-Lung 8:阿法替尼和特罗凯针对
肺鳞状细胞癌的临床试验2015年9月27日,勃林格殷格翰公司在欧洲癌症大会(奥地利维也纳)上宣布,与厄洛替尼相比,LUX-Lung 8试验的III期临床新数据进一步凸显阿法替尼用于经治的肺鳞状细胞癌患者的治疗获益。
试验数据表明,该患者人群接受阿法替尼治疗时的无进展生存期(PFS)和总生存期(OS)要优于接受厄洛替尼时的结果。
根据在ECC上所发表的一项新分析,接受阿法替尼治疗后观察到的患者生存结局改善并不受EGFR突变状态的影响。
因此,在LUX-Lung 8试验中,与接受厄洛替尼治疗的患者相比,接受阿法替尼治疗的患者中有更多人报告了整体健康和生存质量的改善,以及一些肺癌相关症状的改善。
根据此临床结果,阿法替尼在2016年分别获得美国FDA和欧盟批准用于治疗铂类化疗时或化疗后病情恶化的晚期肺鳞状细胞癌患者。
不良反应及剂量调整阿法替尼的广谱作用靶点及不可逆结合都提示其临床疗效会比一代TKI更大,但同时也意味着药物的不良反应也会增加。
LUX-Lung7试验显示,虽然总体不良反应发生率无差异,但是阿法替尼3-4级不良反应的发生率要比吉非替尼高(10.6%、4.4%)通过剂量调整,患者的不良反应发生率也明显减少,特别是3-4级的发生率控制得很好。
那减量对患者的临床疗效有影响吗?可喜的是,试验显示,减量的患者无论在患者生存质量还是PFS上与未减量患者比较都不存在统计学差异。
副作用处理1、腹泻:服
用阿法替尼的患者96%都会出现不同程度的腹泻。
调整饮食习惯,包括少食多餐,食用清淡的食物,也要避免使用含咖啡因,酒精,乳制品,脂肪,纤维,柳橙汁,西梅汁,煎炸油腻辛辣食物,加重腹泻。
轻微腹泻可以用蒸苹果,炒米煮粥来调理,如果腹泻每天超过3次以上,考虑思密达,易梦停(用法:口服成人首次4mg,以后每腹泻1次再服2mg,直至腹泻停止或每日用量达16~20mg,连续5日,若无效则停服)。
此外还要考虑补充电解质,以免脱水或者电解质紊乱。
2、皮肤问题:采用不含酒精的的维生素E、C、芦荟胶等保湿,做好防晒措施,使用温和的洗发露和沐浴乳,穿宽松的棉布衣服,避免使用刺激皮肤的衣物。
大疱和剥脱性皮肤疾病:阿法替尼片说明书0.15%患者中发生严重大疱、起泡和去角质病变。
对威胁生命的皮肤反应终止药物。
3、口腔炎:用软毛牙刷,餐后睡前用漱口水,保持良好的口腔卫生。
4、间质性肺病(ILD):在1.5%患者发生。
对肺症状急性发作或恶化应该停药。
5、肝毒性:在0.18%患者中发生致命性肝损伤。
用定期肝检验监视。
对肝检验严重或恶化不给或终止阿法替尼。
6、角膜炎:在0.8%患者中发生。
7、胚胎胎儿毒性:可致胎儿危害。
劝告女性对胎儿潜在危害和使用高效避孕。
在精彩纷呈的肺癌靶向治疗中,阿法替尼又为我们增添了新的治疗选择。
其广谱的治疗机理及临床优势会冲击到一代TKI的用药地位,而其耐受问题也得到了初步
的改善与调整。
相信随着其上市普及,阿法替尼将进一步提高广大肺癌患者的临床疗效。
编者:笨笨猪点击阅读相关热门文章:EGFR基因突变和对应的靶向药物
什么是肺腺癌EGFR基因突变?有哪些可用药物?
肺癌EGFR突变患者靶向治疗
听专家讲:肺癌中最常见的EGFR突变如何治疗?关注我们:搜索微信公众号“癌度”,了解更多关于肿瘤和基因的资讯。
转载文章请注明来源公众号及作者。
